Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Chemicals
Caricato da
LinkSkyword94Copyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Chemicals
Caricato da
LinkSkyword94Copyright:
Formati disponibili
Aldeide alifatica
Chetone alifatico
C
O
H
R C
O
R
R
Ar Ar
Ar
Aldeide aromatica
Chetone aromatico
(H)
Alcol 1
Alcol 2
-H
2
+H
2
C
O
H
C
O
Relazione ossidoriduttiva fra alcoli e composti carbonilici
Chetone RCOR
Aldeide RCHO
-RCHO
(NON
RCOH)
-RCOR
ALDEIDI e CHETONI: IL GRUPPO CARBONILICO
+3
Ossidazione degli alcoli a composti carbonilici ( C=O)
Deidrogenazione
-1 +1
0
+2
alcol primario aldeide
acido carbossilico
alcol secondario chetone
nessuna ossidazione di questo tipo;
nessun H sul C che porta l OH .
nessuna ossidazione di questo
tipo
OH O
H
ossidazione
ossidazione
O
OH
OH O
ossidazione
H
+ H
2
+ H
2
[O]
[O]
[O]
-Un prerequisito per ossidazione alcoli la presenza di H sul
C che porta il gruppo funzionale -OH.
C
O
H
H
metanale
aldeide formica
C
O
H
H
3
C
etanale
aldeide acetica
C
O
H
C H
3
C
H
H
propanale
aldeide propionica
Nome IUPAC delle aldeidi: suffisso -o (dellidrocarburo saturo
con PARI numero di atomi di carbonio) diventa -ale.
C
O
H
C C
H
H
H
H
H
3
C
butanale
aldeide butirrica
C
O
H
C C
C H
3
H
H
H
H
metilpropanale
aldeide metilpropionica
4 3 2 1
o |
La vecchia nomenclatura (ancora in uso) riportata in corsivo.
Il gruppo aldeidico sempre allinizio della catena, per definizione in posizione 1.
Latomo adiacente alla funzione viene indicato con alfa (o), il successivo con
beta (|), ecc., ultimo omega (e)
1
ClCH
2
CH
2
CH
2
CHO
4 3 2 1
4-cloro-butanale
-cloro butirraldeide
o
|
C
O
CH
3
H
3
C C
O
CH
2
CH
3
H
3
C
C
O
CH
2
CH
2
CH
3
H
3
C
propanone
butanone 2-pentanone
Chetoni : suffisso -o (dellidrocarburo saturo con PARI numero di atomi
di carbonio) diventa -one. Numero + basso possibile.
(dimetilchetone o
acetone)
(etilmetilchetone) (metilpropilchetone)
4-cloro-6-metil-3-eptanone
2,2-dimetil
ciclopentanone
CHO formile
C=O oxo
H H
2
SO
4
SO
3
H H
2
O +
Benzenesulfonic acid
Sulfonation:
+
H RX
AlCl
3
R HX + +
An alkylbenzene
Alkylation:
H R-C-X
O
AlCl
3
CR
O
HX
+
+
Acylation:
An acylbenzene
An acyl
halide
Acido 4-formil
benzensolfonico
OHC
Come sostituenti
1 3
Acido 3-oxo
pentanoico
CH
2
=CHCH
2
CHO
4 3 2 1
3-butenale
priorit
Glicerolo
(1,2,3-propantriolo)
C=O
Gliceraldeide
(2,3-diidrossipropanale)
priorit
C=O
Diidrossiacetone
(1,3-diidrossipropanone)
priorit
H
R o
t
xy
C O
Risonanza fra due forme limite
Struttura elettronica C=O : confronto con alcheni C=C (somiglianze e
differenze!)
C e O: ibridizzati sp
2
planarit
sp
2
-sp
2
:legame o
p-p : legame t
O : non lega atomi, ma porta
2 coppie di non legame
O : pi elettronegativo del C
(R
1
)
Polarit del gruppo carbonilico e propriet (chimiche e fisiche)
E
+
Nu
C O
C
(2)
Attacco da parte di elettrofili
(3)
H in alfa al carbonile pi acido di un H legato a un C
H
o
+
o
-
(1)
Attacco da parte di nucleofili
(Nu:
-
o Nu-H)
o
(1 e 2). Reazioni di addizione nucleofila
Reattivit del gruppo carbonilico: 3 regioni reattive
*Tautomeria cheto-enolica;
*Condensazione aldolica
H
+
(catalizzatore acido o Nu-H)
+
Composto tetraedrico
di addizione
sp
2
sp
3
1. Reazioni di addizione nucleofila
:Nu
:Nu-H
|
MECCANISMO: 2 percorsi.
1. Senza catalisi acida : nucleofili forti
2. Con catalisi acida nucleofili deboli
HOH ROH NH
o
-
o+
o
-
o+
I nucleofili possono essere carichi negativamente o neutri :
ione alcossido
sp
2
sp
3
sp
3
C
O
R
R
o+
o-
Nu
_
C
O
R
Nu
R
_
H
3
O
+
C
OH
R
Nu
R
H
2
O
+ OH
-
reagente
1 stadio: addizione nucleofila al C
2 stadio: protonazione ossigeno ( a spese del solvente)
Nucleofili forti anioni Nu:
-
ione idruro e ione ossidrile
Meccanismo generale con Nu:
-
1 stadio: il nucleofilo attacca il sito elettrofilo C
o+,
dona una coppia di elettroni e
forma un nuovo legame C-Nu, rompe il legame t, formando un intermedio
tetraedrico ione alcossido (base forte). Il carbonio passa da ibridazione sp
2
a
sp
3
. 2 stadio: segue la protonazione dellossigeno a spese del solvente.
neutri Nu:H ammoniaca e ammine
1 percorso : senza catalisi acida
C
O
R
R
o+
o-
Nu
_
C
O
R
Nu
R
_
H
3
O
+
C
OH
R
Nu
R
C
O
R
R
o+
o-
Nu
_
C
O
R
Nu
R
_
H
3
O
+
C
OH
R
Nu
R
H
C
O
R
R
o+
o-
Nu
_
C
O
R
Nu
R
_
H
3
O
+
C
OH
R
Nu
R
H
+
C
O
R
R
o+
o-
Nu
_
C
O
R
Nu
R
_
H
3
O
+
C
OH
R
Nu
R
Meccanismo generale con :NuH
1 stadio: il nucleofilo attacca il sito elettrofilo C
o+,
dona una coppia di elettroni e
forma un nuovo legame C-Nu, rompe il legame t, formando un intermedio
tetraedrico ione alcossido (base forte). Il carbonio passa da ibridazione sp
2
a
sp
3
. Il nucleofilo si carica positivamente !!
2 stadio: segue la protonazione dellossigeno, in questo caso per trasferimento
del protone da Nu a O
-
.
1 stadio: addizione nucleofila al C
2 stadio: protonazione ossigeno
(a spese dellidrogeno legato al nucleofilo)
H
1 percorso : senza catalisi acida
..
Chetone
sp
2
Ione alcossido
sp
3
Alcol 2
sp
3
Riduzione ad alcoli: ioni H:
-
H
2
O
da NaBH
4
Formazione di aldeidi e chetoni idrati (gem-diolo 1,1): ioni OH
-
R C
H
O
O H
-
R C
H
O
O H
H
2
O
O H
-
R C
H
OH
OH
Aldeide idrata
sp
3
Aldeide
sp
2
Ione alcossido
sp
3
Formazione IMMINE : gruppo funzionale C=N
H
3
C C
H
O
N H H
C H
3
H
3
C C
H
O
N
H
H
C H
3
H
|+
Aldeide sp
2
Ione alcossido sp
3
H
3
C
C
H
N C H
3
Aldimmina o Base di Schiff
H
3
C C
H
O
N C H
3
H
H
|
+ H
2
O
2) trasferimento di un protone: amminoalcol intermedio (prodotto di
addizione);
Nucleofilo neutro:Nu-H NH
3
e ammine primarie R-NH
2
stesso meccanismo, intermedio carico positivamente su Nu e rapido trasferimento
del protone da Nu-H a ossigeno.
1) Addizione nucleofila
3) Eliminazione acqua : formazione dellimmina
A, H
+
:
Aldeide + ammina 1 aldimmina + acqua
..
..
R C
H
O
R ' N H
2
R C
H
N R '
H
2
O
R C
H
O
R ' N H
2
R C
H
N R '
H
2
O
R
R
Chetone + ammina 1 chetimmina + acqua
Immina o Base di Schiff: composto contenente un doppio legame C=N
Immine sono intermedi metabolici comuni
(esempio: metabolismo amminoacidi. Transaminasi.)
Piridossalfosfato amminoacido (alanina) immina o base di Schiff
Da Mc Murry, Zanichelli
R C
H
O
R C
H
O H
H
+
2 percorso : con catalisi acida
Nucleofili deboli richiedono lattivazione del C=O prima
dellattacco del nucleofilo.
HOH, ROH, (RNH
2
)
R
H
C
OH
|
+
..
..
*Gruppo carbonile protonato,
stabilizzato per risonanza,
reso pi elettrofilo!
(carbocatione)
1 stadio: protonazione del carbonile su O e formazione del carbonile
protonato*
2 stadio: addizione di :Nu-H
:NuH
R C
H
O H
Nu H
H
+
R C
H
OH
3 stadio: perdita di un protone
(si rigenera catalizzatore!)
+
+
+
Nu
Addizione nucleofila di acqua in ambiente acido : aldeide o
chetone idrato : gem-diolo (1,1-diolo).
Addizione nucleofila di alcoli in ambiente acido : emiacetali e
acetali.
Stechiometria della reazione!
1 1
emiacetale
/emichetale
Eccesso alcol
Acetale / chetale
Emiacetale una molecola che contiene
un OH e un OR sullo stesso carbonio
Acetale una molecola che contiene
due gruppi OR sullo stesso
carbonio
H
+
Provare seguendo
meccanismo generale
R C
H
O
R C
H
O H
R C
H
O H
O R
H
H
+
O
H
R
H
+
R C
H
O H
O R
semiacetale
(idrossietere)
R
OH
+
|
+
H
C
semiacetale
protonato
Passaggio 1.
Reazione acido/base.
Il catalizzatore acido protona
lossigeno basico del carbonile
e forma il carbonile protonato
pi propenso ad accogliere il
nucleofilo.
Passaggio 2.
Lossigeno nucleofilo dellalcool
attacca il C elettrofilo del C=O
rompendo il legame t e
donando gli elettroni allO
+
.
Semiacetale protonato.
Passaggio 3.
La perdita di un protone
restituisce il catalizzatore
acido formando lemiacetale.
Formazione emiacetale
Formazione acetale
Reazione del semiacetale con una seconda molecola di alcol forma un
acetale ( da unaldeide) o un chetale (da un chetone).
H
+
R C
H
OH
(R)
OR
+
ROH
R C OR
OR
H (R)
SOSTITUZIONE NUCLEOFILA.
-OH gruppo uscente (esce come acqua)
-OR gruppo entrante (entra come alcol indissociato)
+
H
2
O
Eccesso alcol
emiacetale
acetale
C
H
O H
O R
H
+
R C
H
O H
O R
H
H
2
O
R C
H
O R
R O H
R C
H
O R
O
R H
H
+
R C
H
O R
O R
Passaggio 4:
Reazione acido/base.
La protonazione di OH lo
trasforma in un
miglior gruppo uscente.
Passaggio 6:
L O nucleofilo dellalcool
attacca il C elettrofilo e
si forma acetale protonato.
Passaggio 5:
Uscita dell acqua e
formazione
carbocatione
Passaggio 7.
La perdita di un
protone
restituisce il
catalizzatore
acido formando
lacetale.
R
+
HOCH
2
CH
2
CH
2
CH
2
CHO
5-idrossipentanale
Gruppo emiacetalico ciclico:
il gruppo etereo OR fa parte di
un anello a 6 termini
Intermedio
alcossido
o+
..
..
2
3
4
OH
H
..
..
4-idrossialdeidi e 5-idrossialdeidi:
formazione emiacetali ciclici. Reazione intramolecolare.
La formazione degli emiacetali e degli acetali parte centrale della chimica dei
carboidrati. Il glucosio, per esempio, si trova in soluzione in equilibrio tra una forma
aperta (idrossialdeide) e una forma chiusa semiacetalica ciclica.
Molte molecole di glucosio si uniscono poi a formare lamido e la cellulosa con legami
acetalici.
OR
C O
C
(2)
Attacco da parte di elettrofili
(3)
H in alfa al carbonile pi acido di un H legato a un C
H
o
+
o
-
(1)
Attacco da parte di nucleofili
(Nu:
-
o Nu-H)
o
Reattivit del gruppo carbonilico: 3 regioni reattive
H
+
(catalizzatore acido o Nu-H)
Presenza del gruppo carbonilico
aumenta lacidit del chetone
rispetto allalcano di un fattore
pari a 10
40
K
a
= 10
-19
K
a
= 10
-60
o+
C
H
H
H
O
H
C
OH
-
H
2
O
C
H
H
O
H
C
C
H
H
H
C
O
C
H
H
H
O
H
C C
H
H
O
H
C H C
H
H
C
H
O
C
H
H
C
H
O
H C
H
H
C
H
O
C
H
H
C
H
O
H C
H
H
C
H
OH
C
H
H
C
H
O
H
2
O
OH
-
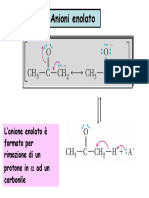
carbanione anione enolato
Nucleofilo al carbonio
pKa
*STABILIZZAZIONE PER RISONANZA DELLANIONE ENOLATO : CARICA
NEGATIVA DELOCALIZZATA SU OSSIGENO
CH
3
CH
2
CH
3
50
CH
3
COCH
3
19
CH
3
CHO 17
CH
3
COCH
2
COCH
3
8,8
ACIDITA DEGLI ATOMI DI IDROGENO IN ALFA:
LO IONE ENOLATO
Nel dichetone acidit aumenta
notevolmente!
o
Da Mc Murry - Fondamenti di Chimica
organica Zanichelli
Tautomeria cheto-enolica : ISOMERIA costituzionale
I composti carbonilici con idrogeni in o si equilibrano rapidamente con i
corrispondenti enoli (ene + alcol).
Interconversione nota come tautomeria cheto-enolica.
I singoli isomeri differiscono per posizione di un atomo di H (tautomeri)
Tautomero chetonico 99,999% Tautomero enolico 0,000001%
veloce
H
H
H
C C
O
C
H
H
H
H
C C
C
H
H
O
H
H
H
Movimento concertato di elettroni e protoni intramolecolare
Propen-2-olo Acetone
H
H
H
C
O
C H
C
C
H
O H
H
H
etanale o acetaldeide
alcol vinilico
Solo gli H in alfa sono acidi !!!
Gli atomi di H in |-, -, o- NON sono acidi poich lo ione che si
forma NON stabilizzato dalla risonanza (non coniugato)
REAZIONI DI CONDENSAZIONE ALDOLICA
Reazioni tra 2 composti carbonilici che formano un solo
prodotto (ALDOLO = aldeide + alcol).
Si forma legame C-C
Formazione di
|-idrossialdeide o 3-idrossialdeide
|-idrossichetone o 3-idrossichetone
Il Co (C2) di un composto carbonilico (nucleofilo) si lega al
C carbonilico (elettrofilo) dellaltro composto che diventa
(C3) o beta-idrossi
Condensazione aldolica
C
H
H
H
O
H
C
OH
-
H
2
O
C
H
H
O
H
C
C
H
H
H
C
O
C
H
H
H
O
H
C C
H
H
O
H
C H C
H
H
C
H
O
C
H
H
C
H
O
H C
H
H
C
H
O
C
H
H
C
H
O
H C
H
H
C
H
OH
C
H
H
C
H
O
H
2
O
OH
-
Passaggio 1: formazione del nucleofilo carbanione-anione enolato
a)
b)
c)
C
H
H
H
O
H
C
OH
-
H
2
O
C
H
H
O
H
C
C
H
H
H
C
O
C
H
H
H
O
H
C C
H
H
O
H
C H C
H
H
C
H
O
C
H
H
C
H
O
H C
H
H
C
H
O
C
H
H
C
H
O
H C
H
H
C
H
OH
C
H
H
C
H
O
H
2
O
OH
-
Passaggio 2 : attacco nucleofilo su una seconda molecola di aldeide
(ione alcossido)
C
H
H
H
O
H
C
OH
-
H
2
O
C
H
H
O
H
C
C
H
H
H
C
O
C
H
H
H
O
H
C C
H
H
O
H
C H C
H
H
C
H
O
C
H
H
C
H
O
H C
H
H
C
H
O
C
H
H
C
H
O
H C
H
H
C
H
OH
C
H
H
C
H
O
H
2
O
OH
-
Passaggio 3: protonazione a spese del solvente e formazione di una
|-idrossialdeide
Nu:
H
3
C C
C H
3
O
H
3
C C
C H
3
O H
C
H
H
C
C H
3
O
H
3
C C
C H
3
O
H
3
C C
C H
3
O
?
+
acetone
Questo il legame che si formato
4-idrossi-4-metil-2-pentanone
(aldolo)
OH
-
o
o |
REAZIONE RETRO-ALDOLICA
o |
C
H
H
H
O
H
C
O H
-
H
2
O
C
H
H
O
H
C
C
H
H
H
C
O
H
H C
H
H
C
H
O
C
H
H
C
H
O
Rottura del legame o- |
C
H
H
H
O
H
C
OH
-
H
2
O
C
H
H
O
H
C
C
H
H
H
C
O
C
H
H
H
O
H
C C
H
H
O
H
C H C
H
H
C
H
O
C
H
H
C
H
O
H C
H
H
C
H
O
C
H
H
C
H
O
H C
H
H
C
H
OH
C
H
H
C
H
O
H
2
O
OH
-
+ C
H
H
H
O
H
C
OH
-
H
2
O
C
H
H
O
H
C
C
H
H
H
C
O
C
H
H
H
O
H
C C
H
H
O
H
C H C
H
H
C
H
O
C
H
H
C
H
O
H C
H
H
C
H
O
C
H
H
C
H
O
H C
H
H
C
H
OH
C
H
H
C
H
O
H
2
O
OH
-
Catabolismo dello zucchero fruttosio 1,6-difosfato
o
|
C
C
C
Gliceraldeide 3-fosfato
Diidrossiacetonfosfato
Esercizio da fare
Propriet fisiche
o-
o+
o+
o-
Dipolo-dipolo
Composto peb (C)
Etilene -104
Formaldeide -21
2-metilpropene -140
Acetone 56
Solubilit
Addizione nucleofila di acqua in ambiente acido : aldeide o chetone
idrato : gem-diolo (1,1-diolo).
R
H
C
OH
+
|
+
..
..
R C
H
O
R C
H
O H
R C
H
O H
O H
H
H
+
O
H
H
H
+
R C
H
O H
O H
Passaggio 1.
Reazione acido/base.
Il catalizzatore acido protona
lossigeno basico del carbonile
e forma il carbonile protonato
pi propenso ad accogliere il
nucleofilo.
Passaggio 2.
Lossigeno nucleofilo dellacqua
neutra attacca il C elettrofilo del
C=O rompendo il legame t e
donando gli elettroni allO+.
Gem-diolo protonato.
Passaggio 3.
La perdita di un protone
restituisce il catalizzatore
acido formando il gem-diolo.
Potrebbero piacerti anche
- Nomenclatura chimica inorganica. Reazioni redox. Principi di stechiometriaDa EverandNomenclatura chimica inorganica. Reazioni redox. Principi di stechiometriaNessuna valutazione finora
- 11 - Aldeidi e ChetoniDocumento40 pagine11 - Aldeidi e ChetoniJasmineLuciaNessuna valutazione finora
- Cap.14 Aldeidi e ChetoniDocumento38 pagineCap.14 Aldeidi e ChetoniGabriele GuerraNessuna valutazione finora
- Gruppi Funz FaddaDocumento53 pagineGruppi Funz FaddaMarynaNessuna valutazione finora
- Aldeidi e ChetoniDocumento21 pagineAldeidi e Chetonijuve6Nessuna valutazione finora
- Reazioni AldeidiDocumento20 pagineReazioni AldeidistvlnpllNessuna valutazione finora
- Le acque minerali - Guida alla lettura delle etichetteDa EverandLe acque minerali - Guida alla lettura delle etichetteNessuna valutazione finora
- Chimica - Reazioni Di Organica by SilvioDocumento12 pagineChimica - Reazioni Di Organica by SilvioIvanoBarnabaNessuna valutazione finora
- Chimica OrganicaDocumento31 pagineChimica Organicakuritaro100% (1)
- Aldeidi e ChetoniDocumento21 pagineAldeidi e ChetonimikadoboomNessuna valutazione finora
- Aldeidi ChetoniDocumento70 pagineAldeidi ChetoniAldo BlesiNessuna valutazione finora
- Reazioni OrganicaDocumento21 pagineReazioni OrganicaRoberta PirasNessuna valutazione finora
- Dispensa Acidi CarbossiliciDocumento20 pagineDispensa Acidi CarbossiliciFrancesco BerniniNessuna valutazione finora
- 13 Chimica OrganicaDocumento29 pagine13 Chimica OrganicaFabrizio FantasiaNessuna valutazione finora
- Appunti Di Chimica Organica IIDocumento5 pagineAppunti Di Chimica Organica IIFederica Moro100% (1)
- Ioni EnolatoDocumento15 pagineIoni EnolatoWolframio74Nessuna valutazione finora
- Alcoli Eteri e TioliDocumento25 pagineAlcoli Eteri e TioliRenato GavaNessuna valutazione finora
- Chimica OrganicaDocumento50 pagineChimica Organicamarco50% (2)
- Esercizi Chimica OrganicaDocumento108 pagineEsercizi Chimica OrganicaminchiazzurraNessuna valutazione finora
- E6 ChetoniDocumento3 pagineE6 ChetoniDiletta MontanelliNessuna valutazione finora
- Gruppi Funzionali, Polimeri e CarboidratiDocumento10 pagineGruppi Funzionali, Polimeri e CarboidratiLuca CanegratiNessuna valutazione finora
- Acizi Carboxilici Si Derivati Functionali Partea IDocumento8 pagineAcizi Carboxilici Si Derivati Functionali Partea IRaul Cris Ciobanca100% (1)
- Corso Chimica - 13 Reattività Da Alcani A ChetoniDocumento59 pagineCorso Chimica - 13 Reattività Da Alcani A ChetoniGuenhNessuna valutazione finora
- Chimica OrganicaDocumento94 pagineChimica OrganicaAndrei (aesthetic demon)Nessuna valutazione finora
- Reazioni Alcheni MeccDocumento13 pagineReazioni Alcheni MeccGuido PiroliNessuna valutazione finora
- Chimica Del CarbonioDocumento18 pagineChimica Del Carbonioalcione12Nessuna valutazione finora
- Alcani, Alcheni, AlchiniDocumento19 pagineAlcani, Alcheni, AlchiniMassimiliano CameroniNessuna valutazione finora
- Alchini PDFDocumento5 pagineAlchini PDFdavidetrtNessuna valutazione finora
- Aldehidos y CetonasDocumento63 pagineAldehidos y CetonasLEYTON HCNessuna valutazione finora
- Reazioni AlcheniDocumento12 pagineReazioni AlcheniAndreazza IlariaNessuna valutazione finora
- Breve Descrizione Reazioni Chimica OrganicaDocumento16 pagineBreve Descrizione Reazioni Chimica OrganicaAlessio MenegonNessuna valutazione finora
- Atkins GlossarioDocumento33 pagineAtkins GlossarioAndrea Bucci0% (1)
- 3 Gruppi Funzionali PDFDocumento28 pagine3 Gruppi Funzionali PDFciccioNessuna valutazione finora
- C. Organica COMPLETODocumento18 pagineC. Organica COMPLETOAndra IoanaNessuna valutazione finora
- Gli AlcoliDocumento33 pagineGli AlcoliJacopo BallariniNessuna valutazione finora
- Metode Generale de Obtinere A Compusilor OrganicDocumento10 pagineMetode Generale de Obtinere A Compusilor Organicalyen333Nessuna valutazione finora
- Chimica Generale RipassoDocumento36 pagineChimica Generale RipassoEster CellucciNessuna valutazione finora
- 08 - Alcoli e EteriDocumento25 pagine08 - Alcoli e Eterijuve6Nessuna valutazione finora
- 2T Chimica OrganicaDocumento20 pagine2T Chimica OrganicaAndrea MagrisNessuna valutazione finora
- Cap. 13 Benzene e DerivatiDocumento77 pagineCap. 13 Benzene e DerivatiGabriele GuerraNessuna valutazione finora
- Sintesi Di Williamson EpossidiDocumento22 pagineSintesi Di Williamson EpossidiRoberta Lo IzzoNessuna valutazione finora
- Aldeidi e ChetoniDocumento51 pagineAldeidi e ChetoniMajorana.WEBNessuna valutazione finora
- 05 Alcoli PDFDocumento42 pagine05 Alcoli PDFCeceNessuna valutazione finora
- 8 - Competizione Tra E e SNDocumento40 pagine8 - Competizione Tra E e SNDouglas MaloneNessuna valutazione finora
- Reazioni Alcoli MeccDocumento10 pagineReazioni Alcoli MeccorganicaloverNessuna valutazione finora
- Tabella Proprietà Composti OrganiciDocumento8 pagineTabella Proprietà Composti OrganiciLovelyJadeNessuna valutazione finora
- Nozioni Di Carboidrati Versione Aggiornata (B J Kakos)Documento27 pagineNozioni Di Carboidrati Versione Aggiornata (B J Kakos)Vassily KakosNessuna valutazione finora
- DomandeDocumento4 pagineDomandewatsy-92Nessuna valutazione finora
- 18 CarboidratiDocumento43 pagine18 Carboidratirodrigue yanNessuna valutazione finora
- Chimica PDDocumento37 pagineChimica PDerrorinsideNessuna valutazione finora
- Nomenclatura ChimicaDocumento11 pagineNomenclatura ChimicaGabriele MichelisNessuna valutazione finora
- Chimica Organica - Principali ReazioniDocumento7 pagineChimica Organica - Principali ReazioniStefanoNessuna valutazione finora
- Transizioni Ordine-Disordine Nei BiopolimeriDocumento61 pagineTransizioni Ordine-Disordine Nei BiopolimeriOriona DhamoNessuna valutazione finora
- Fondamenti Di Chimica OrganicaDocumento36 pagineFondamenti Di Chimica OrganicaDamianoScrasciaNessuna valutazione finora
- Appunti Chimica OrganicaDocumento53 pagineAppunti Chimica OrganicamantovanNessuna valutazione finora
- PerossidiDocumento3 paginePerossidiPaoloMMNessuna valutazione finora
- Diapo Colori Degli AlimentiDocumento24 pagineDiapo Colori Degli AlimentiLinkSkyword94Nessuna valutazione finora
- Testico LoDocumento38 pagineTestico LoLinkSkyword94Nessuna valutazione finora
- Testico LoDocumento38 pagineTestico LoLinkSkyword94Nessuna valutazione finora
- Sbobine Cardio PDFDocumento235 pagineSbobine Cardio PDFLinkSkyword94Nessuna valutazione finora
- Appunti Di Chimica GeneraleDocumento46 pagineAppunti Di Chimica GeneraleLinkSkyword94Nessuna valutazione finora
- SANDRINI METALLI Lamiere Grecate Sistema Tetto PDFDocumento44 pagineSANDRINI METALLI Lamiere Grecate Sistema Tetto PDFsilvioNessuna valutazione finora
- Descrizione Delle Opere Edificio A1a2 CanziDocumento22 pagineDescrizione Delle Opere Edificio A1a2 CanziAnonymous YjN488Nessuna valutazione finora
- Diagrammi Di Stato PDFDocumento94 pagineDiagrammi Di Stato PDFscienziatoNessuna valutazione finora
- Calcolo Solaio Ferro - LateriziDocumento8 pagineCalcolo Solaio Ferro - LateriziFilippo VecchiarelliNessuna valutazione finora
- Fermentazione Alcolica Del Lievito Di Birra 3Documento23 pagineFermentazione Alcolica Del Lievito Di Birra 3api-241505890Nessuna valutazione finora
- Materiali Dentali2Documento62 pagineMateriali Dentali2Marco Camagni100% (1)
- Come Fare Un Pane DeliziosoDocumento2 pagineCome Fare Un Pane DeliziosoRut Capcha GarciaNessuna valutazione finora
- Fisiologia GastrointestinaleDocumento19 pagineFisiologia Gastrointestinalenature_of_fireNessuna valutazione finora
- Germano 1Documento27 pagineGermano 1Luigi LutriNessuna valutazione finora