Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Domande Nefrologia
Caricato da
Marco Sparavigna0 valutazioniIl 0% ha trovato utile questo documento (0 voti)
955 visualizzazioni46 pagineutili consigli
Copyright
© © All Rights Reserved
Formati disponibili
PDF, TXT o leggi online da Scribd
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoutili consigli
Copyright:
© All Rights Reserved
Formati disponibili
Scarica in formato PDF, TXT o leggi online su Scribd
0 valutazioniIl 0% ha trovato utile questo documento (0 voti)
955 visualizzazioni46 pagineDomande Nefrologia
Caricato da
Marco Sparavignautili consigli
Copyright:
© All Rights Reserved
Formati disponibili
Scarica in formato PDF, TXT o leggi online su Scribd
Sei sulla pagina 1di 46
DOMANDE DI NEFROLOGIA
1) Definite la malattia renale cronica
E un quadro clinico e fisiopatologico che non individua quindi una patologia, ma si instaura
in conseguenza alla maggioranza delle patologie renali. Tali patologie vengono globalmente
indicate con la definizione di malattie renali croniche. Si pu definire come:
Danno renale presente da almeno 3 mesi, quale definito dalla presenza di alterazioni
anatomiche o funzionali del rene con o senza riduzione del filtrato glomerulare (GFR),
che si manifesta con alterazioni patologiche oppure presenza di marcatori di danno
renale (per esempio alterazioni della composizione delle urine o dei tests di imaging).
GFR<60mL/min/1,73m
2
per almeno 3 mesi, con o senza alterazioni patologiche o altri
segni di danno renale.
2) Indicate quali sono i criteri utilizzati per diagnosticare la malattia renale
Per stabilire la presenza di insufficienza renale ci si basa su:
Misurazione del GFR (mediante clearance di creatinina, clearance di inulina, cistatina C
oppure uso di radioisotopi).
Creatininemia
Azotemia
Diagnosi di IRC:
Documentata IR (riduzione GFR, iperazotemia, ipercreatininemia) da almeno 3 mesi
Segni e sintomi di uremia da almeno 3 mesi
Segni e sintomi di osteodistrofia renale
Riduzione bilaterale delle dimensioni dei reni
3) Definite la sindrome nefrologica Insufficienza renale cronica
Sindrome determinata dalla riduzione progressiva ed irreversibile della massa renale (cio del
numero di nefroni) funzionante, e quindi delle molteplici funzioni del rene, come indicato dalla
riduzione del filtrato glomerulare (GFR), quantificabile con la clearance della creatinina o con
varie formule che stimano la velocit di filtrazione glomerulare.
La riduzione della massa renale funzionante porta quindi ad alterazione delle funzioni renali
come:
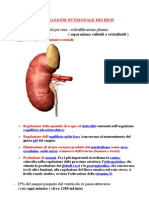
1. regolazione della quantit di acqua ed elettroliti contenuti nellorganismo (equilibrio
idroelettrolitico)
2. regolazione dellequilibrio acido-base
3. eliminazione di cataboliti come urea, creatinina, acido urico)
4. produzione di ormoni. Fra i pi importanti: la renina, coinvolta nella regolazione della
pressione arteriosa; l'eritropoietina, che stimola la produzione dei globuli rossi e le
prostaglandine che concorrono, tra le altre funzioni, alla regolazione del flusso ematico
nel rene stesso. A livello renale, inoltre, avviene l'attivazione della vitamina D.
4) Indicate le metodiche usate in clinica per misurare e stimare il filtrato glomerulare
La stima del filtrato glomerulare (GFR) e il monitoraggio di questo valore nel tempo sono
fondamentali per valutare la funzione renale. Le metodiche usate per misurare questo
parametro sono:
Creatininemia - la creatinina sierica (mg/dL VN 0.7-1.3 mg/dL)
un marker molto utilizzato perch si tratta di un esame semplice e routinario,
ma il risultato necessita di alcune approssimazioni quindi deve essere affiancato
ad altre valutazioni;
la creatinina una molecola di piccole dimensioni liberamente filtrata,
il GFR direttamente proporzionale alla quota di creatinina escreta con le urine
ed inversamente proporzionale a quella sierica, di conseguenza ad un aumento
della creatininemia corrisponde una diminuzione del GFR;
sono tuttavia necessari alcuni accorgimenti, poich una piccola quota di
creatinina pu essere secreta a livello del tubulo prossimale determinando una
sovrastima del GFR, assunzione di carne cotta ed attivit fisica intensa possono
invece determinare un aumento della creatinina sierica e una sottostima del GFR;
il valore della creatininemia comunque utilizzato nelle formule su cui si basano
le altre metodiche di valutazione del GFR.
Clearance della creatinina la clearance della creatinina (ml/min VN 90-130 ml/min)
la misura del volume di plasma depurato dalla creatinina nell'unit di tempo e si
valuta a partire dai valori di creatininuria (mg/dL sulle urine delle 24h) e creatininemia
tramite la formula:
Clearance (ml/min) = [U (creatininuria) x P (creatininemia)] / V (diuresi delle 24h/1440)
Pu sovrastimare GFR perch creatinina viene escreta sia per filtrazione
glomerulare che per secrezione tubulare
Clearance dellinulina
Cistatina C
EQUAZIONI:
- formule che vengono utilizzate nella pratica clinica per ovviare alle approssimazioni
presentate dal calcolo della clearance della creatinina, tenendo conto di variabili individuali
che influenzano tale valore come et, peso, sesso ed etnia:
Cockcroft Gault fornisce una stima della clearance della creatinina
Clearance della creatinina (ml/min) = (140 - et) Peso Corporeo ideale(Kg) / (72
creatininemia (mg/dl) 0,85 per le donne
MDRD equation fornisce una stima del GFR
Equazione di Schwartz usato nei bambini <18 anni
Clearance (ml/min) = (0,55 x altezza cm)/Scr(mg/dl)
Equazione Connahan Barratt usato nei bambini
GFR(ml/min/1,73m
2
) = (0.43 x altezza cm)/Scr (mg/dl)
Equazione di Nankivell
GFR (ml/min) = 6,7/Scr(mmol/l) + peso/4 urea/2 100/altezza + 35(nelluomo) o
25(donna)
5) Riportate la classificazione in stadi di malattia renale cronica
La classificazione in stadi della malattia renale cronica uno schema che permette di valutare
la gravit del quadro clinico del paziente, indipendentemente dall'eziologia, inquadrandolo in
uno schema che prevede 5 stadi:
1. Stadio 1 Nefropatia cronica ma funzione renale conservata (GFR 90ml/min)
Soggetto a rischio di IRC
Non presente nessuna alterazione metabolica importante
2. Stadio 2 Insufficienza renale lieve (GFR 60-89 ml/min)
Comapiono le prime manifestazioni di danno renale
Completo compenso biochimico-metabolico.
Non si osservano segni laboratoristici di IRC (solo comincia a salire PTH quando
GFR 60-80ml/min)
3. Stadio 3 Insufficienza renale moderata (GFR 30-59 ml/min)
Cominciano ad osservare i segni dello scompenso funzionale: assorbimento
calcio, malnutrizione, insufficienza ventricolare sinistra, anemia
4. Stadio 4 Insufficienza renale severa (GFR 15-29 ml/min)
Compaiono altre alterazioni biochimico-metaboliche: trigliceridemia,
iperfosfatemia, acidosi metabolica, iperkaliemia.
5. Stadio 5 Insufficienza renale terminale (GFR < 15 ml/min o pz in terapia
sostitutiva)
Iperazotemia importante
Configurazione della sindrome uremica con alterazioni di quasi ogni apparato
Necessaria la terapia sostitutiva o trapianto
6) Descrivete brevemente il meccanismo ritenuto pi importante fra quelli che
determinano la progressione di IRC
Nella IRC si assiste a un progressivo decremento di numero di nefroni funzionanti.
Nelle fasi iniziali si instaura un meccanismo di compenso consistente nellaumento del GFR
nei singoli nefroni residui (SNGFR).
I meccanismi di compenso comprendono:
ipertrofia compensatoria,
attivazione del sistema RAAS
vasodilatazione afferente.
Questa condizione porta a Ipertensione sistemica e se non si interviene il processo patologico
progredisce, portando a ipertensione glomerulare.
Lipertensione glomerulare causa:
Aumento della tensione sulla membrana glomerulare condizione che favorisce il
danno ai capillari glomerulari e quindi il rilascio di mediatori infiammatori
Proteinuria favorisce laumento di proteine nel lume tubulare e quindi un
eccessivo riassorbimento e conseguente accumulo di proteine a livello del citoplasma
delle cellule tubulari.
Questo accumulo provoca lattivazione di geni pro-infiammatori (mediata da NfkB) e
fattori di crescita che porta a un processo di infiammazione interstiziale e aumento di
proliferazione di fibroblasti che determinano glomerulosclerosi e fibrosi tubulo-
interstiziale, quindi perdita di funzione dei nefroni residui.
7) Descrivete brevemente la patogenesi delle alterazioni del metabolismo del fosfato
nellIRC e le sue conseguenze.
Una delle prime manifestazioni della riduzione della funzione renale, anche modesta,
un'inadeguata eliminazione del fosfato, che presente nel sangue a bassa concentrazione e
risente quindi subito della riduzione della capacit di filtrazione.
Una riduzione di nefroni funzionanti causa riduzione dellescrezione di fosfato e ioni H+.
La riduzione dellescrezione dei fosfati porta a iperfosfatemia.
Liperfosfatemia stimola il rilascio di PTH quindi si ha iperparatiroidismo secondario.
Laumento di PTH provoca stimolazione del catabolismo osseo causando osteodistrofia e
calcificazione vascolare.
8) Descrivete il tipo di acidosi che si rileva nella malattia renale cronica lieve-moderata
ed il meccanismo principale che la determina.
La perdita progressiva di parenchima renale che si osserva nella malattia renale cronica
determina, tra gli altri effetti, anche uno stato di acidosi.
Durante le fasi iniziali di IRC si instaura una acidosi metabolica ipercloremica senza gap
anionico, dovuta alla ritenzione di Cl-, come conseguenza della diminuzione di HCO3-
plasmatico.
Infatti le urine vengono ancora acidificate, ma si produce meno NH4+ e non si elimina una
normale quantit di protoni in combinazione con questo tampone.
Iperkaliemia se presente contribuisce a deprimere ulteriormente la produzione di NH4+.
9) Descrivete il tipo di acidosi che si rileva nella malattia renale cronica severa e
terminale ed i meccanismi principali che la determinano.
Nella IRC avanzata si ha generalmente una acidosi metabolica normocloremica, associata a
gap anionico [Na+]>[Cl-]+[HCO3-].
La riduzione della filtrazione e il riassorbimento di anioni organici contribuiscono alla
patogenesi. Con il progredire della malattia renale il numero di nefroni funzionanti diventa
insufficiente a far fronte alla produzione netta di acidi. L'acidosi uremica quindi caratterizzata
da una minore produzione/escrezione di NH4+, dovuta principalmente a riduzione della massa
renale complessiva.
Raramente la [HCO3-] scende al di sotto di 15 mmol/l e il gap anionico raramente supera le 20
mmol/l, indicando il coinvolgimento di tamponi diversi da quelli contenuti nel compartimento
extracellulare. La ritenzione di acidi nell'insufficienza renale viene tamponata da sali alcalini di
derivazione ossea.
L'acidosi metabolica cronica provoca una notevole perdita di massa ossea a causa della
riduzione del carbonato di calcio contenuto nell'osso. L'acidosi cronica aumenta anche
l'escrezione urinaria di Ca proporzionalmente alla ritenzione cumulativa di acidi.
10) Descrivi brevemente la patogenesi delle alterazioni del metabolismo del calcio
nellIRC e le sue conseguenze
Lomeostasi del calcio viene controllato mediante:
Neoformazione ossea
Riassorbimento osseo
Escrezione renale del calcio
Assorbimento intestinale di calcio (sotto lazione di vitamina D3)
In situazione di IRC viene meno la formazione di calcitriolo e quindi diminuisce
lassorbimento intestinale di Ca2+, questo provoca ipocalcemia a cui lorganismo risponde
aumentando in modo compensatorio il rilascio di PTH, quindi iperparatiroidismo
secondario.
- L'azione del PTH in caso di MRC limitata all'attivazione del riassorbimento osseo tramite
la differenziazione terminale degli osteoclasti, per far fronte all'ipocalcemia.
- L'iperattivazione del riassorbimento osseo causa osteodistrofia
- l'iperfosfatemia in associazione all'ipercalcemia conseguente al riassorbimento osseo provoca
calcificazione dei tessuti molli, in particolare calcificazione vascolare.
11) Elencate le forme di osteodistrofia renale che si possono riscontrare in un pz. con
IRC terminale dopo anni di terapia dialitica.
Losteodistrofia renale (ODR) la patologia ossea peculiare dei pazienti con insufficienza
renale cronica in trattamento conservativo e sostitutivo. LODR causata dalle alterazioni dei
fattori che controllano in modo diretto o indiretto il metabolismo osseo.
L'ODR si pu presentare in varie forme caratterizzate da una diversa entit dei processi di
rimodellamento e dai corrispettivi quadri istologici associati:
Osteodistrofia a elevato rimodellamento osseo la forma pi frequente, aumentata
attivit osteoclastica, come conseguenza di iperparatiroidismo. Aspetto di:
Osteite fibrosa aumento di processi di rimodellamento con fibrosi peritrabecolare
Osteopatia mista osteite fibrosa lieve associata a difettosa mineralizzazione
Clinica:
Prurito
Miopatia prossimale
Tendenza alle fratture patologiche
Osteodistrofia a normale rimodellamento osseo osteopatia lieve
Osteodistrofia a basso rimodellamento osseo - si presenta in 2 forme:
Osteomalacia normale formazione della matrice osteoide che non viene
mineralizzata.
Malattia adinamica dellosso riduzione di formazione di trabecole ossee dovuta
alla riduzione dellattivit di PTH e resiztenza dellosso allazione di questormone
12) Quali sono i provedimenti terapeutici messi in atto per ridurre liperfosfatemia del
pz. in dialisi
Diversi studi hanno dimostrato una correlazione positiva tra iperfosfatemia e mortalit per
cause cardiovascolari nei pazienti dializzati. Il meccanismo alla base di questa correlazione
sembra essere l'accelerata progressione delle calcificazioni vascolari ma anche il danno
endoteliale diretto, dovuto anche alla stimolazione della produzione di PTH e FGF23 da parte
del P.
I provvedimenti terapeutici si basano essenzialmente su:
Riduzione dellapporto dietetico di fosfati - La restrizione dellapporto di quegli
alimenti che hanno un elevato contenuto di P per grammo di peso o per grammo di
proteine, quali il latte e i formaggi, pu consentire la prescrizione di una dieta
moderatamente ipofosforica (900-1000 mg/die), ma adeguata per apporto proteico (1-1.2
g/kg/die), utile ad ottenere un buon controllo della fosfatemia se abbinata ad altre
misure, senza incorre nel rischio di sviluppare malnutrizione.
La rimozione dialitica di P pu essere aumentata incrementando la durata o la frequenza
dei trattamenti dialitici. Maggior parte dei pazienti comunque necessita di chelanti per
ridurre lassorbimento intestinale di fosforo
Chelanti del fosfato sono efficaci nel ridurre lassorbimento intestinale di fosforo
Carbonato di calcio
Acetato di calcio
Sevelamer ed analoghi
Lantanio carbonato
Sali di magnesio
In particolare nei pazienti dializzati si tende ad utilizzare i sali di Ca a basse dosi come chelante
di prima scelta, a cui si affianca sevelamer nel caso in cui non si riesca ad ottenere un adeguato
controllo della fosfatemia.
13) Indicate i fattori che stimolano e quelli che inibiscono la secrezione di PTH ed il loro
comportamento nel pz. con insufficienza renale moderata-severa
PTH un ormone ipercalcemizzante e fosfaturico e la sua secrezione regolata da:
Calcemia sistema a feedback-
Se elevati livelli di calcemia inibizione della secrezione di PTH
Se bassi livelli di calcemia stimolazione della secrezione di PTH
Fosfatemia
Direttamente stimolando la secrezione di PTH
Indirettamente riduzione concentrazione plasmatica di Ca2+ quindi
stimolazione della secrezione PTH
Vitamina D
Inibisce PTH riducendo la trascrizione del gene PTH
Recettore sensibile al Ca2+ - stimola la secrezione di PTH
Nella IRC si assiste a:
Riduzione di GFR con ritenzione di fosfati e conseguente iperfosfatemia che stimola sia
direttamente che in modo indiretto la secrezione di PTH
Ipocalcemia come conseguenza di ridotta produzione di calcitriolo stimola la
secrezione di PTH
Bassi livelli di vitamina D attiva come conseguenza della perdita funzionale del rene
contribuiscono alliperparatiroidismo sia causando ipocalcemia, sia agendo direttamente
sulla trascrizione del gene del PTH.
Il PTH nel paziente con IRC non riesce per a compensare l'iperfosfatemia n l'ipocalcemia,
proprio a causa della perdita della funzione renale che limita la secrezione di vitamina D attiva
e non permette l'eliminazione del fosfato in eccesso
L'azione del PTH in questi pazienti limitata quindi all'attivazione del riassorbimento osseo e
la differenziazione terminale degli osteoclasti portando alla caratteristica osteodistrofia renale.
14) Descrivete le caratteristiche della diuresi in un pz. con insufficienza renale e filtrato
glomerulare intorno a 25ml/min
L'insufficienza renale cronica in un paziente con GRF pari a 25ml/min pu essere definita
severa.
In IRC la capacit di concentrare le urine si riduce progressivamente al diminuire di
GFR
Anche la capacit di diluizione viene persa
Come conseguenza si ha:
Poliuria isotonica
Nicturia
Perdita di capacit di far fronte ad un aumento dellapporto di liquidi
Perdita di capacit di far fronte a disidratazione o perdite extrarenali
Inoltre si ha ritenzione idrica con espansione del volume extracellulare e comparsa di
edemi
Iperkaliemia,
Acidosi metabolica con gap anionico,
Alterazioni del metabolismo di calcio e fosfati (ipocalcemia, iperfosfatemia, ridotta
sintesi di calcitriolo, iperparatiroidismo secondario, aumento della fosfatasi alcalina
ossea),
Anemia.
15) Indicate la patogenesi dellanemia nellIRC, distinguendo fra meccanismo principale
ed eventuali fattori secondari.
L'insufficienza renale cronica si associa solitamente ad un'anemia ipoproliferativa di grado
moderato-grave che in genere correlata alla gravit dell'insufficienza renale e si manifesta
quando il GFR arriva a valori intorno ai 40 ml/min (prima in caso di nefropatia diabetica). Gli
eritrociti sono solitamente normocitici e normocromici, il numero di reticolociti ridotto.
La principale causa di anemia in corso di IRC rappresentata da una produzione
insufficiente di EPO (eritropoietina) in seguito a malfunzionamento renale.
Fattori secondari:
Carenza di ferro
Malnutrizione proteica
Infiammazione acuta o cronica con compromissione di rilascio di ferro
Iperparatiroidismo severo con conseguente fibrosi del midollo osseo
Sopravvivenza ridotta dei globuli rossi in condizioni di uremia
Perdita di sangue (dialisi, frequenti prelievi, emorragia occulta)
Intossicazione da alluminio
Carenza di acido folico e vitamina B12
16) Elencate gli esami di laboratorio di 1 livello indicati in un pz. con insufficienza
renale per escludere che la sua anemia non sia correlata alla malattia renale.
Le indagini di primo livello per la valutazione dell'anemia in un paziente con IRC servono a
stabilire una correlazione con la patologia renale e comprendono:
Hb
MCV, MCH, MCHC, reticolociti
metabolismo del ferro
proteina C reattiva.
- Le caratteristiche degli eritrociti, la conta reticolocitaria e i parametri di metabolismo del
ferro sono utili per evidenziare stati anemici che non dipendono dal deficit di eritropoietina.
Lanemia che si associa a MRC generalmente normocromica e normocitica.
- La microcitosi pu indicare deficit di ferro, accumulo di alluminio, emoglobinopatie,
perdite croniche.
- La macrocitosi pu indicare deficit di folati o di vitamina B12, eccesso di ferro, e anche
terapia con epoetina (immissione in circolo di eritrociti immaturi e pi grandi).
- Una conta reticolocitaria elevata >100.000/mm3 (considerato il grado di anemia) pu
indicare unattivit emolitica (sindrome emolitica uremica) o perdite gastro-intestinali.
- Conte leucocitarie o piastriniche anormali possono riflettere un disturbo delle altre linee
midollari oltre alleritroide (patologia neoplastica, vasculiti).
17) In un pz. con insufficienza renale terminale in terapia dialitica, quali sono i livelli
raccomandati di Hb e perch?
Nei pz. dializzati si cerca di non superare i 12 g/dl di Hb perch cos il sangue rimane meno
viscoso e passa pi facilmente attraverso i macchinari per la dialisi.
Correzioni migliori, sebbene abbiano un effetto benefico sulla qualit della vita, hanno effetti
collaterali importanti quali:
l'aumento del rischio di incidenti cerebrovascolari,
l'aumento del rischio di dialisi inadeguata per trombosi durante la procedura dialitica o
trombosi della fistola arterovenosa,
aumento del rischio cardiovascolare
18) Descrivete il tipo di alterazione del metabolismo di K+ che si rileva in un pz. con
MRC terminale in terapia dialitica e le conseguenze cliche di tale alterazione
NellIRC terminale si assiste ad un iperkaliemia perch:
Lescrezione di K+ come dellacqua e degli altri ioni estremamente ridotta (quando
GFR < 20 ml/min)
I farmaci anti-ipertensivi che interferiscono con il sistema RAA provocano tutti aumento
di ritenzione di K+
Iperkaliemia pu essere aggravata dallapporto di K+ esogeno o da qualunque evento
importante di lisi cellulare
L'iperkaliemia pericolosa perch interferisce con il ciclo di ripolarizzazione delle cellule,
in particolare quelle del nodo SA, e pu causare aritmie nodali e ventricolari, predisponendo
all'asistolia.
Clinica:
Manifestazioni cardiache
Alterazioni di ECG
Aritmie atriali o ventricolari
Disfunzione del pacemaker fisiologico
Manifestazioni neuromuscolari
Parestesie
Astenia
Paralisi
Manifestazioni di elettroliti renali
Riduzione produzione NH4+
Natriuresi
Manifestazioni endocrine
Aumento secrezione aldosterone
Aumento secrezione insulina
Il paziente in dialisi deve perci limitare l'assunzione di potassio attraverso l'alimentazione e
fare uso di resine a scambio potassico per ridurre l'assorbimento ed evitare aumenti della [K]
nel periodo interdialitico.
19) Definite la calcifilassi
una sindrome di calcificazione vascolare, trombosi e necrosi tissutale che si riscontra quasi
esclusivamente in pz. con IRC in stadio 5. Calcifilassi un tipo di calcificazione extraossea che
avviene quando il prodotto delle concentrazioni di ionio Ca2+ e fosfato >55 (in genere >70)
perci si ha precipitazione di fosfato di calcio in sedi extraossee, soprattutto a livello della
tonaca media delle arterie.
Il ruolo del paratormone nel meccanismo patogenetico di questa sindrome non ancora del
tutto chiaro. Nella maggior parte dei casi si presenta entro il primo anno dallinizio del
trattamento dialitico e le probabilit della sua insorgenza aumentano negli stati di malnutrizione
proteica e di ipercoagulabilit come anche con lassunzione del Warfarin, che diminuisce la
rigenerazione vit K dipendente della proteina GLA della matrice, importante per la prevenzione
della calcificazione vascolare.
20) Descrivete brevemente un accesso vascolare per emodialisi e le varie modalit con
cui viene realizzato
La fistola, le protesi o il catetere attraverso cui si preleva il sangue rientrano nel novero di
accessi vascolari.
La modalit preferita di sistemazione di un accesso vascolare la fistola nativa (fistola
artero venosa, FAV), consite nel creare unanastomosi tra larteria radiale e la vena
cefalica (fistola Cimino Brescia). Si crea cos un arterial line che dallarteria radiale
conduce il sangue al filtro dializzatore e una venous line che dal filtro riporta il sangue
dializzato alla vena cefalica. Altre sedi teorici: inguinale, axillo-ascellare ma raramente
utilizzati.
Le fistole necessitano di un tempo di maturazione e possono deteriorasi per varie cause e
quindi non garantire un accesso affidabile. Quindi alternative:
Le FAV protesiche consistono nellanastomosi fra unarteria ed una vena attraverso
lutilizzo di una protesi. E indicata solitamente quando a causa dellesaurimento del
patrimonio vascolare non pi possibile confezionare una FAV tradizionale. Le protesi
possono essere utilizzate per collegare unarteria ed una vena molto distanti fra loro, ed
in questo caso si punge il vaso originario del paziente. Oppure come neo-vaso quando si
dispone di una vena profonda. In questo caso si punge il lume protesico.
Gli innesti ed i cateteri (CVC) tendono ad essere utilizzati in pazienti che hanno vene di
calibro troppo piccolo o non pi sfruttabili, il catetere inoltre la modalit preferita in
caso di urgenza, quando non si ha la possibilit di attendere la maturazione della fistola
oppure quando fistole ed innesti non hanno dato buoni risultati.
Solitamente i CVC permanenti vengono posizionati nella vena giugulare che per la sua
configurazione anatomica offre vantaggi quali il calibro adeguato ed un decorso retto, oltre ad
essere meglio tollerato dal paziente.
La vena giugulare sarebbe da preferire anche nei CVC durgenza in quanto il
posizionamento in succlavia pu causarne la stenosi con una riduzione del flusso
ematico ed compromettere in questo modo lo sviluppo della FAV.
La vena succlavia solitamente viene utilizzata nei CVC durgenza in quanto
facilmente reperibile anche in condizioni di shock. Come visto in precedenza questo
tipo sede pu comportare una stenosi della succlavia.
In urgenza viene utilizzata anche la sede femorale, che non compromette il futuro
sviluppo della FAV. Per presenta notevoli svantaggi in termini di deambulazione,
rischio infettivo e ostruzione del lume
21) Descrivete lassetto lipidico caratteristico di un pz. con MRC terminale
Oltre alla perdita delle principali funzioni renali (funzioni escretrice, omeostasi idroelettrica,
produzione sostanze endocrine), la malattia renale cronica terminale associata ad una serie di
complicanze metaboliche-endocrine, tra cui un alterato metabolismo lipidico. La dislipidemia
caratterizzata da:
Livelli di colesterolo plasmatico diminuiti
Livelli di colesterolo LDL e HDL ridotti
Ipertrigliceridemia per riduzione catabolismo e aumento sintesi VLDL epatica e
iperinsulinemia
22) Elencate i sintomi delluremia
La sindrome uremica dovuta non solo alla ritenzione delle scorie azotate, ma anche alla
perdita delle altre funzioni del rene, con alterazioni del ricambio idro-elettrolitico,
dellequilibrio acido-base, del metabolismo lipidico e glucidico, dellomeostasi circolatoria e
delleritropoiesi; ci si ripercuote su tutte le cellule dellorganismo e quindi sui pi svariati
organi ed apparati. Pertanto, la sindrome uremica caratterizzata da una serie di disturbi che
possono essere classificati sulla base del coinvolgimento dorgano o della gravit dei sintomi.
Coinvolgimento dorgano:
Apparato gastrointestinale : alito uremico, anoressia,nausea,vomito,dolore addominale,
alterazioni transito intestinale(stipsi) e diarrea.
Sistema nervoso centrale : sono interessate la sfera affettiva e la sfera cognitiva.
Sintomi lievi (insonnia, depressione, euforia, perdita dellattenzione)
Condizioni pi serie (disturbi cognitivi, disturbi dello stato di coscienza,
convulsioni, coma e morte).
Polineuropatia :
di tipo sensitivo (gambe urenti)
di tipo motorio ( sindrome della gamba senza riposo).
Mononeuropatia sensitiva: tipico disturbo uremico mal controllabile.
Prurito :disturbo mal controllabile. Risponde solo agli antipsicotici.
Pericardite: manifestazione rara;
non ha le tipiche alterazioni allECG, ma si comporta come una pericardite
essudativa
esiste il rischio di tamponamento cardiaco, e dal punto di vista semeiologico
analoga.
La terapia dialitica la risolve.
In base alla gravit dei sintomi:
Vengono divisi in sintomi lievi, moderati o severi.
23) Cosa si intende per tossine uremiche e come si classificano queste sostanze
Sono sostanze prodotte dal catabolismo proteico che normalmente vengono eliminate dal rene,
ma nellIRC vengono ritenute e sono causa di uremia.
Queste tossine sono:
Sostanze inorganiche
Urea
Molecole di medie dimensioni
-2-microglobulina
PTH
AGE (advanced glycosylation-end-products)
GIP-1 e GIP-2 (granulocyte inhibiting protein)
DIP (degranulation inhibiting protein)
Molecole di grosse dimensioni
Leptina
Cistatina C
RBP (retinol binding protein)
Guanidine
Creatinina - omoarginina
Metilguanidina - creatina
Acido guanidinosuccinico - arginina
Acido -guadinobutirrico - ADMA
Metilguanidina - SDMA
Ossalato
Fosfati organici
P-cresolo
Omocisteina
Indolo
CMPF
24) Cosa si intende per anomalie urinarie isolate e quali sono le forme principali di
anomalia urinaria isolata
Le anomalie urinarie sono alterazioni dei parametri urinari rilevati per motivi occasionali con
un comune esame delle urine in assenza di malattia urinarie e sistemiche .
Le alterazioni pi frequenti sono la microematuria, la proteinuria, la glicosuria (?) e la
cilindruria (?) .
La proteinuria isolata (< 3g/24h) generalmente un reperto occasionale in paziente
asintomatico, in assenza di alterazioni del sedimento urinario e della funzione renale.
Essa pu essere transitoria (proteinuria ortostatica, proteinuria febbrile, proteinuria
da sforzo) o persistente.
Una modesta proteinuria pu accompagnarsi anche allo scompenso cardiaco
congestizio e al decorso delle malattie infettive. Tuttavia in alcuni pazienti la
proteinuria pu rappresentare una manifestazione precoce di una patologia
glomerulare pi seria.
Non facile stabilire la causa di proteinuria isolata, soprattutto se lieve. Spesso i
pazienti hanno una storia clinica suggestiva di patologie che potrebbero aver causato
un danno, rigorosamente passate inosservate.
Microematuria isolata: pu osservarsi in quasi tutte le nefropatie, ma pu anche
comparire in diverse malattie delle vie urinarie. Una microematuria isolata pu
osservarsi in nefropatie familiari a decorso benigno (ematuria familiare benigna) o
viceversa a carattere evolutivo (sindrome di Alport).
Glicosuria glicosuria isolata con funzione renale normale, ereditata solitamente quale
tratto autosomico dominante ma talvolta anche come tratto recessivo.
Cilindruria -
25) Indicate i principali segni e sintomi di Sindrome Nefritica
Esordio improvviso
Insufficienza renale acuta
Oliguria (diuresi <400 ml/die) (50%)
Riduzione GFR di grado lieve moderato (creatininemia <2 mg/dl) che porta a:
ritenzione di liquidi quindi edema (85%)
ipertensione arteriosa (60-80%)
Sedimento urinario
ematuria macroscopica, "a lavatura di carne" (30%)
microematuria glomerulare (100%)
proteinuria glomerulare subnefrosica (100%)
cilindruria
dolore lombare (10%)
encefalopatia ipertensiva (1%)
risoluzione in circa 1-2 settimane
26) Indicate i principali sintomi e segni di Sindrome nefrosica
La sindrome nefrosica un insieme di sintomi e segni clinici causati da una alterazione dei
glomeruli renali che comporta una perdita di proteine con le urine di oltre i 3,5 grammi al
giorno. La sindrome caratterizzata dalla triade: perdita di proteine con riduzione delle
proteine nel sangue, edemi ed ipercolesterolemia.
proteinuria glomerulare "nefrosica" (> 3,5 g/1.73 m2.24h)
ipoalbuminemia
eccessiva perdita urinaria
ipercatabolismo renale
aumento "inappropriato" della sintesi epatica
edemi periferici
da "underfilling"
da ritenzione idrosodica primaria
- inizialmente a livello degli arti inferiori
- possibile versamento pleurico o pericardico
- edema particolarmente al volto e a livello periorbitale
iperlipemia
ipercolesterolemia
ipertrigliceridemia nei casi pi gravi
lipiduria
iperlipidemia o lipiduria (favoriscono aterosclerosi) per:
- aumentato sintesi di VLDL
- ridotto catabolismo di LDL
- perdita di fattori regolatori
Ipercoagulabilit (iperfibrinogenemia, perdita urinaria di antitrombina III,
riduzione/alterazione proteina C e proteina S, riduzione fibrinolisi, aumento
aggregabilit piastrinica)
trombosi venosa profonda (arti inferiori)
trombosi della vena renale
embolia polmonare
malnutrizione proteica
anemia (deficit di transferrina)
ipocalcemia (deficit di cholecalciferol-binding protein)
ipotiroidismo (deficit di thyroxine-binding protein)
aumentata suscettibilit alle infezioni (deficit di IgG e complemento): sepsi da Gram +
capsulati
alterazioni della farmacocinetica dei farmaci
27) Indicate quali glomeruonefriti si manifestano pi frequentemente con Sindrome
nefritica
Glomerulonefriti proliferativi diffuse endocapillari o focali
La pi importante glomerulonefrite diffusa post-streptococcica
Glomerulonefrite rapidamente progressiva (a semilune)
Glomerulonefrite membranoproliferativa
Glomerunefrite a depositi mesangiali
Nefrite lupica
28) Indicate quali glomerulonefriti si manifestano pi frequentemente con Sindrome
Nefrosica
Glomerulonefrite a lesioni minime
Glomerulonefrite focale segmentaria
Glomerulonefrite membranosa
Glomerulonefrite membrano-proliferativa
Nefropatia diabetica
Amiloidosi renale
29) Indicate le principali cause secondarie di glomerulopatie membranose
La glomerulonefrite membranosa una patologia dovuta alla deposizione di immunocomplessi
nella matrice extracellulare della membrana di filtrazione. Le cause secondarie di
glomerulopatia membranosa sono:
Infezioni
Epatite B e C, Schistosomiasi, Lebbra, Filariasi, Ecchinococcosi, Malaria, HIV
Neoplasie
Carcinoma (polmone, colon, stomaco, mammella, cervello)
Malattie linfoproliferative e sostanze tossiche
Malattie autoimmuni
LES, artrite reumatoide, connettiviti, Sindrome di Sjogren, dermatomiosite,
sarcoidosi, CBP, arterite temporale
Farmaci
Sali doro, D-penicillamina, mercurio, trimetadione, probenicid, captopril, FANS,
formaldeide
Malattie metaboliche
Tiroidite, anemia a cellule falciformi, diabete
30) Definite la glomerulonefrite ad IgA
Glomerulonefrite primitiva a patogenesi anticorpo-mediata, con impegno prevalentemente
mesangiale.
Le IgA depositate sono tipicamente polimeriche. Questi depositi si formano in circolo, e
rimangono intrappolati a livello glomerulare a causa di unalterata glicosilazione che ne altera
la clearance e che ne favorisce luptake da parte delle cellule mesangiali (presenza di recettori
per Fc ), facendo produrre citochine che favoriscono la proliferazione mesangiale.
Si manifesta soprattutto con ematuria che pu essere sia macro che microscopica e si pu talora
associare a proteinuria, raramente nel range nefrosico.
31) Riportate la classificazione della nefropatia lupica
Classificazione istologica di Nefrite lupica - 6 classi:
Classe I rene essenzialmente normale anche in microscopio ottico
Depositi mesangiali minimi evidenziabili allimmunofluorescenza
Classe II Glomerulonefrite mesangiale
Aumento della matrice mesangiale
Lieve ipercellularit mesangiale
Membrane basali sono indenne
Classe III Glomerulonefrite proliferativa focale e segmentare
Aree di proliferazione delle cellule di mesangio e endotelio
Presenza di infiltrato infiammatorio
Necrosi e sclerosi
Decorso molto variabile. Sono comuni ipertensione,sedimento urinario e proteinuria,
che nel 25-33% dei pazienti ha valori di range nefrosico
Nel 25% dei pazienti si riscontrano livelli sierici elevati di creatinina
Classe IV Glomerulonefrite proliferativa diffusa
Proliferazione soprattutto delle cellule endoteliali
Infiltrato infiammatorio
Necrosi e sclerosi
Semilune
Sono coinvolti diffusamente oltre il 50% dei glomeruli.
I pazienti di classe IV presentano titoli elevati di anticorpi anti-DNA,bassi livelli
sierici di complemento,ematuria,cilindri eritrocitari, proteinuria,ipertensione e una
ridotta funzionalit renale.
La met dei pazienti ha valori di proteinuria in range nefrosico.
I pazienti che alla biopsia presentano lesioni a semiluna hanno la prognosi peggiore.
Il trattamento deve combinare dosi elevate di steroidi con ciclofosfamide o mofetil
micofelonato.
Classe V Glomerulonefrite membranosa diffusa
Diffuso e marcato ispessimento della membrana basale glomerulare (MBG)
Non si ha presenza di infiltrato infiammatorio
Una sottocategoria delle lesioni di classe V associata a lesioni proliferative ed
talvolta chiamata malattia proliferativa e membranosa mista.
Il trattamento delle lesioni analogo a quello delle lesioni di classe IV.
Il 60% dei pazienti si presenta con sindrome nefrosica o con quantit minori di
proteinuria. Questi pazienti sono predisposti a trombosi delle vene renali e altre
complicanze trombotiche.
Una minoranza di pazienti affetta dalla malattia di classe V si presenta con
ipertensione e disfunzione renale.
Classe VI Glomerulonefrite sclerosante
Glomerulonefriti sclerotici >90%
Fibrosi interstiziale
32) Descrivete le manifestazioni cliniche della nefropatia ad IgA
La nefropatia da IgA una delle forme di nefropatia pi comuni al mondo. Ha una
preponderanza maschile e un picco di incidenza tra la seconda e terza decade di vita. Si tratta di
una glomerulo nefrite mediata da immunocomplessi, definita dalla presenza di immunodepositi
mesangiali diffusi di IgA, spesso associati a ipercellularit mesangiale.
Clinicamente si manifesta con:
40-50% - Ematuria macroscopica spesso associata ad uninfiammazione acuta delle
vie aeree superiori. Lematuria da nefropatia ad IgA tipicamente sincrona ad un
episodio di faringite e febbre, a differenza della glomerulo nefrite post streptococcica
(post faringitica). Gli episodi di macroematuria sono di breve durata (uno o pi giorni),
ma possono recidivare. Sovente si accompagnano con febbre, malessere, astenia, dolori
muscolari e lombari.
30-40% - Ematuria microscopica persistente asintomatica associata a proteinuria e
cilindruria.
<10% - Sindrome nefritica acuta
Porpora di Schonlein Henoch forma sistemica della malattia. Pi frequentemente in
bambini. Clinicamente si ha porpora, artralgie e coinvolgimento intestinale.
Sindrome nefrosica Raramente
Raramente i pazienti si presentano con insufficienza renale acuta e con un quadro
clinico di rapida progressione
La nefropatia da IgA una patologia benigna nella maggior parte dei casi, con una
progressione verso linsufficienza renale che si osserva solo nel 25-30% dei pazienti con pi di
20-25 anni. I fattori di rischio associati alla perdita di funzione renale comprendono:
ipertensione, proteinuria, assenza episodi di macroematuria, et avanzata, lesioni istologiche
gravi.
Trattamento: ACE inibitori, cicli di steroidi associati o non a immunosoppressori.
33) Descrivete le manifestazioni cliniche di glomerulonefrite membranosa
Clinicamente la glomerulonefrite membranosa si manifesta con:
Sindrome Nefrosica
Proteinuria non selettiva
Ipoalbuminemia
Microematuria nel 50% dei casi
Ipertensione arteriosa
Insufficienza renale cronica
Decorso
1/3 dei casi remissione spontanea
1/3 dei casi alternanza remissioni/riacutizzazioni
1/3 dei casi prosegue lentamente verso IRC in 10-15 anni
34) Cosa si intende per ematuria glomerulare e per ematuria urologica e come si
distinguono fra loro queste forme.
Ematuria = GR > 2.000.000/die (2 elementi per campo ad alto ingrandimento)
Ematuria glomerulare presenza di eritrociti nellurina in numero > 2.000.000/die di origine
glomerulare. Le cause pi frequenti sono le glomerulonefriti.
Ematuria urologica presenza di eritrociti nellurina, pi di 70% normali di origine tubulare o
non glomerulare. Cause: i traumi,la litiasi renale,le infezioni delle vie urinarie e le neoplasie del
rene e delle vie urinarie.
Diagnosi differenziale fra loro:
Se il sedimento urinario rileva ematuria: guardare gli eritrociti se sono normali o
dismorfici e un eventuale presenza di proteinuria.
Se si ha proteinuria e Globuli rossi dismorfici >70% - Ematuria glomerulare
Se non si ha proteinuria e Globuli rossi normali >70% - Ematuria urologica
Caratteristiche di ematuria glomerulare sono:
Cilindri eritrocitari
Acantociti >5% - Si ritiene che la presenza di protuberanze o estroflessioni sulla
superficie dei globuli rossi (acantocitosi) sia altamente suggestiva della loro
origine glomerulare. Tuttavia la presenza di acantociti un indicatore
relativamente poco sensibile di microematuria glomerulare perch ha una
sensibilit di appena il 52%. Daltra parte lassenza di acantociti dal sedimento
urinario un rilievo importante in quanto ha una specificit del 98% che consente
di escludere con alta probabilit lematuria glomerulare.
Globuli rossi poveri in emoglobina >70%
La presenza di cilindri eritrocitari e proteinuria > 500 mg/die conferma lorigine
glomerulare dellematuria
Certamente non problematico definire lorigine dellematuria quando al sedimento urinario le
emazie sono uniformemente inalterate o uniformemente dismorfiche. Tuttavia nella pratica
clinica il sedimento pu mostrare un mix di emazie in parte normali e in parte alterate che
rende meno certa linterpretazione (ematuria mista o indeterminata)
35) Indicate quali sono le cause pi comuni di microematuria glomerulare isolata
Le cause pi comuni di ematuria glomerulare isolata sono:
Nefropatia da depositi mesangiali di IgA: patologia caratterizzata dallespansione del
mesangio ,talvolta ipercellularit mesangiale e immunodepositi mesangiali. Si presenta
clinicamente con vari gradi di proteinuria e,comunemente,con ematuria. Pu essere
secondaria a nefropatia da IgA, alla malaria da P. falciparum, nella glomerulonefrite
post infettiva in via di risoluzione. Il decorso pu essere benigno (in caso di ematuria
isolata) o andare verso linsufficienza renale occasionalmente,specie se presente una
pesante proteinuria.
Nefrite ereditaria ( sindrome di Alport): si riscontra ematuria,assottigliamento e
sdoppiamento della GBM, proteinuria moderata e glomerulo sclerosi cronica. Patologia
dovuta nell85% dei casi a mutazioni ereditarie X-linked a carico della catena 5 del
collagene. Un 15% di pazienti presenta alterazioni delle catene 3 e 4 del collagene
(forma autosomica recessiva).
Malattia delle membrane basali sottili (ematuria benigna familiare) :membrane basali
del glomerulo diffusamente sottili. Talvolta vi pu essere proteinuria modesta o
macroematuria.
36) Come si classifica la proteinuria
La proteinuria pu essere classificata :
Secondo lintensit (g/24ore)
Lieve < 0,5
Moderata 0,5-3,5
Grave > 3,5
Secondo caratteri clinici :
Isolata
Intermittente
Persistente
In base alla patogenesi :
Proteinuria glomerulare
Proteinuria da overflow
Proteinuria tubulare
Proteinuria glomerulare: deriva da unalterazione della membrana di filtrazione
glomerulare ed quindi indice di patologia glomerulare. Il meccanismo prevede
liperfiltrazione di macromolecole (albumina) attraverso unalterata membrana di
filtrazione.
La proteinuria glomerulare viene definita selettiva quando il glomerulo, nonostante
laumentata permeabilit, trattiene ancora le proteine plasmatiche di dimensioni
molecolari particolarmente elevate.
Nella proteinuria non selettiva consentito il passaggio di tutte le proteine
(composizione proteica urinaria ricalca quella plasmatica).
Proteinuria da overflow: le proteine a basso peso molecolare sono in grado di attraversare
in una certa misura la membrana di filtrazione e di passare nel filtrato glomerulare. In
seguito, esse sono demolite da proteasi e peptidasi della membrana tubulare e riassorbite da
carriers dellepitelio tubulare. Quando la quota di queste proteine a basso peso molecolare
aumenta in modo eccessivo, aumenta la loro concentrazione nel filtrato e la capacit di
riassorbimento tubulare viene superata. Pertanto tali proteine compaiono nelle urine.
Lesempio pi noto la proteinuria di Bence-Jones in corso di gammopatia monoclonale.
Proteinuria tubulare: dovuta ad unincapacit del tubulo renale a riassorbire le proteine
filtrate attraverso il glomerulo. Tra le proteine eliminate con le urine, in questo tipo di
proteinuria risultano tipicamente aumentate talune proteine plasmatiche con Mr
relativamente bassa (1 microglobulina, 2 microglobulina, lisozima).
La proteinuria pu inoltre essere:
Funzionale (scompenso cardiaco congestizio, febbre, sforzo fisico, convulsioni, ecc)
Ortostatica: assente nelle urine emesse dopo il riposo notturno ma compare dopo
aver assunto la posizione eretta per un certo tempo.
Le proteine presenti nelle urine in questi casi sono quelle normalmente presenti in circolo,
ma il fenomeno ha quasi sempre significato benigno. Queste condizioni vanno tenute ben
presenti per evitare di diagnosticare una glomerulonefrite in un soggetto che presenta
proteinuria perch ad esempio ha avuto la febbre o svolto attivit sportiva.
37) Cosa si intende per GN rapidamente progressiva?
Forma di nefrite caratterizzata da un rapido deterioramento della funzione renale, per accumulo
di cellule infiammatorie e materiale fibrinoide nello spazio di Bowman del glomerulo, con
successiva formazione di numerose semilune, per cui la GN definita proliferativa diffusa
extracapillare. La creatinina sierica aumenta rapidamente a causa dellinfiammazione a
sviluppo rapido.
38) Quali sono le forme anatomocliniche principali di glomerulonefrite rapidamente
progressiva e come si distinguono fra loro.
Esistono tre forme di GNRP, distinguibili grazie agli studi ad immunofluorescenza su prelievo
bioptico:
I Glomerulonefrite da anticorpi anti MBG
Deposizione a livello della MBG di anticorpi diretti verso antigeni strutturali
specifici di MBG (contro collagene IV).
il danno pu coinvolgere solo il rene, oppure estendersi anche al polmone
(Sindrome di Goodpasture, la presenza di emottisi pu essere utile per la
diagnosi).
L'immunofluorescenza rivela il tipico quadro a fumo di sigaretta.
Clinicamente: oligoanuria preceduta da febbre con artralgie e mialgie
II Glomerulonefrite da immunocomplessi
Depositi di IgG e complemento sulla MB e nel mesangio
Climincamente: febbre, malessere, ipertensione
III Glomerulonefrite Paucimmune
Presenza in circolo di anticorpi ANCA (p-ANCA anti-MPO, c-ANCA anti-
proteasi 3)
Assenza di depositi immuni sul glomerulo
Clinicamente: stanchezza, febbre, astenia, calo ponderale, malessere, artromialgie
39) Indicate quali sono le terapie usate nel trattamento della sindrome nefrosica
idiopatica
Dieta ipoproteica e iposodica
Somministrazioni di albumina
Diuretici tiazidici
Antialdosteronici e corticosteroidi
ACE inibitori
Eparina o aspirina
Immunosoppressori
40) Descrivete l'iter diagnostico della sindrome nefrosica nel paziente adulto
Sintomatologia clinica (vedi domanda 26)
Esami di laboratorio
Protidemia con elettroforesi (ipoproteinemia e ipoalbuminemia)
colesterolemia e trigliceridemia (ipercolesterolemia e ipertrigliceridemia, sierico
LDL e VLDL)
creatininemia,
calcemia,
proteinuria nelle 24 ore (>3,5g/24h conferma sindrome nefrosica)
analisi delle urine per valutare sodio urinario e sedimento
Biopsia renale
41) Indicate le pi comuni complicanze della sindrome nefrosica
Ipovolemia che porta a Edema stato anasarcatico, e ipotensione posturale
Perdita IgG e fattore B properdina aumento suscettibilit alle infezioni
Perdita transferrina anemia
Perdita Zn e Cu malnutrizione
Perdita antitrombina III e aumento di fibrinogeno contenuto nel sangue e di fattore V,
VII, VIII, IX, attivatore del plasminogeno e TBX trombosi. Contribuiscono anche
limmobilizzazione a letto ed emoconcentrazione.
Iperlipidemia aterosclerosi
Perdita di proteine leganti vitamina D ipocalcemia, iperparatiroidismo
Perdita globulina ipotiroidismo
Perdita di ormoni steroidei ipocorticismo
42) Descrivete le pi comuni manifestazioni della GN post-streptococcica
GN post-streptococcica si manifesta con una sindrome nefritica acuta
Esordio brusco caratterizzato da:
Ematuria macroscopica
Cefalea
Nausea e vomito
Anoressia e malessere generale
Il declino improvviso della funzione renale si manifesta con:
Oliguria
Edemi
Ipervolemia e ipertensione
Lesame delle urine mostra sedimento di tipo nefritico:
Ematuria macroscopica
Cilindri eritrocitari
Piuria
Proteinuria sub-nefrosica
43) Quali son le pi frequenti GN che si manifestano con IRRP
Generalmente GN proliferativa extracapillare GN a semilune.
Le GN pi importanti che si manifestano con questo aspetto sono:
GN anti GBM (primitiva)
GN con semilune idiopatica isolata (primitiva)
GN secondarie a vasculiti ( Sindrome di Weneger, Sindrome di Churg-Strauss,
Micropoliarteriti)
44) Indicate le principali cause secondarie di FSGS.
Infezioni virali (HIV, HBV)
Farmaci (analgesici, eroina)
Neoplasie (linfomi)
Malattie congenite renali (malattia di fabry, malattia di charcot-marie-tooth)
Ridotta massa renale (agenesia renale monolaterale, ablazione chirurgica)
Uropatia ostruttiva
Reflusso vescico ureterale
Obesit grave
Trapianto renale
45) Quali sono i valori normali di proteinuria delle 24h nel pz adulto
46) Quali sono i valori normali di proteinuria delle 24h nel pz adulto
Per proteinuria si intende la perdita di proteine con lurina. Fisiologicamente, tutti noi perdiamo
una certa quota di proteine al giorno, non superiore a 150 mg/24 h. E importante che la misura
delle proteinuria sia ottenuta mediante la raccolta delle 24 h; lesame standard delle urine
infatti inattendibile, poich strettamente correlato alla concentrazione delle urine di quella
particolare minzione. I 150 mg di proteine fisiologicamente perse al giorno, sono soprattutto
proteine tubulari.
Le proteine del sangue (soprattutto lalbumina) non devono essere presenti nelle urine, in
quanto la membrana di filtrazione glomerulare strutturata in modo da non lasciare passare
proteine di dimensioni superiori a 150 KDa.
Le proteine tra 70 e 150 potrebbero in teoria passare, ma la carica negativa della membrana
respinge a sua volta proteine cariche negativamente come lalbumina. Il limite superiore di
perdite di albumina con lurina oggi stato fissato al limite inferiore per la microalbuminuria,
ovvero <30 mg/24h.
47) Proteinuria da overflow: descrivete la patogenesi, le forme principali, le possibili
conseguenze a livello renale e gli esami utili per la diagnosi
Patogenesi:
Le proteine a basso PM sono in grado di attraversare in un certo grado la membrana di
filtrazione glomerulare e di passare il filtrato glomerulare. In seguito esse sono demolite da
proteasi e peptidasi della membrana tubulare e riassorbite da carriers dellepitelio tubulare.
Quando la quota di queste proteine aumenta eccessivamente, aumenta la loro quota nel filtrato
glomerulare e la capacit di riassorbimento tubulare (Tmax) viene superata, pertanto tali
proteine compaiono nelle urine e si ha una proteinuria da overflow o sovraccarico.
Forme:
Tipici esempi sono dati da:
Mioglobina proteina muscolare rilasciata in circolo in corso di malattie muscolari
scheletriche e infarto acuto del miocardio,
Emoglobina in corso di malattie emolitiche per saturazione dellaptoglobina,
La proteinuria di Bence-Jones in corso di gammapatia monoclonale.
La proteinuria di Bence-Jones associata a lesioni a livello renale nella maggior parte dei casi
(rene da mieloma) e marcata anemia. Il 25% dei pazienti sviluppa insufficienza renale acuta
(per ostruzione dei tubuli da parte di cilindri contenenti catene leggere o infiltrazione da parte
di plasmacellule mielomatose) e cronica. Il 20% dei pazienti sviluppa sindrome nefrosica, con
una caratteristica saliente rappresentata dalliperprotidemia (solitamente nelle altre forme di
sindrome nefrosica c ipoprotidemia).
Alterazioni a livello renale sono presenti in pi del 50% dei pazienti.
Ci pu essere:
coinvolgimento glomerulare con glomerulosclerosi nodulare
danno tubulare con comparsa di anemia di Fanconi ( acidosi tubulare , glicosuria,
aminoacidemia, ipokaliemia, ipofosfatemia, ipouricemia ,proteinuria)
tubulopatia ostruttiva
danno vasale di tipo amiloidosico (deposizione di proteine fibrillari patologiche ).
Diagnosi
Per quanto concerne la diagnosi i metodi elettroforetici sono dimportanza assoluta
nellindividuazione della proteinuria di Bence-Jones. Infatti la proteinuria dipstick- negativa e
le tecniche di elettroforesi, compresa la capillare, limmunoelettroforesi, limmunofissazione
elettroforetica, sono lunico metodo in grado di evidenziare la morfologia delle catene leggere
libere, consentendo diagnosi in caso di monoclonalit. Pu essere richiesta la biopsia renale e
del midollo osseo per conferma.
48) Cosa si intende e come si diagnostica una proteinuria tubulare
La proteinuria tubulare costituita da proteine plasmatiche di basso PM o microglobuline.
Queste proteine (PM< 50000Da) sono liberamente filtrate dal glomerulo a causa delle loro
piccole dimensioni come la beta2microglobulina e lalfa1microglobulina, lisozima, la RBP
(retinol binding globulin).
Patologie tubulointerstiziali possono determinare danno tubulare e conseguente deficit di
riassorbimento delle proteine filtrate. Si avr cos proteinuria tubulare.
Diagnosi - Si fonda su:
esame delle urine basato sulluso di dipstickis (strisce reattive)
sulle urine delle 24h
sulle prime urine del mattino( rapporto proteine-creatinina v. n. = 0,2).
La valutazione qualitativa si fonda sullesame elettroforetico delle proteine urinarie
49) Indicate le pi comuni cause di microalbuminuria nel soggetto non diabetico ed il
significato clinico della sua presenza
La microalbuminuria assume una particolare rilevanza clinica in quanto spesso il primo segno
di comparsa della nefropatia diabetica.
Esistono comunque altre patologie che possono determinare microalbuminuria e fra queste si
ricorda:
l'ipertensione arteriosa
la cirrosi epatica
l'insufficienza cardiaca
il lupus eritematoso sistemico.
La microalbuminuria considerata parametro affidabile predittore di rischio cardiovascolare.
Deriva da un danno vascolare che si instaura in pazienti ipertesi, fumatori, obesi come segno di
uniperfiltrazione compensatoria.
La persistenza di microalbuminuria esprime la presenza di lesioni glomerulari istologicamente
evidenti.
50) Elencate le cause principali di nefrite tubulo interstiziale cronica
La nefrite tubulointerstiziale cronica un processo patologico prettamente a carico dei tubuli e
dellinterstizio renale, caratterizzato da fibrosi interstiziale, un infiltrato di cellule
mononucleate, presenza di atrofia, dilatazione dei lumi e ispessimento della membrana basale.
Le cause di nefrite tubulointerstiziale cronica possono essere schematizzate in :
malattie renali ereditarie (rene policistico, malattia cistica midollare, rene a spugna
midollare)
tossine esogene (nefropatia da analgesici, da piombo, da litio, da ciclosporina e altri
metalli pesanti)
alterazioni metaboliche (iperuricemia, ipercalcemia, ipokaliemia, cistinosi, malattia di
Fabry)
malattie autoimmuni (sindrome di Sjogren)
neoplasie (leucemie, linfomi, mieloma multiplo)
altre malattie ( pielonefrite cronica, ostruzione cronica delle vie urinarie, nefropatia da
anemia a cellule falciformi, nefrite da radiazioni, nefropatia dei Balcani, malattia
tubulointerstiziale secondaria a danno glomerulare vascolare)
51) Quali sono le manifestazioni cliniche e le indagini necessarie per diagnosticare la
nefrite tubulo interstiziale acuta allergica
La nefrite tubulointerstiziale acuta allergica deriva da reazioni di ipersensibilit a svariati
farmaci tra cui betalattamici, sulfonamidi, antitubercolari tra cui isoniazide e rifampicina,
allopurinolo, FANS e inibitori COX-2, inibitori di pompa protonica.
Clinica:
Improvviso e inaspettato deterioramento della funzione renale a 2-3 settimane dallinizio
della terapia con il farmaco
Febbre, rash cutaneo maculo-papulare, artralgie, eosinofilia
Dolore lombare
Il quadro clinico si pu confondere con quello di una glomerulonefrite acuta, ma comparsa
IRA, ematuria, eosinofilia pi altri sintomi fa pensare che sia pi probabile una nefrite tubulo-
interstiziale acuta.
Lesame del sedimento urinario:
Microematuria
Macroematuria in 1/3 dei casi
Leucocituria
Proteinuria variabile in genere lieve o moderata tranne nei casi indotti dai FANS
inibitori di COX-2
Occasionalmente presenti eosinofili
Segni di disfunzione tubulare
Acidosi tubulare prossimale
Glicosuria
Aminoaciduria
Uricosuria
Isostenuria
Biopsia Renale diagnosi di certezza
Si osservano lesioni nellinterstizio, dove sono presenti marcato edema, infiltrato di
polimorfonucleati, linfociti, plasmacellule e anche grande quantit di eosinofili.
Se il quadro grave si possono individuare necrosi e rigenerazione delle cellule tubulari
Gli studi con tecniche di immunofluorescenza o si sono rivelati negativi o hanno dimostrato
deposizione di Ig e complemento lungo la membrana basale tubulare.
52) Indicate i meccanismi principali implicati nella patogenesi della nefropatia diabetica
La nefropatia diabetica una complicanza cronica sia del diabete mellito di tipo 1 sia di tipo 2,
alla cui patogenesi concorrono:
- i fenomeni che attraverso liperglicemia cronica portano a danno microangiopatico
(analogamente a quanto si verifica negli altri organi e apparati)
- lipertensione glomerulare specifica per il rene
Liperglicemia cronica attraverso
lattivazione della via dei polioli e conseguente accumulo di sorbitolo,
lincremento del meccanismo di glicazione non enzimatica di proteine strutturale e
enzimi con conseguente formazione di AGE (advanced glycation endproducts),
lattivazione della fosforilazione ossidativa con formazione di intermedi reattivi
dellossigeno e conseguente stress ossidativo,
determina
attivazione illegittima delle molecole di segnalazione cellulare, con attivazione delle
proteinchinasi C,
alterata espressione dei geni e alterata funzione proteica.
Da qui deriva disfunzione e danno cellulare: angiogenesi abnorme, iperpermeabilit delle
membrane, flusso sanguigno abnorme, ispessimento della membrana basale.
Ipertensione glomerulare
La pressione glomerulare dipende dalla pressione arteriosa sistemica e dalla sua modulazione
tramite il tono delle arteriole afferente ed efferente.
A parit della pressione arteriosa:
pressione glomerulare aumenta per vasodilatazione dellarteriola afferente o
vasocostrizione dellarteriola efferente
pressione glomerulare diminuisce per vasocostrizione dellarteriola afferente e/o
vasodilatazione dellarteriola efferente
Nel diabetico si ha un aumento di GFR per iperglicemia.
Leccesso di glucosio filtrato viene riassorbito nel tubulo prossimale dal sistema di cotrasporto
Na+/glucosio.
Questo pu portare a due conseguenze importanti nella patogenesi di nefropatia diabetica:
1) accumulo di sodio e quindi di acqua con espansione di volemia provoca stimolazione dei
recettori di stiramento atriale e secrezione cardiaca di ANP, potente vasodilatatore
dellarteriola afferente. Quindi aumento della pressione glomerulare e del GFR.
2) Ridotta quantit di Na+ che raggiunge la macula densa in conseguenza delleccessivo
riassorbimento prossimale modifica il feedback tubulo-glomerulare, attivando i
meccanismi (angiotensina) che portano alla vasocostrizione dellarteriola efferente.
Lipertensione glomerulare tra i principali determinanti del danno a carico della membrana
glomerulare e quindi dellinsorgenza della nefropatia diabetica.
Nella patogenesi della nefropatia diabetica concorre anche liperproduzione di citochine e
fattori di crescita (GH, IGF-1, TGF beta, PGDF, FGF, VEFG, TNF alfa, prostaglandine,
trombossani, angiotensina II, endotelina).
53) Riportate la classificazione in stadi di nefropatia diabetica
Stadio Denominazione Clinica Patogenesi
I Iperfiltrazione Poliuria, glicosuria
Microalbuminuria reversibile
GFR>160ml/min
Pressione arteriosa normale
Aumento volume glomeruli
Aumento pressione
intraglomerulare
II Nefropatia
silente
Escrezione renale albumina
normale (microalbuminuria)
GFR normale o aumentato
Pressione arteriosa normale
Aumento sintesi di membrana
basale
Aumento volume mesangiale
III Nefropatia
incipiente
(a 5-10 anni da
diagnosi)
Microalbuminuria elevata (30-
300 mg/die)
GFR normale
Pressione arteriosa normale o
aumentata
Notevole ispessimento
membrana basale e volume
mesangiale.
Inizio occlusione glomerulare
IV Nefropatia
conclamata
(10-20 anni da
diagnosi)
Macroalbuminuria
GFR ridotto o normale
Ipertensione
Ulteriore aumento di membrana
basale e mesangio
Accentuazione dellocclusione
Obliterazione di parte dei
glomeruli con ipertrofia di
quelli residui
V Uremia
(insufficienza
proteinuria,
aumento di AER(escrezione
Obliterazione generalizzata di
glomeruli
renale)
(25-30 anni da
diagnosi)
renale di albumina)
flusso renale <10 ml/min
ipertensione severa
54) Definite la nefropatia diabetica incipiente
Stadio III della nefropatia diabetica che precede la comparsa di manifestazioni cliniche e
caratterizzato da:
presenza di microalbuminuria ( 20-200 microgr/min o 30-300 mg/die),
GFR normale
PA normale o discretamente aumentata.
Sono presenti evidenti segni di alterazione glomerulare come aumento dello spessore della
membrana basale e espansione mesangiale, questultima espressione della perdita dei podociti.
55) In quali condizioni patologiche possibile rilevare una microalbuminuria
Per microalbuminuria si intende la perdita di albumina nelle urine compresa tra i 30 e i 300 mg
nelle 24 h. Una microalbuminuria sempre segno di alterazione a livello renale.
tipica della nefropatia incipiente o stadio 3 della nefropatia diabetica come conseguenza
delliperfiltrazione. Inizialmente intermittente, per poi diventare persistente e
ingravescente. Si tratta infatti di un danno pregressivo causato dalliperglicemia che
interessa tutti i nefroni, che pu evolvere a proteinuria e raramente anche a sindrome
nefrosica.
Nonostante sia segno di alterazione renale, una certa quota di soggetti presenta
microalbuminuria in assenza di patologia renale. Essa in questo caso deriva da un danno
vascolare che si instaura in pazienti ipertesi, fumatori, obesi come segno di
uniperfiltrazione compensatoria. La microalbuminuria, quindi considerata parametro
affidabile predittore di rischio cardiovascolare.
56) Indicate il significato prognostico della microalbuminuria nel pz. con diabete
tipo 1, diabete tipo 2 e con altre condizioni morbose diverse da diabete
Diabete tipo 1
Il segno pi precoce di nefropatia diabetica rappresentato dalla microalbuminuria. Circa il
15% dei pazienti normoalbuminurici con DM tipo 1 da almeno 7 anni sviluppano
microalbuminuria. In assenza di terapia specifica, l80% dei pazienti diabetici tipo 1 che
sviluppa microalbuminuria persistente presenta un incremento dellAER e una velocit di circa
il 10-20 % allanno fino a raggiungere stadio di nefropatia conclamata (albumina > 300 mg/die)
in circa 10-15 anni. Nel frattempo il paziente diventa iperteso e presenta graduale riduzione del
GFR. Il 50% dei pazienti diabetici tipo 1 con nefropatia conclamata raggiunge lERSD entro 10
anni e pi del 75% entro 20 anni.
Diabete tipo 2
I pazienti con DM di tipo 2 presentano invece microalbuminuria gi al momento della diagnosi,
perch il diabete presente gi da diversi anni e perch pu essere provocata anche da cause
concomitanti (obesit). Senza terapia specifica, il 20-40% dei pazienti con microalbuminuria
sviluppa nefropatia conclamata, ma nei 20 anni successivi solo il 20 % di questi raggiunge
lERSD (anche perch lelevata mortalit cardiovascolare nei pazienti con DM2 riduce il
numero di pazienti che raggiungono lERSD).
Altre condizioni
Alcuni soggetti presentano microalbuminuria in condizioni diverse dal diabete, in questo caso
essa deriva da un danno vascolare che si instaura in pazienti ipertesi, fumatori, obesi, con
dislipidemia, come segno di infiltrazione compensatoria. La microalbuminuria quindi pu
essere considerata parametro affidabile predittore di rischio cardiovascolare.
57) Cosa si intende per microalbuminuria e come possibile misurarla
Per microalbuminuria si intende la perdita di albumina nella urine compresa tra i 30 e i 300 mg
nelle 24 h. oltre i 300 mg/die si parla di proteinuria. Questi valori hanno un significato pratico :
da 300 mg/die lalbumina diventa identificabile anche allesame standard delle urine, mentre al
di sotto evidenziabile solo richiedendo dosaggio specifico per la microalbuminuria.
Questultimo pu essere effettuato attraverso tre metodiche:
misurazione rapporto albumina-creatinina
raccolta urine nelle 24h con misurazione contemporanea della creatininemia perla
simultanea determinazione della clearance della creatinina
raccolta urinaria overnight
La misurazione del rapporto albumina-creatinina pratica ma imprecisa, la raccolta delle urine
nelle 24h e quella overnight sono le pi usate e da preferirsi a causa della nota variabilit
circadiana dellescrezione urinaria di albumina.
58) Indicate i principali provvedimenti terapeutici necessari in un pz. con nefropatia
diabetica incipiente ed i parametri di laboratorio da monitorizzare per valutare
lefficacia della terapia.
In un paziente con nefropatia diabetica incipiente, lindividuazione della microalbuminuria in
uno stadio precoce, consente di istituire una terapia efficace. Lo screening per la
microalbuminuria deve essere effettuato nei pazienti con DM di tipo 1 da almeno 5 anni e in
quelli con diabete di tipo 2 (in quanto gi presente al momento della diagnosi) e comprende
misurazioni annuali della creatinina per stimare il GFR.
Gli interventi efficaci nel rallentare la progressione della microalbuminuria verso la nefropatia
conclamata e nei casi pi gravi lERSD comprendono :
Misure volte a portare la glicemia a valori basali ( lemoglobina glicata deve essere
mantenuta sotto il 7%)
Stretto controllo pressorio (al di sotto di 130/80 mmHg ) e somministrazione di ACE-
inibitori e ARB, farmaci che pi di altri riducono la pressione di filtrazione e quindi
consentono di contenere il danno meccanico glomerulare.
trattamento della dislipidemia ( mantenere colesterolo LDL <100mg/dl e somministrare
statine)
abolizione del fumo
restrizione dietetica di proteine nel paziente con GFR >60 ml/min ( ha i suoi sostenitori
e detrattori in quanto non facile prescrivere una dieta ipoproteica ad un soggetto che
deve
59) Indicate le principali cause di morte del paziente sottoposto a trapianto di rene
Il paziente sottoposto a trapianto renale pu andare incontro a morte per svariate cause. La
mortalit :
del 37% per quanto concerne le cause cardiovascolari (vedi domanda 70)
del 7% per attacchi ischemici transitori
il 20% per gravi infezioni(vedi domanda 60)
del 13% per linsorgenza di neoplasie (vedi domanda61)
controllare anche lintroito glucidico e lipidico)
60) Indicate le principali infezioni che colpiscono il paziente trapiantato dal primo al
sesto mese dopo lintervento
La terapia immunosoppressiva cui sottoposto il paziente trapiantato, gravata dalla terribile
complicanza dellinsorgenza di infezioni opportunistiche. I segni e i sintomi di infezione
talvolta possono risultare anche mascherati o atipici. comune linsorgenza di febbre.
Le infezioni batteriche (legionellosi, Listeriosi) sono pi frequenti nel primo mese
post trapianto.
Particolarmente pericolose sono le polmoniti a decorso rapido che possono
portare a morte il paziente entro 5 giorni dallesordio. In tal caso necessario
sospendere il trattamento immunosoppressorio ad eccezione della terapia con
prednisone.
In caso della temibile infezione di pneumocystic carinii il trattamento di scelta
il trimetoprim-sulfametossazolo, che si rivelato abbastanza efficace.
Linfezione da Citomegalovirus frequente e pericolosa nei soggetti trapiantati. In
genere si evidenzia dopo il primo mese dal trapianto e linfezione attiva spesso confusa
e associata a episodi di rigetto.
I pazienti pi ad alto rischio per infezione grave da CMV sono quelli privi di
anticorpi anti CMV che ricevono rene da un donatore positivo per anticorpi anti
CMV.
La diagnosi precoce in un soggetto con sospetto clinico e febbre pu essere
attuata ricercando nel sangue la carica virale di CMV. Anche laumento di IgM
diagnostico .
Lesame colturale pu risultare meno sensibile.
Linvasione tissutale da CMV pi frequente a livello gastroenterico e
polmonare, se non trattata pu comportare retinopatia da CMV.
Altre infezioni in corso di trattamento immunosoppressivo sono quella del virus epatico
B e C, EBV, adenovirus, papillomavirus, ecc.
61) Caratterizzate il rischio neoplastico del paziente sottoposto a trapianto di rene
Lincidenza di neoplasie maligne nei pazienti in terapia immunosoppressiva del 5-6%,
approssimativamente 100 volte maggiore di quella della popolazione generale. I rischi
aumentano proporzionalmente alla dose totale di immunosoppressivi e al tempo trascorso dal
trapianto.
Le neoplasie pi comuni sono:
il sarcoma di kaposi ( incidenza pi alta di400-1000 volte),
le neoplasie cutanee (180 volte), labiali( 29 volte), genitali e anali (20 volte),
i linfomi soprattutto non Hodgkin (28-49 volte),
carcinoma epatico (20-38 volte).
Minor incidenza hanno il carcinoma della mammella, della prostata, del polmone, del
colon-retto, stomaco, vescica
62) Quali sono le classi di antigeni di istocompatibilit utilizzate nella pratica clinica?
Gli antigeni HLA sono codificati da un cluster di geni del complesso maggiore di
istocompatibilit sul braccio lungo del cromosoma 6. Si distinguono gli antigeni HLA di classe
I e quelli di classe II.
Gli antigeni di classe I constano di una catena alfa biallelica che viene espressa sulla
membrana in associazione con beta2microglobulina. Esistono diversi loci HLA di classe
I cui corrispondono altrettanti alleli : HLA-A, HLA-B, HLA-C, HLA- E, HLA-F, HLA-
G.
Vi sono poi le molecole di classe II, ciascuna costituita da due catene, (una alfa e una
beta) bialleliche che possono combinarsi in modo vario ( es. catena alfa di un allele con
la beta di un altro allele) questi alleli sono HLA-DP, HLA-DQ, HLA-DR.
Per cui ogni individuo eredita dai propri genitori un aplotipo ( un pacchetto genico di catene
alfa e beta associate) materno e paterno.
Le molecole MHC servono per far si che i linfociti T specifici per un determinato antigene
riconoscano tale antigene e montino una risposta immunitaria specifica contro di esso. Perch
questo si verifichi necessario che:
- i linfociti T riconoscano solo antigeni non self
- i linfociti T riconoscano i peptidi antigenici solo quando presentati da molecole MHC self.
63) Cos il cross-match e quando si esegue?
Il cross-match, indagine finale una volta selezionato il potenziale ricevente del trapianto renale,
consente di valutare la reazione esistente tra siero del ricevente e linfociti B e T del donatore.
Un cross-match positivo solitamente indicativo di rigetto iperacuto. I linfociti T del donatore,
che esprimono solo antigeni di classe I, vengono usati come bersaglio per la rilevazione di
anticorpi anti classe I. Anche la presenza di anticorpi preformati contro antigeni di classe II
(HLA-DR) diretti contro epitopi del donatore comportano un rischio maggiore di perdita del
rene dopo il trapianto (per eseguire questo test si usano i linfociti B che esprimono sia antigeni
di classe I sia II). Il cross-match esplora anche antigeni non presenti a livello linfocitario come
lABO, lRh non presente nel tessuto di rene trapiantato) e il kell.
64) Quali sono gli esami che vengono eseguiti nel laboratorio di immunogenetica nel
paziente in attesa di trapianto di rene?
Gli esami eseguiti nel laboratorio di immunogenetica nel paziente in attesa di trapianto sono :
tipizzazione tissutale
screening anticorpale
cross-match pretrapianto
La tipizzazione HLA viene effettuata nei pazienti in attesa di trapianto, sul donatore al
momento di prelievo dellorgano e su tutti i candidati donatori ( parenti e non). Si articola in
due tipi di indagine :
Tipizzazione sierologica che si avvale di sieri specifici per identificare gli antigeni
di classe I ( A, B, Cw) e di classe II ( DP, DQ, DR)
Tipizzazione molecolare, indagine che consente di sequenziare i loci corrispondenti
ai vari alleli al fine di identificare gli specifici aplotipi.
Tra le tre coppie di HLA del donatore e quelle del ricevente possono quindi essere presenti
da 0 a 6 mismatch. Pi alto il numero di mismatch pi alto il rischio di rigetto acuto e
minore la compatibilit.
Lo screening anticorpale si pone essenzialmente due obiettivi :
individuare anticorpi anti HLA nel siero del paziente
se sono presenti anticorpi, individuare verso quale antigene sono diretti, verso
quale particolare aplotipo, di che classe sono e quanti sono.
Segue infine il cross-match che consiste nella valutazione della reattivit esistente tra siero
del ricevente e linfociti B e T del donatore (vedi domanda 63)
65) Elencate i farmaci principali attualmente utilizzati nella terapia immunosoppressiva
di Induzione
La terapia immunosoppressiva di induzione precede il trapianto, volta a provocare uno stato
di immunosoppressione profondo per far si che lorgano attecchisca senza che si verifichi
rigetto acuto. I farmaci usati sono:
Corticosteroidi
mauronomab (anti CD3), dachizumab, basiliximab(anti CD25)
ATG
66) Elencate i farmaci principali attualmente utilizzati nella terapia immunosoppressiva
di Mantenimento
La seconda fase della terapia immunosoppressiva quella di mantenimento, che sar proseguita
indefinitamente per ottenere uno stato di tolleranza immunitaria e per prevenire il rigetto. Il
regime di mantenimento si fonda sulluso di:
inibitori della calcineurina
inibitori di mTOR
antimetaboliti (azatioprina, mofetil-micofenolato)
corticosteroidi a basse dosi
Gli schemi terapeutici variano a seconda della fase, dei segni di rigetto e delle singole
situazioni.
67) Quali sono i principali effetti collaterali dei farmaci immunosoppressivi?
I farmaci immunosoppressivi a nostra disposizione sopprimono in genere tutti gli aspetti della
risposta immunitaria, inclusa quella verso batteri, funghi, virus e tumori maligni. Per questo,
nonostante lampia gamma di farmaci, questi possono favorire la comparsa di infezioni e
neoplasie, nonch effetti collaterali avversi.
Glucocorticoidi
Gli effetti collaterali dei glucocorticoidi, quali il ritardo della guarigione delle ferite e la
predisposizione a infezioni, rendono importante la riduzione della dose nellimmediato periodo
postoperatorio. Molti centri addirittura ne sospendono luso a causa degli effetti collaterali a
lungo termine sullosso (osteoporosi), del metabolismo glucidico e lipidico (IGT, diabete,
dislipidemie, ipertensione).
Lazatioprina determina soppressione midollare con conseguente leucopenia, anemia,
trombocitopenia oltre a determinare alopecia ed ittero.
Il mofetil-micofenolato caratterizzato da un certo grado di tossicit gastrointestinale ( diarrea,
crampi), tossicit epatica e minima soppressione del midollo osseo.
La ciclosporina ha una potente attivit immunosoppressiva ma gravata da potenti effetti
collaterali: nefrotossicit, epatotossicit, irsutismo, tremore, iperplasia gengivale, diabete. La
nefrotossicit costituisce un problema difficilmente gestibile, tanto che riduce luso del farmaco
solo nel periodo in cui il rene abbia raggiunto un certo grado di funzionalit.
Il tacrolimus, macrolide fungino, presenta stesso meccanismo dazione e stessi effetti
collaterali della ciclosporina, non provoca per irsutismo e iperplasia gengivale. Linsorgenza
del diabete pi comune con luso di tacrolimus.
Il sirolimus anchesso un macrolide fungino e come effetti collaterali presenta iperlipidemia
e trombocitopenia
68) Quali sono i segni e sintomi che inducono al sospetto di rigetto acuto?
Il rigetto acuto, che pi frequente nei primi mesi post trapianto, caratterizzato da:
un brusco peggioramento dei parametri di funzionalit renale ( soprattutto aumento
creatinina sierica, proteinuria)
contrazione della diuresi (anche non presente)
aumento della pressione arteriosa.
Nei casi pi severi si accompagna a febbre, sudorazione intensa e senso di tensione e
dolorabilit nella zona dellorgano trapiantato
69) Come si diagnostica il rigetto acuto?
Una diagnosi precoce di rigetto acuto permette di iniziare prontamente la terapia per preservare
la funzione renale e prevenire danni irreversibili.
La diagnosi si fonda sul sospetto clinico e sulla biopsia renale.
Clinica
Il rigetto pu manifestarsi con un incremento della creatinina sierica con o senza riduzione del
volume urinario. Ci pu essere febbre e senso di tensione nellarea dellorgano trapiantato.
Biopsia renale
La diagnosi certa di rigetto acuto richiede la biopsia renale, che viene eseguita attualmente nel
20-30 % dei nuovi trapianti ed solo raramente gravata da complicanze emorragiche. Si
evidenziano : tubuliti, arteriti endoteliali per danno anticorpo mediato, danno endoteliale con
deposizione di C4 del complemento.
Esami strumentali
Lecodoppler e langio-RMN sono utili nel valutare i cambiamenti di vascolarizzazione
renale, anche in assenza di cambiamenti del flusso urinario.
Lecografia la procedura di scelta per escludere lostruzione urinaria o confermare la
presenza di raccolte perirenali di urina, sangue e linfa.
70) Quali sono i fattori di rischio cardiovascolare tipici del paziente sottoposto a
trapianto di rene?
Al trapianto di rene associato un non indifferente rischio cardiovascolare, tanto che in Europa
le patologie cardiovascolari sono responsabili del 36% della mortalit totale del paziente
trapiantato.
Il rischio relativo del trapiantato di due volte per malattie cardiache quali la cardiomiopatia
ischemica, lo scompenso e lipertrofia del ventricolo sinistro, per malattie cerebrovascolari con
trombosi e emorragie, e per malattie vascolari periferiche.
I fattori di rischio per patologie cardiovascolari nel trapiantato sono:
lipertensione,
il diabete,
la dislipidemia,
let, sesso, genotipo (fattori non reversibili)
terapia immunosoppressiva
71) Quali sono i geni le cui mutazioni sono note come causa di ADPKD?
72) Quali sono i geni le cui mutazioni sono note come causa di ADPKD?
Il rene policistico, una condizione patologica che si trasmette con modalit autosomica
dominante (recessiva nel bambino) dovuta a unampia gamma di mutazioni a carico del gene
PDK1 localizzato sul cromosoma 16 e del gene PDK2 localizzato sul cromosoma 14 che
codificano rispettivamente per la policistina 1 e la policistina 2.
La policistina 1 un recettore di membrana capace di legarsi e interagire con proteine
(collagene, fibronectina, laminina)carboidrati e lipidi e determinare risposte
intracellulari con un meccanismo di fosforilazione.
La policistina 2 una proteina tubulare che forma un canale per il calcio e altri cationi;
la sua funzione quella probabilmente di trasmettere allinterno della cellula segnali
derivati dallinterazione tra policistina 1 e ambiente extracellulare.
Le mutazioni a carico dei geni delle policistine sono moltissime e danno origine a proteine
tronche inattive. Nei soggetti eterozigoti per la mutazione, i geni non provvedono alla carenza
delle proteine, infatti la malattia si ha in seguito a un second hit , capace di causare una
mutazione somatica a carico dellallele wild (sano). Levento raro, giustificando la natura
focale della malattia (solo il 17% delle cellule nella variante PDK1formano cisti e solo il 45%
in quella PDK2 avrebbero seconda mutazione) in pi pare che la policistina vada
frequentemente incontro a mutazioni spontanee. Quindi durante lembriogenesi, nella
maggioranza delle cellule, le policistine vengono prodotte correttamente, in quelle dove si
verifica la seconda mutazione o non vengono prodotte o prodotte in maniera anomala. Le
cellule vanno incontro a proliferazione incontrollata, si assiste a espressione abnorme di fattori
di crescita, perdita dellorientamento con polarit invertita ( la pompa sodio/potassio si viene a
trovare sulla membrana luminale e le acquaporine sulla membrana basolaterale). Con
laccumulo di liquido le cisti aumentano di volume, si separano dal nefrone, comprimono il
parenchima renale circostante e compromettono la funzione renale.
73) Approccio terapeutico al paziente con ADPKD
Oggi il trattamento dellADPKD in gran parte di supporto, poich nessuna terapia singola si
dimostrata capace di prevenire il declino della funzione renale.
Il controllo dellipertensione arteriosa raccomandato. Un approccio
polifarmacologico (da 4,5 a 6 farmaci tra cui Minoxidil) comprendente agenti che
inibiscono il RAS (sistema renina a ngiotensina II), frequentemente richiesto poich si
tratta di unipertensione di III grado difficilmente controllabile.
Gli antibiotici liposolubili tra cui i chinolonici rappresentano la terapia di scelta per il
rene infetto e le cisti epatiche (anche se in questultimo caso si predilige il drenaggio).
La terapia del dolore richiede occasionalmente il drenaggio delle cisti per aspirazione
percutanea, scleroterapia con alcol o raramente drenaggio chirurgico.
I pazienti con ADPKD sembrano avere vantaggio in termini di sopravvivenza per
emodialisi e dialisi peritoneale rispetto ad altri pazienti con altre cause di ERSD.
Le recenti linee terapeutiche prevedono anche :
la soppressione dellADH bevendo 5 l di H2O al giorno o usando un antagonista specifico
dei recettori V2 dellADH. Questa strategia si rivelata deludente
la terapia citostatica: le cellule della cisti si sono rivelate sensibili al blocco della via mTOR
e sono stati provati farmaci come tacrolimus, sirolimus. Anche questi si sono rivelati
deludenti anche perch somministrati in pazienti gi in malattia avanzata.
74) Descrivete brevemente la storia naturale dell'ADPKD
Un caposaldo dellADPKD la grande eterogeneit fenotipica come dimostrato da membri di
una stessa famiglia con medesima mutazione che per hanno diverso decorso clinico. I soggetti
affetti sono spesso asintomatici nel 4 o 5 decennio di vita.
Clinica
I sintomi e i segni iniziali comprendono:
la dolorabilit addominale,
lematuria
linfezione delle vie urinarie,
lipertensione,
laumento della creatinina sierica
reni cistici agli studi di imaging
possibile reflusso gastro-esofageo
possibile insufficienza respiratoria
possibile ernia digestiva
Nella maggior parte dei pazienti la funzione renale declina progressivamente nel corso dei 10-
20 anni successivi alla diagnosi, ma non in tutti i pazienti con ADPKD. La velocit di
progressione differente nei pazienti con mutazione PDK1 e PDK2.
Grossolanamente, prendendo come punto di riferimento i pazienti con malattia conclamata si
ritiene che :
un paziente con ADPKD 1 raggiunga lERSD tra i 45 e i 55 anni senza differenze di
sesso
un paziente con ADPKD 2 raggiunga lERSD tra i 60-80 anni e in alcuni casi lo stadio
terminale non viene raggiunto
75) Descrivete brevemente la presentazione clinica dell'ADPKD
Caratteristica dellADPKD la grande eterogeneit fenotipica come dimostrato dai membri di
una stessa famiglia con medesima mutazione, che presentano decorso clinico diverso.
Clinica
Il paziente con rene policistico :
Ipertensione nel 60-100% dei casi: la compressione, lischemia, liperproduzione di
renina da parte dellepitelio cistico favoriscono linsorgenza dellipertensione, che
aggrava considerevolmente landamento della malattia.
Proteinuria raramente presente
Ematuria macroscopica presente nel 50% dei casi: risulta da rottura di cisti del dotto
collettore o dai calcoli urinari.
La nefrolitiasi - presente nel 20% dei pazienti.
Linfezione delle cisti renali o epatiche una complicanza seria e pi spesso dovuta a
batteri Gram e si presenta con dolore, febbre e brividi.
Laspetto sintomatologico che pesa pi nella vita del paziente il dolore che pu essere
di due tipi:
cronico continuo, sordo, viscerale: legato a espansione della massa
acuto dovuto a insorgenza di complicanze come impegno di un calcolo in
uretere, emorragia acuta intracistica, infezione cistica.
Linsufficienza renale come stadio finale dellADPKD identica a quella che si verifica nelle
malattie renali croniche, ma con differente aspetto morfologico e anemia spesso meno
accentuata.
Oltre che a livello renale lADPKD si caratterizza anche per manifestazioni a livello
extrarenale
complicanze cardiovascolari e cerebrovascolari
complicanze digestive
complicanze epatiche
complicanze respiratorie
76) Quali sono i geni le cui mutazioni sono note come causa di ADPKD?
Vedi la domanda 71
77) Quali sono le principali complicanze extrarenali dell'ADPKD?
Le complicanze extrarenali dellADPKD possono essere classificate in :
complicanze digestive
complicanze epatiche
complicanze respiratorie
complicanze cardiovascolari e cerebrovascolari
- A livello gastrointestinale, i diverticoli del colon costituiscono una manifestazione comune,
ma nei pazienti con rene policistico, si assiste a una maggiore incidenza di perforazione. Si
manifestano pi frequentemente anche ernie inguinali e della parete addominale.
- A livello epatico frequente il riscontro di cisti che generalmente sono asintomatiche.
Eccezionalmente una cisti pu crescere e determinare sintomatologia ostruttiva. Raramente si
ha rottura, infezione, torsione, emorragia cistica. Altrettanto rari sono i casi in cui il fegato si
presenta farcito di cisti al paro del rene, in tal caso si parla di fegato policistico. I soggetti pi
colpiti generalmente sono le donne in et fertile, probabilmente per il loro assetto ormonale.
- A livello respiratorio una complicanza rappresentata dallinsufficienza respiratoria
restrittiva.
- A livello cardiovascolare frequente il riscontro di prolasso mitralico e di insufficienza
mitralica, aneurisma dellaorta addominale e toracica.
- Infine aneurismi sacculari del circolo cerebrale anteriore possono essere scoperti nel 10%
dei pazienti asintomatici allo screening con risonanza magnetica. Lemorragia intracranica si
manifesta nei pazienti con et superiore a 50 anni e con familiarit.
78) Non c domanda
79) Definire la sindrome nefrologica insufficienza renale acuta
Sindrome nefrologica caratterizzata da riduzione acuta (ore o giorni) del filtrato
glomerulare, con ritenzione dei prodotti terminali del catabolismo proteico tra cui urea e
creatinina, e da alterazioni dellequilibrio idroelettrolitico e dellequilibrio acido-base.
La presenza di oliguria (<500 ml/die) o anuria (<100 ml/ die) utile nellaa diagnosi ma non
obbligatoria
80) Quali sono i criteri AKIN per il danno renale acuto?
Recentemente da parte dell AKIN Acute Kidney Injury Network stata proposta una
classificazione del danno renale acuto in 3 stadi, il cui fine quello di rendere il tutto pi
maneggevole sul piano clinico.
I criteri di riferimento presi in considerazione nella stadiazione sono la creatinina sierica e
lescrezione urinaria.
Il I stadio caratterizzato da un aumento da 1,5 a 2 volte della creatinina o da aumento
della creatinina maggiore o uguale a 0.3mg/dL. Lescrezione urinaria invece < 0.5
ml/kg/h per 6 ore.
Il II stadio caratterizzato da aumento da 2 a 3 volte della creatinina e da escrezione
urinaria < 0,5 ml/kg/h per 12 ore.
Il III stadio caratterizzato da aumento > 3 volte della creatinina o creatinina sierica
maggiore o uguale a 4mg/dl con aumento acuto > 0,5 mg/dl o diminuzione del GFR >
75%. Lescrezione urinaria <0.3 ml/kg/h per 24 ore o da assenza di urine per 12 ore.
81) Classificazione etio-patogenetica dell'insufficienza renale acuta
Le cause che possono condurre a insufficienza renale acuta possono essere classificate in :
riduzione del flusso e della pressione di perfusione renale: Azotemia (IRA) prerenale
(55-60% dei casi)
malattie del parenchima renale (necrosi tubulare ischemica e tossica, nefrite interstiziale,
glomerulonefrite acuta): Insufficienza renale acuta organica o renale (35-40% dei
casi)
ostruzione totale o parziale del deflusso urinario: Insufficienza renale acuta postrenale
(5% dei casi )
82) Quali sono le principali cause dell'insufficienza renale acuta pre-renale?
Le cause pre renali sono tutte quelle che determinano una riduzione della volemia, sia in senso
assoluto, sia relativo.
Riduzioni della volemia assoluto (ipovolemia vera)
emorragie massive esterne o interne
qualsiasi situazione di deplezione di volume:
perdita di fluido gastrointestinale ( vomito, diarrea, fistola
enterocutanea..),
perdita di fluido renale (diuretici, diuresi osmotica, iposurrenalismo,
diabete insipido nefrogeno)
sequestro extrarenale : ustioni, pancreatiti, ipoalbuminemia grave
Riduzione della perfusione renale per insufficienza cardio-circolatoria
infarto miocardico
tamponamento pericardico
endocardite
shock settico distributivo per vasodilatazione sistemica
Riduzione volume plasmatico efficace
Sindrome nefrosica
Cirrosi epatica fase ascitica: si verifica una condizione di underfilling.
Situazione a rischio la paracentesi evacuativa, perch se non si usano
correttamente i plasma expanders si rischia di provocare una gravissima
ipovolemia.
Scompenso cardiaco congestizio
Perdita di capacit di autoregolazione del flusso renale (riduzione improvvisa del
FER)
Trombosi, stenosi, embolia
Ipercalcemia induce vasocostrizione a livello renale
FANS inibiscono la sintesi di prostaglandine vasodilatatrici in sede renale,
favorendo uno stato di necrosi ischemica a livello tubulare
ACE-inibitori /sartani pericolosi negli individui in cui la volemia efficace viene
mantenuta grazie al sistema renina angiotenzina, quindi soprattutto in pz. con
stenosi bilaterale dellarteria renale e con scompenso cardiaco
Sindromi da iperviscosit
Iperproduzione di cataboliti azotati
Emorragie digestive
Crisi emoglobinemica del favismo
LIRA da cause prerenali essenzialmente funzionale; se per non viene rimossa la causa
scatenante, il danno funzionale determina necrosi tubulare su base ischemica e a questo punto
si instaura anche una componente organica renale, cio la necrosi tubulare acuta.
83) Quali sono le principali cause dell'insufficienza renale acuta renale
Le cause renali sono eventi che si verificano primitivamente nel parenchima renale. Sono cause
abbastanza rare di IRA. Si possono ulteriormente distinguere in:
Necrosi tubulare acuta
Su base ischemica
Da agenti nefrotossici
Endogeni - a) la mioglobina in corso di mioglobinuria causata da
rabdomiolisi massiva, b) lemoglobina in corso di anemie emolitiche per
saturazione dellaptoglobina, c) proteine intratubulari come accade nel
mieloma multiplo con la proteinuria di Bence- Jones, d) Acido urico, e)
Ossalati ecc.
EsogenI veleni, farmaci (antibiotici nefrotossici come aminoglucosidi,
mezzi di contrasto, chemioterapici)
Nefropatie tubulo-interstiziali
Nefrite interstiziale da ipersensibilit (autoimmune)
Pielonefrite acuta (infettiva)
Nefropatie infiltrative (neoplastica)
Malattie dei vasi renali di grandi e medie dimensioni
Trombosi dellarteria renale
Embolia arteriosa
Ateroembolismo
Aneurisma dissecante dellaorta
Vasculiti
Trombosi della vena renale
Malattie glomerulari e del microcircolo
Glomerulonefriti primitive e secondarie
Malattie ematologiche
Ipertensione maligno
Eclampsia
Contesti clinici
Chirurgia maggiore
Traumatismi severi
Ustioni estese
Emorragia
Deplezione volume
Sepsi
84) Quali sono le principali cause dell'insufficienza renale acuta post-renale?
Sostanzialmente sono tutte le cause di ostruzione urinaria che si distingue in :
ureterica (bilaterale o in caso di rene unico, unilaterale):
intraluminale: calcoli, coaguli, materiale di sfaldamento della papilla, cancro,
intramurale: edema postoperatorio della papilla
extramurale: legatura accidentale, compressione esterna ( per es. fibrosi
retroperitoneale), infiltrazione neoplastica.
collo della vescica: vescica neurogena, calcoli, coaguli, cancro
uretrale: strozzatura o valvole congenite
85) Elencate gli esami di laboratorio di primo livello indicati in un paziente con
insufficienza renale acuta
Esame delle urine (chimico-fisico, proteinuria, esame microscopico del sedimento,
colorazione specifica per eosinofili)
Esami bioumorali di routine (emocromo con formula e piastrine, enzimi, azotemia,
creatinina, sodio, potassio, cloro, calcio, fosforo, bicarbonati )
Lanalisi delle urine e gli esami ematochimici possono essere utili per distinguere unIRA
prerenale, dallIRA intrinseca , ischemica o nefrotossica.
86) Indicare gli strumenti diagnostici utili nella diagnosi differenziale delle diverse cause
di insufficienza renale
Tra i vari strumenti offerti dalla diagnostica per immagini delle vie urinarie,
lecografia pu essere utile per escludere unIRA post renale.
In alternativa si pu ricorrere a una TC o RM.
Pur essendo la dilatazione della pelvi e dei calici un segno di ostruzione delle vie urinarie, essa
pu mancare nel periodo immediatamente successivo allostruzione o nei casi in cui gli ureteri
risultino intrappolati dalla trama tissutale prodotta in corso di fibrosi retroperitoneale o di una
neoplasia.
La pielografia anterograda o retrograda pu fornire una localizzazione precisa del sito
di ostruzione.
Laddome in bianco o TC spirale sono buone tecniche di screening iniziale nei pazienti
con sospetta nefrolitiasi.
Langio- RM spesso usata in pazienti con sospetta ostruzione vascolare.
Langiografia con cateterismo pu essere necessaria per arrivare a conferma
diagnostica e pu essere impiegata anche a scopo interventistico.
La biopsia renale viene solitamente riservata a pazienti in cui lIRA prerenale e post
renale sono state escluse e la causa di IRA intrinseca non chiara, ovvero quando la
valutazione clinica e gli esami di laboratorio indicano condizioni diversa da una
nefropatia tossica, come una glomerulonefrite, vasculite, o nefrite interstiziale allergica
che possono rispondere a una terapia mirata.
87) Insufficienza renale acuta (approccio diagnostico)
Lapproccio diagnostico in caso di IRA prevede di :
1) Stabilire la presenza di IRA
2) Stabilire se lIRA prerenale, organica oppure ostruttiva
3) Identificare la causa responsabile dellIRA
1) Stabilire la presenza di IRA
Monitoraggio dei pazienti a rischio
Aumento progressivo di creatininemia ed azotemia, associato ad
incremento di potassio e fosfato ed a riduzione di calcio e bicarbonati
Considerare aumento spurio di creatininemia ed azotemia
Considerare insufficienza renale cronica
2) Classificare lIRA come prerenale, organica oppure ostruttiva ed identificare la
causa
Anamnesi ed esame obiettivo (contesto clinico)
Ecografia dellapparato urinario (da ripetere dopo 24 ore)
Esame delle urine (sedimento urinario ed indici di insufficienza renale)
Esami utili in casi selezionati :
Esami sierologici
Anticorpi anti-GMB, anti-DNA, ANCA, ASLO, ecc.
Complemento, crioglobuline, immunocomplessi, etc.
Esami radiologici
Rx addome in bianco, pielografia retrograda, TC spirale, RNM, angiografia
Biopsia renale: indicata in particolare se:
IRA da cause non altrimenti identificate
Sospetto di malattie sistemiche
Sospetto da malattie glomerulari (ematuria e proteinuria
glomerulari)
Ipertensione senza espansione della volemia
Oliguria prolungata (> 2 settimane)
Anuria in assenza di ostruzione
88) Indicare il significato diagnostico dell'escrezione urinaria di sodio (o dell'FENa) nel
paziente con insufficienza renale acuta
La FENa mette in relazione la clearance del sodio con quella della creatinina. In un paziente
con IRA prerenale, il sodio viene ampiamente riassorbito dal filtrato glomerulare per
ripristinare il volume intravascolare (FENa <1%).
La FENa nellIRA renale >2%. La FENa nellNTA ischemica elevata, in quella tossica pi
bassa.
La creatinina invece non viene riassorbita n nel primo caso n nellaltro.
89) Indicare il significato diagnostico dell'osmolarit urinaria (o del rapporto U/Posm)
nel paziente con insufficienza renale acuta
E importante nella diagnosi differenziale tra IRA funzionale ed organica.
Se la oliguria dipende da una deplezione del VEC ed il rene funziona, esso riassorbe tutta
lacqua e tutto il sodio che pu (per mantenere il VEC). Quindi la osmolarit urinaria alta
(>500 mOsm/ kg).
Se la oliguria dipende da un danno al rene, esso non pu funzionare. La capacit di
concentrare/diluire lurina persa, cos come la capacit di riassorbire sodio.
La osmolarit urinaria (<350 mOsm/kg) uguale a quella plasmatica e la sodiuria non molto
bassa.
90) Indicare i principali biomarkers di insufficienza renale acuta ed il loro significato
(utilit)
La diagnosi di insufficienza renale acuta al giorno doggi pu basarsi sulla valutazione di un
insieme di parametri che sono poi integrati secondo i criteri RIFLE o secondo i criteri AKIN: si
tratta di misurazioni rapide da effettuare su sangue ed urine, quindi molto rapide. Questo
significa per che non esiste un singolo marcatore che ci consenta di fare diagnosi di IRA
La creatinina un prodotto del metabolismo muscolare ed i suoi livelli plasmatici
dipendono dalla massa muscolare del soggetto e sono influenzati da numerosi altri
fattori, nonch dal tempo necessario per linstaurarsi del danno e dallintervallo fra la
comparsa di IRA ed il momento della misurazione. Non quindi raro trovare soggetti
con IRA ed oligo-anuria e valori di creatinina relativamente bassi . Quando si instaura
linsufficienza renale acuta, generalmente la creatinina, come le altre scorie azotate,
iniziano ad accumularsi.
Nelle prime ore dopo linsorgenza dellIRA, la creatinina pu essere normale o poco
elevata anche le la funzione renale cessata del tutto. Per questo c molto interesse
nellindividuazione di nuovi possibili markers di danno renale acuto.
La Cistatina C uno di questi nuovi biomarkers:in corso di IRA la sua utilit sembra
essere notevole. Infatti la cistatina C sierica aumenta con un anticipo di circa 24-48 ore
rispetto allinnalzamento della creatinina. Un elemento da considerare, per, che la
cistatina C, pi che un marker di danno renale, un marker di riduzione del GFR.
Un altro biomarker promettente la lipocalina associata alla gelatinasi neutrofila
(NGAL), una proteina che viene rilasciata non appena si verifica un danno renale,
agendo quindi come una sorta di proteina di fase acuta renale.
IL-18
KIM-1 (kidney injury molecule-1) proteina transmembrana con un dominio
immunoglobulinico e uno mucinico
N-acetil--d-glucosaminidase
91) Quali sono i principali provvedimenti terapeutici messi in atto nel paziente con
insufficienza renale acuta?
Nel paziente con danno renale reversibile se si in presenza di NTA ischemica si procede a
ristabilire lemodinamica sistemica e la perfusione renale, si ripristina il volume e si usano
vasopressori.
Nella NTA nefrotossica si eliminano le sostanze nefrotossiche e si procede con diuresi alcalina
forzata nella rabdomiolisi, allopurinolo nella sondrome da lisi tumorale.
Poich non ci sono farmaci specifici per lIRA la prevenzione e il trattamento delle
complicanze rivestono un ruolo essenziale:
Sovraccarico del volume intravascolare: si procede con la restrizione di acqua e Sali,
diuretici, ultrafiltrazione.
Iponatriemia: restrizione di acqua
Iperkaliemia:
restrizione apporto dietetico di potassio,
diuretici dansa per promuoverne leliminazione,
resine a scambio ionico che si legano al potassio;
insulina e glucosio o beta agonisti per promuovere il riassorbimento cellulare,
calcio gluconato o calcio cloruronato per stabilizzare il miocardio;
dialisi.
Acidosi metabolica: bicarbonato di sodio e altre basi; dialisi
Iperfosfatemia: restrizione apporto dietetico di fosfati, agenti che legano il fosfato
(calcio carbonato, calcio acetato)
Ipocalcemia: calcio carbonato, calcio gluconato
Ipermagnesemia: sospendere antiacidi contenenti Mg
Iperuricemia: se necessario allopurinolo, diuresi alcalina forzata
Altri accorgimento sono quelli dietetici : apporto proteico e calorico per evitare bilancio
netto negativo
La dialisi per prevenire le complicanze dellIRA.
La scelta dei farmaci deve evitare agenti nefrotossici, ACE inibitori, ARB (sartani) ,
aminoglicosidi, FANS, mezzo di contrasto. Il dosaggio deve essere adeguato ai tempi di
somministrazione
92) Indicazioni alla terapia sostitutiva della funzione renale nel trattamento
dell'insufficienza renale acuta
Le indicazioni alla terapia sostitutiva della funzione renale nel trattamento dellIRA sono:
iperkaliemia incontrollabile
uremia severa
acidemia
sovraccarico grave di acqua e Sali non responsivo al trattamento con diuretici
La dialisi:
necessaria nell85% delle forme oliguriche e nel 30% di quelle non oliguriche
Migliora la sopravvivenza
Potrebbe ritardare la ripresa della funzione renale (?)
Va eseguita con membrane biocompatibili
93) Descrivete la patogenesi dellipertensione in caso di stenosi monolaterale dellarteria
renale
Un processo che causi stenosi critica di unarteria renale (>70%), determina: ipoperfusione
renale e riduzione del GFR.
Ci determina lattivazione del RAS (sistema renina angiotensina II) per riduzione del carico di
sodio in arrivo alla macula densa. Da qui segue normalizzazione del GFR a valori normali al
prezzo di causare ipertensione angiotensina II dipendente.
A livello del rene non stenotico, si avr una pressione glomerulare aumentata (per
lipertensione sistemica). Grazie al feedback tubuloglomerulare si avr soppressione del RAS e
un aumento dellescrezione di sodio (pressure natriuresis) con normali livelli di PA nella vena
periferica.
Il blocco farmacologico del RAS, non determina alcun effetto a livello del rene non stenotico,
ma osserviamo una riduzione del GFR nel rene stenotico (in cui il GFR dipende dal RAS) e un
abbassamento della pressione arteriosa.
Nelle fasi avanzate si hanno danni vascolari e parenchimali anche nel rene sano controlaterale
per cui lipertensione diviene renino indipendente.
94) Descrivete la patogenesi dellipertensione in caso di stenosi bilaterale dellarteria
renale
Un processo che causi stenosi oltre una soglia critica delle arterie renali (>70%), determina
ipoperfusione e riduzione del GFR. Entrambi i reni in questo caso portano avanti la stessa
attivit: mantengono iperattivo il RAS per mantenere costante il proprio GFR.
Da qui segue ipertensione determinata non solo dallangiotensina II, ma anche dallespansione
volemica che rischia di precipitare in un edema polmonare acuto, per tendenza del liquido in
eccesso di accumularsi nel compartimento a minor pressione.
In questo caso il blocco farmacologico del RAS determina marcata riduzione del GFR e solo
dopo deplezione volemica, si avr ipotensione.
95) Quali sono le cause principali della stenosi dellarteria renale?
Leziologia della stenosi renale pu essere ricondotta essenzialmente a due patologie:
la displasia fibromuscolare (10%)
laterosclerosi (90%).
La displasia fibromuscolare processo patologico ad eziologia sconosciuta che coinvolge
lintima, lavventizia e soprattutto la media dei vasi conferendo un tipico aspetto a
cavaturacciolo allangiografia.
Colpisce principalmente i soggetti giovani, soprattutto donne tra i 15 e i 30 anni di et ,anche se
sono stati descritti casi di et superiore( fino a 60 anni).
Molto raramente determina occlusione renale e in tal caso sono coinvolti vari meccanismi
trombotici.
Laterosclerosi invece rende conto del 90% dei casi di stenosi renale.
Si verifica nel contesto dellaterosclerosi polidistrettuale (soggetti anziani, diabete,
ipertensione, dislipidemie, fumo, coronariopatie, malattie cerebrovascolari).
Coinvolge generalmente laorta addominale e si estende allostio e al terzo prossimale
dellarteria renale;
spesso associata ad aterosclerosi iliaco femorale (spesso sintomatica con claudicatio
intermittens) o pi raramente mesenterica.
Si tratta soprattutto nei diabetici di una malattia progressiva che se estesa a entrambe le arterie
renali, determina un quadro di insufficienza renale e aggrava un quadro di ipertensione
essenziale spesso preesistente.
96) Quali sono le manifestazioni cliniche pi frequenti in caso di stenosi aterosclerotica
dellarteria renale?
Circa il 90% delle cause di stenosi dellarteria renale, abbiamo visto essere dovuti ad
aterosclerosi.
Dal punto di vista clinico la stenosi aterosclerotica si manifesta con:
Ipertensione
Improvviso aumento della pressione arteriosa ad un et uguale o superiore ai 50
anni
Ipertensione accelerata o maligna
Ipertensione refrattaria (non responsiva alla terapia con 3 o pi farmaci)
Alterazioni renali
Azotemia inspiegabile
Azotemia indotta dalluso di ACE inibitori
Dimensioni ridotte di un rene (differenza allecografia tra i due reni >1,5 cm)
Ipokaliemia inspiegabile
Altre manifestazioni cliniche:
Dolore addominale, dolore a un fianco o entrambi
Retinopatia severa (3 o 4 allesame del fondo oculare)
Malattie cardiovascolari o vascolari periferiche
Scompenso cardiaco congestizio o edema polmonare acuto
Soffio addominale sisto-diastolico
97) Qual il trattamento pi frequentemente utilizzato nel paziente con stenosi
fibrodisplasica dellarteria renale
Nel paziente con stenosi fibrodisplastica dellarteria renale, gli ACE inibitori e i bloccanti del
recettore dellangiotensina II sono efficaci nel86-92% dei casi, ma la perdita della massa
renale e la riduzione della pressione di filtrazione possono produrre IR acuta e cronica che
potenziata dalla deplezione di sodio ( di solito reversibile se diagnosticata prontamente).
Quindi la terapia di rivascolarizzazione (angioplastica con posizionamento di stent ) in genere
quella di scelta. La procedura ha successo nell 82- 100% dei pazienti e la stenosi ricorre solo
nel 10-11% dei casi.
98) Cos lateroembolismo, quando si verifica e quali sono le sue conseguenze a livello
renale?
Per ateroembolismo si intende locclusione delle arteriole renali (150-200 microm) da parte di
cristalli di colesterolo provenienti da placche aterosclerotiche.
Fattori di rischio
Sesso maschile,
et avanzata,
diabete costituiscono
frequente nellanziano con aterosclerosi polidistrettuale, raramente spontanea, in genere
iatrogena (angiografia, angioplastica, chirurgia vascolare, terapia trombolitica).
Clinica di solito le manifestazioni comprendono
quelle dellinsufficienza renale acuta (con oliguria) o subacuta
ipertensione
leucocitosi eosinofila
proteinuria
eosinofilia
aumento degli enzimi nel siero e nelle urine.
Linfarto renale secondario a embolizzazione, unevenienza rara.
Sono frequenti segni di ischemia anche a livello di altri organi: cervello, arti superiori e
inferiori, intestino, occhio, cute (livedo reticularis e colorazione bluastra o gangrena delle dita
dei piedi).
Potrebbero piacerti anche
- Esplorazione Funzionale Dei Reni10Documento28 pagineEsplorazione Funzionale Dei Reni10Aldo HoxhaNessuna valutazione finora
- NEFROLOGIADocumento37 pagineNEFROLOGIAFedericoPppzPippoNessuna valutazione finora
- Appunti Di Medicina D'emergenza (TS)Documento88 pagineAppunti Di Medicina D'emergenza (TS)Giuseppe Doc Marini50% (2)
- 22 03Documento9 pagine22 03Ioana ManoleNessuna valutazione finora
- Nefrologia 2° LezioneDocumento9 pagineNefrologia 2° LezioneMariarita Di BenedettoNessuna valutazione finora
- Ne Frolo GiaDocumento70 pagineNe Frolo GiaJosephine C.Nessuna valutazione finora
- 09 Sindrome EpatorenaleDocumento3 pagine09 Sindrome Epatorenaleantonio nennaNessuna valutazione finora
- SV - 09 - Malattie Del Metabolismo - Gotta, Obesità e Diabete in Gravidanza - Lapolla - 31-03-2022Documento15 pagineSV - 09 - Malattie Del Metabolismo - Gotta, Obesità e Diabete in Gravidanza - Lapolla - 31-03-2022Michele GiordanoNessuna valutazione finora
- Ascites PredavanjeDocumento17 pagineAscites PredavanjeAnonymous JMnKM6KrNessuna valutazione finora
- Manuale PrelievoDocumento46 pagineManuale PrelievoDaniele GiordanoNessuna valutazione finora
- Farmaci AntipertensiviDocumento71 pagineFarmaci AntipertensiviNicola LauroraNessuna valutazione finora
- Tema 18 Insufficienza Cardiaca e DigitaliciDocumento6 pagineTema 18 Insufficienza Cardiaca e DigitalicijoseNessuna valutazione finora
- Caz Seria E Var 1Documento6 pagineCaz Seria E Var 1Carp TheodorNessuna valutazione finora
- Appunti Di Fisiopatologia Generale (Merkel)Documento53 pagineAppunti Di Fisiopatologia Generale (Merkel)//Nessuna valutazione finora
- Dieta Per Malattia Renale Cronica e Insufficienza Renale CronicaDocumento4 pagineDieta Per Malattia Renale Cronica e Insufficienza Renale CronicaDaniela RigolinoNessuna valutazione finora
- Seconda ParteDocumento29 pagineSeconda ParteJosé Pedro Mendoza RíosNessuna valutazione finora
- Terapia Renale Sostitutiva Nel Paziente Critico 1Documento3 pagineTerapia Renale Sostitutiva Nel Paziente Critico 1TetengiNessuna valutazione finora
- Riassunto Biochimica ClinicaDocumento23 pagineRiassunto Biochimica ClinicaFrancesco Maria ZechiniNessuna valutazione finora
- Appunti NefrologiaDocumento46 pagineAppunti NefrologiaPasquale CacciatoreNessuna valutazione finora
- GottaDocumento9 pagineGottaannaricci.aNessuna valutazione finora
- Insufficienza Renale AcutaDocumento3 pagineInsufficienza Renale AcutaMarcello VecchioNessuna valutazione finora
- Farmacologia Della Regolazione Del Volume Dei Liquidi Corporei PDFDocumento32 pagineFarmacologia Della Regolazione Del Volume Dei Liquidi Corporei PDFNiculina IstratiNessuna valutazione finora
- Malattie Rene e Vie UrinarieDocumento12 pagineMalattie Rene e Vie UrinarieEnrico CarrettaNessuna valutazione finora
- Lezione 3Documento9 pagineLezione 3Nicolas MincuzziNessuna valutazione finora
- Resuscitarea Volemica201Documento42 pagineResuscitarea Volemica201Andreea Cristina AndreeaNessuna valutazione finora
- Nefrologia. Sbobinature 2013-14Documento131 pagineNefrologia. Sbobinature 2013-14fradoctorNessuna valutazione finora
- Lezione 17 Fine DiabeteDocumento27 pagineLezione 17 Fine DiabeteChiara PaolicelliNessuna valutazione finora
- Fisiopatologia Clinica PT.2Documento13 pagineFisiopatologia Clinica PT.2FedericoPppzPippoNessuna valutazione finora
- Apparato Urinario PDFDocumento6 pagineApparato Urinario PDFPaolo PinnaNessuna valutazione finora
- Dispensa Di Patologia Clinica 2020-2021Documento121 pagineDispensa Di Patologia Clinica 2020-2021Massimiliano CarifiNessuna valutazione finora
- Capitolo 48Documento17 pagineCapitolo 48Francesco ScognamiglioNessuna valutazione finora
- Lezione 3, 13-03-2019, NefrologiaDocumento14 pagineLezione 3, 13-03-2019, NefrologiaMaría P SNessuna valutazione finora
- Chetoacidosi DiabeticaDocumento7 pagineChetoacidosi Diabeticabella-emyNessuna valutazione finora
- Panoramica Sulle Alterazioni Del Volume Dei LiquidiDocumento63 paginePanoramica Sulle Alterazioni Del Volume Dei LiquidiRoberta Lulù TerranovaNessuna valutazione finora
- Nefrologia Lezione 3Documento7 pagineNefrologia Lezione 3Orsola MorelloNessuna valutazione finora
- Lezione 13Documento8 pagineLezione 13Morena MaddalenaNessuna valutazione finora
- Hematoloski AnaliziDocumento34 pagineHematoloski AnaliziStevco Donev MakedonskiNessuna valutazione finora
- Patologia Clinica FegatoDocumento14 paginePatologia Clinica FegatoBarbara BranconeNessuna valutazione finora
- Paziente Con Ascite ECCEINFADDocumento9 paginePaziente Con Ascite ECCEINFADSara SilvaNessuna valutazione finora
- Linee Guida Per Il Buon Uso Del SangueDocumento25 pagineLinee Guida Per Il Buon Uso Del SangueHary SeldonNessuna valutazione finora
- Patologia Clinica ReneDocumento9 paginePatologia Clinica ReneBarbara BranconeNessuna valutazione finora
- 2 - Urine e FeciDocumento31 pagine2 - Urine e Fecifrancesca.mazzilli63Nessuna valutazione finora
- 4 - Profilo GlucidicoDocumento6 pagine4 - Profilo Glucidicofrancesca.mazzilli63Nessuna valutazione finora
- Metabolismo Dei FarmaciDocumento51 pagineMetabolismo Dei Farmaciapi-26155364Nessuna valutazione finora
- Fisiologia e Fisiopatologia Del Diabete MellitoDocumento10 pagineFisiologia e Fisiopatologia Del Diabete Mellitosiluma11100% (1)
- DiureticiDocumento45 pagineDiureticiNicola GuantiNessuna valutazione finora
- Sindrome Nefrosica: PatogenesiDocumento22 pagineSindrome Nefrosica: PatogenesiDario AnobileNessuna valutazione finora
- Artificialnutritionandsepsisiii 100113055903 Phpapp01Documento15 pagineArtificialnutritionandsepsisiii 100113055903 Phpapp01icubedNessuna valutazione finora
- 4 Crisis Hiperglicemia Del AdultoDocumento12 pagine4 Crisis Hiperglicemia Del AdultoKARLA VASQUEZNessuna valutazione finora
- Insulina 2018Documento56 pagineInsulina 2018Filippo NovelliNessuna valutazione finora
- Alterato MetabolismoDocumento9 pagineAlterato MetabolismoLucrezia RoselliNessuna valutazione finora
- Insufficienza Renale AcutaDocumento43 pagineInsufficienza Renale Acuta1Sam_89Nessuna valutazione finora
- Libretto Asnit 2013Documento34 pagineLibretto Asnit 2013Lidia Nartaki VinogradovaNessuna valutazione finora
- 1.1 ShockDocumento12 pagine1.1 ShockElenaNessuna valutazione finora
- NefrologiaDocumento45 pagineNefrologiaKaterineMariNessuna valutazione finora
- Laboratorio GlicemiaDocumento14 pagineLaboratorio GlicemiaKarenNessuna valutazione finora
- Esame ChirurgicheDocumento9 pagineEsame ChirurgicheMarco SparavignaNessuna valutazione finora
- Libro Cardiologia SICDocumento197 pagineLibro Cardiologia SICMarco Sparavigna100% (3)
- Ri As Sunti Antibiotic IDocumento8 pagineRi As Sunti Antibiotic IMarco SparavignaNessuna valutazione finora
- RosaceaDocumento18 pagineRosaceaMarco SparavignaNessuna valutazione finora
- Classificazione DM, DM Tipo 1Documento22 pagineClassificazione DM, DM Tipo 1Marco SparavignaNessuna valutazione finora
- Bio Chi Mica Del Sistema NervosoDocumento24 pagineBio Chi Mica Del Sistema NervosoMarco SparavignaNessuna valutazione finora
- La Spirometria - Simona MartinelliDocumento29 pagineLa Spirometria - Simona MartinelliSirAuronNessuna valutazione finora
- Equilibrio Acido Base, Fisiologia RespiratorioDocumento2 pagineEquilibrio Acido Base, Fisiologia RespiratorioVanessa SpinelliNessuna valutazione finora
- Alcool E Nicotina Di Rudolf SteinerDocumento26 pagineAlcool E Nicotina Di Rudolf SteinerBelva64100% (6)
- Il Programma TeacchDocumento9 pagineIl Programma Teacchnovalis30001248Nessuna valutazione finora