Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Basi Teoriche NMR
Caricato da
RobCopyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Basi Teoriche NMR
Caricato da
RobCopyright:
Formati disponibili
www.pianetachimica.
it
Basi teoriche
della Spettroscopia NMR
Premessa
La Spettroscopia di Risonanza Magnetica Nucleare (NMR) una tecnica analitica molto potente
che permette di ottenere dettagliate informazioni sulla struttura molecolare dei composti in esame.
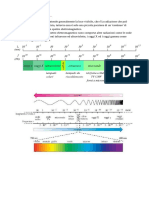
La spettroscopia NMR misura lassorbimento di radiazione elettromagnetica in molecole immerse
in un forte campo magnetico. Questo assorbimento avviene ad opera dei nuclei di particolari atomi
(tipicamente 1H o 13C).
Quindi con l'NMR si esaminano direttamente i nuclei atomici e non gli elettroni. Ogni informazione
sull'intorno chimico viene dedotta osservando il comportamento dei nuclei atomici.
Spin nucleare
Sono osservabili allNMR solo i nuclei che hanno un momento magnetico nucleare di spin , e che
quindi si comportano come lago di una bussola che si pu orientare in un campo magnetico
applicato. Il momento magnetico nucleare di spin legato allo spin nucleare I dalla relazione
= I h/2
dove il rapporto giromagnetico, I il numero quantico di spin nucleare, h la costante di Plank.
Lo spin nucleare viene prodotto dalle particelle che costituiscono il nucleo, protoni e neutroni.
Queste si comportano come se fossero in rotazione (spin) attorno al loro asse e hanno spin 1/2.
In molti atomi (come nel 12C) gli spin sono tutti appaiati, uno in opposizione all'altro e quindi si
annullano reciprocamente e il nucleo atomico ha uno spin risultante I uguale a zero. In alcuni atomi,
per (come in 1H e in 13C), il nucleo possiede uno spin risultante I diverso da zero. Le regole per
determinare lo spin nucleare si possono cos riassumere:
1) Se i protoni e i neutroni sono entrambi pari, allora il nucleo ha spin zero.
2) Se i protoni e i neutroni sono gli uni pari e gli altri dispari, allora il nucleo ha spin semi
intero (1/2, 3/2, 5/2, ...).
3) Se i protoni e i neutroni sono entrambi dispari, allora il nucleo ha spin intero (1, 2, 3, ...).
Rientrano nel primo caso 12C e 16O che hanno I = 0 e quindi non hanno momento magnetico di
spin e non sono osservabili allNMR.
Rientrano nel secondo caso 1H, 19F, 13C, 31P e 15N che hanno I = 1/2 e quindi sono osservabili
allNMR.
Rientrano nel terzo caso 2H e 14N che hanno I = 1 e quindi anche questi sono osservabili allNMR.
Livelli energetici in un campo magnetico
Quando un nucleo dotato di spin viene immerso in un campo magnetico, si comporta come l'ago di
una bussola, sottoposto ad una coppia di forze
che lo fanno ruotare per allinearlo col campo
magnetico esterno.
Le possibili orientazioni che il nucleo pu
assumere in un campo magnetico sono governate
dal numero quantico m che pu assumere i
valori da I a +I (con incrementi di una unit) e
quindi pu assumere 2I+1 valori diversi. Nel
caso di un nucleo con spin 1/2 (come 1H) ci sono
due possibili orientazioni:
una con m = 1/2 e una con m = +1/2.
Prof. Mauro Tonellato ITIS Natta Padova Basi teoriche dellNMR 1
www.pianetachimica.it
Il momento magnetico nucleare non sta fermo, ma continua ad oscillare attorno al campo
magnetico applicato Bo compiendo un moto di precessione simile a quello di una trottola.
I due stati possibili del nucleo non hanno la stessa energia, ma lo stato con m = +1/2 (allineato con
il campo) si trova ad energia leggermente pi bassa di quello con m = 1/2 (opposto al campo)
Il moto di precessione dei momenti magnetici nucleari avviene con una frequenza proporzionale
alla differenza di energia tra i due livelli detta frequenza di Larmor data dalla formula
= Bo /2 (in Hertz)
dove il rapporto giromagnetico che dipende dal nucleo in esame. Allaumentare del campo
applicato Bo, aumenta la frequenza di Larmor e quindi la differenza di energia tra i livelli.
Poich la differenza di energia tra i due livelli piccolissima, dell'ordine di 9 106 kcal mol1, la
popolazione di nuclei nei due stati praticamente identica con una piccolissima prevalenza per lo
stato a bassa energia allineato con il campo. A temperatura ambiente, in un campo magnetico di
1.41 Tesla (60 MHz) abbiamo un nucleo in pi nello stato di bassa energia ogni duecentomila
nuclei, in un campo di 7.05 Tesla (300MHz) abbiamo 5 nuclei in pi nello stato di bassa energia
ogni duecentomila nuclei.
Eppure sono proprio questi pochi nuclei in eccesso allineati con il campo magnetico Bo quelli che
permettono di generare il segnale NMR.
Si noti che con un campo magnetico pi intenso (7.05 T) c una maggiore differenza di energia tra
i livelli e quindi una maggiore frequenza di Larmor (300 MHz) e un maggior numero di nuclei in
pi allineati con il campo (5 su duecentomila) e quindi una maggiore sensibilit nellanalisi NMR.
Assorbimento di energia
Se il campione viene irradiato con una radiazione elettromagnetica di frequenza uguale alla
frequenza di Larmor, ci sar una interazione della componente magnetica della radiazione con i
momenti magnetici nucleari (anche questi oscillanti alla frequenza di Larmor). Lenergia della
radiazione potr cos essere trasferita ai nuclei. Ogni assorbimento di radiazione comporta un
cambiamento di orientazione dello spin nucleare che ruoter da allineato con il campo ad
opposto al campo. Quando si verifica questa transizione di spin, si dice che i nuclei sono in
risonanza con la radiazione applicata, da qui il nome di Risonanza Magnetica Nucleare, NMR.
Prof. Mauro Tonellato ITIS Natta Padova Basi teoriche dellNMR 2
www.pianetachimica.it
Anche nello stato di massima eccitazione, la popolazione dei nuclei nei due livelli permessi sar
circa uguale, data la piccolissima differenza di energia tra i livelli. Lo stato eccitato sar solo
leggermente pi popolato di quello fondamentale con un rapporto di popolazioni invertito, cio, in
un campo di 7.05 Tesla (300MHz) ci potranno essere 5 nuclei in pi nello stato di alta energia ogni
duecentomila nuclei.
Produzione del segnale NMR
Il segnale NMR negli strumenti pi moderni viene generato con il metodo ad impulso.
Con questa tecnica tutti i nuclei di una specie vengono eccitati contemporaneamente da un impulso
di radiofrequenza che contiene tutto lintervallo di frequenze necessario.
Per capire come limpulso di radiofrequenza interagisce con i nuclei in esame dobbiamo introdurre
un vettore chiamato Magnetizzazione Macroscopica Mo che la risultante di tutti i momenti
magnetici nucleari. Dato che esiste un leggero eccesso di nuclei che si trovano allineati col campo
magnetico Bo, Mo sar piccolo e allineato col campo. Indichiamo questa direzione come asse z.
Se ora il campione viene irradiato lungo lasse x con un impulso di radiofrequenza che contiene
anche la frequenza di Larmor dei nuclei in esame (ad es 1H), i nuclei assorbiranno energia e
subiranno una transizione di spin. A livello macroscopico si osserva che il vettore Magnetizzazione
Macroscopica Mo ruota allontanandosi dallasse z per avvicinarsi al piano xy iniziando un moto di
precessione attorno allasse z.
A questo punto limpulso di radiofrequenza cessa ed entra in funzione un circuito ricevente che ha
lo scopo di misurare loscillazione della componente y del vettore M. E un po come se, dopo
aver gridato di fronte a una parete rocciosa, restassimo in silenzio per ascoltare leco.
Prof. Mauro Tonellato ITIS Natta Padova Basi teoriche dellNMR 3
www.pianetachimica.it
Lenergia assorbita dai nuclei viene lentamente ceduta agli atomi vicini a causa di fenomeni detti di
rilassamento e il vettore M, compiendo delle spirali di precessione attorno allasse z, si riporta al
valore iniziale Mo, posizione per la quale la componente My vale zero.
La durata t(p) dellimpulso di radiofrequenza deve essere determinata con precisione per produrre
un forte segnale NMR. Se t(p) tale da piegare Mo di 90, allora si produrr il vettore My massimo.
In genere t(p) di alcuni microsecondi.
Il segnale raccolto un segnale oscillante con frequenza , la frequenza di Larmor del nucleo in
esame, che si smorza nel tempo e che viene detto FID (Free Induction Decay), libero decadimento
dellinduzione.
In figura illustrato il FID del CH3I per latomo di idrogeno.
Dato che nella molecola CH3I gli idrogeni sono equivalenti, avranno tutti la stessa frequenza di
risonanza. Nel grafico questa frequenza facilmente individuabile misurando la lunghezza d'onda
(la distanza tra due creste successive) e calcolandone il reciproco, secondo la formula:
=1/
dove la frequenza e la lunghezza donda.
Si ottiene cos il seguente grafico in funzione delle frequenze, chiamato spettro NMR, che mostra
la frequenza assorbita dagli atomi di idrogeno nella molecola CH3I:
Se il campione contiene nuclei con differenti frequenze di risonanza, questi vengono tutti eccitati
contemporaneamente dallimpulso di radiofrequenza e quindi il segnale raccolto sar una curva
complessa, chiamata interferogramma, data dalla combinazione di pi FID semplici, uno per ogni
frequenza assorbita dai nuclei.
Per poter risalire alle singole frequenze che combinandosi tra loro hanno generato il tracciato
complesso, necessario applicare una procedura matematica detta Trasformata di Fourier che
permette di passare dal grafico in funzione del tempo, il FID, al grafico in funzione delle frequenze,
lo spettro NMR.
Prof. Mauro Tonellato ITIS Natta Padova Basi teoriche dellNMR 4
Potrebbero piacerti anche
- Introduzione NMRDocumento17 pagineIntroduzione NMRaliceinrockNessuna valutazione finora
- 7 - Spettroscopia NMRDocumento79 pagine7 - Spettroscopia NMRorsolaNessuna valutazione finora
- Teoria NMRDocumento9 pagineTeoria NMRFrancesco GiansantiNessuna valutazione finora
- Analisi Di Biomolecole - Spettroscopia NMRDocumento105 pagineAnalisi Di Biomolecole - Spettroscopia NMRPAOLO GAMBACORTANessuna valutazione finora
- RM - Principi Di FunzionamentoDocumento27 pagineRM - Principi Di FunzionamentoGuglielmo CannellaNessuna valutazione finora
- CoppiGarulli NMRDocumento10 pagineCoppiGarulli NMRussaNessuna valutazione finora
- EPRDocumento11 pagineEPR88alexiaNessuna valutazione finora
- RM PrincipiDocumento18 pagineRM PrincipiSante Giuliano TroiaNessuna valutazione finora
- Risonanza Magnetica SlidesDocumento47 pagineRisonanza Magnetica SlidesDarjn EspositoNessuna valutazione finora
- Principi Fisici Di Risonanza Magnetica Originale PDFDocumento29 paginePrincipi Fisici Di Risonanza Magnetica Originale PDFMarioNessuna valutazione finora
- TesiDocumento74 pagineTesirockerrabbitNessuna valutazione finora
- Lezione1 - Spettroscopia UV VisDocumento51 pagineLezione1 - Spettroscopia UV VisventilabroNessuna valutazione finora
- Roba VariaDocumento8 pagineRoba VariaNino 16Nessuna valutazione finora
- Metodi Chimico Fisici D'indagine Applicati Ai Sistemi Molecolari e NanostrutturatiDocumento12 pagineMetodi Chimico Fisici D'indagine Applicati Ai Sistemi Molecolari e NanostrutturatinazzaNessuna valutazione finora
- 1.RMN PrincipiDocumento19 pagine1.RMN PrincipiGiacomo BattagliaNessuna valutazione finora
- Meccanica QuantisticaDocumento3 pagineMeccanica QuantisticaIkram LazarNessuna valutazione finora
- 01 AtomoDocumento47 pagine01 Atomozakaria.moubarak4Nessuna valutazione finora
- MeccanicaQuantistica 01Documento23 pagineMeccanicaQuantistica 01complex77Nessuna valutazione finora
- Riassunto Di ChimicaDocumento67 pagineRiassunto Di ChimicaMarioNessuna valutazione finora
- La Risonanza Magnetica SlideDocumento111 pagineLa Risonanza Magnetica SlideandreaNessuna valutazione finora
- Fisica Delle RadiazioniDocumento14 pagineFisica Delle Radiazioniblablabla25Nessuna valutazione finora
- Spettroscopia AADocumento25 pagineSpettroscopia AAMatteo TreviNessuna valutazione finora
- Struttura Atomica (2018-2019)Documento50 pagineStruttura Atomica (2018-2019)becienzoNessuna valutazione finora
- Lezione 3 SB22Documento71 pagineLezione 3 SB22Martina PorcuNessuna valutazione finora
- Tesina Completa Radioattivita'Documento31 pagineTesina Completa Radioattivita'zambesi_returnsNessuna valutazione finora
- 04 La Struttura AtomicaDocumento63 pagine04 La Struttura Atomicapb9kft9rwtNessuna valutazione finora
- Laser Principi Di FunzionamentoDocumento31 pagineLaser Principi Di FunzionamentoEmanuele86% (7)
- Interpretare Gli Spettri IRDocumento23 pagineInterpretare Gli Spettri IRbobasa9655Nessuna valutazione finora
- Spettroscopia NMRDocumento32 pagineSpettroscopia NMRTrandafir LacramioaraNessuna valutazione finora
- Struttura Elettrica Della Materia, Particelle ElementariDocumento2 pagineStruttura Elettrica Della Materia, Particelle Elementarialessandro temelliniNessuna valutazione finora
- Lezione 9 La Struttura AtomicaDocumento45 pagineLezione 9 La Struttura AtomicaDestiny DuruNessuna valutazione finora
- Lo Spettro ElettromagneticoDocumento4 pagineLo Spettro ElettromagneticoGabriele VisentinNessuna valutazione finora
- AtomoDocumento24 pagineAtomoFederica ZiccolellaNessuna valutazione finora
- Prima Lez RM 2013Documento53 paginePrima Lez RM 2013Andrea VanoniNessuna valutazione finora
- La Struttura Elettronica Degli Atomi e Le Proprietà PeriodicheDocumento5 pagineLa Struttura Elettronica Degli Atomi e Le Proprietà PeriodicheIkram LazarNessuna valutazione finora
- Lezione 3 - Meccanica Quantistica - Prima ParteDocumento38 pagineLezione 3 - Meccanica Quantistica - Prima ParteRiccardo GroppoNessuna valutazione finora
- Gli SpecchiDocumento136 pagineGli SpecchiMariaGloriaNessuna valutazione finora
- RadiazioniDocumento14 pagineRadiazioniEleonora Francesco Consalvo DonzelliNessuna valutazione finora
- Onde Elettromagnetiche PDFDocumento7 pagineOnde Elettromagnetiche PDFOsteofisioNessuna valutazione finora
- Disposizione Degli Elettroni Nell'AtomoDocumento3 pagineDisposizione Degli Elettroni Nell'AtomoAlessioContu100% (1)
- Frova MataloniDocumento115 pagineFrova MataloniNicola TraficanteNessuna valutazione finora
- AEM Capitolo8 0708Documento21 pagineAEM Capitolo8 0708TrinchettoNessuna valutazione finora
- Chimica Lez 03Documento23 pagineChimica Lez 03mikaelNessuna valutazione finora
- Dualismo Onda ParticellaDocumento2 pagineDualismo Onda Particellagionx03 ggNessuna valutazione finora
- Lezione 3. Teoria ElettronicaDocumento42 pagineLezione 3. Teoria ElettronicaRagne FranciscoNessuna valutazione finora
- Strumentazione BiomedicaDocumento15 pagineStrumentazione BiomedicaMarco AmatrudaNessuna valutazione finora
- Quanto Meccanico e L'effetto Fotoelettrico ColoreDocumento1 paginaQuanto Meccanico e L'effetto Fotoelettrico ColoreFatima CaccamoNessuna valutazione finora
- Relazione Chimica FisicaDocumento14 pagineRelazione Chimica FisicaDavide LuiseNessuna valutazione finora
- Microsoft PowerPoint - 2 Sorgente Ei e Sett MagnDocumento30 pagineMicrosoft PowerPoint - 2 Sorgente Ei e Sett Magnmastermv2013Nessuna valutazione finora
- La Forza Magnetica e Le Linee Del Campo MagneticoDocumento5 pagineLa Forza Magnetica e Le Linee Del Campo MagneticoAntonio TerraccianoNessuna valutazione finora
- Radioprotezione - Parte I - Aa 15 - 16Documento108 pagineRadioprotezione - Parte I - Aa 15 - 16B BadamNessuna valutazione finora
- Elettrone 578Documento65 pagineElettrone 578RupilenzoNessuna valutazione finora
- Magnetoterapia 5Documento33 pagineMagnetoterapia 5Walter PelaezNessuna valutazione finora
- Gli Orbitali e La Densità Elettronica. Configurazione Elettronica Degli ElementiDocumento7 pagineGli Orbitali e La Densità Elettronica. Configurazione Elettronica Degli ElementiCristina IngheseNessuna valutazione finora
- Dispensa Illuminotecnica 13 14Documento95 pagineDispensa Illuminotecnica 13 14Claudio CiavattaNessuna valutazione finora
- chimica - capitolo 7 e 9Documento4 paginechimica - capitolo 7 e 9giovannidifonzo10Nessuna valutazione finora
- Il Campo MagneticoDocumento17 pagineIl Campo MagneticoPierluigi CastellanetaNessuna valutazione finora
- La Crisi Della Fisica ClassicaDocumento13 pagineLa Crisi Della Fisica Classicadavide abbattistaNessuna valutazione finora
- Fisica EsameDocumento21 pagineFisica EsameGiovanni TinoNessuna valutazione finora
- Tecniche Induzione Sogno LucidoDocumento60 pagineTecniche Induzione Sogno LucidoDiletta CaccìaNessuna valutazione finora
- Articolo Macri Et Al 2012-03Documento18 pagineArticolo Macri Et Al 2012-03RobNessuna valutazione finora
- Allegati AV 1 Ita 2MbDocumento80 pagineAllegati AV 1 Ita 2MbRobNessuna valutazione finora
- Manuale Istruzione Lavastoviglie Bosch Synthesi SigmaDocumento28 pagineManuale Istruzione Lavastoviglie Bosch Synthesi SigmaRob0% (1)
- Bando Speciale 2014 Progetti AutofinanziatiDocumento24 pagineBando Speciale 2014 Progetti AutofinanziatiAlessandro CuccinielloNessuna valutazione finora
- Lezione 2Documento8 pagineLezione 2RobNessuna valutazione finora
- Lezione 4Documento6 pagineLezione 4RobNessuna valutazione finora
- Lezione 3Documento7 pagineLezione 3RobNessuna valutazione finora
- Lezione 3Documento7 pagineLezione 3RobNessuna valutazione finora
- RIMINI-Convocazione Ufficiale 2014Documento19 pagineRIMINI-Convocazione Ufficiale 2014RobNessuna valutazione finora
- Manuale Istruzione Lavastoviglie Bosch Synthesi SigmaDocumento28 pagineManuale Istruzione Lavastoviglie Bosch Synthesi SigmaRob0% (1)
- Bando Speciale 2014 Progetti AutofinanziatiDocumento24 pagineBando Speciale 2014 Progetti AutofinanziatiAlessandro CuccinielloNessuna valutazione finora