Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Anatomia - Patologica - Il - Matt O CPN NEFRO DA 478 PDF
Caricato da
soniablaireTitolo originale
Copyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Anatomia - Patologica - Il - Matt O CPN NEFRO DA 478 PDF
Caricato da
soniablaireCopyright:
Formati disponibili
Appunti di Anatomia Patologica
Canale B
A cura di:
G. Mazzanti
C.A. Mazzoli
1
NOTA:
Gli appunti presenti in questo documento sono relativi al programma di Anatomia Patologica del
canale B.
Non tutti gli argomenti trattati corrispondono a lezioni svolte dai Docenti, per questo motivo alcuni
argomenti non sono altro che la schematizzazione ottenuta dalla lettura e dalla successiva
rielaborazione di pi testi trattanti la materia tra cui, soprattutto, il testo consigliato per la preparazione
dellesame (Robbins- Le basi patologiche delle malattie).
Questo non significa in nessuna maniera che questo documento si prefigge di sostituire il testo
consigliato!.
A causa della continua evoluzione della materia, dellaggiornamento dei testi consigliati e degli
argomenti trattati a lezione si consiglia di utilizzare questi appunti come un supporto allo studio della
materia e non come unico punto di riferimento nella preparazione dellesame.
Buona Lettura.
2
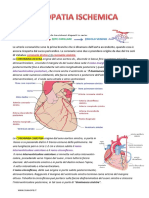
Cardiopatia ischemica
(Prof. XXX)
Termine generico utilizzato per indicare una serie di sindromi derivanti da
unischemia miocardica.
Con il nome ischemia non si considera solamente linsufficienza di ossigeno, cio
lipossiemia, ma anche una ridotta disponibilit di substrati nutritivi ed unindeguata
rimozione di metaboliti.
Dunque con il nome ischemia si considera la riduzione della perfusione rispetto alle
richieste nutritive del miocardio medesimo.
Le cardiopatie ischemiche sono la prima causa di morte nei paesi evoluti, costituendo
la causa di 1/3 dei decessi.
Le manifestazioni cliniche della cardiopatia ischemica possono essere divise in quattro
sindromi
- angina pectoris: lischemia non in grado di provocare la necrosi del muscolo
cardiaco
- infarto miocardico: la durata e la gravit dellischemia sono in grado di provocare la
morte del muscolo cardiaco
- cardiopatia ischemica cronica
- morte cardiaca improvvisa
Di queste linfarto miocardico acuto, langina pectoris di tipo instabile e la morte
cardiaca improvvisa sono dette sindromi coronariche acute.
CAUSE DELLE CARDIOPATIE ISCHEMICHE
Aterosclerosi delle coronarie
La principale causa delle cardiopatie ischemiche la riduzione del flusso ematico
coronarico dovuta ad aterosclerosi arteriosa coronarica.
Laterosclerosi, venendo ad essere un ostruzione al flusso sanguigno, costituisce di per
s una causa di ischemia miocardica, che per nelle fasi iniziali generalmente
compensata da meccanismi fisiologici.
Il passaggio ad un processo non pi compensato e dunque evidente clinicamente, pu
avvenire attraverso diversi meccanismi.
Restringimento aterosclerotico fisso di dimensioni tali da provocare stenosi
permanente delle arterie coronariche (pi del 75% del lume ostruito).
Modificazioni acute della morfologia della placca, che passa da una condizione di
stabilit ad una di instabilit. La placca pu andare incontro a:
a) emorragia interna dellateroma: conseguente crescita di dimensioni della placca che
pu dunque provocare stenosi permanente erosione/ulcerazione della placca:
vengono esposti i componenti della mbr basale endoteliale con conseguente
3
attivazione di un processo di cicatrizzazione ed aumento delle probabilit di
formazione di un trombo.
b) Fissurazione: emorragie che espongono le strutture connettivali dellendotelio, con
conseguente cicatrizzazione ed aumento delle probabilit di formazione del trombo.
c) Rottura: esposizione delle strutture connettivali dellendotelio, con conseguente
cicatrizzazione ed aumento delle probabilit di formazione del trombo.
Dunque queste modificazioni acute della morfologia della placca si traducono in tutti i
casi in un processo trombotico che comporta ostruzione del lume e dunque stenosi
coronarica.
La trombosi intraluminale che sovrasta la placca aterosclerotica rotta o ulcerata pu
dare anche esiti di embolizzazione del trombo.
aggregazione piastrinica
vasospasmo
Normalmente questi quattro meccanismi interagiscono fra loro e concorrono
reciprocamente a causare un processo aterosclerotico.
Processo infiammatorio persistente
Un processo infiammatorio persistente e dunque cronico comporta una lesione
endoteliale a cui deve conseguire un processo continuo di riparazione.
Secondo una moderna teoria la lesione infiammatoria vedrebbe riparazione attraverso
la migrazione delle cellule muscolari lisce dello strato subendoteliale verso gli strati
superficiali dellendotelio.
Queste cellule mimano le normali cellule muscolari, ma si differenziano in modo tale
da avere nel citoplasma una minore quota contrattile ed una maggiore possibilit di
sintesi del connettivo e del collagene.
Sono denominate miofibroblasti: una volta giunte negli strati superficiali riparano la
lesione producendo grandi quantit di collagene di tipo I che pi fibroso del normale
collagene di tipo III prodotto dai fibroblasti e normalmente presente a livello
endoteliale.
La secrezione di collagene di tipo III si traduce dunque in un processo di fibrosi cronica
che comporta sclerosi della parete del vaso: la maggiore quantit di collagene fibroso
porta infatti ad una diminuzione dellelasticit della parete vasale.
Nel momento di insorge di una contrazione muscolare della parete vasale, dunque di
un vasospasmo, la perdita di elasticit provoca un ritorno elastico pi lento della
parete vasale e dunque uno stato di costrizione pi prolungato.
Oltre a queste cause primarie di cardiopatia ischemica vi sono condizioni che
concorrono ad aumentare lischemia:
- aumento della richiesta energetica cardiaca (ipertrofia, esercizio fisico, emozioni,
stress)
4
- diminuzione della disponibilit di sangue ed ossigeno, per diminuzione della
pressione arteriosa sistemica (shock)
- ipossia
- aumento della frequenza cardiaca che:
aumenta la richiesta energetica cardiaca (maggior numero di contrazioni al
minuto)
riduce lapporto di sangue (diminuzione della durata relativa della diastole)
Restringimento aterosclerotico fisso
La placca aterosclerotica pu provocare progressiva ostruzione del lume che porta a
stenosi.
Le occlusioni che si sviluppano lentamente nel tempo possono stimolare lo sviluppo di
circoli collaterali che proteggono dallischemia miocardica distale.
Laterosclerosi coinvolge spesso tutti e tre i rami principali coronarici: discendente
anteriore sinistra, circonflessa sinistra, coronarica destra.
Talvolta sono anche interessate le principali diramazioni epicardiche secondarie..
Non vi solitamente aterosclerosid ei rami intramurali.
Lesione ostruttiva del 75% o maggiore: ischemia sintomatica indotta dallo sforzo.
Laumento del flusso coronarico fornito da meccanismi di vasodilatazione
compensatoria non sufficiente a fronteggiare anche modesti aumenti di richiesta del
miocardio
Lesione ostruttiva del 90%: ischemia sintomatica anche a riposo.
Modificazioni acute della placca
Le modificazioni acute della placca sono levento scatenante di quasi tutte le sindromi
coronariche acute.
La placca, precedentemente stabile, diviene una lesione aterotrombosica
potenzialmente pericolosa per la vita a causa di:
- emorragia intramurale
- erosione superficiale
- ulcerazione
- fissurazione
- rottura della placca aterosclerotica.
Stabilit della placca:
Le placche che:
- contengono grandi quantit di necrosi, di cellule schiumose e lipidi extracellulari
nel loro nucleo centrale
- sono provviste di un cappuccio fibroso molto sottile o con poche cellule muscolari
liscie
5
- presentano ammassi di cellule infiammatorie nel nucleo centrale sono pi
predisposte alla rottura e dunque sono dette placche vulnerabili.
Influenze intrinseche sulla stabilit della placca:
Infiammazione:
la formazione di una placca aterosclerotica richiede comunque la presenza di un
lesione iniziale o comunque unalterazione dellendotelio che provoca aumento della
sua permeabilit, aumento dellespressione di molecole di adesione endoteliale, che
facilitano linterazione con cellule dellinfiammazione circolanti, aumento del rilascio
di chemochine.
Di conseguenza nel momento di creazione della placca aterosclerotica, si ha:
- Interazione cellule endoteliali-leucociti circolanti.
- Accumulo di cellule T e macrofagi nella parete dellarteria
- Fagocitosi di lipidi da parte dei macrofagi e trasformazione in cellule schiumose
- Danno tissutale mediato da fattori rilasciati dalle cellule infiammatorie e
comparsa di aree di necrosi.
Il cappuccio fibroso della placca si forma ad opera dei miofibroblasti, migrati
nellintima endoteliale dallo strato muscolare liscio dellendotelio stesso. Esso il
principae responsabile della stabilit della placca.
Il cappuccio fibroso per in continuo rimodellamento: continuamente prodotto dalle
cellule muscolari lisce e degradato ad opera di metallo proteasi secrete dai macrofagi.
Una destabilizzazione della placca pu facilitare il rilascio di metallo proteasi ad opera
dei macrofagi e di conseguenza spostare lequilibrio verso la distruzione del cappuccio
fibroso medesimo facilitando ulteriormente la rottura della placca.
Inoltre la presenza di forte infiammazione provoca aumento delle aree necrotiche nel
nucleo centrale della placca, ceh dunque diviene meno consistente e pi fragile agli
stimoli meccanici.
Uninfiammazione persistente provoca infine fibrosi e dunque sclerosi della placca, con
tardivo rilasciamento successivamente ad un vasospasmo.
Influenze estrinseche sulla stabilit della placca
Statine
Le statine sono farmaci con effetto ipolipemizzante e anti-infiammatorio.
Per queste due caratteristiche contribuiscono a stabilizzare la placca
Stimolazione adrenergica
Pu aumentare lo stress meccanico sulla placca attraverso vasospasmo ed induzione di
ipertensione.
6
Trombosi
Leffetto delle modificazioni acute della placca in tutti i casi ( tranne emorragia
intraluminale) lesposizione delle componenti interne dellendotelio, con conseguente
esiti cicatriziali trombotici nella maggior parte dei casi.
Il trombo che si sovrappone alla placca rotta, prima solo parzialmente stenotica pu
provocare:
- occlusione completa trombo transmurale
- occlusione incompleta trombo murale che pu anche andare incontro ad aumento
o riduzioni nel tempo.
Il trombo murale pu andare incontro ad embolizzazione.
Il trombo inoltre potente attivatore di molti segnali che inducono proliferazione delle
cellule muscolari lisce, che possono contribuire alla crescita delle lesioni
aterosclerotiche.
Aggregazione piastrinica
Sempre presente in seguito a ulcerazione, fissurazione o rottura della placca, poich
queste modificazioni comportano la necessit di un processo cicatriziale.
Le piastrine attivate producono fattori pro-infiammatori e fattori che inducono
vasospasmo, dunque che contribuiscono alla destabilizzazione della placca e ad una
sotanziale ischemia cardiaca.
Vasospasmo
Fattori che stimolano un vasospasmo:
- Agonisti adrenergici circolanti
- Fattori rilasciati localmente in seguito allaggregazione piastrinica.
- Alterato rapporto nella secrezione endoteliale di fattori vasocostrittori rispetto a
quelli vasodilatanti, dovuta alle disfunzioni endoteliali associate alla formazione
dellateroma.
- Mediatori rilasciati dalle cellule infiammatorie
La vasocostrizione contribuisce al processo ischemico:
riducendo le dimensioni del lume
aumentando le forze meccaniche locali sulla placca e facilitandone la rottura.
Angina pectoris
Sindrome clinica caratterizzata da attacchi parossistici e recidivanti di dolore toracico
retrosternale o precordiale (descritto come oppressivo, costrittivo, soffocante o
7
trafittivo) causati da ischemia miocardica transitoria (15 secondi-15 minuti) che dura
troppo poco per indurre necrosi del miocardio.
Langina pectoris si divide in:
Angina stabile
la forma pi comune anche detta angina pectoris tipica
provocata dalla riduzione della perfusione cardiaca ad un livello critico a
causa di aterosclerosi coronarica stenosante cronica e fissa
il cuore vulnerabile a qualsiasi aumentata richiesta energetica
una forma alleviata dal riposo o dalla nitroglicerina, potente vasodilatatore.
Angina variante di Prinzmetal
una forma rara
provocata da vasospasmo coronarico e si verifica a riposo
i soggetti affetti possono avere aterosclerosi coronarica ma ci non
determinante; dimostrato dal fatto che il dolore non influenzato da attivit
fisica, frequenza cardiaca, pressione arteriosa
alleviata dalla nitroglicerina a cui risponde prontamente
Angina instabile o ingravescete
una forma che presenta frequenza e durata progressivamente crescenti ed
scatenata da sforzi progressivamente minori.
indotta da rottura della placca a cui si sovrappone trombosi e successiva
embolizzazione e/o vasospasmo.
unischemia molto vicina ad indurre infarto acuto di cui spesso rappresenta il
prodomo tanto da essere anche definita angina preinfartuale.
Infarto miocardico
Necrosi di unarea del muscolo cardiaco causata da ischemia locale. Le dimensioni
dellarea necrotica perch si possa parlare di infarto devono essere maggiori di 3 cm.
Le lesioni minori di 3 cm. infatti non sono necessariamente dovute ad ischemia, ma
possono riconoscere altre causa
Incidenza e fattori di rischio
Si tratta della forma pi importante di cardiopatia ischemica essendo da sola la
principale causa di morte negli USA e nei paesi industrializzati.
I fattori di rischio coincidono con quelli dellaterosclerosi: ipertensione, diabete mellito,
ipercolesterolemia, iperlipoproteinemia, fumo.
Il rischio dunque cresce progressivamente con let.
I maschi sono pi colpiti delle femmine, le quali sono protette durante let fertile, ma
il cui rischio aumenta molto durante la menopausa per il calo dei livelli estrogenici.
8
Interessamento della parete cardiaca
Gli infarti miocardici possono suddividersi in:
Infarti transmurali:
sono la prevalenza
la necrosi interessa lintero spessore della parete ventricolare
solitamente larea necrotica corrisponde al territorio di irrorazione di una
singola arteria coronaria
sono correlati allaterosclerosi coronarica, con rottura della placca e successiva
sovrapposizione trombotica.
Infarti subendocardici (non transmurali):
sono pi rari
larea di necrosi limitata al terzo pi interno della parete ventricolare
frequentemente larea necrotica si estende lateralmente rispetto al territorio di
irrorazione di un singola coronaria
la regione subendocardica la prima ad essere colpita da ischemia perch
sviluppa meno facilmente circoli collaterali e perch durante la sistole si ha
compressione delle strutture vascolari al suo interno con conseguente riduzione
della perfusione
le cause che possono determinare infarto subendocardico sono:
- rottura della placca aterosclerotica e formazione di un trombo che
va per incontro a lisi prima che la necrosi si sia estesa a tutto lo
spessore della parete ventricolare.
- stato ipotensivo importante e prolungato (shock) che causa ridotta
perfusione complessiva ed un infarto subendocardico
tendenzialmente circonferenziale
Eziologia
Le cause dellinfarto sono paincipalmente:
occlusione delle coronarie (85%)
tromboembolia (10%)
vasospasmo (5%)
inspiegati
Occlusione delle coronarie
- Formazione della placca aterosclerotica.
- Modificazione acuta della placca che implica esposizione del collagene
subendoteliale e del suo contenuto interno.
- Adesione delle piastrine, con formazione di un monostrato e loro attivazione con
rilascio di potenti fattori aggreganti (TXA2).
- Aggregazione piastrinica con rilascio di mediatori che inducono:
- vasospasmo: riduzione del lume endoteliale
- attivazione della via estrinseca della coagulazione: cicatrizzazione
9
e formazione del trombo.
- In pochi minuti il trombo diviene occludente.
Tromboembolia
Per rottura di un frammento del trombo e formazione di un embolo
Vasospasmo
Isolato, intenso, relativamente prolungato, pu essere in associazione o meno con
aterosclerosi coronarica.
Spesso associato alluso di cocaina ed a fattori rilasciati dallaggregazione piastrinica.
Inspiegati
Sono infarti senza riscontro di aterosclerosi o trombosi, che possono essere causati per
esempio da malattie dei piccoli vasi coronarici intramurali.
Localizzazione del danno ischemico
Frequenza delle stenosi critiche e trombosi di ognuno dei tre tronchi coronarici
principali e corrispondenti aree di necrosi miocardica:
- coronaria discendente anteriore sinistra (40-50%): parete anteriore del ventricolo
sx ed apice; porzione anteriore del setto interventricolare.
- Coronaria destra (30-40%): parete inferiore/posteriore del ventricolo sx (base);
porzione posteriore del setto interventricolare
- Coronaria circonflessa sinistra (15-20%) parete laterale del ventricolo sx, senza
apice.
Risposta del miocardio
Generale
Locclusione di unarteria coronarica principale determina ischemia e potenzialmente
necrosi nellarea interessata dalla sua irrorazione.
Le lesioni ischemiche hanno inizio a livello subendocardico e mano a mano la necrosi
avanza come un fronte donda coinvolgendo progressivamente uno spessore pi ampio.
10
Approssimativamente la risposta del miocardio pu essere cos schematizzata:
tempo Modificazioni chiave
secondi Cessazione della glicolisi aerobia
Innesco della glicolisi anaerobia, con mancata produzione di ATP ed
accumulo di prodotti tossici, come lacido lattico.
< 2 minuti Perdita di contrattilit del miocardio, che a volte pu provocare comparsa
di insufficienza cardiaca acuta prima dellinsorgenza della ncrosi
miocardica
10 minuti Diminuzione dellATP fino al 50% del normale
Alterazioni ultrastrutturali del danno reversibile (deplezione di
glicogeno, rigonfiamneto cellulare e mitocondriale)
40 minuti Diminuzione dellATP fino al 10% del normale
Alterazioni ultrastrutturali del danno reversibile (deplezione di
glicogeno, rigonfiamneto cellulare e mitocondriale)
20-40
minuti
Comparsa di danno cellulare irreversibile (principalmente difetti
strutturali del sarcolemma)
Necrosi coagulativa dei miociti (in minore misura anche apoptosi
> 1 ora Danno microvascolare
Dunque in sintesi si ha che
La necrosi coagulativa con morte dei miociti si verifica dopo 30 minuti dallinizio
dellinfarto.
Linfarto miocardico che pre nta una necrosi e tesa, si verifica in seguito ad
unischemia severa prolungata, per almeno 2-4 ore.
se s
La necrosi porta a perdita permanente della funzionalit della regione interessata.
In alcuni casi questa perdita di funzionalit si pu accompaganare anche a presenza di
aritmie.
In studi sperimentali in 6 ore si ha la necrosi dellintera regione irrorata dallarteria
coronarica occlusa.
In alcuni pazienti invece la necrosi completa insorge in tempi molto pi lunghi (10-12
ore o pi), perch la presenzadi stenosi parziale ed aterosclerosi ha indotto lo sviluppo
di circoli collaterali.
Modificazioni macroscopiche
Le modificazioni macroscopiche dovute a infarto miocardico sono cos schematizzabili:
tempo Modificazioni macroscopiche
1-4 ore Nulla
4-12 ore Occasionalmente si ha marmorizzazione scura: comparsa sui prelievi
fissati di chiazza rosso-bluastre, dovute alla presenza di sangue
stagnante o intrappolato
12-24 ore Evidente marmorizzazione scura.
Presenza di aree anemiche, pallide del mocardio
11
1-3 giorni Comparsa di aree centrali di rammollimento necrotico, giallo-brunastre
3-7 giorni Estensione delle aree centrali di rammollimento necrotico, giallo-
brunastro
Comparsa di un bordo iperemico rosso, che delimita la zona necrotica,
costituito da abbondante tessuto di granulazione molto vascolarizzato.
Questo un momento pericoloso in quanto larea necrotica richiama
abbondante infiltrato infiammatorio.
Una situazione di infiammazione si accompagna dunque ad un
rammollimento della struttura ed alla mancanza di strutture resistenti.
Qui si rischia la rottura.
7-21 giorni Massima estensione dellarea necrotica giallo-bruna delimitata da bordi
iperemici depressi soffici colore rosso scuro
2-8
settimane
Cicatrice grigio-biancastra che progredisce dalla periferia verso il centro
dellinfarto.
Allinfiammazione segue dunque la riparazione in quanto non vi la
possibilit di sostituire i miociti, che sono cellule perenni
> 2 mesi Cicatrice completa
Una volta guarita la lesione non pi databile.
Modificazioni al microscopio ottico
Le modificazioni microscopiche visibili al microscopio ottico sono cos schematizzabili:
tempo Modificazioni microscopiche (m.o.)
1-4 ore Comparsa ai margini di fibrocellule ondulate, per leffetto delle fibre vive
hanno sulle fibre morte.
Le fibre morte non sono contrattili.
Le fibre vitali adiacenti alle fibre morte, stirano le stesse nella sistole
producendo effetto ondulato.
Miocitolisi: degenerazione vacuolare reversibile, con comparsa di vacuoli
entro le cellule.
pi frequente nella zona di miociti vitali subendocardici
4-12 ore Necrosi coagulativa iniziale evidente, con comparsa delle prime
alterazioni della colorazione
12-24 ore Estensione necrosi coagulativa ( nuclei picnotici e citoplasma eosinofilo).
Comparsa della necrosi a bande di contrazione: le bande di contrazione
sono bende trasversali, eosinofile, composte da pacchetti di sarcomeri
ipercontratti.
Sono probabilmente dovute allalterazione della permeabilit della
membrana che provoca esposizione delle cellule morenti ad elevate
concentrazioni di calcio, con conseguente ipercontrazione.
Iniziale infiltrato neutrofilo
1-3 giorni Necrosi coagulativa con perdita dei nuclei e delle striature trasversali.
Infiltrato neutrofilo
3-7 giorni Disintegrazione dei miociti e dei neutrofili morti.
Fagocitosi macrofagica delle cellule morte.
Formazione di tessuto di granulazione
7-21 giorni Tessuto di granulazione ben sviluppato con abbondante
vascolarizzazione e depositi di collagene
12
2-8
settimane
Aumento dei depositi di collagene con riduzione della cellularit
> 2 mesi Cicatrice densa collagene
Modificazioni l microscopio elettronico
Le modificazioni microscopiche visibili al microscopio elettronico sono cos
schematizzabili:
Fase reversibile: perdita di glicogeno, rigonfiamento cellulare e mitocondriale,
rilassamento delle miofibrille.
Fase iireversibile: rottura del sarcolemma
Riperfusione del miocardio
La perfusione del tessuto in corso di ischemia cardiaca consente di limitare al massimo
il danno prodotto dallinfarto.
Tecniche per ripristinare il flusso:
Trombolisi: dissoluzione del trombo per azione della streptochinasi o
dellattivatore tissutale del plasminogeno, che consentono attivazione del
sistema fibrinolitico.
Angioplastica con il palloncino (percutaneous transluminal coronary
angioplastic o PTCA): consente non solo di eliminare il trombo, ma anche la
placca sottostante.
Bypass aorto-coronarico: consente di ristabilire il flusso a valle.
Poich ad un determinato momento dallinizio dellinfarto non tutto il miocardio
ugualmente ischemico (regione subendoteliale, colpit per prima, avr ischemia pi
avanzata etc..) gli esiti della riperfusione varieranno a seconda della rapidit con cui il
cuore viene riperfuso ed a seconda della regione miocardica.
Riperfusione miocardica entro 15-20 minuti:
Prevenzione della necrosi in tutto lo spessore della parete cardiaca.
Nelle aree pi danneggiate alla riperfusione segue stordimento miocardico o
disfunzione ventricolare prolungata post-ischemica.
Questo consiste nella persistenza di alterazioni biochimiche e funzionali dei miociti
salvati dalla riperfusione che si possono tradurre in uno stato di scompenso cardiaco
reversibile.
La situazione pu essere superata mediante temporanea assistenza cardiologica.
13
Riperfusione miocardica entro 3-6 ore:
Salvataggio del tessuto ischemico ma ancora vitale, che per rimane stordito.
Le aree necrotiche non sono salvabili e tali rimangono anche dopo riperfusione
Riperfusione miocardica dopo 6 ore:
Non riduce apprezzabilmente le dimensioni dellinfarto.
Pu tuttavia avere un effetto benefico limitando lestensione dellinfarto.
Danni causati da riperfusione
Stravaso emorragico dellinfarto incompleto: alcuni vasi colpiti dallischemia
hanno alterate condizioni di permeabilit
Accelerazione della morte dei miociti gi danneggiati
Aumento della necrosi a bande di contrazione nei miociti gi danneggiati: per
leumentata esposizione al calcio dovuta alla maggiore presenza di sangue.
Lesione di una certa quantit di cellule ex-novo, per la maggiore produzione di
radicali liberi da parte dellinfiltrato leucocitario trasportato dal sangue: si
parla in questo caso di danno da riperfu ione. s
Riginfiamento endoteliale con occlusione dei capillari ed ostacolo alla
riperusione medesima (miocardio non perfuso, no-reflow.
Diagnosi
La diagnosi si fa in base a tre parametri:
Caratteristiche cliniche
ECG
Esami di laboratorio
Caratteristiche cliniche
Quelle tipiche di ogni infarto sono:
- polso debole e rapido
- profusa sudorazione
- dispnea
ECG
Comparsa di nuove onde Q
Esami di laboratorio
14
Misurazione dei livelli plasmatici di alcune macromolecole plasmatiche che
fuoriescono dalle cellule danneggiate dallischemia. In partcolare si utilizzano:
TroponinaI e troponinaT
Sono i marker di danno cardiaco pi utilizzati in quanto altamente sensibili (non sono
normalmente dosabili in circolo) e specifici (sono assolutamente cardio-specifici).
Dopo infarto miocardico i loro livelli aumentano entro 2-4 ore raggiungendo il picco in
24-48 ore.
I livelli rimangono elevati nei 7-10 giorni dopo levento acuto.
Frazione MB della creatina chinasi
Questo isoenzima presente nel miocardio, ma anche in quantit variabili nel muscolo
scheletrico.
Il suo dosaggio dunque sensibile, ma non specifico (i livelli di CK-MB sono elevati
alche in condizioni di lesione del muscolo scheletrico).
Dopo infarto miocardico i loro livelli aumentano entro 2-4 ore raggiungendo il picco in
24 ore.
I livelli tornano normali dopo circa 72 ore.
In assenza di aumento dei livelli sierici delle CK-MB nei primi due giorni di dolore
toracico e delle troponine nei giorni seguenti si pu escludere la diagnosi di infarto.
Conseguenze e complicanze dellinfarto
Disfunzione contrattile: alterazioni della funzionalit ventricolare sx proporzionali alle
dimensioni della necrosi. Si pu giungere a scompenso cardiaco sx (ipotensione,
congestione ed edema polmonare) o addirittura nel 10% dei casi ad una grave
insufficienza di pompa, generalmente associata ad infarti di grandi dimensioni.
Aritmie: disturbi della conduzione o delleccitabilit miocardica dovuti a squilibri
elettrolitici, alluso di farmaci o allaumento della tensione del muscolo cardiaco. Le
aritmie possono tradursi in fibrillazione
Rottura del miocardio: avviene generalmente a 3-7 giorni dallinizio dellinfarto,
quando si ha necrosi ed infiammazione che rammoliscono il tessuto e non si ha
alcun processo riparativo completo. Pu avvenire:
nella parete libera del ventricolo: si ha emopericardio (versamento di sangue nello
spazio compreso fra pericardio e muscolo, spesso fatale).
nel setto interventricolare: shunt sx-dx.
nel muscolo papillare: insufficienza mitralica acuta, di grado severo a cui fanno seguito
rigurgiti.
Pericardite: negli infarti transmurali dopo 2-3 giorni sviluppo di una pericardite che
costituisce lepifenomeno della infiammazione evocata dal sottostante infarto
miocardico.
Estensione dellinfarto: nuove necrosi nelle aree adiacenti a quelle del precedente
infarto che infine confluiscono.
Re-infarto: dovuto ad una situazione di eccitabilit e di conduzione elettrica alterata.
Trombosi murale: la combinazione di anormale contrattilit miocardica regionale che
provoca stasi di sangue, con un danno endocardico, che crea una superficie
trombogenica porta alla creazione di un trombo murale che pu embolizzare.
15
Cardiomiopatia ostruttiva: una complicanza tardiva che si pu verificare se le
cicatrici fibrotiche sono molte o molto estese. I miociti cercano di compensare la
mancanza di tessuto cardiaco funzionante andando incontro ad ipertrofizzazione,
con conseguente diminuzione delle dimensioni delle camere cardiache e possibile
ostruzione delle medesime.
Insufficienza cardiaca congestizia: una complicanza tardauva dovuta alla coesistenza
di fenomeni fibrotici e di ipertrofia (non ostruttiva), i quali provocano alterazioni
del rientro o diminuzione della compliance cardiaca, con conseguente aumento
della pressione polmonare ed eventualmente congestione ed edema polmonare.
Aneurisma ventricolare: dilatazione patologica circoscritta a carico della parete del
ventricolo, delimitata da miocardio cicatrizzato. Pu realizzarsi in due modi:
protrusione della parete ventricolare in corrispondenza dellarea dellinfarto
laneurisma produce irregolarit del profilo della parete e pu essere occupato da un
trombo murale.
Mancanza di protrusione e dunque di irregolarit del profilo della parete, che rimane abbastanza
omogenea. Presenza per di fibroblastosi e dunque inspessimento della parete senza trombosi
murale associata.
Cardiopatia ischemica cronica
la condizione dei pazienti, prevalentemente anziani, che sviluppano insufficienza
cardiaca p ogressiva, come conseguenza di danno miocardico da ischemia severa. r
Nella maggior parte dei casi si tratta di pazienti che sono andati incontro a grave
infarto pregresso, coinvolgente tutte le branche principali delle coronarie, con
conseguente inadeguato apporto sanguigno e perdita di miociti a livello dellintero
miocardio, fibrosi cicatriziale diffusa e diminuzione progressiva ed omogenea della
compliance cardiaca.
La reazione post-infartuale del cuore dunque quella di tentare un ipertrofia
compensatoria.
Lesaurimento funzionale dellipertrofia compensatoria comporta scompenso cardiaco,
conseguente cardiomiopatia dilatativa e dunque infine insufficienza cardiaca.
Il cuore di questi pazienti infatti si presenta sempre ingrossato e pesante (ipertrofia)
ed enormemente aumentato di dimensioni (dilatazione).
C sempre aterosclerosi stenosante grave, associata alle maggiori richieste
energetiche del cuore ipertrofico.
Solitamente sono presenti le cicatrici dei pregressi infarti.
Morte cardiaca improvvisa
Si tratta della morte inattesa per cause cardiache, che si verifica immediatamente
dopo la comparsa dei sintomi (entro 1 ora) o anche senza linsorgenza degli stessi.
Cause
Principalmente dovuta ad un ischemia cardiaca cronica che comporta come
complicanza la comparsa di aritmie letali, come asistolia o fibrillazione ventricolare.
16
La prognosi di questi pazienti migliorata dallimpianto di un defibrillatore elettrico.
Altre cause che si fanno via via pi frequenti con il decrescere dellet possono essere:
- malattie delle coronarie (malformazioni congenite, vasculiti, embolia)
- stenosi valvolare aortica
- alterazioni ereditarie o acquisite del sistema di conduzione
- altre malattie specifiche del miocardio (miocarditi, cardiomiopatie ipertrofiche o
dilatative)
- malattie valvolari (insufficienza valvolare, prolasso della mitrale)
- ipertensione polmonare
17
Valvulopatie
Sono le patologie a carico delle valvole cardiache.
Possono determinare:
- stenosi: impossibilit della valvola di aprirsi completamente, ostacolando il
flusso anterogrado.
- Insufficienza: incapacit della valvola di chiudersi completamente
determinando flusso retrogrado.
Le anomalie delle valvole cardiache possono essere:
- pure: se presente solamente la stenosi o linsufficienza
- miste: se insufficienza e stenosi coesistono nella medesima valvola, con
prevalenza eventuale di uno dei due difetti sullaltro.
La patologia pu essere:
- isolata: se viene colpita una sola valvola
- combinata: se siano colpite pi valvole contemporaneamente (compromissione
plurivalvolare).
La patologia pu essere dovuta a :
- anomalia primitiva delle valvole: quasi sempre nella stenosi
- anomalia delle strutture di sostegno senza correlata anomalia delle valvole: pu
succedere nellinsufficienza cardiaca. Il flusso retrogrado infatti pu essere
causato anche da
Dilatazione della camera ventricolare con spostamento associato dei
muscoli papillari verso il basso e verso lesterno, impedendo
laccollamento dei lembi valvolari insufficienza atrio-ventricolare
Dilatazione dellaorta o dellarteria polmonare con conseguente
allontanamento delle commessure valvolari insufficienza aortica o
polmonare
Alterazioni nelle corde tendinee e nei muscoli papillari.
La patologia pu essere:
- congenita
- acquisita
Le alterazioni del flusso sono speso riscontrabili per la produzione di rumori cardiaci
detti soffi.
Le pi frequenti valvulopatie in assoluto sono:
- stenosi acquisita della valvola aortica: per calcificazione di una valvola aortica
normale o congenitamente bicuspide
- insufficienza aortica: per diltazione dellaorta ascendente conseguente
allipertensione arteriosa ed allet.
- Stenosi mitralica: conseguente a malattia reumatica
- Insufficienza mitralica: conseguente a degenerazione mixomatosi o prolasso
mitralico.
18
Degenerazione valvolare conseguente a calcificazione
Le valvole sono sottoposte a notevoli stress meccanici ripetitivi a causa di:
- > 40 milioni di cicli cardiaci/ anno
- deformazione tissutale meccanica ad ogni ciclo
- gradiente presso rio transvalvolare presente nella fase di chiusura.
Le valvole dunque soffrono di danno meccanico cumulativo, che viene ad esplicarsi
spesso in una calcificazione senile.
Stenosi aortica calcifica
Stenosi aortica acquisita conseguente al processo di usura e lacerazione progressivo e
conseguente linvecchiamento, con conseguente calcificazione della valvola aortica.
La valvola aortica interessata da stenosi calcifica pu essere:
- Normale: nella maggior parte dei casi. La stenosi aortica diviene evidente
intorno ai 70-80 anni.
- Congenitamente bicuspide:
presente nell1,4% dei nati vivi.
Formata solamente da 2 cuspidi, solitamente asimmetriche; la cuspide di
dimensioni > presenta spesso un rafe mediano, residuo dellincompleta
separazione delle cuspidi durante lo sviluppo.
Il rafe rappresenta la sede pi frequente di calcificazioni e predispone la
valvola congenitamente bicuspide ad una calcificazione pi precoce, che si
manifesta dunque intorno ai 60-70 anni.
Necessaria differenziazione con le valvole bicuspidi acquisite (divengono
bicuspidi in seguito a lesioni infiammatorie, a cui segue la fusione
cicatriziale), che presentano una cuspide di dimensioni dopie rispetto
allaltra, con commessura fusa nel suo centro.
Morfologia
Presenza di masserelle calcifichi soprattutto alla base delle cuspidi, con protrusione
allinterno dei Seni di Valsala, impedendo cos lapertura delle cuspidi.
Perch si parli di stenosi aortica larea valvolare funzionale si deve ridurre al punto di
costituire evidente ostacolo allefflusso, con progressivo sovraccarico del ventricolo sx.
Diagnosi differenziale con la stenosi aortica conseguente al malattia reumatica
rispetto alla quale la stenosi calcifica senile vede:
- mancanza di fusione delle commessure
- assenza di anomalie strutturali a carico della mitrale.
19
Clinica
i. Ostacolo allefflusso del ventricolo sx.
ii. Sovraccarico presso rio del ventricolo sx.
iii. Sviluppo compensatorio di ipertrofia concentrica per mantenere costante la
gittata cardiaca.
iv. Ipertrofia che predispone il miocardio allischemia angina pectoris e deficit
miocardio.
v. Insufficienza cardiaca cronica.
vi. Scompenso cardiaco.
In questo caso la presenza o lassenza di una sintomatologia evidente un fattore
predittivo fondamentale della prognosi:
- presenza di sintomatologia evidente: linizio della presentazione dei sintomi
preannuncia lesaurimento delle capaci compensatorie del cuore. Prognosi
sfavorevole, a meno di non intervenire chirurgicamente mediante sostituzione
valvolare.
- Assenza di sintomatologia evidente: prognosi favorevole.
Calcificazione anulus mitralico
Depositi calcifici degenerativi nellanello fibroso della valvola mitrale.
Pi comune:
- nelle donne, di et > 60 anni
- nei pazienti con prolasso mitralico (degenerazione mixomatosa)
- nei pz con elevata pressione interventricolare sx.
Morfologia: noduli di 2-5 mm. irregolari, duri, localizzati dietro ai lembi valvolari.
In genere non compromette la funzione valvolare.
Raramente provoca:
- stenosi: riduzione dellaperture dei lembi
- reflusso retrogrado: interferenza con la contrazione sistolica dellanello
valvolare
- aritmie
- morte improvvisa: molto rara, solo se i depositi di calcio sono cos profondi da
ledere il sistema di conduzione atrio-ventricolare.
I pz con calcificazione dellanello mitralico sono a maggiore rischio di:
- ictus: i noduli calcifici sono sede di apposizione trombotica con possibilit di
embolizzazione
- endocardite infettiva
20
Degenerazione mixomatosa (prolasso) della valvola mitrale
Processo patologico molto diffu o che denominato: s
o
s
e
- prolasso mitralico: punto di vista clinico
- degenerazione mixomatosi: punto di vista anatomo-patologico.
caratterizzato dal fatto che uno o entrambi i lembi mitralici sono di consistenza
molle (floppy) e prolassano, sporgendo come un palloncino nellatrio sx, durante la
sistole ventricolare.-
Morfologia
Caratteristiche primarie:
- lembi colpiti che si presentano slargati, ridondanti ( a cappuccio), ispessiti.
- Corde tendinee allungata, assottigliate, occasionalmente si rompono.
- Anello valvolare allargato
- Non vi fusione delle commessure (caratteristica della valvulopatia
conseguente a malattia reumatica)
Caratteristiche secondarie:
- ispessimento fibroso dei lembi valvolari, soprattutto nei punti di sfregamento ed
attrito reciproco
- ispessimento fibroso dellendocardio a livello del ventricolo sx, dove schioccano
le corde tendinee enormemente allungate
- ispessimento fibroso dellendocardio a livello dellatrio sx, per lo sfregamento dei
lembi che prolassano
- formazione di trombi nella spf atriale dei trombi
Eziologia
Associata a:
- disturbi ereditari del tessuto connettivo
- alterazione primitiva emodinamica, cellulare o metab lica che induce
danneggiamento e/o rimodellamento del tessuto valvolare mitralico
Clinica
La maggior parte dei pz si pre enta asintomatica.
A volte insufficienza mitralica:
auscultabile come soffio sistolico telesistolico
sintomatologia: dispn a, dolore simil-anginoso, affaticabilit, sintomi
psichiatrici
Nel 3% dei casi si sviluppa una di queste complicanze gravi
Aritmie
Ictus: per embolizzazione aprtire dai trombi valvolari
Endocardite infettiva
Insufficienza mitralica grave, chirurgica:
- ad inizio lento: deformazione delle cuspidi, dilatazione dellanello,
allungamento delle corde
- ad esordio improvviso e brusco: rottura delle corde
21
Febbre reumatica e cardiopatia reumatica
La febbre reumatica una malattia infiammatoria acuta, immunomediata,
multiorgano, che segue di alcune settiamn un episodio di faringite da streptococco di
gruppo A.
e
t
t
e
r
r
Si manifesta generalmente nei bambini tra i 5 ed i 15 anni, con un 20% degli episodi
che si verifica in et adulta.
Clinica
una malattia che colpisce mol i organi e che dunque caratterizzata da molti
elementi.
Manifestazioni maggiori (sintomatologia specifica):
- poliartrite migrante delle grandi articolazioni: una grande articolazione dopo laltra
diviene dolorante e gonfia per alcuni giorni, per poi guarire spontaneamente senza
limitazioni funzionali residue.
- Cardite acuta: infiammazione acuta che colpisce pericardio, miocardio ed
endocardio, da cui la comune denominazione di pancardite. Caratterizzata da
sfregamenti pericardici., rumori cardiaci deboli, aritmie. In alcuni casi la
miocardite acuta pu essere causa di dilatazione cardiaca, che pu evolvere in
scompenso cardiaco.
- Noduli sottocutanei
- Eritema migrante della cute
- Corea di Sydenham: anche detto Ballo di S. Vito, un disordine neurologico
caratterizzato da movimenti involontari, rapidi e non finalizzati.
Manifestazioni minori (sintomatologia non specifica):
- febbre
- artralgia
- livelli plasmatici elevati, per quanto riguarda le pro eine della fase acuta.
La febbre reumatica acuta, si sviluppa pincpalmente dopo 10 giorni, 6 settimane, dopo
lepisodio di faringite acuta da streptococco di tipo A.
Si ritiene che essa sia una reazione di ipersensibilit indotta dagli streptococchi di tipo
A.
Gli anticorpi diretti contro la proteia M streptococcica, cross-reagiscono con anitigeni
self del cuore, delle articolazioni e degli altri tessuti.
Si tratterebbe dunque di una reazione auto-immune.
Dopo il primo episodio acuto la vulnerabilit dellorganismo alla riattivazione della
malattia notevolmente aumentata e si verificano episodi ricorrenti.
Nel corso di questi episodi si pu avere una progr ssione da una cardite reumatica
acuta ad un quadro di cardiopatia reumatica cronica.
Questo generalmente asintomatcio, pur provocando valvulopatia fibrosa
deformante, che provoca in particolare stenosi mitralica, che pu comporta e a
distanza di decenni p oblemi cardiaci severi e talora fatali.
Diagnosi
Si basa sui criteri di Jones:
22
Storia di una precedente infezione da streptococchi di gruppo A associata a 2
manifestazioni maggiori o 1 manifestazione maggiore + 2 manifestazioni minori.
Morfologia
Cardite reumatica acuta:
Presenza a livello di endocardio, miocardio e pericardio (pancardite) di un quadro
infiammatorio acuto.
Le lesioni infiammatorie hanno morfologia caratteristica e vengono dunque
denominate corpi di Aschoff.
I corpi di Aschoff sono lesioni granulomatose, caratterizzate da focolai di collageno,
circondati da linfociti T, rare plasmacellule e macrofagi gonfi, patognomici di FR
(cellule di Anitschow), che talora divengono multinucleati diventando le cosiddette
cellule giganti di Aschoff.
Nel pericardio essudato fibrinoso o siero-fibrinoso (pericardite a pane e burro) che
generalmente si risove senza organizzazione e senza sequele.
Nel miocardio abbondanzadi corpi di Aschoff, soprattutto nel connettivo interstiziale
perivascolare.
Nellendocardio lesioni subendocardiche nellatrio sx, continuamente sollecitate dal
reflusso che danno luogo ad ispessimenti (placche di MacCallum).
Cardiopatia reumatica cronica:
Conseguente allorganizzazione dellessudato fibrinoso, con con eguente fibrosi e
deformazione permanente.
s
t
Caratterizzato da:
- lembi valvolari ispessiti e retratti
- fusione delle commessure stenosi a bocca di pesce o ad asola.
- accorciamento, inspessimento ed avolte fusione delle corde tendinee.
- Cicatrizzazione fibro ica dei corpi di Aschoff.
Nel 65% dei casi vi interessamento della sola valvola mitrale (che sempre
deformata), nel 25% dei casi anche di quella aortica, a volte clinicamente pi
significativa.
Endocardite infettiva
Dovuta a colonizzazione o invasione delle valvole cardiache o dellendocardio parietale
da pare di microbi, con formazione di vegetazioni voluminose e friabili, formate da
fibrina, cellule infiammatorie e ricche di microbi, spesso associate alla distruzione dei
sottostanti tessuti.
Le endocarditi sono divise in :
23
Endocarditi acute:
infezione a carattere tumultuoso e distruttivo sostenuta da microrganismi molto
virulenti
colpisce generalmente valvole cardiache normali
porta a morte pi del 50% dei pz in giorni/settimane nonostante terapia
antibiotica o chirurgica.
Determina la formazione di lesioni necrotizzanti e ulcerative, difficili da trattare
con gli antibiotici e che dunque richiedono la chirurgia. Un esempio
rappresentato da un erosione a carico del sottostante miocardio, con creazione di
una cavit ascessuale (ascesso anulare).
Endocardite subacuta:
infezione a decorso insidioso che pu essere protratto per settimane o mesi
sostenuta da microrganismi meno virulenti
colpisce generalmente cuori gi affetti da lesioni, come deformit valvolari
il trattamento con antibiotici utile e spesso le lesioni guariscono anche
spontaneamente
causa minore distruzione valvolare dellendocardite acuta
Eziologia
Fattori predisponesti:
- diverse alterazioni cardiache: cardiopatia reumatica, prolasso mitrale, stenosi
calcifica aortica
- neutropenia, immunodeficienza
- diabete mellito
- abuso di alcolici o di droghe intravenose
- depositi sterili di fibrina e piastrine che si formano nelle sedi di lesione da urto del
flusso
Nella maggior parte dei casi neleziologia delle endocarditi infettive sono implicati i
batteri:
1. Streptococcus aureus:
colpisce valvole danneggiate, cos come valvole sane
responsabile del 10-20% di tutte le endocarditi infettive
2. Streptococcus viridans
o Colpisce valvole danneggiate precedentemente (endocardite
subacuta principalmente)
3. Batteri del gruppo HACEK (Haemophilus, Actinobacillus,
Cardiobacterium, Eikenella, Kingella)
Caratterizzati dallessere commensali del cavo orale.
4. stafilococchi coagulasi negativi
endocardite su protesi valvolari
24
Clinica
Sintomatologia generale:
- febbre
- astenia, perdita di peso, sindrome simil-influenzale
- soffi: nel 90% dei pz
Vegetazioni non infettive
Sono caratterizzate dalla assenza di microrganismi a livello delle lesioni valvolari.
Endocardite trombotica non batterica (ETNB)
Caratterizzata dalla deposizione di piccole (1-5 mm.) masserelle composte da materiale
trombotico (fibrina, piastrina ed altre componenti del sangue), singolarmente o a
gruppi lungo il margine di chiusura dei lembi delle valvole cardiache.
Le vegetazioni dellETNB non contengono microrganismi e non sono accompagnate da
reazione infiammatoria.
Eziologia e patogenesi
LETNB spesso associato a trombosi venosa o ad embolie polmonari e questo
suggerisce che la sua causa sia uno stato di ipercoagulabilit, come pu essere la CID,
con conseguente attivazione sistemica della coagulazione anche a livello del cuore.
Per questo motivo lETNB si riscontra spesso in pz debilitati da:
- neoplasie:
adenomi mucinosi: in relazione con leffetto
procoagulante della mucina circolante
leucemia promielocitica acuta
- stati di sepsi: danneggiamento dellendotelio liberazione fattore tissutale in
grandi quantit ipercoagulabilit
- ustioni estese: danneggiamento dellendotelio liberazione fattore tissutale in
grandi quantit ipercoagulabilit.
Endocardite in corso di lupus eritematoso sistemico (morbo
di Libman-sacks)
In corso di LES a volte si verifica una valvolite mitralica e tricuspidalica con piccole
vegetazioni sterili, detta endocardite di Libman-Sacks.
Morfologia
Lesioni singole o multiple di piccole dimensioni (1-4mm.)
25
Lesioni ste ili ( no microrganismi) a spf granulosa e di colore rosa r
e
Localizzazione: spf ventricolare delle valvole atrioventricolari e corde tendinee.
Pu essere associata unintensa valvulite, con necrosi fibrinoide del tessuto valvolare
adiacente le vegetazioni.
Diagnosi differenzial con endocardite infettiva ed endocardite trombotica non
batterica.
Talora gli esiti cicatriziali e la deformazione valvolare possono creare un problema di
diagnostica differenziale con la cardiopatia reumatica cronica.
Eziologia
Di tipo autoimmunitario.
Complicanze delle valvole artificiali
Tipi di pro esi t
1. protesi meccaniche: sono composte da biomateriali non fisiologici, come palline
ingabbiate in un anello, dischi inclinabili, lembi semicircolari incardinati
nellanello valvolare. Utilizzano sistemi di chiusura rigidi e mobili.
2. bioprotesi: lembi valvolari animali trattati chimicamente ( valvola aortica
porcina, conservata in soluzione diluita di gliceraldeide e poi montata su
supporto meccanico.
Complicanze
Sviluppate dal 60% di portatori di protesi entro 10 anni daalintervento sostitutivo.
i. Complicanze troboembolitiche:
ostruzione trombotica della valvola o tromboembolizzazione a distanza
problema principale delle valvole meccaniche
necessitano di terapia anticoagulante a lungo termine che a sua volta pu
creare problemi emorragici.
ii. Endocardite infettiva:
complicanza infrequente ma grave
infezione a livello dellinterfaccia protesi-tessuto, con formazione di
ascessi anulari ed eventuale perforazione della valvola con reflusso di
sangue. A volte vegetazioni anche sulle cuspidi proteiche.
Provocata principalmente da stafilococchi della cute (S. aureus, S.
epidermidis), streptococchi, funghi.
iii. Deterioramento strutturale:
principale causa di fallimento della bioprotesi: calcificazioni o rottura
responsabili di rigurgito.
Raramente nelle protesi meccaniche
26
Malattie primitive del miocardio
Miocarditi
Sotto questo processo sono raggruppati quei processi infiammatori a carico del
miocardio, che inducono danno ai miociti cardiaci.
Bisogna per sottolineare che la presenza isolata di uno stato infiammatorio non
diagnostica di miocardite: lo stato infiammatorio pu infatti essere la risposta e non la
causa di un danno al miocardio.
Nelle miocarditi lelemento caratteristico che il processo infiammatorio la causa del
danno miocardico.
Il processo infiammatorio che interessa il miocardio nelle miocarditi caratterizzato
da:
- infiltrato infiammatorio interstiziale leucocitario, costituito nelle forme pi comuni
prevalentemente da linfociti
- necrosi focale dei miociti adiacenti alle cellule infiammatorie.
Le miocarditi possono colpire qualsiasi fascia di et, in quanto molto spesso
costituiscono conseguenze di una malattia infettiva che viene a dare complicanze.
Sintomatologia:
La sintomatologia associata alla miocardite estremamente ampia.
Se da un lato la malattia pu essere completamente asintomatica, dallaltro pu
vedere rapida insorgenza di insufficienza cardiaca con conseguente morte improvvisa.
Tra i due estremi si colloca una sintomatologia generalmente caratterizzata da:
febbre
dolore toracico pericardico
segni di scompenso cardiaco: sincopi e palpitazioni
aritmie severe
Le caratteristiche cliniche della miocardite richiedono dunque diagnosi differenziale
con lo scompenso cardiaco di altra natura, dovuto a differenti cause.
Frequentemente la diagnosi differenziale fatta in base a queste caratteristiche
distintive delle miocarditi:
- insorgenza in et giovane
- frequenza di eiezione minore del 4,5%
- esclusione della presenza di malattie coronariche o valvulopatie
Clinicamente le miocarditi possono essere classificate in :
- miocarditi fulminanti
- miocarditi acute
27
- miocarditi subacute
- miocarditi croniche o ricorrenti
Generalmente le miocarditi vanno frequentemente incontro a guarigione completa.
A volte sono presenti esiti cicatriziali, per la formazione di una cicatrice fibrosa che
provoca alterazioni del meccanismo di pompa con rientri del sangue e dunque aritmie.
Se la miocardite va incontro a cronicizzazione si ha un continuo crearsi e ricrearsi di
aree di necrosi che vanno incontro a cicatrizzazione fibrotica.
Viene ad essere cos perso progressivamente tessuto contrattile con conseguente
ipertrofia compensatoria delle aree non fibrotiche.
Questa reazione ipertrofica pu comportare un insufficiente nutrimento della parete
cardiaca, ispessita con conseguente generazione dello scompenso cardiaco.
Il sovraccarico cardiaco non pi compensato genera dilatazione cardiaca, con
assottigliamento delle pareti e passaggio ad una cardiomiopatia dilatativa
inequivocabile.
Eziologia
Le miocarditi possono essere suddivise in:
Miocarditi ad eziologia nota:
infettive:
da batteri (Staphylococcus aureus, corynebacterium diphtariae, neisseriae
meningitidis, borrelia9
virali: sono le pi frequenti (coxsackievirus, echovirus, adenovirus,
citomegalovirus, HIV)
da parassiti (toxoplasma, tripanosoma malattia di Chagas-)
da funghi (candida)
tossiche:
da increzione di catecolamine
da antracicline
sali di litio: nei pz psicotici
interferone
cocaina nei tossico dipendenti
da ipersensibilit:
a farmaci: penicilline, sulfamidici, streptomicina, isoniazide, tetracicline
da agenti fisici
ipotermia
radiazioni
colpo di calore
28
Miocarditi idiomatiche:
Hanno causa sconosciuta e dunque sono identificate in base al tipo di infiltrato ad esse
associato.
Da sottolineare il fatto che anche le miocarditi ad eziologia nota danno infiltrato
differente a seconda dellagente eziologico.
infiltrato linfocitario:
infiltrato neutrofilo: importanti effetti tossici dei polimorfonucleati sul
miocardio
infiltrato eosinofilo
infiltrato a cellule giganti:
di origine miogena
di origine macrofagica
Diagnosi
La diagnosi di miocardite attualmente si basa sui criteri di Dallas, in accordo ai quali
la miocardite attiva viene definita come infiltrazione di cellule infiammatorie del
miocardio con associata necrosi e degenerazione dei miociti adiacenti, senza che si
realizzi il quadro tipico della lesione ischemica da malattia coronaria.
Secondo i criteri di Dallas linfiltrato deve trovarsi allinterno delle cellule contrattili.
La conseguenza la presenza di vacuolizzazione dei miociti, presenza di margini
cellulari irregolari, nuclei presenti.
Vi inoltre necrosi per disintegrazione dei miociti, con presenza di linfociti e macrofagi
dentro le cellule miocardiche.
La diagnosi viene sempre fatta mediante biopsia cardiaca.
Alla prima biopsia a seconda che la miocardite sviluppi o meno i criteri di Dallas si
pu avere:
- Certezza di miocardite (con o senza fibrosi)
- Miocardite border-line: vede assenza di degenerazione dei miociti, con
infiltrato infiammatorio moderato con linfociti scarsi. In questo caso pu essere
necessario ulteriore prelievo bioptico
- No miocardite
Alle successive biopsia si pu avere un quadro di:
- Miocardite persistente: quadro simile alla prima biopsia con o senza fibrosi
- Miocardite in via di risoluzione: con o senza fibrosi.
- Miocardite guarita: con o senza fibrosi.
29
Tutti i quadri di miocardite possono essere accompagnati da fibrosi, dunque presenza
di tessuto di connettivo che viene gradualmente a sostituire il tessuto necrotizzato,
formando focolai fibrotici confluenti.
Secondo i criteri di Dallas nel quadro istologico della miocardite abbiamo:
-
Infiltrato infiammatorio
Composizione prevalente:
linfociti ( prevalentemente linfociti T)
granulociti neutrofili (PMN)
granulociti eosinofili e plasmacellule e macrofagi.
Intensit
Lieve
Moderato
Severo
Estensione
Focale
Confluente
Diffuso
Si pu avere una progressione attraverso i tre stadi: inizialmente si hanno piccoli
infiltrati focali che confluiscono luno con laltro dando un quadro di infiltrato diffuso.
La diagnosi differenziale con un infiltrato di tipo ischemico pu essere fatta sulla base
di due caratteristiche istologiche delle miocarditi:
- presenza di depositi di emosiderina
- i miociti subendocardici, dunque quelli che sono rivolti verso la cavit, sono
risparmiati.
Necrosi
a singoli elementi miocitari
a gruppi
Fibrosi
Dipende dalla durata della malattia. Pu essere:
endocardica
sostitutiva
interstiziale
30
Grading delle modificazioni ultrastrutturali
0 Ultrastruttura normale
1 Alterazione di miociti isolati < 5%
Dilatazione reticolo sarcoplasmatico ed iniziale lisi miofibrillare
1,5 Alterazione di miociti isolati 6-15%
Dilatazione reticolo sarcoplasmatico ed iniziale lisi miofibrillare
2 Alterazione di aggregati di miociti 6-15%
Lisi miofibrillare, vacuolizzazione
2,5 Alterazione di numerosi miociti 26-35%
Lisi miofibrillare, vacuolizzazione
Necessaria dose aggiuntiva di farmco
3 Alterazione di miociti >35%
Danno severo
No dose aggiuntiva di farmaco
Diagnosi differenziale in associazione al tipo di infiltrato infiammatorio
Infiltrato linfocitario
Miocardite idiopatica ad infiltrato linfocitario
Miocardite provocata da virus
Miocardite provocata da sarcoidosi: si tratta di un granuloma del muscolo
cardiaco
Miocardite tossica, da svariati tipi di farmaci
Linfoma con metastasi al miocardio
Infiltrato neutrofilo
Miocardite idiopatica ad infiltrato neutrofilo
Miocardite provocata da batteri
Miocardite ischemica
Miocardite provocata da virus nella sua fase iniziale. Inizialmente la
miocardite virale vede un infiltrato formato da neutrofili e soltanto in un
secondo momento subentrano i linfociti.
Infiltrato eosinofilo
Miocardite idiopatica ad infiltrato eosinofilo
Miocardite da parassiti
Sindrome ipereosinofila che colpisce pi organi compreso il miocardio
Miocardite da ipersensibilit
Miocardite a cellule giganti
Miocardite idiopatica a cellule giganti
Miocardite da funghi
Malattia reumatica
Tubercolosi
Sarcoidosi: in questo caso le cellule giganti si ritrovano in associazione ai linfociti
31
Trattamento e prognosi
La miocardite si tratta pricipalmente con agenti immunosoppressivi essendo la sua
eziologia legata allinfiammazione.
A volte una miocardite fulminante pu presentare prognosi migliore a lungo termine e
migliore risposta ai farmaci rispetto ad una miocardite acuta che frequentemente
evolve in cardiomiopatia dilatativa.
Miocarditi virali
Le infezioni virali sono fra le cause pi comuni di miocardite, in particolare negli Stati
Uniti.
I maggiori virus responsabili sono:
- Coxsackievirus A e B ed altri enterovirus
- Adenovirus
- Herpes Simplex Virus
- Citomegalovirus (CMV) che provoca uno stato di immunosoppressione e meggiore
sensibilit ad ulteriori infezioni virali
- HIV che provoca uno stato di immunosoppressione e maggiore sensibilit ad
ulteriori infezioni virali
- Virus influenzali
- Agenti virali di malattie esantematiche dellinfanzia
Il meccanismo mediante il quale i virus provocano la miocardite non ancora chiaro.
Le ipotesi sono due:
- risposta auto-immune virus indotta contro le cellule miocardiche
- infezione miocardica diretta virale: nel modello murino un trattamento con
interferon inibisce la miocardite, dunque il virus medesimo, infettando le cellule
miocardiche a provocare linfiltrato infiammatorio.
Miocardite a cellule giganti
Pu essere:
- idiopatica (miocardite isolata di Fredor)
- secondaria a malattie sistemiche a patogenesi auto immune
Et: colpisce prevalentemente giovani o adulti (et media: 43 anni).
Prognosi: rapidamente fatale.
Istopatologia: esteso infiltrato infiammatorio cronico (cellule giganti multinucleate
frammiste a linfociti citotossici, eosinofili, plasmacellule, macrofagi), associato a
necrosi frequentemente estese.
Le cellule giganti si trovano nelle zone marginali della necrosi e possono avere origine:
- dai macrofagi: cellule giganti istiocitarie.
32
- dai miociti: cellule giganti miogene
Bisogna fare diagnosi differenziale con:
- malattia reumatica: nella quale le cellule giganti, o di Aschoff, si ritrovano al centro
del focolaio e vi sarcoidosi, fibrosi, presenza di granulomi e mancanza di eosinofili
- granuloma da funghi
- granuloma da micobatteri
- granuloma da corpo estraneo
Miocardite tossica da catecolamine
Le catecolamine hanno un effetto tossico diretto nei confronti dei cardiomiociti.
Questo tipo di miocardite riscontrabile nei pazienti affetti da feocromocitoma, a
causa delle catecolamine secrete dalla neoplasia e nei tossicodipendenti che fanno uso
di cocaina, che induce ipersecrezione di catecolamine.
Miocardite tossica da antracicline
Gli agenti chemioterapici della famiglia delle antracicline sono causa riconosciuta di
danno tossico, potenzialmente causa di cardiomiopatia dilatativa.
Leffetto tossico dose-dipendente ed attribuito soprattutto alla perossidazione
lipidica del sarcolemma miocitario, poich le antracicline, come farmaci anti-
neoplastici provocano la liberazione di radicali liberi.
Questo tipo di miocardite colpisce prevalentemente soggetti di et maggiore di 70 anni,
che siano stati sottoposti a cicli multipli di chemioterapia.
necessaria la diagnosi differenziale con la controparte da ipersensibilit, che si pu
fare per la frequente presenza di vasculite necrotizzante in questo tipo di miocardite.
Un altro farmaco chemioterapico dotato di cardiotossicit la ciclofosfamide che non
produce per tossicit diretta ai miociti, bens ha un effetto tossico sul sistema
vascolare, determinando emorragia miocardica.
Miocardite da ipersensibilit
correlata a reazioni allergiche nei confronti di un particolare farmaco, dunque
dose-indipendente e caratterizzata da alta percentuale di eosinofili nellinfiltrato
infiammatorio.
Nellinfiltrato infiammatorio vi possono anche essere granulomi
33
Miocardite eosinofila idiopatica
Frequentemente conseguenza dellipereosinofilia idiopatica (malattia di Loeffler), che
provoca ipereosinofilia periferica in diversi distretti dellorganismo.
Da un punto di vista istopatologico, vi necrosi tossica dei miociti, provocata da
proteine contenute nei granuli liberati dagli eosinofili, che agiscono su sarcolemma e
mitocondri.
Vi la presenza di trombi eosinofili delle arterie coronariche miocardiche.
Miocardite neutrofila idiopatica
Pu rappresentare la fase inizialae di una miocardite massiva idiopatica, dato che i
granuli allinterno dei neutrofili inducono un danno molto abbondante oltre la normale
necrosi, che richiama molte cellule dellinfiltrato infiammatorio.
necessaria la diagnosi differenziale con la malattia reumatica nella sua variante a
decorso fulminante.
Miocardiopatie
Nella maggior parte dei casi le disfunzioni del miocardio insorgono secondariamente
ad altre patologie cardiache.
Con il termine cardiomiopatia si intende invece una cardiopatia derivante da
unalterazione primitiva del miocardio, dunque una malattia che coinvolge
primitivamente il miocardio.
Le cardiomiopatie si distinguono in tre profili clinici funzionali e patologici:
cardiomiopatia dilatativa
cardiomiopatia ipertrofica
cardiomiopatia restrittiva
La diagnosi delle cardiomiopatie viene fatta attraverso le biopsie endomiocardiche: inserimento
transvenoso di uno strumento detto biotomo, sino al cuore destro e prelievo con le pinze di piccoli
frammenti di miocardio settale, che dunque vengono analizzati dal patologo.
Cardiomiopatia dilatativa (CMPD)
la forma pi comune di cardiomiopatia costituendo il 90% dei casi.
34
caratterizzata da progressiva dilatazione cardiaca e disfunzione della contrattilit
sistolica, solitamente associata ad ipertrofia.
Si pu verificare ad ogni et, ma colpisce pi frequentemente soggetti tra i 20 ed i 50
anni.
Morfologia
Cuore voluminoso (ampia dilatazione), con peso aumentato di 2-3 volte (ipertrofia e
dilatazione), flaccido (disfunzione della contrattilit sistolica).
Poich lipertrofia si associa alla dilatazione lo spessore delle pareti pu essere
maggiore, uguale o minore.
I trombi murali sono frequenti e possono dare origine a embolia.
Le arterie coronarie sono generalmente libere da stenosi significative.
Eziologia
Miocarditi: dimostrata una possibile progressione da miocardite a CMPD.
Frequentemente nei reperti bioptici delle cardiomiopatie dilatative sono stati
trovati reperti bioptici di coksackievirus B o di altri enterovirus.
Alcool: labuso di alcool fortemente associato a CMPD (anamnesi di etilismo
nel 10-20% dei pz). I metaboliti dellalcool hanno effetto tossico sul miocardio ed
inoltre labuso di alcool pu causare uno squilibrio nutrizionale a cui consegue
cardiomiopatia dilatativa.
Altre sostanze tossiche: per esempio agenti chemioterapici, come ladriamicina
che contribuiscono alla patogenesi delle miocarditi e dunque della CMPD.
Peripartum: frequentemente si verificano cardiomiopatie nelle fasi tardive della
gravidanza o dopo settimane o mesi dal parto, a causa di un insieme di
condizioni favorenti come ipertensione, sovraccarico di volume, carenze
nutrizionali, disordini metabolici o eventi immunologici non ancora chiariti
molto bene.
Fattori genetici: costituiscono il 25-35% dei casi. Si tratta nella maggior parte
dei casi di patologie a trasmissione autosomica dominante e di casi pi rari di
forme X-linked. Solitamente le alterazioni geniche sono correlate a difetti nelle
proteine del citoscheletro. La CMPD x-linked la forma meglio caratterizzata
ed associata al gene che codifica per la distrofina, colpendo tipicamente gli
adolescenti.
Idiopatica: causa sconosciuta.
Clinica
insufficienza cardiaca congestizia a lento sviluppo inizialmente compensata ma
comunque con sintomi evidenti: respiro corto, facile affaticabilit, capacit fisica
ridotta.
Passaggio in tempi brevi ad uno stato di scompenso.
35
Riduzione della frazione di eiezione a causa della ridotta contrattilit sistolica fino
ad una frazione di eiezione < 25% (dove quella normale del 50-60%)
A volte presenza di insufficienza mitralica secondaria, aritmie ed embolie a
partenza dai trombi intracardiaci.
Cardiomiopatia ipertrofica (CMPI)
Presenta ipertrofia miocardica, con conseguenti alterazioni del riempimento diastolico
e circa in un terzo dei casi ostruzione intermittente del tratto di efflusso ventricolare
sinistro.
La disfunzione diastolica, mentre solitamente la funzione sistolica conservata
Richiede DD con amiloidosi e cardiopatia ipertensiva.
Morfologia
Cuore con ipertrofia massiva, ma non dilatato.
Ipertrofia settale asimmetrica: inspessimento del setto interventricolare
sproporzionato rispetto a quello della parete ventricolare sx libera, localizzato
prevalentemente nella regione sub-aortica.
Sezione trasversa: ventricolo sx che non ha pi la normale forma globosa, ma assume
forma a banana per la protrusione del setto interventricolare inspessito nel lume
ventricolare.
Frequenti inspessimenti dellendocardio o vere e proprie placche fibrose nel tratto di
efflusso del ventricolo sx, con associato inspessimento del lembo anteriore della
mitrale: ci dovuto al frequente contatto, durante la sistole del lembo mitralico
anteriore con il setto ostruzione del tratto di efflusso del ventricolo in un terzo dei
casi.
Eziologia
La CMPI sempre dovuta ad una mutazione di uno dei qualsiasi geni che codificano
per le proteine strutturali dei sarcomeri, dunque sempre una malattia genetica
Clinica
riduzione del volume cavitario
scarsa compliance parietale
diminuzione della gittata sistolica dovuta allalterato riempimento diastolico, per la
massiccia ipertrofia ventricolare sx
ostruzione funzionale del tratto di efflusso ventricolare sx nel 25% dei casi aspro
soffio sistolico da eiezione allauscultazione.
Aumento secondario della pressione venosa polmonare (per la diminuzione della
gittata sistolica sx) con consgeuente dispnea da sforzo.
Ischemia miocardica focale, dovuta a massiccia ipertrofia (aumentate richieste),
aumento della pressione nella camera ventricolare sx, possibili anomalie a carico
delle arterie intraluminali. Conseguente dolore anginoso.
Complicanze: fibrillazione atriale, trombi murali con embolizzazione, insufficienza
cardiaca intrattabile, morte improvvisa.
36
Terapia
Terapia medica che facilita il rilasciamento ventricolare.
Resezione chirurgica riduttiva della massa muscolare del setto ventricolare, effettuata
solo in alcuni casi.
Cardiomiopatia restrittiva
Riduzione primitiva della compliance ventricolare con alterato riempimento
ventricolare nella diastole, mentre la funzione sistolica generalmente mantenuta.
Morfologia
I ventricoli hanno dimensioni normali, le cavit non sono dilatate ed il miocardio ha
maggiore consistenza.
Frequentemente dilatazione di entrambi gli atri.
Eziologia
Pu essere idiopatica (cause sconosciute) o presentarsi in associazione con altre
malattie che colpiscono il miocardio.
37
Scompenso cardiaco
un risultato finale estremamente comune di molte patologie cardiache.
Scompenso cardiaco o insufficienza cardiaca congestizia:
- situazione di sovraccarico cardiaco non compensato.
- il cuore non pi in grado di pompare sangue in quantit commisurata alle
richieste metaboliche dei tessuti periferici o lo pu fare solo con elevate pressioni di
riempimento.
Il cuore possiede diversi meccanismi fisiologici di mantenimento della pressione
arteriosa e della perfusione periferica in condizioni di sovraccarico:
- meccanismo di Frank-Starling
- aumento della massa muscolare cardiaca
- attivazione di sistemi neurormonali (rilascio di noradrenalina, attivazione sistema
renina-angiotensina, rilascio del peptide natriuretico atriale).
Tuttavia se il cuore sottoposto troppo a lungo o in modo troppo intenso ad un
sovraccarico funzionale questi meccanismi di compensazione possono non bastare.
Si pu avere dunque
un progressivo deterioramento della funzione di contrazione cardiaca
disfunzione sistolica
unincapacit crescente delle camere cardiache ad espandersi e riempirsi
sufficientemente nella diastole disfunzione diastolica
a questo punto che soppraggiunge una situazione di scompenso cardiaco.
Qualunque ne sia la causa lo scompenso cardiaco viene per ad essere cartterizzato da:
diminuita gittata cardiaca (insufficienza anterograda) o da;
ristagno di sangue nella circolazione venosa (insufficienza retrograda) o da;
entrambe le situazioni
Dunque lo scompenso cardiaco una sindrome clinica che viene ad avere i suoi
maggiori risvolti soprattutto al di fuori del sistema cardiovascolare, sia in senso
anterogrado (scarsa perfusione dorgan), sia in senso retrogrado (dispnea, edema
periferico).
Avviene in molte situazioni patologiche che lo scompenso cardiaco sia preceduto da
ipertrofia cardiaca, essendo questa una delle risposte compensatorie principe del cuore
in una situazione di sovraccarico cardiaco.
Ipertrofia cardiaca: progressione fino allo scompenso
Il miocita cardiaco una cellula a differenziazione terminale, che non si pu dividere.
38
Di conseguenza in risposta ad un aumento del carico meccanico sul cuore i miociti non
possono rispondere con iperplasia, ma solo con ipertrofia, dunque aumento delle
dimensioni cellulari.
Grado dellipertrofia
Viene a variare in base alle patologie che sono alla base dellipertrofia medesima.
Il peso normale del cuore di 250-300g. nella donna, 300-350g. nelluomo.
Grado di ipertrofia (peso del cuore) Patologie alla base dellipertrofia
350-600g (fino a 2 volte il peso del cuore) Ipertensione polmonare
Cardiopatia ischemica
400-800g. (fino a 2-3 volte il peso del
cuore)
Ipertensione sistemica
Stenosi aortica
Insufficienza mitralica
Cardiomiopatia dilatativa
600-100g. (3 o pi volte il peso del cuore) Insufficienza aortica
Cardiomiopatia ipertrofica
Tipo di ipe trofia r
Viene a riflettere la natura dello stimolo.
1. Stimolo pressorio:
Se lo stimolo un sovraccarico di pressione si ha sviluppo dellipertrofia da
sovraccarico pressorio o ipertrofia concentrica del ventricolo sinistro.
Questa caratterizzata da aumento della superficie trasversale dei miociti, senza
aumento della lunghezza cellulare.
Dunque si ha aumento dello spessore parietale del ventricolo sx che pu anche
comportare riduzione del diametro della cavit
2. Stimolo volumetrico:
Se lo stimolo un sovraccarico di volume si ha sviluppo dellipertrofia da sovraccarico
di volume.
Questa caratterizzata da un aumento della lunghezza dei miociti per deposizione di
nuovi sarcomeri, senza aumento delle dimensioni degli stessi.
Dunque si ha aumento del diametro del ventricolo sx: lo spessore parietale sarebbe
aumentato in proporzione al diametro della camera, ma data la dilatazione esso pu
risultare normale o inferiore alla norma.
Alterazioni che accompagnano lipertrofia
Le alterazioni che accompagnano lipertrofia sono le seguenti:
1. Alterazioni trascrizionali:
aumento della sintesi proteica con produzione di proteine anomale
attivazione dei geni precoci
39
attivazione del programma genico tipico dello sviluppo cardiaco fetale
2. Alterazioni morfologiche: sono dovuta allaumento delle dimensioni dei miociti che
provoca
Riduzione della densit capillare
Aumento della distanza intercapillare
Deposito di tessuto fibroso
Una dunque ridotta perfusione cardiaca si accompagna ad un maggiore consumo di
ossigeno del cuore dovuto a:
- aumento della massa muscolare
- aumento della tensione parietale
- aumento della frequenza cardiaca
- aumento della contrattilit
Lipertrofia cardiaca dunque viene a costituire un meccanismo di adattamento
fisiologico al limite con una situazione potenzialmente patologica.
La formazione di nuovi sarcomeri o laumento delle dimensioni dei miociti rientrano
nelladattamento fisiologico.
Il ridotto apporto capillari-miociti, laumento del tessuto fibroso e le sintesi proteiche
alterate sono meccanismi potenzialmente dannosi.
Lipertrofia protratta dunque pu evolvere nello scompenso cardiaco, perch vi sono
una serie di alterazioni che inizialmente mediano laumento della funzione, ma che
possono col tempo contribuire allo scompenso.
Si possono verificare indipendentemente uno scompenso destro ed uno sinistro anche
se generalmente, poich il sistema cardiovascolare un circuito chiuso, linsufficienza
di una sezione (in particolare sx) comporta eccessivo carico sullaltra e conseguente
scompenso cardiaco globale.
Scompenso cardiaco sinistro
Cause
Cardiopatia ischemica
Ipertensione
Valvulopatie aortiche e mitraliche
Miocardiopatie non ischemiche
Effetti
Derivano principalmente da:
progressivo ristagno di sangue nel circolo polmonare ( il cuore sx non pi in grado
di raccogliere sangue dal circolo polmonare)
riduzione del flusso e della pressione sanguigna sistemica in periferia.
40
Polmone
a. patogenesi:
i. progressivo aumento della pressione nelle vene polmonari
ii. trasmissione dellaumento pressorio per via retrograda a capillari ed arterie
iii. congestione polmonare ed edema
b. sintomatologia:
i. dispnea: esagerazione del noramle affanno dopo lo sforzo. il primo sintomo a
comparire
ii. ortopnea: dispnea che insorge quando ci si sdraia e trova giovamento da sdraiati o
da seduti. Insorge quando vi peggioramento ulteriore.
iii. dispnea parossistica notturna: estensione dellortopnea che consiste in attacchi di
dispnea notturna che arrivano quasi al soffocamento.
La tosse frequente sintomo
Reni
Patogenesi:
riduzione della gittata cardiaca
riduzione della perfusione renale
attivazione sistema renina-angiotensina-aldosterone
ritenzione di sale ed acqua
espansione del volume ematico
peggioramento delledema polmonare
Questa reazione controbilanciata dal rilascio di ANP
Cervello
Solo nello scompenso molto avanzato lipossia cerebrale pu causare encefalopatia
ipossica
Scompenso cardiaco destro
Cause
Generalmente secondario ad uno scompenso cardiaco sinistro per aumento del carico
sulle sezioni destre del cuore ad esso conseguente.
Primitivo tipicamente nel caso di ipertensione polmonare cronica per sovraccarico
della pressione sul cuore destro dovuto ad aumento delle resistenze polmonari.
Effetti
Generalmente vi una congestione polmonare minima, mentre la congestione
marcata a livello di altri tessuti.
Fegato
i. Aumento edematoso di dimensioni e peso eptomegalia congestizia
ii. Necrosi delle regioni pi distanti dalla vena centrolobulare che appaiono
giallastre.
iii. Nei casi pi gravi necrosi centrolobulare
41
Sistema Portale
Vi elevata pressione nella vena porta e nei suoi rami tributari che comporta:
i. aumento edematoso di dimensioni e peso della milzasplenomegalia cronica
ii. edema cronico della parete intestinale, che pu influenzare lassorbimento di
nutrienti
iii. accumulo di trasudato nella cavit peritoneale
Reni
La congestione dei reni marcata
Cervello
Vedi scompenso cardiaco sx
Spazi pleurici e pericardici
Si pu avere accumulo di liquido nello spazio pleurico ( in maggiore misura in quello
destro) e nello spazio pericardico (effusioni).
Tessuti sottocutanei
Tipici edema delle porzioni declivi del corpo, soprattutto delle caviglie e degli spazi
pre-tibiali.
Si pu avere poi edema massivo e generalizzato del tessuto sottocutaneo (anasarca).
42
Patologia del pericardio
Generalmente le patologie del pericardio sono quasi sempre secondarie ad altre
malattie. La malattia isolata del pericardio rara.
Emopericardio
Pericardio normale: nel sacco pericardico normalmente vi sono circa 30-50 ml. di un
liquido limpido, trasparente, color paglierino.
In alcune situazione si ha versamento pericardico (accumulo di liquido nel sacco
pericardico):
- di sangue emopericardio
- di pus pericardite purulenta
Le conseguenze dellaccumulo di liquido dipendono:
- capacit di dilatazione del pericardio parietale
- velocit di accumulo del liquido
- quantit di liquido che si accumula
Se il liquido si accumula lentamente e non supera i 500ml. si ha solo ingrandimento
globoide dellombra cardiaca.
Se il liquido si accumula velocemente (emopericardio dovuto a rottura), anche un
versamento del volume di 200-300ml. pu determinare compressione sulle pareti degli
atri e dei ventricoli o delle vene cave, con conseguente ostacolo al riempimento
cardiaco tamponamento cardiaco potenzialmente fatale.
Pericardite
Infiammazione del pericardio.
Generalmente secondaria: solo raramente primitiva e generalmente di origine virale.
Cause di pericardite:
Agenti infettivi: virus, batteri piogeni, tubercolosi, funghi.
Cause immunomediate: febbre reumatica, lupus eritematoso sitemico, scerodermia,
post-infarto miocardico (sd di Dressler)
Altri: infarto miocardico, uremia (insufficienza renale che provoca pericardite), post
intervento cardiochirurgico, neoplasia, trauma.
Pericarditi acute
Pericardite sierosa
Caratteristica dei processi infiammatori , ma non infettivi.
Il liquido contiene rari leucociti e macrofagi, ha un volume modesto (50-200ml.) e si
accumula lentamente.
Non vi quasi mai organizzazione dellessudato con formazione di aderenzee fibrose.
43
Cause:
- malattia reumatica, LES, sclerodermia
- insufficienza cardiaca congestizia
- ipoalbulinemia
- uremia
Pericardite fibrinosa e siero-fibrinosa
Sono i tipi pi frequenti di pericardite.
Il liquido sieroso e misto ad un essudato fibrinoso.
La fibrina pu essere digerita con risoluzione dellessudato oppure andare incontro ad
organizzazione.
Il segno pi caratteristico di pericardite fibrinosa la comparsa di rumore di
sfregamento pericardico, che per pu essere eventualmente mascherato da una
raccolta sierosa che separi i due foglietti pericardici.
Cause:
- malattia reumatica, LES, post-infarto miocardico
- infarto miocardico acuto
- uremia
- traumi
Pericardite purulenta
Caratteristica dei processi infiammatori infettivi, acuti.
Lessudato pu essere liquido o formato da un pus cremoso, con volume che pu
raggiungere i 500ml.
Il pericardio sieroso rossastro, granuloso e ricoperto dallessudato.
Cause:
- presenza di microrganismi infettivi nel cavo pericardico (batteri, funghi, virus) che
possono provenire anche da focolai infiammatori contigui
Pericardite siero-emorragiche
Essudato composto da sangue misto a fibrina o a pus
Cause:
- trauma
- neoplasia maligna che si estende al cavo pericardico.
Pericardite caseosa
Dovuta allinfezione tubercolare, che raggiunge il pericardio per diffusine diretta da
focolai tubercolari nei linfonodi tracheo-bronchiali.
Chilopericardite
Dovuta ad ostruzione linfatica mediastinica
44
Pericarditi croniche
In alcuni casi il processo di organizzazione della fibrina pu portare a formazione di
- placche di inspessimento fibroso delle sierose
- formazione di aderenze
- completa obliterazione del sacco pericardico con adesione fra il foglietto parietale e
quello viscerale pericardite adesiva
Mediastinopericardite adesiva
Pu fare seguito a pericardite purulenta o caseosa.
Il sacco pericardico obliterato e presenta aderenze con le strutture circostanti.
Il cuore sottoposto ad un notevole incremento di lavoro poich per contrarsi deve
vincere le resistenze offerte dal pericardio parietale e la trazione esercitata dalle
strutture circostanti.
Laumento del carico di lavoro comporta ipertrofia e dilatazione cardiaca che possono
essere massive e mimare una cardiomiopatia dilatativa
Pericardite costrittiva
Il cuore intrappolato in una denso strato cicatriziale del pericardio, fibroso, o
fibrocalcifico, dello spessore di 0,5-1 cm., che in alcuni casi pu divenire un calco
calcifico (concretio cordis).
Il cuore dunque limitao nellespansione diastolica e la sua gittata cardiaca
severamente ridotta in modo da simulare una cardiomiopatia restrittiva.
La principale terapia la pericardiectomia, cio la rimozione chirurgica della corazza
di tessuto fibroso.
45
Il polmone
Anatomia normale
Il polmone un organo formato da:
- 3 lobi a dx
- 2 lobi a sx
Sebbene la lingula presente a sx sia lequivalente del lobo medio a dx, il polmone
destro ha volume < rispetto al polmone sinistro.
Allo stesso modo il bronco principale dx pi diretto ed allineato con la trachea
rispetto al bronco sx (tendenza del materiale estraneo eventualmente aspirata ad
entrare nel polmone dx).
Allinterno del polmone si distribuiscono le vie aeree.
Si ha ramificazione e divisione dicotomica dei bronchi principali, a formare bronchi che
a loro volta si suddividono in modo dicotomico, dando luogo ad unestesa
arborizzazione. Il diametro e la lunghezza dei bronchi si riducono progressivamente ad
ogni successiva divisione, assieme al supporto cartilagineo, che scompare del tutto nei
condotti di circa 1mm.
Tutti i condotti aerei successivi sono detti bronchioli terminali e sono dunque
caratterizzati da:
- mancanza di scheletro cartilagineo
- piccolo diametro
- ghiandole sottomucose nello spessore delle pareti
- sono immersi nella matrice connettivale del polmone e dunque il loro diametro
dipende strettamente dal volume polmonare.
Dai bronchioli terminali hanno origine i bronchioli respiratori, cos chiamati perch
partecipano agli scambi gassosi; infatti nelle loro pareti si cominciano ad aprire i primi
alveoli, il cui numero va aumentando con le successive divisioni, fino a che le pareti dei
bronchioli sono quasi del tutto occupate dalle aperture degli alveoli.
Queste branche terminali sono dette dotti alveolari e proseguono in un sacco alveolare
a fondo cieco, la cui parete costituita da una successione di alveoli.
Si chiama acino polmonare la parte terminale del polmone (bronchioli respiratori-
sacco alveolare), che coinvolta attivamente negli scambi gassosi.
detto lobulo un gruppo di 3-5 bronchioli terminali ognuno con il rispettivo acino.
La ramificazione delle vie aeree accompagnata dalla doppia vascolarizzazione
arteriosa del polmone:
1. arterie polmonari
2. arterie bronchiali
Le vie aeree sono inoltre dotate di:
- nervi motori: il muscolo liscio innervato da fibre del nervo vago (divisione
parasimpatica)
46
- nervi sensoriali: nelle giunzioni intercellulari e sotto le cellule epiteliali e sono
sensibili allo stiramento ed alle sostanze irritanti.
Mucosa bronchiale:
- epitelio colonnare ciliato pseudostratificato
- cellule caliciformi muco-secernenti nelle vie aeree con scheletro cartilagineo
- cellule neuroendocrine contenenti granuli neurosecretori (serotonina, calcitonina)
Pareti alveolari (versante ematicoversante gassoso)
- endotelio capillare
- membrana basale e circostante tessuto interstiziale: nelle parti pi sottili le mbr
basali dellendotelio e dellepitelio alveolare sono fuse, mentre nelle porzioni pi
spesse sono separate dallinterstizio polmonare
- epitelio alveolare: formato da
Pneumociti di tipo I: appiattiti e sottili, funzionali allo scambio gassoso,
ricoprono il 95% della spf delle pareti alveolari.
Pneumociti di tipo II: fonte del surfactante polmonare e principali cellule
coinvolte nella riparazione dellepitelio alveolare dopo eventule distruzione.
- macrofagi alveolari: adesi alle cellule epiteliali, o liberi nel lume alveolare
Pori di Kohn: perforazioni della parete dei diversi alveoli che permettono il passaggio
di batteri ed essudato tra alveoli adiacenti.
1. Danno polmonare acuto
In seguito a danno polmonare acuto possiamo avere uno spettro di manifestazioni
cliniche, a partire dalledema e congestione, che dunque possono progredire fino alla
sindrome da distress respiratorio acuto e fino alla polmonite acuta interstiziale.
1a. Edema polmonare
1) edema polmonare emodinamico o cardiogeno: dovuto a scompenso, insufficienza
cardiaca sx, o qualsiasi causa che comporti aumento della pressione idrostatica del
circolo polmonare con conseguente stravaso di essudato, che avviene prima nelle
regioni basali, dove la pressione idrostatica maggiore.
Macroscopicamente: polmoni pesanti ed imbibiti.
Istologicamente:
- capillari alveolari ingorgati
- lume alveolari con eventuali microemorragie e macrofagi ripieni di emosiderina
- fibrosi ed inspessimento delle pareti alveolari in caso di congestione cronica.
2) edema da leisoni microvascolari: lesioni dei capillari dei setti alveolari che
comportano aumento della permeabilit capillare, con consueguente fuoriuscita di
liquidi e proteine nello spazio interstiziale e dunque nello spazio alveolare. Pu
progredire nel caso di forme generalizzate in sindrome da distress respiratorio
acuto.
47
1b. Sindrome da distress respi atorio acuto (ARDS) r
Sindrome clinica caratterizzata da danno diffuso dei capillari alveolari.
Cause
Le principali cause, di cui lARDS rappresenta una complicanza, sono:
1. sepsi
2. infezioni polmonari diffuse
3. aspirazione di contenuto gastrico
4. trauma meccanico
Patogenesi
Stimoli infiammatori infettivi o non infettivi
Entro 30 minuti: attivazione della risposta infiammmatoria acuta:
produzione di citochine ad azione chemiotattica (IL-8)
produzione di citochine flogistiche (IL-1 e TNF)
sequestro di neutrofili a livello del microcircolo
polmonaremarginazionefuoriuscita nello spazio alveolareattivazione
liberazione di prodotti da parte dei neutrofili che causano:
danno alla mbr dei capillari alveolari
permeabilit vascolare
essudazione intra-alveolare
perdita della capacit di essudazione
diffusa distruzione tissutale
alterazioni della distribuzione del sulfactante
Dunque vi presenza di uno stimolo che induce danno iniziale che viene amntenuto
dalla risposta infiammatoria dellorganismo.
Lessudato e la diffusa distruzione tissutale in questo caso non sono facilmente
risolvibili ed il risultato unorganizzazione con cicatrizzazione, che conduce a
pneumopatia cronica.
Evoluzione clinica
Di solito i pz che sviluppano ARDS sono gi ricoverati per una delle condizioni
elencate prima.
Sintomi precoci: dispnea e tachipnea (difficolt negli scambi gassosi)
Sintomi tardivi: cianosi, ipossiemia ingravescente, refrattaria allossigenoterapia,
insufficienza respiratoria, che pu evolvere in insufficienza multiorgano (MOFS
Multiple Organ Failure Sindrome).
Radiografia: comparsa tardiva di infiltrazione radiografica diffusa.
Istologia: danno alveolare diffuso.
48
Morfologia
1. fase acuta.
- polmoni pesanti, rossi, imbibiti
- edema interstiziale ed intra-alveolaredepositi di fibrinaformazione di
membrane ialine (essudato ricco in fibrina, con residui delle cell epiteliali
necrotiche) nelle pareti alveolari.
2. fase organizzativa
- proliferazione pneumociti II per rigenerare il rivestimento alveolare
- organizzazione dellessudato fibrinosofibrosi alveolareinspessimento dei setti
alveolari.
1c. Polmonite acuta interstiziale
Lesione acuta del parenchima polmonare con decorso acuto e rapidamente progressivo,
simile a quello dellARDS.
Leziologia solitamente sconosciuta, ma spesso segue ad uninfezione delle vie
respiratorie superiori (rinite, faringite, laringite) di durata < alle 3 w.
I pz presentano un quadro di insufficienza respiratoria acuta.
Mortalit del 50% con la maggior parte dei decessi entro 1-2 mesi.
2. Malattia polmonare ostruttiva
caratterizzata da un aumento della resistenza al flusso, dovuto alla parziale o totale
ostruzione che si pu verificare ad ogni livello.
I test di funzionalit polmonare manifestano una riduzione del picco massimo di flusso
durante unespirazione forzata, misurata con il volume espiratorio forzato in 1 sec.
Le malattie ostruttive pi diffuse sono:
1. broncopneumopatia cronica ostruttiva (BPCO): vede frequentemente il sovrapporsi
di due patologie con caratteristiche cliniche ed anatomiche distinte: enfisema (a
livello acinare), bronchite (a livello bronchiale).
2. Asma: una patologia totalmente distinta e solo in alcuni casi pu sovrapporsi alla
BPCO.
3. Bronchiectasia.
Il rapporto tra BPCO, enfisema, bronchite ed asma piuttosto complesso. I pazienti
che manifestano segni di bronchite cronica o di enfisema senza ostruzione al flusso
aereo hanno una di queste patologie o entrambe ma non la BPCO.
La maggior parte dei pazienti con BPCO, che per definizione ha un'ostruzione al flusso
aereo, ha segni sia di bronchite cronica che di enfisema.
I pazienti affetti da asma caratterizzato da un'incompleta reversibilit dell'ostruzione
bronchiale sono considerati affetti da una forma di BPCO (chiamata bronchite
asmatica), dal momento che spesso non possono essere differenziati dai bronchitici
cronici ed enfisematosi con ostruzione bronchiale reversibile e iperreattivit
bronchiale.
Quelli con ostruzione bronchiale completamente reversibile senza segni di bronchite
cronica o di enfisema sono affetti da asma ma non da BPCO.
49
2a. Enfisema
Ingrandimento anomalo e permanente dello spazio aereo distale ai bronchioli
terminali, accompagnata da distruzione delle pareti alveolari, ma senza evidenza di
fibrosi.
Classificazione dellenfisema
Lenfisema viene caratterizzato secondo la sua distribuzione anatomica nel contesto
del lobulo.
1) enfisema panacinare: gli acini sono uniformemente e tutti dilatati, dal bronchiolo
respiratorio fino agli alveoli respiratori. pi comune e grave nelle regioni antero-
inferiori del polmone. associato a deficit di alfa1-antitripsina.
2) Enfisema centrolobulare: coinvolge solo le regioni centrali degli acini, in
corrispondenza dei bronchioli respiratori, mentre le regioni terminali sono
risparmiate. pi comune e grave nelle regioni apicali del polmone. Colpisce
soprattutto i forti fumatori, spesso in associazione a bronchite cronica; costituisce il
95% dei casi di enfisema causante ostruzione di flusso rilevante.
3) Enfisema lobulare distale (parasettale): coinvolge in modo > le regioni distali degli
acini, mentre la parte prossimale di solito risparmiata. Si manifesta in sede
sottopleurica o lungo i setti fibrosi interlobulari. Il resto del polmone spesso
risparmiato, cosicch la funzione polmonare pu essere ben conservata nonostante
molte aree di malattia localmente grave. Questo tipo di enfisema, che interessa
spesso gli apici, causa pneumotorace spontaneo nelle persone giovani e pu
produrre bolle giganti.
4) Enfisema irregolare: lacino interessato in modo irregolare in modo
invariabilmente associato a fenomeni di cicatrizzazione. Di fatto la forma pi
comune di enfisema, perch le lesioni cicatriziali sono un riscontro molto comune in
seguito a processi infiammatori guariti. Tuttavia nella maggior parte dei casi
asintomatico e clinicamente irrilevante.
Patogenesi
a. enfisema panacinare
La teoria pi accreditata che si tratti di uno squilibrio proteasi-antiproteasi, dovuto a
deficit genetico di alfa1-antitripsina, e che dunque coinvolge lintero acino.
Lalfa1-antitripsina una proteina plasmatica sintetizzata dal fegato: si tratta di una
proteina dellinfiammazione acuta dato il suo ruolo di grande importanza nella
regolazione del processo flogistico.
Su tratta infatti di una dei principali inibitori delle proteasi secrete dai neutrofili
durante linfiammazione e dunque anche dellelastasi, di cui i PMN sono fra i
principali produttori e che sarebbe in grado di degradare anche il tessuto polmonare.
Si spiega dunque come nei soggeti con carenza di alfa1-antitripsina qualsiasi stimolo
in grado di aumentare il numero di PMN nei polmoni e di provocare rilascio dei loro
granuli contenenti elastasi, provoca distruzione tissutale incontrollata, perch
- presente una bassa attivit anti-proteasica di regolazione
- i PMN attivati rilasciano radicali liberi che lattivit delle poche alfa1-
antitripsine presenti.
b. enfisema centrolobulare
In questo caso il fattore eziologico principale il fumo di sigaretta.
Nei fumatori si ha:
50
1. effetto chemiotattico della nicotina su PMN e macrofagi nellalveolo polmonare:
PMN produzione di elastasi
produzione di radicali liberi dellossigeno (ROI) che inibiscono alfa1-
antitripsina
macrofagi produzione di proteasi resistenti allazione dell alfa1-antitripsina e
in grado di esercitare attivit proteolitica su alfa1-antitripsina medesima.
2. Presenza di numerosi ROI nel fumo:
inibizione dellazione dell alfa1-antitripsina
consumo del corredo fisiologico di anti-ossidanti presenti a livello polmonare
3. Stimolazione dellattivit elastasica macrofagica da parte del fumo.
Il deposito delle particelle di fumo avviene principalmente a livello della biforcazione
dei bronchioli respiratori con conseguente aumento dellattivit proteolitica
soprattutto centroacinare
Morfologia
Macroscopica:
- enfisema panacinare: in fase avanzata volume dei polmoni con parziale
sovrapposizione al cuore.
- enfisema centroacinare: meno peculiare. Parte superiore del polmone pi colpita
- enfisema lobulare distale o irregolare: formazione di bolle (blebs), spazi aerei che
possono diventare enormi, occupando un intero emitorace. Le bolle possono essere
degli spazi completamente vuoti o attraversate da tralci di tessuto polmonare.
Microscopica:
- alveoli molto dilatati separati da setti sottili
- pori di Kohn enormemente ingranditi
- presenza di bolle talvolta
- spesso bronchioli respiratori e vasi alterati, compressi dallalterazione
enfisematosa.
Clinica
- Dispnea: il primo sintomo; compare insidiosa, ma sempre ingravescente.
- Tosse o sibili: presente di solito tardivamente e con scarso espettorato.
- Calo ponderale: sempre presente.
- Cuore polmonare (insufficienza cardiaca dx, dovuta a ipertensione polmonare
secondaria) ed insufficienza respiaratoria: in fase terminale ed associati a prognosi
infausta.
Il paziente con enfisema tipicamente presenta torace a botte, ed ha imparato a
compensare la sua patologia espirando lentamente ed in modo prolungato; si siede
dunque con il busto in avanti, in posizione incurvata ed espira attraverso le labbra
corrugate.
Tipicamente con la spirometria, si vede che il suo massimo flusso espiratorio
diminuito, ma in molti casi attraverso liperventilazione la sua ossigenazione pu
rimanere buona; questi pz sono detti pink puffers.
51
2b. Bronchite cronica
Condizione caratterizata da una tosse cronica produttiva per almeno 3 mesi di 2 anni
successivi, quando altre possibili cause, come le infezioni da Mycobacterium
tuberculosis, il cancro del polmone o lo scompenso cardiaco cronico, sono state escluse.
definita:
- bronchite cronica semplice: tosse produttiva senza segni di ostruzione delle vie aree
- bronchite asmatica cronica: caratterizzata da iperreattivit delle vie aeree con
broncospasmo intermittente e sibili espiratori.
- Bronchite cronica ostruttiva: caratterizzata da ostruzione cronica del flusso.
Tipicamente associata allenfiema nella BPCO.
Patogenesi
Sostanze irritanti ( fumo, silicio, polvere di granaglie)che provocano lesione dei bronchi
e dei bronchioli
reazione dei PMN con conseguente produzione di proteasi che aumentano il danno ed
inducono
reazione metaplastica della mucosa bronchiale:
ipertrofia della ghiandole sottomucose di trachea e bronchi
ipersecrezione di muco delle grandi vie respiratorie
Lesione continua e ripetuta da parte delle sostanze irritanti
Sovrapposizione di infezioni batteriche e virali
Piccoli bronchi e bronchioli:
aumento in numero e dimensioni delle cellule caliciformi (metaplasia)
formazione di tappi mucosi nel lume
infiammazione e fibrosi della parete bronchiolare
ostruzione precoce e reversibile
Lesione continua e ripetuta (sosatnze irritanti) ed infezione continua e ripetuta
Bronchite cronica
Se la bronchite cronica comporta ostruzione delle vie aeree allora associata a
broncopneumopatia cronica ostruttiva.
Morfologia:
Macroscopica:
- iperemia tumefazione edema della mucosa (reazione flogistica)
- ipersecrezione mucosa o mucopurulenta
- bronchioli a volte ripieni di cilindri di materiale purulento
Microscopica:
- ipertrofia delle ghiandole sottomucose muco-secernenti di trachea e bronchi
- dimensioni e numero delle cellule caliciformi a livello bronchiale e bronchiolare
eventuale formazione di tappi mucosi
52
- marcato restringimento dei bronchioli con a volte obliterazione completa per fibrosi
bronchiolite obliterante
Clinica
- Tosse produttiva persistente: il sintomo cardinale
- Dispnea: lieve, si sviluppa tardivamente
- Infezioni: ricorrenti e recidivanti
- Insufficienza respiratoria con ipossiemia, ipossia e lieve cianosi: compaiono spesso
- Cuore polmonare: una complicanza frequente
I pazienti con questo tipo di patologia sono anche detti blue bloater per il qudro di
cianosi associato allespettorazione purulenta.
2c. Asma
Malattia infiammatoria cronica delle vie aeree dovuta probabilmente al fatto che
linfiammazione provoca iperreattivit bronchiale (broncospasmo) a diversi stimoli,
altrimenti innocui. Di solito associata a broncocostrizione ed ostruzione diffusa e di
grado variabile, ma generalmente reversibile spontaneamente dopo adeguato
trattaemento.
Classificazione dellasma
Non esiste una vera e propria classificazione dellasma, ma ve ne sono molte nessuna
delle quali completa.
1. classificazione basata su frequenza e gravit dei sintomi
- lieve, moderata e grave
- intermittente, persistente
2. classificazione basata sulla terapia
- asma steroido-dipendente
- asma steroido resistente
- asma difficile
- asma instabile
3. classificazione su base eziologica
- asma estrinseca: iniziata da reazione di ipersensibilit di tipo I, indotta da
esposizione ad antigene estrinseco
- asma intrinseca: iniziata da meccanismi diversi da quelli immunitari: ingestione di
aspirina; freddo; infezioni; irritanti; stress; attivit fisica)
4. classificazione in base allagente scatenante
- asma stagionale, indotta dallattivit fisica, farmaco-indotta, professionale,
bronchite del fumatore
Patogenesi
Le principali condizioni che portano allo sviluppo di asma sono:
1. predisposizione genetica allipersensibilit di tipo I:
Poich la maggior parte delle asme di tipo estrinseco (atopico), un predisiposizione
allipersensibilit di tipo I comporta un fattore importante di genesi dellasma.
Normalmente esistono due classi di linfociti, TH1 e TH2, le quali rispondono a stimoli
differenti e cosituiscono un circuito di immunoregolazione, per cui le citochine secrete
da una delle due classi vanno ad inibire il differenziamento nellaltra classe e
viceversa.
53
Probabilmente la predisposizione allipersensibilit di tipo I nasce da uno squilibrio
della regolazione reciproca: i linfociti TH1 non secernono pi le citochine inibitorie
della risposta di tipo TH2 e dunque si ha differenziamento delle cellule T francamente
deviato in direzione TH2. Questo comporta il facile instaurarsi di:
2. stato di flogosi acuta o cronica delle vie aeree:
Lo stato infiammatorio che pu essere indotto anche in assenza di una ipersensibilit
di tipo I, in risposta a differenti stimoli (infezioni, farmaci, inalazione di sostanze
tossiche) un fattore chiave della patogenesi dellasma poich conduce alla sua
condizione caratteristica che quella di una
3. iperreattivit bronchiale: aumentato aumento della reattivit bronchiale
(broncocostrizione, secrezione di muco) in risposta a diversi stimoli.
Inoltre sembra sia possibile riscontrare la presenza di modificazioni strutturali delle
parete dei bronchioli (includenti ipertrofia della muscolatura liscia bronchiale ed
ipertrofia delle ghiandole), a seguito, ma anche precedentemente linstaurarsi dello
stato flogistico. Dunque sembra che questo rimodellamento bronchiale possa essere:
- una conseguenza dello stato infiammatorio
- in alcuni casi un fattore determinato geneticamente che predispone allo sviluppo di
infiammazione e dunque di asma.
1. Asma atopica
il pi comune tipo di asma ed insorge prevalentemente durante linfanzia.
frequente unanamnesi familiare positiva per atopia perch vi pu essere una
predisposizione genetica a questo tipo di patologie (vedi predisposizione verso la
differenziazione in direzione delle cellule TH2).
Il modello di patogenesi per lasma atopica il seguente:
A. sensibilizzazione allantigene:
inalazione di antigeni irritanti (allergeni)
risposta di tipo TH2 preponderante
attivazione delle cellule TH2 e rilascio di citochine, come:
- IL-4 che induce produzione di IgE da parte dei linfociti B; la porzione Fc delle IgE
si viene dunque a legare alla superficie dei mastociti, la cui proliferazione
indotta sempre dallIL-4
- IL-5 che induce reclutamento e proliferazione degli eosinofili
In questo modo la mucosa bronchiale sensibilizzata allantigene e pronta ad evocare
una risposta infiammatoria in seguito a successivo contatto.
B. asma scatenata dalla successiva esposizione allallergene:
a. risposta acuta (entro pochi minuti):
Lesposizione dei mastociti presensibilizzati e ricoperti di IgE al medesimo
antigene scatena cross-linking delle IgE e rilascio dei mediatori dei mastociti, che si
trovano sulle spf mucose (antigene inalato)
I mediatori provocano
- allentamento del le tight junction con passaggio degli allergeni verso i pi
numerosi mastociti nella sottomucosa
- stimolazione diretta dei recettori subepiteliali vagali che provocano
broncocostrizione.
54
Effetti complessivi della risposta acuta:
- broncocostrizione
- aumento della permeabilit vascolare ed edema
- ipersecrezione di muco
- ipotensione in condizioni estreme ( edema)
b. risposta tardiva (comincia dopo 4-6 e persiste fino a 12-24 h o pi)
Il rilascio di citochine dai mastociti nella risposta acuta provoca anche afflusso di
altri leucociti, soprattutto eosinofili e loro attivazione.
Si ha rilascio di nuovi mediatori da parte di leucociti, endotelio e cellule epiteliali.
Questi mediatori provocano la reazione tardiva o ritardata.
- leucocotrieni C, D, E: bronoccostrizione prolungata ed permeabilit vascolare
- acetilcolina; broncocostrizione
- istamina: broncocostrizione
- prostaglandina D: broncocostrizione e vasodilatazione
- PAF: aggregazione piastrinica e liberazione di istamina e serotonina dai granuli
piastrinici.
2. Asma non atopica
In genere scatenato dalle infezioni dellapparato respiaratorio, generalmente dovute a
virus e dunque alla conseguente flogosi virus-indotta della mucosa respiratoria che
riduce la soglia dei recettori vagali subepiteliali per gli stimoli irritanti
(iperreattivit).
Mentre nel caso precedente lo stato infiammatorio era dovuto alla esposizione agli
allergeni, qui lo stato infiammatorio dovuto ad uninfezione virale: c un elemento
predisponente in meno.
3. Asma farmaco-indotta
La pi comune quella indotta dallaspirina, poich laspirina inibisce la via
metabolica dellacido arachidonico nella sua variante ciclo-ossigenasica, senza tuttavia
influenzare la via lipossigenasica e spostando lequilibrio verso la sintesi di leucotrieni
broncocostrittori.
4. Asma professionale
Provocata dallesposizione ripetuta ad agenti irritanti che causa una iperreattivit nei
confronti dei medesimi
Morfologia
Macroscopica:
- iperdistensione dei polmoni
- occlusione di bronchi e bronchioli da parte di tappi mucosi
Microscopica:
- tappi mucosi formati da aggregati vorticoidi di cellule epiteliali ( spirali di
Curshmann)
- numerosi eosinofili
- numerosi aggregati di materiale cristalloide proteine di mbr degli eosinofili
- rimodellamento bronchiale:
55
inspessimento mbr basale
edema ed infiltrato infiammatorio della parete dei bronchi e bronchioli
ipertrofia ghiandole sottomucose
ipertrofia parete muscolare liscia del bronco
Clinica
Tipicamente si intervallano crisi asmatiche ( specialmente durante la notte o alle
prime ore del mattino) tra le quali i pz possono essere del tutto asintomatici.
A volte si ha uno stato asmatico prolungato (giorni-settimane) che pu portare anche a
morte.
Attacco asmatico:
- dispnea
- sibili espiratori
- fame daria
- senso di costrizione
- tosse con eventuale espettorazione delle secrezioni mucose (notevole riduzione della
difficolt respiartoria)
Diagnosi: analisi dellespettorato e riscontro di eosinofili, spirali di Curshmann e
aggregati cristalloidi
Terapia: anti-infiammatoria, per alleviare gli attacchi. Di solito comunque la
broncocostrizione spontaneamente reversibile.
2d. Bronchiectasie
Dilatazione permanente di bronchi e bronchioli per distruzione del tessuto muscolare
ed elastico, associata ad infezioni croniche necrotizzanti.
Eziologia e patogenesi
Pu essere associata a :
1. malattie congenite o ereditarie: per esempio fibrosi cistica:
difetto genetico nel meccanismo di secrezione dei cloruri
secrezione di ioni cloruro nel muco e intake cellulare di sodio ed acqua
accumulo di secrezioni dense e viscose che ostruiscono le vie aeree
suscettibilit alle infezioni batteriche
ulteriore danneggiamento della parete bronchiale e distruzione del muscolo liscio, dei
tessuti elastici e fibrosi
dilatazione dei bronchi
progressiva ostruzione dei bronchi a causa della fibrosi di riparazione
2. stati postinfettivi: per ampia distruzione indotta direttamente dai patogeni o
indirettamente dalla reazione infiammmatoria
3. ostruzione bronchiale: neoplasie, corpi estranei, ritenzione di muco
56
Morfologia
Macroscopica:
- vie aeree dilatate fino a 4x (bronchiecatsie cilindriche slargamenti a forma di
tubo; bronchiectasie sacculari slargamenti fusiformi o sacculari).
Microscopica
- intensa essudazione infiammatoria nelle pareti bronchiali desquamazione
epiteliale ulcerazione necrotizzante aree fibrotiche nei casi pi cronicizzati
- spesso flora mista che pu essere isolata dai bronchi
Clinica
- tosse intensa e persistente con espettorato maleodorante
- dispnea
- occasionalmente emottisi
- a volte febbre , nel caso vi siano patogeni virulenti
Comunque rimane sempre associata ad uno stato infiammatorio che comporta
distruzione delle pareti delle vie aeree.
3. Malattia polmonare restrittiva
Comprendono un gruppo di malattie caratterizzate da ridotta espansione del
parenchima con diminuzione della capacit polmonare totale, e della compliance
polmonare, mentre il flusso massimo espirato normale o proporzionalmente
diminuito.
Le malattie restrittive si possono osservare generalmente in due condizioni:
1) malattie della parete toracica in presenza di un normale parenchima polmonare
malattie neuromuscolari come la poliomielite, malattie della pleura.
2) Malattie infiltrative o interstiziali acute o croniche
Si tratter solo delle malattie interstiziali.
Acute: se ne gi parlato. Sono classici esempi di questo tipo di patologia lARDS e la
polmonite acuta interstiziale.
Croniche: sono un grande gruppo di malattie caratterizzate dalla compromissione
cronica del parenchima polmonare soprattutto a livello interstiziale.
Fisiopatologia: impedimento allespansione dei polmoni, per un aumento della rigidit
polmonare dovuto a incremento della componente collagene su quella elastica; ne
consegue riduzione della capacit polmonare totale e della compliance polmonare.
Manifestazione clinica: dispnea, tachipnea, difficolt nellinspirazione, senza sibili o
segno alcuno di broncocostrizione. La diffusa fibrosi o cicatrizzazione pu provocare
restringimento delle arterie con conseguente possibilit di ipertensione polmonare ed
insufficienza polmonare destra terminale (cuore polmonare).
RX: diffusa infiltrazione dellinterstizio polmonare (da cui il termine malattia
interstiziale infiltrativa).
Istologia: nelle fasi precoci sono distinguibili, nelle fasi tardive sfociano tutte in
cicatrici e distruzione massiva del polmone. In base alle carattersitiche istologiche
possono essere classificate in:
- malattia cronica polmonare interstiziale fibrosante (fibrosi polmonare)
57
Polmonite interstiziale comune (fibrosi polmonare idiopatica)
Polmonite interstiziale aspecifica (fibrosi interstiziale diffusa)
Polmonite criptogenetica in via di organizzazione
Associata a collagenopatie
Pneumoconiosi
- malattia cronica polmonare interstiziale granulomatosa
sarcoidosi
polmonite da ipersensibilit
- malattia cronica polmonare interstiziale eosinofila
- malattia cronica polmonare interstiziale correlata al fumo
Patogenesi: indipendentemente dallagente eziologico noto o sconosciuto di ognuna di
queste patologie, si ritiene che la patogenesi di tutte le interstiziopatie converga in
unalveolite, cio in un infiammazione a livello delle pareti e degli spazi alveolari. Si
ha dunque accumulo di cellule dellinfiammazione e immunitarie nella parete e negli
spazi alveolari che comporta:
- distorsione della normale struttura alveolare
- rilascio di mediatori infiammatori con conseguente danno del parenchima
Se questo danno e questa condizione infiammatoria cronica la risposta del tessuto
il tentativo di riaparazione attraverso la formazione di una cicatrice e dunque la
fibrosi.
FIBROSI POLMONARE
3a. Fibrosi polmonare idiopatica
La fibrosi polmonare idiopatica (Idiopathic Pulmonary Fibrosis, IPF), o alveolite
sclerosante criptogenica , un termine che si riferisce ad una specifica sindrome
causante il 50-60% di tutti i casi di malattia polmonare interstiziale idiopatica.
La IPF ha specifiche caratteristiche cliniche e anatomo-patologiche, perci questo
termine non deve essere utilizzato per descrivere tutte le malattie interstiziali
polmonari di eziologia ignota.
La polmonite interstiziale comune (Usual Interstitial Pneumonia, UIP), un particolare
quadro istopatologico di polmonite interstiziale, il classico quadro osservato alla
biopsia polmonare nella IPF.
Il riscontro di questo quadro necessario ma non sufficiente a fare diagnosi di IPF: un
quadro simile infatti si pu riscontrare anche in altre patologie (patologia polmonare
associata a collagenopatie ed asbestosi).
Patogenesi
Gli agenti eziologici sono sconosciuti.
Si pensa per che la genesi dellIPF sia dovuta a cicli ripetuti di infiammazione
alveolare acuta (alveolite), provocata da stimoli non identificati.
La riparazione del danno provocherebbe proliferazione fibroblastica con formazione di
foci fibroblastici.
Alla formazione di queste zone di proliferazione fibroblastica seguirebbe dunque la
fibrosi e dunque la formazione di aree di collagene denso, con perdita della
funzionalit polmonare.
Morfologia
Macroscopica
58
- spf pleurica con aspetto ad acciottolato, per la retrazione cicatriziale lungo i setti
interlobulari
- la fibrosi del parenchima polmonare diffusa soprattutto lungo i setti e nelle
regioni subpleuriche
Microscopica
- presenza di fibrosi interstiziale a chiazze, non omogenea
- le lesioni fibrotiche variano dintensit con il tempo.
Lesioni precoci: foci fibroblastici caratterizzati da alta cellularit e proliferazione
fibroblastica esuberante
Lesioni tardive: cicatrizzazione e formazione di aree di fibrosi pi ricche di
collagene e meno cellulari
Infine: la densa fibrosi pu provocare collasso della parete alveolare e formazione
di aree a nido d'ape, formate da spazi aerei fibrotico-cistici, frequentemente rivestiti
da epitelio bronchiolare e pneumociti di tipo II iperplastici (riparazione)e riempiti di
muco polmone a favo dapi.
- infiltrato flogistico lieve delle aree necrotiche
La distribuzione sottopleurica e parasettale, il carattere disomogeneo e l'eterogeneit
temporale sono le caratteristiche pi utili per identificare la UIP.
Clinica
Le manifestazioni cliniche della IPF comprendono la dispnea da sforzo, la tosse non
produttiva e i crepitii inspiratori simili al suono del velcro all'auscultazione del torace.
Nelle fasi avanzate della malattia, possono comparire i segni dellipossiemia ,
l'ippocratismo digitale (perdita del normale angolo a livello del letto ungueale) e la
cianosi.
Il decorso della IPF nella maggior parte dei casi progressivo, nonostante la terapia
farmacologia e la media di sopravvivenza < 3 anni.
Lunica terapia definitiva il trapianto di polmone.
3b. Polmonite interstiziale aspecifica
Gruppo di malattie interstiziali polmonari diffuse, ad eziologia del tutto sconosciuta.
Le biopsie polmonari non riescono a dimostrare un quadro sovrapponibile a nessuna
delle patologie interstiziali ben caratterizzate.
La diagnosi molto importante per perch questi pz presentano una prognosi
decisamente migliore rispetto ai pazienti con UIP.
Morfologia
Flogosi interstiziale cronica lieve o moderata, con distribuzione uniforme.
Fibrosi interstiziale diffusa ed uniforme, senza eterogeneit temporale (assenza di
focolai fibroblastici)
Clinica
Dispnea e tosse per molti mesi.
Prognosi decisamente migliore rispetto a quello della UIP.
3c. Polmonite criptogenetica in via di organizzazione
La polmonite criptogenetica in via di organizzazione (Cryptogenic Organizing
pneumonia COP) anche detta bronchiolite obliterante evolutiva in polmonite.
59
Clinica: dispnea e tosse
Rx: aree non uniformi di addensamento parenchimale in sede subpleurica o
peirbronchiale
Istologia: fibrosi intralveolare formazione di tappi polipoidi di connettivo lasso
fibrotico nei dotti alveolari e negli alveoli, mentre la sottostante architettura
polmonare mantenuta normale.
Non vi fibrosi interstiziale o polmonite a favo dapi.
Terapia: guarigione spontanea o dopo trattamento steroideo.
3d. Interessamento polmonare nelle collagenopatie vascolari
Sclerosi sistemica: malattia cronica ad eziologia sconosciuta caratterizzata da abnorme
accumulo di tessuto fibroso nella cute ed in molti organi. Probabilmente dovuta ad
accumulo di risposte immunitarie anomale e danno vascolare, che portano ad
accumulo locale di fattori di crescita che agiscono stimolando la produzione di
collagene.
I polmoni sono coinvolti nel 50% dei pz: pu provocare ipertensione polmonare
(disfunzione endoteliale vascolare dei polmoni vasocostrizione polmonare) e fibrosi
polmonare.
Il quadro della fibrosi polmonare, quando presente indistinguibile da quello della
polmonite interstiziale aspecifica.
Lupus eritematoso sistemico: malattia di origine multifattoriale che vede attivazione
delle cellule T helper e B con conseguente produzione di auto anticorpi di diverse
specie e che reagiscono contro numerosi organi. Il polmone frequentemente coinvolto
con pleurite e versamenti pleurici e meno frrequentemente con fibrosi interstiziale
cronica, che si manifesta istologicamente con un quadro di infiltrati parenchimali
disomogeni e transitori.
Artrite reumatoide: malattia infiammatoria cronica, dovuta a meccanismi autoimmuni
a loro volta scatenati dallesposizione di un ospite geneticamente sensibile ad un
antigene artritogenico. Aggredisce principalmente le articolazioni anche se pu colpire
in realt molti organi, fra cui anche il polmone. A livello polmonare pu causare:
1. pleurite cronica, con o senza versamento
2. fibrosi interstiziale diffusa
3. noduli reumatoidi intrapolmonari
4. ipertensione polmonare
Linteressamento polmonare in queste malattie solitamente associato a prognosi
peggiore, anche se sempre migliore della UIP idiopatica
3e. Pneumoconiosi
Termine che comprende uno spettro di patologie causate dallinalazione di particelle
organiche e inorganiche, fumo, vapori chimici.
Patogenesi
La patogenesi risulta differente per ogni tipo di pneumoconiosi, ma alcune
caratteristiche patogenetiche accomunano tutte queste patologie.
Lo sviluppo e la gravit della pneumoconiosi dipendono da:
a. quantit di polvere trattenuta nei polmoni: a sua volta influenzata da
concentrazione della polvere nellaria
60
durata dellesposizione
efficacia dei meccanismi di clearance.
b. Dimensioni, forma e galleggiabilit delle particelle:
le particelle pi dannose hanno diametro di 1-5 m. riescono a raggiungere gli
alveoli e possono localizzarsi nei setti
in condizioni normali i macrofagi alveolari sono pochi, ma se la polvere raggiunge gli
alveoli il loro numero aumente rapidamente induzione di una risposta
infiammatoria
c. Solubilit e reattivit biochimica delle particelle
Tanto pi piccola e pi solubile la particella, tanto pi facilmente si scioglie nei
liquidi polmonari, raggiungendo rapidamente effetti tossici danno polmonare acuto
Se invece la particella grande e poco solubile, resiste con facilit alla dissoluzione e
persiste nel parenchima polmonare per molto tempo danno polmonare cronico
Il tutto anche influenzato dalla reattivit della particella
d. possibili ulteriori effetti di altri irritanti (fumo)
Il fumo di tabacco peggiora gli effetti di tutte le polveri minerali inalate, poich blocca
le ciglia dellepitelio respiratorio e dunque diminuisce la clearence delle vie
respiratorie nei cfr delle particelle inalate.
Tuttavia il fumo viene ad esercitare il > effetto peggiorativo se sommato agli effetti
dellasbesto.
Alcune particelle non vengono ad esercitare solo unazione irritante locale, ma possono
scatenare reazioni infiammatorie sistemiche, una volta raggiunto il circolo linfatico o
ematico (direttamente o trasportate dai macrofagi).
PNEUMOCONIOSI da MINATORI DI CARBONE
Si possono presentare 3 quadri clinici in seguito allesposizione prolungata a polvere di
carbone nelle miniere di carbone:
1) antracosi asintomatica: di comune riscontro in tutti coloro che vivono in un
ambiente metropolitano.
2) pneumoconiosi semplice dei minatori di carbone (coal workers pneumoconiosis
CWP) scarsa o assente disfunzione polmonare
3) CWP complicata o fibrosi progressiva polmonare (progressive massive fibrosi PMF)
funzionalit polmonare compromessa. Il termine PMF genereico e caratterizza una condizione
istologica che si pu verificare come complicanza di qualsiasi pneumoconiosi
Morfologia
1) antracosi:
- facogitosi ed accumulo del carbone inalato da parte dei macrofagi alveolari o
interstiziali.
- Deposito dei macrofagi lungo i linfatici o nel linfoide organizzato lungo i bronchi o
allilo strie lineari ed aggregati di pigmento antracotico nei linfatici e linfonodi
polmonari.
2) CWP semplice:
- macule di carbone (1-2mm.): macrofagi ripieni di carbone
- noduli di carbone (> 2mm.) : macrofagi ripieni di carbone tenuti insieme da una
sottile rete collagene
61
- lesioni distribuite uniformemente nel polmone, ma con > concentrazione nei lobi
superiori, soprattutto vicino ai bronchioli respiratori, sede delliniziale accumulo di
polvere.
3) CWP complicata:
- cicatrici nere (> 2 cm e fino a 10 cm) multiple formate da collagene denso e
pigmentato, con al centro spesso aree di necrosi
- la fibrosi coinvolge gradualmente vasi sanguigni e vie aeree.
Clinica
La CWP semplice non si associa ad alcun sintomo respiratorio o la riduzione della
funzionalit polmonare davvero modesta
La CWP complicata mostra disfunzione polmonare, ipertensione e cuore polmonare nel
10% dei casi associato a PMF
SILICOSI
La silicosi, la malattia professionale respiratoria pi diffusa al mondo, insorge in
genere dopo inalazione prolungata di piccole particelle di silice cristallina libera nelle
miniere di metalli (di piombo, antracite, rame, argento, oro), nelle fonderie, nelle
fabbriche di ceramica e vetro e nelle industrie estrattive delle rocce arenarie e del
granito.
Dunque le categorie professionali pi a rischio sono minatori e soffiatori di vetro.
Di solito, sono necessari 20-30 anni di esposizione prima che la malattia si renda
manifesta, sebbene si sviluppi in < 10 anni quando l'esposizione alle polveri molto
alta.
Molto meno comunemente, lesposizione da mesi fino a pochi anni pu provocare
silicosi acuta.
Patogenesi
La silice presente in forma cristallina e amorfa; le forma cristalline ed in particolare
il quarzo che ne la pi diffusa, sono molto pi fibrinogeniche di quelle amorfe.
Le particelle di silice respirabili sono fagocitate dai macrofagi alveolari: parte dei
macrofagi muore per gli effetti tossici della stessa silice ma rimagono macrofagi vitali,
nei quali la silice causa attivazione e rilascio di enzimi citotossici e mediatori che
inducono fibrosi del parenchima polmonare. Quando un macrofago muore, le particelle
di silice vengono liberate e fagocitate da altri macrofagi e il processo pu ripetersi.
Se unito ad altri minerali il quarzo ha ridotto effetto fibrogenico e questo importante
perch negli ambienti lavorativi esso non quasi mai puro.
Morfologia
Macroscopica
- Fasi iniziali: noduli piccoli e ialini appena palpabili nelle zone superiori dei polmoni
- Fasi successive: fusione dei noduli fibrotici con formazione di cicatrici dure e
fibrotiche che possono presentare rammollimento centrale (sovrapposizione di TBC
o di ischemia) marcata distorsione dell'architettura polmonare
- Eventuale presenza di calcificazioni a guscio duovo nei linfonodi: sottili lamine di
calcificazioni che circondano aree dove la calcificazione assente.
- Fase terminale: PMF
Microscopica
62
- noduli: strati concentrici di collagene ialinizzato circondati da una capsula di
collagene pi denso.
Clinica
I pazienti con silicosi nodulare semplice non presentano n sintomi n, solitamente,
compromissione respiratoria. Essi possono lamentare tosse ed espettorazione, ma tali
sintomi sono dovuti alla bronchite industriale e si presentano con la stessa frequenza
nei soggetti con rx normale.
La silicosi a noduli confluenti, al contrario, pu determinare grave dispnea, tosse ed
espettorato. La gravit dell'affanno correlata alla dimensione delle masse confluenti
nei polmoni. Quando le masse sono molto estese, il paziente raggiunge una grave
invalidit. Man mano che le masse invadono e obliterano il letto vascolare, si
instaurano ipertensione polmonare e ipertrofia ventricolare destra.
Lesordio clinico comunque avviene sempre con dispnea ed avviene negli stati finali
della malattia: da quel momento in poi la malattia progressiva anche se il paziente
non pi esposto.
La silicosi porta ad aumentata predisposizione alla TBC che molto spesso si
sovrappone al quadro di silicosi.
Questo avviene perch la silicosi deprime la risposta cellulo-mediata e perch i cristalli
di silice inibiscono la capacit, gi limitata, dei macrofagi di uccidere i micobatteri.
controverso un eventuale ruolo della silicosi nella patogenesi del carcinoma
polmonare.
Malattie legate allasbesto
Asbesto (amianto): cristalli idrati di silice
Lesposizione professionale allasbesto pu provocare:
- placche pleuriche: placche ben circoscritte di collagene denso e calcio sulla zona
anteriore e postero-latreale della pleura parietale e sulla cupola diaframmatica.
Non contengono evidenze che le correlino alla patologia da asbesto (corpi
asbestosici), ma si manifestano quasi sempre in pz con storia di esposizione
allasbesto.
- Fibrosi pleurica viscerale diffusa: molto rara, pu portare alla formazione di
aderenze polmone-cavit toracica
- Versamenti pleurici: solitamente sierosi, a volte ematici
- Carcinoma polmonare: rischio 5x nei lavoratori dellasbesto. Se in associazione con
fumo di sigaretta rischio 55x
- Mesoteliomi: sono rari tumori del tessuto mesoteliale (pleura e peritoneo). Rischio
1000x. Il fumo di sigaretta non aumenta il rischio
Patogenesi
Vi sono 2 distinte forme di asbesto:
1) serpentino: fibre ricche e flessibili, pi frequenti negli ambienti lavorativi.
La struttura flessibile ed allungata rende pi facile il loro intrappolamento nelle vie
respiratorie superiori ed eliminazione dallapparato mucociliare.
63
Sono maggiormente solubili, dunque anche se penetrano a livello polmonare, vengono
gradualmente eliminati.
Di conseguenza sono fibre meno patogene; in elevata concentrazione sono comunque
associate a tutte le patologie amianto-correlate, tranne che al mesotelioma
2) anfibolo: fibre dritte e rigide, fragili, meno frequenti negli ambienti lavorativi.
La struttura dritta e rigida permette loro di rimanere nel flusso aereo e di essere
trasportati in profondit nei polmoni, dove possono penetrare nelle cellule epiteliali e
raggiungere linterstizio.
Sono poco solubili, dunque non vengono facilmente eliminati.
Di conseguenza sono fibre pi patogene, in particolare associate allinduzione di
mesoteliomi.
Il meccanismo patogenetico il seguente:
arresto delle fibre asbestosiche a livello della biforcazione delle piccole vie aeree
penetrazione delle fibre con lesione
attivazione di macrofagi che tentano di fagocitare ed eliminare le particelle
produzione di citochine pro-infiammatorie (amplificazione della risposta) e
fibrogeniche da parte dei macrofagi.
Deposizione di fibrina e instaurarsi di una reazione infiammatoria cronica, dunque
persistente, che mantiene lo stimolo flogistico e fibrogenico
Fibrosi interstiziale
Se le fibre asbestosiche assorbono sostanze potenzialmente tossiche e cancerogene,
come quelle contenute nel fumo, potenziano i loro effetti, trasportandole nella
profondit del polmone: per questo che lesposizione ad asbesto associata al fumo
aumenta in modo cos ingente il rischio di carcinoma polmonare.
Morfologia
- fibrosi interstiziale polmonare diffusa, indistinguibile da quella dovuta ad altre
cause
- patognomonica la presenza in grande quantit di corpuscoli asbestosici: corpi
filiformi marroni-dorato, traslucidi. Sono formati da fibre di asbesto ricoperte da
materiale proteinaceo contenente ferro. Si formano nel tentativo dei macrofagi di
fagocitare ed eliminare le fibre di amianto (ferro dalla ferritina dei macrofagi)
- inizia intorno ai bronchioli respiratori e poi diffonde a sacchi alveolari ed alveoli,
dando luogo ad un quadro molto simile alla UIP: presenza di focolai fibroblastici
alternati a vari gradi di fibrosi fibrosi diffusa che distorce larchitettura
polmonareformazione di spazi cistici racchiusi in pareti fibrose polmonite a
favo dapi
- la caratteristica distintiva la presenza di corpuscoli asbestosici.
Clinica
La dispnea il primo sintomo ( di solito dopo 10-20 anni dalla prima esposizione).
64
La malattia pu rimanere stabile o progredire verso insufficienza respiratoriacuore
polmonaremorte.
MALATTIE GRANULOMATOSE
3f. Sarcoidosi
Malattia sistemica ad eziologia ignota, caratterizzata dalla formazione di granulomi
non caseosi in molti tessuti ed organi. Linteressamento polmonare si pu vedere nel
90% dei casi.
Prevalenza pi alta nelle donne e nei neri americani degli Stati Uniti. invece molto
rara nei cinesi e negli abitanti del Sud Est asiatico.
Eziologia e patogenesi
Leziologia sconosciuta. Sono stati individuati alcuni fattori sicuramente
predisponenti:
1. fattori immunologici: nel granuloma sarcoidotico vi sono numerose alterazioni
immunologiche che suggeriscono sviluppo di una risposta cellulo-mediata di tipo
TH ad antigeni ambientali, come base per la formazione del granuloma medesimo.
Questi fattori sono:
- accumulo di cellule T CD4+
- espansione oligoclonale delle cellule T
- livelli di citochine prodotte dai TH1 (IL2 espansione T-cellulare;
IFNattivazione dei macrofagi)
2. fattori genetici: la predisposizione genetica dimostrata da
- raggruppamento di casi in gruppi familiari
- associazione con alcuni genotipi HLA
3. Fattori ambientali: ruolo incerto
Morfologia
Granuloma non caseoso: caratterizzato dalla presenza di:
- cellule epitelioidi molto raggruppate
- cellule di Langhans o cellule giganti da corpo estraneo
- rara necrosi centrale
- reazione fibrosclerotica perifierica o, nelle fasi pi avanzate, cicatrici fibrose ialine
che sostituiscono completamente il granuloma
- corpi di Schaumann: concrezioni lamellari composte da calcio e proteine
- corpi asteroidi: inclusioni stellate dentro le cellule giganti.
Nessuno di questi reperti patognomonico di sarcoidosi perch pu essere riscontrato
anche a livello di altri tessuti.
Il quadro suddiviso per i diversi organi interessati il seguente:
a. polmone:
macroscopica non vi sono alterazioni dimostrabili. Raramente piccoli noduli dovuti
alla coalescenza dei granulomi
microscopica granulomi diffusi soprattutto lungo i linfatici, i bronchi ed i vasi
sanguigni. Forte tendenza a guarire delle lesioni a livello polmonare, dunque marcata
fibrosi e ialinizzazione
b. linfonodi:
interessati nel 90% dei casi (soprattutto ilari e mediastinici).
65
Sono aumentati di volume, separati, talvolta calcificati
c. milza:
coinvolta microscopicamente in dei casi.
Ingrandita macroscopicamente in 1/5 dei casi
d. fegato:
coinvolto un po meno della milza.
Pu essere leggermente ingrandito
e. midollo osseo:
frequente sito di coinvolgimento
f. lesioni cutanee
assumono aspetti macroscopici diversi noduli sottocutanei palpabili, placche
eritematose leggermente rilevate, lesioni piane un poco arrossate e desquamate
g. occhio, ghiandole lacrimali, ghiandole salivari:
h. interessamento muscolare:
spesso sottodiagnosticato, perch pu essere asintomatico
Clinica
La malattia ha diverse presentazioni cliniche a causa della variet di organi e tessuti
interessati.
Gli esordi clinico pi diffuso sono insidiosi e vedono:
- alterazioni respiratorie: affaticamento, tosse, dolore toracico
- sintomatologia generale: affaticamento, febbre, calo ponderale, anoressia,
sudorazioni notturne
Il decorso pu essere anchesso molto vario:
- progressivo e lentamente peggiorativo
- presenza di periodi di acutizzazione alternati a remissione
Il 70% dei pz guarisce con reliquati minimi o nulli.
20% guarisce con alterazioni permanenti della funzionalit polmonare o visiva
10-15% morte per fibrosi polmonare progressiva, o pi raramente per patologia
cardiaca.
3g. Polmonite da ipersensibilit
una malattia granulomatosa interstiziale diffusa del polmone, determinata da una
reazione allergica all'inalazione di polveri organiche inalate o, meno frequentemente,
di sostanze chimiche semplici.
In realt definisce uno spettro piuttosto ampio di malattie, provocate da prolungata
esposizione (mesi o settimane) a polveri.
Le pi comuni sono:
- polmone del contadino: per inalazione di polveri generate dal fieno raccolto umido e
tiepido, che ospita e permete la proliferazione di spore di actinomiceti termofili.
- Polmone dellallevatore di piccioni: per inalazione di polveri contenenti le proteine
del siero, delle secrezioni o delle piume dei piccioni
- Polmone da aria condizionata/umidificatore: inalazione di polveri contenenti batteri
termofili presenti nellacqua riscaldata dei serbatoi.
La caratteristica comune che la sovraesposizione provoca aumento della risposta
immunomediata contro lantigene inalato e dunque infiammazione ed iperreattivit
che si manifesta a livello alveolare; lesposizione continua anche successivamente agli
attacchi acuti, pu determinare progressione verso malattie polmonari croniche
66
fibrotiche. Lallontanamento dallagente ambientale una forma di prevenzione
sempre efficace, previo sviluppo della forma cronica.
Patogenesi
La polmonite da ipersensibilit considerata immunologicamente mediata, sebbene la
patogenesi non sia completamente chiarita.
Di solito si dimostrano Ac precipitanti contro gli Ag responsabili, il che depone per una
reazione allergica di tipo III, sebbene la vasculite non sia un reperto frequente.
La risposta granulomatosa primaria del tessuto e i riscontri nei modelli animali
indicano una reazione di ipersensibilit di tipo IV.
Si pensa dunque che rappresenti una risposta immunomediata ad un Ag estrinseco
che stimoli sia reazione da immunocomplessi, sia reazione di ipersensibilit ritardata.
Morfologia
1) polmonite interstiziale con accumuli di linfociti, plasmacellule e macrofagi
(ipersensibilit III)
2) granulomi non caseosi molto frequenti
3) nelle fasi avanzate fibrosi interstiziale ed eventuale bronchiolite obliterante
Clinica
Nella forma acuta si manifestano episodi di febbre, brividi, tosse e dispnea in un
soggetto gi sensibilizzato, tipicamente 4-6 h dopo la riesposizione all'Ag. Possono
essere presenti anche anoressia, nausea e vomito.
Alla radiografia del torace si vedono infiltrati diffusi e nodulari.
Le prove di funzionalit respiratoria mostrano un quadro restrittivo con volumi
polmonari ridotti
L'ostruzione delle vie aeree infrequente nella malattia acuta, ma pu svilupparsi
nella forma cronica.
Nella forma cronica, si possono sviluppare nel giro di mesi o anni di prolungata
esposizione, dispnea da sforzo ingravescente, tosse produttiva, astenia e perdita di
peso; la malattia pu evolvere fino all'insufficienza respiratoria.
Nella forma cronica non si hanno pi riacutizzazioni in deguito allesposizione
allantigene.
4. Malattie di origine vascolare
4a. Ipertensione polmonare
Si parla di ipertensione polmonare quando la pressione polmonare media raggiunge o
supera di quella sistemica (normalmente 1/8).
Pressione polmonare normale:
<25 mmHg a riposo
<30 mmHg sotto sforzo
Ipertensione:
lieve; 26-35 mmHg
moderata: 36-45 mmHg.
Severa: >45 mmHg.
Lipertensione polmonare pu essere
67
1) primaria o idiopatica: rara e si presenta in pz in cui tutte le cause note di
ipertensione polmonare sono state escluse. Pu essere a sua volta:
familiare (6% delle cause totali di ipertensione): dovuta a trasmissione
autosomica dominante. La dominanza per incompleta, dunque di fatto solo
il 20-30% dei membri familiari sviluppa malattia conclamata
sporadica: dovuta a disordini autoimmuni, sostanze tossiche o altro che
provocano probabilmente una mutazione ex novo. molto rara
2) secondaria: la pi frequente ed dovuta a condizioni strutturali
cardiopolmonari che aumentano il flusso o la resistenza ad esso, o la resistenza
al flusso ematico nel cuore sinistro. L e condizioni comprendono:
precedenti cardiopatie congenite o acquisite: pz con stenosi mitralica,
incremento della pressione striale sinistra, incremento della pressione
venosa e dunque arteriosa polmonare.
Malattie diffuse ostruttive e restrittive: comporta riduzione dellarea
totale del letto vascolare, a causa della distruzione del parenchima
polmonare con riduzione del letto capillare alveolare (patologia restrittiva) o
della riduzione del lume delle vie aeree(patologia restrittiva). La
conseguenza laumento della pressione venosa polmonare e dunque
aumento anche della pressione arteriosa polmonare.
Tromboembolie ricorrenti: pazienti con embolie polmonari ricorenti
vedono diminuzione dellarea totale del letto vascolare polmonare, ostruito
dagli emboli ricorrenti e conseguente aumento delle resistenze.
Disturbi autoimmuni: molte malattie autoimmuni interessano il circolo
polmonare causando patologia di tipo restrittivo e dunque fibrosi ed
ipertrofia anche a livello vascolare.
Patogenesi
IPERTENSIONE POLMONARE PRIMITIVA
a) Familiare
Causata da mutazione del gene che codifica per il recettore di tipo2 della proteina
morfogenica dellosso (BMPR2). Normalmente la BMPR2 una proteina
recettoriale di superficie, che lega una variet di citocchine tra cui il BMP, cio la
proteina morfogenetica dellosso. La via di segnalazione innescata dal legame BMP-
BMPR2, non coinvolta esclusivamente nellaccrescimento dellosso, ma anche
nelembriogenesi, nellapoptosi e nella proliferazione e differenziazione
cellulare.Nelle cellule muscolari lisce dei vasi, il meccanismo di trasmissione del
segnale per la BMPR2 causa inibizione della proliferazione e favorisce lapoptosi.
Liperetnsione polmonare primitiva dunque causata da mutazioni inattivanti del
gen della BMPR2, con conseguente proliferazione delle cellule muscolari liscie, e
delle cellule intimali e restringimento del lume dei vasi con aumento della
resistenza al flusso.
b) Sporadica:
Dovuta a mutazioni insorte ex.novo del gene che codifica per la BMPR2.
La manifestazione clinica di entrambi i tipi di ipe tensione polmonare primitiva
richiede lassoziazione con una serie di fattori genetici ed ambientali:
r
68
- esistenza di geni modificatori, principalmente quelli che controllano il tono
vascolare
- farmaci: anfetamine, triptofano, anoressanti che stimolano tutti la produzione di
serotonina (vasocostrittrice, effetto fitogeno sul muscolo liscio, aumenta
aggregazione piastrinica)
- condizioni fisiche: sesso femminile ( pi frequente), gravidanza, splenectomia.
- Patologie associate: infezione da HIV, collagenopatie ecc
IPERTENSIONE POLMONARE SECONDARIA
Il danno tipico della patologia associata comporta infine aumento del flusso o della
resistenza al flusso.
Da un punto di vista molecolare frequentemente si ha:
- aumento della produzione di endotelina ( sostanza vasocostrittri e) c
c
r
tr
r
- riduzione della produzione di prostaciclina ed NO (sostanze vasodilatatri i):
questa riduzione comporta inoltre stimolo dellativazione ed aggregazione
piastrinica, con eventuale trombosi sovrapposta ed ulteriore riduzione del lume.
- Produzione e rilascio di Gf e di citochine che stimolano la migrazione e la
replicazione delle cellule muscolari lisce dei vasi.
Morfologia
Lipertensione provoca disfunzione e danno a livello endoteliale: da esso deriva la
caratterizzazione morfologica dellipertensione.
Il danno vascolare pu interessare lintero albero vascolare polmonare ma
generalmente vengono colpite soprattutto a teriole e piccole arterie. Frequentemente
si ha:
- ipertrofia della tonaca media ed iperplasia intimale delle medesime
- eventuale fibrosi intimale con ulteriore restringimento del lume
- nei casi es emi si ha arteriopatia plessogenica polmonare: ciuffo di vasellini a
plesso (tessuto di granulazione) che circonda i lumi delle piccole arterie e pu
arrivare ad occluderne i lumi
Nei casi pi gravi sono interessate le grandi arterie polmonari con:
- aterosclerosi, del tutto simile allaterosclerosi sistemica.
In ogni caso la risposta endoteliale allipertensione polmonare, comporta ulteriore
ispessimento delle pareti arteriolari (raramente delle grandi arterie), con conseguente
ulteriore riduzione del lume ed aggravamento dellipe tensione.
IPERTENSIONE POLMONARE PRIMITIVA
- danno arteriolare severo
IPERTENSIONE POLMONARE SECONDARIA
- danno arteriolare meno severo ed associato a segni della patologia che lha
indotto (trombi, interstiziopatia, enfisema)
Clinica
Lesordio clinico avviene sempre nella fase avanzata della malattia
IPERTENSIONE POLMONARE PRIMITIVA
Colpisce soprattutto donne fra 20 e 40 anni.
Sintomi allesordio: dispnea ed affaticamento, eventualmente dolore toracico di tipo
anginoso
69
Sintomi successivi: grave difficolt respiratoria e cianosi
Sintomi terminali: ipertrofia ventricolare dx e cuore polmonare.
Se non viene eseguito trapianto si ha morte tra i 2 ed i 5 anni nell80% dei pz.
IPERTENSIONE POLMONARE SECONDARIA
Colpisce soprattutto gli anziani, a vote in modo quasi parafisiologico.
Il decorso lento e la prognosi ampiamente dipendente dalla patologia che ha indotto
lipertensi ne medesima. o
r
4b. Embolia, emorragia ed infarto polmonare
I trombi che occludono le arterie polmonari sono quasi sempre di origine embolia e
dunque si pu parlare tranquillamente di embolia polmonare riferendosi ad essi.
Il tipo pi comune di embolia polmonare un trombo migrato comunemente da una
vena degli arti inferio i o della pelvi (95%).
Larresto dellembolo pu avvenire a livello di
- tronco dell'arteria polmonare, oppure a livello dell
- arteria polmonare destra o sinistra oppure ad uno dei
- rami di suddivisione periferici e dunque pi piccoli.
Alle diverse localizzazioni corrispondono quadri differenti per sintomatologia e per
svolgimento.
L'embolia polmonare un'emergenza cardiovascolare grave, non infrequente, con una
mortalit del 30% nei casi con riconoscimento e trattamento precoce, che arriva quasi
al 100% quando la diagnosi viene effettuata tardivamente.
Fattori predisponesti allo sviluppo di embolia polmonare sono:
- presenza di una malattia cronica, come cardiopatie o tumori che provocano gi
un quadro di circolazione insufficiente a livello polmonare
- pz immobilizzati per giorni osettimane: il maggiore rischio si ha in quelli con
frattura del bacino
- stati di ipercosgulabilit primaria o secondarai
- cateteri venosi centrali a permanenza, che possono essere causa di trombi
nellatrio dx che danno origine ad emboli.
Morfologia
EMBOLO di GRANDI DIMENSIONI
Si pu fermare nel tronco dellarteria polmonare, localizzarsi a livello della
biforcazione (embolo a sella), o nei due rami principali dellarteria polmonare.
Ne consegue spesso ostruzione al flusso dellintero polmone che causa in modo molto
veloca:
- compromissione respiratoria totale del polmone: tutto il polmone dx o sx, oppure
entrambi sono ventilati ma non per fusi.
- Compromissione emodinamica acuta: aumento critico della resistenza
polmonare. Insorgenza di cuore polmonare, morte praticamente istantanea.
In questo caso durante la rianimazione si osserva caratteristicamente una
dissociazione elettromeccanica: lECG mostra una traccia, ma mancano i polsi
periferici a causa di massiccio arresto di sangue nella circolazione venosa.
70
EMBOLO di PICCOLE DIMENSIONI
Si ferma nei vasi periferici.
- nei pz con fnz cardiovascolare n rmale, le arterie bronchiali sostengono
temporaneamente lapposrto sanguigno al parenchima polmonare. Gli emboli spesso
si risolvono attraverso fibrinolisi. A volte la sovrapposizione di numerosi emboli
ripetuti pu provocare ipertensione polmonare, che pu poi dare luogo a sclerosi
vascolare polmonare e cuore polmonare cronico.La cosa importante che
linsorgenza di un picclo embolo pu fare prevedere linsorgenza di un successivo
embolo pi grande che si verifica nel 30% dei casi.
o
c
- Nei pz con circolazione gi insufficiente, si verifica invece infarto polmonare,
classicamente emorragico ( per necrosi delle cellule endoteliali a valle
dellocclusione). Classicamente linfarto emorragico a forma di cuneo, dalla
periferia del polmone con apice diretto verso lilo; il vaso occluso vicino allapice
dellinfarto.
Si ha conservazione della struttura alveolare pre-esistente.
Sono interessati i lobi inferiori e frequentemente si hanno lesioni multiple.
Fasi preco i: area rilevata di colore rosso-bluastro.
Entro 48 ore: inizio della lisi dei globuli rossi . gradualmente linfarto diviene pallido
ed infine di colore rosso-marrone per la produzione di emosiderina. Quindi inizia la
sostituzione fibrosa che porta infine linfarto a divenire una cicatrice.
- se lembolo setticoe causa infarto (infarto settico) si ha maggiore infiltrazione di
neutrofili, ed possibile evoluzione in ascesso polmonare.
Clinica
EMBOLO di GRANDI DIMENSIONI
- morte istantanea nella >parte dei casi
- se il pz sopravvive si pu sviluppare una sd clinica che simula linfarto miocardio
(dolore anginoso, dispnea, shock, aumento della temperatura e della LDH sierica.
EMBOLO di PICCOLE DIMENSIONI
- in mancanza di infarto: dolore toracico transitorio, tosse e brevi emorragie
polmonari
- se presente infarto: dolore toracico, tosse, dispnea, tachipnea, febbre.
La radiografia pu evidenziare linfarto 12-36 h dopo, come addensamento a forma
di cuneo.
La TAC o il dosaggio del D-dimero possono diagnosticare embolia. Langiografia
polmonare lesame pi specifico, ma rischioso per il pz.
La prevenzione dellembolia si pu fare con:
- precoce ripresa della deambulazione nel post-operatorio e nel post-partum
- utilizzo di calze elastiche a compressione graduata nei pz allettati
- uao di anticoagulanti
Terapia con antitrombotici ed anticoagulanti
71
4c. Sindrome emorragica polmonare diffusa
SINDROME di GOODPASTURE
Rara malattia autoimmune caratterizzata da auto-Ac circolanti contro la catena 3 del
collagene IV.
Gli epitopi che scatenano la reazione autoimmune sono normalmente nascosti
allinterno della molecola, dunque per lo sviluppo della malattia necessaria
lesposizione a fattori ambientali (infezioni, idrocarburi solventi, fumo) che
smascherino lantigene.
Gli anticorpi determinano distruzione delle mbr basali di:
- glomeruli renali glomerulonefrite rapidamente progressiva
- alveoli polmonari polmonita interstiziale necrotizzante emorragica
La maggior parte dei casi si sviluppa durante ladolescenza con prevalenza nel sesso
maschile
Morfologia
Macroscopica: polmoni pesanti, con aree rosso-marroni
Microscopica:
- necrosi delle pareti alveolari con emorragie intra-alveolari
- presenza di macrofagi ripieni di emosiderina
- reazione di riparazione negli stdi avanzati; fibrosi dei setti, ipertrofia pneumociti di
tipo II, organizzazione del sangue negli spazi alveolari.
Immunofluorescenza:
- depositi lineari di immunoglobuline, lungo le membrane basali delle pareti dei setti
Clinica
Esordio clinico tipico: sintomatologia polmonare emottisi, e addensamenti polmonari
focali alla rx
Manifestazioni successive: sintomatologia renale insufficienza renale rapidamente
progressiva
Morte frequentemente per uremia
Terapia:
- plasmaferesi: eliminazione degli auto-Ac circolanti e dei mediatori
dellinfiammazione
- terapia immunosoppressiva
EMOSIDEROSI POLMONARE IDIOPATICA
Rara malattia ad eziologia sconosciuta (si ipotizza meccanismo immunologico) che
vede emorragia alveolare diffusa ed intermittente.
Colpisce pi frequentemente i bambini.
Lesordio insidioso con tosse produttiva, emoftoe, anemia e calo ponderale. Alla rx del
torace addensamenti polmonari diffusi.
Terapia: vi risposta favorevole allimmunosoppressione e questo favorisce lipotesi di
una eziologia immunitaria della malattia.
GRANULOMATOSI di WEGENER
una malattia autoimmune che interessa soprattutto tratto aereo superiore (orecchio,
naso, seni paranasali) e polmoni, con presenza di:
- granulomi necrotizzanti acuti; diffusi, indefiniti
72
- capillarite; vasculite necrotizzante che colpisce i vasi di piccole dimensioni.
Di solito nella triade presente anche interessamento renale con glomerulonefriti
necrotizzanti, focali e spesso a semilune.
I maschi sono pi colpiti, tipicamente intorno ai 40 anni, con picco nella quinta
decade.
Clinica
Lesordio spesso con emoftoe.
Tipicamente poi si ha:
- polmonite persistente con infiltrati nodulari bilaterali che spesso vanno incontro a
cavitazione
- sinusite cronica
- ulcerazioni del rino-faringe
- sintomi renali
Senza terapia la malattia ha decorso maligno con morte entro 1 anno.
Diagnosi
Per la diagnosi necessario fare una biopsia polmonare transbronchiale: tuttavia
poich il materiale che puoi prelevare con questo esame piccolo rischi di prelevare
campioni privi del quadro istologico caratteristico e dunque non identificativi.
5. Infezioni polmonari
Le infezioni dellapparato respiratorio in generale sono le pi rilevanti dal punto di
vista epudemiologico e costituiscono la prima causa di interessamento medico nei
bambini e negli anziani
Le infezioni che si verificano a livello del polmone inoltre hanno spesso conseguenze
gravi, in particolare se associate ad altre patologie, ed hanno ancora un discreto grado
di morbidit e di mortalit; la polmonite dunque ancora gravata da unalta
percentuale di prognosi infausta.
Le vie respiratorie sono dotate di importanti meccanismi di difesa naturali; dunque
la polmonite pu insorgere in seguito a:
- compromissione dei meccanismi di difesa
- compromissione locale o generale delle difese immunitarie.
Alcuni dei meccanismi pi implicati nella compromissione dei meccanismi di difesa
sono:
Perdita del riflesso della tosse: nel coma, nellanestesia, in presenza di alterazioni
neuromuscolari, dovuta a farmaci. Pu provocare aspirazione del contenuto gastrico
Danno e compromissione della funzionalit dellapparato mucociliare: fumo di
sigaretta, inalazione di sostanze tossiche, patologie pregresse.
Interferenze con la capacit battericida dei macrofagi.
Congestione ed edema polmonare
Accumulo di secrezioni
Alcuni dei meccanismi pi implicati nella compromissione dei meccanismi immunitari
sono:
deficit immunologici genetici
73
deficit immunologici indotti da patologie
trattamenti immunosoppressivi
Si ha prevalenza di queste infezioni nei mesi freddi (> probabilit di sovraffollamento
in ambienti chiusi, < movimento delle ciglia, > probabilit di situazioni di flogosi
indotte dal freddo).
Solitamente la trasmissione avviene per inalazione di aerosol infetti (goccioline di
Plflugge).
Raramente si ha polmonite secondaria alla diffusione ematogena di unaltra infezione
5a. Polmoniti acute comunitarie
Per polmonite comunitaria si intende una polmonite riscontrata al di fuori dellambito
ospedaliero.
Le polmoniti comunitarie acute, possono essere batteriche o virali.
Le virali sono racchiuse nel capitolo delle polmoniti comunitarie atipiche.
Linfezione batterica spesso segue infezione virale del tratto respiratorio superiore
Nellinfezione batterica si ha formazione di essudato infiammatorio di tipo acuto
allinterno degli alveoli polmonari, con addensamento del tessuto polmonare, e
scomparsa del murmure vescicolare (crepitio riscontrabile a causa dellestensione degli
alveoli) allauscultazione.
Agenti eziologici
- streptococcus pneumoniae
- staphylococcus aureus
- Haemophylus influenzae
- Enterobatteri gram
- Pseudomonas aerugionosa specie negli immunodepressi
- Legionella pneumophila
- Moraxella catarrhalis
- Klebsiella pneumoniae
Morfologia
Allesame radiologico e macroscopico la polmonite batterica presenta due quadri:
1) broncopolmonite lobulare: formazione di foci multipli di infiltrazione ed
addensamento a livello peribronchiolare, opacit focali allrx
2) polmonite lobare: addensamento fibrinoso suppurativo di gran parte o di tutto il
lobo, con opacizzazione lobare allrx.
Molto spesso una broncopolmonite lobulare, vede espansione e convergenza degli
infiltrati multifocali, determinando addensamento lobare totale e dunque evolve verso
in una polmonite lobare. I due quadri clinici non sono cos distinti.
Clinicamente ci che pi importante e determina differenziazione della prognosi e
della terapia lidentificazione dellagente eziologico e dellestensione della malattia.
Broncopolmonite lobulare
Aree addensate di infiammazione suppurativa acuta, con diametro fra i 3-4cm.
Addensamento a chiazze e multilobare, presente soprattutto in zona basale.
Presenza di essudato purulento che riempie bronchi, bronchioli e alveoli adiacenti al
focolaio stesso.
74
Polmonite lobare
Sono stati descritti 4 stadi della risposta infiammatoria, applicabili soprattutto alla
polmonite lobare:
d) congestione congestione vascolare ed edema, dovuta alla risposta infiammatoria
allinvasione batterica.
macroscopica: polmone pesante, edematoso, rosso
microscopica: essudato intra-alveolare con molti batteri e pochi neutrofili che stanno
cominciando ad accumularsi.
e) epatizzazione rossa la risposta infiammatoria prosegue con aumento
dellessudazione
macroscopica: polmone rosso, duro, di consistenza epatica
microscopica: essudazione massiva di globuli rossi, neutrofili e fibrina negli spazi
alveolari
f) epatizzazione grigia progressiva lisi dei g.r. e essudazione fibrinosa che prosegue
macroscopica: polmone di colore marrone grigiastro, con spf asciutta
microscopica: disgregazione dei globuli rossi, essudato ricco di fibrina che comincia ad
organizzarsi, iniziale presenza di macrofagi
g) risoluzione progressiva digestione enzimatica dellessudato intra-alveolare, fino
alla produzione di una sostanza semifluida che:
- viene fagocitata dai macrofagi
- viene espettorata
- viene organizzata dai fibroblasti
Vi pu essere pleurite, cio reazione fibrinosa della pleura al di sopra
dellinfiammazione: pu risolveri venendo riassorbita, ma pi frequentemente causa
aderenze.
Complicanze
- formazione di ascessi danno e necrosi tissutale
- empiema reazione fibrinoso-suppurativa intrapleurica dovuta a diffusione
dellinfezione alla cavit pleurica
- organizzazione dellessudato trasformazione di una parte del polmone in tessuto
solido
- disseminazione batterica
Clinica
Esordio clinico:
- febbre alta progressiva o con brividi (infezione da pneumococco),
- tosse che pu essere produttiva, con escreato muco-purulento, a volte con strie
ematiche,
- emottisi in alcuni casi
Se vi pleurite associata si hanno dolore e sfregamenti pleurici
Terapia
Nella maggior parte dei acsi antibiotica, dopo identificazione dellagente eziologico
tramite indagine sullespettorato
75
5b. Polmoniti atipiche comunitarie
Vengono cos denominate, le polmoniti caratterizzate da:
- modesta quantit di escreato
- radiografia rx che evidenzia: mancanza di opacizzazione del parenchima, ma
presenza di infiltrato infiammatori e fibrosi a livello interstiziale e nei setti
alveolari.
- moderato aumento della conta leucocitaria
- scarso essudato alveolare
Agenti eziologici
- Mycoplasma pneumoniae: la pi comune forma di polmonite atipica, presente
soprattutto tra bambini ed adolescenti
- Chlamydia pneumonia
- Coxiella Burnetii
- Virus: influenzali e parainfluenzali, adenovirus, rinovirus, coronavirus
Patogenesi
Frequentemente secondaria ad uninfezione delle vie respiratorie superiori causata dai
medesimi virus, che si estende a livello polmonare, con flogosi interstiziale degli
alveoli.
Morfologia
- la reazione infiammatoria prevalentemente interstiziale, allinterno delle pareti
degli alveoli
- la reazione infiammatoria prevalentemente di tipo mononucleato, vedendo un
infiltrato nei setti alveolari formato da limfociti, istiociti e solo a volte
plasmacellule (poco presenti neutrofili)
- i setti alveolari sono inspessiti ed edematosi inizialmente e poi possono andare
incontro ad organizzazione fibrotica
- gli alveoli hanno essudato assente o scarso e costituito da materiale proteinaceo e
cellule mononucleate.
- Presenza di mbr ialine di colore rosa che rivestono le pareti alveolari (come
nellARDS)
Leradicazione dellinfezione vede il normale reinstaurarsi dellarchitettura polmonare.
Le sovrainfezioni batteriche modificano il quadro istologico.
Clinica
Caratteristicamente questo tipo di infezioni presenta un esordio clinico con pochi
sintomi che permettono di identificare la localizzazione polmonare.
Lesordio pu essere anche senza tosse e caratterizzato solo da febbre, cefalea, dolori
muscolari ed alle articolazioni.
Seguono i sintomi tipici del ridotto scambio gassoso: dispnea, tachipnea, dolore
toracico ed eventualmente cianosi.
5c. Polmoniti nosocomiali
Per polmonite nosocomiale si intende una polmonite contratta in ambito ospedaliero,
cio almeno dopo 48h di ricovero.
Condizioni predisponenti sono:
- laffollamento che si ha in ambito ospedaliero
76
- la presenza di infezione cronica pre-esistente o di condizione di immunodepressione
- la presenza di ascessi o cateteri intravascolari che possono frequentemente portare
allinterno dellorganismo (nel sangue) patogeni
- le procedure invasive a livello respiratorio (come intubazioni)
Inoltre i batteri che causano infezioni nosocomiali spesso hanno acquisito antibiotico-
resistenza nellambito ospedaliero e spesso vanno ad instaurarsi su pz gi debilitati:
questo spiega perch le infezioni nosocomiali siano un reale problema sanitario che
frequentemente pu portare anche a morte.
Gli agenti eziologici pi comuni sono: batteri gram (enterobatteri gram-,
pseudomonas, legionella) e Staphylococcus aureus.
5d. Polmonite da aspirazione
Si verifica in pz molto debilitati, che hanno riflessi della deglutizione anormali, per:
- aspirazione di contenuto gastrico dovuta a stato di incoscienza (coma, ictus,
anestesia)
- episodi di vomito ripetuti
La polmonite viene ad essere contemporaneamente:
- chimica effetto estremamente irritante del succo gastrico acido sul polmone
- batterica contaminazione da parte della flora batterica orale (organismi
anarerobi)
In entrambi i casi la polmonite causa rapida necrosi e il suo decorso clinico pu essere
fulminante o causare, nei soggetti che sopravvivono, formazione di ascessi.
5e. Ascesso polmonare
Processo suppurativo locale del polmone, caratterizzato principalmente dalla presenza
di necrosi purulenta del parenchima polmonare.
Eziologia e patogenesi
Le cause pi comuni associate ad ascesso polmonare sono:
- aspirazione di materiale infetto motivazioni viste precedentemente. pi
frequente nel polmone dx (bronco principale dx pi verticale) ed spesso singola.
Gli agenti eziologici sono organismi anaerobi, normalmente commensali del cavo
orale.
- Infezioni batteriche precedenti generalmente da S. Aureus, Klebsiella
Pneumoniae o pneumococchi. Sono pi facili nei soggetti sottoposti a trapianto o
immunodepressi. Sono di solito ascessi basali e diffusi.
- Embolia settica emboli settici provenienti da tromboflebiti o da endocardite
batterica del cuore dx. Sono generalmente ascessi numerosi (embolia ricorrente)
che possono interessare qualsiasi zona del polmone.
- Neoplasia nella zona a valle dellostruzione neoplastica (polmonite
postostruttiva).
- Miscellanea trauma diretto penetrante dei polmoni; diffusione per contiguit di
infezioni extra-polmonare; disseminazione ematogena al polmone di germi piogeni.
Morfologia
- lesioni di alcuni mm-6 cm che interessano qualsiasi parte del polmone, singole o
numerose.
- Si ha necrosi purulenta della zona centrale dellascesso e infiltrazione essudativa di
neutrofili e detriti suppurativi nellintorno.
77
- Se c comunicazione con una delle vie aeree lessudato purulento pu essere
parzialmente drenato creando una cavit piena di aria
- Se linfezione persiste si ha formazione di cavit grandi, fetide, di colore verde-
nerastro, con scarsa demarcazione dei margini (gangrena polmonare).
- Facile colonizzazione da parte di infezioni saprofitiche.
Clinica
- tosse con abbondante escreato fetido purulento o ematico
- febbre, dolore toracico, calo ponderale
- ippocratismo digitale di mani e piedi entro alcune settimane adllesordio
La diagnosi clinica e confermata da rx.
Dopo la diagnosi importante escludere la presenza di carcinoma sottostante,
presente nel 10-15% dei casi.
6. Pleura
Linteressamento patologico della pleura pu essere:
- secondario alla presenza di malattie sottostanti : occasionalmente la patologia
pleurica viene ad avere ruolo dominante nelle manifestazioni cliniche polmonite
batterica che provoca empiema
- primitivo: principalmente dovuto a
infezioni batteriche intrapleuriche primitive batteriemia transitoria che nel suo
passaggio viene ad interessare solo la pleura come focus isolato
neoplasie primitive della pleura mesotelioma
6a. Versamento pleurico
Manifestazione frequente di molte patologie polmonari, primitive o secondarie.
Normalmente il liquido pleurico costituito da non pi di 15ml di siero chiaro,
relativamente acellulare.
Il versamento pleurico pu essere:
a) infiammatorio
b) non infiammatorio
VERSAMENTI PLEURICI INFIAMMATORI
Sono le cosiddette pleuriti:
sierosa
siero-fibrinosa
fibrinosa
che riflettono la formazione di essudato infiammatorio precoce (sierosa) o
relativamente pi tardiva (fibrinosa) nella cavit pleurica.
Le cause pi comuni sono le malattie infiammatorie polmonari bronchiectasie,
infarto polmonare, polmonite, ascesso polmonare, tubercolosi
Anche alcune malattie sistemiche che interessano secondariamente il polmone possono
provocare pleurite sierosa o siero-fibrinosa lupus eritematoso, srtrite reumatoide,
infezioni sistemiche diffuse, interessamento metastatico della pleura.
Laccumulo di grandi quantit di liquido pu determinare compressione polmonare.
78
Un caso particolare lempiema: essudato pleurico purulento dovuto a disseminazione
batterica o micotica della cavit pleurica, per diffusione dei microrganismi da contigua
infezione intrapolmonare.
caratterizzato da raccolta di pus saccata (localizzata a formare dei sacchi), giallo-
verdastra, cremosa, formata da neutrofili associati ad altri leucociti.
Lempiema pu risolversi ed essere riassorbito, ma pi facilmente si avr
organizzazione dellessudato e formazione di aderenze fibrose dense ridotta
espansione polmonare
Un altro caso particolare rappresentato da pleurite emorragica, poco frequente ed
associata a diatesi emorragiche (deficit generale della cascata della coagulazione),
nelle rickettsiosi e nellinteressamento neoplastico del cavo pleurico.
Si tratta di unessudazione siero-ematosa ad origine infiammatoria e non di un
emotorace.
VERSAMENTI PLEURICI NON INFIAMMATORI
Idrotorace
Raccolta non infiammatoria di liquido sieroso, chiaro, di colore paglierino, nella cavit
pleurica.
La causa pu essere:
- aumento della pressione idrostatica insufficienza cardiaca congestizia che
provoca prima edema polmonare e dunque idrotorace
- Diminuzione della pressione osmotica sindrome nefrosica ( escresione di
proteine plasmatiche) o cirrosi epatica ( sintesi proteine plasmatiche) che causano
edema generalizzato e dunque idrotorace.
La raccolta di liquido di solito non saccata, ma diffusa alle regioni basali, quando il
pz in posizione ortostatica.
Vi compressione ed atelettasia (incompleta espansione del polmone) nelle regioni
adiacenti al versamento.
Se la causa si risolve, lidrotorace si riassorbe senza reliquati
Emotorace
Fuoriuscita non infiammatoria di sangue entro la cavit pleurica.
complicanza fatale di aneurisma aortico o trauma vascolare.
La risposta infiammatoria generalmente assente perch la morte subentra in
minuti-ore.
Chilotorace
Raccolta non infiammatoria di liquido lattesecente, per la presenza di grassi finemente
emulsionati, nella cavit pleurica.
Le cause principali sono:
- traumi del dotto toracico
- ostruzione dei principali dotti linfatici (neoplasie che si formano nella cavit
toracica e che comprimono i dotti) con loro conseguente rottura.
6b. Pneumotorace
Il termine pneumotorace si riferisce alla presenza di aria o gas nelle cavit pleuriche.
Pu essere:
79
- spontaneo
- spontaneo idiopatico
- traumatico
- terapeutico
PNEUMOTORACE SPONTANEO
Pu essere la complicanza di qualsiasi malattia polmonare che vede rottura di un
alveolo.
pi frequente se vi sono cavit ascessuali che comunichino con lalveolo e con lo
spazio pleurico.
Frequentemente associato anche ad asma, enfisema, tubercolosi.
Il riassorbimento dellaria lento, se le comunicazioni si chiudono spontaneamente
PNEUMOTORACE SPONTANEO IDIOPATICO
Si presenta di solito in soggetti relativamente giovani, ed probabilmente dovuto alla
rottura di piccole bolle periferiche subpleuriche ed apicali; la regressione spontanea
ed il riassorbimento dellaria pi rapido.
PNEUMOTORACE TRAUMATICO
Causato da lesioni perforanti la parete toracica che possono:
- non attraversare il polmone una via di ingresso dellaria alle cavit pleuriche
- attraversare il polmone due vie di ingresso dellaria alle cavit pleuriche
Il riassorbimento dellaria lento, se le comunicazioni si chiudono spontaneamente
Clinica: compressione, atelettasia, fino al marcato collasso polmonare importante
distress polmonare.
In particolare se il difetto che provoca pneumotorace consente lingresso di aria
nellinspirazione e non consente la fuoriuscita di aria nellespirazione si ha importante
distress polmonare.
In particolare se il difetto che provoca pneumotorace consente lingresso di aria
nellinspirazione e non consente la fuoriuscita di aria nellespirazione si ha
progressivo della quantit di aria e della pressione intrapleurica. Si parla di
pneumotorace iperteso e questo pu comprimere le strutture vitali mediastiniche e
laltro lobo polmonare.
6c. Neoplasie della pleura
Solitamente secondarie a metastasi ( di solito da tumori primitivi del polmone o della
mammella)
Fra le primitive riscontriamo solo la presenza di
1. tumori fibrosi solitari localizzati
2. mesotelioma
TUMORI FIBROSI SOLITARI LOCALIZZATI
Sono tumori benigni del connettivo che hanno come sede preferenziale di insorgenza la
pleura e meno comunemente il polmone o altri organi.
Sono tumori circoscritti e delimitati, che tendono a rimanere limitati alla spf
polmonare.
80
Possono essere piccoli o di dimensioni enormi, ma generalmente non causano
versamento pleurico.
Morfologia macroscopica: noduli di tessuto fibroso denso, con occasionali cisti piene di
liquido viscoso
Morfologia microscopica: rete di fibre reticolari e collagene tra le quali cellule fusate
simili a fibroblasti
Immunoistochimica: CD34+, cheratina-
MESOTELIOMA MALIGNO
Rari tumori maligni che originano dalla pleura viscerale o parietale.
La loro incidenza:
- molto aumentata in persone con esposizione cronica allasbesto
- non ulteriormente aumentata in seguito ad esposizione allasbesto sommata a
fumo di nicotina, a differenza del carcinoma polmonare correlato allasbesto, la cui
incidenza molto aumentata dal fumo.
un tumore molto diffuso e molto esteso nella cavit pleurica, che dunque quasi
sempre associato a versamento pleurico.
Invade direttamente le strutture toraciche (polmone soprattutto) e metastatizza con
facilit ai linfonodi ilari, dunque al fegato e ad altri organi a distanza.
Morfologia
Macroscopica:
- il polmone interessato avvolto da spesso strato di tessuto tumorale soffice,
gelatinoso, grigiastro.
Microscopica:
nella loro perdita di differenziazione le cellule mesoteliali hanno la possibilit di
svilupparsi in due modi:
- cellule di rivestimento simil-epiteliali predominano nel tipo epitelioide di
mesotelioma
- cellule mesenchimali stromali predominano nel tipo sarcomatoide di
mesotelioma
Tipo epitelioide:
cellule colonnari, cubiche o appiattite epiteliali che formano strutture tubulari o
papillari simili alladenocarcinoma.
La DD con ladenocarcinoma polmonare si fa perch le cellule del mesotelioma
presentano:
1. Alla colorazione immunoistochimica:
positivit per il mucopolisaccaride acido
negativit per Ag glicoproteici epiteliali generalmente espressi dal ca polmonare
positivit molto forte per la cheratina (DD con tumori fibrosi solitari localizzati)
2. Alla microscopia elettronica (glod standard
Cellule con lunghi microvilli ed abbondanti tonofilamenti, prive di corti microvilli
e corpi lamellari
Tipo sarcomatoide:
aspetto di sarcoma a cellule fusate, simile al fibrosarcoma
81
Clinica
Esordio clinico: dolore toracico, dispnea, versamenti pleurici ricorrenti.
Asbestosi (fibrosi) polmonare concomitante nel 20% dei casi.
Morte del 50% dei pz entro 1 anno dalla dg e della quasi totalit entro i 2 anni.
82
Neoplasie dellesofago
Generalit
Lesofago rappresenta la porzione del tubo digerente che congiunge lorofaringe con lo
stomaco e serve a veicolare il materiale deglutito dentro a questo ultimo.
La mucosa esofagea caratterizzata da due tipi di epitelio:
I 2/3 superiori sono tappezzati da un epitelio squamoso pluristratificato non
cheratinizzante
Il 1/3 inferiore presenta un epitelio colonnare specializzato
Le neoplasie che possono colpire questo tratto sono fondamentalmente di tre tipi:
Carcinoma squamoso: con origine dallepitelio nativo
Adenocarcinoma: con origine dalle ghiandole del 1/3 inferiore
Tumori della muscolatura liscia della tonaca muscolare o dei vasi
Carcinoma squamoso
Sono i tumori esofagei pi frequenti e coprono il 90% delle neoplasie dorgano anche se
ultimamente stanno cedendo il passo agli adenocarcinomi che sono, quindi, in forte
ascesa.
Colpisce prevalentemente maschi oltre la 5 decade di et.
Anche in questo caso come in tanti altri esiste il concetto di precancerosi, esistono
lesioni che precedono la neoplasia conclamata che, se tempestivamente riscontrate,
possono essere trattate e prevenire linsorgenza del tumore.
Il problema la diagnosi precoce visto che non usuale effettuare unendoscopia di
controllo e, spesso, sia le lesioni precancerose che le neoplasie a stadi iniziali vengono
osservate in corso di endoscopia per gastrite da H. Pylorii o per altri problemi correlati
allo stomaco.
Questo tumore ha unalta incidenza nel Nord Italia e nel Nord della Francia, in Cina
(a causa del consumo frequente di cibi bollenti), in Sud Africa e nel Sud del Brasile.
Fattori predisponenti
Abuso di alcool
Tabagismo
Fattori ambientali
Abuso di bevande calde
HPV (20-40%) riscontrato per ora solo in Cina dove, in questi casi, la malattia
conseguente a una condilomatosi esofagea.
83
Precancerosi
Le avvisaglie di una neoplasia in atto di sviluppo sono due:
Neoplasia intraepiteliale: espandendosi via via a tutto lepitelio da origine al
carcinoma squamoso
Iperplasia delle cell basali: pu assomigliare a una displasia di basso grado
dellepitelio squamoso in realt una cancerogenesi che porta al carcinoma
basalioide e che si pu verificare anche a livello del canale anale. Inoltre questa
patologia fa parte delle cos dette neoplasie head & neck che danno numerose
metastasi che provocano tumefazioni laterocervicali per interessamento
omolaterale dei linfonodi di quella zona.
Morfologia
Si manifesta inizialmente come lesione in situ localizzata:
20% nel terzo superiore
50% nel terzo medio
30% nel terzo inferiore
Nel corso degli anni la neoplasia si espande fino ad abbracciare lintero lume del
viscere con tre diverse modalit:
Forma esofitica (60%): lesione polipoide protrude nel lume.
Forma piatta (15%): crescita intramurale che comporta ispessimento della
parete esofagea.
Forma ulcerata (25%): lesione necrotica si escava interessando le strutture
adiacenti (aorta,vie respiratorie, mediastino)
Spesso la diagnosi posta quando la massa gi di entit notevole, ha gi invaso le
strutture adiacenti e ha dato metastasi ai linfonodi cervicali, mediastinica,
paratracheali
Fenotipo
P53 il suo gene viene spesso riscontrato soggetto a mutazioni puntiformi.
Gene p16 metilato gene che in questa forma spinge la cell alla proliferazione,
si riscontra specialmente negli adenomi del colon
Ciclina D1
EGF Receptor il recettore per il fattore di crescita epiteliale e si riscontra
anche nelle neoplasie del polmone e della mammella. La
sovraespressione di questo recettore rende la malattia
particolarmente sensibile al farmaco Iressa (Cetuximab)
Clinica
Lesordio insidioso visto che solo in fase avanzata causa disfagia e occlusione.
84
Linconscio adattamento a uninsufficiente nutrizione porta a calo ponderale e
debolezza.
Spesso si osserva aspirazione di cibo nelle vie respiratorie a causa di fistole tracheo-
esofagee prodotte dal tumore.
Lo screening e il miglioramento degli interventi di resecazione hanno contribuito a un
miglioramento della prognosi a 5 anni; la presenza di metastasi linfonodali riduce
drasticamente la sopravvivenza.
Adenocarcinoma della giunzione esofago-gastrica
Come precedentemente detto questa patologia in forte ascesa specie nei paesi
occidentali.
Patogenesi
A livello dello sfintere esofageo inferiore dove c il passaggio da epitelio squamoso a
epitelio colonnare (linea Z) capita spesso di osservare una metaplasia dovuta spesso
alla presenza di una patologia da reflusso (GERD). Da queste metaplasia parte spesso
la cancerogenesi.
I pz affetti da esofago di Barrett hanno il 10% di possibilit di sviluppare un
adenocarcinoma.
Pu anche capitare che, nellinfezione da H.Pylorii si instauri una gastrite cronica che
porti a un ripetuto reflusso che causa, prima, displasia e poi carcinomatosi.
Fattori predisponenti
Esofago di Barrett
Tabagismo
Obesit
Infezione da H. Pylorii
Esofago di Barrett
Il reflusso di materiale gastrico in esofago la principale causa di esofagite.
Normalmente una GERD dovuta, per esempio, a unernia iatale colpisce normalmente
gli adulti ma ultimamente si riscontrato che in molti bambini, addirittura in et
neonatale, gi presente questa patologia.
La GERD pu causare dolori che mimano un infarto e si pensa che questi dolori
toracici siano alla base di una buona parte dei pianti notturni dei neonati che spesso
passano mettendoli seduti e dando loro un bicchiere dacqua.
Se linsulto alla mucosa esofagea dovuto al reflusso cronicizza si instaurano delle
lesioni che possono arrivare fino allesofago di Barrett.
85
Questa patologia colpisce il 10% degli affetti da reflusso cronico ed il principale
fattore di rischio per lo sviluppo di un adenocarcinoma.
Nellesofago di Barrett lepitelio squamoso distale sostituito da epitelio cilindrico
metaplastico in risposta ai prolungati stimoli lesivi.
La diagnosi si basa su:
1. Evidenza endoscopica di epitelio cilindrico al di sopra della giunzione gastro-
esofagea con area di mucosa a fiamma costituita da linguette rosa salmone che
dalla linea Z si portano cranialmente.
2. Evidenza istologica di metaplasia intestinale nei campioni bioptici con le tipiche
ghiandole presentanti le globed cell e cell simili a enterociti con caratteristiche
assorbenti.
Allanalisi istologica possibile determinare un grado di displasia delle cell osservate
con cell a basso grado di displasia che presentano un nucleo basale e cell ad alto grado
di displasia che presentano nucleo apicale.
Nel 50% degli esofagi di Barrett ad alto grado displasico anche riscontrato un
adenocarcinoma!
I fattori predisponenti sono:
Sali biliari
Enzimi pancreatici
Predisposizione genetica
Lesofago di Barrett suddiviso in tre sottotipi:
Long Barrett (LSBE): si estende cranialmente di oltre 3cm sopra la linea Z
Short Barrett (SSBE): si estende non oltre i 3cm
Very Short Barrett (VSSBE): si estende non oltre 1cm
La clinica consta di frequente pirosi spesso accompagnata da rigurgito accompagnata
da stenosi e da sanguinamenti dovuti ad ulcerazioni.
Morfologia
I tipi di metaplasia che possono portare alladenocarcinoma sono due:
Metaplasia colonnare gastrica specie in zona cardiale o fundica
Metaplasia colonnare intestinale specializzata derivante dallesofago di Barrett.
In questo caso quando le ghiandole assumono laspetto schiena a schiena
siamo gi in presenza della neoplasia.
Fenotipo
Dal punto di vista del profilo molecolare sono molto importanti le citocheratine (CK).
Normalmente la CK7 espressa nelle ghiandole mentre la CK20 espressa a livello
intestinale.
86
Da questo si osserva che:
CK7 se riscontrata in esofago patognomonica dellesofago di Barrett
CK20 patognomonica della metaplasia intestinale cardiale
Inoltre..
Traslocazione nucleare della -catenina
Amplificazione di p53 in risposta al continuo insulto al genoma nelle displasie
e sua mutazione nella neoplasia.
Tetraploidia e aneuploidia
Clinica
I pz presentano difficolt a deglutire, calo ponderale, sanguinamento, dolore toracico,
vomito e pregressa sintomatologia da esofago di Barrett.
La prognosi infausta ma la sopravvivenza migliora in caso di resezione precoce.
A questo proposito bene tener conto della collocazione della neoplasia per lo
svolgimento delloperazione.
La porzione esofagea sopracardiale ha un drenaggio linfatico intratoracico mentre la
zona cardiale e la giunzione gastro-esofagea hanno un drenaggio intraddominale; ci
comporta due diverse tecniche di rimozione dellesofago e dei linfonodi coinvolti che
comportano diversi rischi.
Diagnosi
Ultimamente si effettuano endoscopie a scopo di screening su pz affetti da esofago di
Barrett ma la diagnosi resta comunque difficile per diversi motivi:
Difficolt dindagine del fondo dello stomaco per la sua risalita verso lalto; da
ci ne pu derivare unindagine cardiale parziale.
La neoplasia o il Barrett possono essere ricoperti da normale epitelio squamoso
e quindi sfuggire allosservazione dellendoscopista.
87
Malattie non neoplastiche dello stomaco
Gastrite
E linfiammazione della mucosa gastrica che pu essere acuta o cronica.
La diagnosi istologica!
Le gastriti possono essere classificate in diversi modi, il primo criterio basato
sullentit dellinfiltrato:
Quiescenti: infiltrato di tipo cronico costituito da plasmacellule e monociti, non
sono presenti granulociti
Attive: in questo caso sono presenti granulociti che aggrediscono lepitelio
Un altro tipo di classificazione riguarda le modificazioni strutturali che subisce la
mucosa in seguito al processo flogistico:
Semplici: se la flogosi non incide sullarchitettura
Atrofiche: se la flogosi determina atrofia con diminuzione dellepitelio, aumento
dello stroma e conseguente perdita delle pliche allesame macroscopico
Importante ricordare in fine la divisione in gastrite acuta e gastrite cronica che spesso
racchiude in due grandi gruppi i criteri sopraelencati.
Gastrite acuta
E un processo infiammatorio acuto della mucosa gastrica, spesso transitorio.
Le forme pi gravi possono presentare erosione della mucosa con emorragia acuta
gastrointestinale.
Patogenesi
Non ancora ben chiara ma spesso associata a:
Uso di FANS
Abuso di alcool
Tabagismo
Stress intenso
Traumi meccanici o termici
Si pensa che alla base del danno vi sia unipersecrezione di acido troppo grande per
essere tamponata dal muco che viene distrutto con conseguente danno diretto
allepitelio.
Questi problemi si associano a ischemia, a reflusso di materiale dal duodeno,
insufficiente produzione di prostaglandine. Una quota di questa patologia resta ancora
di natura idiopatica.
88
Morfologia
Nelle forme lievi la lamina propria risulta edematosa e si riscontrano neutrofili tra le
cell epiteliali o nei lumi delle ghiandole mucose; la loro presenza non normale a
questo livello perci, una volta individuati si pu fare diagnosi di gastrite.
Nei casi peggiori si pu arrivare a unerosione della mucosa che non va, chiaramente,
mai oltre la muscolaris mucosae; in questi casi possibile riscontrare emorragie.
Clinica
Pu essere asintomatica o presentarsi con un corteo di sintomi come
Dolore epigastrico sx
Nausea e vomito
Emorragia franca con ematemesi e melena
Gastrite cronica
Definita dalla presenza di alterazioni infiammatorie croniche della mucosa che
conducono ad atrofia della mucosa e a metaplasia intestinale di solito in assenza di
erosioni.
Le displasie che si vengono a formare in questa condizioni possono essere linizio dello
sviluppo di un processo carcinomatoso.
Patogenesi
Questa patologia si associa a
Infezione cronica da H. Pylorii
Patologie autoimmuni
Tossici come alcool e fumo di sigaretta
Postumi di interventi chirurgici
Patologie della motilit
Radiazioni
Malattie granulomatose
Infezione cronica da H. Pylorii (antro dello stomaco)
Questo patogeno il maggior responsabile delle gastriti attive ed presente nel 90%
delle gastriti croniche e nella maggioranza dei casi la patologia asintomatica.
Questi pz hanno aumentato rischio di sviluppare ulcera peptica e cancro gastrico (tipo
Cag 1) anche se questo batterio, allinterno della patologia neoplastica dello stomaco,
esplica il suo ruolo di maggior rilevanza nello sviluppo di LZME gastrico.
Dopo linfezione la gastrite pu presentarsi in 2modi:
Gastrite a predominanza antrale con ipersecrezione di acido con rischio di
ulcera duodenale
Gastrite atrofica multifocale con bassa secrezione acida e rischio di sviluppare
adenocarcinoma
89
Di solito i pz migliorano in seguito a terapia antibiotica e vengono trattati anche con
inibitori della pompa protonica.
Gastrite autoimmune (corpo dello stomaco)
Rappresentano meno del 10% dei casi di gastrite cronica.
Si riscontrano Ig anti-cell parietali delle ghiandole gastriche.
Sviluppandosi prevalentemente a livello del corpo dello stomaco, oltre a inibire la
secrezione acida, deprime anche quella di fattore intrinseco con diminuzione
dellassorbimento di B12 e conseguente anemia perniciosa.
Come spesso accade queste patologie si associano ad altre patologie di tipo
autoimmune.
Morfologia
Pu colpire diverse zone dello stomaco, per es, la gastrite da H. Pylorii colpisce
prevalentemente lantro mentre quella autoimmune il corpo.
La mucosa si presenta arrossata con trama pi grossolana del solito.
Le alterazioni istologiche sono simili con infiltrato infiammatorio formato da linfociti e
plasmacellule nella lamina propria. Se si tratta di una flogosi attiva vi anche la
presenza di neutrofili.
Vi sempre rigenerazione in risposta al danno specie a livello del colletto delle
ghiandole. Si osservano alterazioni rigenerative marcate.
Si pu osservare metaplasia intestinale che sorge in risposta allaumento del pH.
Queste cell intestinali derivano dalle cell staminali presenti nella mucosa gastrica che
possono riprodurre qualsiasi tipo di cell del tratto gastrointestinale. Se, a causa della
diminuita secrezione gastrica, il pH sale verso 5-6 le cell staminali differenziano verso
quelle cell del tratto gastrointestinale che normalmente vivono in un microambiente
analogo ovvero gli enterociti. Queste cell metaplastiche intestinali hanno, come gli
enterociti veri e propri, maggiori capacit assorbenti con le quali assorbono i
cancerogeni immessi con la dieta peggiorando la situazione.
Latrofia un altro aspetto ricorrente. Deriva dal depauperamento delle strutture
ghiandolari ed spesso associato a gastrite autoimmune o da H. pylorii. Per
compensare la diminuita secrezione gastrica si verifica uniperplasia delle cell G
secernenti gastrina.
E importante ricordare che la secrezione acida dello stomaco uccide la gran parte dei
batteri e inattiva i cancerogeni che noi immettiamo col cibo perci, se diminuisce
lacidit gastrica, aumentano i tossici assimilabili e, unito al potere assorbente della
metaplasia intestinale, come gi detto, si capisce come vengano assorbiti pi
cancerogeni!
La displasia si manifesta col perdurare dello stimolo infiammatorio; le cell proliferanti
e/o metaplastiche cominciano a presentare alterazioni della normale morfologia che
90
possono facilmente evolvere in un carcinoma in situ. Per questo motivo la displasia,
che spesso segue la metaplasia, considerata lesione precancerosa.
Da notare che H. Pylorii sempre assente nei focolai di metaplasia intestinale ma pu
colonizzare i focolai di metaplasia pilorica nel duodeno; questo testimonia il suo
tropismo per la mucosa gastrica.
Clinica
Spesso la gastrite cronica asintomatica oppure si manifesta con vomito, nausea e
disturbi epigastrici.
Nei casi di grave perdita di cell parietali si pu arrivare a uno stato di ipocloridria o
acloridria con gastrinemia elevata.
Ulcera peptica
Dal punto di vista istologico una soluzione di continuo della mucosa del tubo
digerente che, attraversando la muscolaris mucosae, approfonda fino alla sottomucosa
e oltre.
Le ulcere peptiche duodenali e gastriche sono le pi comuni!
Lulcera peptica una lesione cronica, che non supera i 4cm di diamtetro,
generalmente singola, che pu interessare qualunque zona del digerente esposta
allazione dei succhi gastrici (peptici).
Le porzioni pi frequentemente coinvolte sono la prima porzione del duodeno e lantro
gastrico.
Nonostante la guarigione sono facili recidive dovute a infezioni croniche da H. Pylorii.
Patogenesi
Questa patologia deriva da uno squilibrio tra le difese della mucosa e gli agenti
digestivi, in particolare acido cloridrico e pepsina.
Non quasi mai necessaria uniperacidit bens basta uninsufficienza delle difese
della mucosa.
91
Malattie tumorali e simil-tumorali dello stomaco
Tumori benigni
Polipo: qualunque nodulo o massa che sporga che sporga al di sopra della superficie
della mucosa circostante.
Normalmente si sviluppano dalla mucosa ma possono essere anche lipomi o leiomiomi.
Morfologia
I polipi gastrici sono rari e come gli altri polipi del tratto gastroenterico si dividono in
neoplastici e non neoplastici.
Il 90% dei polipi gastrici sono non neoplastici e, quindi, di natura iperplastica.
Questi polipi sono composti in diverse proporzioni da epitelio iperplastico e ghiandole
con dilatazione cistica.
Lepitelio pu essere in rigenerazione in seguito a flogosi o erosione.
Il tipico polipo iperplastico si presenta come una piccola lesione sessile a livello
dellantro; nel 25% dei casi raggiungono il considerevole numero di 20.
Le lesioni neoplastiche polipoidi consistono negli adenomi gastrici che in s presentano
displasie e quindi un certo potenziale di malignit; costituiscono il 5-10% delle lesioni
polipoidi dello stomaco.
Questi adenomi si possono presentare in due forme:
Sessili
Peduncolati
Anche queste lesioni si manifestano principalmente a livello dellantro e sono, di
norma, singole.
In alcuni casi la massa adenomatosi pu interessare superficialmente ed estesamente
la mucosa senza, perci, presentare masse.
Clinica
I polipi iperplastici sono associati spesso a una gastrite cronica e, nonostante siano
presenti nel 20% dei casi di carcinoma, non si considerano potenzialmente maligni ma
solo una conseguenza della gastrite come anche il carcinoma stesso.
Gli adenomi sono associati a un quadro di gastrite cronica con metaplasia intestinale.
Lincidenza di questa patologia aumenta con let, specie dalla 7 decade e,
preferenzialmente nel sesso maschile.
Siccome con lendoscopia non si possono distinguere polipi iperplastici da adenomi
sempre indicata la biopsia!
92
Carcinoma gastrico
Da queste parti, nellAppennino tosco-emiliano in particolare, il carcinoma gastrico era
molto frequente e, fino alla fine degli anni 70, era la principale causa di morte per
tumore.
Al giorno doggi la sua incidenza, a contrario della maggior parte dei tumori, calata e
questo dovuto alla dipendenza di questa malattia da ben determinati fattori
ambientali.
Fino a qualche decennio fa era abitudine bere lacqua prelevata dai pozzi che, per,
veniva contaminata dai fertilizzanti usati nei campi.
In questo modo gli abitanti di queste zone ingerivano ogni giorno uningente quantit
di nitriti e nitrati che sono potenti cancerogeni.
Associato a ci cera anche il fatto che H. Pylorii era endemico negli appennini.
I due fattori addizionati contribuivano alla drammatica incidenza di neoplasia
maligna gastrica.
Al giorno doggi labbandono di queste abitudini e lintroduzione dello screening
mediante endoscopia ha migliorato di molto lincidenza.
Patogenesi
Il quadro di partenza quello gi trattato della gastrite cronica, in particolare quella
provocata dallinfezione da parte di H. Pylorii.
I processi patologici della gastrite portano in diversi casi a metaplasia intestinale che
pu essere:
Completa con anche la presenza delle cell di Paneth
Incompleta senza cell di Paneth
Arrivati a un certo punto si instaura un processo di iperplasia delle ghiandole
metaplastiche intestinali e questa la vera e propria fase di promozione neoplastica.
Durante la moltiplicazione delle cell ghiandolari si accumulano atipie e mutazioni che
consistono principalmente nellalterazione del rapporto nucleo/citoplasma. Questo
oramai conclamato processo displastico ormai inevitabilmente indirizzato verso una
situazione carcinomatosa.
Per questo motivo i pz con gastrite cronica e metaplasia intestinale devono essere
seguiti con indagini endoscopiche e bioptiche periodicamente.
Morfologia
Il carcinoma dello stomaco pu essere diviso principalmente secondo due criteri, il
primo la distinzione secondo Lauren che li cataloga dal punto di vista biologico:
Intestinale: deriva dalla metaplasia intestinale e quindi insorge in un quadro di
pregressa gastrite cronica; per questo motivo prevedibile con lo screening
Indifferenziato diffuso: insorge inaspettatamente e indipendentemente da ogni
fattore, per questa sua imprevedibilit ha unalta mortalit, la sua peculiarit
sono le cos dette cell con castone ovvero cell mucoide immature che non
riescono a espellere il muco prodotto dal proprio citoplasma.
93
La seconda divisione basata sullo stadio della malattia:
Precoce: pu presentarsi quando ancora confinato alla mucosa (metastatizza
nell1% dei casi) o pu avere gi passato la muscolaris mucosae ed essere
arrivato nella sottomucosa (metastatizza nel 4-5% dei casi).
Avanzato: in questo caso la malattia si presenta che arrivato fino alla tonaca
muscolare o, addirittura, fino alla sierosa (metastatizza nel 40% dei casi).
Tecnicamente si dovrebbe usare la stadiazione TNM ma nella pratica non si usa
perch le due tipologie di cancro presentano aspetti macroscopici molto diversi tra loro.
Le lesioni precoci possono essere:
Polipoidi
Piatte:
- Rilevate, possono simulare un polipo non precanceroso
- Piatte, difficili da vedere allendoscopia ma si osservano con attenzione per
il loro aspetto a zattera in mezzo al mare visto che la lesione lunica
parte della mucosa a non contrarsi.
- Depresse
Escavate: possono simulare unulcera.
Infine queste lesioni possono infiltrare tutta la parete radialmente e in maniera
superficiale risultando pi difficili da osservare.
Le ulcerazioni del carcinoma gastrico possono essere ricoperte da epitelio sano perci
dopo la fine della terapia con linibitore della pompa protonica e altri farmaci analoghi
necessaria unendoscopia di controllo per accertarsi della scomparsa dellulcera, se
non scompare neoplastica.
Le ulcere da carcinoma avanzato entrano spesso in DD con lulcera peptica e vi sono
tre criteri fondamentali per distinguerla: bordi imbolliti, fondo emorragico e mucosa
atrofica adiacente
A causa delle diverse morfologie di queste lesioni e la possibilit che vengano
camuffate da altre patologie della mucosa si effettuano sempre non meno di 9 prelievi
bioptici in corso di endoscopia anche su una banale ulcera.
Una particolare manifestazione del carcinoma indifferenziato la linite plastica.
Questa forma ha una stadiazione molto avanzata poich le cell con castone hanno
imbottito la totalit della parete gastrica sostituendo tutti i diversi tessuti da cui essa
normalmente costituita. In questi casi la parete dello stomaco pu raggiungere i 3cm
di spessore!
Questa patologia si presenta principalmente nei giovani e la sopravvivenza a 1 anno
<10%, la resezione chirurgica spesso inefficace per la difficolt di lasciare margini
puliti.
Per dimostrare laggressivit delle neoplasie gastriche basti pensare che un polipo
colico che ha infiltrato oltre la membrana basale ma non la muscolaris mucosae
considerato benigno mentre nello stomaco assolutamente no visto che una lesione del
genere gi metastatizzante nell 1-2% dei casi!
94
Sindromi da malassorbimento
Il malassorbimento caratterizzato da un insufficiente assorbimento di:
Grassi
Vitamine liposolubili e non
Proteine
Carboidrati
Elettroliti
Sali minerali
Acqua
Il sintomo pi tipico la diarrea con steatorrea (eccessivo grasso nelle feci).
Alla base di questo malassorbimento vi lalterazione di almeno uno dei seguenti
meccanismi:
Digestione endoluminale: processo di scissione di proteine, grassi e carboidrati
con formazione di molecole assimilabili. Questo processo comincia nella bocca
con la saliva, continua con la digestione peptica gastrica e prosegue
nellintestino con lintervento dei succhi biliari.
Digestione terminale: processo di idrolisi dei carboidrati e dei peptidi ad opera
delle disaccarasi e delle peptidasi a livello dellorletto a spazzola della mucosa
intestinale.
Trasporto transepiteliale: processo di trasferimento di nutrienti, liquidi ed
elettroliti dal lume intestinale al circolo attraverso gli enterociti.
Le sindromi da malassorbimento possono coinvolgere diversi sistemi e apparati:
Tratto gastrointestinale: diarrea dovuta alleccessiva secrezione intestinale con
flatulenza e dolori addominali.
Apparato emopoietico: anemie da deficit di ferro, vit. B12 e folati ed emorragie
da deficit di vit. K
Sistema muscoloscheletrico: osteopenia e tetania da carenza di calcio, magnesio
e vit. D
Sistema endocrino: amenorrea, impotenza e sterilit da malnutrizione
generalizzata; ipeparatiroidismo secondario a deficit di calcio e vit. D
Epidermide: porpore e petecchie da deficit di vit. K, edema da deficit di proteine,
dermatite e ipercheratosi da deficit di vit. A
Sistema nervoso: neuropatia periferica da deficit di vi. B12 e vit. A
I fattori principali responsabili del malassorbimento sono:
Morbo celiaco
Morbo di Crohn
Insufficienza pancreatica (spesso secondaria a pancreatine cronica)
Sovraccrescita batterica
95
Morbo celiaco
E una malattia cronica con caratteristiche lesioni del tenue e deficit da assorbimento
che migliora eliminando dalla dieta la gliadina del grano e le proteine dei cereali
correlate.
Colpisce prevalentemente soggetti di razza caucasica
Patogenesi
Il disturbo primario lintolleranza al glutine che una componente proteica alcool-
solubile ma non idrosolubile del grano e dei cereali affini.
La malattia caratterizzata da una flogosi cronica mediata da linfociti T con aspetti
autoimmuni probabilmente dovuti alla perdita della tolleranza per il glutine.
La patogenesi il risultato di uninterazione tra fattori genetici predisponenti, risposta
immunitaria e fattori ambientali.
Sotto stimolazione data dallingestione di glutine la mucosa intestinale del tenue
accumula T CD8 intraepiteliali e T CD4 nella lamina propria sensibilizzati alla
gliadina. Lipotesi che lattivazione dei linfociti porti alla liberazione dellinterferon
e che, a sua volta, questa sostanza danneggi la mucosa.
I linfociti T CD8 non riconoscono la gliadina e sembra che siano richiamati dal danno a
cui soggetta la parete intestinale.
Morfologia
- Al microscopio si evidenzia unenterite diffusa con ipotrofia o atrofia dei villi.
- Gli enterociti mostrano degenerazione vacuolare e perdita dellorletto a spazzola.
- Le cripte mostrano una certa attivit mitotica con conseguente iperplasia volta a
mantenere lo spessore della mucosa compensando la perdita dei villi.
- La lamina propria risulta infiltrata da cell della serie bianca.
Queste alterazioni colpiscono pi marcatamente il terzo prossimale del tenue.
Clinica
I sintomi variano di molto a seconda del pz: da diarrea nellinfanzia con ritardo della
crescita a sintomi lievi che si manifestano dopo la 5 decade di et.
Il quadro clinico caratteristico comprende:
diarrea e flatulenza
calo ponderale
affaticabilit
I sintomi extraintestinali possono oscurare le manifestazioni intestinali.
96
Diagnosi
Si basa su:
Documentazione clinica di malassorbimento
Biopsia con osservazione delle tipiche lesioni della mucosa
Miglioramento dei sintomi e del quadro istologico dopo depriva ione di glutine z
Ulteriore biopsia dopo stimolo col glutine
Ricerca di anticorpi anti-gliadina e anti-transglutaminasi tissutale
Morbo di Whipple
E una rara patologia causata dal batterio Tropheryma whippelii.
E una malattia sistemica, virtualmente pu coinvolgere qualsiasi organo, ma si
manifesta soprattutto a tre livelli:
Intestino
SNC
Articolazioni
T. whippelii un actinomicete gram+che prolifera nei macrofagi e non evoca
significative risposte immunitarie.
Morfologia
La caratteristica tipica lobliterazione della lamina propria del tenue da parte di
macrofagi rigonfi.
Se non trattata, la patologia, pu arrivare a interessare anche i neutrofili.
I villi assumono un aspetto irregolare e ledema causa un aumento dello spessore della
parete intestinale.
La patologia coinvolge anche i linfonodi mesenterici obliterandoli e facendone derivare
una deposizione di lipidi a livello dei villi.
Clinica
E riscontrata principalmente nei caucasici, nella 4-5 decade con una prevalenza di 10
volte del sesso maschile.
La malattia si presenta con malassorbimento associato a diarrea e calo ponderale.
Il sintomo iniziale lartropatia.
Diagnosi
Si basa sulla dimostrazione dei macrofagi rigonfi e dei microrganismi al loro interno.
La terapia antibiotica ottiene quasi sempre risultati immediati.
97
Malattie infiammatorie intestinali idiopatiche
Le enteriti possono avere, dal punto di vista eziologico, diverse origini:
Da virus
Da farmaci
Ereditarie
Idiopatiche
Due delle principali malattie infiammatorie del tratto intestinale ad origine idiopatica
sono la rettocolite ulcerosa e il morbo di C ohn. r
Queste due patologie, in alcuni casi possono avere caratteri sovrapponibili e,nei casi in
cui non si riesca a porre DD tra le due patologie si parla di coliti indeterminate che
costituiscono in 10% delle patologie idiopatiche del tratto intestinale.
Rettocolite ulcerosa
Interessa i giovani adulti in una fascia di et trai 15 e 30 anni.
Collocazione
Interessa il colon dalla valvola ileo-cecale alle colonne del Morgagni.
Il materiale infiammatorio del ceco pu rifluire nellileo e causare ileite terminale.
Preferibilmente colpisce il colon sx ma pu estendersi causando un quadro di pancolite
ulcerosa.
Eziologia
E correlata ad alcune classi di HLA.
In circolo si riscontrano Ig anti-Ag delle cell epiteliali del colon.
Si correla poi a un stato psicosomatico associato a stress.
Macro
Interessa porzioni continue dellintestino che si pu espandere ma senza lasciare spazi
sani sulla mucosa
La flogosi pu arrivare a interessare al max la sottomucosa.
La parete colica risulta sottile con erosione della mucosa e ulcerazioni.
Istologia
Si evidenzia un infiltrato flogistico linfomonocitario non follicolare che aggredisce le
cripte con accumuli di granulociti (ascessi unicriptici) nelle ghiandole della mucosa.
Clinica
Si manifesta principalmente con dolori addominali e diarrea che risulta mucoematica
per lo sfaldamento della mucosa.
98
Pu simulare colite infettiva autolimitante (colera).
Si associa ad altre malattie autoimmuni come la colangite sclerosante primitiva (6%),
leritema nodoso e alcune artropatie autoimmuni.
Si trovano in circolo Ig anti-ANCA che sono autoanticorpi contro il citoplasma dei
neutrofili.
Complicanze
Acuta: Megacolon tossico; la mucosa del colon si assottiglia fino a pochi mm perch la
malattia ha iniziato a mangiarsi la muscolare.
Tardiva: Cancro, dovuto al continuo stimolo flogistico. Si evidenzia un 10% del rischio
in pi per ogni decennio di malattia.
I pz possono sviluppare polipi adenomatosi simili a una placca piana dovuti alle
alterazioni della mucosa, questi polipi sono pi difficili da vedere e danno meno
sintomi perch si ulcerano molto meno. La difficolt della diagnosi alla base della
prognosi peggiore per i cancri che si sviluppano secondariamente a questa patologia.
Trattamento
Antinfiammatori come aspirina e cortisonici danno unottima risposta con periodi di
benessere lunghi anni prima di una recidiva che spesso si presenta con caratteri pi
gravi.
In presenza di megacolon devono essere operati con rimozione totale del colon e
anastomosi dellileo con lano.
E importante rimuovere tutta la mucosa lesionata perch se si lascia anche solo un
piccolo pezzo questo pu dare un cancro.
Morbo di Crohn
Interessa una fascia det trai 25 e 30 anni.
Collocazione
Pu potenzialmente interessare tutto il tratto gastroenterico dalla bocca allano.
E pi frequente a livello dellileo terminale (ultimi 20cm, ultima ansa).
50% nellileo terminale
50% solo colon o ileo terminale + un altro distretto.
Nel caso colpisca solo il colon necessaria DD con la rettocolite ulcerosa.
Eziologia
NOD2 e CARD15 sono geni correlati alla capacit degli enterociti di sopportare
infezioni batteriche, in particolare la traslocazione dal lume intestinale allenterocita
stesso di batteri non propri della flora intestinale.
99
La malattia trova due grossi fattori scatenanti nella perdita di questi geni e nello
squilibrio della flora batterica.
Una delle ipotesi del momento deriva dallosservazione di un aumento dellincidenza
della malattia nelle zone dove viene utilizzato maggiormente il frigorifero. La
conservazione dei cibi alle T dei frigoriferi selezionerebbe la popolazione batterica sul
cibo stesso uccidendo i microrganismi buoni e mantenendo quelli patogeni.
In particolare si parla di micobatteri atipici che entrerebbero senza ostacoli per la
mancanza di Ag scatenanti flogosi.
Una riprova laspetto macroscopico granulomatosa della malattia che assomiglia ai
granulomi da TBC.
Si osservato anche la patologia favorita dal tabagismo probabilmente perch
stimolerebbe produzione di TNF- ma queste sono tutte ipotesi.
Macro
Colpisce in maniera segmentale (focale) ed interessa tutta la parete; comincia a livelli
profondi e si estende alla mucosa (al contrario della rettocolite ulcerosa).
Il lume risulta ristretto, la parete spessa, la mucosa pu presentare ulcere singole e
lineari che danno il caratteristico aspetto ad acciottolato.
Istologia
Infiltrato flogistico follicolare con cell giganti polinucleate e granulomi che danno
fistole che ulcerano la mucosa.
Si osserva metaplasia pilorica con cell di Paneth ed eosinofili; linfiltrato giunge fino ai
plessi mioenterico e sottomucoso.
Clinica
Si manifesta con dolori addominali e diarrea.
Il dolore si manifesta in fossa iliaca dx e quindi necessaria una DD con patologie
dalla sintomatologia simile come lappendicite.
Si associa a uveiti escleriti.
Complicanze
Fistole con altri organi o con lesterno:
Perianale (le pi frequenti)
Enterovescicali
Enterovaginali
Unaltra complicanza la stenosi dovuta allinspessimento della parete che pu
simulare una neoplasia.
100
Si associa, inoltre, al cancro dellileo e del digiuno (rari) e ai linfomi dei centri
follicolari per il particolare tipo di infiltrato infiammatorio che presenta.
Trattamento
Si usano farmaci specifici come limmunoterapia; Ig anti - TNF- che scatena la
necrosi nel morbo.
Si utilizzano anche probiotici, specie ultimamente si stanno studiando protocolli
terapeutici mirati al ristabilimento della flora intestinale come risoluzione del
problema.
In alcuni casi si interviene chirurgicamente resecando la porzione di intestino malato
lasciando il margine libero.
101
Cirrosi
E tra le prime 10 cause di morte nei paesi occidentali.
Le cause principali sono:
Alcolismo (60-70%)
Epatiti virali (10%)
Idiopatica (10%)
Malattie delle vie biliari (5%)
Come stadio finale dellepatopatia caratterizzata da tre aspetti:
Setti fibro i sottili o sottoforma di vere e proprie cicatrici s
t
Noduli parenchimali contenenti epatociti proliferanti e circondati da fibrosi; le
loro dimensioni variano da pochi mm a qualche cm
Sovvertimento dellintera architettura epa ica
Nel concetto di cirrosi insito che il danno parenchimale sia a carico di tutto il fegato e
non focalizzato in alcuni punti.
La formazione di noduli un requisito diagnostico che testimonia il rapporto tra
rigenerazione epatica e fibrosi costrittiva.
Larchitettura vascolare viene riorganizzata con creazione di anastomosi anomale tra
vasi afferenti ed efferenti; ne deriva un by-pass del sangue arterioso e portale che salta
una quota di epatociti funzionanti grazie a questi circoli patologici.
La fibrosi laspetto chiave del danno epatico; la sospensione dellinsulto lesivo pu
fare regredire la fibrosi anche in stati di cirrosi conclamata grazie alla lenta azione
delle metalloproteasi e delle collagenasi presenti nel fegato.
Patogenesi
Meccanismi patogenetici principali:
Fibrosi progressiva
Riorganizzazione dellarchitettura vascolare
Il collagene di tipo I e III si deposita nel lobulo in tralci sottili o spessi invece che nei
tratti portali e attorno alle vene centrali come nel soggetto sano. Se lo stimolo persiste
la fibrosi aumenta e il collagene si stabilizza con ulteriori legami crociati.
Il collagene, inoltre, si deposita nello spazio di Disse occludendo le fenestrazioni dei
sinusoidi e impedendo, perci, gli scambi metabolici tra epatociti e la messa in circolo
delle proteine plasmatiche.
Leccesso di collagene imputabile alle cell perisinusoidali stellate che, in condizioni
normali, fungono da cell di deposito mentre nella cirrosi si attivano assumendo
caratteristiche di miofibroblasto.
Lattivazione comporta un aumento dellattivit mitotica e una iperproduzione di
matrice extracell.
102
Questa attivazione ad opera delle citochine secrete dalle cell di Kupfer in seguito a
danno epatico.
Unultima osservazione che si pu fare sullattivazione delle cell stellate che,
acquisendo una componente miofibrillare, aumentano la resistenza vascolare nel
parenchima epatico che contribuisce ai problemi circolatori gi in atto in corso di
cirrosi che portano a ipertensione portale e ascite.
Clinica
Tutte le forme possono essere silenti e quando sono sintomatiche causano
manifestazioni aspecifiche:
- Anoressia
- Calo ponderale
- Astenia
- Osteoporosi
- Debilitazione
Si pu sviluppare uninsufficienza epatica incipiente aggravata da sovraccarico
metabolico o da emorragia gastrointestinale.
Sintomi pi peculiari sono:
Ipoalbuminemia con conseguente edema periferico
Iperammoniemia con conseguenti disfunzioni cerebrali
Eritema palmare e angiomi stellati cutanei per alterato metabolismo
estrogenico
Coagulopatie per mancanza di fattori della coagulazione
Sindrome epato-renale per abbassamento della perfusione renale con ritenzione
di Na
Due parole in particolare vanno spese per lipertensione portale derivante da cirrosi,
questa pu scatenare diverse conseguenze:
Ascite: aumento liquido nella cavit peritoneale che si manifesta clinicamente
superati i 500mL di contenuto. Secondariamente causa perdita di liquidi a
livello intestinale per compressione dei capillari intestinali che causa, a sua
volta, iperaldosteronismo con ritenzione di Na e H2O.
Shunt porto-sistemici: provocano emorroidi e varici esofagee e gastriche.
Splenomegalia: dovuta allinsufficiente drenaggio portale.
Gli esami ematochimici evidenziano:
Alterazioni delle colestasi e altri indici di citonecrosi
Diminuzione PLT
Diminuzione colesterolo
Nei casi in cui la cirrosi porti a decesso si osservano tre cause principali:
Insufficienza epatica progressiva
Complicanza correlata allipertensione portale
Sviluppo di carcinomi epatocellulari
103
Epatite acuta
Leziologia di questa malattia varia:
Infezioni virali
Intossicazioni (es. Alcool)
Malattie dismetaboliche (emocromatosi, diabete..)
Malattie autoimmuni
Le due caratteristiche principali dal punto di vista istologico sono:
Necrosi
Infiltrato infiammatorio:
- Linfociti nelle infezioni virali
- Plasmacellule nelle patologie autoimmuni
- Neutrofili nei dismetabolismi
- Macrofagi in ogni quadro.
Si pu quindi avere una rigenerazione con aspetti diversi a seconda di quale sia
lagente lesivo:
Epatociti in mitosi (la rigenerazione avviene ogni 450gg)
Aumento dellattivit dei poli biliari (recupero epitelio biliare)
Fe2+ ed elementi ceroidi nelle cell di Kupfer (rimaneggiamento)
Statosi
Corpi di Mallory: sono accumuli PAS+ a zolle perinucleari o a cerchio sul nucleo
che si evidenziano con 2 Ig monoclonali perch sono ubiquitina+ e p62+
La necrosi pu avvenire:
Per apoptosi: non vi presenza di infiltrato infiammatorio e nellacino rimane il
corpo di Cauciman
Focale a spruzzo: morte di gruppi di 8-10 epatociti (scala a pioli), linfiltrato
linfocitario presente indipendentemente dallagente eziologico. Se il pz
guarisce si ha restituzione della funzione.
A ponte: una necrosi confluente che unisce lo spazio portale alla vena
centrolobulare o a un altro spazio portale. Vi collasso della trama reticolinico
che viene sostituita da trame fibrose che rendono i sinusoidi convoluti. La
liberazione di IL-1 e GF stimola le cell di Ito che fungono da fibroblasti
deponendo matrice.
Panlobulare: una necrosi massiva che colpisce interi acini con importanti
alterazioni del parenchima; questa necrosi tipica dellepatite fulminante da
tossici.
Istologia
Degenerazione balloniforme: considerata borderline. Il nucleo normale
mentre il citoplasma vacuolizzato, presente rigonfiamento diffuso.
Corpo di Cauciman: un corpo eosinofili lungo i sinusoidi, nucleo picnotici che
rimane in seguito ad apoptosi.
Infiltrato flogistico: specialmente a livello portale, responsabile
dellaggressione agli epatociti e induce la necrosi.
104
Diagnosi
E prevalentemente clinica.
Si basa anche sui picchi di transaminasi che sono direttamente proporzionali alla
quota di necrosi.
ES: lepatite da HCV innalza moderatamente le transaminasi e infatti questo virus
causa epatite cronica.
Steatoepatite alcolica e non alcolica (ASH e NASH)
La ASH correlata unicamente allabuso di alcool!
La NASH pu essere collegata a obesit, dislipidemie e diabete di tipo 2; in generale si
associa a tutte quelle condizioni che causano uno squilibrio del metabolismo lipidico!
La caratteristiche sono le medesime nei due casi:
Alterazioni morfologiche
Danno epatocitario necrotico
Infiammazione
Fibrosi (che porta poi a cirrosi)
Le GT aumentano peculiarmente nei danni epatici da alcool e dopo 2 mesi di
astinenza tornano a livelli normali.
La diagnosi si pone dopo tre osservazioni:
Corpi di Mallory
Apoptosi
Statosi
Linfiltrato presenta:
Prevalenza linfocitaria
Neutrofili (responsabili delle zone necrotiche spotty tipiche)
Aumento delle cell di Kupfer (con Fe2+ ed elementi ceroidi)
Aumento fibrosi pericellulare che si forma attorno agli epatociti balloniformi e
si espande verso lo spazio portale e la vena centrolobulare. Per questa
confluenza si ha unalterazione parenchimale con unione dei canali vascolari.
La colorazione PAS evidenzia nuclei glicogenati tipici delle epatopatie dismetaboliche.
Epatite fulminnte
Si parla di epatite fulminante quando linsufficienza epatica progredisce dallinizio dei
sintomi fino allencefalopatia epatica in 2-3 settimane.
Le cause sono:
12% Infezioni virali da HAV o HBV (anche riattivazioni), raramente da HHV.
105
52% Farmaci e intossicazioni chimiche
Altre cause tra cui lingestione della tossina del fungo ammanita phalloides
18% sconosciute
Vi sono poi altre cause abbastanza rare come lischemia epatica, infiltrazione
maligna massiva, malattia di Wilson, ipertermia e la statosi epatica gravidica
acuta.
La giovane et un fattore prognostico positivo.
Morfologia
Le alterazioni morfologiche sono sempre le medesime indipendentemente dallagente
scatenante.
Il fegato pu essere interessato totalmente o a zone casuali con ingenti perdite di
massa che possono ridurre il fegato fino a 500g. In questi casi lorgano si presenta
flaccido, rossastro e con la capsula raggrinzita per la riduzione di taglia.
A livello microscopico vi la completa distruzione epatocitaria che lascia una struttura
reticolare collassata e i tratti portali conservati.
Se il pz muore velocemente allautopsia non risulta quasi nessuna reazione
infiammatoria mentre se sopravvive una settimana si inizia a vedere lattivit
macrofagica di pulizia e linizio di una rigenerazione.
Se il pz supera le prime settimane la rigenerazione a partire dalle cell staminali pu
portare a una guarigione la cui struttura dipende dallentit del danno alla rete
stromale di sostegno.
Clinica
Esordisce con ittero, encefalopatia epatica fetor hepaticus, se si protrae la
sintomatologia pu risultare simile a quella dellepatite acuta.
La mortalit varia dal 25 al 90% in assenza di trapianto.
106
Epatite acuta
Leziologia di questa malattia varia:
Infezioni virali
Intossicazioni (es. Alcool)
Malattie dismetaboliche (emocromatosi, diabete..)
Malattie autoimmuni
Le due caratteristiche principali dal punto di vista istologico sono:
Necrosi
Infiltrato infiammatorio:
- Linfociti nelle infezioni virali
- Plasmacellule nelle patologie autoimmuni
- Neutrofili nei dismetabolismi
- Macrofagi in ogni quadro.
Si pu quindi avere una rigenerazione con aspetti diversi a seconda di quale sia
lagente lesivo:
Epatociti in mitosi (la rigenerazione avviene ogni 450gg)
Aumento dellattivit dei poli biliari (recupero epitelio biliare)
Fe2+ ed elementi ceroidi nelle cell di Kupfer (rimaneggiamento)
Statosi
Corpi di Mallory: sono accumuli PAS+ a zolle perinucleari o a cerchio sul nucleo
che si evidenziano con 2 Ig monoclonali perch sono ubiquitina+ e p62+
La necrosi pu avvenire:
Per apoptosi: non vi presenza di infiltrato infiammatorio e nellacino rimane il
corpo di Cauciman
Focale a spruzzo: morte di gruppi di 8-10 epatociti (scala a pioli), linfiltrato
linfocitario presente indipendentemente dallagente eziologico. Se il pz
guarisce si ha restituzione della funzione.
A ponte: una necrosi confluente che unisce lo spazio portale alla vena
centrolobulare o a un altro spazio portale. Vi collasso della trama reticolinico
che viene sostituita da trame fibrose che rendono i sinusoidi convoluti. La
liberazione di IL-1 e GF stimola le cell di Ito che fungono da fibroblasti
deponendo matrice.
Panlobulare: una necrosi massiva che colpisce interi acini con importanti
alterazioni del parenchima; questa necrosi tipica dellepatite fulminante da
tossici.
Istologia
Degenerazione balloniforme: considerata borderline. Il nucleo normale
mentre il citoplasma vacuolizzato, presente rigonfiamento diffuso.
Corpo di Cauciman: un corpo eosinofili lungo i sinusoidi, nucleo picnotici che
rimane in seguito ad apoptosi.
Infiltrato flogistico: specialmente a livello portale, responsabile
dellaggressione agli epatociti e induce la necrosi.
107
Diagnosi
E prevalentemente clinica.
Si basa anche sui picchi di transaminasi che sono direttamente proporzionali alla
quota di necrosi.
ES: lepatite da HCV innalza moderatamente le transaminasi e infatti questo virus
causa epatite cronica.
Steatoepatite alcolica e non alcolica (ASH e NASH)
La ASH correlata unicamente allabuso di alcool!
La NASH pu essere collegata a obesit, dislipidemie e diabete di tipo 2; in generale si
associa a tutte quelle condizioni che causano uno squilibrio del metabolismo lipidico!
La caratteristiche sono le medesime nei due casi:
Alterazioni morfologiche
Danno epatocitario necrotico
Infiammazione
Fibrosi (che porta poi a cirrosi)
Le GT aumentano peculiarmente nei danni epatici da alcool e dopo 2 mesi di
astinenza tornano a livelli normali.
La diagnosi si pone dopo tre osservazioni:
Corpi di Mallory
Apoptosi
Statosi
Linfiltrato presenta:
Prevalenza linfocitaria
Neutrofili (responsabili delle zone necrotiche spotty tipiche)
Aumento delle cell di Kupfer (con Fe2+ ed elementi ceroidi)
Aumento fibrosi pericellulare che si forma attorno agli epatociti balloniformi e
si espande verso lo spazio portale e la vena centrolobulare. Per questa
confluenza si ha unalterazione parenchimale con unione dei canali vascolari.
La colorazione PAS evidenzia nuclei glicogenati tipici delle epatopatie dismetaboliche.
Epatite fulminnte
Si parla di epatite fulminante quando linsufficienza epatica progredisce dallinizio dei
sintomi fino allencefalopatia epatica in 2-3 settimane.
Le cause sono:
12% Infezioni virali da HAV o HBV (anche riattivazioni), raramente da HHV.
108
52% Farmaci e intossicazioni chimiche
Altre cause tra cui lingestione della tossina del fungo ammanita phalloides
18% sconosciute
Vi sono poi altre cause abbastanza rare come lischemia epatica, infiltrazione
maligna massiva, malattia di Wilson, ipertermia e la statosi epatica gravidica
acuta.
La giovane et un fattore prognostico positivo.
Morfologia
Le alterazioni morfologiche sono sempre le medesime indipendentemente dallagente
scatenante.
Il fegato pu essere interessato totalmente o a zone casuali con ingenti perdite di
massa che possono ridurre il fegato fino a 500g. In questi casi lorgano si presenta
flaccido, rossastro e con la capsula raggrinzita per la riduzione di taglia.
A livello microscopico vi la completa distruzione epatocitaria che lascia una struttura
reticolare collassata e i tratti portali conservati.
Se il pz muore velocemente allautopsia non risulta quasi nessuna reazione
infiammatoria mentre se sopravvive una settimana si inizia a vedere lattivit
macrofagica di pulizia e linizio di una rigenerazione.
Se il pz supera le prime settimane la rigenerazione a partire dalle cell staminali pu
portare a una guarigione la cui struttura dipende dallentit del danno alla rete
stromale di sostegno.
Clinica
Esordisce con ittero, encefalopatia epatica fetor hepaticus, se si protrae la
sintomatologia pu risultare simile a quella dellepatite acuta.
La mortalit varia dal 25 al 90% in assenza di trapianto.
109
Malattie delle vie biliari intraepatiche
Cirrosi biliare primitiva
E una patologia autoimmuni cronica che possiede unevoluzione particolare in quanto
passa attraverso vari stadi allinterno di un concetto globale di epatite cronica
autoimmune e non prevedibile la durata di questi stadi che possono durare fino a 20
anni con una certa latenza della malattia.
Si definisce come una colangite cronica non suppurativa (i neutrofili non sono i primi
mediatori) mentre la maggior parte delle colangiti, di solito, lo .
La pz tipica una donna trai 45 e i 55 anni in piena salute che lamenta prurito
specialmente nelle ore notturne.
il medico di base solitamente prescrive degli antistaminici che danno sollievo per
tre giorni dopodich il prurito si ripresenta
oltre al prurito dovuto ai sali biliari in circolo vi anche la presenza di subittero
nelle sclere e nel frenulo della lingua
la pz lamenta inoltre patologie concomitanti come sclerodermia, tiroiditi croniche
(Hashimoto), morbo celiaco, artrite reumatoidetutte patologie che difficilmente
sfuggono allosservazione.
I valori sierici sono i seguenti:
GOT e GPT nella norma
Aumento di una sola colestasi
GT nella norma per escludere abuso alcolico
AMA nel 90% dei casi
Picco di IgM (mentre di solito sono le IgG quelle alte in questi casi)
Le Ig anti-dotti biliari danneggiano anche altre strutture duttali come le ghiandole
lacrimali, quelle salivari e quelle sudoripare.
La terapia incentrata sulluso dellacido ursodesossicolico che facilita lemuntorio
biliare.
Grado e Stadio
La diagnosi clinica ma la biopsia serve per determinare lo stadio e il grado e per
porre diagnosi nei casi in cui i pz risultino AMA- allIIC.
Il grado, come sempre, si basa sullentit dellinfiammazione in corso, sullinfiltrato,
sul danno cellulare da esso causato e sullentit della fibrosi riparativa.
Gli stadi vanno da 1 a 4 non hanno una durata predefinita:
1. Danno biliare + infiltrato linfocitario con qualche plasmacellula, presenza di
necrosi di interfaccia e di aggregati follicolari. Vi la dissoluzione della
110
membrana basale e, per questo motivo, i biliociti arrivano persino a scomparire.
Levidenza istologica la scomparsa del dotto biliare in prossimit dellarteriola
alla quale quasi sempre si accompagna. Iniziano a formarsi i primi granulomi a
livello degli spazi portali che poi vanno a interessare tutto il lobulo. Questa fase
pu durare fino a 20 anni!
2. Al danno segue levento riparativo con rigenerazione duttulare, evidenze di
necrosi periportale, a volte necrosi confluente e fibrosi
3. Progressione fibrosi
4. Cirrosi
Pu recidivare in tempi imprevedibili e comunque in maniera blanda.
Colangite sclerosante
E una patologia autoimmuni che colpisce prevalentemente i maschi di giovane et e
consiste nel depauperamento dei dotti biliari nativi ce vengono sostituiti da fibrosi che
causa stenosi e dilatazioni sacciformi.
La diagnosi si effettua con la Wirsungrafia retrograda.
Questa patologia pu avere una latenza massima di 7 anni dopodich evolve in cirrosi
e vi la necessit di un trapianto.
Questa patologia spesso associata ad altre patologie autoimmuni come la rettocolite
ulcerosa e il morbo di Crohn.
A livello sierico si evidenziano alti livelli di Ig anti-ANCA.
Morfologia
Danno allo spazio portale:
Edema che fa risultare lo spazio portale bianco
Fibrosi concentrica a bulbo di cipolla a livello periduttale
Flogosi portale danneggia il dotto biliare che scompare lasciando un globulo
ialino
I segni lasciati dalle colestasi sono:
Rosette epatocitarie
Trombi biliari
Degenerazione schiumosa
La diagnosi si effettua solo con imaging e anche escludendo man mano altre possibili
patologie.
Questa patologia aumenta il rischio di carcinoma ai dotti biliari e pancreatici.
111
Tumori e lesioni simil-tumorali del fegato
DISCORSO INTRODUTTIVO
Le lesioni maligne riguardanti il fegato sono:
Per il 75% di origine metastatica
Per il 25% di origine primitiva
Vi sono 10.000 casi lanno al S.Orsola e sono in forte ascesa visto che nei primi anni 80
ve ne era solo 1 allanno.
Lincremento dovuto alla forte presenza di epatopatia ed epatiti virali che sono
endemiche nella nostra zona e che sono fattori altamente promuoventi lo sviluppo di
tumori.
Come in altri paesi industrializzati sono le abitudini di vita a favorire, a loro volta, lo
sviluppo di queste patologie; per esempio c stato un forte incremento nella fascia
giovanile dopo il boom degli anabolizzanti.
Normalmente la diagnosi occasionale perch non ci sono sintomi e il pz si mantiene
in stato di completo benessere, per cercare di aumentare lo screening:
Si consigliano check-up periodici
Si tengono sotto osservazione le fasce a rischio:
- Pz con epatiti virali
- Pz con stadi evolutivi di epatopatie croniche come la cirrosi
La realt che ora si riesce a guarire se la diagnosi tempestiva!
I tumori primitivi del fegato si dividono in benigni e maligni, i pi comuni sono quelli
epiteliali che possono trarre origine da:
Epatocita
Biliocita
Cell staminali
I tumori mesenchimali del fegato sono poco frequenti
La prima evidenza il riscontro, mediante ECO al fegato, di una lesione occupante
spazio.
La prima cosa da capire se si tratta di un interessamento primario o secondario.
Per questo motivo si verifica se il pz ricade in una delle fasce a rischio.
Se ci troviamo di fronte a un pz cirrotico possiamo escludere con una certa sicurezza
che si tratti di metastasi. Il fegato cirrotico, a causa delle alterazioni del suo circolo,
si presenta come un pessimo accettare di metastasi!!!
Patogenesi, diagnosi e terapia
In questa sede ci interessa analizzare, chiaramente, la patogenesi dei tumori primari
del fegato.
112
Di solito tutto parte dalla deregolazione di un clone di formazione epatocitaria, queste
cell non sono ancora maligne e possono persistere anni senza diventare carcinomatose.
La cirrosi una condizione epatica nella quale si persa la struttura tipica del
parenchima dellorgano e che mostra noduli di rigenerazione separati da tralci fibrosi.
Questi noduli di rigenerazione accolgono epatociti proliferanti che tentano di riparare
al danno subito dal fegato.
E allinterno di questi noduli che avviene la deregolazione di un clone, questo prolifera
aumentando le dimensioni del nodulo fino a renderlo evidente allECO.
Queste strutture vengono chiamate noduli macrorigenerativi.
Dopo levidenza ecografica non si pu avere una prova certa di malignit finch non si
effettua una biopsia.
La biopsia viene per effettuata solo in casi speciali visto che il pz cirrotico
solitamente scoagulato a causa dellinsufficienza epatica.
Per prevenire questi problemi si fa una stima approssimativa coi mezzi della
diagnostica per immagini:
Nodulo con diametro >2cm considerato maligno
Nodulo con diametro <2cm considerato boarderline
Questa classificazione per tuttaltro che rigorosa.
Per la diagnosi ci si appella poi anche alla clinica:
Pz non cirrotico:
- Neoplasia primitiva (colangiocarcinoma o epatocarcinoma)
- Metastasi
Pz cirrotico: spesso il tumore primario
Le capacit rigenerative del fegato vengono perse nella cirrosi perci, in caso di
malattia, bisogna valutare il grado di resecazione al fine di non causare insufficienza
epatica.
**Oggi si trapianta anche un fegato di 90 anni a patto che rispetti certi parametri.
Infine la biopsia chiarisce, anche se in parte, la natura benigna o maligna della lesione
tenendo conto che resta ancora una certa gamma di situazioni boarderline.
Caso 1
Se ci si presenta un pz cirrotico con un nodulo si sospetta subito una neoplasia
maligna.
Si procede distruggendo il noduloin che modo? Si introduce dellalcool assoluto sotto
guida ECO che causa necrosi coagulativa o si bloccano i vasi afferenti al nodulo stesso.
Se siamo in presenza di pi noduli di difficile raggiungimento si procede con il
trapianto il prima possibile per ridurre il rischio di recidive.
Caso 2
Se il fegato non cirrotico si procede allanalisi della lesione che pu risultare maligna,
benigna o metastatica; nellultimo caso si analizzano le cell cercando di capire la sede
primaria del tumore.
113
In questi casi possiamo effettuare resecazione perch le potenzialit rigenerative del
fegato sono intatte.
**Variante fibrolamellare: una forma che si credeva benigna e in realt non lo
affatto; si presenta come massa occupante spazio con
allinterno una cicatrice stellata.
** Tumore camaleonte: in alcuni tumori allinterno della massa si trovano tutti i tipi di
tumori maligni epiteliali; questo perch le cell staminali
possono dare tutti i tipi di epiteli a seconda delle condizioni del
microambiente.
Tumori primitivi del fegato
Possono avere tre origini biologiche:
Epatocita Epatocarcinoma
Biliocita Colangiocarcinoma
Cell staminale epatocarcinoma o colangiocarcinoma
Le cell staminali o cell ovali si trovano in prossimit dei dotti di Hering, a questo
punto possono migrare in due direzioni:
Verso la vena centrolobulare diventano epatociti
Verso lo spazio portale diventano biliociti
Normalmente queste cell sono in stato quiescente; quando si verifica un danno
accadono due cose:
Proliferazione degli epatociti
Differenziazione delle cell staminali
E in questo momento che queste cell sono soggette a rischio di cancerogenesi.
A riprova dellorigine staminale di alcuni tumori epatici basta paragonare
lepatocarcinoma ad alcuni colangiocarcinomi
I tumori degli epatociti producono albumina come la loro variante sana, il
colangiocarcinoma dellilo apatico (tumore di Klatskin) non produce albumina ed
lunico tumore delle vie biliari epatiche che origina da biliociti maturi e, per questo, ha
anche fattori di rischio diversi dagli altri colangiocarcinomi che restano limitati al
fegato e producono albumina.
Iperplasia nodulare focale
Nel fegato non cirrotico si possono sviluppare noduli epatocellulari iperplastici singoli
o multipli.
114
Liperplasia nodulare focale si presenta come una massa occupante spazio specie nelle
donne di mezza et.
La patogenesi dipende da condizioni di alterato flusso ematico.
Morfologia
Si presenta come un nodulo ben demarcato ma scarsamente capsulato che pu
raggiungere diversi cm di diametro.
La massa si presenta pi chiara rispetto al parenchima circostante con una cicatrice
stellata grigio-biancastra al centro. Questa cicatrice contiene grandi vasi leggermente
alterati . I setti radianti della cicatrice presentano infiltrati linfocitari e metaplasia
duttulare degli epatociti con proliferazione di dotti biliari; vi accumulo di rame.
Il parenchima circostante risulta normale ma organizzato in lamine caratteristiche
della rigenerazione.
Adenoma epatocellulari
E una neoplasia benigna del fegato che trae origine dagli epatociti e si manifesta
specialmente nelle giovani donne che assumono contraccettivi orali, di solito
regredisce con la soppressione dellassunzione. Si associa anche al diabete familiare.
Sono clinicamente importanti per tre motivi:
1. possono essere confusi col carcinoma
2. possono lacerarsi in gravidanza sotto stimolo estrogenico e causare emorragie
3. possono nascondere un carcinoma
Morfologia
Si presentano come noduli pallidi giallo-brunastri localizzati ovunque nel fegato.
Questi noduli sono composti da epatociti normali ma non presentano la comune
struttura del parenchima epatico!
Possono raggiungere un diametro di 30cm!
Istologicamente presentano lamine e cordoni di cell simili a normali epatociti con
lievissime atipie e citoplasma chiaro per lingente presenza di glicogeno.
Se la neoangiogenesi non riesce a seguire la crescita della massa si forma necrosi
centrale che allECO pu sembrare anche un carcinoma.
Carcinoma epatocellulare (HCC)
E una neoplasia non troppo frequente che ricopre il 5% di tutte le neoplasie.
Oltre l85% di HCC si verifica nei paesi con alto tasso dinfezione da epatite B.
115
In queste zone il tumore si presenta anche in assenza di cirrosi mentre nei paesi
occidentali, dove HBV non prevalente, il 90% associato a cirrosi.
Patogenesi
Sono state stabilite tre associazioni eziologiche principali:
infezione virale (HBV e HCV)
alcolismo
contaminanti alimentari (specie aflatossine)
tirosinemia ereditaria e forme ereditarie di emocromatosi
I fattori promuoventi sono:
cicli di morte e rigenerazione cell dovuti alle epatiti croniche
alterazioni preneoplastiche come la displasia epatocitaria causate da mutazioni
dei fattori di crescita e dallinterazione delle proteine virali
accumulo di mutazioni durante i cicli rigenerativi che possono ledere il sistema
di riparazione del DNA
integrazione del genoma di HBV che determina aberrazioni cromosomiche,
traslocazioni e duplicazioni
Morfologia
Pu essere presente come
massa unificale
noduli multifocale epatomegalia!!
massa diffusamente infiltrante
Tutti questi tipi hanno una forte propensione a invadere il lume vascolare dando
metastasi intraepatiche e ai vasi afferenti (cava sup e inf, porta).
Le lesioni possono essere ben differenziate o totalmente indifferenziate!
Vi pu essere anche la variante fibrolamellare di cui si gi parlato, questa forma ha
una prognosi migliore
Clinica
La clinica non molto caratteristica perch mascherata dalla sintomatologia della
malattia di base.
Neppure il laboratorio di aiuto pi di tanto.
Tumori metastatici
Linteressamento metastatico rappresenta il 75% delle neoplasie epatiche!!
Linteressamento metastatico del fegato molto frequente sia da parte di neoplasie
sottodiaframmatiche come il carcinoma del colon, sia da neoplasie
sopradiaframmatiche come il carcinoma delle mammella e il carcinoma broncogeno.
116
Non a caso le tre neoplasie primitive che metastatizzano pi facilmente al fegato sono
quelle del:
colon
polmone
mammella
Tipicamente si osservano noduli multipli che causano epatomegalia e possono
costituire fino l80% del parenchima epatico.
Il fegato da raramente e solo in presenza di uninvasione massiva segni di
insufficienza epatica, la patologia resta silente fino agli ultimi stadi.
Il motivo di questa predisposizione ad accettare metastasi dovuta alla doppia
vascolarizzazione dellorgano.
Si scoperto che lhoming delle metastasi mediato da recettori e molecole di
adesione.
Un esempio sono le metastasi di neoplasie del colon, dello stomaco e dei polmoni.
Come molti altri tumori questi esprimono molecole embrionarie e, in questo caso, la
molecola il CEA. Questa molecola embrionaria espressa da questi tre tumori ha uno
spiccato tropismo per i sinusoidi epatici e serve da proteina dadesione per le
metastasi.
Se arriva un pz con masse epatiche diffuse quasi certamente sono metastasi, ci sono
due step per risalire al tumore primitivo:
si esegue la biopsie epatica visto che abbastanza agevole
si eseguono TAC e PET per evidenziare il metabolismo di questa neoplasia
Grazie allIIC e allanalisi delle CK (citocheratine) si scoprono falsi colangiocarcinomi e
falsi epatocarcinoma che in realt sono metastasi.
117
Patologia neoplastica delle vie biliari
DISCORSO INTRODUTTIVO
Le vie biliari sono un sistema anatomico adibito al transito della bile.
Questo sistema interamente rivestito da un epitelio composto di biliociti con la sola
funzione di rivestimento.
Il sistema composta da due porzioni, una intraepatica e una extraepatica,
nellordine
1. piccoli dotti intraepatici
2. duttuli
3. dotti
4. dotti epatici dx e sx
5. dotto epatico comune
6. coledoco (dotto epatico comune + dotto cistico)
Il coledoco pu sboccare singolarmente o dopo essersi unito al dotto di Wirsung
proveniente dal pancreas a livello della papilla del Vater e quindi dello sfintere di
Oddi.
Ogni punto di questo percorso pu dare cancro con sempre le medesime caratteristiche
ma al giorno doggi si divide la patologia in zone di interessamento in quanto,
nonostante la medesima istopatologia, la sintomatologia e le indicazioni terapeutiche
cambiano.
Patogenesi
Lagente iniziante un cancerogeno escreto nelle bile dopo ingestione e assimilazione!
Il fattore promuovente la flogosi cronica!!...essa trova la sua eziologia in diversi
fattori:
Presenza di calcoli (il fattore pi frequente) specie a livello della colecisti dove i
sali biliari hanno modo di depositarsi.
Infezioni da vermi (specie nel sudest asiatico)
Flogosi iatrogena come nel caso dellapposizione di uno stent per mantenere le
vie biliari pervie
Colangite sclerosante, malattia infiammatoria cronica delle vie biliari
intraepatiche
DD con neoplasie pancreatiche
Lepitelio biliare e quello dei dotti pancreatici hanno la medesima origine embrionale
che risale alla migrazione dei gettoni epiteliali dallintestino primitivo allabbozzo
epatico e allabbozzo pancreatico.
Per questa medesima origine hanno caratteri comuni e le rispettive neoplasie entrano
quasi sempre in DD sul piano clinico, sul piano istologico e sul piano sierologico
facendo risultare molto difficile la distinzione.
118
Per esempio le neoplasie della testa del pancreas hanno la stessa sintomatologia
dellampulloma
Ittero diretto
Feci ipocoliche (o ipocromiche) per mancanza di bilirubina
Urine ipercromiche per urobilinogeno
Prurito per deposizione di Sali biliari nella pelle
Il laboratorio cerca un marker che una proteina embrionale chiamata CA-19-9 che
indice di neoplasia biliare o pancreatica ma presente in circolo anche in altre
patologie non neoplastiche delle due zone o in neoplasie di altri organi perci non
altamente discriminante di tumore.
Normalmente si hanno due valori di riferimento:
<20 g/ml va bene
20< x <100 g/ml mostra buone possibilit di neoplasia ma non c certezza
Colangiocarcinoma
Tutti i tumori delle vie biliari, visto la stesso epitelio di origine, si dovrebbero
chiamare colangiocarcinoma. In realt la definizione rimane ristretta ai tumori
primitivi delle vie biliari intrepatiche.
Le neoplasie dei biliociti si possono verificare a diversi livelli:
A livello periferico (dai piccoli dotti periferici)
Nellilo (tumore di Klatskin) dai grossi dotti dellilo, dalla biforcazione fino a
1cm dalla stessa.
Vie biliari principali
Ampolla del Vater
Colecisti
E stato calcolato che almeno i 2/3 dei colangiocarcinomi (intraepatici) derivano dalle
cell staminali differenziate in senso biliare quindi le cause comprendono anche le
lesioni epatocitaria come linfezione da virus epatici.
Morfologia
E la medesima per tutte le collocazioni: adenocarcinoma con aspetto ghiandolare e
duttale con caratteri comuni a quelli del digerente (squamosi, mucinosi, papillari)
Prognosi
Sono forme molto aggressive perci dipende dalla possibilit di resecare il pi possibile
Colangiocarcinoma (intraepatico)
E una neoplasia maligna che origina dai dotti biliari interni al fegato.
I fattori di rischio sono gi stati elencati ma, in Occidente, spesso questa neoplasia
insorge senza precedenti fattori di rischio.
119
Morfologia
Insorgono nel fegato non cirrotico e possono seguire gli spazi portali intraepatici
formando una massa arboriforme.
Oppure possiamo avere masse tumorali nodulari.
La caratteristica principale linvasione linfatica e vascolare!
Listologia simile a quella degli adenomi e si presenta spesso in forma sclerosante
con strutture ghiandolari e tubulari ben differenziate rivestite da cell cuboidale o
piatte.
Normalmente non presentano bile poich lepitelio da cui sono composti non pu
produrla.
Si osservano casi di tumori misti, ovvero con compresenza di HCC; in questi casi
logico supporre unorigine dalle cell staminali.
Nel 50% dei casi questa neoplasia d metastasi, in particolare a polmoni, vertebre e
cervello.
Clinica
La forma intraepatica non viene normalmente diagnosticate prima che sia giunta
nella sua fase terminale quando ha creato ostruzione al transito nelle vie biliari o ha
dato luogo a una massa epatica sintomatica.
Lesito sempre infausto, la massima sopravvivenza pu protrarsi fino a poco pi di
due anni, normalmente si muore entro 6 mesi dalla diagnosi.
La chirurgia fortemente eradicante lunica speranza di protrarre la sopravvivenza.
Carcinoma dei dotti biliari extraepatici
Sono tumori abbastanza rari, sono insidiose visto che provocano un ittero che si
aggrava ma nessuna manifestazione dolorosa.
Insorgono principalmente nei soggetti anziani con una lieve predilezione per i maschi.
I fattori di rischio sono sempre gli stessi del colangiocarcinoma intraepatico; in
particolare importante la colangite ascendente nel caso lo sfintere di Oddi non
chiuda bene e le basse vie biliare vengano infettate dai batteri del duodeno.
Morfologia
Per lostruzione delle vie biliari causa rapidamente ittero, la diagnosi risulta
abbastanza veloce e si effettua quando il tumore ancora di piccole dimensioni.
120
Si presenta come un nodulo o pi noduli grigi nella parete del dotto che possono
essere:
Infiltranti
Polipoidi
Papillari
La maggior parte di queste neoplasie sono adenocarcinomi che possono secernere o
meno muco. Rare le varianti squamose. Abbondante componente fibrosa
Il tumore di Klatskin origina dal coledoco tra la giunzione del dotto cistico e il dotto
epatico comune; questo tumore presenta una caratteristica crescita lenta e non d
metastasi a distanza.
Clinica
Ittero, feci ipocoliche, calo ponderale, vomito, colecisti palpabile nel 25% dei casi,
epatomegalia nel 50% dei casi, urine pigmentate.
Importante distinguere se littero possa essere dovuto a calcolosi e,nel caso,
assicurarsi che non vi sia la compresenza di una neoplasia.
Ampulloma
Qualsiasi tumore che si presenti entro i 2cm finali delle vie biliari, entro 1cm finale del
dotto di Wirsung o sullampolla del Vater.
Anche un polipo del duodeno se occlude la papilla considerato ampulloma ma la sua
derivazione intestinale deve essere chiarificata perch comporta una diversa terapia e
soprattutto una prognosi migliore.
Lintervento di elezione la duodenocefalopancreasectomia!
121
Patologia della colecisti
Carcinoma della colecisti
E una neoplasia che si manifesta principalmente nella 7 decade di et con una
preferenza per il sesso femminile.
E una malattia che praticamente sempre viene diagnosticata in uno stadio in cui non
pi operabile e la sua sopravvivenza a 5 anni resta dell1%.
In Occidente il 60-90% di queste neoplasie associato a colelitiasi mentre in Asia la %
molto pi bassa a causa delle frequenza di infezioni parassitarie da elminti come
fattore di rischio.
Morfologia
Questa neoplasia pu presentare due tipi di accrescimento:
Infiltrante
Esofitico
Linfiltrante il pi frequente e assume laspetto di unarea non bene definita di
ispessimento diffuso che pu interessare lintera colecisti
Possono formarsi ulcere o fistole che coinvolgono i visceri circostanti.
Lesofitico si presenta come una massa irregolare a forma cavoliforme che cresce nel
lume e invade, contemporaneamente, la parete.
La maggior parte sono adenocarcinomi:
Papillari e moderatamente differenziati
Infiltranti e indifferenziati
Squamosi (5%)
Clinica
La diagnosi preoperatoria si verifica in meno del 20% dei pz.
La diagnosi , come detto, tardiva e avviene solo dopo che il tumore ha gi dato
metastasi infiltrato il letto epatico sul 4 segmento..ora si opera rimuovendo il letto
epatico e questo migliora di poco la sopravvivenza.
I sintomi sono insidiosi perch totalmente confondibili con quelli della colelitiasi:
Dolore addominale
Ittero
Anoressia
Nausea e vomito
LAJCC ha incluso, nella stadiazione del tumore, il T3 trai tumori che perforano la
sierosa, questo li rende operabili secondo protocollo e ci ha leggermente migliorato la
prognosi.
122
Le metastasi linfonodali sono un fattore prognostico negativo.
Bisogna stare attenti a fare la DD da colecistite cronica perch le due patologie hanno
spesso una radiologia sovrapponibile e innalzano ambedue il CA-19-9.
123
Il pancreas endocrino
Struttura normale
Costituito dalle isole di Langerhans, contenenti quattro tipi di cellule maggiori e due
tipi di cellule minori.
I quattro tipi di cellule maggiori sono:
1. cellule (68%) producono insulina. Granuli avvolti da mbr e contenenti un core
denso rettangolare circondato da alone.
2. cellule (20%) producono glucagone, che ha azione antagonista allinsulina.
Granuli rotondi con membrane molto vicine tra loro e zona central pi scura
3. cellule (10%) producono somatostatina, che ha azione sopprimente sia il rilascio
di insulina che il rilascio di glucagone. Granuli grandi e pallidi con membrane
molto vicine tra loro.
4. cellule PP (2%) contengono un particolare polipeptide pancreatico che stimola la
secrezione di enzimi gastrici ed inibisce la motilit intestinale. Granuli piccoli e
scuri presenti anche a livello del parenchima pancreatico e non solo a livello delle
insule.
I due tipi di cellule minori sono:
1. cellule D1 elaborano VIP (vasoactive intestinale polypeptide) che provoca
glicogenolisi ed iperglicemia e stimola la secrezione di fluidi gastrointestinali.
2. Cellule enterocromaffini sintetizzano serotonina.
Diabete mellito
Gruppo di disordini cronici del metabolismo dei carboidrati, dei lipidi e delle proteine,
accomunati dal dato clinico di un iperglicemia dovuta a carenza assoluta, relativa o
assoluta e relativa di insulina.
Colpisce il 3% della popolazione mondiale (140 milioni di individui) ed in costante
aumento, tanto che si pensa che entro il 2025 il numero delle persone che ne sono
affette raddoppier.
Diagnosi
I valori di glicemia sono considerati normali quando:
- glicemia a digiuno < 110 mg/dL
- glicemia dopo 2 ore dal pasto < 140 mg/dL
La diagnosi di diabete si fa quando si osservano almeno per 2 volte un tale aumento
del glucosio ematico:
- glicemia al riscontro casuale >200 mg/dL
- glicemia a digiuno > 126 mg/dL
- glicemia dopo 2 ore dal pasto > 200 mg/dL
Per gli individui con valori di glicemia a digiuno compresi fra 110 e 126, si parla di
alterata omeostasi glucidica.
Per gli individui con valori di glicemia dopo 2 h dal pasto compresi fra 126 e 200 si
parla di intolleranza al glucosio.
In entrambi i casi gli individui in questione hanno un rischio notevolmente maggiore
di sviluppare diabete conclamato; un 5-10% dei casi sfocia verso il diabete mellito.
124
Classifcazione
La classificazione attualmente basata principalmente su dati patogenetici.
a) diabete primitivo
1. diabete di tipo 1 (10%) deficit assoluto di insulina, per la distruzione delle
cellule del pancreas
2. diabete di tipo 2 ( 80-90%) associazione di resistenza periferica allazione
dellinsulina e deficit relativo di insulina, cio disfunzione delle cellule che
impedisce unadeguata risposta compensatoria secretoria.
3. Forme monogeniche di diabete
4. Diabete mellito gestazionale
b) diabete secondario
- ad infezioni (citomegalovirus, rosolia congenita, coksackie B)
- ad endocrinopatie (tumori dellipofisi, del surrene)
- alluso di farmaci
- ad altri difetti genetici (sindrome di Down, sindrome di Turner)
Ad una differente patogenesi di queste forme, corrisponde un comune sviluppo delle
manifestazioni cliniche e degli effetti a lungo termine di tutti questi tipi di diabete.
Fisiologia normale dellinsulina
Linsulina, con lazione del suo ormone antagonista, il glucagone viene ad avere un
importante effetto di regolazione sul metabolismo del glucosio. Linsulina in
particolare viene ad avere le seguenti azioni:
Sul metabolismo glucidico
- favorisce la captazione di glucosio da parte delle cellule muscolari (utilizzo del
glucosio come fonte di energia) o da parte degli adipociti (immagazzinamento sotto
forma di lipidi), mediata da specifici trasportatori insulino-dipendenti (GLUT 4).
- favorisce la glicogenosintesi a livello del muscolo scheletrico e del fegato
- inibisce la gluconeogenesi epatica
Sul metabolismo lipidico
- favorisce la lipogenesi e diminuisce la lipolisi a livello degli adipociti
Sul metaolismo proteico:
- favorisce la capatazione degli amminoacidi
- favorisce la sintesi proteica ed inibisce la degradazione delle proteine.
Funzioni mitogene
- induzione della sintesi del DNA
- induzione del differenziamento cellulare in molte cellule
In definitiva dunque ha azione ipoglicemizzante ed ha un forte potere anabolico,
inducendo la sintesi e promuovendo la cerscita.
125
REGOLAZIONE del RILASCIO di INSULINA
1. Sintesi dellinsulina.
Sintesi della preproinsulina (precursore inattivo) nel RER e trasporto nellapparato di
Golgi
Scissioni proteolitiche in serie che determinano formazione equimolare di
- insulina matura catene e
- peptide di clivaggio peptide C
Accumulo di insulina e peptide C nei granuli.
Secrezione di insulina e peptide C, dopo stimolazione, in quantit equimolari (livelli di
peptide C come indice diagnostico della produzione di insulina endogena).
2. Rilascio di insulina.
Stimolo: aumento della glicemia
Captazione di glucosio nelle cellule del pancreas, da parte di GLUT2 (trasportatore
insulino-indipendente)
Metabolismo glicolitico e produzione di ATP, con aumento della concentrazione di
glucosio intracellulare.
Inibizione dellattivit dei canali del K sensibili allATP sulla mbr.
Depolarizzazione della mbr ed ingresso di calcio extracellulare attraverso i canali del
calcio voltaggio dipendenti.
Incremento del calcio intracellulare
Secrezione di insulina
AZIONE DELLINSULINA
Il rilascio dellinsulina in circolo porta al suo legame con recettori periferici che si
trovano preferenzialmente a livello delle cellule muscolari striate ( muscolo scheletrico
e miocardio) ed a livello degli adipociti.
Il recettore dellinsulina una proteina tetramerica, composta da:
- 2 subunit legano linsulina ed inducono modificazioni conformazionali dei
domini con conseguente loro attivazione
- 2 subunit in seguito ad attivazione acquisisce attivit tirosino chinasica,
provocando una fosforilazione a cascata di molte proteine bersaglio.
Si possono dividere le vie di attivazione del segnale i due grandi categorie:
- via mitogena mediata dallattivazione della MAP kinasi
- via metabolica mediata dallattivazione della fosfatidil-inositolo-3- chinasi (PI-
3-K).
126
Patogenesi del diabete mellito tipo 1
un malattia autoimmune in cui si vede la distruzione delle insule pancreatiche
mediata dalla risposta immunitaria contro antigeni ancora poco caratterizzati delle
cellule .
MECCANISMI di DISTRUZIONE delle CELLULE
I meccanismi che concorrono alla distruzione delle cellule sono diversi:
1. linfociti T che reagiscono contro antigeni delle cellule questo testimoniato
dalla presenza nei primissimi stadi della malattia di insulite (infiltrazione
linfocitaria e necrosi) con presenza di linfociti TCD4+ (danno mediato
dallattivazione dei macrofagi) e di linfociti TCD8+ (citotossici, distruggono
direttamente le cellule ). La specificit di queste cellule del tutto sconosciuta.
2. Citochine prodotte localmente che danneggiano le cellule
3. Autoanticorpi contro antigeni delle cellule insulari ( compresi Ac contro GAD,
decarbossilasi dellacido glutammico) ed insulina, presenti nel sangue del 70-80%
dei pz.
Inoltre nella reazione autoimmune vediamo nelle cellule aumentata espressione di
molecole MHC di classe I ed espressione aberrante di antigeni MHC di classe II,
questultima probabilmente indotta da citochine prodotte localmente dai linfociti
CD4+.
Essendo il diabete di tipo I una malattia autoimmunitaria un ruolo importante nella
patogenesi di questa malattia viene svolto da:
1. suscettibilit genetica vi sono vari loci associati alla malattia, ma quello pi
importante il locus della classe II dellMHC, responsabile da solo di circa la met
della suscettibilit genetica.
2. fattori ambientali sono poco noti, ma sono evidenziati dallevidenza che
emigranti di una etnia hanno un rischio di ammalarsi pi simile alle popolazioni
del paese di destinazione. Probabile il coinvolgimento di alcune infezioni virali
nellautoimmunit; in particolare si pensa alle infezioni da Coxsackie B e
secondariamente a parotite, morbillo, rosolia e mononucleosi, visto che linsorgenza
del diabete sembra avere un trend stagionale simile a quello di queste infezioni. Il
meccanismo mediante cui le infezioni provocherebbero autoimmunit pu essere di
due tipi:
- le infezioni provocano danni tissutali ed infiammazione, con conseguente
esposizione di Ag prima nascosti dalle cellule e con conseguente reclutamento ed
attivazione di linfociti ed altri leucociti nel tessuto.
- I virus producono proteine che simulano e cross-linkano con proteine delle
cellule , con conseguente attivazione di una risposta immunitaria contro auto-
antigeni.
Patogenesi del diabete mellito tipo 2
Il diabete mellito di tipo 2 caratterizzato da 2 difetti metabolici:
- insulino-resistenza minore capacit dei tessuti periferici di rispondere
allinsulina. Patogenesi legata a
127
difetti genetici
situazione di obesit e stile di vita sedentario
- disfunzione delle cellule inadeguata secrezione di insulina in adattamento
allinsulino-resistenza.. Patogenesi legata a difetti o predisposizione genetica.
INSULINO-RESISTENZA
Linsulino-resistenza la resistenza agli effetti dellinsulina..
Comporta:
- < assorbimento di glucosio nelle cellule muscolari e nel tessuto adiposo
- incapacit dellinsulina di sopprimere la gluconeogenesi epatica.
dovuta ad alterazioni qualitative e quantitative delle vie di segnalazione controllate
dallinsulina, e nelle vie che determinano secrezione insulinica.
La patogenesi dellinsulino-resistenza non ben chiara, ma sicuramente legata a:
1. difetti genetici del recettore e della via di regolazione dellinsulina (intermediari a
valle del recettore dellinsulina) difficile identificare precisamente i geni
coinvolti, anche se il fatto che vi sia una componente genetica certo (50-90% di
concordanza tra gemelli monozigoti).
2. Obesit: stato dimostrato che il rischio di sviluppare diabete aumenti con
laumento della massa corporea e sia associato in modo particolare ad unobesit
addominale, centrale. Probabilmente lobesit gioca un ruolo centrale nel
determinare insulino-resistenza attraverso tre meccanismi:
- acidi grassi liberi (FFA) tipicamente nei pz obesi si osserva un aumento del
livello FFA plasmatici con conseguente accumulo di trigliceridi intracellulari.
Questi, insieme ai prodotti del metabolismo degli acidi grassi diminuiscono la
sensibilit del tessuto allinsulina.
- Adipochine: leptina, adiponectina e resistina sono citochine rilasciate dagli
adipociti nel circolo sistemico; la disregolazione della loro secrezione, che si osserva
frequentemente nei pz obesi, pu portare ad insulino-resistenza.
La leptina infatti sensibilizza gli organi periferici allazione dellinsulina in
modo mediato dal SNC, sui cui recettori essa agisce.
La resistina aumenta linsulino-resistenza a livello del muscolo perifierico.
Ladiponectina aumenta la sensibilit allinsulina a livello del muscolo
periferico
- PPAR (peroxisome-activated receptor ) e tiazolidinedioni (TZD): I
tazolidinedioni sono farmaci che agiscono sul PPAR, un recettore nucleare che
modula la trascrizione di adipochine nel tessuto adiposo, portando infine ad una
diminuzione dellinsulino-resistenza.
DISFUNZIONE delle CELLULE
Per disfunzione delle cellule nel diabet mellito di tipo 2 si intende lincapacit delle
medesime di adattarsi allinsulino-resistenza periferica ed allaumento di richiesta di
secrezione di insulina.
Nello sviluppo del diabete mellito di tipo 2 si hanno tre fasi:
- fase1 si ha una ocndizione di insulino-resistenza che del tutto compensata
da > livelli di secrezione insulinica,, con conseguente normoglicemia
128
- fase2 la compensazione delle cellule diventa inadeguata, per dellinsulino-
resistenza accompagnato dalliniziale esaurimento delle cellule . Si ha uno stato di
alterata tolleranza od omeostasi glucidica.
- fase3 linsulino-resistenza si mantiene costante, ma si ha una compensazione
che diviene sempre pi inadeguata, con crescita dellinsufficienza delle cellule . Si
ha diabete conclamato.
La disfunzione delle cellule qualitativa e quantitativa:
- disfunzione qualitativa: si ha alterazione del normale schema della secrezione di
insulina con attenuazione della prima fase di secrezione rapida dellinsulina in
risposta allaumento della glicemia. Con il tempo il difetto interessa tutte le fasi
anche se persiste una certa secrezione basale, ampiamente insufficiente.
- Disfunzione quantitativa: si ha una diminuzione della massa delle cellule , per
degenerazione di una parte delle insule, con deposito di amiloide.
Patogenesi delle complicanze del diabete
La morbilit associata al diabete e quasi sempre dovuta alle complicanze di questa
patologia e non alla patologia in s.
Principalmente le complicanze sono vascolari ed interessano:
1. arterie di medio e grande calibro macroangiopatia. Gli effetti sono
principalmente unaterosclerosi accelerata, con maggiore rischio di infarto del
miocardio, di ictus o di gangrena degli arti inferiori.
2. Arteriole e capillari degli organi bersaglio microangiopatia. Gli effetti sono
principalmente un inspessimento della mbr basale prevalentemente a livello della
retina (retinopatia), del rene (nefropatia) e dei nervi periferici (neuropatia).
Queste complicanze sono dovute naturalmente allo stato iperglicemico ed in
particolare sono implicate tre distinte vie metaboliche:
a. formazione di AGE (prodotti finali della glicosilazione avanzata), per la reazione
non enzimatica tra precursori glucosio-derivati e gruppi aminici di proteine intra
ed extra cellulari.
Gli AGE hanno azione lesiva sulla matrice extracellulare e sulle proteine
plasmatiche circolanti.
- sulla matrice extracellulare la formazione di AGE provoca
cross-linking tra polipeptidi della medesima proteina: collagene di tipo I nei
grandi vasi ( elasticit e sovraccarico ematico conseguente), collagene di tipo IV
della mbr basale ( permeabilit ai fluidi).
Intrappolamento delle proteine non glicosilate: LDL nei grandi vasi, con
conseguente loro ossidazione ed aumento del rischio di aterosclerosi, proteine
plasmatiche nei capillari con conseguente dello spessore della mbr basale.
Resistenza alla digestione proteolitica.
- il legame dei precursori glucosio-derivati a proteine plasmatiche porta alla
formazione di AGE circolanti che:
si legano ai recettori per gli AGE su monociti e cellule endoteliali
provocano lattivazione della via mediata da Nf- con conseguente:
rilascio di citochine e fattori di crescita
aumento della permeabilit vascolare
induzione dellattivit procoagulante
129
aumentata proliferazione e sintesi di ECM da parte di fibroblasti e cellule
muscolari liscie
b. attivazione della proteina chinasi C: normalmente attivata da ioni calcio e da
diacilglicerolo (DAG). La sintesi ex novo di DAG pu essere stimolata
dalliperglicemia intracellulare con conseguente abnorme attivazione della pKC che
ha i seguenti effetti principalmente:
Produzione di VEGF, proteina proangiogenica, implicata nella
neovascolarizzazione che caratterizza la retinopatia diabetica.
Aumento dellattivit vasocostrittrice ( secrezione endotelina)
Produzione di molecole profibrogeniche
Produzione della molecola procoagulanete PAI-1 che comporta ridotta
fibrinolisi.
Produzione di citochine pro-infiammatorie.
c. iperglicemia intracellulare che causa alterazione della via dei polioli.
Avviene nei tessuti che non richiedono insulina per lassunzione di glucosio, dove
liperglicemia porta ad aumento del glucosio intracellulare, che viene metabolizzato
a polioli (sorbitolo e fruttosio). Nel processo consumato NADPH, che anche
cofattore dellenzima glutatione reduttasi, che rigenera il glutatione ridotto,
fondamentale meccanismo antiossidante. In presenza di iperglicemia prolungata
sono compromessi i meccanismi di rigenerazione del glutatione ridotto e dunque
viene acquisita maggiore suscettibilit cellulare allo stress ossidativo.
Morfologia del diabete e delle sue complicanze
PANCREAS
- Riduzione numero e dimensioni delle insule pi spesso nel tipo 1,
tardivamente a volte anche nel tipo 2
- Infiltrato leucocitario delle insule (insulite) tipicamente nel tipo 1 alle
primissime fasi dellesordio clinico
- Degranulazione delle cellule per la mancanza di granuli di insulina nelle
cellule danneggiate. Tipicamente nel tipo 1 negli stadi iniziali, quando sono ancora
presenti alcune cellule .
- Amiloidosi delle insule deposito di materiale amorfo rosa, inizialmente nei
capillari e fra le cellule ed arriva fino allobliterazione quasi completa delle insule, con
riscontro di fibrosi. Tipica del tipo 2
- Iperplasia diffusa delle isole pancreatiche interessa tipicamente neonato e
lattante da madri diabetiche. Il feto a lungo esposto alliperglicemia materna, risponde
con aumento delle dimensioni e del numero delle proprie insule e questo pu
eventualmente provocare gravi episodi di iperglicemia.
MACROANGIOPATIA DIABETICA
- Accelerata aterosclerosi nelle arterie di grande e medio calibro, con conseguente
grosso aumento del rischio di:
infarto miocardico da aterosclerosi delle coronarie
ictus
gangrena degli arti inferiori
aterosclerosi renale il rene uno degli organi pi spesso e gravemente colpiti.
130
- accelerata ateriolosclerosi ialina: inspessimento ialino, amorfo della parete delle
arteriole, che provoca restringimento del lume.
MICROANGIOPATIA DIABETICA
il diffuso inspessimento delle mbr basali da parte di strati concentrici di materiale
ialino, contenente collagene IV, che si evidenzia soprattutto a livello dei capillari:
- del rene nefropatie
- della retina retinopatia
- dei nervi periferici neuropatie periferiche
Malgrado lincremento dello spessore questi capillari sono pi permeabili a causa del
cross-linking delle molecole di collagene IV, mediato dagli AGE, quindi se si a livello
cutaneo si pu avere anche edema diffuso.
RENE
I reni sono particolarmente colpiti dal diabete nefropatia diabetica.
Si possono avere:
1. lesioni glomerulari
2. lesioni vascolari renali aterosclerosi ed arteriolosclerosi renale
3. pielonefrite infiammazione acuta o cronica che ha origine nel tessuto
interstiziale e dunque si propaga ai tubuli. I diabetici sono molto pi colpiti ed in
modo pi grave da questo genere di infiammazione purulente. Il quadro tipico di
presentazione nei diabetici quello della necrosi della papilla renale.
Un approfondimento necessario per quello che riguarda le lesioni glomerulari che
consistono principalmente in tre tipi di lesioni:
a. inspessimento della mbr basale glomerulare
b. sclerosi mesangiale diffusa diffuso aumento della mbr mesangiale, sempre
associato ad inspessimento della mbr basale. Pu causare sd nefrosica quando
marcata.
c. Glomerulosclerosi nodulare depositi nodulari di matrice laminare alla periferia
del glomerulo. Questa forma di glomerulosclerosi patognomonica del diabete.
Induce ischemia sufficiente a causare una microsclerosi di tutto il rene.
OCCHIO
- retinopatia la lesione fondamentale consiste in una neovascolarizzazione della
retina. Compare in circa il 60-70% dei pz dopo 15-20 anni dalla diagnosi.
- Glaucoma lesione del nervo ottico provocata da pressione oculare
- Cataratta
NEUROPATIA
Si pu avere:
- neuropatia sensitivo-motoria che provoca grande riduzione della sensibilit
della porzione distale degli arti e alterazioni motorie meno evidenti.
- Neuropatia autonomica colpisce il 20-40% dei diabetici in associazione alla
neuropatia sensitivo-motoria
131
- Neuropatia periferica focale o multifocale a carico di un solo nervo o a carico
di pi nervi disposti in modo asimmetrico
Probabilmente insorgono per insufficienza vascolare che provoca danno ischemico del
nervo periferico.
Caratteristiche cliniche del diabete
DIABETE di tipo 1
Solitamente insorge nellet infantile, e si rende manifesto nella pubert, prima dei 25
anni, ma di fatto pu comparire ad ogni et.
La maggior parte dei parte dei pazienti dipende dallinsulina per la sua sopravvivenza,
anche se nei primi 1-2 anni dalla sua insorgenza la richiesta di insulina esogena
minima, per una secrezione residua di insulina endogena (periodo luna di miele).
Le manifestazioni cliniche della malattia insorgono
Tardivamente dopo che pi il 90% delle cellule stato distrutto
Improvvisamente la transizione da una ridotta tolleranza al glucosio al diabete ben
conclamato spesso brutale.
Lesordio dunque acuto e caratterizzato da:
- Poliuria la secrezione incontrastata di ormoni antagonosti dellinsulina
provoca assieme alla forte diminuzione dellassorbimento del glucosio nei tessuti
muscolare ed adiposo e al ridotto accumulo di glicogeno nel fegato e nel muscolo
laumento della glicogenolisi. Ne risulta una iperglicemia che supera la soglia
renale di assorbimento, con conseguente glicosuria. Il glucosio un metabolita
osmoticamente attivo che richiama acqua con conseguente diuresi osmotica e grave
perdita di acqua ed elettroliti.
- Polidipsia la perdit di acqua, insieme con liperosmolarit dovuta agli elevati
livelli di glicemia, porta a stimolazione degli osmocettori dei centri cerebrali della
sete.
- Polifagia il bilancio metabolico si sposta a favore del catabolismo, con
conseguente produzione di un bilancio energetico negativo ed aumento
dellappetito.
- Calo ponderale e debolezza muscolare perch nonostante laumentato appetito
prevale leffetto catabolico.
Una complicanza metabolica acuta del diabete di tipo 1 la chetoacidosi diabetica
dovuta a :
- disidratazione dovuta alla diuresi osmotica
- attivazione del meccanismo chetogenico :
carenza di insulina stimolazione della lipoproteina lipasi
eccessiva degradazione delle riserve adipose
aumento del livello di acidi grassi liberi
nel fegato gli FFA vengono esterificati ad acil CoA
132
ossidazione delle molecole di acil CoA nei mitocondri con produzione di corpi
chetonici chetonemia e chetonuria
se lescrezione urinaria dei chetoni compromessa da disidratazione ne risulta una
chetoacidosi metabolica sistemica perch i corpi chetonici non riescono ad essere
eliminati.
Questa situazione se scompensata pu portare a coma chetoacidosico.
DIABETE di tipo 2
Solitamente i pazienti sono pi anziani (> 40 anni) e frequentemente obesi.
Tuttavia con lincremento dellobesit anche fra una popolazione pi giovane, si visto
che il diabete di tipo 2 pu insorgere anche nei bambini e negli adolescenti, con
frequenza sempre maggiore.
Lesordio non acuto ed improvviso come quello del diabete di tipo 1, ma pi
insidioso e sfumato, tanto che solitamente la diagnosi avviene dopo esame di routine
delle urine o del sangue in pazienti asintomatici.
Nelle situazioni di scompenso i pazienti possono sviluppare coma iperosmolare
nonchetosico, sindrome generata dalla grave disidratazione che si acompagna alla
diuresi osmotica.
In entrambi i tipi di diabete comunque le maggiori cause di mortalit e di morbilit
sono le complicanze a lungo termine del diabete, che compaiono circa 15-20 anni dopo
lesordio.
Le complicanze sono:
1. accelerata aterosclerosi nelle arterie di grande e medio calibro
patogenesi che coinvolge molti fattori:
- formazione di AGE
- attivazione della pKC alterazione della vasodilatazione e aumento
dellattivit procoagulante (PAI 1)
- obesit fattore indipendente di rischio
- ipertensione presente in molti casi di diabete di tipo 2, forse come
manifestazione secondaria della disfunzione endoteliale indotta
dalliperglicemia. un fattore indipendente di rischio
- dislipidemie presenti in molti casi di diabete di tipo 2. Comprendono aumento
dei trigliceridi e delle LDL e diminuzione delle HDL.
- disfunzione piastrinica negli stati di insulino-resistenza (diabete di tipo 2), si
osserva aumentata adesivit piastrinica, forse per un equilibrio trombossano-
prostaciclina spostato a favore del trombossano A2.
Conseguenze dellaterosclerosi:
- infarto del miocardio
- patologie cerebrovascolari
- insufficienza renale cardiovascolare
2. nefropatia diabetica una delle principali cause di insufficienza renale.
Manifestazioni cliniche precoci microalbuminuria
Manifestazioni cliniche tardive nefropatia franca con macroalbuminuria, di
solito con ipertensione
133
3. diminuzione della vista a volte fino alla cecit
retinopatia diabetica
glaucoma
cataratta
4. neuropatia diabetica
5. aumentata suscettibilit alle infezioni infezioni della cute, tubercolosi,
polmonite, pielonefrite
Neoplasie endocrine del pancreas
Sono molto rare e rappresentano solo il 2% dei tumori di questorgano.
Poich colpiscono un organo endocrino, possono essere annoverati tra i tumori
neuroendocrini e dunque assomigliano alla loro controparte (carcinoidi) che pu
trovarsi in qualunque porzione del tratto alimentare e che pu trovarsi teoricamente
in qualunque organo data la presenza del sistema neuroendocrino diffuso.
Le neoplasie endocrine del pancreas possono essere:
- benigne
- maligne: frequentemente metastatizzano ai linfonodi regionali o al fegato
Vi sono vari criteri diagnostici che permettono di distinguere tra neoplasia benigna e
maligna.
Neoplasia benigna Neoplasia maligna
Struttura organoide: tendenza alla
formazione di strutture pseudoinsulari,
simili a quelle dellorgano di appartenenza
Struttura solida
Citologia tipica della cellula endocrina ; la
struttura della cellula assomiglia a quella
della cellula dorigine, i nuclei sono
omogenei e simili a quelli della cellula
dorigine
Citologia atipica: la struttura della cellula
non assomiglia pi a quella della cellula
dorigine, ma a quella della stem-cell.
Tutti i tumori in fase finale sono molto
simili.
Attivit proliferativa scarsa Attivit proliferativa marcata
Necrosi assente o focale Necrosi estesa perch la proliferazione
supera le capacit di neo-angiogenesi.
p53 assente: non vi sono n mutazioni, n
accumuli della p53.
La proteina p53 wild type ha emivita
molto breve (4-5h) e dunque non
visualizzabile con limmunoistochimica.
La presenza di p53 dunque rispecchia
sicuramente una mutazione della stessa
che pu essere:
- pre trascrizionale
- post-trascrizionale: legame di
polimeri e stabilizzazione
P53 spesso presente
Altri criteri di malignit possono essere:
- metastasi a linfonodi regionali ed organi distanti
134
- invasione vascolare
- invasione massiva dei visceri adiacenti
- infiltrazione del parenchima pancreatico oltre la capsula del tumore
Le pi frequenti sindromi cliniche associate alle neoplasie endocrine pancreatiche
sono:
- iperinsulinismo
- sindrome di Zollinger- Ellison
Iperinsulinismo
dovuto ad insulinoma, cio a tumore delle cellule , che responsabile di una
produzione di insulina tale da provocare ipoglicemia importante.
La triade di sintomi che caratterizza la crisi ipoglicemica associata allinsulinoma :
- insorgenza per glucosio < 50 mg/dL.
- Manifestazioni principalmente a carico del SNC confusione, stupore, perdita
di coscienza
- Attacchi provocati dal digiuno o dallattivit fisica e migliorano rapidamente con
alimentazione o somministrazione di glucosio
La morfologia solitamente benigna:
- noduli piccoli, con diametro < 2 cm, incapsulati
- Noduli simili ad insule giganti, che conservano la disposizione a cordoni di
cellule con orientamento verso i vasi
- Allindagine immunoistochimica, presenza di insulina nelle cellule
Sindrome di Zollinger-Ellinson
una sindrome che vede spiccata ipersecrezione di gastrina, ed frequentemente
mediata da tumori gastrino-secernenti ad origine pancreatica, duodenale o dai tessuti
molli peripancreatici.
probabile che le cellule endocrine di intestino e pancreas possano esserne lorigine.
I tumori gastrino-secernenti in pi della met dei casi al momento della diagnosi
hanno gi metastatizzato, o mostrano invasivit locale, anche se istologicamente si
presentano di solito come benigni.
La sindrome di Zollinger-Ellinson caratterizzata da spiccata secrezione di gastrina
ed acido gastrico, con conseguente formazione di ulcerazioni peptiche, solitamente
multiple, a volte con localizzazioni insolite (digiuno) e spesso non responsive ai
protocolli terapeutici utilizzati abitualmente per lulcera peptica.
Nonostante questo il trattamento viene di solito effettuato con inibitori della pompa
ATPasica idrogeno-potassio, al fine di controllare la secrezione gastrica, seguito da
resezione della neoplasia.
135
Patologia del glomerulo renale
Struttura del glomerulo renale
Il glomerulo renale una porzione fondamentale del nefrone ed localizzato nella
parte corticale del rene.
Formato da una rete anastomotica di capillari, rivestiti da endotelio fenestrato ed
incorporati allinterno di una doppia membrana, la capsula di Bowmann.
La membrana interna detta epitelio viscerale: incorporato nella parete capillare, di
cui diviene parte integrante, separato dalle cellule endoteliali da una sottile
membrana basale.
La membrana esterna detta epitelio parietale: lo spazio che la separa dalla
membrana interna detta spazio urinario ed la cavit che inizialmente raccoglie il
filtrato plasmatico.
La parete del capillare glomerulare costituisce la membrana responsabile della
filtrazione del sangue.
Essa costituita, dallinterno verso lesterno, dalle seguenti strutture:
- Cellule endoteliali: hanno la caratteristica di essere fenestrate, cio di avere pori di
circa 70-100 nm.
- Membrana basale glomerulare (MBG): costituita da collagene di tipo IV che forma
una sovrastruttura a rete alla quale si attaccano altre glicoproteine e proteoglicani
polianionici: questo intreccio rende ragione delle sue funzioni di filtro. formata da
tre strati:
1. strato interno: lamina rara interna
2. strato centrale: lamina densa ( spesso ed elettrondenso)
3. strato esterno: lamina rara esterna.
- Cellule epiteliali viscerali: si tratta di cellule epiteliali modificate dette podociti.
Sono elementi fondamentali del rene, dotati di prolungamenti, detti pedicelli, che
aderiscono alla lamina rara ext della MBG. I pedicelli sono fra loro interdigitati e
separati da piccoli spazi di 20-30nm che prendono il nome di fessure di filtrazione e
che sono chiuse da un sottile diaframma. La membrana basale su cui si appoggiano
i pedicelli, ne determina lorientamento ed il loro versante funzionale, facendo
inoltre da ponte fra pedicelli e cellule endoteliali dei vasi. I podociti, oltre alla loro
fondamentale funzione di filtrazione, sono anche gli elementi che sintetizzano gran
parte della MBG.
Lintera massa glomerulare sostenuta dal mesangio, struttura formata da:
- Cellule mesangiali: cellule presenti fra le anse capillari, che presentano funzione
molto variabile a seconda delle necessit. Hanno origine mesenchimale e
presentano capacit contrattili, di produzione di matrice e collagene, di secrezione
di mediatori attivi, capacit istiocitarie al fine di eliminare elementi di rifiuto e
scarto.
136
- Matrice mesangiale: di costituzione simile alla mbr basale, forma un reticolo che
sostiene le cellule mesangiali e supporta le anse capillari, trovandosi tra esse
interdigitato.
La principale funzione del glomerulo e quella di filtrare il sangue e costituire una
barriera selettiva, capace di discriminare il passaggio delle diverse molecole, in
particolare delle proteine selezionate in base alla carica ed alla dimensione.
La barriera dimensione-carica dipendente correlata alla struttura della parete
capillare, che vede fenestrature endoteliali (facile passaggio di acqua e piccoli soluti),
accanto alla presenza di una MBG porosa e ricca di valenze anioniche ed alla presenza
di diaframmi di filtrazione fra i pedicelli.
Per questo molecole di dimensioni maggiori dellalbumina non sono filtrate cos come
non lo lalbumina medesima, data anche la sua elevata carica negativa.
Malattie glomerulari
Le patologie che riguardano il glomerulo renale sono dette glomerulonefriti o
glomeulopatie, se non presentano componente cellulare infiammatoria.
Si pu parlare di:
- glomerulonefriti primitive: forme che interessano solo (o in modo prevalente) e
primitivamente il rene
- glomerulonefriti secondarie o complesse: la patologia renale associata alla
presenza di altre malattie primitive, come malattie sistemiche (LES), vascolari
(ipertensione e poliartrite nodosa), metaboliche (diabete).
Il quadro clinico e le alterazioni morfologiche della forme primitive e secondarie
possono essere simili.
Le manifestazioni cliniche associate alle diverse malattie glomerulari sono
sontetizzabili in cinque sindromi:
1. sindrome nefritica a uta c
2. glomerulonefrite rapidamente progressiva
3. sindrome nefrosica
4. insufficienza renale cronica
5. ematuria o proteinuria asintomatica
**Glossario
- Diffuso: interessante tutti i glomeruli
- Focale: interessante < 50% dei glomeruli
- Globale: interessante tutto il singolo glomerulo
- Segmentale: interessante una porzione del singolo glomerulo
- Ipercellularit: aumento del numero di cellule del glomerulo presente in alcune
patologie glomerulari. Esso dovuto a una o pi dei seguenti fattori:
1. proliferazione cellulare: del mesangio o delle cellule endoteliali.
2. Infiltrazione leucocitaria: di neutrofili, monociti, talvolta linfociti.
3. Formazione di crescent o semilune.
137
- Ialinosi: accumulo di materiale acellulato, omogeneo ed eosinofilo al m.o. Si tratta
di materiale amorfo extracellulare, dato da proteine plasmatiche trasudate dal
torrente circolatorio alle strutture vascolari. Vi dunque un aumento della
componente filamentosa della matrice
- Sclerosi: aumento della porzione glicoproteica della matrice, senza corrispondente
aumento della componente collagene. La sclerosi unevoluzione della ialinosi,
caratterizzata dalla compressione fino allobliterazione dei lumi capillari del
glomerulo.
- Fibrosi: aumento della componente collagene
- Crescent o semilune: sono strutture semilunari date dalla proliferazione delle
cellule epiteliali parietali associata ad infiltrazione di leucociti (principalmente
neutrofili e macrofagi). La fibrina che a volte penetra nello spazio urinario
attraverso le membrane endoteliali danneggiate, costituisce uno stimolo alla
formazione delle semilune.
- Sinechie: date da uneccessiva crescita delle strutture a semiluna fino a che non
prendono contatto con le anse capillari
Patogenesi del danno glomerulare
Fondamentalmente il danno glomerulare primitivo e spesso anche secondario dovuto
ad una serie di meccanismi immunologici, che sono:
1. Lesioni anticorpo mediate: da anticorpi che reagiscono in situ dentro il glomerulo
con antigeni glomerulari insolubili fissi, o con molecole circolanti che si sono
impiantate dentro il glomerulo.
2. Deposizione nel glomerulo di immunocomplessi circolanti
3. Anticorpi citotossici
4. Lesione immunitaria cellulo-mediata
5. Attivazione del complemento
Lesioni anticorpo-mediate
Gli Ac reagiscono direttamente con antigeni intrinseci o impiantati nel glomerulo.
Anticorpi contro Ag intrinseci
Sono presenti due modelli animali che riproducono questo danno glomerulare.
Nefrite da anticorpi anti-MBG
Gli anticorpi sono diretti contro Ag intrinseci renali situati a livello della membrana
basale glomerulare.
Il modello sperimentale vede liniezione di Ac anti rene nel ratto, con legame degli
anticorpi lungo tutta la lunghezza della MBG, evidenziabile allimmunofluorescenza
come una colorazione diffusa e lineare. La malattia glomerulare che ne deriva detta
nefrite di Masugi ed causata dalla reazione contro un Ag della membrana
glomerulare.
Nelluomo si hanno due patologie correlate alla reazione contro uno specifico antigene
della MBG: la forma classica della nefrite da Ac antiMBG e la sd di Goodpasture nella
quale gli anticorpi contro lantigene della membrana basale cross-reagiscono anche con
antigeni presenti a livello degli alveoli pomonari.
138
Nefrite di Heymann
Il modello sperimentale vede liniezione nel ratto di antigeni derivanti da preparati
dellorletto a spazzola dei tubuli prossimali. I ratti sviluppano anticorpi contro questo
antigene, che cross-reagisce con un complesso antigenico sulla spf basale delle cellule
epiteliali viscerali, provocando glomerulonefrite membranosa.
Questa evidenziabile allimmunofluorescenza come colorazione granulare e non
lineare ed al microscopio elettronico si evidenziano depositi elettron-densi nel versante
subepiteliale della membrana basale.
Nelluomo la patologia corrispondente una glomerulonefrite membranosa, di cui non
ancora stato identificato lantigene responsabile. Si ha ugualmente produzione di Ac
che reagiscono contro componenti della membrana cellulare epiteliale, con
conseguente attivazione del complemento, e danno alla membrana medesima.
Numerose forme di glomerulonefriti autoimmuni inoltre possono essere indotte
sperimentalmente da farmaci, da agenti infettivi, dalla reazione di rigetto verso
lospite (graft-versus-host-reaction)
Anticorpi contro Ag impiantati
Gli anticorpi possono reagire in situ con antigeni che non sono normalmente presenti
nel glomerulo e vi sono stati impiantati, che dunque si localizzano nel rene reagendo
con elementi intrinseci del medesimo.
Si tratta per esempio:
- molecole cationiche che si legano ai numerosi siti anionici gomerulari
- DNA, nucleosomi e proteine nucleari che presentano unaffinit con le componenti
della MBG
- Prodotti batterici
- Grossi aggregati proteici, come immunoglobine aggregate o gli stessi
immunocomplessi che si depositano nel mesangio
Il quadro allimmunofluorescenza tipicamente granulare.
Deposizione di immunocomplessi circolanti
Il danno glomerulare causato dallintrappolamento dei complessi antigene-anticorpo
circolanti allinterno del glomerulo. Gli anticorpi non presentano una specificit
immunologica per i costituenti glomerulari, ma i complessi si localizzano nel glomerulo
a causa delle loro propriet fisico-chimiche e per i peculiari fattori emodinamici
presenti nel glomerulo.
Gli immunocomplessi si formano in circolo e successivamente vengono intrappolati nel
glomerulo, dove causano la lesione, con successiva infiltrazione leucocitaria, seguita
spesso da proliferazione delle cellule mesangiali ed endoteliali.
Il microscopio elettronico mette in evidenza gli immunocomplessi come depositi
elettrondensi che possono essere localizzati:
- nel mesangio
- tra cellule endoteliali e MBG (depositi subendoteliali)
- tra cellule epiteliali e MBG (depositi subepiteliali)
139
Limmunofluorescenza mette in evidenza gli immunocomplessi come depositi granulari
Gli immunocomplessi depositati nel rene possono alla fine essere degradati, da parte
dei neutrofili e dei macrofagi nellinfiltrato, delle cellule mesangiali, delle proteasi, con
conseguente spegnimento della reazione infiammatoria.
Quando vi per una continua esposizione allantigene, come nel LES o nellepatite
virale, si susseguono cicli continui di formazione degli immunocomplessi e di loro
deposizione.
Gli antigeni che formano gli immunocomplessi possono essere di natura:
- esogena (prodotti dellinfezione)
- endogena (DNA, antigeni tumorali)
Le dimensioni e la carica degli immunocomplessi sono importanti al fine della
localizzazione glomerulare e del danno.
Carica:
- sostanze cationiche: attraversano la MBG e tendono a localizzarsi in sede
subepiteliale
- sostanze anioniche: non riescono ad attraversare la MBG e quindi si localizzano in
sede subendoteliale o non sono nefro-lesive
- sostanze neutre: tendono a localizzarsi nel mesangio
Dimensioni:
- immunocomplessi di grandi dimensioni: non nefritogeni perch eliminati dai
macrofagi
- immunocomplessi di piccole dimensioni: pi facilmente nefritogeni
Anticorpi citotossici
Si tratta di anticorpi diretti contro antigeni della cellula glomerulare, che dunque
reagendo contro la componente cellulare, causano morte della cellula e danno
glomerulare per la loro citotossicit.
Possono essere rivolti:
- contro componenti cellulari mesangiali: mesangiolisi seguita da proliferazione
mesangiale
- contro componenti cellulari endoteliali: lesioni endoteliali e trombosi intravascolare
- contro componenti cellulari epiteliali viscerali: proteinuria.
Le malattie associate a questo tipo di danno non mostrano alla microscopia elettronica
ed allimmunofluorescenza depositi immuni visibili.
Lesione immunitaria cellulo-mediata
Probabilmente la causa primaria di tutte le glomerulonefriti riconducibile ad un
meccanismo mediato da anticorpo.
Tuttavia in certi di tipi di glomerulonefriti vi un infiltrazione di linfociti T i quali
possono essere mediatori di danno glomerulare, causando a volte anche la
progressione della malattia.
Attivazione della via alternativa del complemento
Avviene nellentit clinico-patologica detta glomerulonefrite membranoproliferativa di
tipo II o malattia a depositi densi.
140
Diagnosi delle malattie glomerulari
La biopsia renale costituisce lesame diagnostico fondamentale per lanalisi delle
malattie glomerulari, poich ci viene a fornire informazioni su:
- tipo di malattia
- natura della malattia: meccanismo patogenetico alla base delle lesioni.
- Localizzazione ed estensione delle lesioni: se sono diffuse o focali, globali o
segmentali.
- Evoluzione della malattia: contiene elementi che aiutano il clinico ad avere
unindicazione prognostica della malattia.
La diagnosi attraverso biopsia renale dunque permette una pianificazione del
trattamento ma anche unindicazione della prognosi.
Molto spesso una diagnosi di malattia glomerulare necessita di un triplice esame della
biopsia renale:
1. al microscopio ottico: dopo inclusione in paraffina e colorazione con PAS, che
consente la visione della mbr basale e delle sue alterazioni.
2. al microscopio elettronico: che costituisce per una serie di patologie lunico metodo
diagnostico, essendo per molte altre fondamentale per la conferma diagnostica.
Consente di vedere la formazione dei depositi densi corrispondenti agli
immunocomplessi, spesso presenti nella patologia glomerulare.
3. Con metodiche di immunofluorescenza: evidenziano la presenza di
immunocomplessi, o di anticorpi sulle membrane glomerulari.
Sindrome nefritica acuta
Caratterizzata da:
- presentazione con ematuria e cilindri di globuli rossi nelle urine.
- Iperazotemia: grandi livelli di azoto e solitamente di creatinina nel sangue, per una
diminuzione della capacit renale di filtrazione (GFR: Glomerular Filtring Rate)
- Ipertensione da lieve a moderata.
- Oliguria con edema
- Proteinuria (meno grave di quella presente nelle sindromi nefrosiche).
la sindrome che caratterizza la presentazione clinica di:
- glomerulonefriti acute: glomerulonefriti acute proliferative (post-streptococcica e
post-infettiva)
- patologie multisitemiche coinvolgenti anche il glomerulo.
Glomerulonefrite acute proliferative
Le glomerulonefriti acute proliferative sono:
- acute: perch caratterizzate da un punto di vista anatomico da alterazioni
infiammatorie dei glomeruli
- proliferative: perch caratterizzata da un punto di vista istologico da diffusa
proliferazione di cellule glomerulari, associata ad afflusso di leucociti legato
allinfiammazione.
Sono tipicamente causate da lesioni da immunocomplessi.
141
Lantigene causale pu essere esogeno (glomerulonefrite post-streptococcica) o
endogeno (glomerulonefrite acuta proliferativa in corso di LES).
Glomerulonefrite post-streptococcica
Colpisce generalmente bambini di 6-10 anni di et.
Compare generalmente da 1 a 4 settimane dopo uninfezione streptococcica faringea o
cutanea
Il periodo di latenza tra linfezione e la nefrite compatibile con il tempo richiesto per
la produzione di anticorpi anti-streptococcici e per la successiva formazione di
immunocomplessi.
Leziologia mediata da deposizione di immunocomplessi della malattia confermata
da:
- Evidenze sperimentali
- presenza di depositi granulari allimmunofluorescenza
- presenza di depositi elettron-densi al microscopio elettrico
la componente antigenica streptococcica responsabile della formazione di
immunocomplessi rimasta sconosciuta a lungo.
Morfologia
Al microscopio ottico:
- glomeruli grandi ed ipercellulati: infiltrazione diffusa di leucociti, proliferazione
diffusa di cellule endoteliali e mesangiali, formazione di semilune nei casi gravi
- rigonfiamento delle cellule endoteliale
- a volte obliterazione dei lumi capillari per combinazione di infiltrazione,
proliferazione e rigonfiamento.
Al microscopio elettronico:
- depositi elettondensi sul versante epiteliale della membrana, spesso con laspetto di
gobbe
Allimmunofluorescenza:
depositi granulari di IgM, IgG e C3 nel mesangio e lungo la membrana basale.
Clinica:
Il bambino ha un esordio con sindrome nefritica acuta (emturia con urine color coca-
cola, ipertensione lieve, oliguria, edema periorbitale, proteinuria lieve), accompagnata
da febbre, nausea, malessere.
Pi del 95% dei bambini guarisce completamente.
Nelladulto la malattia ha esordio pi atipico ed insidioso e presenta prognosi meno
benigna.
Solo il 60% dei casi si glomerulonefrite guarisce spontaneamente, mentre gli altri
possono pregredire in una glomerulonefrite cronica o rapidamente progressiva.
142
Glomerulonefrite post-infettiva
Si verifica sporadicamente in associazione con altre infezioni batteriche, malattie
virali ed infezioni parassitarie.
Glomerulonefrite rapidamente progressiva (GNRP)
una sindrome associata a grave danno glomerulare.
caratterizzata da un punto di vista clinico:
- grave oliguria
- progressiva perdita della funzione renale (insufficienza renale acuta)
- se non trattata, morte nel giro di poche settimane.
-
caratterizzata da un punto di vista istologico:
- reni ingranditi e pallidi, spesso con petecchie emorragiche sulla superficie corticale
- presenza di semilune nella maggior parte dei glomeruli. provocato dalla
proliferazione delle cellule parieteli e dalla migrazione di monociti e macrofagi. A
volte anche dallinfiltrato di neutrofili e monociti.
- Strie di fibrina tra gli strati delle semilune: la fibrina costituisce uno stimolo per la
proliferazione delle cellule parietali e dunque per la formazione di semilune.
- Al microscopio elettronico distruzione focale della MBG: questo permette a leucociti
e macrofagi di passare nel glomerulo, con conseguente formazione di semilune
- Sclerosi progressiva delle semilune nella maggor parte dei pazienti.
associata a diverse manifestazioni patologiche, idiopatiche quanto secondarie.
provocata da danno glomerulare immuno-mediato.
La GNRP suddivisibile in tre differenti tipologie:
1. GNRP I o sindrome da anticorpi anti-MBG
2. GNRP II da immunocomplessi
3. GNRP III o pauci-immune
GNRP I
dovuta alla presenza di Ac diretti contro componenti della membrana basale del
glomerulo renale.
Allimmunofluorescenza si vedono depositi lineari di IgG, e C3 lungo tutta la
membrana basale.
La terapia prevede utilizzo della plasmaferesi al fine di rimuovere gli anticorpi
patogeni circolanti, affiancata a terapia immunosoppressiva.
Patologia associata
La GNRPI associata caratteristicamente alla Sindrome di Goodpasture
Gli anticorpi ragiscono contro la membrana basale glomerulare e con le membrane
basali degli alveoli polmonari.
Il quadro clinico di insufficienza renale associata ad emorragia polmonare.
143
Lantigene di Goodpasture, che scatena la reazione anticorpale, un peptide presente
nel collagene di tipo IV.
Esiste una predisposizione genetica a questo tipo di fenomeni autoimmunitari.
GNRP II
una malattia dovuta al deposito di immunocomplessi.
Allimmunofluorescenza si vedono depositi immuni caratteristicamente granulari.
I pazienti non traggono beneficio dalla plasmaferesi e la terapia differenziata a
seconda del tipo di patologia associata.
Patologia associata
La GNRPII pu essere una complicanza di una qualsiasi malattia da
immunocomplessi, come glomerulonefrite post-infettiva, LES, nefropatia da IgA,
porpora di Schoenlein-Henoch.
GNRP III
caratterizzata dalla mancanza, allimmunofluorescenza e con la microscopia
elettronica, di anticorpi anti-membrana basale e di immunocomplessi.
La sua eziologia non molto chiara.
La maggior parte dei pazienti presenta nel siero ANCA (anticorpi diretti contro
antigeni citoplasmatici dei neutrofili), che giocano un ruolo importante nella
patogenesi di alcune vasculiti.
In base a questa evidenza si ipotizzato che la GNRP III sia dovuta alla presenza di
vasculiti, che possono essere sistemiche (in questo caso GNRP III secondaria) oppure
interessare solo il glomerulo (in questo caso GNRP III idiopatica o primitiva).
Questo spiegherebbe anche lassenza di immunocomplessi o anticorpi contro
componenti glomerulari in questo tipo di patologia.
Patologia associata
Vasculiti sistemiche (granulomatosi di Wegener o poliarterite microscopica) o vasculiti
di piccoli vasi limitate al glomerulo.
Tutti e 3 i tipi di GNRP possono essere associati a patologie renali o extra-renali
specifiche, ma un 50% idiopatico.
Si tratta quindi di una sindrome a cui riconducibile il quadro clinico di molte
patologie, ma che costituisce da sola una patologia a s stante.
Sindrome nefrosica
Sindrome caratterizzata da:
proteinuria massiva: perdita giornaliera > 3,5g di proteine
ipoalbulinemia: albumina plasmatica < 3g/dl
edemi generalizzati
iperlipidemia e lipiduria
144
Patogenesi:
1. Alterazione della parete capillare del glomerulo
2. Aumentata permeabilit alle proteine plasmatiche: solitamente si ha permeabilit
selettiva con perdita soprattutto di proteine a basso peso molecolare, cio di
albumina
3. Proteinuria massiva: proteine che passano dal plasma al filtrato glomerulare. Pu
essere:
altamente selettiva: perdita solo delle proteine a basso peso molecolare
(albumina e non globuline). ci che avviene solitamente
scarsamente selettiva: perdita oltre che di albumine, di proteine a peso
molecolare maggiore, dunque anche di globuline.
4. In entrambi i casi si ha deplezione delle albumine, frequentemente al di sopra delle
possibilit compensatorie del fegato, associata ad aumento del catabolismo renale
delle albumine filtrate
5. Ipoalbulinemia, frequentemente con inversione del rapporto albumine/globuline.
6. Riduzione della pressione colloido-osmotica del sangue
7. Edema generalizzato
8. Ipovolemia che induce ritenzione di acqua e sodio compensatori
9. Aumento delledema
10. A questo si associa incremento della sintesi epatica di lipoproteine, alterato
trasporto delle particelle lipidiche circolanti e ridotto catabolismo delle particelle
lipidiche medesime con conseguente iperlipidemia
11. Attraversamento della parete capillare da parte delle aumentate lipoproteine
12. Lipiduria: comparsa dei lipidi nelle urine come grassi liberi e come corpi adiposi
ovali (lipoproteine riassorbite dallepitelio tubulare poi desquamate con le cellule in
degenerazione).
Cause:
malattie sistemiche: diabete, amilodosi, LES
malattie primitive del glomerulo:
- Glomerulopatia a lesioni minime
- GN prolife ativa mesangiale r
r
- Glomerulosclerosi focale e segmentale
- Glomerulopatia membranosa
- GN membranoprolife ativa
- Nefropatia da IgA
Glomerulopatia a lesioni minime
Primitiva ed idiopatica.
la causa pi frequente di sindrome nefrosica nei bambini con picco di incidenza fra i
2 ed i 6 anni.
Caratterizzata dalla perdita dei pedicelli dei podociti in glomeruli che al microscopio
ottico appaiono normali.
Patogenesi:
Anche se mancano depositi autoimmuni levidenza sperimentale indica la genesi
immunologica.
145
Lipotesi pi accreditata la presenza di una qualche disfunzione autoimmune
risultante nella produzione di una citochina da parte dei linfociti T, che danneggi le
cellule epiteliali viscerali. Il danno si esplicherebbe a carico del diaframma di
filtrazione, con perdita delle sue cariche polianioniche, e conseguente alterazione dei
pedicelli.
Questo difetto della barriera carica-dipendente sarebbe il principale determinante
della proteinuria.
Morfolgia:
Al microscopio ottico:
- glomeruli normali
Al microscopio elettronico:
- diffuso e uniforme appiattimento dei pedicelli delle cellule epiteliali viscerali, detto
fusione dei processi pedicellari.
- Perdita dei diaframmi di filtrazione tra pedicello e pedicello, e conseguente perdita
della barriera polianionica di filtrazione proteinuria selettiva nei cfr delle
albumine
- Alterazioni degenerative dei pedicelli: vacuolizzazione del citoplasma e comparsa di
microvilli che si formano nel versante urinario dei podociti e sembrano riempire lo
spazio lasciato libero dai pedicelli.
Allimmunofluorescenza:
- mancanza di depositi di immunoglobuline o complemento
- molto raramente: occasionali depositi di IgM e di C3.
Lappiattimento dei processi pedicellari presente in molte altre forme di malattie
glomerulari: la diagnosi di glomerulopatia a lesioni minime si pu fare solo nel caso in
cui questa lesione non si associ a nessunaltra alterazione ed i glomeruli si presentino
dunque normali al microscopio ottico.
Clinica:
Vi massiva proteinuria altamente selettiva, ma la funzione renale rimane buona, con
assenza di ematuria ed ipertensione.
Secondo alcune ipotesi la glomerulopatia a lesioni minime, rappresenta solamente il
primo stadio, facilmente curabile, di una serie di patologie ad andamento progressivo
che sono:
- glomerulopatia a lesioni minime
- glomerulonefrite proliferativa mesangiale
- glomerulosclerosi focale e segmentale
Terapia:
Generalmente vi risposta eclatante alla terapia corticosteroide, con prognosi
eccellente.
Tuttavia nei casi in cui la malattia non riesca ad essere curata o non sia trattata,
presenta spesso landamento evolutivo sopra detto.
Glomerulonefrite proliferativa mesangiale
Si tratta di una patologia che clinicamente risulta indistinguibile dalla glomerulopatia
a lesioni minime.
146
Probabilmente si tratta di unevoluzione della malattia a lesioni minime non trattata
che vede una reazione del mesangio, con conseguente proliferazione del medesimo.
Le differenze si riscontrano allesame della biopsia renale.
Morfologia:
Al microscopio ottico:
- crescita del mesangio ed aumento della cellularit del medesimo
Al microscopio elettronico:
- fusione dei pedicelli
- perdita dei diaframmi di filtrazione
- alterazioni degenerative dei podociti: vacuolizzazione, aumento della quantit di
organuli citoplasmatici, iperplasia dei microvilli.
- Comparsa nel mesangio di depositi elettrondensi di colore grigio: rappresentano
lespressione di un primo deposito di immunocomplessi mesangiali.
Allimmunofluorescenza:
- evidenza di depositi di IgM e di C3 nel mesangio: questo depone a favore
dellipotesi di una progressione di questa malattia a partire dalle rare forme di
malattia a lesioni minime con iniziali depositi di IgM e di C3.
Terapia:
Trattamento con farmaci corticosteroidi che determina una prognosi favorevole nel 30-
50% dei casi.
Glomerulosclerosi focale segmentale
Lesione caratterizzata dalla sclerosi di alcuni, non di tutti i glomeruli (focale); nei
glomeruli interessati solo una parte del convoluto capillare coinvolta (segmentale).
Cause:
Si manifesta in tutta una serie di situazioni:
- In associazione ad altre patologie note: infezione da HIV, dipendenza delleroina,
anemia falcifome, obesit.
- Determinate forme ereditarie
- Evento secondario, esito di un evento cicatriziale glomerulare
- Da ablazione renale: come complicanza di malattie renali e non renali che
determinano riduzione della massa renale.
- Come forma idiopatica, primitiva: evoluzione della progressione malattia a lesioni
minime glomerulonefrite proliferativa mesangiale glomerulosclerosi focale
segmentale oppure malattia distinta?
Morfologia
Al microscopio ottico:
molti glomeruli sono intatti, non sclerotici e normali, dunque le lesioni segmentali
non possono essere rilevate se il frammento bioptico contiene un numero
insufficiente di glomeruli.
Le lesioni coinvolgono inizialmente i glomeruli iuxta-midollari
I glomeruli sclerotici presentano:
collasso della membrana basale
aumento dei nuclei mesangiali con moderato incremento della matrice
trasudazione di proteine plasmatiche lungo la parete dei capillari, con
formazione di depositi ialini PAS negativi
147
estensione dei depositi con aggregati allinterno dei capillari e compressione
degli stessi: occlusione e scomparsa delle anse vascolari
gocce lipidiche e cellule schiumose macrofagiche
occasionali sinechie
la capsula del Bowmann pu essere plurilaminata in corrispondenza delle
sinechie: questo dimostra che alla diffusa proliferazione mesangiale, si
accompagna la proliferazione un po di tutte le altre cellule, con alterazioni
della capacit filtrante delle anse sempre pi compresse e calo progressivo
della capacit renale.
Al microscopio elettronico:
glomeruli non sclerotici: presentano un quadro del tutto simile a quello dei
glomeruli nella nefropatia a lesioni minime:
appiattimento e fusione dei pedicelli
vacuolizzazione, aumento degli organuli citoplasmatico e iperplasia dei
microvilli dei podociti
formazione di pseudocisti.
glomeruli sclerotici:
aumento enorme dellarea occupata dalla matrice, che dunque ingloba la
membrana basale
matrice che viene a formare ponti di unione tra il gomitolo capillare e la
capsula
membrana basale glomerulare raggrinzita e contratta
aree sclerotiche del mesangio caratterizzate da una degenerazione delle
cellule mesangiali che causa ipocellularit, accompagnata da grande aumento
della matrice mesangiale
ipertrofia delle cellule endoteliali
Allimmunofluorescenza:
presenza di depositi di IgM e C3 nelle aree sclerotiche e nel mesangio.
Clinica
Caratterizzata da:
ematuria
ridotta frazione di filtrazione glomerulare (GFR)
ipertensione
proteinuria non selettiva: dovuta alla perdita della selettivit della filtrazione
proteica per carica (perdita dei diaframmi di filtrazione), per taglia (per esteso
danno della membrana glomerulare
Patogenesi
Non ancora chiaro se la glomerulosclerosi focale e segmentale idiopatica rappresenti
levoluzione della malattia a lesioni minime oppure sia una malattia distinta.
In ogni caso abbiamo una proteinuria non selettiva dovuta alla mancanza del
diaframma ed allesteso danno selettivo, dunque la perdita di proteine plasmatiche,
che rimangono intrappolate nel glomerulo e causano ialinosi.
Laccumulo di proteine plasmatiche, associato alla proliferazione cellulare conseguente
al danno ed allipertrofia delle cellule endoteliali determina compressione dei capillari,
fino alla scomparsa delle anse sclerosi.
148
Recentemente sono state identificate alcune forme familiari di glomerulosclerosi focale
segmentale, associate a mutazioni genetiche.
- GSFS autosomica recessiva o sd nefrosica steroido-resistente dellinfanzia: deriva
da mutazioni a carico del gene NPHS2, che codifica per un prodotto proteico, la
podocina, localizzato a livello del diaframma di filtrazione. tipica dei bambini
- GSFS autosomica dominante: deriva da mutazioni a carico del gene che codifica
per la proteina legante lactina dei podociti. una forma insidiosa che spesso
evolve verso uninsufficienza renale.
Queste mutazioni hanno in comune lalterazione della struttura del diaframma o del
citoscheletro dei podociti adiacenti, suggerendo limportanza dellintegrit di queste
strutture per mantenere la normale barriera di filtrazione glomerulare.
Terapia e prognosi
Vi scarsa tendenza alla remissione spontanea
La risposta alla terapia corticosteroidea variabile e se c assenza di reattivit si ha
progressione, nella quale alla sclerosi segue la fibrosi, considerata lultimo stadio.
I bambini hanno una migliore prognosi rispetto agli adulti e la prognosi migliore se
manca sindrome nefrosica.
Il 20% dei pz presenta unevoluzione molto rapida, con proteinuria massiva,
intrattabile che porta allinsufficienza renale in 2 anni.
Dopo trapianto si osservano recidive nel 25-50% dei casi.
Glomerulonefrite membranosa
la pi comune causa di sindrome nefrosica nelladulto.
caratterizzata da diffuso inspessimento della parete capillare glomerulare e
dallaccumulo di depositi elettrondensi di immunoglobuline lungo il lato subepiteliale
della membrana basale.
Cause
- GN membranosa idiopatica (85%)
- Secondaria a farmaci: penicillamina, FANS
- Associata a tumori maligni: soprattutto carcinomi del polmone, del colon e
melanomi
- Associata a LES, artrite reumatoide, trombosi.
- Secondaria ad infezioni (HIV, HBV)
- Secondaria ad intossicazione da metalli pesanti
Patogenesi
una forma cronica di malattia immuno-mediata.
Le lesioni presentano stretta somiglianza con quelle della nefrite di Heymann e
Come questa, si tratta di una malattia autoimmune, legata ad alterazioni nel locus
MHC, che conferiscono maggiore predisposizione a produrre anticorpi contro lantigene
nefritogeno.
Allinterno del glomerulo non si trovano neutrofili, monociti e piastrine (assenza di
una evidenziabile risposta infiammatoria), ma si trova praticamente costantemente il
complemento, che media danno glomerulare:
- direttamente: complesso di attacco alla membrana C5b-C9
149
- indirettamente: C5b-C9 che media attivazione delle cellule glomerulari epiteliali e
mesangiali inducendole alla liberazione di proteasi ed agenti ossidanti, con
conseguente ulteriore danno della parete capillare.
Lattivazione del complemento pu essere indotta da antigeni circolanti o derivanti da
biosintesi locali allinterno del glomerulo medesimo.
Morfologia
Levoluzione della glomerulonefrite membranosa pu essere suddivisa in 5 stadi che
hanno diverse caratteristiche al microscopio ottico ed al microscopio elettronico.
Stadio 1:
formazione di depositi continui di immunocomplessi che si appoggiano lungo il
versante epiteliale della membrana basale, in posizione subepiteliale (tra pedicelli e
membrana basale).
Al microscopio ottico: parete cellulare normale; con colorazione PAS sono evidenziabili
depositi granulari
Al microscopio elettronico: depositi subepitelili elettrondensi, membrana basale che si
presenta normale. Inizia ad intravedersi qualche spike (spicule irregolari che
protrudono dalla membrana basale per inglobare gli immunocomplessi).
Stadio 2:
La membrana emette protrusioni irregolari, dette spikes, che avvolgono gli
immunocomplessi, perch essi siano inglobati allinterno della membrana medesima.
Si vede qualche deposito che sembra dentro la mbr.
Al microscopio ottico: inspessimento della parete vascolare e formazione degli spikes.
Al microscopio elettronico: risultano molto in evidenza gli spikes ed i depositi
granulari elettron densi
Stadio 3:
Si ha inglobamento completo degli immunocomplessi con grande aumento dello
spessore della membrana.
Al microscopio ottico: inspessimento della parete vascolare con presenza ancora di
irregolarit dovute alla presenza di spikes prominenti che tendono a fondersi
Al microscopio elettronico: depositi granulari ancora pi elettrondensi, grande
inspessimento della membrana basale.
Stadio 4:
Gli immunocomplessi inglobati nella membrana cellulare sono degradati e
metabolizzati. La membrana glomerulare assume un aspetto tarlato.
Al microscopio ottico: glomeruli opsalescenti a volte con ialinosi ( per il danno alla
membrana a cui segue trasudazione di proteine plasmatiche)e sclerosi locali (per
inspessimento della membrana e compressione del lume capillare). Raramente
sinechie focali.
Al microscopio elettronico: membrana basale ancora inspessita, ma depositi
gradualmente meno evidenti
Stadio 5:
poich in questo caso la malattia primitiva e vi una continua esposizione
allantigene, il processo di deposizione di immunocomplessi non ha termine.
150
Si pu vedere dunque a questo punto nuova deposizione di antigeni con compresenza
dello stadio 1 e 4
Allimmunofluorescenza sempre dimostrabile la presenza di immunoglobuline, anche
se in questo caso si tratta di IgG e non di IgM, con quantit variabili di complemento.
Clinica
Generalmente si ha esordio con sd nefrosica e nel 15% dei pz con proteinuria senza sd
nefrosica.
Nel 15-35% dei pz si ha ematuria ed ipertensione di lieve entit
La proteinuria di tipo non selettivo e spesso non si ha risposta a trattamento con
corticosteroidi.
La prognosi generalmente buona anche se nel 50% dei pazienti si ha una
progressione della malattia che si associa allaumento della sclerosi renale e della
proliferazione cellulare, con conseguente insufficienza renale in 2-3 anni e sviluppo di
ipertensiona arteriosa.
Fattori positivi per la prognosi sono:
- sesso femminile
- giovane et
- assenza di sd nefrosiche precedenti
- buona funzionalit renale
Glomerulonefrite membranoproliferativa (GNMP)
Rappresenta il 10-20% dei casi di sindrome nefrosica del bambino e del giovane adulto.
Caratterizzata da:
- alterazioni della membrana basale
- proliferazione delle cellule glomerulari, principalmente a carico del mesangio.
- infiltrazione leucocitaria
La GNMP primitiva si divide in due tipi principali.
GNMP di tipo I
Morfologia
Al microscopio ottico:
- ipercellularit con formazione in molti casi di semilune. Essa deriva da:
proliferazione delle cellule mesangiale
proliferazione dellendotelio capillare
presenza di lucociti infiltranti
- aumento della matrice mesangiale
- aspetto lobulato dei glomeruli, dato loro da proliferazione cellulare e stromale
- MBG inspessita e spesso presentante un doppio contorno, una sorta di
slaminamento della membrana, causato da:
neosintesi di un nuovo strato di membrana basale
interposizione di elementi cellulari, mesangiali, endoteliali, leucocitari nello
spessore della mambrana
151
Al microscopio elettronico:
- depositi elettrondensi granulari subendoteliali.
Allimmunofluorescenza
- depositi costituiti da C3, IgG, e dalle componenti precoci del complemento C1q e
C4.
Patogenesi
Il fatto che si osservino immunocomplessi e attivazione delle vie classica ed
alternativa del complemento, suggerisce una patogenesi immuno-mediata.
In particolare sembra che si tratti di una reazione anticorpale nei confronti di antigeni
infettivi che si siano impiantati nelle strutture glomerulari, o contenuti in complessi
immuni preformati depositati nel glomerulo dalla circolazione.
GNMP di tipo II o malattia a depositi densi
Morfologia
Al micorscopio ottico:
- analoga a quella della GNMP di tipo I
Al microscopio elettronico
- lamina densa della MBG che diviene una struttura elettrondensa, molto irregolare
e nastriforme a causa della deposizione di materiale denso al suo interno, di origine
ignota.
Allimmunofluorescenza:
- presenza di C3 in focolai granulari o lineari su entrambi i lati della mbr basale.
- Presenza di C3 nel mesangio sotto forma di aggregati circolari caratteristici (anelli
mesangiali)
- Assenza di C3 nei depositi elettrondensi
- Assenza di IgG
- Assenza delle componenti precoci del complemento (C1q e C4)
Patogenesi
Il fatto che si osservi deposito di C3, ma assenza di IgG e delle componenti precoci del
complemento suggerisce una patogenesi legata allattivazione della via alternativa del
complemento.
Nella via alternativa del complemento C3 direttamente clivato in C3b, dopo
interazione iniziale di C3 con sostanze come polisaccaridi batterici, endotossine ed
aggregati di IgA, in presenza di fattori B e D.
Ci porta alla generazione di C3bBb, convertasi della via alternativa, che un
prodotto instabile e genralmente viene degradata.
Sembra che il 70% dei pz con malattia a depositi densi, presenti un autoanticorpo
circolante detto fattore nefritico C3 (C3NeF), che lega la C3 convertasi della via
alternativa e la stabiliza proteggendola dalla degradazione enziamtica.
Non chiaro come la C3 convertasi sia correlata al danno glomerulare.
152
Clinica (comune a GNMPI e II)
Lesordio solitamente con sindrome nefrosica, anche se talvolta si ha presentazione
con ematuria o con una pi insidiosa proteinuria.
La remissione spontanea davvero rara e nella maggior parte dei casi la malattia
segue un decorso clinico progressivo, evolvendo a volte in glomerulonefrite
rapidamente progressiva e nel 50% in insufficienza renale cronica nei 10 anni
successivi.
La terapia con corticosteroidi non ha efficacia ben dimostrata.
Nei pz trapiantati si ha alta frequenza di recidiva.
Nefropatia da IgA (malattia di Berger)
Forma di glomerulonefrite con prominenti depositi di IgA nelle regioni mesangiali
La diagnosi dunque, anche se pu essere sospettata anche al microscopio ottico,
posta solo sulla base di tecniche di immunofluorescenza.
Cause:
nefropatia da IgA primitiva
nefropatia da IgA secondaria a
porpora di Schoenlein-Henoch
LES
Patologie epatiche (cirrosi) ed intestinali
Patogenesi
Normalmente le IgA, Ig delle secrezioni mucose, si ritrovano a basse concentrazioni
nel siero normale, soprattutto in forma monomerica, poich la forma polimerica
catabolizzata dal fegato.
Nella nefropatia da IgA si ha aumento delle IgA polimeriche nel siero e formazione di
immunocomplessi circolanti contenenti IgA.
Questi immunocomplessi vengono ad essere intrappolati nel glomerulo, soprattutto a
livello del mesangio, con conseguente attivazione della via alternativa del
complemento (presenza di C3, ma assenza di C1q e C4) e danno glomerulare.
Laumento della concentrazione di IgA sieriche probabilmente dovuto ad una
alterazione genetica o acquisita della regolazione immune, che porta ad un aumento
della loro sintesi a livello delle mucose, in risposta allesposizione dellapparato
respiratorio o gastrointestinale ad agenti infettivi.
Unaltra ipotesi vede come meccanismo patogenetico, lo sviluppo successivo ad
infezione di anticorpi IgA, che cross-reagiscono con antigeni self del glomerulo renale:
non si tratterebbe dunque di una patologia da deposizione di immunocomplessi, bens
da produzione di Ac rivolti contro le componenti glomerulari.
Morfologia
Al microscopio ottico:
- proliferazione dello stroma e delle cellule mesangiali (reazione alla deposizione di
IgA)
- occasionale sclerosi focale e segmentale, per guarigione della lesione focale
proliferativa.
153
- Crescent localizzato, che possono portare tardivamente a fibrosi
- Presenza di infiltrato infiammatorio.
Al microscopio elettronico:
- depositi elettrondensi mesangiali
Allimmunofluorescenza:
- depositi mesangiali di IgA, associati a C3
- assenza delle componenti precoci del complemento (C1q e C4)
- assenza o scarsa presenza di IgG e di IgM
Di nefropatia da IgA vengono distinte 5 classi morfologiche per assicurare una
migliore diagnosi differenziale.
Clinica
Interessa ogni fascia di et anche se prevalentemente dai 12-21 anni
Ha prevalenza nei maschi rispetto che nelle femmine
Lesordio solitamente con ematuria massiva, dopo infezione dellapparato
respiratorio e meno spesso dellapparato gastrointestinale o urinario.
Tipicamente lematuria dura diversi giorni dunque scompare per ripresentarsi ogni
pochi mesi.
Il decorso poi variabile, anche se generalmente la prognosi favorevole.
Frequente la recidiva dopo trapianto.
Nefriti ereditarie
Gruppo di patologie renali familiari associate a danno glomerulare.
Sindrome di Alport
Se completamente sviluppata si manifesta con
- nefrite che evolve verso insufficienza renale cronica
- ipoacusia sensoriale
- dislocazione del cristallino, cataratta posteriore, distrofia corneale
La forma pi comune una forma legata al sesso, al cromosoma X, nella quale i
maschi esprimono la sindrome in modo completo, mentre le femmine sono portatrici,
con manifestazioni solo legate allematuria.
Patogenesi
Anomala produzione di collagene IVAlterata sintesi di MBG
Morfologia
Al microscopio ottico:
- glomeruli normali
154
Al microscopio elettronico:
- MBG con focolai di ispessimento, alternati ad assottigliamento, con slaminamento
e frammentazione della lamina densa.
- In alcuni reni cellule interstiziali del tubulo renale che acquistano aspetto
schiumoso per laccumulo di grassi e mucopolisaccaridi (cellule schiumose).
- Con progredire della malattia possibile sclerosi, atrofia tubulare e fibrosi
interstiziale.
Clinica
Esordio con ematuria macroscopica o microscopica, frequentemente con cilindri
ematici.
Si pu avere proteinuria e raramente sindrome nefrosica.
Sintomi che si manifestano tra i 5 ed i 20 anni.
Insorgenza di uninsufficienza renale conclamata tra i 20 ed i 50 anni.
Ematuria benigna familiare
E una forma abbastanza comune che consiste in unematuria macroscopica o
microscopica con decorso favorevole che pu presentarsi associata ad altre
glomerulopatie.
A differenza della sindrome di Alport non presenta ipoacusia e anomalie oculari.
Al microscopio si osserva una marcata riduzione dello spessore delle membrane che
passano dai normali 361nm a 191nm. Anche la lamina basale appare assottigliata e
segmentata mentre si osserva un ispessimento della matrice mesangiale che forma
depositi.
La malattia deriva da unalterazione genetica riguardante la sintesi del collageno IV.
155
Malattie dei tubuli e dellinterstizio renale
Sono fondamentalmente di due tipi:
1) necrosi tubulare acuta
2) nefrite tubulo-interstiziale
Necrosi tubulare acuta
unentit clinico-patologica che caratterizzata:
- morfologicamente: distruzione delle cellule epiteliali tubulari
- clinicamente: riduzione acuta o perdita della funzionalit renale. Si tratta
solitamente di una lesione renale reversibile
Cause:
1) Ischemia NTA ischemica. Inadeguato flusso ematico al rene, per danno dei
vasi intrarenali o per una situazione di riduzione del volume circolante
(ipotensione e shock).
2) Danno tossico diretto del tubulo NTA nefrotossica. Innescata da farmaci, da
mezzi di contrasto radiologici, da veleni, ma anche da emoglobine (crisi
emolitiche che provocano emoglobinuria) e mioglobina (danni della muscolatura
scheletrica con conseguente mioglobinuria).
Patogenesi:
La patogenesi simile per entrambi i casi e parte da un danno diretto delle cellule
tubulari dovuto a ridotta perfusione o danno tossico.
Il danno inizialmente reversibile e comporta una serie di alterazioni strutturali e
funzionali:
a. rigonfiamento cellulare
b. vacuolizzazione
c. perdita dellorletto a spazzola e della polarit cellulare: a causa della
ridistribuzione delle proteine di trasporto dalla spf luminale a quella
basolaterale
d. espressione di citochine e molecole di adesione da parte delle cellule
danneggiate.
e. distacco delle cellule danneggiate dalla membrana basale.
c. Perdita dellorletto a spazzola e della polarit cellulare
Implica:
1. anomalo trasporto ionico attraverso la cellula
2. aumento del flusso di iodio a livello del tubulo distale
3. feedback tubulo-glomerulare con stimolazione del sistema renina-angiotensina
156
4. aumento del rilascio del vasocostrittore angiotensina e diminuzione del rilascio
di NO e PGI
5. vasocostrizione
6. ridotto flusso plasmatici glomerulare
7. ridotta GFR
8. oliguria
d. Espressione di citochine e di molecole di adesione da parte delle cellule danneggiate
Implica:
1. reclutamento dei leucociti nellinterstizio
2. danno della membrana basale subendoteliale
3. fluidi che dal lume tubulare raggiungono linterstizio
4. edema interstiziale
5. aumento della pressione interstiziale
6I. ulteriore danno tubulare
6II. Riduzione del flusso tubulare
7. oliguria
e.Distacco delle cellule tubulari danneggiate dalla membrana basale
1. ostruzione del lume tubulare
2. aumento della pressione endotubulare
3. ridotta GFR
4. oliguria
Oltre a ci laumento della pressione endotubulare contribuisce anche alla fuoriuscita
di fluidi dal lume allinterstizio e dunque alledema interstiziale.
Con il passare del tempo il danno diviene irreversibile con conseguente:
a. necrosi ed apoptosi delle cellule tubulari danneggiate
a. Necrosi ed apoptosi delle cellule tubulari
1. passaggio di liquido tubulare nellinterstizio
2. diminuzione del flusso tubulare
3. oliguria
Se la causa scatenante viene rimossa si pu avere una pronta riparazione dei focolai
necrotici, data lirregolare distribuzione della necrosi e il mantenimento dellintegrit
della membrana in molti segmenti.
Morfologia
1. NTA ischemica
- necrosi tubulare che colpisce tratti relativamente brevi di tubuli, in particolare
il tratto dritto dei tubuli prossimali e il braccio ascendente dellansa di Henle.
- Zone di rottura delle membrane basali (tubuloressi)
- Zone di occlusione dei lumi tubulari da parte di cilindri in particolare nei tubuli
distali e nei dotti collettori.
- Edema interstiziale
157
- Accumuli di leucociti allinterno di vasi dilatati
- Aree di rigenerazione epiteliali (si osservano spesso).
2. NTA tossica
- estesa necrosi lungo il tubulo contorto prossimale. La necrosi pu essere
istologicamente del tutto aspecifica o presentare aspetto caratteristici
dellavvelenamento da alcuni agenti tossici.
- Zone di occlusione dei lumi tubulari da parte di cilindri in particolare nei tubuli
distali e nei dotti collettori.
- Edema interstiziale
- Accumuli di leucociti allinterno di vasi dilatati.
- Aree di rigenerazione epiteliale (si osservano spesso)
Clinica
Suddivisa in tre fasi:
1. Fase iniziale
- Dominata dagli eventi scatenanti della necrosi medesima (eventi medici,
chirurgici, ostetrici).
- Lunico segno a livello renale la lieve riduzione del flusso urinario con lieve
aumento dellazotemia.
2. Fase di mantenimento
- severa diminuzione del flusso urinario (oliguria: da 40 a 400ml.)
- sovraccarico di sali ed acqua nelle urine (per aumento dellapporto di sodio nel
lume tubulare)
- aumento delazotemia e della potassiemia.
3. Fase di guarigione
- rapido incremento del volume urinario (fino a 3l./die) con conseguente massiccia
perdita nel flusso urinario di acqua, sodio, ma anche potassio.
- Ipopotassiemia
- Aumento della suscettibilit agli agenti infettivi
In circa il 50% dei casi la NTA si manifesta non con oliguria ma con un aumento del
flusso urinario.
Si parla di NTA non oliguria.
Prognosi
Se si ha solamente coinvolgimento renale la prognosi molto buona nel 90% dei casi.
Altrimenti, in caso di coinvolgimento multiorgano, lindice di mortalit pu salire oltre
il 50%.
Nefrite tubulo-interstiziale
Si tratta di un gruppo di malattie renali caratterizzato da alterazioni istologiche e funzionali
coinvolgenti i tubuli e linterstizio.
Tubuli e d interstizio possono essere coinvolti:
- Primitivamente nefriti tubulo interstiziali primitive.
158
- Secondariamente a coinvolgimento del glomerulo nefriti tubulo-interstiziali
secondarie
Inoltre le nefriti tubulo-interstiziali possono essere:
- acute:
rapida insorgenza
edema interstiziale
infiltrazione leucocitaria soprattutto da parte di neutrofili ed eosinofili
necrosi tubulare focale
- croniche
insorgenza lenta
fibrosi interstiziale
infiltrazione leucocitaria prevalentemente mononucleata
atrofie tubulari acute
Le nefriti tubulo-interstiziali primitive sono un gruppo di patologie con differenti
cause e differenti meccanismi patogene.
Si distinguono clinicamente dalle malattie tubuleri per lassenza di sindrome nefrosica
o nefritica e per la presenza di alterazioni della funzione tubulare che si possono
mettere in evidenza in modo insidioso con:
- ridotta capacit di concentrazione delle urine (poliuria o nicturia)
- perdita di sali
- ridotta capacit di escrezione di sali
- deficit isolati di riassorbimento o di secrezione
Pielonefrite ed infezione delle vie urinarie
La pielonefrite una grave complicanza delle infezione delle vie urinarie che possono
colpire vescica o reni e loro sistemi collettori, ed interessa tubuli, interstizio e pelvi
renale.
La pielonefrite pu essere:
- pielonerfite acuta: infiammazione suppurativa acuta causata dal danno diretto
di alcuni batteri e virus alla pelvi renale
- pielonefrite cronica: linfezione batterica gioca comunque un ruolo dominante,
ma levoluzione pi lenta e sono coinvolti altri fattori (reflusso vescica-
uretrale, ostruzioned ellle vie urinarie).
Patogenesi
Nella maggior parte dei pz con infezione del tratto urinario, i microrganismi infettanti
derivano dalla flora fecale del pz medesimo, e sono bacilli gram -, normali abitanti del
tratto intestinale (E. coli, Proteus, Klebsiella).
Si ratta dunque di uninfezione endogena che pu raggiungere il rene attraverso 2 vie:
159
- via ematogena: attraverso il flusso sanguigno. la via meno comune. Si verifica
in corso di setticemia o di endocardite infettiva. Si manifesta pi
frequentemente in pz molto debilitai, immunosoppressi o con grave ostruzione
renale
- infezione ascendente: dalle basse vie urinarie. la forma pi comune, richiede
una serie di passaggi poich vescica ed urine normalmente sono sterili.
TAPPE dellINFEZIONE ASCENDENTE:
1. colonizzazione della parte distale delluretra da arte di batteri coliformi: i
batteri devono possedere la capacit di aderire alle cellule della mucosa
uretrale.
2. accesso alla vescica dalluretra. Il passaggio vescica uretra pu avvenire in corso
di manovre di cateterizzazione uretrale o di altre manovre strumentali. In
assenza delle medesime linfezione molto pi comune nelle donne (uretra pi
breve, assenza di liquido prostatico che ha propriet antibatteriche,
modificazioni ormonli, traumi uretrali nel corso di rapporti sessuali).
3. moltiplicazione nella vescica. In condizioni normali questa non avviene, poich i
germi sono eliminati con il normale deflusso di svuotamento delle urine.
Tuttavia un ostacolo al deflusso o disfunzioni vescicali che determinino una
situazione di stasi, rendono posibile la moltiplicazione indisturbata dei batteri.
Dunque una patologia ostruttiva delle basse vie urinarie un fattore
predisponente alle infezioni del tratto urinario.
4. reflusso vescico-ureterale. sempre legato ad uninsufficienza della valvola
vescico-ureterale, che consente la risalita dei batteri dalla vescica allinternod
egli ureteri e dunque alla pelvi renale. Linsufficienza della valvola quasi
sempre determinata dallassenza o dallaccorciamento congenito della porzione
intravesciacle delluretere, cosicch luretere non riesce ad essere
sufficientemente compresso dai muscoli della vescica durante la minzione.
5. reflusso intrarenale. Lurina vescicole infetta spinta fino alla pelvi e penetra
profondamente nel parenchima renale lungo i dotti collettori che si aprono a
livello degli apici delle papille. pi frequente nei poli inferiore e superiore.
Pielonefrite acuta
Infiammazione suppurativa acuta del rene causata da alcuni batteri e da alcuni virus.
Condizioni predisponesti
- ostruzione del tratto urinario
- manipolazioni strumentali (cateterizzazione)
- reflusso vescicoureterale
- gravidanza: 4-6% delle gestanti che sviluppa una batteriuria che se non trattata
porta ad infezione urinaria sintomatica nel 20-40% dei casi
- sesso ed et del pz: 1-40 anni infezioni pi frequenti nelle donne. Con
laumentare dellet lincidenza negli uomini aumenta per lo sviluppo di
unipertrofia prostatica e le frequenti manipolazioni strumentali
- lesioni renali pre-esistenti, che possono causare cicatrizzazione ed ostruzione
intrarenale
- diabete mellito (> suscettibilit alle infezioni, pi frequenti manipolazioni)
- immunosprressione ed immunodeficienza
160
Morfologia
Caratterizzata da:
- flogosi interstiziale suppurativa distribuita a chiazza (ascessi focali), ma
soprattutto nei poli superiore ed inferiore. Inizialmente linfiltrato neutrofilo
limitato allinterstizio, poi coinvolge i tubuli con loro distruzione.
- Aggregati intraluminali di neutrofili distribuiti dentro i tubuli di tutto il
neurone coinvolto.
- Necrosi tubulare
- Il glomerulo carttersiticamente risparmiato
Complicanze: sono 3 caratteristicamente:
1. necrosi papillare: principalmente nei diabetici o nei pz con ostruzione delle vie
urinarie. Generalmente bilaterale, coinvolge entrambe le piramidi renali.
2. pionefrosi: in presenza di unostruzione totale o quasi, in particolare se nelle
alte vie urinarie. Lessudato suppurativo non drenato e riempie la pelvi
renale, i calici, luretere.
3. ascesso perinefrinico: estensione dellinfiammazione al tessuto perirenale
attraverso la capsula renale.
Guarigione:
1. linfiltrato neutrofilo viene sostituito da un infiltrato mononucleato con
macrofagi e plasmacellule e linfociti.
2. i foci infiammatori sono sostituiti da cicatrici, che si associano per quasi
sempre ad infiammazione, fibrosi, deformazione dei calici e della sottostante
pelvi.
Clinica
Esordio improvviso con:
- dolore allangolo costo-vertebrale
- segni sistemici di infezione (febbre e malessere)
- segni di irritazione vescicale ed ureterale: disuria, minzione imperiosa.
- Urina contenente leucociti (piuria): non permette la differenziazione delle
infezioni della lte e delle basse vie urinarie.
- Reperto di cilindri leucocitari, ripieni di neutrofili nelle urine, che dimostra il
coinvolgimento del rene (i cilindri si formano solo nei tubuli).
La pielonefrite non complicata ha generalmente decorso benigno ed i sintomi
scompaiono entro pochi giorni dallinizio della terapia antibiotica.
Pielonefrite cronica
La caratteristica fondamentale della pielonefrite cronica una flogosi tubulo-
interstiziale cronica, associata a cicatrici renali ed associata al coinvolgimento
patologico di calici e pelvi.
161
Solo la pielonefrite cronica e la nefropatia da analgesici colpiscono anche i calici.
Nefropatia da reflusso
la forma pi comune.
Si verfica precocemente nellinfanzia, per sovrapposizione di una infezione urinaria su
un reflusso vescico-ureterale ed intrarenale congenito.
Il reflusso pu essere unilaterale o bilaterale e conseguentemente portare a
cicatrizzazione ed atrofia di uno o di entrambi i reni.
Pielonefrite cronica ostruttiva
Lostruzione renale predispone alle infezioni renali e contribuisce allatrofia del
parenchima in un quadro di infiammazione cicatrizzazione ricorrenti, cio di
pielonefrite cronica.
Pu essere bilaterale (es. alterazioni ostruttive delluretra) e porta ad insufficienza
renale. Oppure monolaterale (es. calcolosi).
Morfologia
Macroscopica:
- reni irregolarmente cicatriziali.
- Se bilaterale il coinvolgimento asimmetrico (nella glomerulonefrite cronica i
reni sono diffusamente e simmetricamente cicatriziali).
- Si ha retrazione cicatriziale cortico-midollare grossolana, che sovrasta calici
tozzi, dilatati e deformati.
Microscopica:
- tubuli: atrofici in alcune porzioni, dilatati in altre. In presenza di infezione
attiva, vi possono essere cilindri di pus al loro interno.
- Interstizio: infiammazione cronica e fibrosi. Neutrofili in corso di infiammazione
attiva.
- Calice: circondato da fibrosi e da marcato infiltrato cronico
- Glomeruli di solito normali, con a volte fibrosi periglomerulare.
Pielonefrite xantogranulomatosa: forma rara caratterizzata da accumulo di macrofagi
schiumosi, frammisti a plasmacellule, linfociti, leucociti polimorfonucleati e a volte
cellule giganti. Spesso associato allinfezione da Proteus.
Clinica
Lesordio generalmente silente o insidioso.
162
I pz giungono allosservazione in fase relativamente avanzata, per la comparsa
graduale di insufficienza renale associata ad ipertensione oppure di giuria e
batteriuria ad un esame di routine.
La perdita della capacit di concentrazione tubulare pu provocare poliuria e nicturia.
Alcuni pazienti hanno una cicatrizzazione pielonefritica che determina alterazioni
glomerulari adattative secondarie alla perdita di massa renale, che sfociano in una
glomerulosclerosi focale e segmentale con elevata proteinuria.
La comparsa di proteinuria e glomerulosclerosi un segno prognostico sfavorevole.
Nefrite tubulo-interstiziale da farmaci ed agenti tossici
Farmaci ed agenti tossici possono provocare lesioni renali con 3 meccanismi:
1) innescano reazione immunologia interstiziale nefrite acuta da
ipersensibilit indotta da meticillina
2) provocano danno tubulare subdolo, ma cumulativo, che richiede anni pr
manifestarsi ed esita in insufficienza renale cronica nefropatia da
abuso di analgesici.
3) Provocano insfuiicienza renale acuta
Nefrite acuta da ipersensibilit
Reazione scatenata da una serie di farmaci in costante incremento.
In conseguenza dellassunzione di penicilline sintetiche (meticillina, ampicillina),
diuretici (tiazidici), FANS ecc
Inizia 15 gioni dopo lesposizione al farmaco.
Lesordio caratterizzata da:
- febbre
- eosinofilia
- rash cutaneo (25%)
- manifestazioni renali: ematuria, lieve proteinuria, leucocituria (con eosinofili),
sviluppo di insufficienza renale acuta con oliguiria (50%)
Morfologia
Alterazioni a carico dellinterstizio che mostra:
- edema pronunciato
- infiltrato leucocitario mononucleato (linfociti, macrofagi, eosinofili)
A volte tubulite, infiltrazione linfocitaria dei tubuli.
Patogenesi
Meccanismo di tipo immunitario dose-indipendente.
Si tratta di una reazione di ipersensibilit che pu essere:
- di tipo I (IgE mediata)
- di tipo IV (ritardata).
Probabilmente i farmaci agiscono su apteni che, durante la secrezione nei tubuli, si
fissano a componenti citoplasmatici o extracellulari delle cellule tubulari, acquisendo
cos propriet immunogene.
163
Il danno risltane dnque dovuto ad una reazione di tipo immunitario contro le cellule
epiteliali del tubulo o contro le loro mbr basali.
Clinica
Limmediata sospensione del farmaco prontamente seguita dalla guarigione.
Solo in alcuni pz anziani si pu avere,a volte, danno irreversibile del rene.
Nefropatia da analgesici
una forma di nefropatia cronica causata da unassunzione eccessiva di miscele
analgesicheI pz che sviluppano la malattia ingeriscono grandi quantit di una miscela
di almeno 2 antipiretci; nella maggior pare dei casi la miscela contiene fenacetina.
caratterizzata da necrosi papillare renale, che si instaura per prima, associata a
nefite tuvulo interstiziale e corticale che costituisce una manifestazione secondaria.
Pi comune negli uomini che nelle donne.
Particolarmente frequente in individui con cefalea riccorrente o dolori muscolari
cronici.
Morfologia
Macroscopica:
- reni normali o poco ridotti di volume
- corticale con aree depresse che rappresentano le zone di atrofia corticale che
sovrastano le papille necrotiche.
- Le papille mostrano vari gradi di necrosi, frammentazione, calcificazione e
distacco
Microscopica
- forme iniziali: necrosi a chiazze della papilla
- forme avanzate: necrosi dellintera papilla che speso rimane una passerella
priva di struttura.
Clinica
Sintomi precosi:
- incapacit di concentrare le urine
- acidosi renale
Frequentemente questi sintomi sono accompagnati da:
- cefalea
- anemia, sproporzionata a causa del danno sui globuli rossi indotto dai
metabolici della fenacetina
- sintomi gastrointestinali
- ipertensioni
- infezioni del tratto urinario; complicano circa la met dei casi.
Occasionalmente vengono escreti interi apici di papille renali e ci pu provocare
ematuria massiva o colica renale dovuta ad ostruzione ureterale provocata dai
frammenti necrotici.
164
La progressiva compromissione della funzione renale pu condurre ad insufficienza
renale cronica, ma con la sospensione del farmaco, la funzone renale pu stabilizzarsi
o migliorare..
165
Neoplasie dei testicoli
GENERALITA
I tumori del testicolo possono avere due differenti origini:
Cell germinali (Seminoma o Tumori germinativi non seminomatosi)
Cell dello stroma gonadico (5%)
I primi sono pi frequenti e molto spesso maligni con rapida diffusione metastatica
mentre i secondi sono a norma benigni.
Prognosi:
o Seminoma: 1 e 2(metastasi) decade guariscono il 95% dei pz.
o Non Seminomatose: 1 guarisce il 95%, 2 e 3 il 40%.
o Coriocarcinoma: sempre fatale!!!
Tumori a cellule germinali
Sono in netta ascesa nelle statistiche mondiali e rappresentando il 10% di tutte le
cause neoplastiche di morte e la neoplasia pi comune nei maschi appartenenti a una
fascia di et che va dai 15 ai 34 anni.
In questo tipo di neoplasie derivanti dalle cell gonadiche possiamo nel 40%
Colpisce maggiormente gli individui di razza bianca rispetto ai neri.
In generale sono molto rari ma fra in alcuni lassi di et rappresentano la patologia
neoplastica pi frequente:
25-29 anni per le forme non seminomatose
40-50 anni per le forme seminomatose
Et pediatrica per il tumore del sacco vitellino
Fattori predisponenti:
Criptorchidismo: permanenza di cell germinali a T troppo elevate.
Permanenza elementi germinali lungo la linea mediana: (come sopra).
Trattamenti estrogenici in vita intrauterina
Infertilit oligospermica
Familiarit per neoplasie testicolari o carcinoma mammario
dei casi
osservare lomogeneit istotipica allinterno della neoplasia, nel restante 60% si parla
di tumori germinali composti.
Della tipologia composta molti prendono origine da una neoplasia intratubulare a cell
germinali che si riscontra in compresenza nella quasi totalit delle neoplasie germinali
delladulto.
Tra le due tipologie di tumore vi sono correlazioni riguardanti la ploidia del DNA come
ad esempio nelle sopracitate neoplasie intratubulari (ancora in situ) si osservano
anomalie cromosomiche simili come lisocromosoma 12p.
166
Le osservazioni sul confronto dei vari aspetti dei due tumori depone a favore di una
comune istogenesi di ambedue le patologie, infatti derivano entrambi da cell germinali
in vario stadio di sviluppo.
Per quanto riguarda il primo tipo le cell neoplastiche si differenziano lungo la linea
gonadica dando origine al seminoma oppure possono dare origine a una massa di cell
totipotenti che possono rimanere anaplastiche (carcinoma embrionario) o differenziare
verso una linea extraembrionaria (coriocarcinomi o tumori del sacco vitellino).
Per quanto riguarda i tumori germinativi non seminomatosi (NSGT) si oseervano:
Carcinoma embrionario
Coriocarcinoma
Teratoma maturo ed immaturo
Tumore del seno entodermico o sacco vitellino
Questi tumori tendono a riprodurre le fasi dellembriogenesi e le proprie tappe
maturative.
Sono pi precoci rispetto al seminoma.
Questi tumori mostrano spesso un loro analogo nelle patologie neoplastiche dellovaio!
Patogenesi dei tumori a cell gerinali
Nonostante le precise cause scatenanti non siano ancora note si osservano dei fattori
predisponenti:
Criptorchidismo: la persistenza dei testicoli nelladdome con prolungata
esposizione a T ben pi alte di quelle a cui le gonadi maschili devono trovarsi
causa disfunzioni delle cell germinali.
Disgenesia testicolare: particolarmente indicativo nei pazienti con
femminilizzazione testicolare.
Fattori genetici: sono in corso studi che dimostrerebbero una familiarit nella
possibilit di sviluppare la malattia.
Tumori a cell dello stroma gonadico
Queste neoplasie colpiscono le cell di sostegno del parenchima testicolare
suddividendosi, perci, in due tipologie:
Tumore a cellule di Leydig (interstiziale)
Tumore a cellule del Sertoli (androblastoma)
Seminoma
Questa patologia rappresenta il 30-40% della totalit dei tumori che colpiscono il
testicolo.
Non si manifesta quasi mai nellinfanzia bens in et adulta colpendo principalmente
uomini nella terza decade di et.
Il seminoma ha un corrispettivo a livello dellovaio chiamato disgerminoma.
167
Il seminoma si pu presentare in due forme:
Classico (93%)
Spermatocitico
Seminoma classico
Si presenta come una massa solida, omogenea, giallastra, lucida e lobulata al taglio
con piccole aree di necrosi e componenti non seminomatose, con aspetti cistici ed
emorragici, che pu raggiungere dimensioni dieci volte maggiori quelle del testicolo
normale.
Morfologia
Si osservano nidi di cell neoplastiche circondate da sottili setti fibrosi, linfociti T (80%),
plasmacellule e reazioni granulomatose segno di una reazione che lo rende meno
aggressivo.
Le cell sono grandi, tonde o poligonali, con ampia rima citoplasmatica chiara per la
presenza di glicogeno.
Test diastatico: Si preparano due sezioni del tumore e una la si tratta con diastasi
che degrada il glicogeno. Mentre la prima sezione si colora con PAS quella trattata con
diastasi non si colora a causa della degradazione del glicogeno bersaglio elettivo del
PAS.
Si riscontrano anche numerosi elementi mitotici a causa della spermatogenesi.
Fenotipo
Fosfatasi alcalina placentare (PLAP): nel 40% circa dei pz. si riscontra a livello
plasmatico.
Mancata espressione di cheratine: tipica caratteristica delle forme
seminomatose.
E-caderina+ e -catenina- : utili per la diagnosi differenziale col carcinoma
embrionario o per distinguere diverse tipologie di cell allinterno del tumore.
Clinica
E bene effettuare una biopsia per ogni cm della massa in modo da evitare che
sfuggano focolai di cell tumorali non seminomatose.
I focolai possono essere composti da cell:
- Carcinoma anaplastico
- Cell giganti trofoblastiche
- Elementi del seno entodermico
168
E importante quantificarle per distinguere i tumori germinali misti che sono,
generalmente, pi aggressivi mentre le forme seminomatose con scarsa presenza di
focolai non seminomatosi hanno decorso meno grave.
Seminoma bruciato
Si evidenzia con voluminosa linfoadenite retroperitoneale a causa della diffusione
delle metastasi attraverso i linfatici del testicolo che drenano ai linfonodi situati in
prossimit dellilo renale.
Si chiama bruciato perch in questa tipologia si evidenzia un processo involutivo con
cicatrizzazione riscontrabile anche a livello delle metastasi.
Si possono effettuare biopsie in laparoscopia o tac-mirate ma, con questultimo metodo,
si preleva solo unesigua quantit di tessuto col rischio di prelevare da un zona di
necrosi rendendo cos inattuabile lanalisi istopatologica.
Spesso si trovano tumori lungo la linea mediana perch le cell germinali migrano in
questa zona durante lo sviluppo embrionale e, perci, non vuol dire che masse
tumorali cos localizzate siano per forza metastasi derivanti da neoplasie testicolari.
Seminoma spermatocitico
Costituisce il 4-7% dei seminomi e colpisce principalmente gli anziani.
Si manifesta spesso bilateralmente al contrario del classico.
La prognosi positiva perch non metastatizza e si risolve con terapia chirurgica.
Morfologia
Si osserva una tendenza alla maturazione verso stadi pi avanzati della
spermatogenesi con cell linfocito-simili (diagnosi diff. Con linfoma testicolare).
Assenti reazioni granulomatose e la presenza di glicogeno e PLAP.
Carcinoma Embrionario
Insorge normalmente tra i 20 e i 30 anni.
E pi aggressivo delle forme seminomatose.
Si presenta come una massa solida grigio-biancastra, non omogenea a causa della
disseminazione di focolai emorragici e necrotici dovuti alla crescita del tumore e
allinteressamento vascolare.
169
Se diagnosticato in fase precoce risulta trattabile, al contrario, diagnosticato in fase
tardiva, quasi sempre letale!
Morfologia
Si evidenziano cell immature, molto voluminose ma con rapporto nucleo/citoplasma
nettamente a favore del nucleo (non si evidenzia lampia rima citoplasmatica delle
forme seminomatose).
Le cell mostrano una maturazione verso elementi embrionari con formazione di
strutture alveolari o tubulari simili a papille.
Fenotipo
Cheratine+, E-caderina-, -catenina+ : contrario esatto dei seminomi.
CD30+ : sempre presente negli LH di tipo classico, mette il carcinoma
embrionario in diagnosi differenziale col tumore a grandi cell di tipo linfoide.
**Mai basare una diagnosi su un solo marker!
Teratoma
Teratoma: Tumore che tende a riprodurre disordinatamente delle componenti
dellorgano in cui sviluppa o delle strutture embrionali. Il suo sviluppo e
totalmente afinalistico.
Rappresenta il 5-10% dei tumori del testicolo.
In et infantile si presenta come forma benigna ed trattabile, in et adulta si
presenta in forma pi grave e il suo esito imprevedibile.
Le forme pure si presentano principalmente nei bambini mentre negli adulti si
riscontrano solo nel 2-3% dei casi.
Le forme miste con presenza di altri tipi istologici rappresentano il 45% dei casi.
Il teratoma si suddivide in due forme principali:
Maturo: presenta componenti tessutali mature che danno facilmente metastasi.
Immaturo: presenta ancora aspetti comuni ai tessuti embrionali.
Morfologia
Si presentano come voluminose masse che vanno dai 5 ai 10 cm di diametro.
Laspetto eterogeneo a causa della presenza di pi tessuti con zone solide a volte
cartilaginee e cistiche.
170
Si riscontra necrosi nelle varianti miste che presentano anche carcinoma embrionario
o coriocarcinoma.
I teratomi sono composti da pi tessuti (nervoso, muscolare, cartilagineo) disposto
disordinatamente e immerso in una matrice stremale fibrosa.
Raramente possono andare incontro a trasformazione maligna che si presenta con
linsorgere di tumori non germinali quali adenocarcinoma, carcinoma squamoso o
sarcoma.
Queste forme metastatizzano con molta aggressivit e sono altamente resistenti alla
chemioterapia.
La prognosi sempre data dalla componente pi aggressiva perci importante
effettuare biopsie a pi livelli del tumore per evidenziare eventuali componenti
differenti.
Coriocarcinoma
Rappresenta il 5% dei tumori del testicolo (interessa nella stessa % anche ovaio).
Metastatizza rapidamente colpendo i polmoni (99,9% diagnosi tardiva) Letale!!
per la sua pericolosit importante il suo riscontro nelle forme miste!
Deriva da una componente extraembrionaria e tende a riprodurre la placenta!
per questo motivo molto irrorato e ci fa s che invada i vasi metastatizzando
facilmente e causando aree di necrosi nella massa.
Morfologia
Sinciziotrofoblasti: cell grandi con nuclei atipici e abbondante citoplasma
Citotrofoblasti: cell poligonali e nucleo uniforme
Fenotipo
Cheratina 7+
hCG+ : evidenzia la sua derivazione placentare
Tumore del sacco vitellino (o seno endodermico)
Nei bambini fino a 2 anni la patologia benigna mentre negli adulti risulta molto
aggressivo e, allatto della diagnosi, ha gi dato metastasi poco ed poco responsivo
alla terapia.
Si presenta spesso in forma pura (80%).
Morfologia
Si evidenzia una struttura stromale lassa con formazioni cistiche.
171
Corpi di Sciller-Duval: sono strutture glomeruloidi disposte attorno allasse pascolo-
stromale che protrudono in strutture cistiche. Sono sempre
diagnostici.
Le cell risultano immature con rapporto nucleo/citoplasma fortemente a favore del
nucleo.
Fenotipo
1-fetoproteina+: ___mancano appunti!!!___
1-antitripsina+
transferrina+
cheratina+
Neoplasia germinale intratubulare
Sono forme in situ ovvero dentro i tubuli seminiferi contorti.
Si riesce a operare la diagnosi in tempi precoci.
Si riscontra nell80% dei testicoli affetti da neoplasie infiltrativi.
172
Patologia della prostata
Struttura
Organo extraperitoneale, di circa 20g., che circonda collo della vescica ed uretra.
una ghiandola a composizione tubulo-alveolare.
Le ghiandole sono composte da due strati cellulari:
1. strato basale di epitelio cuboide
2. strato di cellule cilindriche secretorie.
Le ghiandole hanno tutte membrana basale evidente e sono separate da uno stroma
fibromuscolare.
Gli androgeni testicolari sono di primaria importanza per regolare la crescita
prostatica, tanto ce la castrazione comporta atrofia prostatica.
1) Ipertrofia della prostata
2) adenocarcinoma della prostata
Ipertrofia benigna della prostata
Lipertrofia prostatica benigna una patologia molto comune nelluomo di et
superiore ai 50 anni, tanto da essere considerata una situazione parafisiologica.
Si caratterizza per liperplasia delle cellule stromali ed epiteliali che esita nella
formazione di ampi noduli, definiti, tipicamente localizzati nella regione pi centrale
della prostata.
Incidenza
Levidenza dellipertrofia prostatica si reperta:
- nel 20% degli uomini di 40 anni
- nel 35% degli uomini di 50 anni
- nel 65% degli uomini di 70 anni
- nel 90% degli uomini di 90 anni
Eziologia e patogenesi
Laumento di volume della prostata correlato con lazione degli androgeni.
Il mediatore terminale della crescita prostatica il dididrosterone, che viene
sintetizzato dalle cellule stremalei della prostata a partire dal testosterone circolante,
grazie allazione dellenzima 5 reduttasi.
Una volta che stato sintetizzato il DTH si lega a recettori nucleari presenti:
- nelle cellule stremali medesime ( azione autocrina)
- nelle cellule ghiandolari (azione paracrina)
attivando la trascrizione di fattori di crescita ad azione mitogena.
Gli estrogeni invece rendono le cellule stromali pi sensibili allazione del DTH.
La prostata dunque un organo ormono-dipendente che ha uno sviluppo negli anni
correlato alla stimolazione ormonale.
Infatti piccola nel bambino, cresce nel giovane adulto sotto la stimolazione del
diidrotestosterone, cresce ulteriormente nellanziano sotto stimolazione delle crescenti
quantit di estrogeni, che agiscono soprattutto sulla componente stromale.
173
Morfologia
Prostata di peso 60-100g.
Iperplasia nodulare nella zona centrale:
- inizialmente: noduli stromali grigi e pallidi senza secrezione
- successivamente noduli epiteliali tessuto giallo-roseo, di consistenza soffice,
con secrezione simil-lattescente
Clinica
Lipertrofia della prostata porta di fatto a due importanti effetti secondari:
1. Poich si tratta di una patologia della parte interna, centrale della prostata,
laumento di dimensione dei noduli provoca compromissione del canale
delluretra, con restringimento del lume e parziale ostruzione del lume
delluretra prostatica medesima.
2. La crescita del volume della prostata nella sua porzione superiore, alza il livello
del trigono vescicole e dellimbocco delluretra prostatica medesima, provocando
al termine della minzione un residuo urinario in vescica, con conseguente
distensione ed ipertrofia vescicale.
Questi due effetti secondari provocano a loro volta una serie di conseguenze:
a. nicturia e disuria: il pz sente il bisogno di urinare molto spesso, anche
durante la notte. Alla minzione tuttavia il pz urina pochissimo e con un
certo dolore, per lostacolo al flusso determinato dallostruzione
prostatica.
b. Difficolt ad iniziare la minzione e ad arrestare il mitto.
c. Maggiore suscettibilit alle infezioni vescicali, poich lurina che rimane
in stasi come residuo permanente pu infettarsi molto facilmente. Si ha
dunque un frequente sviluppo di cistiti, ma anche di pielonefriti e di
prostaticti, per la migrazione ascendente e discendente dei microbi lungo
le vie urinarie.
Diagnosi
Non viene fatta attraverso indagine bioptica per due motivi:
1. lagobiopsia che perfora tangenzialmente la capsula prostatica, non in grado di
arrivare fino alla zona pi centrale
2. listologia nodulare non pu essere apprezzata su campione cos limitato.
Terapia
IPB iniziale
Trattamento senza approccio farmacologico, n chirurgico, ma solo attraverso
modificazioni dello stile di vita:
- diminuzione dellintroito di liquidi soprattutto prima di coricarsi
- moderata assunzione di alcolici e caffeina
- orinazione ad intervalli definiti
174
IPB moderata o severa
Terapia medica con:
- anti- androgenici: inibitori della 5 redattasi, come il finasteride. Inducono
sostanziale decremento di volume della prostata e del grado di ostruzione.
- -litici che diminuiscono il tono muscolare prostatico, inibendo i recettori
adrenergici.
IPB resistente alla terapia medica
Trattamento chirurgico:
- resezione transuretrale della prostata (TURP): sie ntra con un endoscopio e si
raschia una parte delluretra ipertrofica per permettere il defluire dellurina.
efficace nellaumentare il flusso e diminuire il valore di residuo post-minzionale
Adenocarcinoma prostatico
la pi comune forma di candro nei maschi dei paesi occidentali e la seconda causa di
morte per neoplasia.
Incidenza
1 americano/europeo su 6 nel corso della vita sviluppa un cancro alla prostata.
Ogni 3 minuti viene diagnosticato un nuovo cancro alla prostata.
Il rischio di sviluppare un focolaio microscopico (che dunque non visibile n
allesploarazione rettale, n con metodi ecografici) nel corso della vita del 16%.
Il rischio di sviluppare un carcinoma prostatico metastatico potenzialmente letale
del 3-4%.
A dispetto dellelevatissima incidenza la mortalit per carcinoma prostatico
mediamente molto inferiore a quella di altri tumori epiteliali (es. carcinoma della
mammella).
Fattori di rischio
Accertati:
1. et: il fattore di rischio prevalente. Con il crescere dellet aumenta
esponenzialmente il rischio di carcinoma prostatico. Questo correlato, come si
vedr pi avanti, allaumento dei casi di ipertrofia prostatica benigna.
2. familiarit: Vi sono casi di tumori prostatici correlati alla eredit della linea
germinale di alcuni geni di suscettibilit del cancro prostatico. Questi sono i casi
pi aggressivi che incorrono in et pi giovane. Levidenza di una certa
familiarit di questa patologia stata dimostrata da alcuni studi epidemiologici
che vedono:
175
- 10% dei pz con carcinoma prostatico con un parente di primo grado affetto
- uomini con un parente di primo grado affetto da neoplasia prostatica
hanno rischio raddoppiato
- se i parenti sono due il rischio aumentato di cinque volte
3. razza etnica: gli Afroamericani hanno incidenza e mortalit in assoluto
maggiori, i Caucasici hanno incidenza e mortalit media, Gli Asiatici hanno
incidenza e mortalit in assoluto minori. Questa distribuzione etnica dovuta al
ruolo fondamentale degli androgeni nel mantenimento dellepitelio prostatico e
dunque al ruolo fondamentale degli androgeni come fattore permissivo del
tumore prostatico. Infatti il gene AR codificante per il recettore nucleare degli
androgeni un gene polimorfo, con lunghezza variabile di triplette CAG
ripetute. Studi hanno dimostrato che cellule con poche triplette ripetute di CAG
presentano aumentata sensibilit agli androgeni. Infatti poche ripetizioni sono
state riscontrate negli Afroamericani, i Caucasici hanno lunghezza intermedia,
gli Asiatici hanno la lunghezza maggiore.
Incerti:
1. Androgeni
2. Fattori dietetici
Esclusi:
1. Alcool
2. Fumo
3. Attivit sessuale
Diagnosi
I metodi diagnostici sono diversi:
1. esplorazione rettale: poich la localizzazione della neoplasia preferenzialmente
periferica e posteriore unaccurata esplorazione rettale pu evidenziare alcuni
tumori allo stadio precoce, proprio grazie alla loro posizione posteriore anche se
la metodica ha bassa specificit.
2. ecografia prostatica transrettale: anche questa metodica ha scarsa specificit e
sensibilit dunque viene utilizzata soprattutto durante lesecuzione della
biopsia, appunto, ecoguidata.
3. ricerca dellantigene prostatico specifico (PSA): attualmente utilizzata come
metodica prevalente di screening e di diagnosi del carcinoma prostatico. Il PSA
un prodotto dellepitelio prostatico, normalmente secreto con il liquido
seminale e con funzione lubrificante dei coaguli seminali che si formano a
seguito delleiaculazione. Nel soggetto normale unesigua quantit di PSA
circola nel sangue. Alti livelli di PSA (> 4 ng/ml) sono sempre presenti in caso di
tumore prostatico. Dunque un livello di PSA:
- minore di 4: situazione normale
- fra 4 e 10: possibile situazione neoplastica
- maggiore di 10: fortemente predittivo di neoplasia.
176
Non si tratta per di un marcatore tumore-specifico; elevati livelli di PSA, sebbene
minori, si riscontrano anche nellipertrofia prostatica, nella prostatite, nella
manipolazione strumentale, nelleiaculazione.
Poich la valutazione del PSA costituisce test di screening per le neoplasie, sono
state messe a punto miglioramenti nella valutazione del PSA.
a. valutazione della densit del PSA: rapporto tra il valore del PSA ed il
volume della ghiandola prostatica, che riflette la produzione di PSA per g.
di volume prostatico. Il valore massimo stabilito 0,15.
b. Curva di variazione del PSA nel tempo: pz con tumore alla prostata
mostrano un aumento dei valori di PSA nel tempo rispetto ai pz normali:
una valutazione che si fa su di un periodo di almeno 18/24 mesi, data la
forte variabilit a breve termine delle misure di PSA.
c. Rapporto tra PSA free e PSA legato nel sangue: il PSA esiste in due
forme.
Frazione maggiore: legata all alfa- chemotripsina
Frazione minore: libera
Il valore del rapporto PSA free/ PSA totale pi basso negli uomini con
carcinoma prostatico rispetto alle patologie benigne. Un valore di PSA <
15% fortemente predittivo del tumore.
Lo screening della PSA ha sicuramente rivoluzionato la diagnosi e la clinica del
carcinoma prostatico, ma possiede i suoi pro ed i suoi contro.
Pro:
a. aumento esponenziale del numero di casi diagnosticati
b. diagnosi e trattamento precoce in pazienti sempre pi giovani
c. oggi la maggior parte dei tumori prostatici viene diagnosticata in stadio
T1 dunque quando ancora fortemente confinata alla prostata
Contro:
a. diagnosi di carcinomi prostatici che non si sarebbero mai resi
clinicamente evidenti
b. trattamento chirurgico di tumori con andamento biologico indolente
c. a dispetto della grande quantit di tumori che ha messo in evidenza non
stata dimostrata una effettiva diminuzione della mortalit.
Il difetto della PSA proprio quello di non essere in grado di differenziare un
tumore a decorso indolente che non potrebbe mai essere letale e che dunque non
dovrebbe essere operato, da uno a decorso aggressivo che deve essere operato con
urgenza.
Inoltre nonostante ormai, dopo una fase di aumento esponenziale del numero di
tumori diagnosticati, tutti gli individui con sospetto tumore prostatico siano stati
diagnosticati grazie allo screening con PSA, non si avuto nessun miglioramento
dimostrabile dal punto di vista della mortalit.
Dunque sebbene il PSA non sia il golden standard per la diagnosi di cancro, in
questo momento non esistono test pi specifici e di facile utilizzazione.
4. mapping bioptici: vengono eseguiti mediante sonda ecografia transrettale,
dunque introduzione dellago a partire dal retto; lago perfora tangenzialmente
la capsula prostatica in diversi punti a partire dalla sua parte posteriore. Pu
177
essere eseguita in modo casuale o in modo guidato dallecografia, su zone
sospette, poco riflettenti gli echi degli ultrasuoni. In ogni caso per essere pi
sicuri di trovare il tessuto neoplastico, il numero delle biopsie deve essere molto
alto: si fanno almeno 10-12 biopsie, fino a 20-22 in pazienti molto a rischio,
finch non si ritrova il tumore.
Eziologia
Leziologia e la storia naturale di questo tumore sono state molto studiate, proprio per
la diffusione di questo tumore, che ha fatto s che colpisse anche persone note ed
importanti, e che ha reso possibile un notevole versamento di fondi per il suo studio.
Si cercata una correlazione fra:
- evoluzione morfologica del cancro della prostata
- evoluzione delle alterazioni genetiche
- evoluzione delle lesioni istologiche microscopiche (grading)
Evoluzione morfologica
La storia del cancro della prostata solitamente vede le seguenti tappe:
1. prostata normale con epitelio strutturato e sano
2. ipertrofia prostatica: come gi visto una condizione parafisologica che colpisce
un numero davvero molto alto di uomini. Lepitelio prostatico nellipertrofia si
mantiene normalmente costituito da due strati, quello staminale (basale) e
quello secernente. La prostatite inoltre una condizione predisponente al
verificarsi di infezioni vescicali (cistite) che possono facilmente estendersi alla
prostata.
3. prostatite: molto presente nellanziano a seguito dellipertrofia prostatica, ma
anche nel giovane. caratterizzata da uninfiltrato leucocitario a carico della
prostata, con frequente edema della medesima, associato ad aree di necrosi. Le
prostatiti sono difficilmente curabili con antibiotici e facilmente cronicizzano,
poich la maggior parte degli antibiotici penetra con difficolt nella prostata che
dunque viene a costituire un rifugio per i batteri. La prostatite un fattore
favorente lo sviluppo del cancro anche se non vi implicato direttamente, poich
causa di lesioni prostatiche e dunque di una reazione di difesa della prostata
con proliferazione compensatoria dello strato basale dellepitelio. La
proliferazione costituisce un fattore predisponente la trasformazione neoplastica
4. PIN (neoplasia intraepiteliale prostatica ad alto grado): lesioni focali
considerate precursori del carcinoma. Sono caratterizzate da ghiandole dilatate
benigne, le cui cellule, tutte uguali fra loro, mostrano evidenti atipie citologiche.
Le cellule possiedono gi le alterazioni genetiche tipiche della neoplasia. Inoltre
le lesioni focali tipiche della PIN, compaiono proprio nella zona periferica
esterna della prostata (come il tumore), e sono sempre presenti in caso di
cancro, a lato del medesimo. Tutte queste caratteristiche correlano la PIN al
tumore invasivo maligno. Tuttavia le cellule della PIN, sebbene siano con ogni
probabilit precursori del carcinoma, non sono ancora cellule carcinomatose,
178
poich le ghiandole hanno membrana basale ben definita, il che dimostra che la
lesione non si diffusa, non si infiltrata. Finch la lesione limitata dalla mbr
basale, non si tratta di iperplasia maligna. La Pin costituisce dunque un
campanello dallarme, una lesione pre-carcinomatosa che ci invita al
monitoraggio attento del pz; dopo dagnosi di PIN infatti nel 35% dei casi al
nuovo mapping si ha cancro.
5. Carcinoma prostatico: classicamente interessa la porzione periferico-posteriore
della prostata, rendendosi spesso palpabile allesplorazione rettale come un
tessuto duro e nodoso. Le ghiandole neoplastiche sono tipicamente pi piccole
del normale e viene persa listologia a due strati delle cellule epiteliali; le
ghiandole sono infatti ricoperte da una singola lamina di cellule cuboidi o
cilindriche. La membrana basale assente poich stata diffusamente
infiltrata. Le ghiandole sono affollate di cellule che presentano atipie marcate
come i nucleoli che sono tipicamente molto grandi. Le figure mitotiche in questo
tipo di cancro sono molto scarse e questo lo rende resistente alla terapia
chemioterapia che utilizza tipicamente farmaci citostatici. La scarsit della
proliferazione mitotica spiega anche la scarsit di necrosi, poich la
proliferazione non supera mai la capacit di vascolarizzazione del tumore.
6. Metastasi del carcinoma prostatico: la diffusione colpisce soprattutto le ossa.
Questo poich la PSA ha elevata affinit per le guaine mieliniche e dunque le
cellule neoplastiche tendono a risalire i nervi allinterno della prostata, che
fanno parte della cauda equina, per giungere fino alle ossa, in particolare alle
vertebre lombari, al femore prossimale, alla pelvi ossea, alle vertebre toraciche,
alle coste. Le metastasi ossee coinvolgono tipicamente gli osteoblasti. La
metastatizzazione ossea in fase avanzata si manifesta con erosione delle
vertebre. Vi pu essere anche metastatizzazione per via linfatica ai linfonodi.
Evoluzione delle alterazioni genetiche
1. epitelio prostatico normale
2. Fattore iniziante: perdita di alcuni geni (es. ELAC2), i cui prodotti sono correlati
alla detossificazione dei radicali liberi e dunque alla pulizia delle ghiandole
prostatiche. Questo sarebbe il fattore iniziante i quanto i radicali liberi inducono
lesione e dunque proliferazione cellulare. Dunque uniniziazione del tumore si
avrebbe in caso di prostatite associata a peridta di questi geni.
3. Fattori promuoventi: ulteriori mutazioni o perdita di geni coinvolti nella
proliferazione cellulare. Per esempio la perdita e la metilazione di p27 o
lipermetilazione di GSTP1, gene promotore della glutatione transferrasi, che ne
blocca lespressione. Questo gene un punto importante nelle vie di
segnalazione che prevengono il danno al genoma cellulare.
4. Mano a mano che il tumore evolve verso la malignit, si perde la regolazione
della proliferazione per perdita di geni sempre pi importanti, come PTEN e
p53.
5. Si arriva ad un certo punto in cui la cellula non pi dipendente per la sua
crescita dal DTH. la fase dellormono-indipendenza, dove la crescita cellulare
del tutto incontrollata e smettono di essere efficaci i farmaci anti-androgeni. A
questo punto si devono utilizzare chemioterapici, che sono molto meno efficaci
data la scarsa attivit fitogena del tumore.
179
Grading del tumore
Si utlizza la gradazione di Gleason, che divide il tumore sulla base del profilo
strutturale architettonico in 5 gradi.
Grado 1: tumore ben differenziato. Ghiandole neoplastiche di aspetto
uniforme e tondeggiate, piccole, regolari, vicine tra loro, circoscritte in
noduli ben definiti.
Grado 2
Grado 3
Grado 4
Grado 5: non c pi alcuna differenziazione ghiandolare, il tumore
completamente indifferenziato. Le cellule neoplastiche infiltrano lo
stroma sotto forma di cordoni, lamine, nidi, di aspetto solido.
Dunque si va dal tumore pi differenziato e con maggiore conservazione della
struttura ghiandolare, al pi indifferenziato, con perdita completa della struttura
ghiandolare. La valutazione come visto semi quantitativa e si basa su criteri
architettonici difficilmente quantizzabili.
La maggior parte dei tumori non presenta solo un quadro ghiandolare.
Presenza di due quadri ghiandolari: si somma il grado dominante a quello
sottodominante.
Presenza di tre quadri ghiandolari: si somma il quadro dominante al pi alto dei due
gradi sottodominanti.
Attraverso la somma dei gradi pi rappresentati si ottiene lo score di gleason, che va
da 2 (tumori molto ben differenziati, 1+1) a 10 (i tumori pi anaplastici 5+5).
Lo score di gleason uno dei migliori indicatori per una prognosi predittiva.
Pz con score di Gleason:
- 1-3: hanno prognosi molto buona
- 4-7: hanno una prognosi decisamente peggiore
- 8-10: pz che non vale neppure la pena di trattare chirurgicamente, tanto la
rognosi comunque infausta
Stadiazione del tumore
T1: tumore limitato dalla capsula prostatica. Presente tutto da uno stesso lato
della prostata.
T2: tumore limitato dalla capsula prostatica. Presenta da entrambi i lati della
prostata.
T3a: invasione extraprostatica senza vescichette seminali
T3b: invasione extraprostatica con vescichette seminali
T4: invasione diretta di organi contigui.
180
Inoltre viene valutata la presenza o lassenza di metastasi linfonodale (N0/N1), poich
pu sempre associarsi ad un decorso fatale.
La grande differenza prognostica qui si ha tra gli stadi:
- T1 e T2 (limitati alla prostata): se il tumore viene eliminato il paziente pu
guarire completamente senza andare incontro ad ulteriori recidive.
- T3 (a e b) e T4 ( che hanno attraversato la capsula e si ritrovano anche al di
fuori della prostata): anche se il tumore viene eliminato completamente, non si
pu mai dire che si tratti di guarigione completa.
Da questa serie di valutazioni vengono fuori sostanzialmente due differenti tipi di
tumore:
1) tumore che colpisce prevalentemente soggetti giovani: legato ad una
familiarit, molto aggressivo, con elevato score di Gleason ed elevato
stadio (T3 o T4). Va operato con urgenza.
2) Tumore che colpisce prevalentemente soggetti anziani: frequentemente
non legato a familiarit, ma ad et, si instaura di solito su precedente
ipertrofia prostatica, basso score di Gleason, e basso stadio (T1 o T2). Pu
non necessitare di terapia chirurgica, poich con decorso indolente.
Tuttavia lo screning con la PSA non in grado di fare una differenziazione fra queste
due forme, e sebbene grading e screening siano indicatori utili non possono dirci quali
tumori siano da trattare e quali no. Oggi dunque si tende a trattare aggressivamente
tutti i tumori.
Terapia
1. terapia chirurgica
2. terapia ormonale: si utilizza nei casi di pz non operabili chirurgicamente. Ha
effetti molto forti sul tumore e lo pu portare a regressione completa, prima che
il tumore arrivi allo stadio di ormono-indipendenza, nel quale essa non ha pi
alcun tipo di utilizzo. basata sul blocco della stimolazione androgenica da
parte del DTH che permette la sopravvivenza delle cellule epiteliali., Si
utilizzano tre tipi di bloccanti:
- bloccanti della 5 alfa redattasi
- bloccanti del recettore: impediscono la dimerizzazione del recettore
- bloccanti del recettore GNRH: agiscono a feedback sullipotalamo.
Il blocco completo si ottiene solo attraverso lutilizzo contemporaneo dei tre
bloccanti, che tuttavia sconsigliato perch facilita lo sviluppo di ormono
indipendenza tumorale. Dunque solitamente si utilizzano blocchi di uno-due
farmaci alla volta a cicli intervallati.
Questi farmaci ed in particolare i bloccanti della 5 alfa redattasi. (finasteride),
vengono utilizzati anche nellipertrofia prostatica.
Accade molto spesso che lutilizzo di questi farmaci come cura dellipertrofia
prostatica diminuisca i livelli di PSA plasmatici, provocando molti falsi negativi
allo screening.
Inoltre successivamente allutilizzo di questi farmaci assolutamente impossibile
fare un grading fedele, poich essi, inducendo forte apoprtosi delle cellule epiteliali
181
creano unimmagine morfologica altamente indifferenziata, che sembra di grado 5,
ma che non lo .
Questa terapia conferisce comunque una capacit di sopravvivenza molto lunga, di
almeno 10 anni.
3. Radioterapia: si utilizza in pz con cancro della prostata a presunta bassa
malignit, poich la prostatectomia completa altamente invalidante
(impotenza e molto spesso disuria). Consiste nel posizionamento di semi
radioattivi nella ghiandola prostatica e comporta:
- regressione, talora totale
- tessuti normali che mostrano atipie marcate, per le radiazioni
182
Patologia della mammella maschile
GENERALITA
La mammella maschile consiste in un capezzolo e in un rudimentale sistema duttale
che si conclude in gemme terminali prive di formazioni tubulari.
Ginecomastia
Consiste in un ingrossamento della mammella maschile che pu essere monolaterale o
bilaterale.
Si presenta come un ingrandimento sottoareolare simile a un bottone o, addirittura,
pu simulare una mammella femminile adolescente.
Lunica DD possibile quella dal raro carcinoma della mammella ma non un fattore
di rischio per la patologia neoplastica!
La ginecomastia un segnale di ipersetrinismo che pu essere segno di:
Cirrosi epatica
Tumore testicolare funzionante
Morfologia
Si osserva una proliferazione di un denso tessuto connettivo collageno e uniperplasia
micropapillare dellepitelio dei dotti. Rara formazione di lobuli.
Carcinoma
Si manifesta con un rapporto inferiore all 1:100 rispetto alle donne e con una
percentuale di insorgenza nella vita di un uomo dello 0,11% contro il 13% della donna.
I fattori di rischio sono gli stessi che nella donna:
episodi allinterno della propria famiglia
ridotta funzione testicolare ed epatica con sovraesposizione agli estrogeni
et
infertilit e obesit
I fattori prognostici e listopatologia sono gli stessi della patologia femminile, spicca
unicamente unaumentata espressione dei recettori per gli estrogeni.
La secrezione dal capezzolo un sintomo distintivo!
183
Neoplasie della vulva, vagina e cervice uterina
Cervice uterina
La cervice uterina si divide in due porzioni:
Endocervice: rivestita da un epitelio cilindrico semplice
Esocervice: rivestita da un epitelio squamoso non cheratinizzato
Il punto di passaggio tra queste due tipologie di epiteli prende il nome di
giunzione squamocolonnare ed una zona molto importante perch la sede di
partenza della cancerogenesi che colpisce la cervice.
Nonostante il carcinoma cervicale rappresenti il 5% delle cause di morte per tumore
nelle donne negli ultimi anni si verificato una diminuzione della mortalit
nonostante il mantenimento dellincidenza per merito della diagnosi precoce che si
effettua col PAP Test.
>> Questo esame consiste nel raschiamento delle cell dello strato superficiale
dellepitelio cervicale con conseguente analisi citologica.
Citologia
Le cellule dello strato basale (germinale) dellepitelio sono giovani e ancora allinizio
del processo maturativi: poggiano su una membrana basale e sono le cell staminali
dellepitelio, che servono al turnover dellepitelio medesimo. Man mano che si sale agli
strati superiori, le cell mature modificano le loro caratteristiche citologiche portando a
termine liter maturativo. Il ricambio completo avviene in circa 20-30 giorni.
Allesame microscopico le tappe della maturazione sono principalmente 3:
Cell dello strato basale (immature): Rapporto nucleo/citoplasma a favore del
nucleo.Abbondanza di figure mitotiche. Abbondante nucleo e citoplasma rosa
per ingente presenza di organelli.
Cell degli strati intermedi (maturazione): Aumenta il citoplasma che diventa
pi chiaro per la perdita di alcuni orfanelli, mentre i nuclei si fanno
progressivamente pi coartati.
Cell dello strato superficiale (mature): Si evidenziano cell con citoplasma
molto chiaro e nuclei picnotici, in questo strato le cell vanno apoptosi per
lasciare posto alle cell degli strati sottostanti in maturazione.
PAP Test
Il PAP test unanalisi molto utile ed utilizzata perch consente la valutazione di un numero molto ampio di donne
coniugando un basso costo con una grande efficacia.
Sfrutta la semplicit della cervice che deriva dal fatto di essere:
- formata da due epiteli differenti
- comunicante con lesterno
184
Come detto in precedenza il PAP Test consiste nel prelievo mediante raschiamento
dello strato superficiale dellepitelio cervicale e, mediante striscio su vetrino del
campione ottenuto, si analizza se la pz presenta cell con morfologie potenzialmente
pericolose.
Il test utile perch mira allanalisi di cell che, in un soggetto normale, dovrebbero
risultare mature provenendo esse dallo strato superficiale: dunque le cellule asportate
dovrebbero apparire con citoplasma otticamente vuoto e con piccolo nucleo.
In alternativa si possono asportare:
- cellule non completamente mature circondate da granulociti e spesso da sangue. In questo caso probabile
che si tratti di donne con un disturbo della proliferazione che non viene ad essere necessariamente
neoplastico. Per esempio si tratta spesso di situazioni infiammatorie, che causano iperplasia compensatoria,
come unulcera.
- Cellule con caratteristiche morfologiche molto lontane dalle cellule apoptotiche,
ma anche dalle cellule dello strato basale: si tratta solitamente di cellule
formate pressoch esclusivamente da nucleo ed abnormi. In questo caso le
cellule vengono denominate dal citologo come carcinomatose.
Se, infatti, si trovano cell dallaspetto prevalentemente immaturo in questo campione
il rischio di una patologia neoplastica molto probabile.
Il PAP Test pu presentare tre principali esiti:
Cell mature: completa normalit del campione
Cell giovani con cell grandi 1/3 che risultano essere eosinofili: in questo caso si
riscontra sicuramente un problema di proliferazione dovuto, probabilmente, a
un ulcera che spinge alla proliferazione per riparare il danno.
Cell abnormi con nucleo enorme: queste cell differiscono sia dalle cell mature
che da quelle basali e fanno propendere per una diagnosi di neoplasia.
I passaggi che portano alla trasformazione neoplastica sono i seguenti:
1. epitelio colonnare normale
2. metaplasia (tutti gli epiteli colonnari vanno facilmente incontro a metaplasma
3. alterazione dellequilibrio dellepitelio
4. intervento di fattori trasformanti inizianti (prevalentemente infezione da
papillomavirus) e fattori cotrasformanti.
5. iniziazione e proliferazione neoplastica allinterno dellepitelio
Patogenesi
Si osservato che, nella maggioranza dei casi, la neoplasia cervicale associata
allinfezione da HPV (95%).
I sierotipi pi pericolosi per questo tipo di patologia sono il 16 e il 18.Il genotipo virale
pu essere identificato mediante PCR: dunque una donna affetta da papillomavirus
deve essere caratterizzata anche da un punto di vista molecolare.
Nel 2000 uscita una ricerca su Science con la proposta di sottoporre a resezione
chirurgica della cervice tutte le donne portatrici di HPV 16 e 18 a testimoniare la reale
correlazione tra linfezione virale e lo sviluppo di carcinoma.
185
Il virus esplica la sua funzione oncogena interferendo con la funzione di p53 tramite i
geni virali E6 ed E7.
Molto spesso le cellule infettate da HPV hanno segni distintivi allesame citologico: si
tratta di cellule con ampio citoplasma otticamente vuoto e cromatina addensata e
granulomatosa, dette coilociti.
Altri genotipi di HPV sono responsabili anche di una patologia benigna a trasmissione
sessuale denominata condiloma acuminato della vulva (sono lesioni piatte o
arborescenti che possono interessare anche vagina, perineo, spazio perianale). Nelle
cell di questa patologia il genoma virale si riscontra in forma epitomale mentre nella
neoplasia integrato col genoma cellulare.
Neoplasia intraepiteliale cervicale (CIN)
Nella giunzione squamocellulare lepitelio pu andare incontro a metaplasia squamosa
e, nel caso entri in contatto con altri fattori costraformanti, pu dare origine alla
neoplasia.
Nella CIN si evidenzia sempre la presenza di HPV e lo si fa con due metodi:
PCR con amplificazione del genoma virale e poi elettroforesi
Ibridazione con sonde marcate sul campione patologico stesso (in situ)
Inizialmente viene fatto un esame di diagnostica citologica: questo ci d limpressione di quella che la popolazione di
cellule e permette di dire se sono presenti o meno cellule neoplastiche, ma non apporta nessun contributo al concetto di
grado del tumore. Pu valutare i caratteri di atipica delle singole cellule, ma non consente la valutazione della
displasia, che un concetto citologico ed istologico.
La valutazione della displasia richiede infatti la valutazione della cellula e del
rapporto delle varie cell fra di loro, dunque richiede unanalisi del tessuto, un esame
istologico.
Allinizio si evidenziano le lesioni intraepiteliale squamose ma, non potendo fare una
stima precisa del grado di displasia, si cerca una classificazione generale che tenga
conto di alcuni elementi. Gli esiti possibili sono 4:
La cervice si presenta negativa alla presenza di cell trasformate.
Presenza di granulociti polimorfonucleati, leucociti ed emazie e cellule dello
strato basale che denotano una flogosi Infatti anche una minima alterazione
infiammatoria denota alterazione nello sviluppo delle cellule.
Cell irregolari atipiche coerenti con infezione da HPV (SIL di basso grado).
SIL=lesione epiteliale squamosa)
Cell neoplastiche con eventuali cell infettate da HPV (SIL di elevato grado)
Nel caso sia stata evidenziata una SIL di basso o di elevato grado si procede ad un secondo step che consiste nella
biopsia, con successivo esame istologico; in questa maniera viene valutato un tessuto orientato che permette di valutare
il reale grado di displasia e la reale presenza di tumore.
Allesame istologico si evidenzia un CIN che pu essere classificato in tre differenti
tipi:
CIN1: alterazioni del rapporto nucleo/citoplasma e delle cellule
limitate al terzo inferiore. Displasia lieve. Corrisponde ad un SIN
di basso grado
186
CIN2: alterazioni molto pi marcate delle cellule che interessano
i due terzi inferiore. Displasia moderata. Corrisponde ad un SIN
di grado elevato e le cellule sono chiamate carcinomatose.
CIN3: alterazioni abnormi delle cellule che interessano tutto lo
spessore epiteliale. Inoltre nellepitelio neoplastico compaiono
spesso troppe mitosi. Diaplasia severa. Corrisponde ad un SIN di
grado elevato e le cellule sono chiamate carcinomatose.
Solitamente il problema risiede nella diagnosi delle lesioni precoci che non si riescono
rilevare ad occhio nudo. Viene dunque utilizzato uno strumento, detto colposcopio che
consente di vedere la cervice ingrandita di venti volte.
Allesame con il colposcopio la cervice appare con una forma simile ad una ciambella,
con un buco centrale, lorifizio uterino esterno, che corrisponde alla giunzione squamo-
colonnare.
Con lesame effettuato col colposcopio, la rilevazione di zone di trasformazione atipica
molto pi facile.
Si possono vedere:
- aree atipiche che divengono bianche dopo spennellatura della cervice medesima
con lacido acetico (acetowhite epithelium).
- Vasi atipici: ogni qual volta si rileva la presenza di vasi atipici si tratta di una
lesione iperplastica o neoplastica con conseguente aumento notevole del numero
delle cellule.
Lesame al colposcopio permette dunque di rilevare le zone atipiche e di effettuare una
biopsia mirata, non massiva, dellepitelio dellutero.
Carcinoma a cellule squamose
Si presenta dalla seconda decade di vita fino alla vecchiaia, il picco di incidenza trai
40 e 45 anni, mentre le prime lesioni precancerose si evidenziano intorno ai 30 anni.
Morfologia
Questa patologia si presenta nei tre caratteristici quadri:
Fungoide (pi frequente)
Ulcerato
Infiltrante
Il cancro molto aggressivo ed invade le strutture circostanti fino a raggiungere
peritoneo, retto, vagina, vescica, ureteri e linfonodi locali dando metastasi a fegato,
polmoni e midollo osseo.
Le cell sono molto grandi e presentano tre varianti:
Cheratinizzanti
Non-Cheratinizzanti
Squamose (sottogruppo poco frequente)
187
Il 10-25% di neoplasie della cervice costituito da altre forme di origine ghiandolare
come gli adenocarcinomi e i carcinomi adenosquamosi che presentano caratteri misti e
hanno prognosi pi severa.
Stadiazione
Stadio 0: Carcinoma in situ (CIN III)
Stadio I:
Ia: carcinoma preclinico (diagnosi microscopica)
Ia1: carcinoma microinvasivo (invasione stromale non oltre i 3mm)
Ia2: massima invasione trai 5 e i 7mm
Ib: carcinoma invasivo ristretto alla cervice e maggiore di Ia2
Stadio II: Carcinoma esteso oltre la cervice ma non alla parete pelvica, interessa i 2/3
superiori della vagina.
Stadio III: Esteso alla parete pelvica, invade tutta cavit pelvica e quindi tutta la
vagina.
Stadio IV: Esteso oltre la pelvi alle mucose di vescica e retto. Presenza di metastasi.
Clinica e Trattamento
Prevenzione, controllo e risoluzione delle patologie neoplastiche della cervice si
esplicano secondo uno schema preciso:
Screening (PAP Test)
Test per lHPV
Diagnosi istologica
Rimozione lesioni precancerose
Rimozione chirurgica dei tumori invasivi
Radio e Che mio
Vaccini contro HPV (?? Ancora in fase di studio??)
La patologia evolve lentamente perci opportuna la reiterazione a intervalli regolari
del PAP Test.
Non tutte le atipie evidenziate nellesame citologico sono preludio di cancro perci in
certi casi opportuna unulteriore indagine mediante colposcopia.
Vulva
Condiloma acuminato
Le alterazioni vulvare a crescita benigna o simil-verrucoide si presentano in tre forme:
Condiloma acuminato
Polipi mucosi
Condiloma lato luetico
188
Il condiloma una lesione squamosa indotta dal papilloma, una forma tumorale
benigna a trasmissione sessuale.
Possono essere solitari ma sono frequentemente multipli e coinvolgono la vulva, il
perineo e la zona perianale ma possono estendersi anche alla cervice.
Morfologia
Il condiloma una proliferazione arborescente di epitelio squamoso stratificato
sorretto da uno stroma fibroso.
Le cell presentano atipia nucleare con vacuolizzazione perinucleari (coilocitosi)
I condilomi hanno come agente eziologico lHPV, specie sierotipi 6 e 11, che matura
negli strati dellepitelio ed responsabile della caratteristica coilocitosi.
A eccezione dei pz immunocompromessi i condilomi spesso regrediscono e non sono
considerati lesioni precancerose.
Carcinoma e neoplasia intraepiteliale vulvare
- Neoplasia maligna rara (rappresenta appena il 3% di tutti i tumori genitali
femminili)
- I 2/3 di questi tumori riguardano donne che hanno passato la 6 decade di et
- L85% di questi tumori sono carcinomi a cell squamose
- Il restante 15% sono carcinomi basocellulari, melanomi e adenocarcinomi
Eziologia, patogenesi e manifestazione clinica
Possiamo dividere la neoplasia intraepiteliale in 2 gruppi:
Associato allHPV
Spesso preceduta da neoplasia intraepiteliale vulvare (VIN)
- Atipia delle cell epiteliali
- Aumentata attivit mitotica
- Mancanza di differenziazione
Placche biancastre o pigmentate a livello vulvare
Aumento della frequenza in donne con pi di 40 anni
Frequentemente multicentrica
10-30% associata a neoplasia squamosa di vagina e cervice
90% dei casi contiene il genoma di HPV (in particolare sierotipi 16 e 18)
Regressione spontanea nelle donne giovani
Aumento di progressione verso il cancro con l aumento dellet e con quadri di
immunodepressione
189
Associato a iperplasia delle cell squamose e a lichen scleroatrofico
Non associato ad HPV
Alcune alterazioni genetiche del lichen o delliperplasia possono causare invasione
stromale
Altre alterazione possono portare a una VIN atipica definita VIN simplex (o
differenziata)
Associati a un aumento dellaccumulo della p53
Morfologia
Distinte lesioni color carne o pigmentate
Lesioni lievemente rilevate che possono presentare ipercheratosi
Lo sviluppo pu essere esofitico o endofitico con possibili ulcerazioni
Quelli del secondo gruppo possono svilupparsi nel contesto di una flogosi
Manifestazioni cliniche
Fastidio locale
Prurito
Essudazione dovuta allinfezione
Esame istologico
I tumori associati ad HPV e a VIN presentano una modalit di crescita simil-epiteliale
che pu essere ben differenziata (verrucosa) o scarsamente differenziata (basalioide).
I tumori HPV negativi presentano spesso crescita invasiva con forte cheratinizzazione.
Evoluzione del tumore
Il rischio di evoluzione in corso della VIN in funzione dellet, dellestensione della
neoplasia e dello stato immunitario.
La diffusione metastatica legata anchessa alla dimensione della lesione e alla sua
profondit contando anche il coinvolgimento dei linfatici.
Le stazioni linfonodali colpite sono:
- Inguinali
- Pelvici
- Iliaci
- Periaortici
Dalla disseminazione metastatica gli organi pi colpiti sono:
- Polmoni
- Fegato
- Altri organi
Vi sono delle rare varianti del carcinoma squamocellulare non associate ad HPV:
- Carcinomi verrucosi
- Carcinomi basocellulari
190
Queste forme difficilmente metastatizzano e si trattano con ampia escissione
chirurgica.
Malattia di Paget extramammaria
E una rara lesione vulvare o perianale simile nelle sue manifestazioni cutanee a
quella propria della mammella.
Caratteristiche:
- Pruriginosa
- Colore rosso e ben demarcata
- Incrostata
- A livello delle grandi labbra
Pu essere accompagnata da un ispessimento sottomucoso e da un tumore.
Morfologia
Le cell neoplastiche appaiono:
Ampio citoplasma finemente granulato con presenza di mucopolisaccaridi
Disposte in singolo strato o in ridotti gruppi allinterno dellepidermide
Distinguibili dalle cell epiteliali per presenza di un alone chiaro che le circonda
Possono presentare differenziazione (autocrino, eccrino, cheratinocitico)
Derivano da cell progenitrici primitive
Le lesioni vulvare sono di solito limitate a:
- Epidermide
- Follicoli piliferi
- Ghiandole sudoripare adiacenti
Prognosi
La forma intraepidermica ha prognosi favorevole, pu persistere decenni senza
presentare caratteri invasivi.
La forma associata al carcinoma (rara) ha prognosi sfavorevole.
Presenta recidive frequenti perch le cell di Paget possono estendersi oltre la lesione
macroscopicamente visibile.
Melanoma maligno
E una patologia molto rara che presenta il 5% delle neoplasie vulvare e appena il 2%
di tutti i melanomi nella donna.
Il picco di incidenza tra la 6 e la 7 decade.
Le caratteristiche biologiche e istologiche sono quelle tipiche del melanoma.
191
Il tasso di sopravvivenza a 5 anni <32% per ritardi nella diagnosi e per la
caratteristica di cominciare presto a crescere verticalmente.
La mortalit del 60% per le lesioni che superano in profondit linvasione di 1mm!
DD con malattia di Paget dato che macroscopicamente possono assomigliarsi:
Reattivit ad anticorpi anti-S100
Assenza di reattivit ad anticorpi contro Ag carcinoembrionario
Mancanza di mucopolisaccaridi
Vagina
Neoplasia intraepiteliale e carcinoma squamocellulare
Il carcinoma primitivo della vagina molto raro, rappresenta l1% dei tumori maligni
dellapparato genitale femminile e di questi il 95% sono carcinomi a cell squamose.
La maggior parte associata ad HPV!
I fattori di rischio sono rappresentati dal pregresso carcinoma della cervice e della
vulva.
Morfologia
In genere localizzato nella vagina postero-superiore.
Esordisce con unarea di ispessimento epiteliale associata a displasia delle cell
epiteliali con progressione verso una massa simile ad una placca che invade cervice e
strutture perivaginali.
Le lesioni nei 2/3 inferiori metastatizzano ai linfonodi inguinali.
Le lesioni superiori tendono a coinvolgere i linfonodi iliaci regionali.
Questi tumori si rendono manifesti attraverso:
Sanguinamento irregolare
Leucorrea
Alcune volte possono rimanere silenti o si manifestano con la sola insorgenza di fistole
vescicali o rettali.
192
Neoplasie dellutero
Generalit
Lutero composto prevalentemente da muscolatura liscia, il miometrio che circonda
la cavit endometriale.
Lendometrio che riveste la cavit una mucosa formata da ghiandole endometriali e
da stroma.
Lutero una struttura ormono-dipendente sotto stimolo ormonale continuo.
In particolare lendometrio sotto linflusso di estrogeni e progesterone, sintetizzati
dallovaio sotto controllo a sua volta di FSH e LH prodotti dalladenoipofisi (asse
ipotalamo-ipofisario).
Le strutture regolate da estrogeni e progesterone sono utero, endometrio e mammella.
Lendometrio sottoposto ad un ciclo mensile, il ciclo mestruale, di periodico
sfaldamento della met superiore fino ai due terzi: il terzo basale, non risponde agli
stimoli ovarici ed quindi costantemente preservato.
Il ciclo mestruale vede unalternanza di due fasi di stimolazione:
- fase estrogenica o proliferativa (14gg.): crescita estremamente rapida sia delle
ghiandole sia dello stroma, sotto linflusso degli estrogeni che hanno azione
anabolizzante e che provocano aumento del numero delle cellule. Se il ciclo si
accorcia o si allunga si hanno alterazioni della sola fase estrogenica.
- fase progestinica o secretiva (14gg): le ghiandole endometriali, non proliferano
pi, ma cominciano la loro attivit secretoria, divenendo mano a mano pi
ingrossate e tortuose, sotto lo stimolo del progesterone. Questa fase sempre
stabile e dura sempre 14 giorni.
Se non si ha la fecondazione si ha diminuzione dellimput estro-progestinico con
conseguente sfaldamento della mucosa.
Molte cancerogenesi sono ormono-dipendenti ed in particolare dipendono
dallestrogeno.
Non necessario avere nel siero alti livelli di estrogeno in assoluto, per i meccanismi
di iniziazione del tumore basta solamente una prevalenza della fase estrogenica su
quella progestinica.
Situazioni di iperestrenismo assoluto (elevata concentrazione di estrogeni nel sangue):
Sono situazioni molto rare che possono essere per esempio:
tumori della teca ovarica
patologie dellovaio: ovaio policistico.
Cancro della mammella
193
Situazioni di iperestrenismo relativo (maggiore esposizione agli estrogeni, senza
aumento in assoluto nel sangue dei livelli di estrogeni, ma solo con aumento degli
stessi rispetto al progesterone):
donna con cicli molto lunghi ( aumenta solo la fase estrogenica)
menarca precoce e menopausa tardiva
assenza di gravidanza ( nullipare): la gravidanza blocca lasse ipotalamo-
ipofisario, dunque blocca lovulazione ed il ciclo mestruale.
Obesit: facilita la conversione di ormoni surrenalici, presenti anche nel tessuto
adiposo, come lamminostrenedione, in estrogeni. Questi ormoni infatti hanno
un nucleo in comune a quello del colesterolo e degli ormoni sessuali.
Diabete mellito: un dismetabolismo glucidico, lipidico e protidico.
Liperestrenismo relativo non di per s una situazione gi patologica, bens una
situazione parafisiologica che importante conoscere per valutare quelli che sono i
soggetti a rischio di situazioni pre-cancerose, e mettersi in grado di compiere una
diagnosi precoce.
Diagnosi
Il principale sintomo di una patologia endometriale neoplastica o preneoplastica il
sanguinamento vaginale atipico, in post-menopausa o in fase intermestruale per
esempio.
Se si ha questa sintomatologia bisogna procedere a delle indagini diagnostiche.
Ogni iter diagnostico deve partire dallindagine meno cruenta a quella pi cruenta.
Nel caso dellendometrio abbiamo in successione:
1. ecografia: pu essere compiuta:
attraverso la parete addominale a vescica piena ( per rendere visibile
lutero)
per via transvaginale con una sonda che arriva vicino alllutero
Attraverso lecografia visibile:
spessore: il massimo spessore fisiologico 1-1,5 cm. (nella fase
proliferativa). Tutte le situazioni in cui lo spessore viene ad essere
maggiore di 1-1,5 cm. Sono da ritenersi anomale, atipiche. Chiaramente
un aumentato spessore da considerarsi a maggiore rischio nella post-
menopausa, soprattutto se associato a perdite di sangue.
2. isteroscopia: si compie nella seguente maniera:
si penetra con una sonda
si dilata la parete dellendometrio mediante introduzione di CO2
si vede la mucosa endometriale
si rilevano le aree di maggiore spessore, eventualmente rilevate, con
presenza di vascolarizzazione atipica
si fa prelievo mirato su queste aree
194
Vantaggi:
il prelievo mirato
Svantaggi:
dolorosa
richiede tempo: il personale medico deve assistere a lungo tempo la pz
costosa (costo del tempo-uomo)
3. curettage endometriale (raschiamento dellendometrio): la pz in leggera narcosi,
dunque non una procedura dolorosa, ed di breve durata, ma il prelievo non mirato,
perch loperatore non in grado di vedere ci che prelieva. sempre diagnostica per
lesioni di grandi dimensioni, ma pu dare dei falsi negativi per lesioni di piccole dimensioni.
Iperplasia
laumento numerico delle ghiandole endometriali principalmente rispetto allo
stroma.
Normalmente il rapporto fra stroma e ghiandola 4:1: il mantenimento di un
abbondante stroma importante per limpianto delluvolo.
Laumento delle ghiandole endometriali sullo stroma pu essere:
- lieve: si parla di iperplasia endometriale semplice
- severa: si parla di iperplasia endometriale complessa. Pu arrivare fino ad un
rapporto ghiandola/stroma 1:1 o maggiore.
Liperplasia endometriale merita una speciale attenzione poich pu divenire una
lesione pre-carcinomatosa: numerosi studi ne hanno confermato il ruolo
potenzialmente maligno.
Uniperpasia dellendometrio si associa sempre ad un aumento della rima
endometriale, rilevabile mediante ecografia ed isteroscopia.
Generalmente uniperplasia endometriale si presenta localizzata come rilievi dellutero
e solo pi raramente si manifesta in modo diffuso con a volte manifestazioni
emorragiche.
Latipia citologica rappresenta per lelemento morfologico fondamentale, che nel contesto di un
iperplasia ghiandolare, conduce alliniziazione ed alla trasformazione in senso neoplastico.
Dunque latipia citologica in un quadro di iperplasia rappresenta il precursore morfologico del
cancro.
195
Carcinomi dellendometrio
Il carcinoma dellendometrio il pi comune cancro invasivo del tratto genitale femminile,
responsabile del 7% di tutti i tm invasivi dell donne, se si escludono i tumori della cute.
In passato era molto meno comune rispetto ai tumori della cervice uterina, ma lindividuazione
precoce e leradicazione del CIN hanno invertito questo rapporto.
Attualmente vi sono 34000 nuovi casi di cancro endometriale allanno.
I tumori endometriali colpiscono principalmente donne in post-menopausa con un picco fra i 55 ed
i 65 anni, causando sanguinamento atipico e dunque consentendo una diagnosi precoce.
Classificazione
1. adenocarcinoma endometrioide
variante comune:
adenocarcinoma endometrioide con differenziazione squamosa
varianti rare:
villoglandulare adencarcinoma
secretory adenocarcinoma
ciliated cells adenocarcinoma
2. adencarcinoma sieroso
3. adenocarcinoma a cellule chiare
4. adenocarcinoma mucoso
5. adenocarcinoma a cellule squamose
6. adenocarcinoma di tipo misto
7. carcinoma indifferenziato
Adenocarcinoma endometrioide
Rappresenta l85% della casistica.
Tende ad essere molto simile allepitelio da cui deriva, mimando le normali ghiandole endometriali
proliferanti (endometrioide).
Al tumore endometriode viene applicato un sistema di gradazione in tre livelli che comprende
1. grado1 ben differenziato: quadri ghiandolari facilmente riconoscibili
2. grado2moderatamente differenziato: ghiandole ben formate frammiste ad aree solide di
cellule maligne
3. grado3 scarsamente differenziato: aree solide maligne con presenza di strutture
ghiandolari a malapena riconoscibili ed un maggior grado di atipica nucleare e di attivit
mitotica.
Il grado delladenocarcinoma endometrioide viene a corrispondere allo stadio in modo
molto stretto.
La stadiazione degli adenocarcinomi endometriali la seguente:
stadio I: carcinoma limitato al solo corpo dellutero
stadio II: carcinoma che interessa corpo e cervice
196
stadio III: carcinoma che si esteso all esterno dellutero, ma non al di fuori della
pelvi
stadio IV: carcinoma che si esteso al di fuori della pelvi oppure ha coinvolto in modo
evidente vescica o retto.
La gradazione e la stadiazione sono importanti per impostare un ia terapia ed un
intervento proporzionali alla gravit del tm.
La variante pi comune delladenocarcinoma endometrioide (20% degli stessi) la
presenza di focolai di differenziazione squamosa. Queste aree di tessuto squamoso, che
pu essere esso stesso neoplastico o meno, non cambiano in alcuna maniera la
prognosi del tumore, basata solo sulla gradazione e sulla stadiazione.
Questa differenziazione squamosa pu essere presente ad ogni grado e stadio
delladenocarcinoma endometrioide.
Adenocarcinomi sierosi ed adenocarcinomi a cellule chiare
Questi due istotipi, nella loro storia naturale mancano delle caratterizzazioni
morfologiche della situazione pre-cancerosa e cio di atipia cellulare ed iperplasia.
Sono tumori molto poco differenziati, il che li assimila a carcinomi di grado III
indipendentemente dal quadro istologico.
Colpiscono soprattutto donne tra i 65 ed i 70 anni e sono tumori decisamente con
prognosi peggiore rispetto agli adenocarcinomi endometrioidi: in generale la
sopravvivenza a 3 anni dopo la diagnosi minore del 50%e quella a 5 anni minore
del 35%.
Carcinoma indifferenziato
Le forme di carcinoma indifferenziato rappresentano lo stadio finale di tutti i tipi di
tumoree vengono ad laspetto morfologico di un tumore che assomiglia molto alla
cellula staminale di origine.
Endometriosi
Endometriosi il termine ustao per indicare la presenza di ghiandole endometriali e di
stroma in foci ectopiche, al di fuori dellutero.
Si osserva nelle seguenti sedi in ordine decrescente di frequenza:
1) parete dellutero (miometrio). In questo caso si parla anche di adenomiosi.
2) Entrambe le ovaie
3) Legamenti uterini
4) Peritoneo pelvico
5) Ombelico, vagina, vulva
6) Vescica e colon
7) Mucosa delle fosse nasali e del laringe
197
Si tratta di una patologia dellet pre- menopausale che comincia dal post-menarca e si
conclude con la menopausa e colpisce circa il 10% delle donne.
I focolai ectopici di endometrio rispondono alla stimolazione ciclica ormonale, con
conseguente sfaldamento dellendometrio durante il ciclo mestruale.
Quseto d luogo a micro-emorragie locali che evocano una reazione infiammatoria ed
una risposta di riparazione., con conseguente formazione di coaguli e di zone
fibrotiche, a volte obliteranti.
I segni clinici prevedono la presenza di forte dolore, grave dismenorrea, e spesso
questa patologia porta alla sterilit abbastanza velocemente.
Lintenso dolore in sede ectopica rispetto allendometrio, pu rendere particolarmente
diffcile una diagnosi corretta, fuorviandola.
La localizzazione dellendometriosi nella parete del colon (endometriosi colica) non
molto frequente. Nei casi in cui sia presente essa si manifesta per in stadi molto
avanzati, con una localizzazione prevalente nella parte pi esterna della parete colica
e nel tessuto adiposo esocolico, ma anche eventualmente a livello della regione mucosa
o sottomucosa.
Quando presente nella mucosa o sottomucosa viene a formare lesioni rilevete della
parete colica, che possono mimare la patologia neoplastica e indirizzano spesso la
diagnosi in direzione sbagliata.
In genere risulta diagnostica in questi casi una diagnosi di imaging che consente di
localizzare il focolaio endometrico ectopico.
Se la patologia localizzata sar possibile compiere un intervento di resezione del
focolaio ectopico, mentre nel caso di endometriosi cronica o prolungata, lunica terapia
possibile risulta il blocco degli estrogeni.
Leiomiomi
Vengono denominati leiomiomi tutti i tumori a differenziazione muscolare liscia ed a
morfologia benigna.
In questo caso si parla dei leiomiomi uterini o fibromi, che rappresentano
probabilmente il pi comune tumore umano.
Possono essere presenti in circa il 75% delle donne colpendo tutte le fasce det ma
preferenzialmente le donne tra i 40 ed i 45 anni.
Morfologia
Sono lesioni nodulari che possono essere masse singole o multiple
Hanno dimensioni che vanno da 1 a 25 cm.
Sono tumori ben circoscritti, demarcati, rotondi, di consistenza dura, grigia bianchi,
che solitamente si rinvengono nel contesto del miometrio del corpo.
Allesame istologico sono composti da fasci muscolari lisci, intrecciati che assomigliano
notevolmente al circostante miometrio non coinvolto.
198
I leiomiomi dellutero, anche quando sono molto estesi, possono essere asintomatici,
I sintomi pi importanti sono sanguinamento atipico, compressione della vescica,
dolore dovute ad eventuale ischemia compressiva, compromissione della fertilit.
Diagnosi
La diagnosi agevole.
I leiomiomi sono infatti avvertibili anche per semplice palpazione, come massa che
deforma la morfologia del corpo uterino.
La diagnosi definitiva si fa con lecografia che permette di vedere
- forma
- dimensioni
- localizzazione
- molteplicit
Lindividuazione di questi parametri piuttosto importante, perch determina anche il
rischio di sterilit che il liomioma implica per ostacolamento del passaggio degli
spermatozoi e difficolt nellannidamento delluovo.
Terapia
La terapia consiste nellasportazione delle lesioni, che fino a pochi anni fa avveniva per
asportazione diretta dellintero utero, ma che oggi avviene per asportazione
laparoscopica mirata.
Leiomiosarcomi
Sono rare neoplasie maligne che compaiono ex novo direttamente dal miometrio
oppure dallo stroma endometriale che va incontro a differenziazione muscolare liscia.
Vanno da forme ben differenziate fino a lesioni del tutto aplastiche, con accrescimento
selvaggio.
Sono capaci di dare metastasi anche dopo 5 anni prevalentemente a polmoni, encefalo
e tessuto osseo.
Il tasso di sopravvivenza a 5 anni circa del 40%.
Morfologia
Si presentano come una massa solida indolente; a un secondo esame si osservano
voluminose masse carnose che invadono la parete o masse polipoidi che protrudono nel
lume uterino.
Le cell sono fusiformi e si dispongono in fascicoli intrecciati.
Tipici sono i nuclei a sigaro.
Fra leiomiomi e leiomiosarcomi vi sono una serie di leiomiomi atipici, che possono
essere suddivisi allesame cito-istologico in probabilmente benigni o probabilmente
maligni.
199
Criteri di diagnosi differenziale tra leiomiomi e leiomiosarcomi
leiomioma leiomiosarcoma
Et 30s (in post menopausa
tende a diminuire)
Post- menopausa
Margini della lesione netti indistinti
Dimensioni < 5 cm. > 10 cm.
Multiplicit Generalmente associata a
presenza di leiomiomi
limitrofi
Generalmente unica
Necrosi
Emorragie
Alto indice mitotico
Atipica citologica
Trombosi vascolare (cellule
neoplastiche nei capillari
ematici)
Assente o irrilevante
Presente sempre e
caratteristica di tutti i
tumori maligni
200
Cisti e tumori dellovaio
La corticale contiene i follicoli, uno solo al mese matura .
Lepitelio superficiale cubico o cilindrico ( epitelio celomatico).
La zona corticale ricca di recettori per gli estrogeni e progestinici.
Oltre alla zona corticale vi una zona midollare.
Aspetti clinici
Donne tra i 25 e 65 anni
I sintomi precoci sono assenti o lievi come distensione addominale ascite e dolore
Sintomi urinarie gastrointestinali
Sanguinamento vaginale di tipo funzionale( si ha solo per quei tumori dellovaio che
tendono a produrre estrogeni)
Ancora oggi si evidenzia in stadio avanzato
Diagnosi
Dosaggio del Ca-125: si trova nel liquido ascetico nei tumori sierosi dellovaio e
sierosit anche della pleura e del peritoneo
Ecografia transvaginale
Stadiazione
Si definiscono 4 stadi:
nel 1 il tumore limitato allovaio o a entrambe le ovaie, andando avanti con la
gradazione interessa sempre pi la sierosa extraovarica con diffusione agli organi
limitrofi e ai linfonodi.
Non d metastasi a distanza ma esfolia sul peritoneo e diffonde su questo.
Ha un tropismo per la sierosa peritoneale ed eventualmente per la sierosa pleurica.
Fattori prognostici
Dimensioni
Stadio (ecografia-tac)
Tipo istologico ( prelievo con laparoscopia)
Grado istologico( correla con lo stadio questo per rappresenta lo statodi
differenziazione del tumore e pi alto peggio !!!!)
Residuo tumorale ( dopo chemio neoadiuvante che viene fatta prima dellintervento;
lintento di diminuire la massa ed eliminarla ma purtroppo non succede spesso)
201
Sopravvivenza a 5 anni
Stadio 1 90%
Stadio 2 80%
Stadio 3 15%
Stadio 4 4%
Tabella 22-3 del robbins classificazione WHO
Tumori dellepitelio celomatico di superficie
Tipo cellulare:
sieroso
mucinoso
endometroide
a cellule chiare
transizionale
squamoso
pu avere crescita esofitica o intracistica
la proliferazione cellulare ripresenta benigna maligna o borderline
Intracistico: sostituisce il parenchima ovario
Esofitico: cresce sullepitelio sieroso
Borderline: ha un diminuito potenziale di malignit
Tumori sierosi
30.40% di tutti itumori ovarici
70% benigni
5.10% borderline
20-25% maligni
Possono essere bilaterali, la bilateralit nei sierotipi non sierosi molto spesso indice
di metastasi e non di malattia primitiva es: ca. colon stomaco, mammella.
Tumori benigni
Max incidenza nella V decade. Spesso di riscontro occasionale, possono essere
intravistici o esofitici. Uni multi loculati.
Le cisti sono tappezzate da 1 epitelio piatto o cilindrico ciliato maturo.
Le cisti contengono materiale sieroso limpido.
Es: 55 anni sanguinamento anomalo. Lecografia pu vedere le cisti fluide.
Si fa poi dosaggio del Ca-125 che fluttua anche nelle lesioni benigne, Si pu togliere
per via laparoscopica.
202
Tumori borderline
25.30% dei tumori sierosi non benigni
tra i 30 ed i 50 anni
30% bilaterali
70% diagnosticati allo stadio 1
tumori sierosi borderline ( SBT), MACRO:
Endofitici spesso multiloculati con escrescenze papillari sono esofitici papillari sulla
sierosa dellovaio. In alcuni casi lintera superficie ovarica ricoperta.
Le papille hanno un asse connettivo vascolareb lasso molto edematoso ricoperto da 1
epitelio cubico ciliato con vari gradi di atipica citologica che per non mai
sgarbatissima.
Lattivit mitotica non mai elevata. Ci possono essere focolai di microinvasione.
SNITOMI? MAI
Come si fa a fare diagnosi?
_ primo contatto
_ ecografia transvaginale solitamente si vede una lesione
Ca-125 10 volte pi alto della norma quindi si procede con una laparoscopia
interventistica.
Si identifica o un tumore sieroso benigno bilaterale o un tumore sieroso borderline
Bisogna poi verificare la natura biologica della lesione mandando la laparoscopia
fresca al patologo e poi si fa un esame estemporaneo per fare un vetrino.
La maggior parte dei casi cade nel borderline.
Si toglie la lesione macroscopicamente e poi bisogna controllare il peritoneo facendo un
lavaggio peritoneale o raccogliendo il siero , si osserva la citologia e poi si guarda se ci
sono localizzazioni atipiche se si bisogna fare dei prelievi di questultime.
A questo punto la paziente curata chirurgicamente e stadiata.
IMPIANTI PERITONEALI
Possono essere non invasivi e invasivi.
Sono pi frequenti in donne con SBT esofitici. Si manifestano come placche o noduli
nel peritoneo ( minori di 1 2 cm)
Possono essere anche de novo da residui mulleriani.
NON INVASIVI
Sono l88% dei casi. Si dividono in:
Epiteliali: proliferazioni di cellule epiteliali atipiche che ricordano quelle dellSBT.
203
Desmoplastici: reazione fibrosa/Stromale contenente cell epiteliali atipiche e
occasionali corpi psammomatosi ( che si trovano anche nei tumori papilliferi della
tiroide)
INVASIVI
Sono il 12%
Hanno una proliferazione disordinata di componenti stremale ed epiteliale, le cellule
possono mostrare anche severa atipica, i margini sono infiltrativi.
SBT COMPORTAMENTO BIOLOGICO
Ricorrenza stadio I : 5-10%
Il 5-10% si ripresenta nel giro di 2 anni dallintervento in quanto sono stati
sottostadiati. I casi a prognosi infausta sono correlati alla presenza di impianti
invasivi.
SBT PRIMITIVI DEL PERITONEO
Poco frequenti ma difficili per la diagnosi.
Sembra tutto normale ma la paziente presenta ascite e Ca-125 aumentato.
Istologicamente assomiglia agli impianti non invasivi. La prognosi buona. Lepitelio
ovarico pu essere normale o minimamente coinvolto. Si manifesta con fibrosi o fini
granulazioni . Si localizza principalmente nel peritoneo pelvico. La dd con il ca.
sieroso ovario
Carcinoma sieroso ovarico
Aspetti clinici
Et media 55 anni
Sintomi minimi
Stadio avanzato ( II.III) nel 70% dei casi
Si procede con laparotomia e terapia neoadiuvante citoreduttiva.
Perch un tumore in operabile? Il tumore cresce lungo la sierosa e la infiltra
andando ad invadere tutti gli organi rivestiti da sierosa. Crea aderenze tra utero,
ovaie e organi limitrofi.
Aspetto macroscopico
Pu raggiungere dimensioni maggiori di 20 cm.
E bilaterale in un terzo dei casi
E una massa a struttura grossolanamente cistica con spesse aree di necrosi ed
emorragia.
204
Questi tumori possono prendere la via linfatica.
Esprime la citocheratina 7
Esprime il Ca-125
Questi dosaggi sono fondamentali per sapere se il tumore primitivo o no.
ISTOTIPI MUCINOSI
In uno stesso tumore ci pu essere una componente benigna, borderline e maligna.
Presentano una progressione da benigno a maligno. Non ci sono caratteristiche
macroscopiche differenziabili. Sono monolateral; se bilaterali bisogna pensare ad una
metastasi indipendentemente dallet della paziente.
Danno segno di s in modo improvviso attraverso torsione o rottura. La paziente
arriva in pronto soccorso con un quadro di addome acuto.( Fuoriesce liquido mucoide )
Il Ca del colon pi frequentemente d metastasi allovaio.
Quindi se il tumore esteso a tutte e due le ovaie necessario palpare tutto il colon.
Limmunoistochimica serve per le identificare le citocheratine: la anticitocheratina 20
espressa dalla mucosa colica ed il cdx2 a livello nucleare prevalentemente nei tumori
colici.
Quindi un tumore mucinoso bilaterale quasi mai primitivo ma una metastasi
proveniente da: colon, stomaco, mammella!!!!!
205
Patologia della mammella femminile
Generalit
La mammella femminile un insieme di dotti ramificati che parte dallunit terminale
duttulo-tubulare, progredisce tramite ramificazioni, converge verso il dotto galattoforo
e sbocca, infine, nel capezzolo.
Il dotto terminale extralobulare afferisce allunit terminale duttulo-tubulare, si fa
intralobulare, ramifica nei dotti lobulari e afferisce agli acini.
Nella parte extralobulare lepitelio cilindrico mentre nella parte intralobulare
lepitelio si fa cubico.
Tutte le cell di questo sistema giacciono su uno strato di cell mioepiteliali + lamina
basale. Le cell mioepiteliali servono nellallattamento e per detergere il secreto dai
dotti; inoltre la loro presenza un fattore prognostico positivo in caso di lesione
proliferativa.
Questa struttura di dotti circondata da stroma connettivale che pu essere
intralobulare o interlobulare.
Neoplasie e loro patogenesi
Le neoplasie della mammella possono originare dai due tessuti che costituiscono
questo organo:
Epitelio
Dotti
Acini
Stroma
Intralobulare
Extralobulare
Essendo il parenchima mammellare soggetto al ciclo ormonale femminile si possono
osservare tre fattori che influenzano la proliferazione e, conseguentemente, il rischio
di neoplasia nella donna:
Ciclo mestruale
Gravidanza e allattamento
Menopausa
Estrogeno: stimola le mitosi e quindi causa sia ipertrofia che iperplasia delle unit
duttulo-lobulari e degli acini.
Progesterone: induce secrezione apocrina che fa apparire i duttuli dilatati
PRL e PG: aumentano nellallattamento e stimolano anche loro il parenchima
Durante la menopausa si abbassano notevolmente i livelli di estrogeno e di
progesterone mentre aumentano gli androgeni (specie nelle donne obese o affette da
dismetabolismi). Questa condizione causa atrofia dovuta alla diminuzione della trama
206
vascolare che si compensa con un aumento delladipe e del connettivo; questo processo
fa assomigliare la morfologia della mammella femminile a quella maschile.
Diagnosi
La mammella un organo esterno e, perci, facilmente palpabile.
Per questo motivo lautopalpazione rimane un gradino fondamentale nel iter
diagnostico!
I limiti di questa procedura risiedono nella morfologia della patologia che non sempre
si presenta in forma nodulare e quindi facilmente palpabile e, anche, nelle dimensioni
della stessa tenendo conto che masse con diametro <1cm non sono comunemente
apprezzabili alla palpazione.
Il gradino successivo lecografia che non sempre, per riesce a evidenziare ogni tipo
di lesione, specie se essa e di dimensioni modeste.
A seguire ancora c la mammografia e, infine, la biopsia.
Lesioni epiteliali benigne
Tra le differenti lesioni che possono occorrere alla mammella vi sono quelle di tipo
benigno che sono:
Lesioni non proliferative
Lesioni proliferative
Iperplasia atipica
Queste tre condizioni vengono riscontrate mediante:
Alterazioni mammografiche
Riscontro incidentale
Noduli palpabili
Lesioni non proliferative della mammella (modificazioni fibrocitiche)
Si rendono evidenti soprattutto attraverso il riscontro di cisti.
Questa patologia si presenta allattenzione del medico come
o Per il clinico mammella irregolarmente nodulare
o Per il radiologo mammella densa con cisti
o Per il patologo modificazioni morfologiche benigne
Le aree interessate sono caratterizzate da:
Aumento della consistenza mal definita e diffusa
Possibili calcificazioni che spesso formano raggruppamenti sospetti (carcinoma?)
207
Le cisti sono la causa pi frequente di massa palpabile e risultano allarmanti nei casi
in cui si presentino:
Solitarie
Dure
Fisse ai piani profondi
Spesso sono associate alla secrezione spontanea monolaterale del capezzolo.
Morfologia
Le alterazioni morfologiche sono principalmente di 3 tipi:
Cisti: - Si formano dalla distensione e dalla dilatazione dei lobuli.
- Sono di un colore che va dal marrone al blu a seconda del loro contenuto
che pu consistere in fluido semitrasparente o torbido.
- Sono delimitate da epitelio piatto atrofico o da cell apocrine.
- Frequenti le calcificazioni e le formazioni papillari.
Fibrosi: Le cisti si rompono frequentemente e liberano il materiale secretorio al
loro interno nello stroma adiacente causando infiammazione cronica e
cicatrici fibrose che aumentano la consistenza della mammella.
Adenomi: - Aumenta il numero di acini per lobulo.
- Acini aumentati di volume e non distorti.
- Occasionali calcificazioni dentro il lume.
Adenomi da lattazione masse palpabili in gravidanza o durante lallattamento.
Costituite da tessuto mammario apparentemente normale
con adenomi fisiologici e modificazioni lattazionali
dellepitelio. Non sono una neoplasia ma unesagerata
risposta allo stimolo ormonale
Malattia proliferativa della mammella senza atipia
Raramente forma masse palpabili.
Vengono evidenziati come addensamenti alla mammografia o vengono riscontrate
incidentalmente nelle biopsie eseguite per altri motivi.
Pi dell80% dei papilloma dei grandi dotti si presenta con secrezione dal capezzolo.
Il restante 20% si presenta con piccole masse palpabili o addensamenti alla
mammografia.
Le patologie comprese in questo gruppo sono:
Papilloma grande: Pu andare in contro a infarto spontaneo a causa della torsione
del peduncolo con seguente secrezione ematica. La secrezione
208
non ematica dipende dalle normali secrezioni mammarie o
dallinfiammazione del dotto dovuta al papilloma.
Papilloma piccolo: Si sviluppa in profondit allinterno della mammella, viene
riscontrato accidentalmente e pu presentare calcificazioni
associate.
Iperplasia epiteliale: Definita dalla presenza di pi strati di cell al di sopra della
membrana basale. Riempie e distende i lobuli. I lumi si
presentano irregolari con fenestrazioni.
Adenoma sclerosante: Aumento di almeno il doppio degli acini per dotto terminale.
La normale disposizione globulare conservata. Gli acini
sono compressi e deformati al centro della lesione mentre alla
periferia sono dilatati. Vi sono abbondanti cell mioepiteliali.
La fibrosi stromale pu comprimere gli acini fino a
trasformarli in cordoni a doppie file di cell. Frequenti le
calcificazioni.
Lesione sclerosante complessa: Anche detta cicatrice radiale perch si presenta
come lesione stellata caratterizzata da un
agglomerato centrale di ghiandole intrappolate in
uno stroma ialinizzato.
Papilloma: Composto da assi fibrovascolari con ramificazioni multiple aventi
ognuna un asse di tessuto connettivo rivestito da cell luminali e
mioepiteliali. Si osserva uniperplasia epiteliale con differenziazione
apocrifa frequente.
- Papilloma dei piccoli dotti: Spesso multipli e in profondit con alto
rischio di carcinoma!
- Papilloma dei grandi dotti: Solitari, nei seni galattofori del capezzolo,
probabile correlazione con rischio di
carcinoma.
Adenoma
E una neoplasia benigna a struttura duttulo-ghiandolare che origina dallepitelio e dal
mio epitelio.
Si presenta come una lesione occupante massa (nodulo) nella zona retro areolare.
Spesso si accompagna a secrezione dal capezzoli (gemizio) che pu essere:
Sierosa
Ematica pu fare confondere col carcinoma
Siero-ematica
Nel caso di secrezione ematica pu venire il dubbio che si tratti di carcinoma ma
se la pz giovane lipotesi diventa inverosimile (non impossibile)
si esegue lesame citologico del secreto (difficile da leggere ma se c mioepit. ok!)
si verifica che la massa sia pi mobile di un carcinoma
Eco e mammografia sono inutili
209
si manda la pz dal chirurgo con il compito di eseguire una valutazione
intraoperatoria
il chirurgo manda il campione al patologo:
Se un adenoma il chirurgo pu richiudere
Se un carcinoma il chirurgo deve rimuovere completamente la mammella
Malattia proliferativa della mammella con atipia
Questa patologia comprende:
Iperplasia duttale atipica
Iperplasia lobulare atipica
Iperplasia duttale atipica
Si riscontra nel 5-17% delle biopsie eseguite per calcificazioni come quelle effettuate
per riscontro di masse palpabili o per calcificazioni radiologicamente evidenti.
Vi una somiglianza col carcinoma duttale in situ, le lesioni sono limitate in
estensione e presentano una popolazione cellulare monomorfa con cell posizionate
correttamente ma che non riescono a riempire completamente pi di due spazi duttali.
Iperplasia lobulare atipica
Osservata incidentalmente in meno del 5% delle biopsie.
Vi una somiglianza col carcinoma lobulare in situ, la lesione presenta cell che
riempiono meno del 50% degli acini dellintero lobulo e pu estendersi nei dotti con
rischio di carcinoma invasivo.
Tumori stromali
Si dividono in due categorie:
Stroma intralobulare
Fibroadenoma questi tumori secernono GF che determina
Tumore filloide proliferazione non neoplastica dellepitelio!
Stroma interlobulare stessi tipi del tumore del connettivo
Fibroadenoma
E il pi comune tumore benigno della mammella
Si tratta di una neoplasia fibroepiteliale
Si presenta a qualsiasi et ma pi frequente prima dei 30aa
Spesso multiplo e bilaterale
210
Nelle giovani donne si presenta come massa palpabile mentre nei soggetti pi
anziani come addensamento o calcificazione alla mammografia
E responsivo agli ormoni perci aumenta lievemente di dimensioni nella fase
terminale del ciclo mestruale
Regredisce in seguito alla menopausa
Alcuni studi hanno dimostrato che:
La componente fibrosa (stromale) monoclonale e pu presentare aberrazioni
citogenetiche
La componente epiteliale policlonale e non presenta modificazioni citogenetiche
Se i fibroadenomi insorgono associati a cisti >0,3 cm, adenoma sclerosante,
calcificazioni epiteliali o modificazioni papillari apocrine, hanno un lieve aumento
del rischio di sfociare in carcinoma
Morfologia
Nodulo singolo sferico di dimensioni variabili (da meno di 1 cm fino ad alcuni cm), ben
circoscritto, duro, indolente, rapida crescita e mobile rispetto al parenchima.
Lo stroma delicato, cellulare e spesso mixoide; racchiude ghiandole e spazi cistici
rivestiti da epitelio come lo stroma intralobulare.
Lepitelio deformato dallo stroma compresso che lo circonda.
Si presenta come una massa bianca a margini ben definiti e con cisti che sono dotti
dilatati riccamente cellulati con espansione dello stroma che risulta chiaro perch
edematoso.
Clinica
Si tratta con escissione completa in quanto risulta alquanto agevole visti i margini ben
definiti e la totale mancanza di vincoli col parenchima circostante.
Si verifica spesso una recidiva per escissione incompleta nelle adolescenti in quanto si
mira a un intervento che sia il pi conservativo possibile.
Questa patologia ha un basso rischio di tramutarsi in cancro.
Tumore filloide
Frequente nella 6 decade
La maggior parte si presentano come masse palpabili o evidenti alla
mammografia
Sono manifestazioni relativamente benigne
La maggior parte non presenta aspetto cistico
211
Morfologia
Presenta dimensioni variabili, pu avere un diametro di pochi cm o manifestarsi come
lesione interessante tutta la mammella con protrusioni polipoidi.
DD coi fibroadenomi:
Cellularit
Maggiore indice mitotico
Pleomorfismo nucleare
Eccessiva crescita della quota stromale
Bordi infiltranti
Questa neoplasia spesso recidiva localmente ma di rado metastatizza e in questi casi
solo la componente stromale ad essere interessata dal processo diffusivo.
Terapia
Questi tumori vanno escissi con ampi margini di exeresi oppure pu essere necessaria
la mastectomia totale per evitare metastatizzazione locale.
Infiammazioni
Sono rare.
Si presentano sottoforma di tumefazioni della mammella che possono essere dolorose o
eritematose.
Mastite acuta
E la forma pi frequente di malattia della mammella
Quasi sempre durante lallattamento (in particolare durante il primo mese)
perch la mammella vulnerabile a causa di ragadi e fissurazioni sui capezzoli.
Il patogeno pi frequente lo Stafilococco aureus
I sintomi tipici sono, mammella eritematosa e dolente con febbre
Allinizio si manifesta con un interessamento solo localizzato a una zona della
mammella o con un mero coinvolgimento del solo sistema duttale poi, se non
trattata, pu propagarsi.
Morfologia
Specie in caso di infezione stafilococcica si ha la formazione di ascessi singoli o multipli
che possono fistolizzare sboccando in zona periareolare.
Terapia
- Antibioticoterapia
- Completo drenaggio del latte dalla mammella
- Raramente drenaggio chirurgico
212
Lesioni precancerose
Liperplasia epiteliale pu essere di due tipi:
Semplice non rappresenta una lesione precancerosa
Con atipia citologica pericolo a causa della displasia!
Liperplasia con atipia citologica, specie se insorge su una mastopatia fibrosi cistica,
porta alla formazione di addensamenti e irregolarit palpatorie.
In questo caso, in particolare se la pz ha meno di 40 anni, si effettua lECO e la
mammografia, se questo ultimo esame evidenzia delle microcalcificazioni scatta
lallarme!
Le microcalcificazioni a seconda della loro morfologia sono pi o meno associabili a un
livello di rischio di carcinoma.
Se le calcificazioni appaiono grossolane con margini irregolari sono spesso predittive di
cancro.
Lesioni proliferative maligne
Classificazione del tumore della mammella
Il 95% dei tumori maligni della mammella sono adenocarcinomi che si dividono in:
Carcinomi in situ
Carcinomi invasivi
I carcinomi in situ consistono in una proliferazione di cell neoplastiche limitata ai dotti
e ai lobuli senza superare la membrana basale. Quindi, per definizione, non danno
metastasi.
I carcinomi invasivi consistono in una proliferazione di cell neoplastiche che invade lo
stroma circostante fino ad arrivare ai vasi dando cos metastasi diffuse.
Sia il carcinoma in situ che quello invasivo possono essere divisi in due categorie a
seconda della sede di sviluppo:
Duttale
Lobulare
Carcinoma invasivo
E la neoplasia pi frequente nella donna coprendo fino al 22% di tutti i tumori.
Dei carcinomi invasivi il pi frequente il duttale.
La prognosi buona se la diagnosi precoce!
213
Morfologia del carcinoma duttale invasivo
Queste neoplasie formano noduli duri e scirrosi o infidi per la consistenza simil-
mammaria.
Si manifestano con leggera prevalenza nel seno sx nel quadrante supero esterno.
Uno dei segni distintivi la retrazione del capezzolo o della cute che pu significare
che il tumore subito l sotto o che il tumore ha dato metastasi alla cute ed presente
in tutta altra sede.
Allosservazione microscopiche si osservano strutture duttali alterate con cell piene di
atipie che hanno valicato la membrana basale!
Grado di Elston-Ellis E una scala di gradazione del tumore che si basa sullanalisi
del grado di differenziazione, sul polimorfismo nucleare e
sullindice mitotico. Un elevato grado di questa scala (3) si
associa a una prognosi pi severa.
Allesame clinico il nodulo si presenta fisso perch infiltra il tessuto adiposo e per la
copiosa reazione desmoplastica che lo circonda.
Questa tipologia presenta 5 istotipi:
Tubulare: di origine duttale, ben differenziato (il pi diff.) per questo motivo la
prognosi favorevole in quanto il 100% delle pz libera a 5 anni. Si presenta
come un nodulo duro di dimensioni notevoli per lintensa reazione fibrotica
(desmoplasia). Le cell differenziate si aggregano in tubuli che differiscono dai
normali per la mancanza di mioepitelio. Questo istotipo espone unelevata
concentrazione di recettori per estrogeni e progestinica mentre esprime poco il c-
erb-2 e ha un basso MIB.
Papillifero: pu essere secondario a una lesione papillomatosa o pu insorgere
de novo. Di solito silente tranne quando si sviluppa nei dotti galattofori in
quanto causa secrezione ematica. Le lesioni papillomatose da cui derivano si
evidenziano solo se sono multipli e, proprio in questa forma, se si manifestano
trai 30-40aa sono da considerarsi lesioni precancerose. Anche qui si evidenzia il
grado di differenziazione osservando quanto la neoplasia papillare; in alcuni
casi la neoplasia si manifesta in forma solida, di alto grado con molte atipie e
mitosi, questa forma sdifferenziata la pi pericolosa.
Midollare: Si associa a infiltrato linfoide e plasmacellulare. C un elevato
numero di mitosi aberranti, una citologia nucleare ad alto grado e la presenza di
cell giganti. Rappresenta il 65% della patologia dopo i 50aa e, nonostante la sua
istologia, ha prognosi favorevole (??).
Mucoide: contiene laghi di mucina che pu essere extracellulare oppure
intracellulare nelle cos dette cell ad anello con castone. Questa tipologia ha uno
strano aspetto palpatorio simile a quello della mammella mastopatica.
214
Invasivo micropapillare: una forma molto aggressiva che da numerose
metastasi ai linfonodi. E molto frequente nelle donne in menopausa. Si tratta
con chemio e radio adiuvanti prima dellintervento.
Morfologia del carcinoma lobulare invasivo
Listotipo lobulare il meno frequente e si pu manifestare in con pi focolai e spesso
bilaterale.
Capita che non dia una massa dura ma semplicemente unarea di maggiore
consistenza assieme al grasso limitrofo.
Si evidenzia alla mammografia solo quando ha raggiunto una certa grandezza.
Le cell di questo tumore mostrano la tipica crescita a fila indiana.
Questa tipologia presenta due istotipi:
Classico: cell piccole linfocito simili, poche mitosi, cell in fila indiana, <
aggressivit
Pleomorfo: > aggressivit in base alla scala di Elston-Ellis
Diagnosi
Esame clinico
Eco e mammografia
Citologia/biopsia
Prognosi
I fattori prognostici positivi sono:
post-menopausa
assenza di invasione vascolare
assenza di metastasi linfonodali
diametro < 3 cm
Le forme duttali di alto grado e le forme lobulari di istotipo pleomorfo sono le pi
aggressive!
Punti di un referto di carcinoma della mammella
1) Molti tumori della mammella ricevono una forte stimolazione proliferativa dal ciclo
mestruale e, quindi, dagli ormoni liberati dallovaio. Per questo motivo unopzione
terapeutica consiste nella cura antiormonale dove vengono somministrati
antiestrogenici (tamoxifen). Il referto deve riportare se le cell della neoplasia
esprimono o meno i recettori per gli estrogeni perch in caso non li esprimano la
terapia con tamoxifene inutile.
2) Il referto deve riportare una valutazione dellindice mitotico (MIB)
215
3) Il referto deve riportare se le cell della neoplasia esprimono c-erb-b2. Questa
proteina di membrana un oncogene che viene espresso nella neoplasia della
mammella e si correla col grado della neoplasia. In neoplasia con grado => di 3 si pu
usare una terapia anticorpali contro questo oncogene e, al contempo, la sua
espressione rende inutile la terapia antiormonale anche nei carcinomi che esprimono il
recettore per gli estrogeni.
4) Il referto deve riportare la presenza di linfangite carcinomatosa
5) Il referto deve riportare gli eventuali linfonodi asportati
6) Il referto deve riportare i dati immunoistotipici
Carcinoma in situ
Anche in questo caso, come gi detto, si hanno i due tipi: duttale e lobulare.
Per la definizione di carcinoma in situ necessario che le cell neoplastiche non
abbiano superato la membrana basale dei dotti.
Per questo motivo i carcinomi in situ non danno metastasi per definizione!
Morfologia
Finch non supera i 2mm di diametro risulta impalpabile e invisibile, come valore di
cut off si danno i 30 dotti pieni di cell neoplastiche per essere chiaramente visibile e,
inoltre, si tiene conto delle possibili microcalcificazioni che si visualizzano come aree
grossolane.
La valutazione del grado di queste neoplasia si basa sullanalisi delle atipie del nucleo,
in base a questo si distinguono in generale neoplasie ad
Alto grado: sono masse solide con aree otticamente vuote ripiene di materiale
necrotico (comedocarcinomi)
Basso grado: in queste varianti i lobuli possono assumere aspetto
micropapillare, solido o cribriforme.
La routine diagnostica comprende la mammografia e lesame istologico ma, vista la
frequente ridotta grandezza della massa si usano due ulteriori tecniche:
Mammotome: questa tecnica individua le microcalcificazioni con limaging e le
reseca una ad una con un grosso ago. Una volta esportata tutta larea viene
mandata al patologo. Il vantaggio che tutto si risolve in ununica seduta con
anestesia locale e la pz va a casa subito. Gli svantaggi sono che una tecnica
dolorosa, che lago non pu togliere pi di una certa quantit di tessuto (non >
1cm) e c il rischio di copiose emorragie.
Resezione chirurgica: Si effettua una tecnica di imaging chiamata stereotassi che
evidenzia le zone neoplastiche iniettando in loro prossimit del carbone e
mettendo un filo metallico di repere per il chirurgo. Il filo serve perch la pz sosta
216
quasi sempre una notte in reparto prima dellintervento e, durante il sonno, il
carbone pu spargersi. Il giorno seguente il chirurgo segue il filo e asporta la zona
nera con una porzione di materiale circostante. Il pezzo viene poi orientato con
delle graffette e inviato al radiologo che gli fa una radiografia da sovrapporre
alloriginale per vedere se la lesione stata asportata completamente. In questo
caso non serve lesame estemporaneo del patologo perch la diagnosi complessa e
non basta un piccolo pezzo, servono diverse sezioni. Una volta appurata
lasportazione completa il patologo tatua i margini del pezzo con china e fa
diagnosi dopo averlo tagliato in diverse sezioni.
Il comedocarcinoma normalmente si manifesta come lesione non inferiore ai 5cm
perci il patologo deve poter analizzare tutta la massa per porre diagnosi.
Questo importante perch nel 2% dei casi questa patologia da metastasi ma non
sempre il patologo pu cogliere il punto in cui le cell maligne hanno oltrepassato la
membrana basale, anche questione di fortuna nella preparazione della sezione.
Sempre a questo proposito si osserva come il comedocarcinoma ad alto grado possa
presentarsi con una certa frequenza in forma microinvasiva ovvero che oltrepassa la
membrana basale di non pi di 2mm. Il problema di questa forma che le cell che
metastatizzato sono estremamente anaplastiche, hanno unelevata espressione di c-
erb-2, non presentano recettori per ormoni femminili e hanno un alto MIB. Questa
forma, perci, estremamente aggressiva.
Tecnica del linfonodo sentinella
Col tecnezio99 si individua in primo linfonodo che drena dalla neoplasia e, se il caso,
asporti quello mantenendo il resto della catena evitando cos la metastatizzazione e il
linfedema del braccio per totale rimozione della catena.
Si inietta il tracciante nel nodulo e poi con un rilevatore di radiazioni si osserva fino a
che livello arrivato e da l si asporta.
Lesame istologico dei linfonodi rimossi mette in evidenza tre tipi di metastasi:
Macrometastasi: visibili a occhio nudo
Micrometastasi: <2mm che sono la ripetizione del tumore primitivo
Occulte: pochi elementi anche unicellulari sparsi casualmente nel linfonodo.
RICAPITOLANDO.
Carcinoma duttale in situ
Negli ultimi 20 anni aumentata la frequenza fino al 15-30% di tutti i
carcinomi questo grazie anche allintroduzione dello screening
Pu presentarsi come calcificazione alla mammografia (frequente) o come massa
vagamente palpabile (raro) con secrezione spontanea dal capezzolo o, ancora, si
pu presentare a una biopsia incidentale eseguita per altri motivi.
217
Di solito interessa un solo sistema duttale ma pu estendersi causando lesioni
estese.
Diversi casi progrediscono fino al carcinoma invasivo trattato con successo nel
95% dei casi con mastectomia.
Le rare recidive e decessi sono dovuti alla ripresa della malattia a partire dal
tessuto adiposo sottocutaneo che non sempre viene asportato completamente.
I fattori di rischio sono:
grado
dimensioni
positivit dei margini di exeresi
Morfologia
Questa neoplasia si divide in 5 istotipi:
comedocarcinoma
solido
cribriforme
papillare
micropapillare
..ma la maggioranza ha un quadro composito che comprende pi istotipi.
Listotipo comedonico caratterizzato da proliferazione solida di cell pleomorfe con
marcate atipie nucleari e necrosi centrale. I frammenti necrotici calcificano e vengono
visti alla mammografia come microcalcificazioni a grappoli, lineari o ramificate.
Spesso presente un quadro di flogosi cronica associata a fibrosi.
Gli istotipi non comedonico consiste in una popolazione di cell neoplastiche monomorfe
con grado nucleare da basso ad alto.
- Il tipo cribriforme presenta degli spazi ghiandolari neoformati che sono ben
distribuiti con forma a setaccio.
- Il tipo solido riempie interamente i dotti interessati.
- Il tipo papillare cresce in formazioni papillari con asse fibrovascolari.
- Il tipo micropapillare cresce in protrusioni a forma di stalattite senza asse
fibrovascolari.
La Malattia di Paget del capezzolo una rara carcinomatosi che si evidenzia come
eritema del capezzolo monolaterale con crosta scura e secrezioni composta da fluido
extracellulare. Le cell maligne di Paget si estendono dal carcinoma duttale in situ fino
alla cute senza superare mai la membrana basale del sistema duttale. Nel 50-60% dei
casi questa patologia si accompagna alla presenza di una massa palpabile e, in questi
casi, vi sempre un sottostante carcinoma invasivo!
Carcinoma lobulare in situ
E riscontrato sempre in maniera incidentale in biopsie fatte per altre ragioni perch
non si associa a calcificazioni o a una reazione stromale che possa dare addensamenti.
218
Rappresenta l1-6% di tutti i carcinomi.
In quasi la met dei casi bilaterale.
E comune nelle giovani donne visto che il 90% di questa patologia si manifesta nella
premenopausa.
Per le sue caratteristiche viene considerato non pi come una vera e propria neoplasia
ma come un marker di rischio di sviluppare cancro della mammella.
Donne con CLIS sviluppano cancro con la medesima frequenza delle donne con CDIS.
La terapia consiste in mastectomia profilattica, tamoxifen ed necessario mantenere
uno stretto follow-up della pz.
Morfologia
Le cell anomale del CLIS e del carcinoma lobulare invasivo sono identiche e sono
piccole cell con nuclei ovali o rotondi poco adese tra loro. Sono anche presenti cell ad
anello con castone piene di mucina.
Questa neoplasia esprime recettori per estrogeni e progesterone.
Carcinoma duttale invasivo
E detto anche carcinoma invasivo non a tipo speciale perch rappresenta il 70-80% dei
tumori che non rientrano nei sottotipi definiti.
Morfologia
Si presenta come massa dura dai margini irregolari.
Al centro ci sono focolai di stroma elastico e/o microcalcificazioni.
Presentano una vasta gamma di aspetti:
forme ben differenziate, confondibili con lesioni benigne, che esprimono recettori
ormonali
forme composte da lamine intrecciate di cell pleomorfo che raramente
esprimono recettori ormonali
Le forme tumorali normalmente si manifestano con aspetti compresi trai due estremi
sopraelencati.
Il carcinoma duttale invasivo si accompagna quasi sempre a una certa quota di CDIS e
i gradi delle due varianti, normalmente, corrispondono.
La quasi totalit di questi tumori evoca una reazione desmoplastica che causa un
aumento della componente stromale fibrosa la quale responsabile della consistenza
lignea del nodulo.
219
Carcinoma lobulare invasivo
Si presenta come un nodulo palpabile o come area iperdensa alla mammografia.
Hanno una maggiore incidenza di bilateralit.
La maggioranza di questi tumori presenta una delezione sul 16 di geni coinvolti
nelladesione cellulare.
Danno un peculiare interessamento metastatico localizzato al peritoneo e al
retroperitoneo, alle meningi, tratto gastrointestinale, ovaie e utero.
Morfologia
Si presenta come massa dura dai margini irregolari.
Le cell sono identiche a quelle del CLIS e questa ultima patologia sempre coesistente
in caso di forma invasiv; tipico laspetto delle cell infiltranti a fila indiana e la
presenza di cell ad anello con castone.
Normalmente la risposta desmoplastica minima
220
Neoplasie Linfoidi
GENERALITA
LEUCEMIA: termine utilizzato per descrivere neoplasie linfoidi che si presentano con diffusi
interessamento del midollo osseo, spesso con alto numero di cellule neoplastiche nel sangue periferico.
LINFOMA: termine utilizzato per descrivere proliferazioni linfoidi che si presentano come masse
tissutali distinte.
Non molto chiaro per il confine netto tra il termine leucemia e linfoma.
- I linfomi sono al quarto posto in ordine di incidenza fra le neoplasie al mondo.
- Il linfoma di Hodgkin separato dalle altre forme che sono definite Linfomi non
Hogdkin (LNH), clinicamente, istologicamente, nonch da un punto di vista
terapeutico.
- Nel corso degli ultimi venti anni si avuto incremento esponenziale
dellincidenza dei linfomi non Hodgkin, mentre i linfomi di Hodgkin non hanno
subito incrementi significativi.
- A causa del declinare di alcune patologie e di una crescente diagnosi precoce di
altre (es. tumore della mammella) si stima che i linfomi diventeranno i tumori
pi frequenti nel prossimo mezzo secolo.
- Il rapporto tra Linfoma di Hodgkin e Linfoma non Hodgkin pari a 1:10
Si possono anche fare alcune considerazioni di tipo clinico generalizzate a tutte le
neoplasie linfoidi:
La presentazione clinica delle varie neoplasie linfoidi dettata dalla distribuzione
anatomica della malattia.
- 66% degli LNH e il 100% degli LH si presentano con ingrossamento linfonodale
non dolente localizzato o generalizzato.
- 33% degli LNH insorge in sedi extranodali (cute, stomaco, cervello).
- Le forme leucemiche giungono allosservazione clinica per la soppressione
dellemopoiesi scaturita dallinvasione del midollo osseo.
- Le forme leucemiche infiltrano tipicamente fegato e milza causando
epatomegalia e splenomegalia.
- Le neoplasie plasmacellulari si manifestano con fratture ossee nei casi in cui
coinvolgano lo scheletro.
Per la diagnosi sempre necessario lesame istologico dei linfonodi o degli altri
tessuti coinvolti.
Nella maggioranza delle neoplasie linfoidi, il riarrangiamento dei geni per il
recettore antigenico, precede la trasformazione neoplastica perci le cell derivate
dal progenitore neoplastico esprimono le stesse proteine recettoriali per lAg.
- La monoclonalit delle neoplasie linfoidi messa a confronto con la policlonalit
delle cell linfoidi normali; questo confronto serve a distinguere popolazioni
linfoidi neoplastiche da popolazioni linfoidi reattive.
221
L85% delle neoplasie linfoidi origina da cell B, la restante parte da cell T.
Raramente si osservano neoplasia originate da cell NK
Le neoplasie linfoidi alterano spesso le funzioni del S.I. determinando anomalie
nello stesso.
- Perdita della vigilanza con alta suscettibilit alle infezioni
- Perdita della tolleranza con fenomeni autoimmuni
Le cell B e T neoplastiche tendono ad imitare il comportamento della loro
controparte normale
- Tendono a localizzarsi in determinate sedi tissutali proprie dei loro corrispettivi
sani determinando i tipici quadri clinici dinteressamento dorgano.
Il linfoma di Hodgkin si estende in maniera ordinata e il suo stadio finale
fondamentale per decidere la terapia.
CLASSIFICAZIONE DEI LINFOMI
- Storicamente poche patologie hanno evocato tante controversie e confusa
classificazione come i linfomi.
- Negli anni 80 vi erano sei diversi tipi di classificazione.
- Dal 1994 la situazione molto migliore: vi una sola classificazione ,
promulgata dallOMS nel cosiddetto blue book.
- La Classificazione detta REAL/WHO (Revised European-American Limphoyd
Neoplasm Classification/ World Health Organization); unelencazione di reali
entit clinico patologiche condotta attraverso criteri identificabili mediante le
tecnologie attualmente disponibili.
- Questa classificazione oggi alla base di tutte le malattie emolinfatiche
tumorali.
- Il progredire dello sviluppo tecnologico porta alla necessit di periodici
riaggiornamenti di questa classificazione; il prossimo previsto nel 2008
Le precedenti classificazioni identificavano entit cliniche solo attraverso i caratteri morfologici del
tumore.
Questa classificazione identifica entit clinico patologiche utilizzando ed incorporando criteri oggettivi
insieme alle caratteristiche morfologiche e agli aspetti clinici.
I criteri su cui si basa questa classificazione sono:
morfologia
1) dati clinici
2) identificazione della controparte normale, se fattibile
3) profilo fenotipico
4) caratteristiche citogenetiche e molecolari (profilo genetico, molecolare)
La maggior parte delle entit distinte dalla REAL pu essere diagnosticata in modo riproducibile e
permette la stratificazione dei pazienti in gruppi a buona o cattiva prognosi.
222
I linfomi si possono dividere in
1) Linfomi non Hodgkin:
a) di derivazione linfocitaria B
b) di derivazione linfocitaria T/NK
2) Linfomi di Hodgkin
La classificazione REAL/WHO divide i linfomi in cinque grandi categorie sulla base della loro origine
cellulare:
1) neoplasie derivanti dai precursori : derivano da cellule ancora immature
a. dei precursori B-cellulari: maturazione nel midollo osseo
b. dei precursori T-cellulari: maturazione nel timo
2) linfoma di Hodgkin
3) neoplasie delle cellule periferiche: derivano da cellule mature perch una volta
che si sia realizzata maturazione le cellule migrano nel tessuto linfoide
periferico
a. delle cellule B periferiche
b. delle cellule T/NK periferiche
N.B. i linfomi sono caratteristicamente malattie sistemiche, dunque possono interessare varie sedi,
nodali ed extranodali: la costante deve essere la presenza di tessuto linfoide.
- La grande maggioranza delle neoplasie linfoidi (80%-85%) origina dalle cellule
B, mentre la gran parte dei rimanenti casi costituito da cellule T: solo
raramente tumori di origine NK.
- La differenziazione del tumore, che verifica la somiglianza con la controparte
normale, un indice della malignit di tutti i tumori solidi, ma non dei tumori
emolinfopoietici.
- Anche la morfologia non indice prognostico del grado di malignit del tumore,
ma concorre solo a fare la diagnosi.
- per questo che la REAL/WHO non comprende alcuna indicazione sul grado di
malignit
Unaltra comune distinzione dei tumori quella che viene fatta tra:
a) linfomi indolenti: nel momento in cui si rendono evidenti, comportano
anche se non trattati lunghe aspettative di vita (anni).
b) Linfomi aggressivi: nel momento in cui si rendono evidenti, hanno
progressione rapida e se non trattati portano a morte in breve tempo.
Molto spesso per i linfomi indolenti sono per quelli con peggiore risposta alla terapia, perch, pur non
espandendosi con enorme velocit, si dimostrano molto protetti allapoptosi.
Di conseguenza sono parzialmente insensibili ai farmaci.
223
FATTORI CHE INFLUENZANO IL CORSO DELLA MALTTIA
1) sede primitiva (nodale o extra-nodale)
2) presenza di specifiche alterazioni gnomiche
3) correlazione con agenti infettivi: trattamento di alcuni tumori con antibiotico-
terapia
4) cinetica cellulare (proliferazione-delezione)
5) resistenza pleiotropica (chemioresistenza)
6) possibili bersagli terapeutici (molecolari, genici): attualmente si sta sviluppando
luso di farmaci intelligenti, cio farmaci che tendono a trattare la neoplasia un
po come fa linsulina nei crf del diabete.
PATOBIOLOGIA DEI LINFOMI
Eziologia
- 75% eziologia sconosciuta
- 15-20% dovuta allazione di patogeni:
a) batteri:
H.pilori (carcinoma gastrico)
Campylobacter jujeni
Chlamydia psittaci (occhio)
Borrelia burgdoferi (cute)
b) virus:
HCV: perch interagisce anche con i linfociti con il suo
recettore
HHV8: PEL, malattia di Castlemann
EBV: linfoma di Burkitt, linfoma di Hodgkin
HTLV1: ATL
(HIV): azione facilitante in fnz dellimmunosoppressione
- 5% immunodeficit o autoimmunit
- 0.5-1% pesticidi
Patogenesi
La patogenesi comunque legata a 2 processi fondamentali:
1) Attivazione di proto-oncogeni
2) Inattivazione di onco-soppressori
Traslocazione:
Normalmente si ha traslocazione con giustapposizione di
224
- regione trascrivente per un oncogene o un oncosoppressore
- regione reglatoria di un altro gene espresso costitutivamente o non espresso mai
Dunque pu accadere che il prodotto del gene trascrivente:
- venga costantemente espresso (oncogene)
- venga costantemente silenziato (oncosoppressore)
Es: molto frequente la traslocazione 8-14, dove loncogene di Bcl-2 (8) viene posto
sotto il controllo trascrizionale del promoter del gene per la porzione costante della
catena H delle Ig.
Conseguente abnorme espressione di Bcl-2 proliferazione cellulare incontrollata
neoplasia.
Formazione di un gene di fusione
Per traslocazione con successiva fusione di due regioni trascrizionali di due geni
diversi divenuti contigui.
Formazione di un gene ibrido che trascrive per una proteina chimerica la quale
provoca neoplasia:
- direttamente
- indirettamente: inducendo alterazioni cellulari
Es. linfoma a grandi cellule anaplastiche.
Si ha formazione di un gene ibrido NPM formazione proteina chimerica che:
- coinvolta direttamente nella patogenesi tumorale
- un fattore prognostico: migliore risposta alle terapie
Mutazione di geni regolatori
Mutazioni puntiformi in oncosoppressori (es. p53) o in oncogeni
Fenotipo e genotipo
Fenotipo
Vede :
- maggiore espressione di molecole legate alla proliferazione
- minore espressione di molecole legate allapoptosi
- minore espressione di molecole legate alla differenziazione
Genotipo
- Oggi sappiamo con esattezza nellambito dei tumori linfatici, quali geni siano
costantemente deregolati.
- Questo consente lutilizzo di nuovi protocolli terapeutici
- I protocolli terapeutici utilizzati una volta erano rigidi e basati su dati
epidemiologici e su una chimera, cio lillusione di poter aumentare la dose
farmacologica illimitatamente.
- Oggi si tende alla Taylored Therapy non rigida, che tiene conto dei fattori
caratteristici del singolo paziente.
225
Ontogenesi del sistema linfocitario B
La linfoghiandola o linfonodo la struttura principale del sistema linfatico.
Nella struttura del linfonodo si distinguono:
- CORTICALE: la zona periferica del linfonodo, tipicamente B-linfocitaria.
Contiene follicoli nei quali si collocano e maturano i linfociti B.
- CORTICALE PARAFOLLICOLARE: lo strato pi interno della corticale che
tipicamente T-linfocitario.
- MIDOLLARE: formata da cordoni midollari ramificati, separati da irregolari seni
midollari. Nei cordoni midollari sono contenute soprattutto plasmacellule
differenziate che stanno migrando verso lilo del linfonodo. Nei seni midollari si
ritrovano macrofagi. Cordoni e seni sono entrambi sostenuti da una rete di fibre
reticolari che si estende a partire dalla capsula.
Follicolo linfatico
Una volta che lelemento linfocitario B maturo, fuoriesce dal midollo osseo e si viene
a collocare nei linfonodi in corrispondenza dei follicoli linfoidi primari.
Nei follicoli primari i linfociti B sono maturi, ma ancora vergini e dunque non
differenziati.
Non essendo mai venuti a contatto con Ag presentano alla loro spf. recettori
anticorpali non specifici, IgM e IgD, con il ruolo di riconoscere ed opsonizzare
lantigene.
Nei follicoli primari manca il centro germinativo, riconoscibile come unarea pallida
centrale.
Nei follicoli primari i linfociti B sono per sostenuti da una rete di APC, costituita
principalmente da cellule dendritiche follicolari e secondariamente da macrofagi.
Non appena nei follicoli primari le APC presentano lAg ai linfociti B il follicolo si
differenzia venendo a formare un centro germinativo, in follicolo linfoide secondario.
Struttura follicolo secondario
Vede a partire dallesterno verso linterno:
1) zona marginale: zona un po pi pallida del mantello. Molto sviluppata
caratteristicamente in alcune stazioni linfonodali (es. linfonodo mesenterico),
meno in altre.
226
2) zona mantellare o mantello: la prima periferia del centro germinativo,
intensamente colorata. Contiene cellule vergini residue e elementi B di
memoria. Di solito asimmetrica con maggiore spessore nel lato rivolto verso la
capsula.
3) Centro germinativo: in esso si trovano le cellule che hanno appena riconosciuto
lAg,e stanno andando incontro a proliferazione e differenziazione
(trasformazione blastica). Primo stadio di attivazione: i linfociti B danno vita ai
centroblasti cellule grandi (20 m), ad elevato indice mitotico, presenza di
nucleolini al di sotto della mbr, rima citoplasmatica apprezzabile, nella parte
scura del centro germinativo. Si trovano nella fase di ipermutazione somatica
Secondo stadio di attivazione: linfociti B danno vita ai centrociticellule pi
piccole (8m.), meno figure mitotiche, profilo nucleare inciso, nella parte pallida
del centro germinativo. Si trovano nella fase di selezione.
Il centro germinativo si trova dunque ad essere polarizzato (fase di
polarizzazione):
- centroblasti ad un polo parte pi scura
- centrociti allaltro polo parte pi pallida
I centrociti vanno dunque incontro a nuove divisioni mitotiche e si differenziano
in plasmacellule o cellule B della memoria.
Nel centro germinativo avvengono:
I. Ipermutazione somatica
Colpisce i geni dei linfociti B che hanno riconosciuto
lantigene e sono in fase di attiva proliferazione.
Vede una frequenza di mutazioni puntiformi aumentata di
circa 100 volte in corrispondenza dei geni per le porzioni
variabili delle catene leggere e pesanti delle Ig.
In questo modo vengono originati moltissimi cloni di linfociti B
che possono legarsi con affinit molto variabile allAg che ha
innescato la risposta.
II. Selezione delle cellule ad affinit maggiore.
Parallelamente Ac che sono stati secreti nelle prime fasi, si
legano allAg formando complessi Ag-Ac che attivano il
complemento.
Gli immunocomplessi sono catturati dalle cellule follicolari
dendritiche residenti nel centro germinativo ( recettori per
Fc degli Ac e per C3b) che espongono lAg sulla membrana.
In questo modo le APC che continuano a presentare LAg
fungono da test di prova nei crf dei linfociti B permutati, che
verifica laffinit del legame allAg.
LfcB con Ac a basso grado di specificit apoptosi
LfcB con Ac ad alto grado di specificit sopravvivenza e
differenziazione in plasmacellule (migrazione verso la
midollare, ilo) o cellule memoria (migrazione verso il
mantello).
III. Scambio di classe della catena pesante
227
I linfociti B cominciano a produrre anticorpi di classe diversa
dalle IgM o IgD: miglior adattamento della risposta umorale allo
specifico tipo di patogeni.
Linfoma follicolare
i. Incidenza:
35% dei linfomi degli adulti negli U.S.A (forma pi comune di LNH )
22% dei linfomi altrove
Lincidenza storicamente associata a maschi adulti (et media 59) ma la
malattia di fatto presente in ogni fascia di et
ii. Si presenta solitamente in terzo, quarto stadio: dunque al momento in cui
diviene evidente il tumore gia ampiamente diffuso, facilmente sistemico
(tutte le sedi dove vi linfatico).
iii. Ha una mediana di sopravvivenza di 7-10 anni, che veramente scarsa se il
tumore incorre in et giovanile
iv. Terapia:
dal momento in cui si visto che il tumore incorre anche in et giovanile,
la terapia stata modificata perch la mediana di sopravvivenza cos scarsa,
che necessario puntare alla guarigione.
Fondamentale per la terapia la rilevazione fatta in diagnostica.
La terapia dunque differenziata in base allet; in genere non si ha
miglioramento con una terapia aggressiva
Efficaci i protocolli con adrimacina
Crescita del tumore
1. Formazione di aggregati simil-follicolari
Il linfoma follicolare tende pi spesso alla formazione di aggregati simil-follicolari che
riproducono il centro germinativo.
I follicoli neoplastici appaiono per come strutture:
pi chiare
di dimensione pi omogenea
pi addossati
con tendenza allespansione centrifuga con conseguente fusione.
Dunque vi pu essere una successione temporale di:
1) crescita follicolare
2) crescita follicolare-diffusa in fasi pi avanzate
3) crescita diffusa nelle fai pi avanzate come risultato della progressiva fusione
dei follicoli tra di loro.
Il tumore viene diagnosticato nella terza fase solo nel 5% dei casi.
228
2. Invasione strutture vascolari
Il linfoma follicolare nella sua crescita tende allinvasione delle strutture vascolari del
linfonodo con conseguente possibile infarto del linfonodo se viene colpita larteria
afferente del linfonodo.
Se la biopsia linfonodale dunque in fase diagnostica vede completa necrosi del
linfonodo, si pu avere linfoma follicolare.
Bisogna dunque procedere a nuova biopsia da un altro linfonodo per verificare
lipotesi.
3. Sclerosi tipo Bennet
Colpisce soprattutto i linfonodi retroperitoneali.
Alla diagnosi si palesa come una massa profonda di consistenza lignea spesso
sostenuta dal linfoma follicolare.
Diagnosi
necessario fare diagnosi differenziale con liperplasia follicolare.
Iperplasia follicolare: non una neoplasia ma una reazione adattativa frequente nei
casi di
- collagenopatia
- artrite reumatoide
- lupus eritematoso
- HIV
Le caratteristiche distintive del follicolo neoplastico del linfoma follicolare sono:
- non distribuito topograficamente, ma interessa tutto il linfonodo
- i diversi follicoli hanno forma e dimensioni disomogenee
- per la tendenza alla crescita centrifuga i follicoli comprimono la paracorticale e
vengono a trovarsi in una condizione di crescita schiena-schiena che prelude la
fusione
- non c mantello
- non vi distribuzione polarizzata di centroblasti e centrociti
Grading istologico del linfoma
Si ottiene con utilizzando un ingrandimento molto alto del campione bioptico, detto
CAMPO a FORTE INGRANDIMENTO (CFI).
Quindi vengono valutati 10 campi a forte ingrandimento, valutando il contenuto in
cell.del centro germinativo.
Grado I < 5 centroblasti/CFI
229
Grado II 5-15 centroblasti/CFI
Grado IIIa >15 centroblasti/CFI
Qui la quota di centroblasti maggiore ma non prevalente
Grado IIIb i follicoli tumorali sono formati quasi esclusivamente da
centroblasti
Si ha una differenziazione anche molecolare.
Il grading orienta anche nella scelta della terapia:
Grado I e II: trattati meno aggressivamente
Grado IIIa: trattati pi aggressivamente
Grado IIIb: equiparati con i protocolli pi intensivi fra quelli dei linfomi
a cellule B come se avessero un linfoma a grandi cellule B diffuso.
Fenotipo
La diagnosi fenotipica un criterio oggettivo di valutazione che diviene ancora pi
importante nella diagnosi di tumori che non hanno una chiara morfologia ed
organizzazione architettonica.
Il linfoma follicolare essendo un linfoma di derivazione B linfocitaria esprime:
Marcatori B (molecole tipiche dei linfociti B)
Sono fondamentali per stabilire in modo oggettivo se un linfoma a cellule T o B,
anche perch alcuni linfomi T assumono forma follicolare.
- CD19 e CD79a marcatori precoci, espressi da cellule pre-B del midollo, ma non
da plasmacellule
- CD20, CD23 marcatori pi tardivi, espressi da cellule B mature
Recentemente la molecola CD20 ha acquisito importanza farmacologica.
stata utilizzata infatti come molecola target nei confronti di alcuni farmaci costituiti
da Ac monoclinali umanizzati utilizzati come tali o coniugati ad isotopi radioattivi.
Questi farmaci in vivo hanno:
Se utilizzati come tali: effetto citocida
Se marcati radioattivamente: effettuano radioterapia specifica.
Questi farmaci hanno per due limiti:
a) sono molto costosi
b) non colpiscono solo i linfociti B neoplastici ma anche quelli sani, provocando
importante immunosoppressione.
Dunque per utilizzare come target marcatori CD dei linfociti B devi essere sicuro che
le molecole CD siano ampiamente espresse nel soggetto con neoplasia.
230
Di conseguenza essi devono essere sempre ricercati anche nel follow-up, poich la
terapia medesima pu portare a scomparsa di questi marcatori anche per lunghi
periodi.
Marcatori del centro germinativo
Sono molecole espresse specificatamente dal linfoma follicolare che consentono di
verificare la derivazione dal centro germinativo.
- CD10 una proteina nucleare espressa da cellule B del centro germinativo
- Bcl-6 una zincfinger espressa da cellule B del centro germinativo
La caratteristica del linfoma follicolare rispetto alliperplasia follicolare che si vede la
presenza di queste molecole ancheal di fuori dei centri germinativi e dei follicoli.
Nelliperplasia follicolare, queste cellule sono presenti e sono espresse, ma sono
confinate ai centri germinativi.
Marcatori specifici
- espressione solo dellisotipo K della catena leggera delle Ig
Monoclonalit e monotipicit
I tumori di derivazione B traggono origine da una cellula aberrante con alterazioni tali
da potere prendere il sopravvento sulle altre cellule.
Monoclonalit
Se il tumore prende origine da una sola cellula, nella maggior parte dei casi il
riarrangiamento dei geni per il recettore antigenico precede la trasformazione
neoplastica.
Dunque le cellule derivate dal progenitore neoplastico condividono la medesima
sequenza del recettore per lantigene e sintetizzano proteine recettoriali per lantigene
identiche.
Hanno dunque medesimo riarrangiamento genico per le catene H e L delle Ig.
Monotipicit
Per quanto riguarda le catene leggere:
il riarrangiamento per si verifica solo se fallisce
riarrangiamnto per
in condizioni normale il carattere isotipo della catena L ha una
policlonalit 2/3
Nelle cellule neoplastiche invece le cellule hanno:
tutte riarrangiamento oppure
tutte riarrangiamento
231
Si ha capacit di produrre un solo isotipo di catena leggera delle Ig coerentemente con
il tipo di riarrangiamento presente al momento della aberrazione neoplastica.
N.B. nel tumore trovi una rete di cellule follicolari dendritiche di sostegno:
- pi disordinata
- pi lassa
La sua presenza fa supporre che il tumore necessiti nelle sue fasi precoci delle CFD e
dunque necessiti di attiva stimolazione antigenica.
Frazione di crescita
Rappresenta la percentuale di cellule che in ciclo nel tumore.
Si determina attraverso levidenziazione immunocitochimica di Ag associati alla
proliferazione, come Ki 67.
Questo elemento va costantemente valutato perch il grado proliferativi si viene ad
integrare con il grado del grading.
Es. se hai grading I e FdC elevata opportuno utilizzare farmaci ciclo-specifici.
Genotipo
Traslocazione 1418
lanomalia cromosomiale presente nel 90% dei casi.
La regione codificante del gene BCL2 (18) viene posta sotto controllo del promoter per
il gene della porzione costante della catena pesante delle Ig (14).
Il risultato una sovraespressione di BCL2
BCL2 un antagonista della morte cellulare apoptotica. Ci comporta che i linfociti
del follicolo neoplastico siano enormemente protetti dallapoptosi.
Nel follicolo normale vi sono fenomeni di selezione, con apoptosi delle cellule che non
esprimono Ac ad alto grado di affinit: dunque le cellule norm.sono BCL2 -.
Nel follicolo neoplastico, invece normalmente la crescita non dovuta allattivit
proliferativa, che modesta, bens da una protezione nei cfr dellapoptosi (soprattutto
grado I e II).
Questo rende il tumore pi insensibile ai farmaci citostatici e maggiore bersaglio
invece di Ac monoclonali, che invece utilizzino come bersaglio molecole come CD20,cio
elementi intrinseci che non hanno nulla a che vedere con la cinetica cellulare.
Nei pz con questo tipo di traslocazione essa utilizzata anche nel follow-up a scopo
prognostico:
Infatti i pz con residuo anche minimo di traslocazione sotto il profilo molecolare, sono
spesso soggetti a ricadute e spesso insensibili ai farmaci. Si rende necessaria spesso
una terapia sovramassimale: trapianto.
232
Anomalie atipiche
Nel 10% dei casi non vi traslocazione 14-18. n sovra espressione di BCL2.
Questi casi corrispondono a pz:
- con linfoma follicolare con interessamenti extranodali
- con linfoma follicolare di grado IIIb
- di et giovane
Sistema quantitativo batman
Per utilizzare a scopo terapeutico-prognostico le analisi genotipiche sono necessari
sistemi di analisi genetica come questo che una valutazione quantitativa del numero
di copie di un determinato gene.
Prevede le dimostrazione che il tipo di riarrangiamento dei linfociti di cui si analizza il
genoma sia esattamente quello tipico dellesordio della malattia.
Infatti una traslocazione di BCL2 si potrebbe trovare anche in individui
completamente sani, associata a cellule potenzialmente patogene,ma che non hanno
subito alterazioni che le abbiano portate ad una completa differenziazione in senso
neoplastico.
Una cos precisa quantificazione genetica permette:
1) differenziazione immediata della terapia
2) esitamento di eventuali falsi positivi, corrispondenti ai pz con mutazioni ma non
malati
Trasformazione
La trasformazione istologica del linfoma follicolare si verifica nel 30-50%
dei casi.
Nel linfoma follicolare come nella leucemia mieloide, nellandamento
evolutivo si pu avere dopo molti anni crisi blasticag, con trasformazione in
linfoma a cellule blastiche con proliferazione molto maggiore e dunque, date le
premesse di protezione dallapoptosi, con enorme espansione.
Questo solitamente avviene per la presenza di ulteriori anomalie, come
una minore espressione di p53, per mutazioni puntiformi o come una maggiore
espressione delloncogene c-myc, per riarrangiamenti.
Oggi vi sono tecnologie che operano scansione dei geni umani.
Questo permette lindividuazione dei geni costantemente deregolati in un determinato
tipo di patologia.
Vengono dunque stabilite firme genomiche associate a cellule neoplastiche o pi
semplicemente ad elementi reattivi.
Nel linfoma follicolare si pu avere:
1) firma da risposta immunitaria I (da parte dei linfociti B): comporta prognosi
favorevole.
233
2) firma da risposta immunitaria II (monolito-istiocitaria): comporta prognosi
sfavorevole
Oggi possibile stabilire la firma gnomica di tipo II anche con semplici indagini
immunocitochimiche.
Linfoma a grandi cellule B di tipo diffuso (DLBCL)
i. Incidenza:
30-40% dei tumori linfatici (primo posto in U.S.A., secondo in Europa)
60-70% delle neoplasie linfoidi aggressive
ii. La categoria stata istituita comprendendo tanti casi, tutti trattabili nella
medesima maniera: poi dal 1994 in poi (classificazione REAL/WHO) vi
stata differenziazione.
iii. Lo stessa terminologia ci dice che cresce in modo diffuso con cellule di
diametro maggiore di 20 m.
iv. Possono essere primitivi (la maggior parte) o secondari a trasformazionedi
un altro linfoma (in questo caso, difficilmente trattabili).
v. Tipicamente si presentano con un rapido aumento, spesso sintomatico, della
massa neoplastica in una singola sede (sede primitiva) che pu essere nodale
o extranodale (prognosi migliore).
Morfologia
1. 75% dei casi: composizione citologica polimorfa. Cellule grandi ma non simili
2. Variante centroblastica (minor parte dei casi): composizione citologica omogenea
3. Variante immunoblastica:cellule multilobate a profilo immunoblastico, con
ampia rima citoplasmatica e grosso nucleolo.
4. Variante anaplastica: cellule a profilo reniforme.
5. Linfoma a grandi cellule B ricco in linfociti T: le cellule tumorali si
accompagnano e sono circondate da grandi quantit di elementi reattivi. una
forma che pu essere confusa con il linfoma di Hodgkin: questo errore pu
essere fatale, perch questa una forma molto aggressiva che, se trattata come
il linfoma di Hodgkin, progredisce con estrema rapidit.
6. Variante con sclerosi: si ha reazione fibro produttiva con tendenza delle cellule
ad essere suddivise da tralci fibrosi (compartimentalizzazione). frequente in
sedi extranodali (primitivo dellosso, retrosternale).
234
Fenotipo
Marcatori generali B
Analoghi a quelli del linfoma follicolare. Testimoniano la derivazione B linfocitaria del
tumore.
Espressione di CD5
CD5 una molecola che era denominata in passato molecola T1, perch considerata
come primo marcatore dei linfociti T.
Successivamente si visto che questa molecola pu occorrere anche in piccole
popolazioni di linfociti B ed in particolare in condizioni normali, negli elementi del
mantello ( di conseguenza anche nei tumori mantellari).
una molecola espressa nel 10% dei linfomi a grandi cellule B di tipo diffuso.
I DLBCL che sono CD5+ sono anche ciclina D1- e questo aiuta nella diagnosi
differenziale, poich invece i tumori mantellarisono CD5+ e ciclina D1+.
Il 10% dei DLBCL che esprime la molecola CD5 :
- pi aggressivo
- le cellule neoplastiche tendono a localizzarsi allinterno delle strutture vascolari.
Se vi sono molte cellule tumorali allinterno dei vasi sanguigni il trattamento
terapeutico pu provocare massiva sindrome da lisi tumorale a causa della morte
delle cellule dentro i vasi.
Marcatori del centro germinativo
Lespressione dei marcatori del centro germinativo CD10 e BCL2 variabile.
Se presente riconduce ad una derivazione delle cellule dal centro germinativo.
Ci non porta a confondere il DLBCL con un linfoma follicolare per le evidenti
differenze nel tipo di crescita e nella composizione cellulare.
IRF4 (Interferon4 Regulating Factor).
una molecola che compare normalmente nelle cellule del centro germinativo che
hanno superato la selezione clonale e che dunque si trovano alla periferia del centro
germinativo (migrazione nella midollare plasmacellule; migrazione nel mantello
cellule della memoria.
Il massimo dellespressione di IRF4 si ha nelle plasmacellule gi formate che
esprimono anche CD138.
Altri marcatori
IRTA-1 prodotto dallomologo gene che fa parte di un gruppo di geni di regolazione
della produzione delle catene delle Ig.
Frequentemente espresso nella zona marginale, dove i linfociti B selezionati e maturi
si collocano transitoriamete prima di migrare come plasmacellule mature nei cordoni
midollari.
235
CD30 un marker di attivazione, espresso caratteristicamente dai linfociti B e T
attivati. molto espresso anche nelle varianti del linfoma di Hodgkin classico.
Genotipo
processo di ipermutazione (50% dei casi): interessa:
1) geni che vanno normalmente incontro ad ipermutazione (BCL 6
e FAS)
2) geni che normalmente non vanno incontro ad ipermutazione
ipermutazione aberrante (PIM-1, Rho/TFF, c-myc, pax 6)
traslocazioni: interessano principalmente il gene Bcl 6,
perch in esso vi un punto fragile, comportando riarrangiamento con una
serie di partners molecolari.
Alterazioni legate a forme di tumore secondarie:
1) Riarrangiamenti di c-myc
2) Anomalie di p53
3) Riarrangiamenti di Bcl 2
4) Mutazioni di Bcl 6
Studi basati su micro-array
Vi sono 2 tipi di micro-array:
1) Genomici: la fnz la valutazione del profilo di espressoine genica
2) Tissutali: la fnz la valutazione del profilo di espressione proteica
Micro-array genomici
Su un supporto di piccola taglia poniamo gli acidi nucleici tratti dai geni: il supporto
in grado di contenere parecchie migliaia di geni fino alla totalit del nostro genoma.
Questo tipo di micro-array consente la valutazione dellespressione dei geni, legata ad
un processo patologico, dunque consente di valutare il profilo di espressione
genicagene expression profile.
In un processo neoplastico ne verifica la firma genomica, confrontandola con la firma
genomica della controparte normale, permettendo dunque di conoscere quali e quanti
geni sono espressi patologicamente nei confronti della controparte normale.
In particolare nel linfoma a grandi cellule B di tipo diffuso il confronto viene fatto tra:
1) geni delle cellule del DLBCL
2) geni delle cellule del centro germinativo
3) geni dei linfociti B del sangue periferico, sottoposti dunque a processo di
attivazione.
Rispetto alla controparte normale la tecnica di micro-array mette in evidenza la
presenza di:
- geni espressi normalmente: si evidenziano come rettangoli neri
- geni sovraespressi: si evidenziano come rettangoli rossi
- geni sottoespressi: si evidenziano come rettangoli verdi
-
236
In questo modo divengo in grado di fare un raggruppamento gerarchico; raggruppo
tutti i linfomi con simile firma.
Attraverso questa metodica dunque vengo a differenziare 3 sottogruppi allinterno dei
DLBCL:
1) gruppo con firma simile a quella del centro germinativo: linfomi correlati al
centro germinativo. Nel 70% dei pz si ha prognosi favorevole con guarigione.
2) Gruppo con firma simile a quella degli elementi linfoidi attivati: linfomi attivati.
Solo il 20-30% dei pz ha prognosi favorevole con guarigione e lunghe aspettative
di vita.
3) Gruppo non classificabile, con firma diversa: venuto fuori in un recente studio
condotto su 274 persone.
Dunque questa distinzione viene ad avere anche un valore diagnostico-prognostico.
Il limite delle tecniche di micro-array genomico risiede nella necessit di assoluta
freschezza del materiale che si esamina, perch lmRNA deve essere assolutamente
intatto.
A tal scopo il materiale deve essere congelato a bassissime temperature non appena
prelevato e spedito ai laboratori di analisi con tutte le precauzioni.
Questo costituisce un elemento davvero limitante, tanto da avere reso necessaria la
ricerca di alterative della tecnica di gene expression profilino.
1. aprile 2004: si prende in considerazione lespressione di solo 6 geni (non
necessit di utilizzare micro-array) ed in base a questo vengono differenziati tre
gruppi simili a quelli trovati con la tecnologia di micro-array
2. ricerca dei prodotti proteici dei geni de-regolati. Utilizzo di micro-array tissutali.
Micro-array tissutali
Si cerca lespressione deregolata delle proteine, in ragione dellespressione deregolata
dei corrispondenti geni.
I risultati sono valicati su una casistica molto ampia, creando algoritmi in grado di
ricostruire esatamente quelli che sarebbero i risultati della gene expression profiling.
Il vantaggio che il materiale proteico sempre presente e disponibile e non ha
necessit di grosse precauzioni per la conservazione.
Esempio:
Analisi dei prodotti proteici dei geni:
Bcl 6/CD10
IRF4
Bcl 2
CD 138
CD 30
IRTA-1
237
L'analisi di questo limitato numero di proteine porta alla caratterizzazione di un
profilo di espressione proteica che consente la suddivisione dei DLBCL in tre
sottogruppi comparabili a quelli ottenuti con micro-array genomico.
La tecnologia micro-array dunque permette una classificazione ed identificazione dei
tumori basata solo su criteri biologici ed oggettivi e non morfologici e soggettivi.
Accanto a questi tre sottogruppi genotipici vi sono poi dei sottotipi clinico patologici del
DLBCL.
Una delle forme pi importanti
Linfoma a grandi cellule B primitivo dellintestino
i. Prevalente nelle donne con et intorno ai 30 anni.
ii. La presentazione della malattia quasi sempre drammatica venendo a
costituire spesso delle vere e proprie situazioni di emergenza.
iii. Nonostante questo allesordio clinico la massa tumorale, piuttosto grossa
(diametro >20cm.) ma contenuta interamente nel mediastino (no metastasi).
iv. In 1/3 dei casi al momento dellesordio clinico presente la sindrome della
vena cava superiore che vede reflusso di sangue a livello della vena cava
superiore con edema.
v. Terapia: prevede la possibilit di tre approcci:
Protocollo CHOP: molto utilizzato dagli americani ma
garantisce solo un 40% di guarigione
Protocollo MACOP-B + radioterapia: il protocollo pi
utilizzato in ambito europeo. Garantisce un 80% di guarigioni.
Terapia sovramassimale: prevede trapianto di midollo osseo
generalmente autologo e porta a guarigione una percentuale di pazienti di
poco maggiore del protocollo MACOP-B
vi. Ricadute frequenti in sedi extranodali: polmone, fegato, reni, intestino,
gonadi.
Morfologia
- Cellule di grandi dimensioni.
- Rima citoplasmatica evidente e chiara
- Cellule delimitate da ampi tralci fibrosi: sclerosi da compartimentalizzazione.
Sono confusi molto spesso con
1. tumori di derivazione da cellule germinali
2. tumori di origine epiteliale (carcinoma timico nella variante a cellule chiare)
data laggregazione adesiva delle cellule e la reazione fibrotica.
Fenotipo
Marcatori generali B
238
Marcatori comuni al DLBCL
Bcl-2 (78%)
Bcl-6 (55%)
IRFA4 (75%)
Marcatori comuni al linfoma di Hodgkin
CD30 Presente nell86% dei linfomi a grandi cellule B primitivi del mediastino.
comune anche al linfoma di Hodgkin con il quale necessaria fare diagnosi
differenziale.
Mancanza completa di espressione delle Ig. Sono presenti tutti i fattori di trascrizione
che dovrebbero portare alla produzione di Ig, ma vi incapacit della loro produzione,
probabilmente a causa di un riarrangiamento.
Questo un carattere in comune con il linfoma di Hodgkin di tipo classico anche se in
esso dovuto ad un difetto trascrizionale e non di riarrangiamento.
Marcatori che permettono diagnosi differenziale con LdH
CD45+ presente su tutti i leucociti, anche noto come antigene comune ai leucociti
(LCA). Non espresso nei linfomi di Hodgkin
CD15 tipico dei granulociti. Anche espresso in alcune varianti del linoma di Hodgkin.
Marcatori specifici
Proteina MAL ( dal nome dello scopritore, Miguel Alonso): espressa nel 70% dei casi
di linfoma a grandi cellule B primitivo del mediastino. Compare difficilmente nei
DLBCL e nei linfomi di Hodgkin.
Genotipo
Amplificazione di c-rel
Costantemente presente lamplificazione di c-rel, che entra a fare parte della via di
traduzione del segnale Nf che conduce allapoptosi cellulare.
Non si tratta dunque di un tumore protetto dallapoptosi
Sovraespressione del gene FIG1
Assolutamente caratteristica e peculiare di questo tumore
Anomalia a livello di p9
un amplificazione a livello del braccio corto del cromosoma 9, con conseguente
guadagno, che si osserva anomalia cromosomica ricorrente caratteristica.
La firma genomica di questo tumore assolutamente diversa da quella dei DLBCL,
mentre invece anche nella firma genica si ha ampia corrispondenza con i linfomi di
Hodgkin.
239
Probabilmente tutte e due le patologie derivano da cellule dendritiche presenti:
- a livello del timo : sono molto abbondanti e dette cellule B asteroidi
- in altre sedi
Linfoma di Burkiit
Linfoma di Burkiit tipico (LBT):
Clinica:
E il pi aggressivo!
1) Endemico: - In Africa Centrale ovvero in territorio malarico.
- Colpisce principalmente i bambini.
- Si localizza tipicamente a livello della mandibola e delle
Gonadi.
2) Sporadico: - In Occidente.
- Et variabile.
- Si localizza nellintestino (tumefazione addominale), gonadi
ed SNC (in particolare in corso di HIV).
** I soggetti con infezione da HIV sono la principale categoria a rischio nel linfoma con
interessamento del SNC, tanto che nei primi studi sullHIV era stata ipotizzato il
linfoma di Burkitt come causa dellHIV medesimo.
Questa correlazione ha determinato un aumento del numero dei casi di questa forma
di linfoma negli ultimi anni, in associazione con laumento dellHIV.
E altamente invasivo, cresce a macchia dolio in et pediatrica si tratta con
successo con terapie aggressive.
(+ arduo in et adulta)
Morfologia:
Endemico e sporadico sono istologicamente identici.
Cell con dimensioni simili
Diversi nucleoli
Cromatina densa e reticolare
Rima citoplasmatica estremamente basofila
Limiti cell poco definiti simile a un sincizio
Numerose mitosi X campo
Numerosi corpi apoptotic
Macrofagi adibiti allo smaltimento dei corpi mitotici
Aspetto a Cielo Stellato Dovuto al citoplasma chiaro dei macrofagi
Fenotipo:
Bcl-6 e CD10+ Marcatori tipici del centro germinativo
Bcl-2 Spiega le numerose mitosi osservabili.
240
C-myc+
Mib-1+ 100% ???
Linfoma di Burkiit atipico (LBA):
Clinica:
Si differenzia per una maggiore differenza di volume cell.
Occorre sempre in et adulta.
Richiede terapie molto aggressive (megaterapie).
Morfologia:
Cell con dimensioni variabili.
Alcune cell sono grandi con differenziazione plasmoblastica.
Fenotipo:
CD10
Bcl-6
Bcl-2+ ma non soggetto a traslocazione
Mib-1+ 90% E un valore comunque alto che giustifica le numerose
mitosi.
Genotipo:
Endemico: - Vi la traslocazione del gene delloncogene c-myc vicino al
promoter del gene per la porzione costante della catena pesante
delle I Ig (t8-14). La sovrapproduzione di c-myc comporta lentrata
in circolo di tutte le cell portanti la traslocazione.
- Il genoma cell EBV+!!!
Sporadico: - Vi una deregolazione di c-myc causata dalla t.8-14 dalla t2-8
(catena leggera k) o dalla t8-22 (catena leggera ).
- EBV+ negli HIV+ (50%) e negli HIV- (25%).
Atipico: - t8-14 sempre presente!
**Ipotesi sulla patogenesi della forma endemica:
Questa forma di tumore costantemente associata alla coinfezione latente del virus
EBV.
241
Secondo un ipotesi del 2004 pubblicata da the Lancet Oncology lintegrazione del
virus EBV un fattore predisponente ma non sufficiente per generare da sola il
linfoma.
EBV ha funzione immortalizzante nei confronti dei linfociti infettati, favorendone la
proliferazione, ma vi necessita di altre interazioni.
Allinfezione da EBV segue spesso linfezione da plasmodi, che causano la malaria.
La malaria fornisce unulteriore spinta proliferativa ai linfociti B, indebolendo
oltretutto lazione dei linfociti T, che eliminerebbero le cellule infette.
Segue in molti casi linfezione da Arbovirus, trasmessa dalle mosche; essa fornisce alle
cellule immortalizzate e proliferanti uno stimolo immunitario, cio le porta ad un
processo di maturazione.
La maturazione comporta anche processi di ipermutazione e scambio di classe della
catena pesante, che aumentano le possibilit di rischio di insorgenza di alterazioni nel
DNA, come la traslocazione del gene c-myc.
Infine un ulteriore fattore predisponente pu essere il contatto con Euphorbia tirucalli,
un vegetale utilizzato nella zona africana come medicamento e come gioco.
Ognuno di questi fattori predisponente ad un danno al DNA, non riparato dai
sistemi enzimatici cellulari, con conseguente definitiva trasformazione in senso
neoplastico: linsorgenza del tumore un processo multistep.
Ricapitolando.
EBV: immortalizza le cell
Malaria: causa una spinta proliferativa nelle cell dell S.I.
Arbovirus: anche questi scatenano una proliferazione delle cell dellS.I.
inoltre le loro epidemie sono correlate a picchi di LBT.
Euphorbia Tirucalli: vegetale usato come decotto o come gioco dai bambini
ed capace di danneggiare il DNA facilitando le
traslocazioni.
Linfoma da cellule mantellari (LCM)
*Mantello: Porzione del follicolo non omogenea a causa delle due tipologie di cell
presenti; Cell vergini e Cell della memoria.
La disomogeneit cellulare riflessa a livello molecolare, per quanto riguarda
lespressione fenotipica.
A dispetto della disomogeneit vi per un elemento comune.
Gli elementi B che entrano nel mantello cominciano ad esprimere la molecola CD5
(molecola che fu individuata come caratteristicamente T dipendente e poi fu trovata
espressa anche da alcune popolazioni B).
242
Clinica:
Consiste nel 3-10% dei linfomi non-Hodgkin a livello mondiale (3% USA, 7-9% UE)
Colpisce prevalentemente maschi in et avanzata (5-6 decade di et).
Al momento della diagnosi la malattia gi diffusa a livello sistemico
interessando:
- anello del Waldayer
- milza (polpa bianca)
- midollo osseo (70%)
- componente circolante (10%)
- intestino (poliposi linfomatosa di cui la causa principale!)
Morfologia:
Cell piccole con profilo ripiegato (asse max 8 m)
Nucleo ripiegato
Scarso citoplasma
Le cell possono essere di tre variet:
1. Classico
2. Blastoide: Simile al linfoma linfoplastico (cell precursori)
3. Polimorfa: Pi voluminose, simili al linfoma a DLBCL
Allinizio accresce a livello del mantello (crescita mantellare) dopodich si
espande in direzione centripeta verso il centro germinativo formando dei
noduli (crescita nodulare). Infine, in una fase tardiva, i noduli si fondono
tra loro (crescita diffusa). Nel 70% dei casi la diagnosi avviene in questa fase.
Fenotipo:
CD5+ e CD23 per distinguerlo dalla leucemia linfocitica cronica
Ciclina D1+ (95%) quasi sempre diagnostica per questo linfoma
Genotipo:
Si ha una t11-14.
Sul cromosoma 11 vi il gene B1-1 che codifica per la Ciclina D1.
Il gene per la Ciclina D1 viene traslocato sul cromosoma 14 finendo sotto il
controllo del promoter del gene per la porzione costante delle catene pesanti delle
Ig.
La sovraespressione del gene comporta una sovrapproduzione di Ciclina D1 che
promuove il passaggio G1-S.
Bcl-2+ normale perch sia le cell vergini che le cell della memoria sono cell che
devono vivere a lungo e questa proteina li preserva dallapoptosi.
243
Prognosi e Terapia
I casi con cospicue frazioni di crescita (Ki-67) nel 50% dei casi muoiono entro lanno.
Questi casi, se trattati in maniera convenzionale, hanno poche chance.
In generale possiamo avere due derivazioni utili ai fini diagnostici:
Cell non-mutate (vergini) : 75% dei casi, sono le + aggressive
Cell altamente mutate (cell della memoria): forme meno aggressive
Una terapia convenzionale con questo tipo di tumore d poche possibilit di
guarigione.
Normalmente vengono soprattutto trattati con terapia sovramassimale.
Linfoma Della Zona Extranodale (LZME)
Questi linfomi derivano dalla zona marginale dei follicoli del MALT.
La zona marginale la porzione pi periferica del follicolo secondario.
E molto sviluppata nella milza, nelle placche di Peyer e nei linfonodi mesenterici.
In questi organi linfoidi vi una concentrazione di plasmacellule superiore a quella
presente nei cordoni della midollare perch il tratto gastroenterico viene a contatto
ripetutamente con elementi potenzialmente infettivi.
Il MALT diviso in due tipi:
Congenito: rappresentato da aggregati linfoidi nella mucosa del tenue e del
colon
Acquisito: rappresentato da masse di tessuto linfoide che si possono
localizzare in sedi disparate (polmoni, tiroide, ghiandole salivari, stomaco,
cute) in seguito a un processo infettivo o autoimmune. Questi due fenomeni
possono anche comparire associati.
A seguito del fenomeno flogistico e/o autoimmune si organizza un
tessuto linfoide precedentemente assente.
Questo nuovo sistema organizzato in focolai.
La sua organizzazione interna differente dalle linfoghiandole.
Possiede sistemi di ricircolo peculiari.
Possiedono componenti linfocitari regolatori (CD4 e CD8 soppressori)
Dopo la maturazione i linfociti migrano nella zona marginale e in seguito nei linfonodi
regionali.
Da questo punto in poi possono intraprendere due vie per maturare a plasmacellule:
98% ritornano nellorgano di provenienza.
2% penetra nel dotto toracico e migra verso disparate zone anatomiche.
Lintero processo regolato dai recettori 47 e dalla molecola di adesione MAdCAM-1
244
Il 2% degli elementi linfoidi che migra verso sedi anatomiche differenti da quella di
provenienza servono per proteggere gli altri organi da una seconda eventuale
esposizione allAg in una sede diversa da quella del contatto primario. In sostanza
cercano di anticipare e prevenire una seconda infezione rendendo immunocompetenti
tutti gli organi nei confronti di quel determinato Ag!!
Gli LZME sono spessi correlati alla presenza di microrganismi:
Gastrico: Helycobacter Pilorii
Cutaneo: Borrelia Burgdoferi
Oculare: Chlamydia Psittacii
Intestino: Campylobacter Jejuni
LZME Gastrico:
Correlazioni con infezione da H. Pilorii
Questo linfoma associato alla formazione di MALT gastrico che causa, a lungo
termine, fenomeni autoimmuni.
Vi anche una correlazione con linfezione da Helycobacter Pilorii in particolare dello
stipite CagA+ che risulta essere il pi virulento.
Questo stipite stimola una massiva produzione di IL-8 che, a sua volta, stimola
massivamente lattivit ossidativa dei neutrofili aumentando le probabilit di danno al
genoma dei linfociti B!
Linfezione da H. Pilorii causa, pi frequentemente, di LZME che di carcinoma a
livello gastrico e, nelle zone ad alto tasso dinfezione da questo microrganismo, gli
LZME raggiungono il 20% dei linfomi totali!
Si notato che mettendo in coltura le cellule del linfoma da sole esse morivano.
Se, invece, le cellule venivano messe in coltura con h. Pilorii ed elementi del sistema T
linfocitario (CD40-CD40 ligando/CD153) il tumore proliferava.
Ci port a scoprire che luso della terapia antibiotica volta a eliminare H. Pilorii
causa anche remissione del linfoma in una porzione significativa dei casi!
Sono documentati anche casi correlati allinfezione da HCV che regrediscono dopo
trattamento con ribavirina.
Morfologia
Cell di piccola taglia con diversi profili e forme:
> simili ai centrociti: confondibili con linfoma mantellare
> simili a plasmacellule
>
La patologia la medesima nonostante la forma!
245
Vi sono, inoltre, diversi elementi strutturali:
Hanno la tendenza ad aggredire le strutture ghiandolari della
mucosa gastrica causando lesioni linfoepiteliali normalmente
assenti.
Assumono una distribuzione focale che interessa estesamente il
parenchima dellorgano; per questo motivo in passato la
gastrectomia parziale risultava inefficace.
Diagnosi e Trattamento
Serve lendoscopia con prelievo di materiale bioptico per verificare il livello di
penetrazione nella parete gastrica.
Le lesioni molto infiltrative e con interessamento delle linfoghiandola di rado
regrediscono con la terapia antibiotica, servono altre soluzioni terapeutiche.
In caso di funzionamento dellantibiotico il linfoma va in necrosi.
Dopo opportuno eseguire biopsie a intervalli regolari per tenere sotto controllo la
situazione e prevenire eventuali recidive:
1 biopsia a distanza di un mese per valutare leradicazione del batterio.
2 biopsia 3 mesi dopo per valutare la risposta del tessuto neoplastico (nel caso
non risponda serve il cambio della terapia).
3 biopsia sempre a distanza di 3 mesi per controllare
4 biopsia si possono cominciare ad effettuare a intervalli di 6 mesi/1 anno per
tutta la vita.
In alcuni casi la PCR pu evidenziare una piccola banda monoclonale che pu
rappresentare lo stipite linfoide alterato ma in realt non predittivo, serve sempre e
comunque la biopsia.
Fenotipo
Il marker principe di questa patologia IRTA-1 espresso dagli elementi della zona
marginale.
Genotipo
In questo tipo di linfoma si hanno cell che non vanno pi incontro a ipermutazioni, le
mutazioni somatiche che presentano sono stabili.
Vi un riarrangiamento dei geni per le Ig in particolare per le IgVh in concomitanza
con tre differenti tipi di traslocazioni:
t14-18: una traslocazione differente da quella del linfoma follicolare che porta
il gene MALT1 sotto il controllo del promoter delle catene H delle Ig causando
la sua sovraespressione.
t1-14: questa traslocazione porta il gene Bcl-10 sotto il controllo del promoter
per le catene H delle Ig che porta a una sovraespressione di MALT1
t11-18: questa traslocazione si riscontra nel 35% dei casi e porta alla creazione
di un gene di fusione API1-MALT1 che porta a una sovraespressione di
MALT1.
246
Tutte e tre le traslocazioni portano alla sovraespressione del gene MALT1 che porta
alla sovrapproduzione di NFK- che protegge la cell dallapoptosi.
Schema di Isaacsson
Evalido nel 55% dei casi perch nel restante 45% la malattia non regredisce in seguito
a terapia antibiotica.
Vi sono due elementi discriminanti:
Profondit dellinfiltrato
Anomalie cromosomiche
I casi in cui la malattia non risponde alla terapia antibiotica sono tre:
La malattia occorsa in assenza di H. Pilorii
Il linfoma si altamente infiltrativi
Le cellule neoplastiche portino nel loro genoma t1-14 o t11-18
Linfoma di Hodgkin
Cos chiamato perch scoperto nel Gennaio del 1832 da Thomas Hodgkin, che lo
descrisse sulla base di sette casi studiati, dei quali ancora oggi 5 sono validi e sono
riconosciuti come casi facenti parti del LH.
un tumore del tessuto epiteliale che del tutto sui generis in quanto presenta:
- molte poche cellule neoplastiche (1-2%) del tessuto esaminato
- un abbondante pabulum reattivo che contiene le cellule neoplastiche.
Cellule neoplastiche
Sono di due tipi :
1) cellule di Hodgkin: unilobate
2) cellule di Reed-Stenberg: plurilobate
Le caratteristiche comuni ai due tipi di cellule sono le seguenti:
1) si tratta di cellule molto grandi (in particolare le cell. RS hanno diametro >
60m.
2) Hanno nucleoli molto sviluppati che occupano pi del 50% della spf del nucleo
ed in particolare vi presenza sempre di un grande nucleolo con le
caratteristiche di un inclusione aventi le dimensioni di un piccolo linfocita.
3) La loro particolare morfologia fa s che ci si possa riferire a loro come a cellule
diagnostiche.
4) Sono contenute in un pabulum citologico reattivo (infiammatorio) non
neoplastico. Questo fa s che la loro presenza, sia diagnostica della malattia.
Pabulum reattivo
formato da elementi linfoidi e non linfoidi. Si tratta di un corteo infiammatorio che
dovuto allelevato scambio di mediatori chimici fra il tessuto neoplastico ed i tessuti
limitrofi.
247
I mediatori chimici possono essere prodotti sia da cellule neoplastiche, sia da cellule
dei tessuti limitrofi, e possono avere azione paracrina, cos come azione endocrina, di
autostimolaziione.
Bisogna comunque sottolineare che le cellule di accompagnamento contenute nel
pabulum reattivo costituiscono la grande prevalenza celllulare e che le cellule
neoplastiche si trovano ad essere in netta minoranza.
Istogenesi del LH
Listogenesi del LH stata a lungo sconosciuta, tanto che inizialmente si parlava di
malattia di Hodgkin.
Solo in un secondo momento si scoperta la derivazione linfoide di questa malattia e
le si dato il nome di Linfoma di Hodgkin.
Classificazione del LH
Il linfoma di Hodgkin si pu sostanzialmente dividere in due tipi principali, a loro
volta suddivisibili in sottotipi.
A. LH a prevalenza linfocitaria
Nodulare
Diffusa
B. LH di tipo comune ( di pi frequente osservazione
Forma ricca di linfociti (RL): la componente reattiva
rappresentata da linfociti
Forma a sclerosi nodulare (SN): vi tendenza della popolazione
reattiva e neoplastica ad aggregarsi in noduli circondati da tralci
fibrosi molto grossolani
Forma a cellularit mista (CM): pabulum molto ricco con
popolazione reattiva molto varia.
Forma a deplezione linfocitaria (DL) la componente reattiva ha
pochi linfociti.
Linfoma di Hodgkin a prevalenza linfocitaria
- una variet rara che costituisce il 4-5% dei casi di LH.
- Le caratteristiche cliniche distintive sono:
I. picco di incidenza verso i 40 anni distribuzione unimodale che
rappresentabile con una curva gaussiana.
II. Tendenza alla diffusione nellorganismo uguale a quella dei LNH. Il LH non
insorge mai primitivamente nel midollare ma sempre in una linfoghiandola e
da qui pu quindi distribuirsi variamente allorganismo.
III. Decorso indolente.
248
IV. Spesso presenta recidive a distanza di anni dal momento della remissione
completa (anche dieci anni o pi), ma la prognosi migliore di quella della
forma comune.
V. La malattia ha evoluzione trpida che dunque non progredisce in modo rapido
e sistematico.
VI. Nella sua evoluzione pu anche progredire in un linfoma a grandi cellule B
secondario.
Dunque questa forma di tumore ha un decorso clinico del tutto peculiare, per molti lati
dissimile da quello della forma comune del linfoma di Hodgkin.
Quindi il problema nel trattamento di questa forma rilevante.
Su di esso vengono applicate le medesime terapie utilizzate per la forma comune ma si
tratta molto speso di terapie sovradosate. Nella terapia vengono utilizzati farmaci
tossici che a loro volta possono essere causa di tumori secondari.
Attualmente in via di definizione una terapia ottimale nel rapporto costi/benefici.
Forma nodulare
Costituisce l80% delle forme a prevalenza linfocitaria.
caratterizzata dalla presenza di un infiltrato di noduli costituiti da piccoli linfociti B
(cellule di accompagnamento)frammisti ad un numero variabile di istiociti benigni ed
alle cellule neoplastiche.
Cellule neoplastiche: le cellule diagnostiche qui sono molto difficili da ritrovare e sono
invece pi comuni cellule definite cellule pop-corn.
Le caratteristiche delle cellule pop-corn sono le seguenti:
- cellule voluminose.
- Presenza di un nucleo polilobato ed alla periferia policiclico., simile ad un
nocciolo di pop-corn.
- Nucleoli appariscenti
- Cromatina finemente dispersa.
- Citoplasma relativamente abbondante
Le cellule pop-corn sono cellule neo-plastiche e sono le cellule che si riscontrano pi
comunemente nel nodulo.
I noduli delle forme a prevalenza linfocitaria entrano in diagnosi differenziale con
linvoluzione del centro germinativo.
Terminata la sua funzione infatti il centro germinativo evolve in diversi modi uno dei
quali viene definito, centro germinativo progressivamente trasformato.
La denominazione infausta poich fa pensare ad una trasformazione neoplastica,
quando in realt si tratta di una normale involuzione del centro germinativo e sua
sostituzione con linfociti del mantello.
La diagnosi differenziale sembra facile, poich nel LH a prevalenza linfocitaria vi
presenza delle cellule pop-corn, che sicuramente sono assenti nellinvoluzione normale
del centro germinativo.
249
Tuttavia la diagnosi differenziale complicata dal fatto che pu capitare di vedere le
due strutture contemporaneamente in un medesimo linfonodo. Si possono trovare
soggetti:
- soggetto con un linfoma di Hodgkin che nella precedente biopsia mostrava
centri germinativi progressivamente trasformati.
- Soggetto nel quale il linfoma di Hodgkin sia stato trattato con successo, che
nelle biopsie successive presenta centri germinativi progressivamente
trasformati.
Questo ci porta a concludere che sebbene il centro germinativo progressivamente
trasformato non sia un elemento neoplastico, n sia la causa del LH a prevalenza
linfocitaria, costituisce tuttavia un fattore di rischio, che pu involvere in questa forma
di tumore.
Forma diffusa
Costituisce il 20% delle forme a prevalenza linfocitaria.
dovuta alla diffusione ed alla fusione dei diversi noduli contenenti cellule pop-corn,
dunque la sua realizzazione spesso rappresenta una progressione della malatia.
La progressione biologica e clinica comporta anche ad una variazione delle cellule
reattive di accompagnamento:
- perdita delle cellule follicolari dendiritiche
- mutazione Linfociti B Linfociti T.
Questo porta ad una necessaria diagnosi differenziale con il T cell rich B linphoma
(linfoma a grandi cellule B ricco in linfociti T).
Oggi esistono marcatori molecolari che consentono una distinzione con questo tumore (
e con altre forme di tumori): ci molto importante da un punto di vista terapeutico
perch il linfoma a grandi cellule B ricco in linfociti T molto pi aggressivo e va
dunque trattato diversamente.
Immunofenotipo delle forme a prevalenza linfocitaria
- Ag comune linfocitario: questo un Ag molto espresso dagli elementi
emolinfopoietici e presente anche nelle cellule pop-corn. Costituisce inoltre un
elemento distintivo, poich la variet comune manca di esso.
- Marcatori dei linfociti B:
CD20 cellule pre-B e cellule B mature non plasmacellulari.
CD79 cellule pre-B e cellule mature
- EMA ( Epithelial Mbr Antighen) o Ag epiteliale di membrana: scoperto per la
prima volta su elementi epiteliali, ma non ristretto agli stessi. caratteristico
del linfoma di Hodgkin.
- Bcl-6: molecola che connette il linfoma di Hodking alle cellule del centro
germinativo. Questa correlazione confermata da dati di biologia molecolare.
- Oct-2, BOB1, PU1 sono molecole facenti parte di un sistema trascrizionale che
codifica per i geni che regolano la trascrizione delle Ig. integrato ed altamente
conservato.
250
Le cellule neoplastiche (forma nodulare) si trovano immerse in un pabulum reattivo
costituito da linfociti, principalmente B, ma anche linfociti T.
In particolare nellintorno della cellula neoplastica vi una rosetta di cellule che non
esprimono i marcatori B.
Si tratta di una rosetta di T linfociti (esprimenti CD57) e di cellule follicolari
dendritiche, presenti in grande quantit, le quali confermano la correlazione
fenogenetica del tumore con le cellule del centro germinativo.
Genotipo delle forme a prevalenza linfocitaria
La derivazione da cellule del centro germinativo confermata d studi di biologia
molecolare.
Solitamente gli studi di biologia molecolare sono compiuti tramite estrazione del DNA
o dellmRNA neoplastico, dal campione patologico, poich le cellule neoplastiche sono
le cellule prevalenti nei campioni.
In questa forma di linfoma per le cell. neoplastiche rappresentano solo l1-2% delle
cellule presenti, dunque lestrazione di DNA o mRNA dal campione porta lettura del
genotipo solo degli elementi reattivi.
Dunque deve essere utilizzata una metodologia differente:
1. le cellule sono scontornate: dunque vengono prelevate da materiale
fresco crioconservato singole cellule tumorali.
2. una decina di cellule neoplastiche sono poste in provetta
3. Dunque viene fatta estrazione del DNA o dellmRNA solo da cellule
tumorali.
DNA: il processo di processazione dl DNA e riconoscimento del profilo di espressione
genica stato del tutto completato. Si utilizzata single-PCR cio reazione
polimerasica a catena sul DNA estratto da singole cellule. Ci permette i capire che le
cellule neoplastiche del LH a prevalenza linfocitaria sono:
a. tutti linfociti B
b. monoclinali
c. portano molte mutazioni somatiche le quali spesso sono in fieri e non del
tutto completate (iopening mutations).
Tutto ci permette di ricondurre questo tumore ad una derivazione dalle cellule del
centro germinativo. De resto il CG da origine a molti tumoi di diversa natura proprio
per la sua intrinseca instabilit.
Terapia
Viene erroneamente affermato che dal linfoma di Hodgkin si guarisce con grande
frequenza.
In realt il 30% dei pz con LH non risponde alla terapia e va incontro a morte.
251
Questo vero in particolare modo per il tipo comune di LH, che anche quello di
assoluto maggiore riscontro.
LH a prevalenza linfocitaria se recidiva (cosa abbastanza frequente) risponde
nuovamente alla medesima terapia.
LH di tipo comune non sempre risponde alla terapia:
- fin dallinizio
- dopo recidive: esse non rispondono a terapie anche sovramassimali.
- Andamento strisciante: nonostante la terapia il tumore rimane torpido o crea
uno strano equilibrio con lospite.
Attualmente si sta cercando di raccogliere una casistica ampia di pz che non
rispondono con successo alla terapia in modo da creare un confronto efficace fra:
- profilo di espressione genica dei pz che rispondono alla terapia
- profilo di espressione genica dei pz che non rispondono alla terapia.
La terapia del LH si cmq molto modificata dagli anni 60 in poi:
- una volta veniva utilizzata la terapia MOPP: questa sembrava dare un enorme
numero di risultati positivi, ma successivamente ha determinato un 20% di
tumori secondari di altro tipo.
- Attualmente si sta ancora studiando la terapia. Il linfoma di Hodgkin presenta
ancora problemi e ci dimostrato dalla larga fetta di persone non responsive
alle terapie, nonostante la prevalenza di una prognosi positiva.
Linfoma di Hodgkin di tipo comune
Presente in 4 variet istologiche fondamentali:
- ricco in linfociti RL
- a sclerosi nodulare SN
- a cellularit media CM
- a deplezione linfocitaria DL
le quali presentano un progressivo aggravamento da un punto di vista prognostico.
La distribuzione con let bimodale, dunque vede due picchi:
- nel passaggio fra la seconda e la terza decade : fra i 16 ed i 25 anni
- nel passaggio fra la sesta e la settima decade: fra i 60 ed i 70 anni
Questa forma di neoplasia presenta una possibile correlazione con il virus EBV e ci
dimostrato dallet prevalente di manifestazione del tumore:
Il primo picco del tumore si ha infatti nellet in cui si ha pi frequentemente il primo
contatto con EBV, e si contrae inizialmente la mononucleosi infettiva.
252
Il secondo picco del tumore si ha invece ad un et in cui si ha spesso un fisiologico
abbassamento delle difese immunitarie, con conseguente riattivazione del virus
latente.
La modalit di diffusione di questo tumore ordinata e progressiva (sulla base del
postulato di Kaplan???)
Questo significa che il tumore ha inizio da una stazione linfonodale e
progressivamente, seguendo landamento della linfa coinvolge i nuovi linfonodi.
proprio sulla base di questa diffusione ordinata e progressiva del LH di tipo comune
che stata enunciata una stadiazione dei tumori,che risulta applicabile a molti
tumori, ma valida soprattutto per il LH di tipo comune.
Grado I: interessamento di una sola regione linfonodale (I) o interessamento di un
singolo organo o sito extralinfatico (IE).
Grado II: interessamento di due o pi regioni linfonodali dal medesimo lato del
diaframma (sotto o sopra) (II) o interessamento del solo organo e tessuto extralinfatico
contiguo (IIE)
Grado III: interessamento delle regioni linfonodali su entrambi i lati del diaframma
(III), o interessamento che comprende la milza (IIIs), o/e interessamento che
comprende il solo organo o sito extralinfatico contiguo (IIIE, IIIES).
Grado IV: focolai multipli e disseminati di interessamento di uno o pi organi o tessuti
extralinfatici, con o senza coinvolgimento linfatico.
Questa stadiazione comporta il fatto che non vi pu essere coinvolgimento
contemporaneo di un solo linfonodo e del midollo osseo.
La milza viene a costituire un coinvolgimento importante.
Naturalmente via via che si avanza di grado si hanno prospettive prognostiche
peggiori.
La stadiazione dunque predittiva della prognosi e molto importante da un punto di
vista terapeutico. Essa richiede un attento esame obiettivo e diagnostico,
comprendente procedure di imaging radiologico delladdome, della pelvi e del torace
nonch biopsia del midollo osseo.
LH di tipo comune ricco in linfociti
una forma rara di LH di tipo comune.
Veniva in passato inserita nella pi ampia categoria di LH a prevalenza linfocitaria,
poich le cellule di accompagnamento sono piccoli linfociti.
Ha assunto successivamente autonomia poich:
- non ci sono cellule pop-corn
- le cellule diagnostiche sono di frequente osservazione e non eccezionali.
- Lespressione fenotipica quella del normale LH.
Risulta tuttavia necessaria diagnosi differenziale con LH a prevalenza linfocitaria.
253
Nella maggior parte dei casi i linfonodi sono infiltrati diffusamente, per pu essere a
volte osservata vaga nodularit.
associata allEBV nel 40% dei casi ed ha una prognosi da molto buona ad eccellente.
LH tipo comune a sclerosi nodulare
la forma pi comune costituendo il 65-70% dei casi. Presenta variet di distribuzione
geografica con grande prevalenza in Italia, Francia U.S.A. Nel Nord Europa invece
rappresenta solo un 20-30% dei casi di LH.
Interessa prevalentemente giovani donne.
Nella maggior parte dei casi esordisce con una massa neoplastica mediastinica, il che
dimostra una correlazione con il linfoma a grandi cellule B di tipo diffuso a prevalenza
mediastinica.
Lintegrazione del virus EBV dimostrata nel 33% dei casi, fra cui la quasi totalit dei
casi presenti in Africa.
La morfologia di questo tumore caratterizzata da:
1) struttura del linfonodo con
aggregati nodulari
reazione fibrotica ordinata, con formazione di bande di sclerosi, che di
solito originano dalla capsula, che circondano e dividono i noduli.
2) si trovano poche cellule diagnostiche
3) si ritrova grande prevalenza di un tipo particolare di cell. neoplastiche, le cellule
lacunari, caratterizzate da:
un solo nucleo, leggermente ripiegato o multilobato.
Citoplasma chiaro con pochi organuli.
Se si esegue trattamento con mezzi chimici aggressivi il
citoplasma si raddensa intorno al nucleo, lasciando lacune
nello spazio citoplasmatico (artefatto di fissazione, che
attualmente non si riscontra pi, per luso di mezzi chimici
pi delicati).
4) il pabulum molto variabile e le cellule neoplastiche sono circondate da un vero
e proprio corteo di cellule reattive: linfociti, plasmacellule, eosinofili, macrofagi.
Grading del LH-SN
Fornisce fattori prognostici:
SN di tipo I:
- pi comunemente poche cell. neoplastiche in abbondante pabulum reattivo.
254
SN di tipo II:
- Si verifica quando si presenta un quadro citologico differente; noduli che
contengono molte cellule neoplastiche e molte cellule fibrose o istiocitarie.
- pi dell80% dei noduli deve avere composizione fibro-istiocitaria.
- Pi del 25% dei noduli deve avere prevalenza di cellule neoplastiche
pi aggressivo e richiede dunque un trattamento diversificato.
Linfoma di tipo comune a cellularit mista
Costituisce circa il 25-30% dei casi di linfoma.
di pi comune osservazione nei soggetti di sesso maschile.
Il coinvolgimento linfonodale prende la forma di un coinvolgimento pi o meno diffuso
e pi o meno composto della struttura delle linfoghiandole.
Linfiltrato cellulare molto eterogeneo comprendendo: piccoli linfociti, eosinofili,
macrofagi, plasmacellule, frammiste a cellule neoplastiche.
Le cellule neoplastiche in questo tumore sono facilmente identificabili, ma non
prevalenti. Vi un maggior numero di cellule di Reed-Stenberg.
Vi integrazione del virus EBV nel 90% dei casi.
La prognosi molto buona
Linfoma di tipo comune a deplezione linfocitaria
molto raro venendo a costituire meno del 5% dei casi di linfoma.
caratterizzato dalla scarsit di linfociti contrapposta ad una relativa abbondanza di cellule
neoplastiche.
Ve ne sono due sottotipi:
1. fibroso o fibro-istiocitario: composto da fibroblasti e da cellule istiocitarie.
2. sarcomatoso prevalenza di cellule neoplastiche
Queste due varianti sembrano riunire quella che listologia del linfoma di tipo
comune a sclerosi nodulare di tipo II: la differenza fra questa due forme per
fondamentale perch nel linfoma DL non vi presenza di noduli.
La componente fibrosa o sarcomatosa si diffonde in modo uniforme in ogni tessuto
interessato dal tumore, sostituendosi omogeneamente ai linfociti, senza dare luogo ad
alcun aspetto nodulare.
Questo linfoma un linfoma pi aggressivo e con prognosi meno favorevole dei
precedenti. In particolare la forma sarcomatosa, che la pi aggressiva, entra in
255
diagnosi differenziale con il linfoma a grandi cellule B di tipo diffuso e con il linfoma a
cellule anaplastiche. DL va riconosciuto, perch si tratta invece di una forma pi
aggressiva.
spesso associato con lintegrazione del virus EBV.
Fenotipo del Lh di tipo comune
CD30+: i linfomi di Hodgkin di tipo comune hanno costante espressione di questa molecola, inizialmente
descritta come caratteristica esclusiva dei LH su Nature.
In realt anche se questa molecola sempre presente nei Lh di tipo comune, non
ristretta ad essi.
Si pu trovare anche in situazioni neoplastiche linfoidi di altro genere o in espressioni
non neoplastiche.
infatti una molecola caratteristicamente espressa da elementi linfoidi attivati
celllule B attivate, cellule T e monociti).
espressa in modo variabile anche dalle cellule diagnostiche.
Pu essere utilizzata anche come bersaglio terapeutico di Ac monoclinali. Si tratta di
una immunoterapia ancora gestita da un numero limitato di centri ed utilizzata come
terapia integrativa, volto alleliminazione di malattia residua.
La sua espressione nel linfoma di Hodgkin va di pari passo con la negativit dello
stesso per:
Ag comune linfocitario
Ema espressa eccezionalmente.
CD15+: una molecola normalmente espressa dai granulociti. presente almeno nel
75% dei Lh di tipo comune.
CD45 questo differenzia nettamente la forma a prevalenza linfocitaria da quella di
tipo comune.
Marcatori di linea B (CD20, CD79) o di linea T:
- 75% dei casi fenotipo NULL: negativit per lespressione di marcatori B e T
- 23% dei casi espressione di marcatori prevalentemente di tipo B
- 1-2% dei casi espressione di marcatori di linea T: si tratta di tumori spesso non
coerenti anche con le altre caratteristiche molecolari di questo tumore.
BSAP (B Specific Activator Protein)+:
una molecola molto espressa fin dalle fasi pi precoci dello sviluppo degli elementi
B. Si tratta infatti della prima molecola specifica espressa dai linfociti B, che si
mantiene fino al livello di plasmacellule.
Il 98% dei Lh di tipo comune esprime questa molecola nelle cellule tumorali
diagnostiche. Dunque la maggior parte dei casi riconosce in questo modo una
derivazione delle cellule neoplastiche dai linfociti B.
Questo marcatore importante perch invece, come si visto, molto spesso il fenotipo
per i marcatori di linea B o T null, e per le diagnosi differenziali con gli altri tipi di
tumori.
256
Bcl6
Oct-2, BOB1, PU1 -: manca il sistema trascrizionale tipico dei tumori a prevalenza
linfocitaria.
IRF4+ indicativo del fatto che le cellule neoplastiche derivano da elementi B che
hanno gi lasciato il centro germinativo.
Genotipo del LH di tipo comune
Viene utilizzata nella maggior parte dei casi, la tecnica di isolamento delle cellule tumorali gi
menzionata per il LH a prevalenza linfocitaria.
La single PCR mostra che nella maggior parte dei casi sussistono riarrangiamneti
clonali dei geni per le immunoglobuline il che conferma che il tumore tragga origine
dalle Ig che hanno gi attraversato il centro germinativo.
Solamente nell1-2% dei casi vi un riarrangiamento dei geni per il TCR, il che
conferma loccasione derivazione degli elementi neoplastici dai linfociti T.
Cinetica cellulare
La cinetica connessa con lo studio della frequenza di proliferazione e di apoptosi di un dato tipo di
cellule.
Le cellule neoplastiche del Lh di tipo comune presentano citocinesi inefficiente.
Si ha che il 60-90% delle cellule neoplastiche esprime Ag legati alla proliferazione
celllulare. Secondo questo dato, dunque le cellule neoplastiche dovrebbero
rapidamente soverchiare le cellule reattive, ma ci non avviene.
Questo si spiega attraverso la dimostrazione del fatto che le cellule sono in ciclo, ma si
trovano congelate in ciclo: solo una piccola parte arriva alla fase terminale del ciclo e
dunque va incontro a reale moltiplicazione.
In compenso si tratta di cellule molto protette dallapoptosi, con basso indice
apoptotico.
Questo consente una loro, seppur modesta, crescita.
Il fatto che la maggior parte delle cellule si trovi in ciclo, rende le cellule sensibili ai
farmaci ciclo-specifici.
Lo studio della cinetica cellulare prevede la valutazione dellespressione di Bcl-2 ( che
ha attinenza con la protezione dallapoptosi) e di p53 ( che si collega ad una citocinesi
inefficace, bloccando le cellule in un punto del ciclo).
I casi che vedono espressione di p53 e contemporaneamente di Bcl-2 hanno
comportamento pi aggressivo: in questo modo questi elementi concorrono alla
identificazione di un rischio individuale.
257
Connessione con EBV
Il virus di Epstein-Barr si trova integrato nel menoma delle cellule neoplastiche in una quota notevole
di casi:
- 33% dei casi in forma SN
- 40% dei casi in forma RL
- 90% dei casi in forma CM
Le cellule neoplastiche con integrazione di EBV esprimono le LMP (Late Membrane Protein) che,
stimolando la produzione di NFK-, sono in grado di indurre la proliferazione cellulare e proteggere le
cell dallapoptosi; sono dunque oncotrasformanti.
Nei casi in cui EBV si trova ad essere integrato, dunque, esso viene a fare parte della linfomagenesi.
Attualmente in discussione lutilit preventiva di una eventuale vaccinazione contro EBV per
prevenire il linfoma di Hodgkin.
Lassociazione tra EBV ed il tumore confermata da dati epidemiologici di conferma:
- soggetti ce hanno contratto la mononucleosi infettiva hanno maggiore probabilit di ammalarsi
di LH.
- LH presenta spesso andamento stagionale, con maggiore insorgenza in primavera.
Inoltre alla correlazione con EBV stato riconosciuto un significato prognostico:
a. EBV contratto in et giovanile: non vi significato prognostico negativo.
b. EBV contratto in et senile: fattore prognostico molto negativo.
Terapia
auspicabile che le tecniche di gene expression profiling consentiranno di fare un confronto tra le
mutazioni genetiche presenti:
- nei casi che rispondono alle terapie
- nei casi che non rispondono alle terapie.
Attualmente per il profilo di espressione genica stato studiato su un numero di linee cellulari troppo
limitato, che non rispecchia la variet e la casistica dei linfomi di Hodgkin presenti in realt.
Per il momento questi studi, hanno dimostrato la notevole diversit dei linfomi a prevalenza
linfocitaria, con i linfomi del tipo comune e questo porta ad avere dei dubbi sull attuale protocollo
terapeutico, che prevede la somministrazione della medesima terapia ad entrambe le forme, dove quella
a prevalenza linfocitaria sicuramente meno aggressiva.
258
Tumori dellipofisi
Cenni strutturali:
Organo dalla forma circa di un fagiolo.
- Dimensioni: diametro 1cm. aumenta nel periodo gravidico
- Peso: 0.5g.
- Localizzazione: alla base del cranio, allinterno della sella turcica, nelle
vicinanze del chiasma ottico e dei seni cavernosi.
- Collegata allipotalamo attraverso il peduncolo ipofisario, che fuoriesce dalla
sella turcica mediante un foro della dura madre.
- Funzione: con lipotalamo regolazione delle altre ghiandole endocrine.
Suddivisione dellipofisi:
Lipofisi suddivisa in tre parti principali:
1. lobo anteriore o adenoipofisi:
parte distale: componente pi importante
parte intermedia
parte tuberale: localizzata sulla spf del peduncolo ipofisario.
2. zona intermedia: residui cistici della tasca di Rathke
3. lobo posteriore o neuroipofisi:
infundibulo
peduncolo
lobo posteriore
Adenoipofisi
Costituisce circa l80% della ghiandola
Deriva embriologicamente dalla tasca di Rathke (estroflessione della cavit orale,
dalla quale viene separata dalla progressiva crescita dellosso sferoidale)
Dotata di un sistema vascolare di tipo portale che costituisce il mezzo di trasporto
degli ormoni ipofisari, ma anche ipotalamici.
Tipi cellulari delladenoipofisi
Classificazione su basi tintoriali
- Cellule cromofobe (50%). Assumono pochi coloranti. Non producono ormoni o li
producono, ma li rilasciano con eccessiva velocit.
- Cellule acidofile (40%). Assumono coloranti acidi.
- Cellule basofile (10%). Assumono coloranti basici.
una classificazione desueta, poich oggi si sa che laffinit ai coloranti espressione
solo della loro funzionalit secretoria cio dei granuli contenuti.
Dunque la cellula cromofoba semplicemente una cellula non secernente o secernente
troppo in fretta, ma ci non ha grossa rilevanza da un punto di vista clinico-patologico.
Classificazione funzionale
quella attualmente utilizzata: riflette la classificazione dei tumori.
259
1. Cellule gonadotrope (10%) (FSH-LH):
sono cellule solitamente basofile
producono FSH stimola la formazione dei follicoli ovarici
producono LH induce lovulazione e la formazione del corpo luteo.
2. Cellule tireotrope (5%) (TSH)
Sono cellule solitamente debolmente basofile.
Producono TSH ormone tireo-stimolante
3. Cellule somatotrope (50%) (GH)
Sono cellule solitamente acidofile.
Secernono GH ormone della crescita
4. Cellule lattotrope (mammotrope) (20%) (PRL)
Sono cellule solitamente acidofile
Secernono prolattina ruolo essenziale nella lattazione
5. Cellule corticotrope (15-20%) (ACTH)
Sono cellule solitamente basofile.
Secernono principalmente ACTH ormone adenocorticotropo
Ma anche propiomelonocortina, MSH (ormone stimolante la crescita dei
melanociti), endorfine, lipotropina.
Adenomi dellipofisi
- incidenza: 10-25% dei tumori intracranici
- et: soprattutto donne fra la 3 e la 6 decade di et; il tumore pu insorgere
anche correlato alla gravidanza ed frequente data lalterazione ormonale.
- Dopo gli 80 anni colpito un 20% dei soggetti
- I sintomi clinici sono: cefalea, deficit visivo, incoscienza.
- Numero: meno dell1% dato da tumori multipli
La distinzione di questi tumori pu essere fatta in base a tre caratteristiche:
1. dimensione del tumore:
Microadenomi: diametro < 1 cm.
Macroadenomi: diametro > 1 cm.
2. benignit o malignit:
Benigni: comportamento usuale
Maligni: forme molto rare che sono solitamente localizzate nello spazio
subaracnoideo, e che possono dare metastasi a distanza.
3. invasivit:
non invasive: localizzate allinterno della sella turcica
invasive:
Generalmente di maggiori dimensioni
Hanno maggiore probabilit di dare sintomatologia evidente
Sono loco-regionali nellesordio
260
Successivamente infiltrano dura madre, pavimento della sella
turcica, seno sferoidale, nervi, dunque interessano le varie
strutture allinterno della sella.
Linvasivit determina una prognosi peggiore
Il trattamento terapeutico pi complesso
4. funzionalit:
Adenomi ipofisari silenti:
vi dimostrazione immunoistochimica e/o ultrastrutturale della
produzione ormonale solo a livello tissutale, senza sintomi clinici
riferibili a iperproduzione ormonale.
Sono i pi voluminosi.
Costituiscono un terzo dei tumori ipofisari operati.
Possono rendersi clinicamente manifesti in una fase pi tardiva
rispetto a quelli con sintomi endocrini e per tale motivo si
presentano pi spesso come macroadenomi.
Adenomi ipofisari funzionanti:
Associati ad aumentati livelli ormonali e conseguenti
manifestazioni cliniche.
Sono i pi frequenti.
Adenomi ipofisari non secernenti o da disfunzione endocrina:
Iperpituitarismo (70%) dei casi
Ipopituitarismo (30%) dei casi
o da distruzione o compressione della ghiandola
o per interferenza con il rilascio di ormoni ipotalamici.
Gli adenomi ipofisari sono generalmente costituiti da un singolo tipo cellulare e
producono un singolo ormone predominante, sebbene vi siano eccezioni.
Alcuni adenomi possono secernere due ormoni (GH e prolattina rappresentano
lassociazione pi frequente), pi raramente si hanno adenomi a secrezione multipla.
Sintomi loco regionali
- cefalea:
da stiramento della dura madre
da idrocefalo
- compromissione dei nevi intracranici:
disturbi visivi
oftalmoplegia
compressione 1 e 2 branca del trigemino
- compromissione del chiasma ottico:
emianopsia eteronima bitemporale: vengono compresse nel chiasma le
porzioni nervose che portano il segnale dalla porzione esterna bilaterale del
campo visivo
- rinorrea liquorale e/o meningi ricorrenti:
rare, da erosione della sella turcica.
261
Aspetti macroscopici
- consistenza soffice
- forma irregolare: questo rende spesso difficile la completa escissione chirurgica.
Aspetti istologici
Modalit (pattern) di crescita:
- solido
- alveolare
- trabecolare
- papillare (ACTH+): associato pi frequentemente ad iperpituarismo
- pseudoghiandolare (gonadotropo): associato pi frequentemente ad
iperpituarismo
- fusiforme
Mitosi scarse o assenti
Calcificazioni (7%) e depositi ialini di tipo amiloide soprattutto nelle forme a PRL.
Quseti depositi sono visibili anche con tecniche di imaging).
Classificazione degli adenomi
Classificazione istologica tradizionale degli adenomi
- cromofobi
- acidofili
- basofili
Classificazione immunoistochimica ed ultrastrutturale
Attualmente viene utilizzata questa classificazione funzionale che tiene conto delle
alterazioni ormonali.
- adenomi PRL
sparely granulated (26%)
densely granulated (1%)
- adenomi GH
sparely granulated (7%)
densely granulated (7%)
- adenomi misti GH e PRL (8%)
- adenoma funzionale corticotropo ACTH (14%)
- adenoma tireotropo (1%)
- adenoma gonadotropo (6%)
- adenoma null (26%)
- adenomi pluriormonali non classificati (4%)
La classificazione in densely granulated e sparely granulated aggiuntiva, ma di
scarsa rilevanza prognostica e non fondamentale da un punto di vista clinico-
patologico.
Si basa sulla presenza di granuli di tipo endocrino nelle cellule tumorali.
262
1. Forme densamente granulate: appaiono ricche di granuli voluminosi ripiene di
prodotto ormonale e sono pi intensamente cromofile.
2. Forme scarsamente colorate:granuli pi piccoli, RER ben sviluppato, Golgi
molto evidente, possibili aggregati di filamenti intermedi e/o ormoni. Sono
spesso cromofobe.
Prolattinomi
Rappresentano il tipo pi frequente di adenoma ipofisario iperfunzionante.
Costituiscono il 30% degli adenomi ipofisari diagnosticati clinicamente.
Microscopicamente si dividono in:
- prolattinomi a granuli sparsi (sono i pi frequenti): cellule debolmente eosinofile
o cromofobe.
- Prolattinomi a granuli densi (rari): cellule fortemente eosinofile.
Metodi immunoistochimici, cio Ac anti-prolattina, mettono in evidenza accumuli di
prolattina nei granuli di secrezione citoplasmatica.
I prolattinomi vanno incontro a calcificazioni di tipo distrofico, che vanno da piccoli
corpi psammomatosi (piccoli depositi di calcio) a estesi depositi calcifici che possono
occupare lintera massa tumorale. (calcoli ipofisari), fino alla deposizione di materiale
ialino simil-amorfo o simil-amiloide. Ci pu realizzarsi spontaneamente o dopo
trattamento del prolattinoma con bromocriptina (antagonista dei recettori per la
dopamina che in grado di indurre una diminuzione delle dimensioni del tumore).
La secrezione di prolattina da un adenoma funzionante un processo caratterizzata
da:
- Efficienza: pu causare iperprolattemia
- proporzionalit: secrezioni di prl proporzionali alle dimensioni delladenoma
Clinica
Nella donna (20-40 anni):
sindrome galattorrea- amenorrea: abbiamo un genizio attraverso i dotti galattofori,
associato ad amenorrea (quadro simil-gravidico).
I microadenomi incorrono in maggiore misura nellet fertile.
I macroadenomi sono pi rari ed incorrono di pi in et avanzata.
Nelluomo:
galattorrea associata spesso allimpotenza
C una maggiore frequenza di adenomi.
Adenomi somatotropi (GH-secernenti)
Secondo tipo pi frequente di adenomi funzionanti.
Il 40% dei casi presentano unalterazione genetica che si esprime in un deficit
dellattivit GTPasica.
263
Possono raggiungere notevoli dimensioni, in quanto le alterazioni che da essi derivano
progrediscono per decenni prima di essere diagnosticate.
Microscopicamente si dividono in 2 sottogruppi:
- A granuli sparsi: cellule cromofobe con notevole polimorfismo nucleare. Debole
reattivit immunoistochimica al GH.
- A granuli densi: cellule uniformi ed acidofile. Forte reattivit
immunoistochimica al GH.
Clinica
Nellinfanzia o nelladolescenza (non si ancora completata la saldatura delle epifisi):
- gigantismo: aumento generalizzato delle dimensioni corporee ed ossa di
lunghezza sproporzionata.
-
Nelladulto (si gi completata la saldatura delle epifisi):
- acromegalia:
Eccessiva crescita di cute, tessuti molli, visceri (tiroide, cuore, fegato,
surreni), ossa di faccia, mani e piedi (dita grandi a salsiccia).
Iperostosi: maggiore densit ossea della colonna vertebrale
Prognatismo: aumento delle dimensioni della mandibola che protrude,
con allungamento della parte inferiore della faccia.
A volte vi sono forme miste, se prese in et tardo-adolescenziale.
Sono pi frequenti i macroadenomi con espansione soprasellare ce pu portare ance a
manifestazioni compressive nelladulto (compressione del chiasma).
La terapia mira a riportare i livelli di GH nella norma ed a ridurre i sintomi legati alla
compressione da parte della massa, cercando di non provocare ipopituitarismo.
Il tumore pu essere rimosso chirurgicamente oppure distrutto attraverso terapia
radiante, o ancora viene ridotta la secrezione di GH attraverso terapia farmacologica.
Adenomi corticotropi
Sono adenomi generalmente funzionanti che al momento della diagnosi sono
generalmente di piccole dimensioni (microadenomi).
Microscopicamente si dividono in 2 sottogruppi:
- A granuli sparsi: pi occasionali
- A granuli densi: pi frequenti.
Clinica
1. Adenomi funzionanti:
sindrome di Cushing: iperproduzione surrenalica di cortisolo (stimolata
dallACTH)
sindrome di Nelson:
si tratta di adenomi deostruenti di grosse dimensioni
264
generalmente insorgono dopo rimozione chirurgica delle surrenali
a seguito del trattamento per la sindrome di Cushing.
Si verifica dunque a seguito della perdita delleffetto inibitorio
esercitato dai corticosteroidi surrenalici su un microadenoma
corticotropo pre-esistente.
Non sono pz con ipercortisolismo, ma presentano un notevole
effetto-massa da adenoma ipofisario
Possono presentare iperpigmentazione cutanea a causa della
stimolazione dei melanociti da parte dellMSH.
2. Adenomi silenti:
si tratta di adenomi che pur producendo ACTH non lo liberano, che
mancano dunque della fase escretoria.
LACTH rimane dunque a livello cellulare causando un accumulo ed un
ingrossamento delle cellule secretorie.
Per questo motivo gli adenomi silenti tendono ad essere macroadenomi e
ad andare incontro ad apoplessia, cio necrosi massiva dovuta alla
compressione esercitata dalladenoma.
Lapoplessia comunque si verifichi ( si pu verificare anche a seguito di
alterazioni neoplastiche, o a seguito di emorragia ostetrica) molto temibile
e peggiora notevolmente la prognosi.
Adenomi gonadotropi
Forme non molto frequenti.
Forme di difficile identificazione poich:
- spesso non sono funzionanti (secrezione ormonale inefficace e variabile).
- I prodotti secreti solitamente non provocano sintomatologia evidente.
Clinica
Presenti soprattutto in uomini e donne di mezza et.
Solitamente questi tumori causano ipopituitarismo, cio deficit complessivo nella
produzione di ormoni da parte delladenoipofisi. Ci dovuto alla compressione
dellipofisi nella sede sellare e soprasellare da partesi un macroadenoma.
Dunque i segni sono di tipo compressivo: allo slargamento della sella turcica ed alla
compressione del chiasma segue una sintomatologia neurologica caratterizzata da:
- disturbi della visione
- cefalea
- diplopia
- a volte apoplessia ipofisaria da compressione
In rari casi la sintomatologia con cui si presentano questi tumori proprio dovuta al
secondario deficit nella secrezione di gonadotropine.
Per esempio un deficit nella secrezione dellLH pu portare:
- negli uomini: diminuito testosterone diminuita forza fisica e libido
- nelle donne in pre-menopausa amenorrea
265
Adenomi a cellule tireotrope
Sono rari: 1% degli adenomi ipofisari
Sono costituiti da cellule cromofobe o basofile
Causa poco frequente di ipetiroidismo
Adenomi non funzionanti
Comprendono:
- adenomi funzionanti ma clinicamente silenti
- adenomi non secernenti
Costituiscono il 25% di tutte le neoplasie ipofisarie
Non hanno evidenza immunoistochimica n clinico-laboratoristica di produzione
ormonale.
Et: soprattutto individui adulti.
Sede: sellare o soprasellare
Clinica: segni compressivi a volte associati ad ipopituitarismo (effetto-massa)
In passato erano classificati come adenomi null a causa dellimpossibilit di
dimostrare la presenza di un marker di differenziazione.
In realt le caratteristiche ultrastrutturali e biochimiche della maggior parte degli
adenomi null permettono oggi la loro caratterizzazione come tumori gonadotropi
silenti.
I veri adenomi non secernenti sono rari.
Adenomi pluriormonali
I pi frequenti sono quelli con produzione mista di GH-PRL.
Sono neoplasie pi aggressive della media: si tratta di macroadenomi con propriet
invasive.
Ci si pu trovare di fronte a due tipi di situazioni:
- tumori in cui un medesimo tipo cellulare genera pi ormoni:
si tratta di tumori derivanti da progenitori pluripotenti e dunque ancora
in grado di produrre tutti i tipi ormonali, delle cellule delladenoipofisi.
Sono neoplasie da precursori degli elementi maturi
- tumori dati da una mescolanza di cellule che producono tipi ormonali differenti:
forma derivante da cellule mature.
Elementi citologici con diversa capacit funzionale.
266
La tiroide
Struttura normale
Ghiandola endocrina, del peso di 15-25 gr. formata da due lobi laterali uniti da un
istmo sottile. Frequentemente si ritrova anche un lobo piramidale al di sopra dellistmi
come residuo embriologico del dotto tireoglosso.
Derivazione embriologica: estroflessione dellabbozzo dellepitelio faringeo, che dal
forame cieco si porta in basso fino alla regione cervicale anteriore. Occasionalmente
possibile riscontrare tessuto tiroideo ectopico alla base della lingua (tiroide
sublinguale) o in altre sedi comunque nella parte alta del collo. Raramente questo
tessuto pu subire una trasformazione neoplastica e divenire sede di carcinoma
tiroideo primitivo.
Irrorazione: da parte delle arterie tiroidee superiori ( dalla carotide esterna) e delle
arterie tiroidee inferiori ( dalla succlavia).
Struttura: suddivisione per mezzo di sottili setti fibrosi in lobuli, ognuno composto da
20-40 follicoli. I follicoli sono rivestiti da epitelio cuboidale o colonnare e sono ripieni di
un materiale colloidale dato dalla tireoglobulina.
Meccanismo di funzionamento della secrezione tiroidea:
ipotalamo: produzione di TRH
ipofisi: produzione di TSH (tireotropina)
legame TSH-recettore a livello dellepitelio follicolare
incremento dei livelli intracellulari di cAMP nellepitelio follicolare
conversione tireoglobulina tiroxina (T4) e triiodotironina (T3) da parte delle cellule
dellepitelio follicolare
rilascio di T4 e T3 nel circolo sistemico (T4 prodotta in quantit molto maggiori), dove
questi peptidi si legano in modo reversibile alle proteine plasmatiche (globulina
legante la tiroxina e transtiretina)
Il legame alle proteine plasmatiche funzionale al mantenimento dei livelli di T3 e di
T4 liberi entro limiti precisi ed ad assicurare una loro rapida disponibilit a livello dei
tessuti.
Nei tessuti periferici si ha conversione della maggior parte di T4 libero in T3, che
rappresenta la forma attiva.
Legame T3recettori nucleari per gli ormoni tiroidei, con formazione di un complesso
multiproteico ormone-recettore.
Legame del complesso neoformato a specifici elementi di risposta allormone tiroideo,
nei geni bersaglio, con conseguente regolazione della trascrizione.
Complessivo aumento del metabolismo basale
267
Lormone tiroideo svolge anche un importantissima funzione nello sviluppo cerebrale.
Lormone TSH prodotto dallipofisi stimola anche lincremento di volume della
ghiandola tiroidea.
Il TSH, cos come il TRH sono per inibiti da meccanismi a feedback negativo mediati
dallincremento dei livelli di T3 e di T4 nel sangue.
Vengono perci chiamate gozzigeni una serie di composti che agiscono a livello della
tiroide determinando inibizione della sintesi di T3 e di T4, con conseguente aumento
dei livelli di TSH, non pi inibito a feedback e stimolazione abnorme della tiroide, con
iperplasia della ghiandola.
Ipertiroidismo
La tireotossicosi lo stato ipermetabolico che si viene a determinare in conseguenza
degli elevati livelli ematici delle frazioni libere di T3 e di T4.
La tireotossicosi pu essere dovuta a:
- Ipertiroidismo la grandissima parte delle tireotossicosi
- Tiroidite subacuta granulomatosa (dolorosa) per abnorme liberazione di ormoni
tiroidei preformati
- Tiroidite subacuta linfocitaria (indolore) per abnorme liberazione di ormoni
tiroidei preformati
- Ormoni tiroidei di origine extratiroidea (struma ovarico, tiretossicosi esogena, con
apporto esterno di tiroxina)
Dunque lipertiroidismo la causa primaria di tireotossicosi. Lipertiroidismo si
suddivide in:
- ipertiroidismo primario causato da alterazioni intrinseche della tiroide
- ipertiroidismo secondario causato da processi extra-tiroidei
Le patologie che comportano pi frequentemente ipertiroidismo e di conseguenza
anche tireotossicosi sono 3:
- iperplasia diffusa della tiroide o malattia di Graves- Basedow
- gozzo multinodulare iperfunzionante
- adenoma tiroideo iperfunzionante
Clinica
Le manifestazioni cliniche sono molteplici e sono dovute
1. allo stato ipermetabolico
2. alliperattivit del sistema nervoso simpatico.
Cute:
- aumento del metabolismo basale che comporta aumento del flusso ematico e della
vasodilatazione periferica; la cute e calda ed arrossata e frequentemente si ha
intolleranza al caldo.
Cuore:
- aumento del fabbisogno di ossigeno periferico ed aumento della contrattilit
cardiaca che comportano aumento della portata cardiaca
- tachicardia, palpitazioni e cardiomegalia di comune riscontro
- insufficienza cardiaca congestizia in particolare nei pz anziani, con cardiopatie
preesistenti
Sistema neuromuscolare:
268
- liperattivit del sistema nervoso simpatico determina la comparsa di tremori,
iperattivit, instabilit emotiva, ansia, inacpacit di concentrazione, insonnia.
- Frequentemente debolezza dei muscoli prossimali
- Frequentemente riduzione della massa muscolare
Alterazioni oculari
- iperstimolazione simpatica del muscolo elevatore della palpebra superiore che
comporta fissit dello sguardo e retrazione palpebrale.
- Esoftalmo vero e proprio come caratteristica esclusiva del morbo di Graves-
Basedow
Sistema gastrointestinale:
- aumento della motilit intestinale con conseguente malassorbimento e diarrea
Sistema scheletrico:
- stimolazione del riassorbimento osseo con aumento della porosit e diminuzione di
volume dellosso osteoporosi e maggior rischio di fratture
A livello sistemico
- perdita di peso nonostante laumento dellappetito
Crisi tireotossica:
brusca insorgenza di un grave ipertiroidismo, che si presenta in genere in pazienti con
malattia di Graves- Basedow in atto ed probabilmente causata da improvviso
aumento dei livelli di catecolamine, dovuto ad uno stress di qualsiasi genere. I pazienti
presentano febbre e tachicardia molto forte.
La crisi tireotossica viene a costituire unemergenza medica
Ipertiroidismo apatico:
ipertiroidismo che insorge in soggetti anziani, nei quali let avanzata ed i processi
metabolici concomitanti determinano attenuazione della sintomatologia.
Diagnosi
- Screening iniziale: determinazione dei livelli sierici di TSH che devono essere bassi
(elevata inibizione a feedback negativo)
- Test di conferma: determinazione del T4 e del T3 liberi. Solitamente il T4 ad
essere elevato ( normalemente presente in concentrazioni maggiori). In rari casi il
T4 normale o ridotto e si ha aumento dei livelli di T3.
Nei rari casi di ipertiroidismo secondario (dovuto ad alterazioni ipofisarie), i livelli di
TSH sono normali o aumentati.
- per determinare leziologia della tireotossicosi: determinazione della captazione
dello iodio radioattivo da parte della tiroide. Possono essere riscontrati:
aumento globale della captazione di iodio da parte dellintera ghiandola (morbo
di Graves-Basedow)
aumento della captazione in un singolo nodulo (adenoma)
ridotta captazione (tiroidite)
Ipotiroidismo
Stato ipometabolico da insufficienza della ghiandola tiroide, con conseguenti bassi
livelli ematici di T3 e di T4.
Anchesso pu essere:
- primario anomalia intrinseca tiroidea. A sua volta pu essere:
tireoprivo: dovuto ad assenza o perdita di tessuto tiroideo
269
associato a gozzo: dovuto alla mancata secrezione degli ormoni tiroidei, con
continuo stimolo da parte del TSH,e conseguente ingrandimento della tiroide
- secondario alterazioni ipofisarie
- terziario alterazioni ipotalamiche
-
Le cause dellipotiroidismo primario, che quello di gran lunga pi frequente sono le
seguenti:
1. apporto di iodio deficitario: non vi pu essere organificazione dello iodio cio legame
dello iodio ossidato ai residui di tireoglobulina, passaggio fondamentale per la
formazione degli ormoni tiroidei.
2. ablazione chirurgica o ablazione indotta da radioterapia del tessuto tiroideo
3. ipotiroidismo autoimmune: la causa principale di ipotiroidismo associato a gozzo
nelle regioni geografiche ad adeguato apporto di iodio. Nella maggior parte dei casi
dovuto a tiroidite di Hashimoto
4. farmaci, somministrati allo scopo di ridurre la secrezione tiroidea
5. difetti congeniti nel metabolismo tiroideo: sono una causa di ipotiroidismo non cos
diffusa. Possono coinvolgere uno qualsiasi dei passaggi della sintesi di ormoni
tiroidei
6. sindrome di resistenza agli ormoni tiroidei: molto rara e dovuta a mutazioni
ereditarie dei recettori leganti gli ormoni tiroidei, che conseguentemente non
possono esercitare la loro azione, pur essendo presenti in grandi quantit in circolo.
La medesima resistenza si ha anche a livello dellipofisi, con conseguente mancata
inibizione a feedback, cosicch anche i livelli di TSH tendono ad essere elevati.
Clinica
Le mannifestazioni cliniche dipendono dallet di insorgenza:
- durante lo sviluppo fetale e nella prima infanzia cretinismo
- nelle et successive mixedema
CRETINISMO
Ritardo nello sviluppo fisico e mentale, inapparente alla nascita, si manifesta nelle
prime settimane di vita o nei primi mesi.
Il cretinismo pu essere:
- endemico nelle aree con deficienza endemica di iodio. Era molto pi diffuso in
passato
- sporadico dovuto ad errori congeniti dello sviluppo della tiroide o della
biosintesi degli ormoni tiroidei
Le caratteristiche cliniche del cretinismo comprendono:
- cute rugosa e secca
- ampia distanza interoculare
- naso largo e piatto
- lingua grossa, protrudente
- bassa statura
- ernia ombelicale
- grave ritardo mentale
Tutto ci dovuto al ruolo determinante degli ormoni tiroidei nello sviluppo
scheletrico e del SNC.
MIXEDEMA
lipotiroidismo che insorge nei bambini di et superiore e nelladulto.
270
Nel bambino in particolare si hanno segni e sintomi intermedi tra cretinismo e
mixedema adulto
Nelladulto lesordio progressivo ed insidioso:
- progressivo rallentamento delle attivit psicofisiche, con diminuita resistenza alla
fatica, apatia, torpore mentale, intolleranza al freddo, calo dellattenzione
- la parola e le funzioni intellettuali divengono lente, si ha aumento del peso e
diminuzione della sudorazione.
- La cute appare fredda e pallida sempre pi inspessita e secca
- Con il passare del tempo si sviluppa edema periorbitale, e i lineamenti del volto si
appesantiscono, divenendo pi marcati con ingrossamento della lingua ed
abbassamento del tono della voce
- Mixedema del cuore il cuore appare flaccido ed ingrossato, con le camere
dilatate, a causa delledema interstiziale che provoca accumulo di liquido anche a
livello del sacco periorbitale.
Diagnosi
I livello di TSH risultano aumentati nellipertiroidismo primario per la perdita di
inibizione a feedback.
I livelli di T4 in ogni forma di ipotiroidismo vengono ad essere diminuiti.
Malattia di Graves-Basedow (iperplasia diffusa della tiroide)
la causa pi comune di ipertiroidismo endogeno
Incidenza massima fra i 20-40 anni con incidenza maggiore nelle donne rispetto agli
uomini.
Patogenesi
una malattia autoimmune nella quale possono essere presenti nel siero una grande
variet di anticorpi diretti contro componenti della tiroide. Di questi i pi importanti
sembrano essere gli autoanticorpi anti-recettore per il TSH.
Gli effetti di questi autoanticorpi sono differenti a seconda dellepitopo verso cui sono
rivolti:
- Thyroid stimulating immunoglobulin (TSI) IgG che si lega ai recettori del TSH
stimolandone lazione. specifico per la malattia di Graves-Basedow.
- Thyroid growth-stimulating immunoglobulin (TGI) dirette contro i recettori del
Tsh sembrano implicate soprattutto nella proliferazione dellepitelio follicolare
tiroideo.
- TSH-binding inhibitor immunoglobuline (TBII) impediscono il corretto legame
TSH-recettore sulle cellule epiteliali. Per fare questo alcune forma mimano lazione
del TSH stimolando la funzione tiroidea, mentre altre effettivamente la inibiscono.
Alla base della produzione di questi anticorpi vi probabilmente la perdita della
tolleranza da parte delle cellule Th nei cfr dei diversi componenti della tiroide, con
conseguente produzione di autoanticorpi anti-TSH.
Morfologia
Macroscopica:
- iperplasia diffusa delle cellule follicolari della tiroide
- capsula intatta
271
Microscopica:
- ipercellularit: cellule epieteliali follicolari ingrandite, alte e pi affollate del solito,
protrudono nel lume
- colloide pallida, per il diffuso riassorbimento della stessa
- infiltrati di linfociti (soprattutto cellule T) a livello interstiziale.
Clinica
La malattia di Graves- Basedow caratterizzata da una triade sintomatologica:
- ipertiroidismo con ingrossamento diffuso della tiroide
- oftalmopatia infiltrativa: caratterizzata oltre che dal classico sguardo fisso e
palpebre retratte (dovuto a iperreattivit del simpatico) anche da protusione del
bulbo oculare, dovuta ad una serie di cause:
notevole infiltrato infiammatorio in sede retro-orbitaria, da parte di cellule
mononucleate (linfociti T)
edema infiammatorio con conseguente tumefazione
accumulo di componenti della matrice extracellulare
aumento del numero di adipociti
- dermopatia infiltrativa o mixedema pretibiale: inspessimento del derma dovuto
alla deposizione di glicosaminoglicani e allinfiltrato linfocitario. presente solo in
una piccola percentuale di pz.
Diagnosi
Si riscontrano:
- elevati livelli di T4 e di T3 liberi, con diminuzione dei livelli di TSH
- aumento diffuso della capatazione di iodio radioattivo alla scintigrafia.
Gozzo diffuso e multinodulare
Per gozzo si intende laumento di volume delle tiroide che una delle manifestazioni
pi frequenti della patologia tiroidea, dovuto ad un inadeguata sinetsi romonale
tiroidea, che comporta aumento compensatorio dei livelli di TSH, causa a sua volta
delliperplasia e dellipertrofia delle cellule follicolari, con aumento volumetrico
dellorgano.
Solitamente laumento della massa contrasta da solo il deficit, portando ad uno stato
metabolico eutirorideo.
Se il difetto grave pu svilupparsi anche ipertiroidismo associato a gozzo
GOZZO DIFFUSO non TOSSICO
Si ha interessamento in modo diffuso di tutta la ghiandola, senza formazione di noduli.
Pu essere:
1. gozzo endemico si sviluppa nelle aree dove terreno, acqua ed alimenti,
presentano bassi livelli di iodio, con conseguente ridotta sintesi di ormoni tiroidei
ed aumento del TSH compensatorio. Le differenze nella prevalenza di gozzo in
regioni con uguale carenza iodica hanno portato allipotesi dellesistenza di altri
fattori causali, fra cui lutilizzo di particolari sostanze alimentari dette gozzigene.
2. Gozzo sporadico pi raro nel gozzo endemico, con prevalenza nel sesso femminile
e picco di incidenza alla pubert. Nella maggior parte dei casi il fattore causale non
noto
272
Morfologia
Nello sviluppo di un gozzo diffuso possono essere presenti due fasi:
1. fase iperplastica
- tiroide omogeneamente e diffusamente ingrandita sebbene laumento sia piuttosto
modesto
- i follicoli sono rivestiti da cellule colonnari disposte fittamente
2. fase di involuzione colloidale: avviene solo se successivamente si verifica un
aumento dellapporto di iodio o se diminuisce la richiesta di ormone tiroideo. Vede:
- involuzione dellepitelio follicolare
- la ghiandola rimane ingrandita e diviene ripiena di colloide
Clinica
Solitamente asintomatico ( metabolismo eutiroideo)
Talvola complicazioni dovute alleffetto massa.
GOZZO MULTINODULARE
Dovuto al ripetersi nel tempo di episodi di iperplasia ed involuzione del gozzo diffuso:
per questa sua caratteristica la prevalenza sempre maggiore nelle donne, ma
tender a colpire individui pi anziani.
un ingrossamento della tiroide maggiore, pi irregolare, pi spesso scambiato per
una forma neoplastica.
Patogenesi
Probabilmente insorge a causa di una diversa risposta agli stimoli ormonali ipofisari
da parte delle cellule follicolari.
Alcune cellule in un follicolo sviluppano un anomalia genetica (simile a quelle che
costituiscono levento scatenante gli adenomi della tiroide) che le porta ad avere una
maggiore crescita, con formazione di cloni di cellule a proliferazione spontanea e
dunque di un nodulo.
Dunque nel gozzo multinodulare possono coesistere noduli policlonali e monoclonali,
ma il gozzo deve probabilmente avere acquisito unalterazione genetica che lo
predispone alla crescita.
Iperplasia follicolare disomogenea + generazione di nuovi follicoli + accumulo
disomogeneo di colloide
Produzione di trazioni e stiramenti
Rottura dei follicoli e dei vasi
conseguente emorragia e cicatrizzazione, talvolta anche calcificazione
la cicatrizzazione e le calcificazioni aumentano le trazioni.
In questo ciclo viene favorita la comparsa di anomalie genetiche e la formazione di
nuovi noduli.
273
Morfologia
Macroscopica
- gozzi polilobulati, asimmetrici, enormemente ingranditi (peso fino a 2 kg.)
- lingrandimento del tutto imprevedibile ed un lobo pu essere ingrandito molto
pi di un altro
- si ha frequentemente compressione e dislocazione laterale delle strutture mediane
(trachea ed esofago)
- colloide bruna e gelatinosa presente in qunetit variabile nei noduli irregolari
- alterazioni regressive in partciolare nei noduli pi vecchi emorragie, fibrosi,
calcificazioni
Clinica
Da un punto di vista metabolico la maggior parte dei oz eutiroidea e solo una
minoranza dei pz pu sviluppare ipertiroidismo, dovuto alla presenza di noduli
iperfunzionanti in questo caso il gozzo viene detto tossico e la condizione clinica
detta sindrome di Plummer, e non accompagnata n da oftalmopatia n da
dermopatia.
Tiroiditi
Le tiroiditi sono un gruppo di affezioni accomunate dallinfiammazione che interessa
in modo variabile la ghiandola.
Possono essere:
- manifestazioni acute associate a notevole sintomatologia dolorosa
- manifestazioni subacute in cui linfiammazione presente, ma relativamente
ridotta e la malattia si manifesta principalmente con la compromissione delle
funzioni ghiandolari
TIROIDITE di HASHIMOTO
la causa pi comune di ipotiroidismo in zone con adeguato apporto di iodio.
la causa principale di gozzo non endemico nei bambini
una malattia autoimmune e tra di esse stata le prima ad essere riconosciuta e
descritta e per questo ne costituisce il prototipo.
Insorge prevalentemente tra i 45 ed i 65 anni e colpisce con frequenza >> il sesso
femminile.
Come in tutte le malattie autoimmuni anche nella tiroidite di hashimoto vi una
notevole componente genetica nella patogenesi, anche se non si tratta di
unereditariet di tipo mendeliano, poich consiste nella sottile alterazione nelle
funzioni di molti geni.
Tuttavia alcuni ipotizzano unereditariet autosomica dominante.
Patogenesi
Il sistema immunitario reagisce contro antigeni tiroidei, probabilmente a causa di un
difetto dei linfociti T soppressori tiroide-specifici, con conseguente sopravvivenza e
dunque predominanza di linfociti T CD4+ specifici per Ag tiroidei, che coopererebbero
con i linfociti B alla produzione di anticorpi.
- anticorpi contro le perossidasi tiroidee (Ac anti-microsomiali)
- anticorpi per la tireoglobulina
- anticorpi per il recettore del TSH
I meccanismi che provocano morte dei tireociti sono i sgeuenti:
274
1. morte cellulare mediata da linfociti T CD8+
2. morte cellulare citochino mediata linfociti T che producono citochine che
mediano attivazione dei macrofagi con conseguente danno dei follicoli
3. legame degli anticorpi antitiroide seguito da citotossicit cellulo-mediata anticorpo
dipendente
Morfologia
Macroscopica:
- tiroide diffusamente aumentata di volume
- capsula integra
Microscopica:
- infiltrato infiammatorio mononucleato che interessa diffusamente il parenchima,
formato da linfociti, da plasmacellule e da centri germinativi
- follicoli atrofici con perdita progressiva delle cellule epiteliali follicolari,
gradualmente sostituite da infiltrato infiammatorio e dunque da fibrosi
- a volte i follicoli appaiono rivestiti da cellule epiteliali alterate dette cellule di
Hurthle, che rappresentano una trasformazione metaplastica del normale epitelio
follicolare cuboidale
Clinica
Tumefazione non dolente e diffusa della ghiandola associata ad un certo grado di
ipotiroidismo, che si sviluppa gradualmente. In una piccola parte dei casi
lipotiroidismo preceduto da una tireotossicosi transitoria, causata da distruzione dei
follicoli tiroidei, con rilascio ormonale massivo ( hashitossicosi).
Quando compare lipotiroidismo caratteristicamente alla diagnosi i pz presentano un
diminuito livello di T3 e di T4, accompagnato da incremento di TSH.
Come le altre malattie autoimmuni anche in questo caso i pz affetti hanno un
maggiore rischio di sviluppare altre malattie autoimmuni, come il lupus, il diabete di
tipo 1, la malattia di Graves.
Tiroidite subacuta (granulomatosa)
Ha incidenza molto minore della tiroidite di hashimoto, pur colpendo sempre
preferenzialmente il sesso femminile
Patogenesi
Probabilmente in seguito a infezione virale o processo infiammatorio post-virale in
grado di produrre, in seguito al danno tissuatale, lesposizione di epitopi antigenici,
prima nascosti, di origine tiroidea.
Questo stimolerebbe in partciolare modo i linfociti TCD8+, responsabili del danno alle
cellule follicolari.
Il processo autolimitante perch la risposta immunitaria indotta dal virus non si
automantiene.
Morfologia
Macroscopica
- lieve aumento di volume
- capsula normale
- a volte lieve aderenza con le strutture circostanti
275
Microscopica:
- fase iniziale infiammazione attiva che comporta distruzione focale dei follicoli
con ampio infiltrato neutrofilo a formare microascessi
- fase successiva alterazioni pi specifiche:
aggregati di linfociti, istiociti e plasmacellule intorno ai follicoli danneggiati
presenza di cellule giganti multinucleate (tiroidite granulomatosa)
- fasi avanzate: sostituzione con fibrosi riparativa
Clinica
- dolore in sede cerivicale che irradia a collo, mandibola, gola, orecchie
- ingrandimento variabile della tiroide
- sintomi di accompagnamento: febbre, affaticabilit, malessere, mialgie
- ad una fase iniziale di ipertiroidismo ( follicoli danneggiati che riversano il loro
contenuto allesterno), segue una fase successiva di ipotiroidismo, ma anche questo
transitorio e di solito va incontro a completa guarigione.
Tiroidite subacuta linfocitaria (indolore)
poco frequente, e si manifesta in adulti di mezza et, con prevalenza nelle donne,
soprattutto nel postpartum.
La patogenesi sconosciuta, ma forse si tratta di un meccansimo autoimmune.
La tiroide lievemente ingrossata, con infiltrati di linfociti nel parenchima,
distruzione del parenchima e follicoli tiroidei collassati.
Non ci sono fibrosi n metaplasia
Tipicamente la patologia si manifesta con ipertiroidismo, ed i suoi sintomi tipici, ma
alcuni pz non presentano sintomatologia.
Si hanno elevati livelli di T3 e T4 e bassi livelli di TSH.
276
Neoplasie della corticale del surrene
Nellambito dei tumori della corticale possiamo vedere:
1. neoplasie non funzionanti: generalmente di tratta di carcinomi.
2. neoplasie funzionanti: producono una serie di sindromi:
sindrome da iperaldosteroidismo:
causato quasi sempre da adenoma aldosterone-secernente
colpisce prevalentemente individui di mezza et, specialmente
donne
provoca ritenzione di sodio ipertensione
provoca perdita di potassio ipokaliemia
sindrome di Cushing (iperproduzione di cortisolo)
generalmente provocata da adenoma
Inizialmente ipertensione ed aumento ponderale.
Con il tempo: distribuzione centrale del tessuto adiposo obesit
del tronco, facies lunare, accumulo di tessuto adiposo sulla nuca e
sul dorso (gibbo di bufalo).
Atrofia selettiva delle fibre muscolari rapide debolezza
muscolare, riduzione della massa muscolare.
Induzione della gluconeogenesi, inibizone della captazione
cellulare di glucosio glicemia, glicosuria, diabete secondario.
Aumento del catabolismo proteico, perdita del collagene,
riassorbimento del tessuto osseo cute sottile, fragile, tendenza
allecchimosi, cicatrizzazione lenta, osteoporosi.
Soppressione della risposta immunitaria aumento della
suscettibilit alle infezioni.
Disturbi mentali
Irsutismo
sindrome adreno-genitale:
la corteccia del surrene normalmente esprime de-idro-epi-
androsterone ed androstenedione; questi precursori richiedono la
conversione periferica in androsterone.
Generalmente si tratta di una sindrome associata a carcinomi
surrenalici ad eccessiva androgeno-secrezione.
Comporta solitamente virilizzazione.
Adenoma (incidentaloma)
cos chiamato perch si tratta di un tumore di reperto molto spesso incidentale: si
tratta spesso di un riscontro casuale nel corso di indagini strumentali svolte per altra
causa o in corso di autopsia.
Generalmente il diametro minore di 5cm. ed il peso minore di 50 grammi.
Nonostante le piccole dimensioni si tratta di una neoplasia benigna che espande la
ghiandola surrenale.
un tumore molto ben delimitato, con capsula evidente.
Lascia la corticale con uno spessore normale (non atrofica).
277
Alla sezione presenta una superficie liscia e compatta, colore giallo-zolfo, per la
presenza di lipidi nelle cellule neoplastiche, non interessata da necrosi o emorragie.
Istologia
Allesame istologico si rivela assolutamente benigno.
Infatti le cellule neoplastiche rimangono differenziate e simili a quelle del normale
surrene, riproducendo le caratteristiche della midollare, della fascicolata o di
entrambe.
I nuclei delle cellule tendono ad essere piuttosto piccoli, sebbene a volte vi sia un certo
polimorfismo, con attivit mitotica scarsa.
Diagnosi differenziale
Gli adenomi devono essere assolutamente distinti dai carcinomi.
Questa distinzione non pu essere fatta solo sulla base del peso e delle dimensioni, che
rimangono solo fattori indicativi.
Lipotesi diagnostica al microscopio va invece valicata con esami obiettivi, cio
mediante tecniche di immunoistochimica (vedi fenotipo).
Fenotipo
Dal punto di vista immunoistochimico gli adenomi presentano:
- forte positivit per citocheratine a basso peso molecolare (le citocheratine sono
filamenti intermedi che entrano a fare parte del citoscheletro;sono classificate
sulla base del loro peso molecolare).
- Debole espressione di vimentina (si tratta anche in questo caso di filamenti
intermedi).
- Negativit per EMA.
- Negativit per gli isoantigeni del gruppo sanguigno Lewis.
- Positivit per gli ormoni steroidei.
Genotipo
Lanalisi del DNA rileva alterazioni della ploidia solo in un 20% dei casi.
Carcinoma
Non ci sono predilezioni di sesso, ma let media di insorgenza 50 anni.
Si tratta di un tumore funzionante dunque con produzione di ormoni nel 50% dei casi:
in questi casi associato ad iper-cortico-surrenalismo.
Le dimensioni sono molto maggiori della sua variante benigna e superano spesso i 20
cm. con peso maggiore di 100g.
La loro grandezza fa s che la struttura normale della ghiandola surrenalica non sia
pi distinguibile.
278
Al momento della diagnosi il 50% dei pz presenta gi metastasi.
Si tratta dunque di un tumore molto aggressivo, con tendenza alla diffusione per via
ematica (tumore angio-invasivo) e dunque successivo interessamento secondario di
fegato (60%), linfonodi, polmoni, ossa o cute.
Alla sezione presenta una superficie mal definita, non compatta che contiene:
- aree necrotiche, dovute alla nutrizione insufficiente rispetto alle necessit del
tumore; la velocit della neoangiogenesi inferiore alla velocit di crescita del
tumore;
- emorragie perch la struttura dei vasi neoformati spesso fragile e sottoposta a
notevoli pressioni meccaniche (crescita del tumore) e dovute allinvasione
neoplastica dei vasi principali (vena cava inferiore e vena surrenalica).
- molteplici noduli friabili e soffici.
Istologia
Il tumore pu essere costituito da cellule ben differenziate simili a quelle
delladenoma (problemi di diagnosi differenziale con ladenoma medesimo), cos come
da cellule con elevata atipia, giganti come quelle di un carcinoma che ha
metastatizzato secondariamente nel surrene, o fusate, o con moderato grado di
anaplasia.
Fenotipo
- negativit per citocheratine a basso peso molecolare
- positivit per vicentina
- negativit per EMA
- ci pu essere produzione di ormoni steroidei ma molto pi scarsa di quella
delladenoma.
Genotipo
Lanalisi del DNA rileva alterazioni della ploidia in un 70% dei casi.
Solitamente si ha perdita di omozigosi per p53 e per Rb.
Recentemente si osservata spesso anche una sovraespressione di TRF-1, molecola
che ha attinenza con lo sviluppo dei telomeri.
279
Neoplasie della midollare del surrene
Generalit
La midollare del surrene composta da:
a. cellule cromaffini: cellule specializzate della cresta neurale a funzione
neuroendocrina.
b. cellule sustentacolari: cellule di sostegno.
Le cellule cromaffini presentano numerosi granuli citoplasmatici di deposito delle
catecolamine.
Sintetizzano e secernono catecolamine (adrenalina e noradrenalina)
in risposta a segnali trasmessi da fibre pregangliari del sistema nervoso simpatico.
- noradrenalina: funziona come neurotrasmettitore dei neuroni simpatico post-
gangliari. Raggiunge la circolazione in quota molto ridotta.
- Adrenalina: funziona principalmente come ormone dunque secreta in gran
parte nella circolazione.
La secrezione di queste molecole nella circolazione facilitata dalla ricca
vascolarizzazione dello stroma che circonda le cellule cromaffini.
La funzione della midollare del surrene dunque quella di essere la principale fonte di
catecolamine, configurandosi cos come un importante punto di regolazione di molte
funzioni vitali.
Cellule neuroendocrine del tutto simili alle cellule cromaffini sono ampiamente
distribuite in un sistema extra-surrenalico composto da gruppi di cellule e noduli.
Queste, con la midollare fanno parte del sistema paragangliare.
Questi paragangli extra-surrenalici, strettamente connessi con il sistema nervoso
autonomo sono distinti in tre gruppi, in base alla loro sede anatomica.
1. brachiomerico vicino alle arterie maggiori ed ai nervi cranici della testa e del
collo ( soprattutto glomi carotidei).
2. intravagali distribuiti lungo il nervo vago.
3. aorticosimpatico soprattutto lungo laorta addominale e in posizione
retroperitoneale.
Neuroblastoma
E una patologia tipica dellet pediatrica visto che si manifesta entro i 4 anni di et e
fa parte delle cos dette Small Blue Cell Tumor.
Questo un gruppo di tumori tipici dellinfanzia, accomunati da una derivazione di
tipo blastico, dunque con cellule di aspetto primitivo: nuclei piccoli e rotondi,
intensamente basofili, che occupano quasi interamente la cellula (simil-linfociti)
E il secondo tumore solido maligno per frequenza nellinfanzia dopo quello cerebrale e
rappresenta 7-10% di tutte le neoplasie pediatriche.
280
Nei lattanti la prognosi migliore rispetto agli adulti.
Si nota una possibile familiarit visto che si associa spesso a sindromi geneticamente
trasmissibili.
Circa il 30% di questi tumori origina nella midollare del surrene.
I rimanenti compaiono nel sistema paragangliare aorticosimpatico:il 70% di questi
tumori ha localizzazione retroperitoneale. Pu accadere che abbia collocazione
mediastinica anche un altro tumore a piccole cellule rotonde blu; si tratta di un
linfoma a cellule T che rappresenta una grande causa di morte infantile.
E una neoplasia che metastatizza facilmente:
o Fegato: Sindrome di Pepper
o Cranio: Sindrome di Hutchinson
o Scheletro: Sindrome di Isser-Leury (Issernoidi?)
o Linfonodi
o Ovaio
Morfologia
Sono tumori molto grandi che crescono rapidamente, si presentano come grosse masse di
tessuto grigio-bruno cerebroide con estese zone di necrosi, emorragie, rammollimento,
con occasionali focolai di calcificazioni puntiformi.
Possono essere circoscritti da una capsula fibrosa o essere pi infiltrativi invadendo le
strutture circostanti come vena renale, vena cava, aorta, rene
Le cellule presentano contorni poco nitidi, volume ridotto, caratteristiche linfocito-
simili (nucleo>>citoplasma) e crescita in tipiche lamine solide, dunque mantengono le
caratteristiche di organogenesi della sede della neoplasia.
Tipica la presenza delle Rosette di Homer-Wright: le cell neoplastiche differenziano
in senso neuritico e si organizzano attorno a del materiale amorfo formato dai neuriti
stessi delle cell (neuropili) embricati tra loro.
Il 90% di questi tumori produce uningente quantit di catecolamine che servono per la
diagnosi insieme ai loro metabolici (VMA e HVA) nelle urine.
Fenotipo
- Neurofilamenti (filamenti intermedi degli elementi neuroendocrini)
- Sinaptofisina
- Enolasi neurono-specifiche
- Cromogranina
- VIP
- positivit ad antigeni neurali associati
Clinica
Dunque in tutti i pz con diagnosi di neuroblastoma necessario compiere una biopsia
ostiomidollare di routine per verificare se c iniziale interessamento scheletrico.
281
Molto spesso questo tumore si accompagna a pancitopenia: anemia + piastrinopenia +
leucopenia.
In alcuni casi si accompagna anche a una violenta diarrea molto liquida dovuta al
rilascio massivo di VIP.
Prognosi
Vi un 30% di sopravvivenza entro i tre anni.
Positiva se:
Quasi triploidia
Diagnosi sotto i 2 anni
Presenza Cell di Schwann
Presenza di infiltrato linfoide NK come segno di reazione alla malattia
Presenza in sede extrasurrenalica
Diagnosi in stadi avanzati della malattia
Espressione di Trk-A (recettore per il fattore di crescita neuronale)
Negativa se:
Quasi tetraploidia
Et maggiore dei 2-5 anni
Vi sono bassi VMA/HVA
Amplificazione di N-myc
Espressione di Bcl-2
Espressione della proteina P: in particolare lespressione della proteina P170
conferisce una multidrug resistance.
Patologie affini
Vi sono delle patologie strettamente apparentate con il neuroblastoma ma che
presentano solitamente una prognosi migliore.
Questa maggiore positivit dellesito dovuta alla presenza di cell pi mature con
aumentato volume e aumentato citoplasma riconducibili alle cell gangliari.
Inoltre si riscontra spesso la comparsa di cell di Schwann in questi frangenti , come
detto in precedenza, comportano un miglioramento della prognosi.
Ganglioneuroblastoma
- Presenta una differenziazione in senso gangliare (grandi cellule, citoplasma pi
abbondante, grandi nuclei vescicolosi e prominente nucleolo)
- Si presenta in sede mediastinica o retroperitoneale.
- La malattia va in contro a maturazione in terapia.
Ganglioneuroma
- Si presenta sempre in sede extraperitoneale.
- Presenta cell gangliari mature senza residui simpatoblastici.
282
- E una forma benigna che pu evolvere in una forma sclerotica.
- Necessario valutare tutto il tumore per evidenziare eventuali zone immature
riconducibili al neuroblastoma.
- Pu andare in contro a resezione sclerotica.
Feocromocitoma
Si tratta di un tumore raro, costituito da cellule cromaffini che sintetizzano e
rilasciano catecolamine ed in alcuni casi ormoni peptidici.
E chiamato tumore del 10% perch nel 10% dei casi
E extrasurrenalico
Insorge in et pediatrica (tipico dellet adulta)
E maligno
E extra-surrenalico, sviluppandosi lungo il tragitto dellaorta, dove questo
tumore assume il nome di paraganglioma della midollare del surrene
E in associazione con una sindrome familiare: entra spesso nellambito delle
neoplasie endocrine multiple: MEN2A in cui associato con il carcinoma.della
tiroide e MEN2B in cui associato con la neurofibromatosi.
Dei feocromocitomi surrenalici non familiari bilaterale: questa percentuale
pu raggiungere il 70% nei casi familiari
Morfologia
Le dimensioni vanno da un piccolo tumore circoscritto confinato al surrene ( peso
minimo 1g.), a grandi masse che possono pesare fino a 4kg.
Normalmente si presenta come una massa di grosse dimensioni formata da aggregati
solidi, tralci fibrosi,vasi ed ben delimitata da connettivo o dalla corticale o midollare
medesima compresse.
Nel complesso si pu definire come una struttura organoide: le cellule neoplastiche
cromaffini sono raggruppate a formare piccoli nidi o alveoli ( nidi di zellballen),
circondati da una rete trasecolare fibrosa, riccamente vascolarizzata, che produce una
struttura globulare.
La ricca vascolarizzazione e lo stretto contatto fra aggregati cellulari e vasi fa s che le
catecolamine vengano liberate facilmente nel sangue.
In sezione la superficie dei feocromocitomi appare giallo-bruna, nelle lesioni
voluminose anche interessata da aree di necrosi, di emorragia, o cistiche che fanno
tendenzialmente scomparire il parenchima della ghiandola surrenale.
Se si espone la superficie di sezione,a fresco, al reattivo di Zenker (bicromato di
potassio), si ha viraggio del colore veso il bruno, per ossidazione delle catecolamine ( da
qui il nome delle cellule cromaffini): questo rappresenta un prova efficace della
presenza di granuli di catecolamine.
283
Fenotipo
- Enolasi
- Catecolamine
- Neurofilamenti
- Cromogranina
- Sinaptofisina
Clinica
La caratteristica clinica dominante lipertensione: improvviso aumento della
pressione arteriosa, associato a tachicardia, palpitazioni, sudorazione, mal di testa,
tremori, a volte dolore addominale o toracico, nausea, vomito.
In meno della met dei pz esso produce veri e propri picchi, accessi ipertensivi
intermittenti, scatenate anche da situazioni incidentali (stress emotivi, esercizi fisici,
farmaci, interventi chirurgici, variazioni della postura, palpazione del tumore,
pasti.).
Producendo ingenti quantit di ormoni vasoattivi (catecolamine attive al contrario del
neuroblastoma) pu causare una accesso ipertensivo che pu portare a morte.
Questa produzione pu essere influenzata da farmaci, gravidanza o intervento
chirurgico: se durante unoperazione il chirurgo va a ledere involontariamente la
massa tumorale pu avvenire un rilascio massivo di catecolamine che porta a
decesso il paziente.
Nei rimanenti casi lo stato di ipertensione continuo.
In entrambi i casi comunque lo stato di ipertensione provocato dallimprovviso
rilascio di catecolamine, che pu determinare anche scompenso cardiaco, edema
polmonare, infarto acuto del miocardio.
In alcuni, molto rari casi, i feocromocitomi secernono altri ormoni, come ACTH e
somatostatina, e dunque provocano manifestazioni cliniche differenti.
Prognosi
Non si pu prevedere se la malattia benigna o maligna, lindice di malignit dato
dallinfiltrazione delle cell neoplastiche nei vasi che portano a metastasi e alla rapida
diffusione sistemica delle catecolamine.
Le metastasi hanno uno spiccato tropismo per lo scheletro, in questo caso la prognosi
infausta.
Nel 10% dei casi con potenziale metastatico il tumore porta a morte in un anno.
Paragangliomi
Neoplasie del tutto analoghe al feocromocitoma che si sviluppano nei gangli simpatici
e parasimpatici ( sede carotidea, mediastinica, giugulo temporale)
284
Neoplasie endocrine multiple
MEN2A: paraganglioma + carcinoma midollare della tiroide
una patologia altamente aggressiva e rapidamente letale.
285
Tumori neuroendocrini
Generalmente si parla di tumori neuroendocrini riferendosi al tratto gastrointestinale,
ma in realt ci si potrebbe riferire ad ogni organo per la presenza di un sistema
neuroendocrino diffuso.
Il concetto di sistema neuroendocrino diffuso stato rivisto e modificato negli anni.
Fu definito per la prima volta circa 60 anni fa, come sistema formato da cellule in
grado di captare amine e decarbossilarle, sistema APUD (Amine Precursor Uptake
and Decarboxilation).
Da ci i tumori derivanti da queste cellule furono chiamati apudomi.
Successivamente venne dimostrato che non tutte le cellule del gruppo esibivano questa
funzione e dunque il termine caduto in disuso. Attualmente le cellule appartenenti a
questo sistema sono definite in base alle seguenti caratteristiche:
cellule capaci di produrre amine o peptidi ad azione ormonale o
neurotrasmettitrice
cellule che possiedono vescicole simili alle vescicole sinaptiche o ai granuli
neurosecretori
i loro prodotti di secrezione vengono liberati per esocitosi regolata in risposta a
stimoli esterni
Il gruppo di cellule neuroendocrine include:
- sistema neuroroendocrino gastrointestinale: il pi rilevante ed importante, formato
da molti tipi di cellule che si trovano disperse nella mucosa dellapparato
gastrointestinale e del pancreas. Le cellule secernono ormoni che costituiscono un
sistema bilanciato di antagonisti ed agonisti in grado di regolare e coordinare gran
parte dellattivit gastrointestinale. Alcune di queste sostanze hanno azione
endocrina, altre paracrina, altre agiscono come neurotrasmettitori del SNC.
- Sistema endocrino respiratorio: nel tratto inferiore dellalbero bronchiale si trovano
cellule endocrine diffuse secernenti amine e peptidi, probabilmente implicati nella
regolazione locale ed in quella basata sul sistema nervoso autonomo delle funzioni
respiratorie.
- Sistema neuroendocrino diffuso urogenitale
- Cellule formanti parti distinte di ghiandole endocrine: midollare del surrene,
cellule C della tiroide, insule pancreatiche, cellule che producono ACTH e MSH
dellipofisi
- Cellule secernenti renina dellapparato iuxta-glomerulare
- Chemocettori del corpo carotideo
- ..
Il sistema neuroendocrino diffuso quindi un insieme di elementi cellulari endocrini,
che hanno la medesima origine embriogenetica degli organi di cui fanno parte. Sono
praticamente posizionati in ogni organo e tessuto.
Una volta questi tumori erano definiti carcinoidi, per evidenziare un tipo di neoplasia
simile al carcinoma, ma con decorso clinico pi blando.
286
Ora questo termine in disuso e recentemente stata introdotta una nuova
classificazione dei tumori neuroendocrini, da parte di un professore delluniversit di
Pavia, che molto pi dinamica, e differenzia i tumori in:
1. tumori endocrini ben differenziati
a. comportamento benigno
b. indefiniti a comportamento benigno o potenzialmente maligno (border line)
2. carcinomi endocrini ben differenziati ( basso grado di malignit)
3. carcinomi endocrini scarsamente differenziati (alto grado di malignit)
Questa classificazione si basa sulla valutazione di una serie di criteri diagnostici
allesame del tumore:
- caratteristiche biologiche del tumore
sede
volume
metastasi
angioinvasione
- caratteristiche funzionali del tumore
secernente e funzionante sono le forme di cui pi facile fare diagnosi perch
in base al tipo di secrezione ormonale si pu avere presenza di sindromi associate
(insulinoma, gastrinoma)
secernente e non funzionante la neoplasia produce sostanze che non hanno
funzionalit o non hanno emivita sufficiente, dunque non danno simntomatologia
neuroendocrina
non secerenente e non funzionante il comportamento di questi tumori di solito
quello che presenta il decorso pi aggressivo
- sede del tumore
Questi criteri diagnostici in pratica permettono una differenziazione tra neoplasie
benigne e maligne.
Le principali differenze tra neoplasie benigne e maligne allesame istologico sono le
seguenti:
Neoplasia benigna Neoplasia maligna
Struttura organoide: tendenza alla
formazione di strutture pseudoghiandolari
o pseudotubulari, simili a quelle
dellorgano di appartenenza
Struttura solida
Citologia tipica della cellula endocrina ; la
struttura della cellula assomiglia a quella
della cellula dorigine, i nuclei sono
omogenei e simili a quelli della cellula
dorigine, dunque presentano:
- cromatina granulare sale e pepe
- abbondante citoplasma molto
eosinofilo: grande attivit sintetica
Citologia atipica: la struttura della cellula
non assomiglia pi a quella della cellula
dorigine, ma a quella della stem-cell.
Tutti i tumori in fase finale sono molto
simili.
287
Attivit proliferativa scarsa Attivit proliferativa marcata
Necrosi assente o focale Necrosi estesa perch la proliferazione
supera le capacit di neo-angiogenesi.
p53 assente: non vi sono n mutazioni, n
accumuli della p53.
La proteina p53 wild type ha emivita
molto breve (4-5h) e dunque non
visualizzabile con limmunoistochimica.
La presenza di p53 dunque rispecchia
sicuramente una mutazione della stessa
che pu essere:
- pre trascrizionale
- post-trascrizionale: legame di
polimeri e stabilizzazione
P53 spesso presente
Da un punto di vista di marcatori molecolari del tumore abbiamo:
Neoplasia benigna Neoplasia maligna
Cromogranina A ++
dosabile nel sangue
Cromogranina A
la cromogranina tende a scomparire
nelle forme indifferenziate
NSE (neuro specific enolase) enolasi
neurono specifica ++
dosabile nel sangue
NSE ++
Sinaptofisina ++ Sinaptofisina ++
Con lindagine al microscopio ottico dopo colorazione con ematossilina/eosina si pu
fare solo diagnosi di tumore neurosendocrino e si pu dire se esso poco o ben
differenziato, la presenza di attivit mitotica o la presenza di aree necrotiche.
Dunque diviene necessario eseguire lindagine immunoistochimica. Questa ci serve
anche per valutare in modo pi preciso la proliferazione cellulare di cui marcatore la
proteina Ki67, una proteina nucleare presente in tutte le fasi del ciclo cellulare eccetto
la G0; nel carcinoma mammario la ricerca di questa proteina necessaria e sufficiente
a definire limpostazione della terapia
Il trattamento della neoplasia ben differenziata (tumore o carcinoma) di solito prevede:
- escissione chirurgica sempre, operata anche al fine di analizzare la neoplasia
(qui non possibile fare una microbiopsia per valutare lintera neoplasia con
precisione)
- trattamento farmacologico con somatostatina ed IFN
Il trattamento della neoplasia scarsamente differenziata del tutto diverso e prevede:
- escissione chirurgica soli in casi radicali ( solitamente la chirurgia inutile)
- trattamento chemioterapico e radioterapico aggressivo associato
I tumori neuroendocrini che interessano il tratto gastrointestinale colpiscono in
prevalenza:
- appendice sede di insorgenza pi comune
288
- intestino tenue (ileo soprattutto e frequentemente ampolla del Vater)
- retto
- stomaco
- colon
I tumori neuroendocrini a partenza dallappendice e dal retto raramente
metastatizzano, persino nei casi con diffusa estensione locale.
Al contrario il 90% dei tumori neuroendocrini dellileo, dello stomaco e del colon che
abbiano gi infiltrato per met la tonaca muscolare, ha gi coinvolto linfonodi
regionali e sedi distanti con un particolare tropismo per il fegato.
MORFOLOGIA
Macroscopica
Nellappendice insorgono frequentemente tumori dellapice, spesso obliteranti il lume.
Nelle altre porzioni dellintestino formano masse sottomucose o intramurali che creano
piccole rilevatezze generalmente di diametro inferiore ai 3 cm.
La mucosa sovrastante pu essere integra o ulcerata, mentre sul versante opposto pu
infiltrare la parete intestinale fino ad invadere il mesentere.
Questi tumori sono estremamente duri, e quando coinvolgono il mesentere possono
provocare in esso lesioni sclerosanti, dando luogo ad angolazioni o strozzature
sufficienti a causare occlusioni intestinali.
Microscopica
Le cellule neoplastiche possono formare isole, trabecole, ghiandole, oppure disporsi
diffusamente a tappeto. Solitamente e soprattutto nei casi benigni le cellule tumorali
sono monomorfe, con citoplasma scarso, intensamente eosinofilo e nucleo rotondo ed
ovoidale con fini granuli di cromatina (aspetto sale e pepe)
Nella maggior parte dei casi nel citoplasma si osservano granuli secretori con centro
denso.
CLINICA
I tumori neuroendocrini dellapparato gastrointestinale possono
- essere asintomatici
- provocare sintomi locali (molto raro) dovuti ad angolazione ed occlusione del
tenue
- produrre sindromi ed endocrinopatie se funzionanti in funzione del prodotto
secreto.
- Provocare una classica sindrome detta sindrome da carcinoide si presenta
nell!% dei casi e sembra che molte delle manifestazioni di questa sindrome
dipendano da un eccesso di serotonina nel sangue. Solitamente la serotonina
degradata dal fegato, che la trasforma in un prodotto inattivo. Di conseguenza si ha
di solito questa sindrome nel momento in cui vi siano metastasi epatiche (la
serotonina raggiunge il circolo sistemico sfuggendo alla degradazione epatica) o in
caso di tumori neuroendocrini extra-intestinali (le sostanze prodotte da questi
tumori sono rilasciate direttamente in circolo).
CASO CLINICO I
Il paziente allecografia presenta una massa nel fegato.
289
Bisogna stabilire se il paziente cirrotico, nel qual caso potrebbe trattarsi pi
facilmente di un epatocarcinoma primitivo del fegato, oppure non lo , nel qual caso
aumentano le probabilit di metastasi.
Se possibile dunque si fa biopsia epatica.
Alla biopsia epatica si riscontra un quadro citologico compatibile con quello di un
tumore endocrino ben differenziato.
Questo significa al 99% dei casi che si tratta di metastasi di un tumore neuroendocrino
a locazzazione primitiva intestinale.
Per fare diagnosi definitiva tuttavia vado a ricercare marcatori specifici del tumore nel
siero, dunque ricerco cromogranina A e NSE.
Il tumore primitivo si localizza nel tratto gastrointestinale e risulta negativo per
insulina, gastrina, glucagone, somatostatina e calcitonina. Dunque si tratta di un
tumore non secernente e non funzionante.
tumore endocrino ben differenziato probabile metastasi epatica di un carcinoma
primario occulto.
CASO CLINICO II
Il sistema neuroendocrino deriva da cellule progenitrice che sono in grado di
differenziarsi in senso endocrino cos come in senso epiteliale: dunque il tumore
divenendo indifferenziato pu dare luogo a cellule progenitrici che possono
differenziarsi anche in senso epiteliale.
Nello stomaco le cellule neuroendocrine si ritrovano alla base delle cripte, fra cellule
epiteliali e mbr basale.
I tumori neuroendocrini ben differenziati dello stomaco possono essere:
- del tutto benigni:
con diametro < 1cm
non angioinvasivi
si presentano come piccole rilevatezze della sottomucosa, delle dimensioni della
capocchia di uno spillo
sono multifocali
- border line
con diametro > 1 cm.
Possono essere angioinvasivi
Possono essere benigni ma anche potenzialmente maligni.
Nel nostro caso si ha un maschio di 60 anni, che allesofago-gastro-duodenoscopia
presenta:
- mucosa gastrica marezzata
- lesioni polipoidi nel corpo
Viene fatta una biopsia delle rilevatezze nodulari (polipi) e si vede un quadro istologico
che mostra la proliferazione di elementi cellulari omogenei con nuclei monomorfi e
dallaspetto di cellule di origine endocrina.
Il campione bioptico viene dunque analizzato con tecniche immunoistochimiche
attraverso lutilizzo di Ac anti-cromogranina A e si vede una grossa positivit, una
iperreattivit.
290
Si tratta dunque di un tumore ben differenziato dello stomaco, a cellule ECL
enterocromaffini, che molto spesso si inserisce nel contesto di una gastrite cronica
atrofica del corpo (non fa pensare ad H. Pylori) e dunque di una ipergastrinemia.
CASO CLINICO III e IV
Si analizza lampolla del Vater.
Il tumore pi frequente in questo sito ladenocarcinoma che insorge sul polipo
duodenale, a causa della mataplasia carcinomatosa displastica.
Uno dei primi sintomi precoci della patologia dellampolla di Vater littero ostruttivo,
che per causato anche da altri tipi di patologie e da altri tipi di tumori come il
tumore che colpisce la testa del pancreas.
Nel nostro caso si ha una femmina di 60 anni, che presenta una sintomatologia con
dolore epigastrico associata ad un quadro precedente di neurofibromatosi di tipo1
(patologia gentica caratterizzata dalla formazione di neurofibromi, gliomi del nervo
ottico, noduli pigmentati delliride, macule cutanee iperpigmantate malattia
dellelephant man).
Alla colangiografia vediamo ostruzione delle vie rettali.
Possiamo eseguire una serie di ulteriori indagini come i raggi x del tubo digerente, la
ERCP (retrograda trans duodenoscopica), ma alla fine si deve eseguire ampillectomia,
che un intervento ampio ad alto rischio di mortalit.
Al successivo esame istologico il tumore si presenta molto ghiandolare.
Tuttavia non pu trattarsi di un adenocarcinoma, poich gli adenocarcinomi, anche se
ben differenziati, presentano elevato indice mitotico, mentre questo tumore si presenta
molto monomorfo con un Ki67 di solo il 2,2%.
Allesame della cromogranina hai una reazione molto positiva.
Si tratta dunque di un tumore ben differenziato ed a bassa aggressivit.
Inoltre il tumore positivo alla somatostatina in modo diffuso.
Nel secondo caso abbiamo invece un pz che presenta una sintomatologia con ittero
ostruttivo e perdita di peso.
Eseguendo tutti gli esami si vede che il tumore ha origine dallampolla del Vater e
dunque viene eseguita ampillectomia.
Allesame istologico si vede un tumore:
- poco differenziato
- con cellule piccole, con scarso citoplasma, disposte in cordoni
- le cellule sono fortemente positive per lematossilina perch il rapporto
nucleo/citoplasma nettamente a favore del nucleo
- le cellule presentano positivit per sinaptofisina e NSE
- le cellule presentano negativit per la cromogranina A
Si tratta dunque di un carcinoma endocrino ben differenziato.
291
Malattie vascolari del SNC
Generalit
Le malattie vascolari del SNC ed, in particolare dellencefalo, rappresentano la terza
causa di morte negli USA dopo le malattie cardiovascolari e i tumori arrivando a
coprire il 50% delle lesioni neurologiche.
A livello clinico si suddividono in 3 tipologie principali:
Trombosi
Embolia
Emorragia
Ictus (o Stroke) la denominazione che si applica a questi fenomeni nel caso essi si
manifestino in maniera acuta!
A livello fisiopatologico possiamo dividere la malattia in 2 processi:
Ipossia, ischemia e infarto causati da compromissione del flusso ematico e
dellossigenazione del SNC
Emorragia causata dalla rottura dei vasi del SNC
Ipossia, ischemia e infarto
Lencefalo riceve il 15% della gittata cardiaca ed responsabile del 20% del consumo
corporeo totale dellossigeno.
Il flusso corrisponde a 50ml/min X 100g di tessuto e rimane costante in certi intervalli
di pressione arteriosa e intracranica grazie a un sistema di autoregolazione delle
resistenze vascolari.
Quando il flusso ematico a una zona si interrompe la sua sopravvivenza dipende da:
Disponibilit di circoli collaterali
Durata dellischemia
Entit e rapidit della riduzione del flusso
Alla luce di questi criteri si distinguono due principali tipi di danno ischemico:
Ischemia cerebrale globale: generale calo della per fusione cerebrale
Ischemia cerebrale focale: calo della perfusione localizzato a una zona
Ischemia cerebrale globale
Questa condizione si verifica in caso di arresto cardiaco, shock o ipotensione grave e
lentit del danno correlata alla durata dellinsulto.
Nei casi lievi si possono manifestare stati confusionali con recupero e assenza di
danno. La ripetizione, per, di questi episodi in alcuni pz, a lungo andare, causa danno
irreversibile.
292
Vi una gerarchia dettata dalla sensibilit delle cell nervose allinsulto nella quale i
neuroni si piazzano al primo posto come cell meno resistenti superando i gi
particolarmente vulnerabili astrociti e oligodendrociti (glia).
Vi , inoltre, allinterno dei neuroni, una vulnerabilit selettiva che distingue neuroni
di diverse zone dellencefalo in base allentit del flusso ematico ricevuto e alle
richieste metaboliche.
Nellischemia cerebrale globale si verifica una morte neuronale diffusa indipendente
dalla vulnerabilit regionale.
I pazienti che sopravvivono a questi episodi cadono in stato vegetativo persistente
(coma) che pu giungere fino alla morte cerebrale contraddistinta principalmente da:
Danno corticale diffuso
EEG piatto
Mancanza di stimoli respiratori
Mancanza di stimolo di perfusione cerebrale
Il pz tenuto in vita con la respirazione artificiale mentre il suo cervello va incontro a
un processo autolitico definito rammollimento.
Morfologia
Lencefalo si presenta rigonfio con circonvoluzioni allargate e solchi ristretti.
Si osserva una scarsa demarcazione tra sostanza bianca e sostanza grigia.
A livello istopatologico si osservano 3 modificazioni:
Cambiamenti precoci: (12-24 ore dopo linsulto) si assiste a una
microvacuolizzazione dei neuroni e a una successiva eosinofilia in seguito a
picnosi e carioressi del nucleo. In seguito eventi analoghi si presentano anche
nella macroglia. Inizia infiltrazione di neutrofili.
Cambiamenti subacuti: (24h 2 settimane dopo linsulto) necrosi del tessuto con
comparsa di macrofagi, proliferazione vascolare e gliosi reattiva.
Riparazione: (dopo 2 settimane dallinsulto) rimozione del tessuto necrotico con
perdita della normale organizzazione parenchimale e gliosi.
A seguito di questi fenomeni si verifica una distruzione asimmetrica della neocortex
causata dal coinvolgimento non omogeneo di uno o pi strati della stessa; questo
fenomeno prende il nome di necrosi pseudolaminare.
Gli infarti della zona di confine sono aree cuneiformi localizzate nei campi pi distali
dellirrorazione arteriosa, si verificano di solito in seguito a episodi di ipotensione.
Il cos detto cervello respiratorio si presenta come materiale soffice e disgregato.
Ischemia cerebrale focale
Causata dallocclusione di unarteria cerebrale e diffusa a tutta la zona che larteria
stessa perfonde.
Il danno e la sua entit dipendono dalla zona colpita e, soprattutto, dalla presenza o
meno di circoli collaterali; a questo proposito il poligono di Willis il principale punto
che sopperisce il pi possibile in questi casi.
293
Vi sono poi rinforzi parziali e incostanti per la superficie cefalica dovuti ad anastomosi
cortico-leptomeningee; al contrario lirrorazione delle strutture profonde (talamo,
nuclei della base) non pu contare su circoli collaterali.
La reazione allischemia delle cellule nervose comprende la massiva liberazione di
neurotrasmettitori che possono causare la morte di cellule pi o meno adiacenti
intaccando la funzionalit dei loro canali ionici.
Lischemia cerebrale focale pu essere causata da diversi fattori:
Trombosi in situ
Embolizzazione da una sorgente a distanza
Vasculite infettiva
Vasculiti non infettive
Altre cause
A questi fattori si aggiunge, ovviamente, una forte associazione della patologia con
diabete e ipertensione.
Trombosi
E causata principalmente dallaterosclerosi.
Le sedi pi comuni sono la biforcazione carotidea, lorigine della cerebrale media e ogni
ramo terminale della basilare.
Vasculite infettiva
Negli anni passati si osservava spesso arterite associata a sifilide o tubercolosi; al
giorno doggi si osservano spesso in quadri di immunosoppressione associati a infezioni
opportunistiche da, per esempio, toxoplasma, aspergilo e CMV.
Vasculite non infettiva
La poliarterite nodosa una collagenopatia in grado di causare infarti singoli o
multipli allencefalo.
Langioite primitiva del SNC un disturbo infiammatorio che coinvolge specialmente i
vasi subaracnoidei e parenchimali di piccolo calibro; una flogosi cronica che porta
alla distruzione della parete vasale.
Altre cause
Malattie ematologiche con stati di ipercoagulabilit
Aneurisma dissecante dei vasi epiaortici
Abuso di sostanze stupefacenti
Arteropatia cerebrale autosomica dominante con infarti subcorticali e leucocefalopatia
Forma ereditaria causata da mutazioni del gene Notch3.
La malattia caratterizzata da ictus ricorrenti e demenza.
294
Listologia ha messo in evidenza un ispessimento concentrico della media e
dellavventizia di alcuni vasi parenchimali e leptomeningei.
Angiopatia amiloidea cerebrale
Peptidi identici a quelli della malattia di Alzheimer si depositano nei vasi di piccolo e
medio calibro della corticale e delle meningi.
Ne deriva un indebolimento del vaso e una conseguente emorragia.
Embolia cerebrale
La sorgente pi comune sono i trombi parietali cardiaci che sono conseguenza di:
Infarto del miocardio
Malattia valvolare
Fibrillazione atriale
In ordine di importanza seguono i tromboembolismi arteriosi spesso a livello delle
placche ateromasiche carotidee.
Altre cause:
Embolismo paradosso nei bambini con malformazioni cardiache
Embolia associata a chirurgia cardiaca
Embolia da materiale (grasso, tumore, aria..)
Il distretto di vascolarizzazione della cerebrale media il pi interessato da emboli.
Morfologia
Linfarto pu essere di due tipi
Rosso: in seguito a emorragie petecchiali diffuse che confluiscono; si associa
spesso a un evento embolico e alla riperfusione, tramite circoli collaterali, dei
vasi danneggiati dalla massa occludente, questo fenomeno causerebbe le
emorragie diffuse.
Pallido: si associa solitamente a trombosi.
Infarto emorragico (rosso)
Ha caratteristiche simili a quelle dellinfarto ischemico con aggiunta di stravaso e
riassorbimento ematico.
Da notare come gli infarti venosi siano quasi sempre emorragici in seguito
allocclusione da parte di un trombo dei seni cerebrali.
Infarto non emorragico (pallido)
E un infarto che si modifica nel tempo.
Dopo 48 ore dal danno irreversibile il tessuto diventa molle, pallido e tumefatto;
la giunzione corticomidollare si fa indistinta.
Dopo 2-10 gg il parenchima si fa gelatinoso e friabile; la giunzione si fa ancora
meno definita a causa delledema che circonda la tumefazione.
295
Fino alle 3 settimane dopo il tessuto si liquefa lasciando una cavit in
espansione rivestita da tessuto scuro grigiastro.
Dal punto di vista tissutale si assiste alle seguenti modificazioni:
Fino a 12h: modificazioni neuronali ischemiche (neuroni rossi), edema
vasogenico e citotossico, cell endoteliali e astrociti iniziano a gonfiarsi, le fibre
mieliniche cominciano a disintegrarsi.
Fino a 48h: migrazione dei neutrofili ha un picco poi scema, i macrofagi
derivanti dalla microglia e dai moniciti circolanti assumono un ruolo
predominante fino alle 2-3 settimane.
Dopo 1 settimana: quando i macrofagi sono gi al lavoro da un po si osservano i
primi astrociti reattivi.
Dopo parecchi mesi: le dimensioni cell degli astrociti si riducono e i loro processi
formano un denso agglomerato di fibre gliali frammiste a capillari e rare fibre di
tessuto connettivo. Questi processi sono la testimonianza della riparazione in
atto.
Clinica
A seconda della localizzazione della patologia si pu avere un pz asintomatico o
presentante una vasta gamma di sintomi correlati alla zona colpita che possono
evolvere fino a exitus.
Emorragia intracranica
Le emorragie possono insorgere in qualsiasi sede del SNC.
Possono essere un evento secondario a, per esempio, infarti dovuti a occlusione
vascolare, o possono essere primitive tipicamente in conseguenza di traumi e si
sviluppano nello spazio subdurale ed epidurale.
Le emorragie a livello subaracnoideo, sebbene possano anchesse essere causate da
traumi, sono pi spesso espressione di una malattia cerebrovascolare.
Emorragia intraparenchimale (intracerebrale)
Queste patologie di origine spontanea (non traumatica) mostrano un picco nelle
persone intorno ai 60 anni.
Lipertensione la causa pi comune coprendo il 50% delleziologia dellemorragia
intraparenchimale.
Questo perch lipertensione causa:
Aterosclerosi accelerata delle arterie di grosso calibro
Aterosclerosi ialina dei capillari
Lesioni proliferative e necrosi nelle arteriose
Sviluppo dei microaneurimi di Charcot-Bouchard siti di rottura??
Altri fattori che possono causare emorragia spontanea sono:
Alterazioni della coagulazione
Chirurgia a cuore aperto
Neoplasie
296
Angiopatie amiloidi
Vasculiti
Aneurismi fusiformi
Malformazioni vascolari
Morfologia
Lemorragia di origine ipertensiva origina al nel putamen (60%), talamo, ponte ed
emisferi cerebellari (raro).
Per le loro localizzazioni si dividono in e. gangliari ed e. lobari.
Lo stravaso di sangue causa compressione parenchimale e, a lungo andare, si forma
una cavit con bordo marrone pallido con edema periferico che va riassorbendosi; le
osservazioni istologiche sono le medesime dellinfarto cerebrale.
Clinica
Se colpisce vaste aree pu essere fatale in poco tempo oppure pu essere silente nel
caso linteressamento sia ridotto e circoscritto.
Lematoma va poi riassorbendosi con miglioramento clinico.
La sintomatologia dipende dalla zona colpita.
Emorragia subarcanoidea e aneurismi sacculari
La rottura di un aneurisma sacculare la pi frequente causa di emorragia
subaracnoidea.
Altre cause:
Estensione di un ematoma traumatico
Rottura di unemorragia ipertensiva intracerebrale nel sistema ventricolare
Malformazione vascolare
Tumori
Disturbi ematologici
Laneurisma sacculare il tipo pi comune di aneurisma intracranico, si riscontrano
per la quasi totalit nella circolazione cerebrale anteriore in prossimit dei principali
punti di ramificazione arteriosa.
Patogenesi degli aneurismi sacculari
Leziologia sconosciuta!
Alcuni studi li mettono in correlazione con alcuni disturbi genetici ereditari.
Fumo e ipertensione sono statisticamente considerati fattori di rischio.
Morfologia
Un aneurisma sacculare unestroflessione a parete sottile e traslucida in
corrispondenza di punti di ramificazione lungo il circolo di Willis.
Misurano 2-3 mm di diametro.
297
La rottura del sacco avviene normalmente allapice dellestroflessione con stravaso di
sangue in sede subaracnoidei e/o nella sostanza cerebrale.
La parete del sacco priva della parete muscolare e della lamina elastica ed
costituita da una parete ialina ispessita.
Clinica
Pi frequente nella 5 decade e leggermente pi comune nelle donne.
Maggiore sono le dimensioni dellaneurisma maggiori sono i pericoli di sanguinamento.
La rottura si ha a un aumento della pressione intracranica come durante attivit
sportiva o un rapporto sessuale; il pz manifesta una cefalea lancinante e sviene.
Il 25-50% muore alla prima rottura, gli altri rinvengono in pochi minuti e migliorano.
Le recidive sono imprevedibili e la loro ricorrenza aggrava la prognosi.
Gli effetti possono essere:
Acuti: a seguito entro poche ore del sanguinamento
Tardivi: legati al processo di riparazione
Uno dei pericoli della fase acuta la diffusione di un vasospasmo che si pu estendere
a diversi vasi e causare ischemia nelle zone adiacenti.
Tra gli effetti tardivi vi lalterato flusso di liquor dovuto alla formazione di cicatrici.
Malformazioni vascolari
Classificabili in 4 gruppi:
Arterovenose
Angiomi cavernosi
Teleangiectasie capillari
Angiomi venosi
Malformazioni arterovenose
Sono le pi comuni e interessano i vasi dello spazio subaracnoideo che si estendono
nellencefalo o in quelli esclusivamente allinterno dellencefalo stesso.
Assomigliano a una rete aggrovigliata di canali vascolari vermiformi con notevole
shunt arterovenoso e notevole flusso ematico passante per la malformazione.
Molti si presentano come vasi ispessiti e presentanti alterazioni della lamina elastica o
sostituzione della media con connettivo ialinizzato.
Angiomi cavernosi
Canali vascolari bassamente organizzati, distesi, con pareti sottili e pive di tessuto
nervoso!
Di solito presenti nel cervelletto, ponte e nelle regioni subcorticali.
298
Teleangiectasie capillari
Foci microscopici di canali vascolari a parete sottile, dilatati e separati da parenchima
cerebrale.
Angiomi venosi
Aggregati di vasi venosi ectasici.
Clinica
Maschi sono colpiti il doppio delle donne con picco trai 10 e i 30 anni presentandosi
come disordine epilettico. La pi colpita la cerebrale media.
299
Neoplasie del Sistema Nervoso Centrale
Generalit
Le neoplasie a carico del sistema nervoso centrale sono per -3/4 primitive, ovvero
originano primariamente nel parenchima cellulare nervoso, la restante parte
rappresenta le neoplasie di origine metastatica.
Questi tumori arrivano a costituire fino al 20% di tutte le neoplasie pediatriche con un
peculiare sviluppo nella fossa cranica posteriore in posizione sopratentoriale.
Le neoplasie del SNC presentano due picchi di et:
- 1 decade: raggiunge il 9%di frequenza
- 6 decade: succede perch i tumori pi comuni come, ad es, lastrocitoma, generano
verso i 40 anni ma, a causa della loro crescita lenta, vengono
allevidenza clinica solo nellanziano.
Questi tumori presentano caratteristiche peculiari:
La distinzione tra forme maligne e forme benigne meno marcata:
- Vi sono neoplasie gliali a basso indice mitotico che sono altamente
infiltrative.
- Queste neoplasie sono di difficile eradicazione chirurgica.
- Posso risultare fatali nonostante il loro istotipi a seconda della loro
localizzazione.
Sono formati da cell particolari e non vi presenza di stroma connettivale.
Danno solo raramente metastasi:
- La barriera emato-encefalica viene solo in rari casi valicata da cell
metastatizzanti
- Lo spazio sub-aracnoideo la via sfruttata dalle cell tumorali per
metastatizzare a livello encefalico e midollare.
Normalmente prevalgono a livello statistico le forme benigne ma, come gi accennato,
in questa classe di patologia conta maggiormente il rapporto della neoplasia, sia essa
benigna o maligna, con lambiente circostante che listotipo stesso.
Un meningioma benigno, per esempio, pu comprimere il bulbo causando morte per
arresto respiratorio.
Pi in generale c da dire che questi tumori crescono in spazi ristretti e spesso
causano compressione da cui spesso scaturisce un aumento della pressione del liquor
(norm=20mmHg); da qui il pi comune sintomo riconducibile spesso a queste
malattie ovvero la cefalea.
Le neoplasie del SNC possono derivare da tre tipi di cell:
Neuroni: rari perch sono cell molto stabili.
300
Macroglia: - Astrociti: cell simili ai fibroblasti che possono formare cicatrici in
condizioni particolari
- Oligodendrociti
- Cell ependimali: hanno caratteristiche comuni alle cell epiteliali,
tappezzano i ventricoli e il canale vertebrale.
Microglia: sono cell simili ai macrofagi che possono dare patologie diverse ma
mai tumore
Le neoplasie della macroglia sono di gran lunga le pi frequenti!
Meningiomi: tumori intracranici extra-parenchimali.
Vi sono ancora problemi nella classificazione a causa di forme che si presentano a
componenti miste gliale-neuronale o due tipologie gliali.
Oltre a questa classificazione questi tumori si possono dividere anche in base alla sede
di interessamento:
Sopratentoriale: tipico delladulto
Sottotentoriale: tipico del bambino
Classificazione WHO dei tumori del sistema nervoso
1. T. neuroepiteliali
2. T. dei nervi periferici
3. T. delle meningi
4. Linfomi e neoplasie ematopoietiche
5. T. cellule germinali
6. T. della sella turcica esordio clinico per compressione
7. T. metastatici sono di difficile diagnosi visto che, per es, una metastasi di
adenocarcinoma pu essere confusa con un meningioma vista
la natura a met tra lepiteliale e lendoteliale delle cell
meningee.
Diagnosi
La diagnosi risulta spesso difficile viste le disparate variet di tumore e la variabilit
della sintomatologia manifesta.
Anche limmunoistochimica di scarso aiuto in quanto possiamo evidenziare solo due
marker:
GFAP (proteina gliofibrillare acida): indica una derivazione gliale.
Ig anti-sinaptofisina: indica una derivazione neuronale.
Problema delleradicazione chirurgica
Vi sono neoplasie benigne che diventano di fatto maligne a causa dellimpossibilit di
escissione chirurgica.
Ci non dovuto a una difficolt di accesso ma allinteressamento di una zona
funzionale.
301
Clinica
Come gi detto la clinica molto variabile e dipende principalmente dalla crescita e
dalla sede di sviluppo.
Cefalea: la massa tumorale ha effetto di aumentare la pressione endocranica.
Epilessia: tumore che ha infiltrato la corteccia (gliomi)
Falso segno focale: il tumore spinge masse cerebrali fino a farle erniare dai diversi
fori e causando la compressione dei nervi in quella sede
Vero segno focale: il tumore ernia comprimendo lui stesso il nervo
Emorragia: segno evidente della crescita tumorale che porta con s
neoangiogenesi e, quindi, formazione di vasi non stabili.
Idrocefalo: il tumore cresce dentro al canale cefalo-rachidiano obliterandolo e
rendendo cos impossibile il drenaggio del liquor dallencefalo.
Edema
Tumori neuroepiteliali
Tumori astrocitici
Tumori oligodendrogliali
Gliomi misti
Tumori ependimali
Tumori del plesso coroideo
Tumori gliali di origine incerta
Tumori neuronali e misti neuronali-gliali
Tumori neuroblastici
Tumori del parenchima pineale derivanti dal terzo occhio dei rettili e infatti
presentano cell simili a quelle della retina
Tumori embrionali
Tumori astrocitici
Astrocitoma diffuso:
Fibrillare
Gemistocitico
Protoplasmatico
Astrocitoma anaplastico
Glioblastoma
Astrocitoma pilocitico
Xantoastrocitoma pleomorfo
Astrocitoma subependimale a cell giganti
Gli ultimi tre tipi di astrocitoma sono localizzati e perci hanno una prognosi migliore.
302
Al contrario gli astrocitomi diffusi, nonostante abbiano un pi basso grado istologico,
sono pi infiltrativi e quindi pi maligni; inoltre vengono diagnosticati tardivamente e,
negli anni, possono passare dal basso grado fino a glioblastoma.
Grading
E stata elaborata una nuova scala di valutazione che supera quella di St.Anne/Mayo.
I: Astrocitoma pilocitico
II: Astrocitoma di basso grado proliferazione di astrociti che si mantengono
quasi uguali ai normali con qualche atipia.
Proliferazione lassa perci non vedo mitosi.
III: Astrocitoma anaplastico elementi polimorfi + atipia + mitosi +
neoangiogenesi
IV: Glioblastoma .+ necrosi!!
questo tumore da aspettative di vita che non superano 1 anno nonostante
eventuali interventi chirurgici, la giovane et del pz aumenta un poco le
aspettative di vita; se attacca zone mute la chirurgia pu essere pi
radicale ma recidiva spesso con differenziamento cellulare e anaplasia
ripresentandosi pi aggressivo.
Eziologia
Radiazioni
Sequenze DNA SV40
Eventi molecolari
Nel passaggio da grado II a III, nell astrocitoma diffuso, si ha la perdita di
alleli su 9q e su 13q e unamplificazione su 12q. I geni coinvolti sono tutti
regolatori del ciclo cell.
In sostanza vi pi di un fattore necessario allo sviluppo della patologia.
Fenotipo
Grado II a III: perdita di allele 9p,13q,amplificazione12q (9p21 geni codificanti per p16
e p15 del ciclo cell)
Astrocitoma diffuso
Elevata differenziazione cellulare, lenta crescita;
Et: 30-40 Questa neoplasia rappresenta l80% dei tumori cerebrali
delladulto!
Sesso: maschi > femmine
Grado: II
Localizzazione: sopratentoriale, frontale e temporale; causa perci sindrome
prefrontale con aggressivit, disinibizione e alterazioni
caratteriali
Macro: margini indistinti o massa gelatinosa a confini indefinibili
Istopatologia: cellularit, rare atipie nucleari., mitosi assenti,GFAP+
Sopravvivenza: 6-8 anni
303
Fattori prognostici: et, resezione chirurgica, mutazione TP53 (variante
gemistocitica)
Clinica: convulsioni, cefalea e deficit neurologici
Lastrocitoma, dal punto di vista istopatologico, suddiviso in 3 tipi:
Fibrillari: cell a stella
Gemistocitico: cell con citoplasma eosinofilo e fini processi, la forma pi
aggressiva
Protoplasmatici: cell con piccolo corpo, scarsi e flaccidi processi simili a cell
reattive, degenerazione mucide
Astrocitoma anaplastico
Anaplasia focale o diffusa; marcato potenziale proliferativo; progressione in
glioblastoma
Et: media 41
Sesso: maschi > femmine
Grado: III
Localizzazione: emisfero cerebrale
Macro: indistinguibile dallastrocitoma diffuso
Istopatologia: cellularit + elevata, atipie nucleari, mitosi frequenti
Genetica molecolare: mutazione TP53
Sopravvivenza: 3 anni
Fattori prognostici: et, resezione chirurgica, presenza di oligodendrociti che
rendono meno aggressivo il tumore.
Glioblastoma
In seguito a uno differenziamento che pu essere locale o diffuso avviene il seguente
schema di trasformazione:
astrocitoma fibrillareastrocitoma anaplastico- - ->glioblastoma
Inoltre vi anche la forma primaria.
Astrociti scarsamente differenziati, proliferazione vascolare, necrosi
Vi pu essere una progressione da grado III o insorgenza de novo;
Et: media 45-70 (rare manifestazioni in utero);
Incidenza: 12-15% SNC
Sesso: maschi > femmine
Grado: IV
Localizzazione: sostanza bianca subcorticale dellemisfero cerebrale (temporale,
parietale, frontale)
Macro: massa grigiastra mal definita, necrosi a palizzata, emorragie,
unilaterale o bilaterale (a farfalla); inoltre proliferazione vascolare
glomeruloide (per similitudine col glomerulo renale) che pu dare
emorragia con relativi sintomi.
Diffusione: rapida, attraverso il corpo calloso, rare metastasi via liquor, rare
metastasi via ematica e liquorale (iatrogena)
304
Istopatologia: astrociti poco differenziati., atipia nucleare, marcata attivit
mitotica con strano orientamento dei fusi mitotici, proliferazione
microvascolare (aspetto glomeruloide), necrosi (a palizzata),
strutture ghiandolari (dd con adenocarcinoma), cell giganti
multinucleate (variabile maligna), cell.lipidizzate, cell.granulari
ICC: GFAP+
EM: variabilit morfologica, mitocondri degenerati, presenza filamenti dipende
da differenziazione
Genetica molecolare:
- Mutazione TP53, LOH 17p secondario (progressione da grado III)
- LOH 10p, amplificazione EGFR primario (GBM de novo)
Sopravvivenza: <1 anno indipendente da chemio e radioterapia
Fattori prognostici: et (< 45 anni), necrosi -, resezione chirurgica, EGFR -,
PTEN+, TP53 indiff.
E un tumore dal comportamento imprevedibile ed assurdo, in alcuni casi produce
actina, miosina e risulta GFAP-.
La sopravvivenza non supera un anno nonostante radioterapia e chemioterapia.
Astrocitoma pilocitico
Circoscritto, lenta crescita, pattern bifasico (cell bipolari + fibre di Rosenthal;
cell.multipolari + microcisti e granular bodies)
Et: 10-20 anni
Clinica: cefalea, endocrinopatie, deficit visivi, no epilessia
Sesso: no prevalenza
Grado: I
Localizzazione: nevrasse; principalmente nel cervelletto, nervo ottico, chiasma
ottico, emisfero cerebrale, midollo spinale
Macro: massa discreta ben limitata con cisti
Istopatologia: pattern bifasico, scarsa cellularit, processi hair-like (aspetto
piloide), rare mitosi, proliferazione vascolare, alterazioni
regressive (calcificazioni, necrosi, linfociti)
ICC: GFAP +, fibre di Rosenthal (cristallina dalla degenerazione dei filamenti
del citoscheletro), EGB (1chimotripsina e 1tripsina)
Genetica: correlato a NF1
Sopravvivenza: benigno; a lenta evoluzione con possibilit di stabilizzazione o
regressione, associazione a NF1 pi aggressivo; associato a rare
mitosi, aumentata cellularit, atipia cellulare (astro pilocitico
atipico) non ha significato clinico.
Clinica: deficit visivi, endocrinopatie
Diagnosi: in presenza di cell multipolari e di granuli i pu porre certa diagnosi
Tumori oligodendrogliali
Oligodendroglioma
Oligodendroglioma anaplastico
305
Oligodendroglioma
Cellule oligodendrogliali ben differenziate; diffusamente infiltrante;
Et: 50-60 anni, rari nellinfanzia;
Incidenza: 4.2% SNC
Sesso: maschi > femmine
Grado: II
Localizzazione: sostanza bianca emisferica (frontale)
Clinica: convulsioni epilettiche, cefalea
Macro: massa soffice, grigio-rosata o gelatinosa, calcificazioni
Istopatologia: moderatamente cellulato, cell rotonde con citoplasma chiaro,
microcalcificazioni, rete capillare, occasionali mitosi
ICC: no markers specifici (S-100, Leu7, GFAP, Vim)
EM: cellule rotonde, citoplasma estratto, nucleo regolare, microtubuli
perinucleari, tozzi e corti microvilli, aggregati mitocondriali
Genetica molecolare: perdita eterozigoti per 19q, 1p; forte espressione di EGFR
Sopravvivenza: 3-5 anni
Fattori prognostici: et, localizzazione frontale, resezione chirurgica
La variante anaplastica presenta allEM unaumentata densit cellulare con anaplasia
nucleare, aumento delle mitosi e necrosi. In questo caso la prognosi peggiore.
Vista lassenza di marker distintivi pu essere confuso con lependimoma a cell chiare
o con un neurocitoma (che pu essere sinaptofisina a causa del prolungato fissaggio).
Per questo molto importante la diagnosi differenziale.
Gliomi misti
Oligoastrocitoma
Oligoastrocitoma anaplastico
Tumori ependimali
Ependimoma
Cellulare
Papillare
A cellule chiare
Tanicitico
Ependimoma anaplastico
Ependimoma mixopapillare
Subependimoma
Questo tipo di patologie insorgono spesso in prossimit del sistema ventricolare o del
canale centrale visto che entrambi sono rivestiti da ependima.
306
Ependimoma
Cellule ependimali ben diff; lenta crescita; bambino e giovane adulto; parete dei
ventricoli;
Incidenza: 3-9% dei t. neuroepiteliali
Et: - nel bambino infratentoriale interessando 3 e 4 ventricolo
- nelladulto (30-40 anni) spinale
- bambino e adulto sopratentoriale interessando i ventricoli laterali
Sesso: non prevalenza
Grado: II
Localizzazione: fossa posteriore e midollo spinale; III,IV e ventricoli laterali
Clinica: dipende dalla sede (sottotentoriali, idrocefalo; fossa post, atassia
cerebellare; sopratentoriali, deficit neurologici, convulsioni)
Macro: ben demarcato, soffice, grigiastro-rosa, cisti, foci di necrosi o emorragici
Istopatologia: nuclei monomorfi (basso grado), pseudorosette perivascolari e
rosette ependimali (tipiche del tessuto), mitosi rare o assenti, necrosi
occasionale; GFAP, Vim., S-100, EMA, CK focalipu avere tre aspetti:
- Cellulare con scarse rosette;
- Papillare con papille ben formate
- Cellule chiare che va in DD con oligodendroglioma e neurocitoma; EM
diagnostica
- Tanicitico con aspetto astrocitico
EM: cellule fusate, filamenti gliali, giunzioni zipper-like, microrosette con
microvilli e ciglia
Genetica: correlato a NF2 (neurofibromatosi di tipo 2)
Genetica molecolare: LOH 17p
Sopravvivenza: 5-10 anni indipendente dal grado di resezione chirurgica
Fattori prognostici: giovane et -, localizzazione (spinale, sovratentoriale, fossa)
se la malattia localizzata a livello del 3-4 ventricolo, per la sua vicinanza ai
centri bulbari e pontini difficile la sua resecazione completa; nelle
manifestazioni spinali, invece, la resecazione spesso totale.
Ependimoma mixopapillare
Si manifesta nel giovane adulto a livello del filum terminale della cauda
presentando un pattern papillare
Incidenza: rappresenta il 13% degli ependimomi ed la neoplasia
intramidollare pi comune
Et: media 36
Sesso: femmine>maschio
Grado: I
Localizzazione: cauda equina e, raramente, a livello emisferico
Clinica: dolori alla schiena di lunga durata
Macro: soffice, lobulato, grigiastro
Istopatologia: pattern papillare con cell cuboidali, matrice mixoide, mitosi rare o
assenti;
ICC: GFAP, S-100, Vim
EM: caratteristiche ependimali, lamina basale
307
Sopravvivenza: prognosi buona, 10 anni indipendente dal grado di resezione
chirurgica; recidive rare
Papilloma dei plessi
Et pediatrica
Asse connettivale ricoperto da epitelio cuboidale a volte colonnare che riproduce
fedelmente la struttura di un vero plesso corioideo.
Idrocefalo (anche comunicante per iperproduzione)
Tumori neuronali e misti neuronali-gliali
Gangliocitoma
Astrocitoma infantile desmoplastico/ Ganglioglioma
Tumore neuroepiteliale disembrioplastico (DNT)
Ganglioglioma
Ganglioglioma anaplastico
Neurocitoma centrale
Liponeurocitoma cerebellare
Paraganglioma
Si presentano spesso come entit con pi citotipi diversi prendendo, cos, la
denominazione di misti.
Le variet di questi tumori misti sono in numero molto elevato.
La denominazione ganglioma distingue una famiglia di neoplasie derivanti dalle cell
piramidali.
La denominazione neurocitoma indica la proliferazione neoplastica di piccoli neuroni
derivati dalle cell dei granuli interni del cervelletto che spesso si manifestano in
posizione paraventricolare.
Neurocitoma centrale
Cellule rotonde a diff neuronale; ventricolo laterale;giovane adulto; prognosi
favorevole
Incidenza: 0.25-0.5% SNC
Et: media 29 anni
Sesso: non prevalenza
Grado: II
Localizzazione: ventricoli laterali e III ventricolo
Clinica: pressione intracranica, occasionali deficit visivi e mentali
Macro: massa grigiastra, friabile, calcificazioni e occasionali emorragie
Istopatologia: cellule rotonde, monomorfe, oligo-like; neuropilo (aree fibrillari);
microvascolarizzazione con aspetti di arborizzazione;
308
ICC : Sinaptofisina (falsi + o negativit)
DD: oligodendroglioma, ependimoma a cell chiare, pineocitoma, DNT
EM: cellule rotonde, nucleo monomorfo, microtubuli dispersi, granuli
neuroendocrini, prolungamenti neuritici con microtubuli, strutture simil-
sinaptiche
Genetica molecolare: gain chr.7, isocromosoma 17
Sopravvivenza: prognosi favorevole, resezione completa; pu avere aggressivit
istologica non influente sulla prognosi
Ganglioma
Gruppi irregolari di neuroni displastici, multipolari + componente gliale
costituita da astrociti circondati da stroma reticolinico. Necrosi assente
Incidenza: 0.4% SNC
Et: media tra 8.5 e 25 anni
Sesso: 1.1:1
Grado: I
Localizzazione: cervello, cervelletto, midollo allungato, spinale, nervo ottico,
ipofisi, gh. pineale
Clinica: dipende dalla sede
Macro: massa solida o cistica, occasionali calcificazioni
Tumori embrionari
Medulloepitelioma
Ependimoblastoma
Medulloblastoma
Medulloblastoma desmoplastico Tutti questi tumori esprimono
Medulloblastoma a grandi cellule pochi o nessun marcatore della
Medullomioblastoma cell mature del SNC, per questo
Medulloblastoma melanotico sono detti embrionari o
PNET indifferenziati
Neuroblastoma
Ganglioneuroblastoma
T.rabdoide-teratoide atipico
Medulloblastoma
Tumore invasivo, maligno embrionale del cervelletto; differenziazione
prevalentemente neuronale; bambino; tendenza alla disseminazione mediante
liquor costituisce il 20% dei tumori cerebrali nei bambini.
Incidenza: 0.5 x 100.000
Et: media 7 anni; nelladulto, 21-40 anni
Sesso: 65% nei maschi
Grado: IV
Localizzazione: verme del cervelletto; tendenza ad infiltrare il IV ventricolo
309
Clinica: atassia del tronco, disturbo del passo, ipertensione secondaria ad
ostruzione del canale ependimale, cefalea, vomito mattutino
Macro: consistenza variabile, emorragia massiva
Istopatologia:
- Medulloblastoma classico: cell.rotondo-ovali. Nucleo ipercromatico,
scarso citoplasma, rosette neuroblastiche
- Medulloblastoma desmoplastico: noduli a bassa cell. con nucleo monomorfo,
circondati da aree intensamente cellulate e
proliferanti
- Medulloblastoma a grandi cellule: cell. grandi, nucleo pleomorfo, nucleoli
prominenti, necrosi, elevata attivit mitotica
ICC: nestina, Vim, Sin, NF, GFAP, N-CAM
EM: differenziazione neuroblastica con neuriti, granuli neuroendocrini,
strutture simil-sinaptiche; aree di differenziazione gliale
Genetica: associato a forme famigliari, sindrome di Turcot
Genetica molecolare: amplificazione gene MYC; LOH 17p, 1q, 10q,5q (gene
APC)
Sopravvivenza: 50-70% a 5 anni
- Fattori negativi: et<3 anni, metastasi alla presentazione, resezione
chirurgica parziale, variante a grandi cellule,
differenziazione gliale, LOH 17p, amplificazione MYC.
- Fattori positivi: variante desmoplastica, aneuploidia, differenziazione
neuronale, apoptosi.
Meningioma
Tumore generalmente a lenta crescita, benigno in rapporto alla dura madre
costituito da cellule meningoteliali dellaracnoide . Pu essere multifocale e
recidivare.
Incidenza: 6 x 100.000 (frequenza allautopsia 1.4%)
Et: adulto-anziano
Sesso: femminile (rapporto 2:1)
Grado: I, II (meningioma atipico), III (meningioma anaplastico)
Localizzazione: intracranici (sopra le convessit cerebrali attaccati alla falce),
cavit orbitale e intravertebrale, rari extracranici
Clinica: sintomatologia da compressione delle strutture adiacenti o deficits
specifici relativamente alla sede
Macro: consistenza solida o elastica; lobulato
Istopatologia:
- Meningoteliale o sinciziale: whorls e corpi psammomatosi
- Fibroso: cellule fusate in fasci separati da abbondante collagene
- Transizionale: intermedio tra meningoteliale e fibroso
- Meningioma atipico: mitosi + 3 o piu parametri (cellularita, elevato N/C,
nucleoli prominenti, necrosi, sheet-like),
- Meningioma anaplastico: simil-sarcoma, >20 mitosi x 10HPF
310
Varianti: Psammomatosa, angiomatoso, microcistico,secretorio, metaplastico
,cordoide (II), a cellule chiare (II) , papillare (III), rabdoide (III)
ICC: EMA, VIM, S-100, CEA (secretorio)
EM: desmosomi, prolungamenti citoplasmatici interdigitati, filamenti
intermedi, nuclei con pseudoinclusioni.
Genetica:
- Meningioma, grado I : LOH 22q, mutazioni NF2
- Meningioma atipico, grado II : LOH 1p, 6q, 10q, 18q; gain 1q, 9q, 12q, 15q, 17q,
20q.
- Meningioma anaplastico, grado III: LOH 6q, 9p, 10 e 14 q, amplificazione 17q,
mutazioni rare TP53, PTEN, delezioni rare
CDKN2A
Prognosi: predizione di recidiva e di sopravvivenza (grado III); estensione della
resezione, sede, et, grado, indici di proliferazione (MIB1), recettori per il
progesterone.
Tumori metastatici
Le metastasi, soprattutto di origine carcinomatosa, rappresentano fino alla met delle
neoplasie intracraniche.
Le sedi di derivazione primaria principali sono:
Polmone
Mammella
Cute (melanoma)
Rene
Tratto gastrointestinale
Spesso le masse metastatiche si possono presentare come la prima manifestazione
della neoplasia che le ha generate.
Le masse intraparenchimali risultano ben delimitate, spesso al confine tra sostanza
bianca e sostanza grigia e circondate da una zona edematosa.
Alle volte le metastasi possono essere attorniate da gliosi reattiva.
311
Neoplasie epiteliali della cute
Epidermide normale
Vi sono diversi tipi di cellule da ognuno dei quali pu derivare un tumore.
Cheratinociti
Cellule epiteliali suddivise in diversi strati.
Mano a mano che dagli strati profondi si va verso gli strati superficiali, le cellule
maturano, si differenziano ed assumono caratteristiche diverse.
A partire dallo strato pi interno, verso la superficie, si hanno:
Strato basale: contiene cellule staminali della cute che rigenerano in continuazione.
Essendo indifferenziate e proliferanti sono pi sensibili allo sviluppo del tumore.
Strato spinoso: hanno questo aspetto per la presenza di ponti fra cellula e cellula.
Inoltre nel citoplasma cominciano ad accumularsi tonofibrille composte da
citocheratina (proteina tipica delle cellule epiteliali). Le tonofibrille conferiscono
resistenza e tono alle cellule.
Strato granuloso: sulle tonofibrille che continuano ad accumularsi si va depositando
un collante lipidico, che in questo strato forma dei granuli.
Strato lucido; le tonofibrille ed il collante continuano ad accumularsi formando una
massa amorfa. In questo strato gi non pi visibile il nucleo. Si tratta dunque di
cellule gi morte
Strato corneo: si tratta di cellule completamente differenziate e morte, che vanno
incontro a desquamazione.
Ognuno di questi tipi cellulari pu andare incontro a proliferazione neoplastica.
La cellula neoplastica nella proliferazione tende a ricostituire una struttura uguale a
quella di partenza, ma non riesce a garantire la funzionalit della medesima.
A volte lepitelio perde alcune delle sue caratteristiche proprio nella differenziazione.
Ortocheratosi: normale differenziazione.
Paracheratosi: differenziazione alterata. Nelle cellule degli starti superficiali si vede
ancora il nucleo.
La membrana basale uno strtato che sottende ai cheratinociti.
Fornisce appoggio meccanico alle cellule dellepitelio garantendo la polarizzazione
della differenziazione ( un processo orientato vettorialmente ).
Inoltre il mezzo di contatto tra epidermide e sottostante derma garantendo il
signalling fra di essi.
312
Il fenotipo normale dei cheratinociti li vede fondamentalmente positivi per la
citocheratina.
Melanociti
Sono cellule che si ritrovano nella parte basale dellepitelio.
Derivano dalla cresta neurale, ma sono diverse dai cheratinociti.
Si tratta di cellule dendritiche, dotate di numerosi prolungamenti e capaci di formare
diramazioni.
Producono melanina, un pigmento colore marrone scuro che ha la fnz di proteggere il
DNA dai raggi UV nella cute esposta al sole.
In risposta allo stimolo luminoso, i melanociti producono granuli di melanina, detti
melenosomi, e li trasportano fino alla parte terminale dei loro dendriti, nello strato
superiore:
I cheratinociti dunque fagocitano la porzione terminale dei dendriti, contenente i
melanosomi, acquisendo cos la melanina che li protegge dai danni delle radiazioni.
Il fenotipo normale dei melanociti li vede fondamentalmente positivi per la vimentina
e negativi per la citocheratina.
La vimentina un marker delle cellule mesenchimali in genere.
Cellule di Langherans
Sono cellule epidermiche dendritiche, APC professionali.
Esse catturano e processano gli antigeni, presentandoli poi sulla loro superficie;
dunque, grazie alla loro capacit di movimento discendono nellepitelio ed
attraversano la membrana basale, ponendosi cos a contatto con gli elementi linfoidi.
Fanno quindi parte del sistema immunitario: anche la cute in generale si pu
considerare come parte del compartimento innato del S.I. poich costituisce una prima
barriera fisica allingresso dei microbi
Si ritrovano negli strati al di sopra di quello basale e non sono unite alle altre da
alcuna giunzione specializzata.
Anche queste cellule sono in grado di andare incontro ad una proliferazione
neoplastica, dando luogo ad istiocitosi.
Il marker caratteristico di questo tipo di proliferazione neoplastica lidentificazione
ultrastrutturale di granuli di Birbeck, caratteristici delle cellule di Langhrans.
Cellule di Merkel
Si tratta di elementi neuroendocrini che contengono al loro interno granulazioni
costituenti il neurosecreto.
Si ritrovano nello strato basale dellepidermide.
Anche queste cellule sono in grado di andare incontro ad una proliferazione
neoplastica, dando luogo a merkelosi, un tipo di tumore molto raro.
313
Trasformazioni tumorali dei cheratinociti
Secondo una progressione in senso di acquisizione di malignit, la trasformazione
tumorale dei cheratinociti vede i seguenti stadi:
1. cheratosi attinica: una situazione pre-cancerosa
2. carcinoma in situ
3. carcinoma invasivo
Vi sono diversi fattori che possono portare ad una proliferazione anomala:
- fattori ambientali: es. luce solare
- infezioni virali da virus oncogeno. Es. papillomavirus
La diagnosi differenziale necessaria nei confronti di:
- nevo epidermico
- cheratosi seborroica
- cheratoacantoma
- carcinoma a cellule squamose
- neoplasie poco differenziate (metastasi, carcinoma mesenchimale)
Acantoma a cellule chiare
Si tratta di una neoplasia benigna a partire da cellule squamose epidermiche
cheratinizzate, con citoplasma ricco di glicogeno.
- allesame obiettivo si presenta come un erosione della superficie
- ha una localizzazione preferenziale agli arti inferiori
- colpisce prevalentemente adulti ed anziani, perch dovuta allaccumulo di
mutazioni in sede epiteliale.
- Le cellule sono chiare per la presenza di abbondanti quantit di glicogeno, che
nella fissazione in paraffina o con formalina tende ad essere estratto.
- La diagnosi differenziale molto importante perch allesame obiettivo questo
tipo di tumore si presenta come unulcera.
Cheratoacantoma
una neoplasia benigna derivante da cellule epidermiche dello strato corneo, gi
cheratinizzate.
Ha una prevalenza nei maschi rispetto che nelle femmine, con un rapporto 3:1.
Si presenta come un nodulo cupoliforme, di colore roseo, con una depressione centrale
ripiena di cheratina (aspetto a cratere) circondata da un anello di proliferazione
epiteliale neoplastica.
314
Generalmente un nodulo singolo localizzato prevalentemente nel viso, nel dorso e
nelle mani (principalmente aree cutanee fotoesposte); solamente in condizioni di
immunodepressione a volte ha uno sviluppo multiplo.
Le sue dimensioni sono molto variabili: solitamente il nodulo ha un diametro di 1-2.5
cm., ma a volte raggiunge anche forme giganti con diametro > di 5cm., fino a 20cm.
A differenza degli altri tumori benigni, che generalmente si sviluppano nel corso del
tempo per accumulo di mutazioni, questa una neoplasia a crescita rapida.
necessaria diagnosi differenziale nei confronti del carcinoma squamo-cellulare che a
volte si presenta con una situazione macroscopica di tipo crateriforme
Istologia
una neoplasia, fortemente demarcata rispetto alla circostante cute, sia esofitica
(cresce allesterno) che endofitica (cresce allinterno).
Presenta un cratere centrale ripieno di squame che vengono ad essere
ortocheratosiche, ma comunque con una quantit maggiore di cheratina, che si
presenta come laminata ed eosinofila.
Nella zona marginale vi iperplasia dellepitelio, senza displasia del medesimo: le
cellule epiteliali si estendono intorno ai margini del cratere in un numero aumentato
di strati, come prolungamenti irregolari.
Si tratta comunque di un tumore benigno dunque che pu andare incontro a
regressione spontanea, senza alcun tipo di trattamento.
privo di cheratosi attinica, in presenza della quale vi sarebbe paracheratosi.
Citologia
Le cellule epiteliali sono di dimensioni aumentate, squamose, con abbondante
glicogeno.
Possono presentare atipie citologiche, che sono tuttavia di tipo reattivo e non
displastico (il nucleo nelle cellule cheratinizzate non presente, le alterazioni sono
dovute unicamente alliperplasia).
Queste cellule hanno citoplasma eosinofilo caratteristico e cheratinizzano bruscamente
( senza presenza di un interposto strato granuloso).
Le cellule periferiche che occupano lo strato basale, sono cellule basaliodi, che dunque
assomigliano alle cellule dello strato basale, ma sono meno differenziate.
Nella fase iniziale, di rapida proliferazione, la risposta infiammatoria molto scarsa.
Quando la lesione progredisce invece vi notevole risposta infiammatoria che pu
portare alla formazione di micro-ascessi.
Nel momento in cui il tumore va incontro a regressione e perde le cellule dello strato
corneo, si ha produzione di fibrosi del derma, necessaria alla guarigione dal processo
neoplastico.
315
Diagnosi differenziale
Dal carcinoma squamo-cellulare.
Nel carcinoma squamo-cellulare:
- si ha presenza dello strato granulare
- si ha paracheratosi, dunque pedita del nucleo negli strati superficiali
- si ha invasione del derma
- la crescita pi lenta, ma non si ha mai regressione spontanea, anzi il tm tende
allinvasione
- si ha presenza di aree di necrosi: presenti in tutte le neoplasie maligne, poich
lirrorazione sanguina e dunque il nutrimento sempre insufficiente rispetto
alle necessit della massa tumorale, in rapida crescita.
- Si ha presenza di aree di emorragia, accanto alle aree di necrosi: lemorragia
dovuta alla neoangiogenesi compensatoria che porta alla formazione di vasi con
pareti immature che vanno incontro pi facilmente a rottura. Il risultato la
formazione di aree necrotiche ricche di coaguli.
Dalla cheratosi attinica (situazione pre-cancerosa)
Nella cheratosi attinica:
- si ha ugualmente crescita rapida
- si ha presenza di dotti eccrini proliferanti e metaplastici che secernono un
prodotto differente.
- Si ha pseudoinvasione periferica: in realt non si ha invasione ma solo una
situazione di proliferazione di elementi atipici. Sembra di vedere la presenza di
cordoni che penetrano nel derma, ma non cos.
- La regressione molto lenta ma comunque la prognosi favorevole.
Cheratosi attinica
importante perch viene a costituire la modificazione displastica che precede la
definitiva trasformazione cellulare cancerosa.
causata da una serie di agenti:
- esposizione cronica al sole
- radiazioni ionizzanti: pu essere un problema che insorge post-radioterapia
- idrocarburi ed arsenicati: possono essere sostanze che inducono mutazioni.
Insorge prevalentemente nelladulto/anziano (accumulo di mutazioni)
Fra i fattori predisponenti vi la pelle di carnagione chiara, che pi delicata avendo
meno melanociti.
Le lesioni hanno generalmente diametro<1 cm., colorito rosso bruno, o rosso, ma
comunque eritematoso ( DD con carcinoma basalioide), aspetto a carta vetrata.
Si ha una cheratosi, dunque una produzione molto maggiore di cheratina negli strati
superficiali squamosi: in alcuni casi la produzione di cheratina cos abbondante da
dare luogo alla formazione di un corno cutaneo.
316
Le lesioni sono pigmentate ( DD con lentigo e con lentigo maligna).
Le regioni cutanee pi colpite sono quelle pi frequentemente esposte al sole: volto,
braccia, dorso delle mani.
Istologia
Marker fondamentale di questo tumore da un punto di vista istologico la presenza di
displasia, cio di atipia cellulare.
Latipia cellulare compare inizialmente nelle cellule dello strato basale
dellepidermide, che sono le pi sensibili agli stimoli oncogenici e mano a mano si
propaga agli strati superiori.
Nel momento in cui tutto lo spessore dellepitelio interessato da atipie e displasie si
pu gi parlare di carcinoma in situ.
Le cellule basali atipiche presentano citoplasma rosa o rosso, nuclei allungati
ipercromatici con cromatina raccolta in grosse zolle, a volte ponti intercellulari.
La maturazione di queste strutture alterata, tanto che lo strato corneo ispessito e
vede la presenza di cellule ancora nucleate paracheratosi.
Il tumore pu presentare due varianti:
- variante iperplastica: le cellule displastiche dello strato basale proliferano
attivamente
- variante atrofica: le cellule displastiche dello strato basale vanno incontro a
diffusa atrofia che comporta diffuso assottigliamento della cute.
Il tumore pu essere associato a :
- infiltrato infiammatorio cheratosi attinica licheinoide
- pigmentazione melanica
- elastosi: degenerazione delle fibre elastiche. Vede presenza di una sostanza
amorfa, rossastra, monomorfa, che si associa spesso a teleangioctasia, cio
dilatazione delle strutture vascolari. un aspetto molto comune della cute
esposta ai raggi solari che vede ispessimento della cute, ma, se non si tratta di
tumore, mancanza di atipie.
- Acantolisi: dissoluzione o lisi dei siti di adesione intercellulare allinterno
dellepitelio. Provoca un disordine dello strato basale con conseguente
degenerazione delle cellule neoplastiche e formazione di foci di vescicolazione.
La cheratosi pu essere associata ad un carcinoma micro-invasivo, che dunque tende a
diffondersi nel derma sottostante.
Prognosi della cheratosi attinica
- generalmente buona
- si tratta di una lesione pre-cancerosa, dunque bene eradicarla e non lasciarla
in situ, anche perch di facile identificazione, interessando zone della cute di
grande visibilit.
- Non si conosce la percentuale di casi che evolve verso il carcinoma spino-
cellulare.
317
Carcinoma spino-cellulare
definibile come una proliferazione di cellule epidermiche con caratteristiche di
elementi basali e soprabasali.
il secondo tumore per frequenza, che insorge nella cute fotoesposta, principalmente
a livello di testa e tronco.
Eccetto che per le lesioni degli arti inferiori, questi tumori presentano una maggiore
incidenza tra gli uomini, principalmente nei soggetti anziani ( accumulo di lesioni).
Inizialmente si sviluppa come carcinoma in situ (non infiltra la mbr basale della
giunzione dermoepidermica):
- placca a margini netti di colore rosso (eritematosa)
- a volte ipercheratosica
- DD con le dermatiti infiammatorie che per non hanno ipercheratosi.
Quindi il tumore pu passare allo stato di invasivit (superamento della mbr basale):
- placche dure
- presenza di bordo ipercheratosico, con perdita di squame
- ulcerazione superficiale a volte
- a volte si ha la presenza di un cratere superficiale (DD con cheratoacantoma)
- se interessata la mucosa orale si hanno aree di ispessimento biancastre
leucoplachia
La prognosi di questo carcinoma non mai biologicamente cos maligna come dovrebbe
essere quella di un carcinoma.
La capacit di dare metastasi di questo tumore molto maggiore se esso si localizza a
livello delle mucose, poich si ha una maggiore vicinanza ai vasi.
causata da una serie di agenti:
- esposizione cronica ai raggi UV (sole)
- cancerogeni industriali (catrami ed oli)
- ulcere croniche e vecchie cicatrici da ustioni: vi una continua proliferazione
riparativa, con conseguente aumento della probabilit di insorgenza di
mutazioni.
- radiazioni ionizzanti
- tabacco: causa della comparsa di questo tumore a livello della mucosa orale. Il
calore del fumo infatti uno stimolo irritativi continuo che provoca metaplasia e
dunque successivamente aumentail rischio di neoplasia.
- xeroderma pigmentoso: i soggetti affetti da questa patologia hanno minima
capacit di riparare il DNA.
- HPV36 (papillomavirus): ceppo di virus con propriet oncogeniche spiccate
Istologia
Proliferazione di cellule atipiche a tutti i livelli dellepidermide.
Latipia prevalentemente nucleare: i nuclei sono grand,.polimorfi, con contorno
angolato, ipercromatici, con aumentata attivit mitotica, atipie nella disposizione del
fuso mitotico, nucleoli prominenti..
318
Lo strato corneo, sia nei tumori in situ che in quelli invasivi ispessito, e presenta
paracheratosi.
Lo strato granuloso invece assente o silente.
Vi aumento dellangiogenesi, per fornire un maggiore nutrimento alle cellule
neoplastiche, ma vi anche infiltrato infiammatorio.
Nel momento in cui la cellula epiteliode neoplastica attraversa la mbr basale, il
tumore diventa di tipo invasivo. La mbr basale lo stratodi separazione tra
epidermide e derma ed formata da:
- collagene di tipo IV
- laminina o epiliprina
- integrine: proteine di mbr
Le cellule prendono contatto con i componenti della matrice attraverso strutture
giunzionali dette emidesmosomi.
Le cellule epiteliali acquisiscono la capacit di passare la mbr basale nel momento in
cui le strutture desmosomiali si perdono.
I carcinomi squamocellulari infiltranti mostrano un grado molto variabile di
differenziazione, variando da tumori composti da cellule poligonali squamose disposte
in ordinati lobuli, con ampie aree di ipercheratinizzazione, a tumori formati da cellule
tondeggianti, anaplastiche, con focolai di necrosi e di emorragia.
Alcune varianti della morfologia del tumore sono rappresentate da:
- variante a cellule fusate
- variante con pattern pseudghiandolari: presenza di aree acantolitiche che
potrebbero simulare un lume ghiandolare
La cellula neoplastica tenta sempre di riprodurre funzionalmente la cellula normale,
ma non vi pu riuscire completamente: a volte tentando di conservare la produzione di
cheratina la cellula neoplastica produce negli strati epidermici delle strutture dette
perle cornee, ammassi cheratinizzati, dovuti alla produzione di cheratina allinterno
dellepidermide medesima.
Diagnosi
molto importante stabilire se si tratti di una neoplasia primitiva della cute o di una
metastasi secondaria a livello cutaneo.
Per fare ci vengono utilizzate tecniche di immunoistochimica, che mettono in
evidenza la positivit per le citocheratine delle cellule neoplastiche di derivazione
epidermica.
La diagnosi differenziale importante nei confronti di altre 3 situazioni, di cui 2
neoplastiche:
- melanoma
- linfoma a grandi cellule
- cheratoacantoma: il problema della diagnosi differenziale in questo caso meno
grave
La prognosi solitamente buona.
319
Il tumore metastatizza nel 2-3% dei casi: di questi l11% vede metastasi sulla mucosa
labiale, mentre lo 0.5% vede metastasi sulla cute danneggiata dallesposizione al sole.
Carcinoma basocellulare
una neoplasia maligna derivante da un elemento indifferenziato che d origine a:
- cellule dello strato basale
- dotti delle ghiandole che formano gli annessi
il primo tumore per frequenza, che insorge nella cute fotoesposta, principalmente
nei soggetti anziani (accumulo di lesioni).
Ha crescita indolente
Il fattore cancerogeno pi importante lesposizione cronica ai raggi UV.
Si presenta come una papula grigiastra, traslucida, priva di spessore e ben
circoscritta, associata a teleangiectasia (capillari subepidermici prominenti e dilatati).
Le lesioni avanzate possono ulcerare: lulcerazione sintomo di maggiore invasivit
del tm nel derma. Infatti lulcera si ricrea in continuazione e vi possono essere casi di
invasione locale profonda fino allosso o fino ai seni dellosso mascellare, giustificando
la denominazione di ulcus rodens.
Pu essere fortemente invasivo e raramente presentare anche notevole capacit
metastatica, spesso per via ematica.
Alcune varianti della morfologia del tumore sono rappresentate da:
- variante multifocale: le cellule epidermiche neoplastiche si estendono
lateralmente per molti cm. Quadrati
- variante eritematosa: richiede DD con ca spinocellulare, con melanoma a
crescita radiale nelle prime fasi, con dermatiti infettive.
- Variante pigmentata: placca pigmentata che pu assomigliare ad una forma
precoce di meloma. DD con melanoma a crescita radiale.
Istologia
Le cellule neopastiche formano cordoni ed isole, abbastanza basofile, che si addentrano
nel derma superficiale e profondo; i margini fra cellule non sono quasi distinguibili.
Le cellule neoplastiche hanno nuclei ipercromatici e sono circondate da uno stroma
molto abbondante, contenente molti fibroblasti e linfociti.
Le cellule che formano la periferia dei cordoni si dispongono a palizzata, cio
radicalmente parallele le une alle altre.
Lo stroma intorno ad esse per caratteristicamente retratto, dando luogo a spazi
otticamente vuoti artefattuali, che aiutano nella DD.
La cheratosi attinica non necessariamente presente come tappa pre-cancerosa, ma
pu esserlo: nei casi in cui non vi sia, il carcinoma insorge direttamente nel derma,
lasciando le cellule epidermiche intatte.
320
spesso accompagnato da elastosi, proprio perch una dei fattori cancerogenici
principali costituito dalle radiazioni solari.
Prognosi
La crescita locale aggressiva, anche se la capacit metastatica scarsa, con tendenza
a recidivare nella medesima sede.
Questo tumore ha un particolare tropismo per le cellule neurali e questo costituisce un
problema, soprattutto se localizzato al viso, poich seguendo i rami nervosi pu
giungere fino al SNC.
Diagnosi differenziale con il carcinoma squamocellulare
Il basalioma ha le seguenti caratteristiche che lo distinguono da un
carcinoma squamocellulare:
a. nucleoli non prominenti
b. non vi sono singole cellule che possono invadere il derma
dallepitelio, ma le cellule sono sempre disposte in
cordoni
c. bassa attivit mitotica
d. necrosi a cellule singole e non in aree come nel ca
squamocellulare
e. organizzazione delle cellule neoplastiche in palizzate
perinodulari
f. proliferazione stremale
Lunico problema lo pu creare una variante del basalioma che il basalioma
cheratinizzato: produce cheratina (perle cornee) nonostante le cellule dello strato
basale si trovino ad uno stto precedente di differenziazione.
321
Tumori dei melanociti
Melanoma
Tumore relativamente comune e molto aggressivo,data la sua alta capacit
metastatica, che pu rendersi evidente anche dopo molto tempo.
presente generalmente sulla cute fotoesposta,cio in zone immediatamente visibili,
ma con una certa frequenza si localizza anche in altre sedi, di pi difficile diagnosi.
Queste sono:
- mucosa orale e anogenitale (parte terminale del retto)
- uvea ed occhio
- esofago
- SNC (meningi)
In questi casi naturalmente la diagnosi pi difficile ed il tm risulta pi aggressivo in
quanto risulta pi vicino alla vascolarizzazione; il risultato che il tm d metastasi
abbastanza rapidamente e la diagnosi viene fatta sulle metastasi stesse, dunque
secondariamente.
Il melanoma sempre maligno, ed la neoplasia cutanea letale pi frequente nella
maggior parte delle popolazioni occidentali, con una predisposizione nelle persone di
carnagione chiara.
In effetti lesposizione ai raggi solari sembra essere uno dei principali fattori
predisponenti allo sviluppo del tm: questa per provocare tumore deve essere acuta,
cio saltuaria ed intensa, non ripetuta non continuativa, non cronica.
In accordo con il ruolo eziologico dei raggi solari gli uomini presentano pi spesso
questo tumore nella parte superiore del dorso e le donne pi spesso negli arti inferiori
( perch portano le gonne).
Le cellule del melanoma sono solitamente prive di strutture specifiche e talmente
polimorfe da rendere la diagnosi di tumore davvero difficile, anche perch hanno
scarsa caratterizzazione fenotipica.
La diagnosi dunque, se il melanoma localizzato sulla cute, principalmente
ispettiva.
Una diagnosi precoce ed un intervento chirurgico possono eradicare pi del 30% dei
casi.
Attualmente per la valutare linteressamento metastatico dei linfonodi adiacenti al
tumore si utilizza la tecnica del linfonodo sentinella:
- iniezione di tracciante nella sede del tumore
- si preleva solo il primo linfonodo pi vicino al tumore
- se questo interessato da metastasi, si prosegue al successivo,altrimenti si
interrompono prelievi.
Una volta si faceva uno svuotamento chirurgico linfonodale completo della sede
interessata dal tumore: questo metodo consente invece di prelevare solo i linfonodi
realmente coinvolti metastaticamente.
322
Lescissione dei linfonodi coinvolti metastaticamente utile per fermare la diffusione
metastatica per via linfatica del tumore: il problema rimane nel fatto che questo
tumore diffonde anche per via ematica.
Questo tumore insorge prevalentemente nellet adulta.
Se presente nellinfanzia o nelladolescenza associato a fattori di rischio particolari:
- xeroderma pigmentoso ( minore riparazione del DNA)
- nevo a costume da bagno ( bathing sun nevus)
- sindrome del nevo displastico familiare: nevi di dimensioni maggiori rispetto
alla maggior parte dei nevi acquisiti ( >di 5 mm.), che possono insorgere sotto
forma di centinaia di lesioni sulla superficie neoplastica.
Il melanoma pu formarsi:
3) de novo
4) da nevo melanocitico congenito o acquisito pre-esistente
5) da un nevo blu: nevo superficiale ma che interessa anche il derma tanto
da avere un colorito molto intenso, bluastro
Le cause della formazione del melanoma vengono principalmente ad essere:
- esposizione intensa e saltuaria ai raggi UV (in particolare quelli con lunghezza
donda di 290-320nm.)
- fattori predisponesti genetici
- fattori predisponesti razziali:
I maschi sono sempre pi colpiti delle femmine, ed in essi la mortalit maggiore.
Il melanoma ha una presentazione clinica precoce, come nevo alterato.
Infatti mentre qualsiasi nevo, acquisito o congenito, viene a costituire una neoplasia
benigna a partire dai melanociti, il melanoma viene invece ad essere sempre maligno.
Per evidenziare un nevo che abbia subito trasformazione in senso maligno si utilizza la
regola dellABCDE.
A asimmetria: il nevo dunque cambia forma e da regolare diviene asimmetrico.
B bordo: il margine diviene irregolare
Ccolore: la pigmentazione diviene irregolare ed a volte vi sono anche delle
apigmentosi
Ddiametro: assume un diametro maggiore di 5mm.
Eelevation: assume maggiore rilevatezza, il che testimonia un passaggio dagli strati
superficiali a quelli profondi.
Nel termine melanoma sono incluse diverse entit clinico-patologiche, cio diverse
lesioni con caratteristiche cliniche e fisiologiche che si differenziano dalle altre.
In senso generale il melanoma viene a presentare sempre due fasi di crescita:
a. fase a crescita radiale: lesione proliferativi in situ e limitata
allepidermide. A volte pu essere associata ad una microinvasione del
derma. Questa la prima fase, meno aggressiva del tm, da cui il tm pu
323
anche regredire. Successivamente alla regressione, tuttavia il tm pu
recidivare e ripresentarsi, gi in fase di crescita verticale
b. fase a crescita verticale: invasiva, verso la profondit del derma. Pu
metastatizzare.
Fase a crescita radiale
Crescita indolente, ma progressiva
Non si pu avere metastatizzazione, ma al massimo microinvasione, cio invasione
locale del derma papillare ( strato del derma pi superficiale, lasso e popolato da
cellule; confina con il sottostante derma reticolare, pi denso e fibroso, separato da
esso da vasi sanguigni).
Liperproliferazione tra le cellule del derma papillare, se presente anche detta
melanosi pre-cancerosa o iperplasia aplastica atipica.
In questa fase il tm pu regredire, dando luogo alla formazione di cicatrici fibrose nelle
aree di regressione, oppure pu andare incontro a progressione verso la fase a crescita
verticale.
Istologia
Si hanno melanociti chiari, singoli o in piccoli gruppi, che tendono ad essere presenti
in tutti gli strati dellepidermide, fino allo strato corneo.
I melanociti, che normalmente sono cellule dendritiche, divengono:
- cellule epitelioidi: perdono la loro conformazione specifica e vengono ad
assomigliare morfologicamente sempre di pi alle cellule dellepitelio
- cellule con atipica uniforme: solitamente si hanno cellule pi grandi, con nucleo
irregolare e polimorfo, ipercromatismo, dovuto alladdensamento della
cromatina alla prf della mbr nucleare, mitosi rare nellepidermide, ma presenti
in un terzo dei casi nel derma, segno di un iniziale passaggio alla fase verticale.
Lepidermide si presenta irregolarmente ispessita.
Si ha sempre infiltrato infiammatorio, che si dispone a bande: questa presenza
testimonia la reazione dellorganismo, che pu portare anche a regressione del tumore
necessaria la DD con il nevo displastico che per presenta
- atipia casuale: non tutte le cellule sono uniformemente atipiche
- regolare allungamento delle papille
- infiltrato infiammatorio pathly e solitamente piuttosto scarso
- assenza di regressione (fibrosi) e mitosi.
Fase a crescita verticale
Il tm acquisisce la capacit di proliferazione ed invasione del derma: si ha discesa delle
cellule neoplastiche e loro attraversamento della mbr basale.
324
La neoplasia pu estendersi verso lesterno, provocando una lesione nodulare, rilevata
( melanoma nodulare, che una delle entit clinico-patologiche e che nasce gi nello
stato di crescita verticale, senza passare la fase radiale).
Si possono avere possibili metastasi a distanza
Il nodulo che si viene a formare pu:
- essere pigmentato o amelanotico ( condizione di pi difficile diagnosi)
- pu ulcerare e sanguinare: questo un segno da tenere in grossa considerazione
Vi possono essere metastasi:
- cutanee nella zona intorno al linfonodo(satellitosi)
- nei linfonodi regionali
- a distanza (SNC)
Istologia e citologia
Le cellule vengono ad essere epiteiliodi o fusate, simili a cellule mesenchimali (DD con
sarcoma).
Le atipie cellulari coinvolgono soprattutto il nucleo e sono costanti ed evidenti:
- mitosi aberranti, molto frequenti per la proliferazione esasperata delle cellule
- pseudoinclusioni nucleari: i nuclei sono a tale punto alterati e polimorfi, che
nella sezione pu sembrare che allinterno del nucleo vi siano aree di
citoplasma.
Fenotipo
Questo tipo di tumore presenta:
a. marker aspecifici: vimentina ( marker delle cellule mesenchimali), S-100,
marker delle cellule di derivazione dalla cresta neurale.
b. marker specifici : HMB45 e MART-1. Questi marker possono essere a
volte poco positivi e dunque limmunofenotipizzazione pu essere poco
utile. A questo punto necessario fare ricorso al microscopio elettronico:
infatti nelle cellule neoplastiche di derivazione melanocitica, nonostante
tutte le alterazioni sempre identificabile e presente nel citoplasma il
melanosoma, organulo tipico dei melanociti. Tuttavia nelle neoplasie
molto indifferenziate anche il melnosoma diviene atipico.
Melanoma: stadiazione
Questa di enorme rilievo per stabilire lapproccio terapeutico pi opportuno.
La stadiazione tiene conto di diversi fattori:
a. spessore: quanto discende volumetricamente il tm a partire dallo strato
granuloso oppure a quale strato della cute giunge. Criterio di
fondamentale importanza per il patologo
325
b. invasione linfonodale: rilevata mediante la tecnica del linfonodo
sentinella
c. ulcerazione
d. sede delle metastasi: satellitosi, linfonodi regionali, o metastasi a
distanza
e. valori della DHL: lattico-deidrogenasi
Melanoma: entit clinico-patologiche
a. lentigo maligna lentigo maligna melanoma
b. melanoma maligno a crescita superficiale
c. melanoma maligno acrale lentigginoso
d. melanoma nodulare
Lentigo maligna
Lesione pigmentata, soprattutto nella cute dellanziano (60-70 anni) danneggiata
cronicamente da raggi UV.
Si localizza soprattutto sulle tempie e sulla fronte
Ha crescita estremamente lenta: impiega 10-15 anni prima dello sviluppo della lesione
aggressiva
Non ha capacit metastatica e rimane in situ.
Morfologia.
una macula piatta, a margini irregolari, gradualmente in estensione, variamente
pigmentata, ma spesso con aree di depigmentazione che possono corrispondere alle
aree di regressione
Istologia.
Caratterizzata da melanociti:
- displastici: soprattutto nello strato basale
- atipici: che per continuano a mantenere la forma dendritica
- con organizzazione a palizzata
- che possono coinvolgere lepitelio degli annessi cutanei ( tutti gli epiteli
contengono melanociti)
Questo tipo di neoplasia pu insorgere primitivamente anche nel tratto
gastrointestinale, nel SNC, a partire da cellule indifferenziate, ma derivanti comunque
dalla cresta neurale.
Lepidermide interessata risulta atrofica, con presenza spesso di elastosi solare.
326
Lentigo maligna melanoma
Le cellule sono assolutamente atipiche ed anomale.
Il tm ha acquisito capacit invasiva del derma, che pu esplicarsi in diversi punti (
invasione multifocale).
Melanoma maligno a crescita superficiale
lentit clinico-patologica di pi comune riscontro.
Insorge pressoch in uguale misura nei maschi e nelle femmine, ma con diversa
localizzazione: nei maschi con localizzazione prevalente al dorso, nelle femmine agli
arti inferiori.
Morfologia.
Macula o placca piatta, desquamata, con tendenza ad assumere aspetto nodulare ( il
nodulo rappresenta il passaggio alla fase di crescita nodulare).
La forma irregolare e la pigmentazione variabile.
Pu dare problemi di DD con il carcinoma basocellulare, con il carcinoma
spinocellulare e con neoplasie non maligne: un criterio di differenziazione utile pu
risiedere nel ricordare la regola dellABCDE, ed il fatto che queste alterazioni
insorgono de novo, o a causa di un nevo pre-esistente.
Ci sono varianti amelanotiche o ipopigmentate, con aree edematose
Istologia
Le cellule sono fortemente atipiche:
- epitelioidi: indifferenziate a tale punto da avere perso ogni prolungamento ( a
differenza della lentigo-maligna) e da assomigliare alle cellule epiteliali.
- Citoplasma abbondante
- Nucleo pleomorfo e vescicoloso
- Nucleoli prominenti ( abbondante proliferazione)
- Numerose mitosi
Le cellule non riangono singole, ma si raggruppano in nidi.
Nella prima fase questi nidi cellulari invadono tutto lo spessore dellepidermide
Nella seconda fase questi nidi cellulari discendono verticalmente verso il derma, con
conseguenza presenza di mitosi nel derma medesimo.
Si ha acantosi: notevole proliferazione ed ispessimento dello strato malpighiano
Si ha appiattimento della rete epidermica delle creste.
Melanoma maligno acrale lentigginoso
Denominato:
327
- acrale: perch si localizza prevalentemente alle estremit. Cresce a livello della
pianta del piede o nel dorso delle mani. Le lesioni sono pi aggressive in queste
zone del corpo perch:
in queste regioni la cute e pi sottile e dunque c una maggiore
vicinanza dei melanociti alla vascolarizzazione
in queste regioni vi unirritazione meccanica, uno sfregamento
continuo, che induce la continua rigenerazione epiteliale
in queste regioni unispezione pi difficile
- lentigginoso: perch cresce come la lentiggine, per estensione in modo parallelo
allepidermide.
Si tratta di uniperplasia dellepidermide, con tendenza allinvasione del derma da
parte delle cellule neoplastiche, formanti nidi giunzionali.
Le cellule neoplastiche sono melanociti atipici, dendritici o epitelioidi, a volte giganti,
localizzati nella regione basale dellepidermide.
Si ha invasione a cellule fusate con desmoplasia: dunque nel momento in cui
penetrano nel derma le cellule divengono simil mesenchimali e si ha associazione della
presenza di cellule neoplastiche con aumento dello stroma connettivale- collagenico.
Si ha acantosi.
Melanoma maligno nodulare
Questo melanoma caratteristico per mancare della fase di crescita radiale: esso nasce
nella fase di crescita verticale e questo rende la sua prognosi pi infausta.
pi frequente nei maschi che nelle femmine con un rapporto 2:1
Insorge in et adulta-anziana: 50-60 anni, prevalentemente al tronco e agli arti.
Morfologia.
Aspetto nodulare o polipoide, profondo nel derma.
Molto vascolarizzato e spesso ulcerato.
Pu essere anche amelanotico
Questo insieme di caratteristiche pone il problema della DD con una neoplasia
vascolare.
Non essendoci la fase di crescita radiale non vi sono cellule neoplastiche a livello
dellepidermide.
Istologia
Vi sono diversi possibili tipi cellulari in questo tipo di melanoma:
- cellule epitelioidi:
di dimensioni maggiori
rotonde
con pigmentazione variabile
328
con nucleo vescicoloso ed altamente polimorfo ( presenza di
pseudoinclusioni)
nucleolo prominente (elevata proliferazione)
mitosi atipiche
- cellule fusate
ovalari
con processi citoplasmatici
simili alle cellule mesenchiamali del tutto indifferenziate
- cellule giganti
sono le cellule con massimo grado di indifferenziazione e
conseguente perdita di fnz, che costituiscono forse la tappa comune
di tutte le neoplasie pi maligne. Dunque in questo caso causano il
problema di una DD con metastasi, sarcoma, linfoma anaplastico.
Linfiltrato infiammatorio accompagna sempre il tumore
Diagnosi
La dg particolarmente difficile perch spesso si hanno forme cos indifferenziate che
vengono perse le caratteristiche fenotipiche ed a volte la cellula neoplastica esprime
antigeni per i quali non positiva.
Il campione viene dunque esaminato con diverse modalit fra cui, di fondamentale
rilevanza clinica, risulta quella ultrastrutturale al microscopio elettronico, poich,
come si gi cisto, anche al massimo grado di indifferenziazione queste cellule
contengono melanosomi, anche se talvolta alterati (melanosomi granulari per
esempio).
La diagnosi si fa pi difficile:
- in caso di lesione apigmentata
- se si fa diagnosi delle metastasi secondarie del melanosoma orbita
cavit nasale ed orale
vulva, vagina, uretra, regione anale
raramente: meninge, esofago, stomaco, mammella, bronchi,
surrenale
in questi casi inoltre la prognosi sempre infausta perch il
tumore ha gi metastatizzato in aree altamente vascolarizzate,
dove pu svilupparsi con maggiore aggressivit.
Fattori prognostici
- diagnosi istologica; per stabilire di quale entit clinico-patologica stiamo
parlando
- fase di crescita (radiale o verticale)
- spessore: deve essere quantificato esattamente
- livello di invasione: a quale strato giunto il tumore
329
- mitosi: quantifica la capacit proliferativi del tumore
- presenza o assenza di regressione che generalmente si trova associata alla
presenza di infiltrato infiammatorio
- apoptosi: rappresenta un segno di autolimitazione del tumore: un tumore con
una mutazione di p53 andr incontro ad apoptosi con molta maggiore difficolt e
dunque sar pi aggressivo
- EGFR: recettore per EGF (Epidermal Grow Factor). Molti tumori iperesprimono
EGFR anche in assenza di segnale trascrizionale oppure addirittura hanno
amplificazione del gene che codifica per EGFR. EGFR viene dunque ad essere
pi presente e viene ad essere attivato cosituzionalmente, senza bisogno di un
ligando, con conseguente attivazione di una casacta di segnali che porta anche
alla produzione di oncogeni.
N.B. esistono farmaci di nuova generazione, inibitori delle Tyr chinasi, come EGFR,
che vengono utilizzati (es. nel carcinoma polmonare) ed agiscono selettivamente solo
sulle cellule neoplastiche, senza molti degli effetti collaterali dei farmaci di vecchia
generazione.
Livelli di invasione (classificazone di Clark)
Lo spessore del tm viene quantificato in base allo strato che raggiunge:
- livello 1: melanoma maligno in situ
- livello 2: raggiungimento del derma papillare con cellule singole
- livello 3: invasione dellinterfaccia dermica, cio dellarea del plesso capillare,
tra derma papillare e reticolare
- livello 4: invasione del derma reticolare
- livello 5: invasione del tessuto adiposo sottocutaneo: qui vi massima invasivit
perch vi sono i vasi di maggiore calibro e le strutture nervose
Volume della neoplasia (classificazione di Breslow)
il fattore diagnostico singolo della classificazione del melanoma a crescita verticale.
Si misura dallo strato granuloso superficiale al pi profondo punto di invasione del
derma
- IA <1 mm. (sopravvivenza a 7 anni: 95%)
- IB ( basso richio ) <1, 69mm. (sopravvivenza a 7 anni: 88%)
- II ( medio rischio ) 1,70-3,99mm. (sopravvivenza a 7 anni: 61%)
- III ( alto rischio ) > 4mm. (sopravvivenza a 7 anni: 32%)
330
Potrebbero piacerti anche
- Interna PDFDocumento281 pagineInterna PDFFrancesco LanzaNessuna valutazione finora
- FISIOPATOLOGIADocumento20 pagineFISIOPATOLOGIAVictoria OstahiiNessuna valutazione finora
- Cardiologia Cardiochirurgia Chirurgia Vascolare PDFDocumento286 pagineCardiologia Cardiochirurgia Chirurgia Vascolare PDFvincenzo argentatoNessuna valutazione finora
- Dispensa Marzullo - Serio AP1 PDFDocumento99 pagineDispensa Marzullo - Serio AP1 PDFUmberto CarbonaraNessuna valutazione finora
- Le Malattie CardiovascolariDocumento11 pagineLe Malattie CardiovascolariLauraNessuna valutazione finora
- Aterosclerosi - Disturbi Dell'apparato Cardiovascolare - Manuali MSD Edizione ProfessionistiDocumento8 pagineAterosclerosi - Disturbi Dell'apparato Cardiovascolare - Manuali MSD Edizione ProfessionistiGiovanni CannataNessuna valutazione finora
- ANAPAT CardiovascolareDocumento25 pagineANAPAT CardiovascolaremariNessuna valutazione finora
- Aula Hemodinamica PatologiaDocumento6 pagineAula Hemodinamica PatologiaJuliana MoreiraNessuna valutazione finora
- Appunti Lezioni Malattie CardiocircolatorieDocumento35 pagineAppunti Lezioni Malattie CardiocircolatorieMariarita Di BenedettoNessuna valutazione finora
- AneurismiDocumento8 pagineAneurismiElena RalucaNessuna valutazione finora
- Trombofilia - Lab Tests Online-ITDocumento23 pagineTrombofilia - Lab Tests Online-ITJonasNessuna valutazione finora
- Cardiopatia IschemicaDocumento23 pagineCardiopatia IschemicamariopetraccaNessuna valutazione finora
- ANGIOLOGIADocumento25 pagineANGIOLOGIAFedericoPppzPippoNessuna valutazione finora
- Moroni ModificatoDocumento66 pagineMoroni ModificatoGiuseppe FoggiaNessuna valutazione finora
- 32 Shock IpovolemicoDocumento13 pagine32 Shock IpovolemicoRiccardo IntruglioNessuna valutazione finora
- Cardiopatia IschemicaDocumento67 pagineCardiopatia Ischemicagiuseppesaba100% (1)
- LP StemiDocumento28 pagineLP StemiwheikapNessuna valutazione finora
- App. CardiocircolatorioDocumento180 pagineApp. CardiocircolatorioguglioNessuna valutazione finora
- LeucemiaDocumento3 pagineLeucemiaStefano LegambitNessuna valutazione finora
- Appunti Di Patologia - InvecchiamentoDocumento3 pagineAppunti Di Patologia - InvecchiamentoChloe BujuoirNessuna valutazione finora
- PatologieDocumento12 paginePatologiemarcoNessuna valutazione finora
- 0149.RC - Crush Syndrome e RabdomiolisiDocumento4 pagine0149.RC - Crush Syndrome e RabdomiolisinoloudnessNessuna valutazione finora
- 7 Ischemia IntestinaleDocumento13 pagine7 Ischemia IntestinaleStefania HasanajNessuna valutazione finora
- Lezione 9 - ArteriosclerosiDocumento106 pagineLezione 9 - ArteriosclerosilucaNessuna valutazione finora
- VasiDocumento12 pagineVasiLADYOSCARNessuna valutazione finora
- Patologia Generale Disturbi Di CircoloDocumento24 paginePatologia Generale Disturbi Di Circolobaum14Nessuna valutazione finora
- Patologia CellulareDocumento11 paginePatologia CellularemarinaNessuna valutazione finora
- CARDIO SBOB 10 MessinaDocumento18 pagineCARDIO SBOB 10 MessinaAlessandro PalmaNessuna valutazione finora
- I Parte ATEROSCDocumento65 pagineI Parte ATEROSCMariarita Di BenedettoNessuna valutazione finora
- Fisiopatologia - ShockDocumento6 pagineFisiopatologia - ShockandreaNessuna valutazione finora
- Cardiologia HackmedDocumento103 pagineCardiologia HackmedGiuseppe Di BartoloNessuna valutazione finora
- Shock Settico, Neurogeno, Termico, Anafilattico e CardiogenoDocumento44 pagineShock Settico, Neurogeno, Termico, Anafilattico e CardiogenomaxNessuna valutazione finora
- Cardiopatia Ischemica Nell'anzianoDocumento8 pagineCardiopatia Ischemica Nell'anzianoCarla OlivieroNessuna valutazione finora
- Embriologia CardiovascolareDocumento6 pagineEmbriologia CardiovascolaremenafabNessuna valutazione finora
- Insufficienza Celiaco MesentericaDocumento12 pagineInsufficienza Celiaco MesentericaBarbara Melchioretto100% (1)
- EndocarditiDocumento9 pagineEndocarditiasdNessuna valutazione finora
- 5-Stenosi MitralicaDocumento8 pagine5-Stenosi MitralicaScribdNixNessuna valutazione finora
- Chirurgia VascolareDocumento23 pagineChirurgia VascolareTeresa CozzolinoNessuna valutazione finora
- Fisiopatologia Chirurgica PT.1Documento35 pagineFisiopatologia Chirurgica PT.1FedericoPppzPippoNessuna valutazione finora
- Appunti Di NeuroradiologiaDocumento8 pagineAppunti Di NeuroradiologiaCarlotta ArturiNessuna valutazione finora
- Laporan Pendahulua TrombositopeniDocumento16 pagineLaporan Pendahulua TrombositopeniNovi YuliantiNessuna valutazione finora
- Dispensa AP Cardio-GastroDocumento244 pagineDispensa AP Cardio-GastroMatteo PaluccioNessuna valutazione finora
- Malattie CerebrovascolariDocumento8 pagineMalattie CerebrovascolariEmiliano ManginoNessuna valutazione finora
- Sistema CardiovascolareDocumento11 pagineSistema CardiovascolareBruce WiiNessuna valutazione finora
- FisiopatologiaDocumento23 pagineFisiopatologiaFilippo BiondiNessuna valutazione finora
- CuoreDocumento51 pagineCuoreMichele Cacìa Karol RanieriNessuna valutazione finora
- IctusDocumento11 pagineIctusEnrico CarrettaNessuna valutazione finora
- Lezione 5Documento48 pagineLezione 5Devian ArtNessuna valutazione finora
- Ematomi SubduraliDocumento8 pagineEmatomi SubduralimontparnasseNessuna valutazione finora
- Le AnemieDocumento3 pagineLe AnemiemaddalenaNessuna valutazione finora
- Semeiotica Chirurgica - ShockDocumento15 pagineSemeiotica Chirurgica - ShockMarco CellaNessuna valutazione finora
- Cardiopatia Ischemica Di DonatoDocumento91 pagineCardiopatia Ischemica Di DonatoGiuliadarioNessuna valutazione finora
- EmatologiaDocumento16 pagineEmatologiadiviNessuna valutazione finora
- Appunti Di Fisiologia CardiovascolareDocumento17 pagineAppunti Di Fisiologia CardiovascolareTiziana De FeliceNessuna valutazione finora
- Aneurismi, Dissezioni, ArteropatieDocumento17 pagineAneurismi, Dissezioni, ArteropatieBeatrice ColottiNessuna valutazione finora
- Sistema Cardio CircolatorioDocumento18 pagineSistema Cardio Circolatoriosabah mihratNessuna valutazione finora
- CardiovascularDocumento35 pagineCardiovascularCamila rataNessuna valutazione finora
- La microcircolazione del sangue 101: La prossima generazione dell'assistenza sanitariaDa EverandLa microcircolazione del sangue 101: La prossima generazione dell'assistenza sanitariaNessuna valutazione finora
- Determinazione del fenotipo e del profilo apoptotico delle cellule endoteliali circolanti e dei loro progenitori mediante citofluorimetria a flusso: una possibile applicazione in ambito oncologicoDa EverandDeterminazione del fenotipo e del profilo apoptotico delle cellule endoteliali circolanti e dei loro progenitori mediante citofluorimetria a flusso: una possibile applicazione in ambito oncologicoNessuna valutazione finora
- Diagnostica Per Immagini Con Note - ZannoliDocumento175 pagineDiagnostica Per Immagini Con Note - ZannolisoniablaireNessuna valutazione finora
- Nefrologia CompletoDocumento108 pagineNefrologia CompletosoniablaireNessuna valutazione finora
- 2013 Igiene Generale-Epidemiologia PDFDocumento57 pagine2013 Igiene Generale-Epidemiologia PDFsoniablaireNessuna valutazione finora
- Ipertensione EndocrinaDocumento6 pagineIpertensione EndocrinasoniablaireNessuna valutazione finora