Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Sintesi Dell'Ammoniaca
Caricato da
Vincenzo MatarangoloCopyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Sintesi Dell'Ammoniaca
Caricato da
Vincenzo MatarangoloCopyright:
Formati disponibili
Capitolo
scheda
Reazioni chimiche:
velocit ed equilibrio
La sintesi dellammoniaca
Una delle reazioni pi importanti tra quelle messe a punto dai chimici nel secolo
scorso la sintesi dellammoniaca. La reazione di sintesi a partire dai due elementi
rappresenta senzaltro il modo pi conveniente per produrre questa sostanza, data la
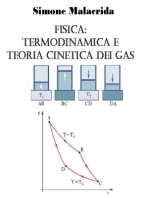
grande disponibilit di azoto, presente in abbondanza nellaria, e la possibilit di ottenere idrogeno attraverso diversi metodi. La sintesi dellammoniaca ci sembra possa riassumere efficacemente i vari aspetti delle reazioni chimiche e di essi si deve tenere conto quando viene prodotta a livello industriale (figura 1).
produzione della miscela di reazione
produzione dellammoniaca
N2 , H2 , CO2
NH3 , N2 , H2
scambiatore
di calore
CH4 , H2O
O2 , N2
H2O
aria
catalizzatore
500 C
compressore
N2 , H2 , CO
materiali di
partenza
catalizzatore
450 C
300 bar
H2O
N2 , H2
NH3
N2 , H2
CO2 , H2O
convertitore
lavaggio
sotto pressione
serbatoio
dellammoniaca
reattore
di sintesi
separazione
dellammoniaca
Scriviamo innanzi tutto lequazione della reazione e la relativa espressione della costante di equilibrio
N2(g) 1 3 H2(g) N 2 NH3(g) 1 q
[NH3]2
Keq 5
[H2]3 [N2]
A temperatura ambiente (25 C) il valore della costante molto alto (Keq 5 4,05 108)
e ci farebbe pensare che i reagenti (mescolati nei giusti rapporti stechiometrici) reagiscano quasi completamente. Nella realt non cos: se si immettono questi due gas
in un recipiente chiuso, non si rileva presenza di ammoniaca, neanche dopo mesi o
addirittura anni! Ci dovuto al fatto che a questa temperatura la velocit della reazione talmente bassa che, in pratica, la reazione non parte neppure.
Per aumentare la velocit della reazione si pu allora innalzare la temperatura,
ma dato che la reazione diretta esotermica, ci fa spostare lequilibrio a sinistra: infatti a 450 C la Keq scende fino a 2,74 1021. In altre parole, aumentando la temperatura si raggiunge pi rapidamente lequilibrio ma la percentuale di prodotti diventa
molto piccola, cio la resa troppo bassa (tabella 1).
Tabella 1 Un aumento di temperatura provoca un aumento della velocit di sintesi dellammoniaca.
Contemporaneamente, per, il valore di Keq e quindi la resa della reazione diminuisce molto.
Temperatura
Keq
Velocit
25 C
4,05 ? 10
450 C
2,74 ? 10
alta
700 C
2,02 ? 1022
molto alta
8
21
molto bassa
Figura 1 Il metodo per ottenere
lammoniaca fu messo a punto negli
anni della Prima guerra mondiale ed
ebbe impulso proprio per motivi bellici.
Lammoniaca, infatti, una materia
prima fondamentale per produrre acido nitrico e, da questo, gli esplosivi.
Venuto meno lapprovvigionamento
dei giacimenti naturali dei composti
azotati cileni (il cosiddetto salnitro o
nitrato del Cile), che rappresentavano
praticamente lunica fonte per produrre su larga scala lacido nitrico, si svilupp rapidamente il processo di sintesi a partire dallidrogeno e dallazoto.
Fortunatamente questa stessa invenzione fu messa a frutto per scopi pacifici e viene utilizzata oggi per produrre
molti materiali di grande utilit (urea,
fertilizzanti agricoli, fibre tessili, sali
dammonio eccetera).
Per saperne di pi
------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------Lazoto il principale componente
------------------------------------------------------------------------------------dellaria, ma la maggior parte degli
------------------------------------------------------------------------------------organismi viventi non in grado di
------------------------------------------------------------------------------------assimilarlo direttamente per forma------------------------------------------------------------------------------------re le proteine. Solo alcuni batteri
-------------------------------------------------------------------------------------
che vivono in simbiosi con le radici
-------------------------------------------------------------------------------------
delle leguminose possono svolgere
-------------------------------------------------------------------------------------
questa funzione. La maggior parte
-------------------------------------------------------------------------------------
delle piante assorbe lazoto solo se
-------------------------------------------------------------------------------------
presente come ione nitrato o, an-------------------------------------------------------------------------------------
cor meglio, come ione ammonio.
-------------------------------------------------------------------------------------
Bagatti, Corradi, Desco, Ropa, Scopriamo la chimica Zanichelli Editore
Capitolo
scheda
La sintesi dellammoniaca
Reazioni chimiche:
velocit ed equilibrio
Si tratta dunque di trovare una soluzione di compromesso tra due opposte esigenze.
Il chimico tedesco F. Haber, dopo numerose prove, decise di far funzionare gli impianti a una temperatura comunque abbastanza alta, intorno ai 400-500 C, per poter
contare su una velocit di reazione accettabile.
Per aumentare ancora la velocit del processo, Haber riusc a mettere a punto un
catalizzatore specifico e anche relativamente economico, il ferro. Furono quindi realizzate sottili reticelle di questo metallo (insieme a tracce di ossidi di ferro e di potassio) e con esse furono ricoperte le pareti interne del reattore in cui avviene la reazione tra idrogeno e azoto (figura 2).
H2
H2
Figura 2 Lazione del catalizzatore
nella reazione di sintesi dellammoniaca.
N2
H2
N
H
H
NH3
N
H
NH3
I protagonisti della scienza
Lo studio cinetico della sintesi dellammoniaca ha permesso di accertare che un passaggio decisivo del meccanismo di reazione costituito dalla rottura dei legami tra
gli atomi nella molecola di azoto: N2 N 2 N.
Il catalizzatore interviene proprio in questa fase: esso trattiene (o adsorbe) sulla
sua superficie le molecole di N2 e rende possibile la loro dissociazione in atomi, cos
come quella delle molecole di H2. Gli atomi liberi possono reagire cos pi rapidamente per formare le molecole di NH3 che non vengono trattenute dagli atomi di ferro e che si staccano dalla superficie. In questo modo i centri attivi del catalizzatore si
rendono liberi per adsorbire altre molecole di azoto e di idrogeno.
Nel processo di sintesi dellammoniaca cos catalizzato, la reazione raggiunge
lequilibrio in minor tempo. Naturalmente viene accelerata anche la reazione inversa.
Ma Haber riusc a migliorare ancora il rendimento economico del processo per altra via. Un passo decisivo per la definitiva messa a punto del processo fu compiuto
infatti quando, con lapporto fondamentale dellingegnere chimico tedesco Carl
Bosch, si riusc a costruire un impianto in grado di reggere pressioni elevate. Haber
infatti sapeva che in questo modo, sulla base del principio di Le Chtelier, lequilibrio della reazione di sintesi dellammoniaca si sposta nella direzione in cui diminuisce il numero di molecole, cio a destra.
Si riusc cos ad aumentare moltissimo la resa della reazione: infatti, operando
alla pressione di 300 bar, si trasforma in ammoniaca pi del 30% dei reagenti. Fu
cos possibile realizzare il primo grande impianto per la produzione chimica su larga
scala dellammoniaca, una materia prima fondamentale e una delle sostanze prodotte in maggiore quantit nel mondo.
Questo processo rappresenta oggi praticamente lunica fonte di ammoniaca prodotta nel mondo. Esso costituisce anche un modo intelligente di sfruttare una risorsa
pressoch illimitata (lazoto dellaria) per riuscire ad aumentare, attraverso luso di
fertilizzanti azotati, la produttivit dei terreni agricoli e soddisfare cos i bisogni alimentari di una buona parte dellumanit.
------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------Fritz Haber (1868-1934) nacque
------------------------------------------------------------------------------------a Breslavia (lattuale Wroclaw), fi------------------------------------------------------------------------------------glio di un commerciante ebreo te------------------------------------------------------------------------------------desco. Fin dallinizio della sua car------------------------------------------------------------------------------------riera tenne in gran conto la stretta
------------------------------------------------------------------------------------relazione tra tecnologia e scienza
------------------------------------------------------------------------------------pura e lesigenza di tenere legati
------------------------------------------------------------------------------------progresso scientifico e vita pratica.
------------------------------------------------------------------------------------Haber cominci i primi studi sulla
-------------------------------------------------------------------------------------
sintesi dellammoniaca fin dal
-------------------------------------------------------------------------------------
1904. Unendo conoscenze scienti-------------------------------------------------------------------------------------
fiche diverse (termodinamica, ci-------------------------------------------------------------------------------------
netica chimica, catalisi eteroge-------------------------------------------------------------------------------------
nea) e grazie agli sviluppi della
-------------------------------------------------------------------------------------
tecnologia, Haber riusc a mettere
-------------------------------------------------------------------------------------
a punto nel 1914 il processo che
-------------------------------------------------------------------------------------
porta il suo nome. Il successo delle
-------------------------------------------------------------------------------------
sue ricerche gli valse nel 1918 il
-------------------------------------------------------------------------------------
premio Nobel. Purtroppo Haber eb-------------------------------------------------------------------------------------
be un ruolo essenziale anche nello
-------------------------------------------------------------------------------------
sviluppo delle armi chimiche che la
-------------------------------------------------------------------------------------
Germania utilizz nella Prima guer------------------------------------------------------------------------------------ra mondiale.
-------------------------------------------------------------------------------------
Bagatti, Corradi, Desco, Ropa, Scopriamo la chimica Zanichelli Editore
Potrebbero piacerti anche
- Esercizi di fisica per licei: fluidodinamica e termodinamicaDa EverandEsercizi di fisica per licei: fluidodinamica e termodinamicaNessuna valutazione finora
- Esercizi di fisica: termodinamica e trasmissione del caloreDa EverandEsercizi di fisica: termodinamica e trasmissione del caloreNessuna valutazione finora
- SyngasDocumento15 pagineSyngasLuca MarlettaNessuna valutazione finora
- Impianti Turbine A VaporeDocumento41 pagineImpianti Turbine A VaporeantoniomambroNessuna valutazione finora
- Acido NitricoDocumento8 pagineAcido NitricoLuca MarlettaNessuna valutazione finora
- VII Esercitazione - Termodinamica Ed Equilibrio - ProcessiDocumento12 pagineVII Esercitazione - Termodinamica Ed Equilibrio - ProcessiMaddalenaNessuna valutazione finora
- Acido Nitrico - Chimica Industriale EssenzialeDocumento14 pagineAcido Nitrico - Chimica Industriale Essenzialepaola.cattozzoNessuna valutazione finora
- Polimi - UreaDocumento8 paginePolimi - Ureasalvatore raffaNessuna valutazione finora
- 3.steam CrackingDocumento10 pagine3.steam CrackingAngelo Francesco IovinoNessuna valutazione finora
- AmmoniacaDocumento32 pagineAmmoniacaOrazio MaffeiNessuna valutazione finora
- Storia Dell'ammoniacaDocumento8 pagineStoria Dell'ammoniacaBiagio CastronovoNessuna valutazione finora
- Appunti Ed Esercizi Di Fisica TecnicaDocumento0 pagineAppunti Ed Esercizi Di Fisica Tecnica43346080Nessuna valutazione finora
- UreaDocumento3 pagineUreaLuca MarlettaNessuna valutazione finora
- ORC BidiniDocumento6 pagineORC BidinilunettinoNessuna valutazione finora
- Ammonia ProdactionDocumento22 pagineAmmonia ProdactionetayhailuNessuna valutazione finora
- Epossidazione 1Documento4 pagineEpossidazione 1Alphonse TimeNessuna valutazione finora
- Tecnologia CasaleDocumento6 pagineTecnologia CasaleChristian TrujilloNessuna valutazione finora
- Nitrificazione A Biomasse SospeseDocumento46 pagineNitrificazione A Biomasse SospeseClaudio Della RoccaNessuna valutazione finora
- F Tecnica 18Documento7 pagineF Tecnica 18luigiNessuna valutazione finora
- Syngas WikipediaDocumento3 pagineSyngas WikipediaLuca MuscianeseNessuna valutazione finora
- 3 Chimica Industriale 22-09-22Documento33 pagine3 Chimica Industriale 22-09-22ana m pelegrin francoNessuna valutazione finora
- Marmitta CataliticaDocumento2 pagineMarmitta Cataliticasalvatore castagninoNessuna valutazione finora
- Esercizi Di Chimica e Stechiometria - 5Documento2 pagineEsercizi Di Chimica e Stechiometria - 5esterNessuna valutazione finora
- Zanichelli Bagatti Scopriamo Cap09 S Ammoniaca PDFDocumento2 pagineZanichelli Bagatti Scopriamo Cap09 S Ammoniaca PDFUmberto ManzaliniNessuna valutazione finora
- Acido AceticoDocumento35 pagineAcido AceticoAmalia RamunnoNessuna valutazione finora
- Alchini PDFDocumento5 pagineAlchini PDFdavidetrtNessuna valutazione finora
- 2 Syngas e IdrogenoDocumento10 pagine2 Syngas e IdrogenoAngelo Francesco IovinoNessuna valutazione finora
- Relazioni Chimica InorganicaDocumento2 pagineRelazioni Chimica InorganicaAngelo Ngiò Francesco IovinoNessuna valutazione finora
- MetanoloDocumento7 pagineMetanoloLuca MarlettaNessuna valutazione finora
- Chimica Industriale - Cinetica 09.02.2011Documento2 pagineChimica Industriale - Cinetica 09.02.2011Anonymous TsymIbNessuna valutazione finora
- Cap 8Documento32 pagineCap 8TrinchettoNessuna valutazione finora
- Hulme - La Protezione Di Generatori Di Vapore Industriale - Vol1di4Documento84 pagineHulme - La Protezione Di Generatori Di Vapore Industriale - Vol1di4Giovanni De CesareNessuna valutazione finora
- C7mtm06 PDFDocumento68 pagineC7mtm06 PDFLoredana MagdaNessuna valutazione finora
- 49815-Cap 9 - Impianti Turbogas PDFDocumento24 pagine49815-Cap 9 - Impianti Turbogas PDFLeonardo GirolamiNessuna valutazione finora
- Manuale Tecnico FIAMMDocumento19 pagineManuale Tecnico FIAMMAnonymous OQ9UN5kNessuna valutazione finora
- CaldaieDocumento37 pagineCaldaielabcompliance100% (1)
- La Produzione Di Idrogeno PDFDocumento10 pagineLa Produzione Di Idrogeno PDFcicciobellosNessuna valutazione finora
- 14963-Turbine A GasDocumento60 pagine14963-Turbine A GasalbpiraniNessuna valutazione finora
- Pirolisi PollinaDocumento6 paginePirolisi PollinaBruno PinNessuna valutazione finora
- Tabella Acciai (Pag 12) CementazioneDocumento15 pagineTabella Acciai (Pag 12) CementazioneZizuNessuna valutazione finora
- Acido NitricoDocumento10 pagineAcido NitricoPaola CattozzoNessuna valutazione finora
- Salomone IDocumento209 pagineSalomone ImimorealNessuna valutazione finora
- Ese5 6Documento18 pagineEse5 6Alessio ScarabelliNessuna valutazione finora
- Primus La SeccheriaDocumento58 paginePrimus La SeccheriaLauro BonanniNessuna valutazione finora
- Ciclo OttoDocumento4 pagineCiclo OttoSara BucciNessuna valutazione finora
- Gruppo#6 2Documento17 pagineGruppo#6 2readwidNessuna valutazione finora
- Aldehidos y CetonasDocumento63 pagineAldehidos y CetonasLEYTON HCNessuna valutazione finora
- 067 - KINDLE - ES - ASSORBIMENTO v2.0 Con GraficiDocumento14 pagine067 - KINDLE - ES - ASSORBIMENTO v2.0 Con GraficiMalec17Nessuna valutazione finora
- Esercizi 22 Dic Acili +redoxDocumento63 pagineEsercizi 22 Dic Acili +redoxalm43541Nessuna valutazione finora
- Volume Fumi StechiometriciDocumento10 pagineVolume Fumi StechiometriciLUCA BENEDETTINessuna valutazione finora
- REFORMING CataliticoDocumento34 pagineREFORMING CataliticoMauricio RamirezNessuna valutazione finora
- Relazione LCA FinaleDocumento18 pagineRelazione LCA FinaleVincenzoLuciNessuna valutazione finora
- Combustione Combustibili 1Documento69 pagineCombustione Combustibili 1bancomat2Nessuna valutazione finora
- Cicli InversiDocumento31 pagineCicli InversiLucia TuvèNessuna valutazione finora
- Riduzione Selettiva Catalitica - WikipediaDocumento3 pagineRiduzione Selettiva Catalitica - Wikipediapaola.cattozzoNessuna valutazione finora
- Quimica AlquiloDocumento20 pagineQuimica AlquiloDelia FloresNessuna valutazione finora
- Impianti Turbine A VaporeDocumento41 pagineImpianti Turbine A VaporeFederico MassaroNessuna valutazione finora
- Cicli CombinatiDocumento30 pagineCicli CombinatiNiccolò Giannotti100% (3)
- Andytonini - Industria Cloro Proc - SolvayDocumento4 pagineAndytonini - Industria Cloro Proc - Solvaymontie3Nessuna valutazione finora
- Fisica Campo El e MegnDocumento1 paginaFisica Campo El e MegnVincenzo MatarangoloNessuna valutazione finora
- La CreazioneDocumento4 pagineLa CreazioneVincenzo MatarangoloNessuna valutazione finora
- GIAPPONEDocumento3 pagineGIAPPONEVincenzo MatarangoloNessuna valutazione finora
- Programma GrecoDocumento1 paginaProgramma GrecoVincenzo MatarangoloNessuna valutazione finora
- UngarettiDocumento1 paginaUngarettiVincenzo MatarangoloNessuna valutazione finora
- La MarciaDocumento4 pagineLa MarciaVincenzo MatarangoloNessuna valutazione finora
- Marconi Chimica OrwellDocumento1 paginaMarconi Chimica OrwellVincenzo MatarangoloNessuna valutazione finora
- Filo SofiaDocumento2 pagineFilo SofiaVincenzo MatarangoloNessuna valutazione finora
- Orbitali IbridiDocumento3 pagineOrbitali IbridiVincenzo MatarangoloNessuna valutazione finora
- Mappe Concettuali MarxDocumento4 pagineMappe Concettuali MarxVincenzo MatarangoloNessuna valutazione finora
- Termini EconomiciDocumento8 pagineTermini EconomiciVincenzo MatarangoloNessuna valutazione finora
- BIOLOGIA I MuscoliDocumento2 pagineBIOLOGIA I MuscoliVincenzo MatarangoloNessuna valutazione finora
- Il Violino Uno Strumento SpecialeDocumento1 paginaIl Violino Uno Strumento SpecialeVincenzo MatarangoloNessuna valutazione finora
- DecapareDocumento6 pagineDecapareVincenzo MatarangoloNessuna valutazione finora
- Dieta Dello SportivoDocumento1 paginaDieta Dello SportivoVincenzo MatarangoloNessuna valutazione finora
- Progettare Strutture in CADocumento186 pagineProgettare Strutture in CAproprioio2Nessuna valutazione finora
- Appunti Geologia 2Documento20 pagineAppunti Geologia 2Touz91Nessuna valutazione finora
- Giuseppe Barzaghi - La Somma Teologica Di San Tommaso D'aquino in Un Soffio (0, Edizioni Studio Domenicano) PDFDocumento36 pagineGiuseppe Barzaghi - La Somma Teologica Di San Tommaso D'aquino in Un Soffio (0, Edizioni Studio Domenicano) PDFCarlos AlbertoNessuna valutazione finora
- Instruction Rayline R806Documento8 pagineInstruction Rayline R806Fresh94Nessuna valutazione finora
- B12CN DN en FN GN HN - 5679853Documento4 pagineB12CN DN en FN GN HN - 5679853Habib KaddachiNessuna valutazione finora
- La Crisi Dei Fondamenti Della MatematicaDocumento10 pagineLa Crisi Dei Fondamenti Della MatematicalegedoNessuna valutazione finora