Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
La Produzione Di Idrogeno PDF
Caricato da
cicciobellosTitolo originale
Copyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
La Produzione Di Idrogeno PDF
Caricato da
cicciobellosCopyright:
Formati disponibili
La produzione di idrogeno
Dott. Samuel Stucki Settore Energia Generale Paul Scherrer Institut 5232 Villigen PSI
1. Introduzione Il metodo pi semplice per produrre idrogeno consiste nel far reagire un metallo con un acido. Chi non ricorda ai tempi della scuola l'esperimento in cui l'insegnante versava dello zinco in un po' di acido cloridrico? Sui granelli di zinco si sviluppava un gas che l'insegnante, se era coraggioso, incendiava... La reazione chimica che si produce sui granelli di zinco la seguente: Zn + HCl ZnCl2 + H2 L'altro esperimento classico quello del bicchiere contenente acido solforico in cui sono immersi due fili. Quando i fili vengono collegati a una comune pila per lampadine tascabili, sul polo negativo si forma idrogeno e su quello positivo ossigeno, in un rapporto di 2:1. La corrente elettrica ha scisso l'acqua (H2O) nei suoi elementi H2 e 1/2 O2. La quantit di materia prima H2O per la produzione di idrogeno presente sulla terra enorme (circa 1 500 000 000 000 000 di tonnellate) e il suo grado di purezza migliore di quello di qualsiasi altra sostanza (l'acqua del mare composta per il 96% di H2O e l'acqua di sorgente addirittura per il 99,95%!). I presupposti tecnici per la produzione di idrogeno sono quindi ideali. Per ottenere idrogeno dall'acqua, tuttavia, necessaria energia di elevato valore, ad esempio sotto forma di energia chimica, come quella contenuta nello zinco metallico, o di energia elettrica, come nel caso dell'elettrolisi. Il problema della produzione di idrogeno appunto rappresentato dall'energia.
2. Produzione di idrogeno ed energia Per scindere l'acqua nei suoi elementi necessaria un'energia pari ad almeno 286 kJ/mol. Questa energia non va persa, ma pu essere ricuperata tramite la combustione dell'idrogeno. In altre parole, immagazzinata sotto forma di idrogeno. questa l'idea di fondo dell'impiego dell'idrogeno nella tecnica energetica. Come mostra la figura 1, per produrre una data quantit di idrogeno partendo dalla materia prima acqua occorre fornire un'energia (freccia verticale) uguale o maggiore al potere calorifico dell'idrogeno. Ci scaturisce dal primo principio della termodinamica (principio di equivalenza). Nei sistemi reali, per, a causa delle perdite di calore la quantit di energia necessaria sempre superiore al 100%.
La termodinamica chimica considera inoltre una funzione G (entalpia libera) che deriva dal secondo principio e indica le quote di energia di reazione da fornire al processo sotto forma di calore e di lavoro (ad esempio energia elettrica o luce). G una funzione della temperatura: a temperatura ambiente, ad esempio, per scindere l'acqua liquida l'83% dell'energia di reazione deve essere energia elettrica, mentre a 1000C tale quota scende a 65%. La scissione dell'acqua unicamente tramite calore possibile solo attorno ai 3000C, una temperatura a cui tecnicamente difficile lavorare. Per questo motivo, la produzione diretta di idrogeno partendo dall'acqua realizzabile solo per elettrolisi dell'acqua o tramite reazioni fotochimiche *) . Al giorno d'oggi, l'elettrolisi dell'acqua l'unica soluzione tecnicamente possibile per ottenere idrogeno dall'acqua (v. presentazione del Dr. Sioli).
150
H (%)
100
Wasserspaltung Heizwert von H2 = 100%
50
H2 H2O H2O H2 + O2
Fig. 1: Diagramma energetico semplificato dell'elettrolisi dell'acqua. L'intero potere calorifico dell'idrogeno viene portato dall'esterno. Si considera che l'acqua ha potere calorifico uguale zero.
*) Nel passato non sono mancati i tentativi di ottenere idrogeno dall'acqua con l'ausilio della luce solare, senza far ricorso
all'energia elettrica. Questa relazione non si sofferma sulle attivit di ricerca in questo campo. Il sogno della fotosintesi artificiale, comunque, non ancora stato realizzato.
150
H (%)
100
Methan Reformierung Heizwert von H2 = 100%
50
CH4 H2
0
CH4 + 2 H2O 4 H2 + CO2
Fig. 2: Diagramma energetico semplificato del "reforming" di metano mediante vapore. Il potere calorifico dei prodotti di partenza (metano + acqua) corrisponde al 78% di quello dei prodotti finali (idrogeno e anidride carbonica). La differenza viene fornita nel processo sotto forma di calore.
La figura 2 mostra il diagramma semplificato della produzione di idrogeno partendo da metano (gas naturale). In questa reazione il metano (CH4) viene trasformato in idrogeno e CO2 in due fasi (non visibili nella figura 2), tramite l'apporto di vapore acqueo. Anche questa reazione richiede energia, che viene tuttavia fornita in gran parte (quasi l'80%) dal potere calorifico del metano stesso. In base alla termodinamica, il reforming di metano in fase vapore a partire da una temperatura di 600C possibile solo con l'apporto di energia termica. In pratica, oggi pi del 90 % dell'idrogeno viene prodotto tramite il reforming di gas naturale in fase vapore. Con un opportuno catalizzatore, la reazione avviene a temperature attorno ai 900C. Il calore necessario viene prodotto dalla combustione di parte del metano. Questo metodo per la produzione di idrogeno, oggi molto diffuso, non prevede alcun immagazzinamento di energia, bench la met dell'idrogeno prodotto provenga dall'acqua. Vediamo ora alcuni esempi di processi in cui la produzione di idrogeno serve a trasformare energie rinnovabili (sole, vento, forza idrica, biomassa) in una forma chimica immagazzinabile e di facile impiego.
3. Produzione di idrogeno dall'acqua ed energie rinnovabili Ad eccezione della biomassa, le forme in cui si presenta l'energia solare (calore, energia cinetica, elettricit) non sono immagazzinabili a lungo termine oppure lo sono, ma a costi eccessivi. Ne risultano vere e proprie catene di trasformazione dell'energia che terminano con la produzione di idrogeno (figura 3). In linea di principio, i processi che presentano un rendimento migliore sono quelli che passano dalla fonte di energia primaria all'idrogeno con un numero minimo di trasformazioni intermedie di energia poich ogni trasformazione comporta perdite irreversibili di energia. I rendimenti delle singole fasi vanno moltiplicati per ottenere il rendimento complessivo di una catena di trasformazione dell'energia. D'altro canto, per, rinunciando all'eleganza della conversione diretta a favore di una tecnica indiretta, ma basata su tecnologie comprovate, possibile ridurre i rischi tecnici della produzione solare di idrogeno.
Photochemie Sonnenstrahlung Wind
Photovoltaik Prozesswrme
Solarchemie
Wasserkraft
Kraftwerk
Biomasse Elektrolyse SolarVergasung Wasserstoff
Fig. 3: Il diagramma rappresenta le vie possibili di produrre idrogeno con l'aiuto delle fonti energetiche rinnovabili
Per esempio, possibile calcolare con una buona approssimazione il rendimento della produzione di idrogeno attraverso calore di processo solare, produzione di energia elettrica e successiva elettrolisi, bench talel processo non sia mai stato realizzato su larga scala finora: tot = Koll * DT * Ely In California, le centrali termiche solari producono energia elettrica con un rendimento del 913% (Koll * DT = 11%). Siccome oggi possibile costruire impianti di elettrolisi commerciali con un rendimento del 75%, ne risulta che il rendimento totale della catena pari
all'8%. I processi diretti, come la scissione fotochimica o fotoelettrochimica dell'acqua o la produzione di idrogeno in un processo termico solare ciclico, dovrebbero permettere perlomeno teoricamente - rendimenti notevolmente superiori. Prima di poterli stimare pi precisamente e realizzare in grossi impianti vanno comunque condotte ulteriori ricerche di fondo. Qui di seguito presentiamo la chimica solare, una possibile opzione interessante a lungo termine per la produzione solare di idrogeno, e la gassificazione della biomassa, un esempio di processo utilizzabile a breve e medio termine. Entrambe queste tecnologie sono in studio presso il Settore Energia Generale del PSI.
3.1. Produzione chimico-solare di idrogeno Nel fuoco dello specchio parabolico convergono le radiazioni solari dirette, facendo salire la temperatura fin sopra i 2000C. Questo calore di processo pu essere utilizzato da un lato per alimentare una macchina termica in modo che produca energia elettrica: negli Stati Uniti e in Spagna, per esempio, esistono impianti pilota con grandi campi speculari che focalizzano la luce solare in una torre posta al centro. D'altro lato le elevate temperature nel fuoco possono anche essere impiegate per scatenare reazioni chimiche, che non si produrrebbero con le consuete fonti di calore, che generano temperature nettamente inferiori. Presso il PSI vengono studiati i cosiddetti processi termochimici ciclici che scindono l'acqua nei suoi elementi attraverso una serie di reazioni termiche, come ad esempio il ciclo dell'ossido di ferro: 1a fase: 2a fase: Somma: Fe3O4 3FeO + H2O H2O 3FeO + 1/2 O2 Fe3O4 + H2 H2 + 1/2 O2 (T>2300C) (T600C)
La riduzione del Fe3O4 in FeO una cosiddetta reazione endotermica, ossia una reazione che utilizza calore. Nella seconda fase, invece, si libera calore. Nel diagramma dell'energia (figura 4) risulta quindi che il potere calorifico del FeO prodotto, rispetto alla forma "pi ossidata" Fe3O4, maggiore di quello dell'idrogeno. La produzione di idrogeno quindi una reazione "in discesa", che libera energia. Dal punto di vista termodinamico, la trasformazione del Fe3O4 in FeO richiede una temperatura di quasi 2200C, mentre la reazione di scissione dell'acqua avviene a circa 500C e genera calore. La ricerca presso il PSI si concentra sui diversi aspetti di questo ciclo, che seduce proprio per la sua semplicit concettuale. gi stato dimostrato che la temperatura di scissione del Fe3O4 pu essere abbassata aggiungendo del manganese, semplificando un po' il problema delle alte temperature. La reazione presuppone comunque lo sviluppo di nuovi reattori non convenzionali. Il concetto elaborato dal PSI rappresentato dal cosiddetto "reattore a nube polverizzata" (figura 5). Sugli impianti del PSI possibile sperimentare reattori chimico-solari sottoponendoli a una potenza termica fino a 30 kW e a una temperatura fino a 1600C.
150
H (%)
100
Eisenoxid-Zyklus Heizwert von H2 = 100%
50
FeO H2
0
Fe3O4 O2 + 3 FeO 3 FeO H2 + Fe3O4
Fig. 4: Diagramma energetico semplificato rappresentante la dissociazione termochimica dell'acqua nel ciclo "ossido di ferro". La riduzione endotermica del Fe3O4 fornisce il prodotto FeO. Il "potere calorifico" di Fe3O4 viene considerato uguale a zero.
Il ciclo dell'ossido di ferro una reazione con un potenziale molto alto, ma comporta pure parecchi rischi in termini di fattibilit tecnica. Le temperature estreme, i problemi connessi di minimizzazione delle perdite termiche tramite irraggiamento e termostabilit dei materiali e i problemi chimici in generale a temperature superiori ai 2000C costituiscono un'enorme sfida per gli ingegneri e i chimici impegnati nel progetto. Forse la chimica solare riuscir a imporsi nel campo della produzione di idrogeno solo con processi ibridi fossili-solari, pi semplici dal punto di vista tecnico. ipotizzabile per esempio alimentare il reforming di metano in fase vapore, descritto nella figura 2 e tecnicamente gi ben noto, con energia solare: il calore di processo solare a una temperatura 1000C pu essere prodotto tramite la tecnologia attuale impiegata nelle centrali solari. La miscela di idrogeno e CO2 risultante conterrebbe una quantit di energia in pi del gas metano di partenza, pari all'energia solare immessa. Forse per i puristi non accettabile l'"inquinamento" con gas naturale, ma per il bilancio globale del CO2 un concetto del genere interessante proprio per via della possibilit d'impiego diretto. Un problema, da risolversi anche con processi relativamente semplici e tecnicamente gi comprovati, la variabilit temporale dell'input solare. La chimica termico-solare, infatti, deve limitarsi a processi semplici e termicamente efficienti, che non richiedano l'installazione di complessi impianti collegati in serie, anche nel caso di realizzazione in regioni ben assolate (ad esempio in Nord Africa).
Fig. 5: Il reattore "nuvole di polvere" per reazioni chimico-solari. La luce solare concentrata viene assorbita direttamente da particelle aerosol sospese in un gas apposito.
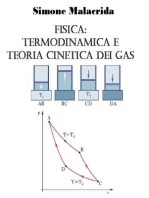
3.2. Gassificazione di biomassa Il metodo attualmente pi economico per produrre idrogeno solare la gassificazione termica di biomassa (legno e altre materie vegetali). Come mostra lo schema dell'energia (figura 6), dal punto di vista termodinamico i rapporti sono analoghi a quelli della produzione di idrogeno da gas naturale. Come il reforming di gas naturale in fase vapore, anche la trasformazione di legno in idrogeno e CO2, con l'apporto di vapore, richiede energia termica, ottenuta di norma con la combustione di parte del legno stesso. In linea di principio, si pu o generare il calore fuori dal carburatore e trasmetterlo alla sostanza da gassificare attraverso le pareti oppure bruciare, con l'apporto di ossigeno, parte del legno in modo che il calore liberato corrisponda all'energia di gassificazione. Questo secondo metodo, pi diffuso, detto gassificazione autotermica o ossidazione parziale del legno.
150
(%)
100
Dampf-Vergasung von Holz Heizwert von H2 = 100%
50
Holz
0
"Holz" +1.33 H2O
H2
2.1 H2 + CO2
Fig. 6: Diagramma energetico semplificato raffigurante la gassificazione endotermica del legno mediante vapore. Si tratta del caso ideale. Legno assolutamente secco ha la formula chimica CH1.55O0.66. Il 72% del potere calorifico dell'idrogeno prodotto contenuto nel legno (biomassa). Le trasformazioni illustrate alle figure 1, 2, 4 e 6 sono essenzialmente idealizzate. Per esempio, la trasformazione del legno con l'apporto di vapore genera non solo idrogeno e CO2, ma tutta una gamma di gas e composti organici condensabili (catrami). Un gas tipico, come quelli prodotti nell'impianto sperimentale a turbolenza del PSI, dopo la scissione dell'acqua cos composto: 48% azoto (dell'aria), 23% CO (monossido di carbonio), 12% idrogeno, 12% diossido di carbonio e 5% metano. L'utile in termini di idrogeno modesto: solo il 22% circa del potere calorifico del gas prodotto sotto forma di idrogeno, mentre il 33% rappresentato da CO e il 45% da metano. La trasformazione solo parziale in idrogeno dipende essenzialmente dal fatto che alle temperature di reazione, attorno ai 900C, sussistono determinati equilibri chimici. In particolare, in presenza di vapore si crea un equilibrio tra il CO e l'H2 (la cosiddetta reazione del gas d'acqua): H2O + CO = CO2 + H2 Tutte le componenti dell'equazione sono contenute nel gas di partenza. Alle alte temperature del carburatore (850C), l'equilibrio spostato a sinistra. Raffreddando i gas, la composizione rimane immutata poich, in assenza di catalizzatori, a temperature inferiori l'equilibrio s'instaura solo lentamente. La quantit d'idrogeno risultante pu essere aumentata, a scapito della quantit di CO, a temperature attorno ai 300C modificando gli equilibri tramite un letto catalitico. I grandi carburatori ottimizzati permettono di raggiungere risultati (in seguito alla conversione del CO) da 0.7 a 0.8 Nm3 di H2 per kg di legno (massa secca), il che corrisponde a un rendimento di trasformazione di quasi il 50% (potere calorifico dell'idrogeno riferito al potere calorifico del legno secco impiegato). In linea di principio, poi, anche il metano del gas di partenza pu essere convertito in idrogeno secondo un processo di reforming in fase vapore tramite un catalizzatore. Di preferenza, il catalizzatore viene allora inserito immediatamente dopo la fase di gassificazione (temperatura di reazione). Il quantitativo relativamente importante di idrogeno prodotto con un carburatore fa s che la produzione di elettricit a partire dal legno, vantaggiosa forse a breve termine, non ha pi alcun senso quando l'idrogeno pu essere prodotto in quantit
economicamente significative per elettrolisi dell'acqua: la trasformazione di biomassa in idrogeno tramite una centrale termica e un processo di elettrolisi, una delle soluzioni previste nella figura 3, non raggiunger mai un rendimento del 50%! La gassificazione di un combustibile contenente carbonio per produrre idrogeno fornisce sempre quale prodotto finale una miscela di gas. Ci significa che l'idrogeno deve ancora essere separato dai gas inerti e dal CO2. Esistono diverse alternative per separare l'idrogeno dalle miscele di gas. Nella PSA (=Pressure Swing Absorption), per esempio, il gas fatto passare, sotto pressione, attraverso tn letto assorbente, che trattiene le componenti gassose indesiderate. Non appena il letto saturo si arresta il passaggio del gas e si abbassa la pressione in modo da permettere il disassorbimento dei gas assorbiti. Un'altra possibilit la separazione tramite membrane, ossia sottili pellicole polimeriche, che permettono la diffusione dell'idrogeno. Al posto della conversione di CO in idrogeno e della successiva separazione dalle altre componenti del gas, il gas di sintesi pu essere trasformato, con un catalizzatore, in metanolo, dopo opportuni processi di depurazione, calcoli stechiometrici e compressioni: 2 H2 + CO CH3OH Larson e Katofsky*) hanno paragonato la produzione da biomassa di metanolo con quella di idrogeno, come pure la produzione da biomassa con quella da gas naturale, rilevando che, su larga scala, la trasformazione del legno in metanolo risulta pi cara del 20% circa rispetto alla produzione di idrogeno. Ciononostante, presso il PSI riteniamo che la sintesi del metanolo rappresenti l'utilizzazione pi sensata del gas prodotto dalla gassificazione del legno, soprattutto se in questo modo si contribuisce all'uso di energie rinnovabili nel settore dei trasporti. L'immagazzinamento dell'idrogeno invece oneroso e costoso. Inoltre, l'introduzione del metanolo quale combustibile liquido pu sfruttare le infrastrutture esistenti (cfr. progetto BIOMETH, contributo dell'autore alla conferenza GLAET dell'ottobre 1995), mentre per l'idrogeno occorre sviluppare una nuova tecnologia di distribuzione e costruire le relative infrastrutture. Per le applicazioni in cui indispensabile utilizzare l'idrogeno quale combustibile, ad esempio le celle di combustibile per applicazioni mobili, attualmente oggetto di studi (v. relazione di E. Fischer), il metanolo pu essere utilizzato anche come vettore di idrogeno.
4. Produzione di idrogeno per le celle di combustibile molto probabile che l'idrogeno si affermer quale vettore energetico dapprima per le sue qualit di combustibile (combustione pulita nei motori a combustione e soprattutto nelle celle di combustibile, per ridurre l'inquinamento dell'aria nei grandi agglomerati urbani) e solo in seguito in sostituzione dell'olio da riscaldamento e del gas naturale sul mercato dell'energia. I progressi realizzati dalla tecnologia delle celle di combustibile e l'interesse manifestato dall'industria automobilistica lasciano presupporre che le automobili a celle di combustibile saranno introdotte entro dieci anni. Decisivo sar non tanto il fatto che l'idrogeno ottenuto da fonti primarie rinnovabili sia pi o meno costoso di quello da gas naturale, ma piuttosto
*) E.D. Larson, R.E. Katofsky, Production of Hydrogen and Methanol via Biomass Gasification, Adv. in Thermochem.
Biomass Conversion, A.V. Bridgwater, Ed., 1993; pp. 495-510.
10
l'eventualit che vengano prescritti valori limite per le emissioni nelle regioni fortemente inquinate, limiti raggiungibili solo introducendo automobili elettriche. Oggi, le cellule di combustibile funzionano esclusivamente a idrogeno. Ma come ottenere l'idrogeno necessario per i veicoli a celle di combustibile entro breve termine? Una delle soluzioni caldeggiate dall'industria automobilistica la produzione di idrogeno da un vettore energetico liquido situato a bordo del veicolo stesso. Ad esempio, tramite il reforming di metanolo in fase vapore, con un opportuno catalizzatore: CH3OH + H2O 3H2 + CO2 Questa reazione presenta un buon rendimento gi a temperature attorno ai 300C (contro i 900C necessari per il reforming del CH4). Un vantaggio del trasporto di idrogeno a bordo del veicolo che si pu rifornirsi di liquido presso una stazione di rifornimento, in altre parole le infrastrutture andrebbero modificate solo lievemente rispetto ai sistemi attuali. Non viene scartata nemmeno l'ipotesi di produrre idrogeno a bordo partendo da benzina, ipotesi comunque molto pi difficile da realizzare. L'alternativa alla produzione di idrogeno a bordo la produzione di idrogeno liquido da gas naturale in grandi impianti, con costi d'esercizio limitati, e la realizzazione di infrastrutture per l'idrogeno liquido con i relativi problemi di accettazione da parte dei consumatori. Un'altra alternativa, piuttosto remota visto l'attuale rapporto di prezzi tra l'energia elettrica e i combustibili, la produzione decentrata di idrogeno attraverso piccoli impianti elettrolitici situati nei garage privati e alimentati tramite la corrente di rete o pannelli solari.
5. Conclusione Sono molte le strade che conducono all'idrogeno. Per l'attuale fabbisogno di idrogeno chimico, comunque, la tecnica di produzione non subir mutamenti a breve termine. L'idrogeno solare ottenibile trasformando l'energia solare primaria in vari modi. Essenzialmente, la fonte di energia a stabilire qual la tecnica migliore. La trasformazione diretta dell'energia solare primaria, come ad esempio nella scissione termochimica dell'acqua in un processo ciclico, racchiude un grande potenziale in termini di efficienza, ma si trova ancora a livello di ricerca fondamentale. Con le tecniche attuale, si pu invece produrre idrogeno con un buon rendimento partendo da biomassa. Le celle di combustibile per il funzionamento di veicoli o di minicentrali di riscaldamento richiederanno presumibilmente la disponibilit di idrogeno di origine fossile, in attesa che si possa produrre in quantit rilevanti idrogeno immagazzinabile da energia solare. L'applicazione delle celle di combustibile potrebbe per gettare le fondamenta per una gestione solare dell'idrogeno.
Potrebbero piacerti anche
- Manuale Corso Livello AvanzatoDocumento178 pagineManuale Corso Livello AvanzatoAntony GattaNessuna valutazione finora
- Tanti Esercizi Di ElettrochimicaDocumento2 pagineTanti Esercizi Di Elettrochimicamarcocorrao100% (1)
- Configurazione Elettronica KleinDocumento35 pagineConfigurazione Elettronica KleinGabriele VisentinNessuna valutazione finora
- Eserciziario - Compito 2a ParteDocumento2 pagineEserciziario - Compito 2a ParteVincenzoABrunoNessuna valutazione finora
- Le SoluzioniDocumento23 pagineLe SoluzioniFrancesco Torrettaro100% (1)
- La Forza Degli Acidi e Delle Basi: NH + H O NH + OhDocumento70 pagineLa Forza Degli Acidi e Delle Basi: NH + H O NH + OhesterNessuna valutazione finora
- Acidi e Basi - IDocumento29 pagineAcidi e Basi - IMarioNessuna valutazione finora
- Acidi e BasiDocumento4 pagineAcidi e Basivittoria dal medicoNessuna valutazione finora
- Zincatura Fai Da Te by Bunjin62 PDFDocumento21 pagineZincatura Fai Da Te by Bunjin62 PDFschioppoNessuna valutazione finora
- Il LaterizioDocumento29 pagineIl LaterizioPopa SilviuNessuna valutazione finora
- Recupero 24-11 B Sol PDFDocumento6 pagineRecupero 24-11 B Sol PDFWolframio74Nessuna valutazione finora
- Stechiometria Ed ElettrochimicaDocumento11 pagineStechiometria Ed ElettrochimicaClaudia BorriNessuna valutazione finora
- Scienza Dei MaterialiDocumento36 pagineScienza Dei MaterialiDavideNessuna valutazione finora
- Cicli CombinatiDocumento30 pagineCicli CombinatiNiccolò Giannotti100% (3)
- Ziegler NattaDocumento7 pagineZiegler NattamikadoboomNessuna valutazione finora
- Acido BaseDocumento44 pagineAcido Basedoinita7Nessuna valutazione finora
- Dispensa - Chimica Organica E Analitica PDFDocumento116 pagineDispensa - Chimica Organica E Analitica PDFrodrigue yanNessuna valutazione finora
- Vol3itino PDFDocumento479 pagineVol3itino PDFGianni CiavattaNessuna valutazione finora
- La Grande Accelerazione Di JDocumento14 pagineLa Grande Accelerazione Di JGiulia BajNessuna valutazione finora
- Esercizi Di Chimica - 0Documento3 pagineEsercizi Di Chimica - 0Luca Corallo100% (1)
- Fuel CellsDocumento39 pagineFuel Cellspajerm80Nessuna valutazione finora
- Idrogeno 1Documento12 pagineIdrogeno 1sdm314Nessuna valutazione finora
- Impianti Meccanici CompletoDocumento78 pagineImpianti Meccanici CompletoMichele AssirelliNessuna valutazione finora
- Velocità Di ReazioneDocumento16 pagineVelocità Di ReazioneFrancesco TorrettaroNessuna valutazione finora
- Stechiometria 5Documento37 pagineStechiometria 5arky93Nessuna valutazione finora
- Andytonini 2 Principi Di Distillazione Parte 1 2Documento9 pagineAndytonini 2 Principi Di Distillazione Parte 1 2andrew wallenNessuna valutazione finora
- Appunti Trasmissione Del Calore 3 PDFDocumento310 pagineAppunti Trasmissione Del Calore 3 PDFMaxNessuna valutazione finora
- Esercizi RedoxDocumento2 pagineEsercizi RedoxevaNessuna valutazione finora
- Il Bilancio Termico Di Una Piscina IDRA2012Documento10 pagineIl Bilancio Termico Di Una Piscina IDRA2012fedelaiNessuna valutazione finora
- Test Di CinematicaDocumento2 pagineTest Di CinematicaLaura RossiNessuna valutazione finora
- Riflessioni Didattiche Su Schiavo EnergeticoDocumento3 pagineRiflessioni Didattiche Su Schiavo EnergeticoDario TamburranoNessuna valutazione finora
- 3 Evaporatori-ConcentratoriDocumento14 pagine3 Evaporatori-ConcentratoriEdLardo GaleanoNessuna valutazione finora
- Guida Alla Protezione CatodicaDocumento10 pagineGuida Alla Protezione CatodicaAlfonzo BadooNessuna valutazione finora
- Thermital BSS 15Documento2 pagineThermital BSS 15InclisaInstalacionesNessuna valutazione finora
- PolimerizzazioneDocumento29 paginePolimerizzazioneAlessio ScarabelliNessuna valutazione finora
- Spettrofotometria Uv VisibileDocumento9 pagineSpettrofotometria Uv VisibileDomenico Paralelo100% (1)
- Appunti MastrulloDocumento84 pagineAppunti Mastrullodar1989Nessuna valutazione finora
- 18 - Energie RinnovabiliDocumento22 pagine18 - Energie RinnovabiliDomenico BevilacquaNessuna valutazione finora
- Appunti Chimica AnaliticaDocumento3 pagineAppunti Chimica AnaliticafabiothekingjamesNessuna valutazione finora
- Storia Dell' ArteDocumento8 pagineStoria Dell' Artedamianomenegon95Nessuna valutazione finora
- Sistemi TamponeDocumento53 pagineSistemi TamponeYann89Nessuna valutazione finora
- 063 - Andytonini - 27b Essiccamento Appunti e Schemi Vers - 1Documento5 pagine063 - Andytonini - 27b Essiccamento Appunti e Schemi Vers - 1Alberto LazzarettiNessuna valutazione finora
- Catalogo Hvac 2015Documento348 pagineCatalogo Hvac 2015VisitOn.T.witte.rNessuna valutazione finora
- Esercizi IC1 9 CFUDocumento57 pagineEsercizi IC1 9 CFUTutti Ganti A PezziNessuna valutazione finora
- Esercitazioni Di Centrali IdroelettricheDocumento97 pagineEsercitazioni Di Centrali IdroelettricheStefano AcciaioliNessuna valutazione finora
- Appunti Per StudiareDocumento110 pagineAppunti Per StudiareRossNessuna valutazione finora
- Influenza Della Temperatura Sulla Velocità Di ReazioneDocumento1 paginaInfluenza Della Temperatura Sulla Velocità Di ReazioneLuca MarlettaNessuna valutazione finora
- Arg.03-Pompe Di CaloreDocumento114 pagineArg.03-Pompe Di CaloreGiuseppe FerrariNessuna valutazione finora
- Esercizi Svolti Elettrolisi 15-16Documento8 pagineEsercizi Svolti Elettrolisi 15-16biagio castronovoNessuna valutazione finora
- CineticaDocumento4 pagineCineticaRoberto SchimmentiNessuna valutazione finora
- 02 Sistemi Trifase 1Documento46 pagine02 Sistemi Trifase 1Lerry AnsaldiNessuna valutazione finora
- Computo MetricoDocumento6 pagineComputo Metricow_fibNessuna valutazione finora
- Curve CCTDocumento2 pagineCurve CCTJayar VillavicencioNessuna valutazione finora
- Diagramma Fe-C FilippiDocumento6 pagineDiagramma Fe-C FilippiEnrico NovelloNessuna valutazione finora
- Encclopedia Degli Idrocarburi - Alchilazione - Cap 4 - 3Documento12 pagineEncclopedia Degli Idrocarburi - Alchilazione - Cap 4 - 3MasterPie1950Nessuna valutazione finora
- Reazioni Di Chimica OrganicaDocumento4 pagineReazioni Di Chimica OrganicamarcellozampollaNessuna valutazione finora
- Chimica - Redox e BiochimicaDocumento12 pagineChimica - Redox e BiochimicaPaolo D'AlessandroNessuna valutazione finora
- Storia Dell'ammoniacaDocumento8 pagineStoria Dell'ammoniacaBiagio CastronovoNessuna valutazione finora
- Stechiometria Esercizi STDocumento54 pagineStechiometria Esercizi STppiccolini100% (1)
- C7mtm06 PDFDocumento68 pagineC7mtm06 PDFLoredana MagdaNessuna valutazione finora
- ORC BidiniDocumento6 pagineORC BidinilunettinoNessuna valutazione finora
- MiseDocumento1 paginaMisecicciobellosNessuna valutazione finora
- Appunti Di Chimica, Chimica in PilloleDocumento33 pagineAppunti Di Chimica, Chimica in PillolecicciobellosNessuna valutazione finora
- Soluzioni DiapositiveDocumento7 pagineSoluzioni DiapositivecicciobellosNessuna valutazione finora
- Chimica Dei Materiali - 1 Chimica Applicata Al Riciclo Dei MaterialiDocumento14 pagineChimica Dei Materiali - 1 Chimica Applicata Al Riciclo Dei MaterialicicciobellosNessuna valutazione finora
- Chimica GeneraleDocumento21 pagineChimica GeneralegpNessuna valutazione finora
- MiseDocumento1 paginaMisecicciobellosNessuna valutazione finora
- Acidi e BasiDocumento29 pagineAcidi e BasicicciobellosNessuna valutazione finora
- Esercizi Di Nomenclatura ChimicaDocumento4 pagineEsercizi Di Nomenclatura ChimicacicciobellosNessuna valutazione finora
- Acidi e BasiDocumento29 pagineAcidi e BasicicciobellosNessuna valutazione finora
- Acidi e BasiDocumento29 pagineAcidi e BasicicciobellosNessuna valutazione finora
- Esercizi Di Nomenclatura ChimicaDocumento4 pagineEsercizi Di Nomenclatura ChimicacicciobellosNessuna valutazione finora
- Acidi e BasiDocumento29 pagineAcidi e BasicicciobellosNessuna valutazione finora
- Esercizi Di Nomenclatura ChimicaDocumento4 pagineEsercizi Di Nomenclatura ChimicacicciobellosNessuna valutazione finora
- Appunti Universitari Online - ChimicaDocumento46 pagineAppunti Universitari Online - Chimicacicciobellos100% (1)
- Esercizi Di Nomenclatura ChimicaDocumento4 pagineEsercizi Di Nomenclatura ChimicacicciobellosNessuna valutazione finora
- Appunti Universitari Online - ChimicaDocumento46 pagineAppunti Universitari Online - Chimicacicciobellos100% (1)
- Esercizi Di Nomenclatura ChimicaDocumento4 pagineEsercizi Di Nomenclatura ChimicacicciobellosNessuna valutazione finora
- Esercizi Di Nomenclatura ChimicaDocumento4 pagineEsercizi Di Nomenclatura ChimicacicciobellosNessuna valutazione finora
- Esercizi Di Nomenclatura ChimicaDocumento4 pagineEsercizi Di Nomenclatura ChimicacicciobellosNessuna valutazione finora
- Appunti Di Chimica, Chimica in PilloleDocumento33 pagineAppunti Di Chimica, Chimica in PillolecicciobellosNessuna valutazione finora
- Esercizi Di Nomenclatura ChimicaDocumento4 pagineEsercizi Di Nomenclatura ChimicacicciobellosNessuna valutazione finora
- Esercizi Di Nomenclatura ChimicaDocumento4 pagineEsercizi Di Nomenclatura ChimicacicciobellosNessuna valutazione finora
- Esercizi Di Nomenclatura ChimicaDocumento4 pagineEsercizi Di Nomenclatura ChimicacicciobellosNessuna valutazione finora
- Esercizi Di Nomenclatura ChimicaDocumento4 pagineEsercizi Di Nomenclatura ChimicacicciobellosNessuna valutazione finora
- Esercizi Di Nomenclatura ChimicaDocumento4 pagineEsercizi Di Nomenclatura ChimicacicciobellosNessuna valutazione finora
- Esercizi Di Nomenclatura ChimicaDocumento4 pagineEsercizi Di Nomenclatura ChimicacicciobellosNessuna valutazione finora
- Esercizi Di Nomenclatura ChimicaDocumento4 pagineEsercizi Di Nomenclatura ChimicacicciobellosNessuna valutazione finora
- Esercizi Di Nomenclatura ChimicaDocumento4 pagineEsercizi Di Nomenclatura ChimicacicciobellosNessuna valutazione finora
- Esercizi Di Nomenclatura ChimicaDocumento4 pagineEsercizi Di Nomenclatura ChimicacicciobellosNessuna valutazione finora
- Monossido Di Carbonio IntossicazioneDocumento1 paginaMonossido Di Carbonio IntossicazionemaxNessuna valutazione finora
- TESI TRIENNALE - S. CompaoreDocumento50 pagineTESI TRIENNALE - S. CompaoreBruno NavarroNessuna valutazione finora
- Cicli BiogeochimiciefDocumento27 pagineCicli BiogeochimiciefIvoGraziotinNessuna valutazione finora
- Esercizi Leggi PonderaliDocumento4 pagineEsercizi Leggi PonderaliVeronica GiamoganteNessuna valutazione finora
- INAIL DallavalutazAllaGestRischioDocumento352 pagineINAIL DallavalutazAllaGestRischioantioco_abisNessuna valutazione finora
- Lo Stato GassosoDocumento22 pagineLo Stato GassosoChi PuòessereNessuna valutazione finora
- Ecologia 1Documento26 pagineEcologia 1katiaNessuna valutazione finora
- (Le Fonti Di Energia Non RinnovabiliDocumento20 pagine(Le Fonti Di Energia Non Rinnovabililiparoti_gfNessuna valutazione finora