Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Le Soluzioni Chimiche Sprint Pack Pro Med
Caricato da
Antonio Bifulco0 valutazioniIl 0% ha trovato utile questo documento (0 voti)
45 visualizzazioni1 paginaTitolo originale
LE-SOLUZIONI-CHIMICHE-SPRINT-PACK-PRO-MED
Copyright
© © All Rights Reserved
Formati disponibili
PDF, TXT o leggi online da Scribd
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
© All Rights Reserved
Formati disponibili
Scarica in formato PDF, TXT o leggi online su Scribd
0 valutazioniIl 0% ha trovato utile questo documento (0 voti)
45 visualizzazioni1 paginaLe Soluzioni Chimiche Sprint Pack Pro Med
Caricato da
Antonio BifulcoCopyright:
© All Rights Reserved
Formati disponibili
Scarica in formato PDF, TXT o leggi online su Scribd
Sei sulla pagina 1di 1
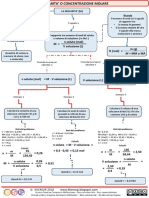
LE SOLUZIONI Pro-Med | Mappe
www.promedtest.it
PROPIETA' SOLVENTI SOLUBILITA' PRINCIPALI MODI PER ESPRIMERE LE
DELL'ACQUA CONCNETRAZIONI DELLE SOLUZIONI
Si definisce
Per alcune specifiche solubilità di un PERCENTUALE MOLARITÀ MOLALITÀ NORMALITÀ FRAZIONE MOLARE
caratteristiche l'acqua è soluto in un
considerata il solvente solvente in certe Indica le moli di soluto Indica il numero di moli Indica il numero di Indica il numero di moli
Quantità di soluto
biologico ideale e per condizioni di presenti in 1l di soluzione di soluto presenti in 1kg equivalenti di soluto di un soluto rispetto al
presente in 100 g di
questo motivo è temperatura e di solvente presenti in un litro di numero totali di moli
soluzione (soluto+
indispensabile per la vita pressione, la soluzione
MASSA/MASSA solvente) M = n soluto / V
della cellula quantità di quel
soluzione m = n soluto / massa X = n soluto / n tot
soluto che si
(mg soluto /mg solvente N = n° equivalenti
POLARITÀ COESIVITÀ scioglie in 100g di
soluzione) * 100 Esempio : calcola la soluto / V soluzione = Esempio: calcola la
solvente per
molarità di una Esempio : Calcola i Molarità * valenza frazione molare dei
ottenere una Indica il volume di un
La presenza di un L'attrazione operativa
soluzione satura soluzione ottenuta grammi di glucosio ( componenti di una
atomo di ossigeno elettrostatica tra poli soluto presente in 100
sciogliendo 20 g di MM= 180 g/mol) da soluzione composta da
più elettronegativo di segno opposto ml di soluzione
VOLUME/VOLUME NaCl (MM =58 g/mol ) in sciogliere in 800 g di n° equivalenti = massa 15g di NaCl (MM= 58 g/
rispetto ai due atomi permette alle Ogni sostanza tende a
(Vml soluto/ Vml 250 ml di soluzione acqua perchè la in grammi soluto / mol) e di 200g di H2O (
di idrogeno molecole d'acqua di sciogliere sostanze
soluzione)*100 soluzione sia 0,5 molale massa equivalente (MEQ) MM= 18 g/mol).
comporta la instaurare dei legami simili a se stessa
creazione di un a idrogeno con altre SVOLGIMENTO
Indica la massa in g di Esempio: Calcola la MEQ = massa
dipolo elettrico molecole di H2O "Il simile scioglie il simile" SVOLGIMENTO SVOLGIMENTO
soluto presente in 100ml normalità di una molecolare / valenza
Per prima cosa è
di soluzione soluzione di 20 g di operativa
Per questo motivo l' MASSA/VOLUME necessario trovare il Partiamo con il calcolare Partiamo con il calcolare
PRODOTTO DI H3PO4 (MM = 98 g/mol)
acqua interagisce (mg soluto/Vml numero di moli, dato dal le moli tramite la il numero di moli dell'
SOLUBILITA' in 750 ml di soluzione La valenza operativa
con diversi soluti e soluzione)*100 rapporto tra la massa in formula inversa della acqua e del cloruro di
Argomento mobile grammi del cloruro di molalità : n°moli = indica il numero di sodio:
viene respinta da
È indice della sodio e la sua massa molalità * massa SVOLGIMENTO elettroni che un atomo n H2O = 200/ 18 = 11 mol
altri
solubilità delle molecolare --> n° moli = (kg) solvente = 0,5*0,8 = di un elemento cede o n NaCl = 15/ 58 = 0,25
varie sostanze in 0.34 mol 0,4 mol mette in comune mol
Da qui la distinzione Partiamo con il calcolare
acqua ed è quando si lega ad altri
tra soluti il numero di moli
indicato da una atomi
Trovate le moli posso Avendo le moli posso facendo il rapporto tra Nel nostro caso il soluto
costante di calcolare la molarità calcolare la massa di è rappresentato dal
la massa in grammi e la
IDROFOBI IDROFILI solubilità (Kps) Assume valori diversi a
prestando attenzione all' soluto moltiplicandole massa molecolare : cloruro di sodio quindi
data dal prodotto unità di misura del per la MM nota : mg = 0, seconda del soluto la frazione molare sarà
n°moli =20/ 98 = 0,2 mol
Composti Composti di concentrazioni volume della soluzione, 4* 180 = 72g data dal rapporto tra le
strutturalmente strutturalmente molari degli ioni che per definizione moli di NaCl e la somma
Avendo moli e volume VALENZA OPERATIVA
poco affini all' molto affini all' creati in deve essere in litri, di queste con le moli di
della soluzione calcolo
acqua e molto acqua e poco soluzione : (A+) * ( quindi: M = 0,34 : 0,25 = acqua
la molarità prestando
affini ai affini ai B-) 1,36 M Acidi --> numero di H+
attenzione alle unità di
solventi solventi rilasciati
misura: M=0,2/0,75= 0, X = 0,25 / (0,25+11) = 0,
oleosi --> oleosi --> Se Kps è molto 27 M 25 / 11,25 = 0,02 --> in
sostanze sostanze Basi --> numero di OH -
bassa allora la percentuale --> 2 %
lipofile lipofobe liberati
sostanza sarà Posso trovare ora la
poco solubile in normalità moltiplicando Reazioni redox -->
acqua la molarità per la numero di elettroni
APPROFONDIMENTO
valenza operativa, nel scambiati nella
Se Kps è alta
nostro caso assume il semireazione
All'interno del corpo umano, e in tutte le cellule che lo allora la sostanza
valore 3 poiché l'acido
compongono, ogni spostamento di soluti o acqua è sarà PAROLE CHIAVE
fosforico libera 3 H+ in Sali --> numero di
finemente regolato grazie a specifici sistemi. Per esempio maggiormente cariche positive o
soluzione: N = 0,27 * 3 =
nel caso dello spostamento di soluti tramite diffusione solubile in acqua -IDROFOBO negative
0,8 eq/ l
facilitata la differenza di concentrazione tra ambiente intra e -IDROFILO
Se il prodotto
extracellulare permette di non utilizzare ATP. Oltre alla -COSTANTE DI
delle
differenza di concentrazione tra i vari soluti è fondamentale, SOLUBILITÀ
concentrazioni è
sempre nel trasporto tra i diversi compartimenti dell' -MOLARITÀ
maggiore di Kps,
organismo e cellulari, la natura chimica degli stessi. In questo -MOLALITÀ
formerà il CORPO
contesto è cruciale la distinzione tra soluti lipofili e idrofili. -NORMALITÀ
DI FONDO
Come saprete sicuramente a memoria, la membrana cellulare -FRAZIONE
è composta da un doppio strato fosfolipidico, all'interno del Se il prodotto -MOLARE
quale le code degli acidi grassi creano un ambiente ionico è = alla Kps -VALENZA OPERATIVA
idrofobo, quindi ostile al passaggio di molecole idrofile e la soluzione è -POLARITÀ
accogliente per quelle lipofile. Per questo motivo grandi satura, quindi all'
molecole polari e molecole cariche, come gli ioni, sono equilibrio
impossibilitate ad attraversare il bilayer lipidico senza l'
ausilio di proteine canale.
Potrebbero piacerti anche
- Concentrazione SoluzioniDocumento4 pagineConcentrazione SoluzioniViolaGNessuna valutazione finora
- A SoluzDocumento7 pagineA Soluzfake frndNessuna valutazione finora
- Le Soluzioni: SolubilizzazioneDocumento53 pagineLe Soluzioni: Solubilizzazionejorane7867Nessuna valutazione finora
- Lezionevi ConcentrazioniDocumento22 pagineLezionevi ConcentrazionifpezNessuna valutazione finora
- Le Proprietà Delle SoluzioniDocumento34 pagineLe Proprietà Delle SoluzioniAlelotitoNessuna valutazione finora
- Proprieta ColligativeDocumento34 pagineProprieta ColligativerobertaNessuna valutazione finora
- Esercitazione 6 - Proprietà ColligativeDocumento1 paginaEsercitazione 6 - Proprietà ColligativeFabrizioNessuna valutazione finora
- Brady Soluzioni Cap15Documento4 pagineBrady Soluzioni Cap15ElenaNessuna valutazione finora
- Rippa 07Documento33 pagineRippa 07Bon MafNessuna valutazione finora
- Substàncies Pures I MesclesDocumento14 pagineSubstàncies Pures I MesclesBalearikNessuna valutazione finora
- Corso Chimica - 5 SoluzioniDocumento46 pagineCorso Chimica - 5 SoluzioniGuenhNessuna valutazione finora
- Proprieta Delle Soluzioni - Parte 1Documento34 pagineProprieta Delle Soluzioni - Parte 1Elisa CirilloNessuna valutazione finora
- Lezione 15-16 2020 Concentrazioni, Reazioni e RedoxDocumento33 pagineLezione 15-16 2020 Concentrazioni, Reazioni e Redoxfake frndNessuna valutazione finora
- Modulo 43 Soluzioni Proprieta colligativeDEFDocumento39 pagineModulo 43 Soluzioni Proprieta colligativeDEFOmero CiavattaNessuna valutazione finora
- Chimica DicembreDocumento26 pagineChimica DicembresaniaNessuna valutazione finora
- Le-Soluzioni, Il Numero Di Moli e La Molarità-1Documento41 pagineLe-Soluzioni, Il Numero Di Moli e La Molarità-1Gabriele VisentinNessuna valutazione finora
- 13 Soluzioni 22Documento10 pagine13 Soluzioni 22sossiocostanzo24Nessuna valutazione finora
- Lezione 21 - 19 - 11 - 2020Documento34 pagineLezione 21 - 19 - 11 - 2020Luigi BellancaNessuna valutazione finora
- Soluzioni e Loro Preparazione30Documento40 pagineSoluzioni e Loro Preparazione30Andrea BacciNessuna valutazione finora
- Soluzioni e ConcentrazioniDocumento21 pagineSoluzioni e ConcentrazioniTotano ArrabbiatoNessuna valutazione finora
- Laboratorio Quimica Analitica2Documento6 pagineLaboratorio Quimica Analitica2Daily VargasNessuna valutazione finora
- Q ConcentrazioneDocumento27 pagineQ ConcentrazioneAnonymous r3MoX2ZMTNessuna valutazione finora
- ChimicaDocumento2 pagineChimicaShams NasrNessuna valutazione finora
- Lezione 13 - Le Soluzioni - Proprieta ColligativeDocumento47 pagineLezione 13 - Le Soluzioni - Proprieta Colligativesossiocostanzo24Nessuna valutazione finora
- Esercizi ChimicaDocumento7 pagineEsercizi ChimicagattullomNessuna valutazione finora
- Laboratorio Quimica Analitica2Documento7 pagineLaboratorio Quimica Analitica2Daily VargasNessuna valutazione finora
- 10-Proprieta - ColligativeDocumento26 pagine10-Proprieta - ColligativeHernan MarianiNessuna valutazione finora
- Le SoluzioniDocumento23 pagineLe SoluzioniFrancesco Torrettaro100% (1)
- Lezioni Di Chimica - 6 - Lo Stato LiquidoDocumento34 pagineLezioni Di Chimica - 6 - Lo Stato LiquidoKlei KleiNessuna valutazione finora
- Conc DiluizioniDocumento6 pagineConc Diluizionidorelia_simonaNessuna valutazione finora
- 2019 - LEZIONE PRATICA ESAME STATO 2x1Documento22 pagine2019 - LEZIONE PRATICA ESAME STATO 2x1alexsseverinoNessuna valutazione finora
- Infor. 3 QuimicaDocumento7 pagineInfor. 3 QuimicaCristian González TatésNessuna valutazione finora
- Assorbimento (13-03-2018)Documento12 pagineAssorbimento (13-03-2018)Valerio CurcioNessuna valutazione finora
- 04 - SoluzioniDocumento32 pagine04 - SoluzioniRoberta ZamparelliNessuna valutazione finora
- Valitutti Concettiblu Proprieta Soluzioni Cap17Documento39 pagineValitutti Concettiblu Proprieta Soluzioni Cap17fake frndNessuna valutazione finora
- Ideedellachimica Cap 14Documento45 pagineIdeedellachimica Cap 14lobocchiarovalentinaNessuna valutazione finora
- Solutii MedicamentoaseDocumento64 pagineSolutii MedicamentoaseAlexandra Scurtu0% (1)
- Le Soluzioni - ChimicaDocumento7 pagineLe Soluzioni - Chimicadavide pudduNessuna valutazione finora
- Slides 8 ADocumento40 pagineSlides 8 Afake frndNessuna valutazione finora
- Test Di Solubilita Final2 1 PDFDocumento13 pagineTest Di Solubilita Final2 1 PDFAzu AzucenaNessuna valutazione finora
- Calcolo Dei FarmaciDocumento12 pagineCalcolo Dei FarmacilarisutzafNessuna valutazione finora
- Scienze - Proprietà Delle SoluzioniDocumento5 pagineScienze - Proprietà Delle SoluzioniAndrea VenaNessuna valutazione finora
- Concentrazioni e RapportiDocumento4 pagineConcentrazioni e RapportiMassimiliano EssolitoNessuna valutazione finora
- Clases 2 IQU 530023Documento79 pagineClases 2 IQU 530023AndresChacanaNessuna valutazione finora
- Chimica Mappa - Concettuale - MolaritDocumento1 paginaChimica Mappa - Concettuale - MolaritandtreaNessuna valutazione finora
- Chimica II EsoneroDocumento36 pagineChimica II EsoneroGianni CataniaNessuna valutazione finora
- CHIMICADocumento4 pagineCHIMICAsupersamugearNessuna valutazione finora
- SoluzioniDocumento6 pagineSoluzionibhuNessuna valutazione finora
- Le Soluzioni-TestDocumento3 pagineLe Soluzioni-TestLuigiNessuna valutazione finora
- 1.introduzione. Soluzioni - Preparativa PDFDocumento107 pagine1.introduzione. Soluzioni - Preparativa PDFbobNessuna valutazione finora
- Le Soluzioni PDFDocumento54 pagineLe Soluzioni PDFLuca MagnoNessuna valutazione finora
- Lab Bichimica ItaDocumento22 pagineLab Bichimica ItaIvan Alberto NinaNessuna valutazione finora
- Lezione 24 Chimica - YMP1 - AllegatoDocumento46 pagineLezione 24 Chimica - YMP1 - AllegatoFrancesco CarrozzoNessuna valutazione finora
- Informe Fisicoquimica.Documento4 pagineInforme Fisicoquimica.Laura CastroNessuna valutazione finora
- Saggio Alla FiammaDocumento2 pagineSaggio Alla FiammaFilippo SannaNessuna valutazione finora
- Concentrazioni Delle Soluzioni AcquoseDocumento5 pagineConcentrazioni Delle Soluzioni Acquoseelia dettiNessuna valutazione finora
- Lezionevii ProprietàcolligativeDocumento22 pagineLezionevii ProprietàcolligativefpezNessuna valutazione finora
- Relazione Di ChimicaDocumento2 pagineRelazione Di ChimicaCarmelo farandaNessuna valutazione finora
- Sistema Immunitario Sprint Pack Pro MedDocumento1 paginaSistema Immunitario Sprint Pack Pro MedAntonio BifulcoNessuna valutazione finora
- Carbonioeidrocarburi PDFDocumento1 paginaCarbonioeidrocarburi PDFTommaso BorsiNessuna valutazione finora
- Simulazione 4Documento28 pagineSimulazione 4Antonio BifulcoNessuna valutazione finora
- Tavola Periodica Con Immagini1 PDFDocumento1 paginaTavola Periodica Con Immagini1 PDFGinevra VINessuna valutazione finora
- Onu Sprint Pack Pro MedDocumento1 paginaOnu Sprint Pack Pro MedAntonio BifulcoNessuna valutazione finora
- Struttura Dell'onu: L'assemblea Generale: Il Consiglio Di SicurezzaDocumento1 paginaStruttura Dell'onu: L'assemblea Generale: Il Consiglio Di SicurezzaAntonio BifulcoNessuna valutazione finora
- Autori 900Documento9 pagineAutori 900Antonio BifulcoNessuna valutazione finora
- Principi Costituzione ItalianaDocumento1 paginaPrincipi Costituzione ItalianaAntonio BifulcoNessuna valutazione finora
- Nuove Cond - MediciDocumento2 pagineNuove Cond - MediciAntonio BifulcoNessuna valutazione finora
- Costituzione ItalianaDocumento1 paginaCostituzione ItalianaAntonio BifulcoNessuna valutazione finora
- 5 - GametogenesiDocumento34 pagine5 - GametogenesiAntonio BifulcoNessuna valutazione finora
- Le Idee Della ChimicaDocumento37 pagineLe Idee Della ChimicaAntonio BifulcoNessuna valutazione finora
- Vademecum Giovane Medico PDFDocumento84 pagineVademecum Giovane Medico PDFParide Di StasioNessuna valutazione finora
- Acidi e Basi 2Documento6 pagineAcidi e Basi 2Antonio BifulcoNessuna valutazione finora
- Fase Luminosa e FotosistemiDocumento8 pagineFase Luminosa e FotosistemipippochiriNessuna valutazione finora
- Olio Di OlivaDocumento51 pagineOlio Di Olivaemiliano ragoni100% (2)
- Esercizi IDocumento2 pagineEsercizi IAriannaNessuna valutazione finora
- Notiz 2008Documento14 pagineNotiz 2008Fabrizio CervelliNessuna valutazione finora
- 1019 - Mapewrap Eq Adhesive - It PDFDocumento2 pagine1019 - Mapewrap Eq Adhesive - It PDFEdgar TorresNessuna valutazione finora