Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Circ Fet
Caricato da
Giugi FalchiTitolo originale
Copyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Circ Fet
Caricato da
Giugi FalchiCopyright:
Formati disponibili
LA CIRCOLAZIONE FETALE La circolazione ombelicale-placentare un sistema circolatorio extracorporeo che viene abbandonato alla nascita quando drastici cambiamenti
i si verificano facendo si che la funzione di scambio dei gas venga trasferita dalla placenta ai polmoni. La circolazione feto-placentare garantisce gli scambi respiratori e nutrizionali tra madre e feto ed resa possibile da strutture destinate a scomparire al momento della nascita: cordone ombelicale e placenta strutture cardiache (dotto di Botallo, Forame ovale e Crista dividens) extracardiache (Dotto Venoso di Aranzio)
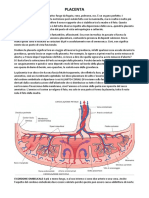
Placenta La placenta un organo deciduo, quindi temporaneo, che si forma nell'utero durante la gravidanza. La placenta deputata a nutrire, proteggere e sostenere la crescita fetale. La placenta comune alla gestante ed al feto; una sua parte, infatti, ha origini materne (costituita dall'endometrio uterino modificato o decidua), mentre la rimanente ha origini fetali (formata dai villi coriali). La placenta, quindi, rappresenta le radici del feto nel terreno della madre. - I villi coriali sono prolungamenti molto vascolarizzati e generati dallo strato di cellule embrionali pi esterno (il corion), che si ramifica affondando nella mucosa uterina (endometrio).
L'endometrio
dell'utero trasformato per la gravidanza chiamato decidua ed costituito da cellule deciduali, molto grosse e ricche di glicogeno e lipidi. Funzioni della placenta La funzione primaria della placenta di permettere gli scambi metabolici e gassosi tra il sangue fetale e quello materno. Feto e placenta comunicano tramite il cordone ombelicale o funicolo, mentre la madre comunica direttamente con la placenta attraverso lacune ripiene di sangue (lacune sanguigne), dalle quali "pescano" i villi coriali.
I vasi ombelicali comprendono una vena ombelicale - che trasporta sangue ossigenato e ricco di nutrienti dalla placenta al feto - e le arterie ombelicali, al cui interno scorre sangue ricco di cataboliti che dal feto vanno alla placenta. Le funzioni di questo organo sono assai numerose, dal momento che esso funge da: polmone: fornisce ossigeno al feto ed allontana l'anidride carbonica; questi gas diffondono facilmente attraverso il sottile strato di cellule che separa i villi coriali dal sangue materno. Rene: depura e regola i liquidi corporei del feto. Apparato digerente: procura e fornisce nutrienti; la placenta permeabile a molte sostanze nutritive presenti nel sangue della madre, come glucosio, trigliceridi, proteine, acqua ed alcune vitamine e sali minerali. Sistema immunitario: consente il passaggio degli anticorpi per endocitosi ma impedisce quello di molti patogeni (fanno eccezione, ad esempio, i virus della rosolia e i protozoi della toxoplasmosi). Barriera protettiva: la placenta impedisce il passaggio di molte sostanze dannose, anche se alcune possono comunque attraversarla e nuocere al feto (caffeina, cocaina, alcol, alcuni farmaci, nicotina ed altre sostanze cancerogene presenti nel fumo di sigaretta...). La placenta ha anche un'importantissima funzione endocrina. Sin dai primi stadi del suo sviluppo, infatti, secerne gonadotropina corionica umana (hCG), un ormone simile all'LH che sostiene la produzione di progesterone da parte del corpo luteo, importante per stimolare la sintesi di testosterone nei testicoli in via di sviluppo del feto maschio. La placenta secerne altri ormoni, come il lattogeno placentale umano, gli estrogeni (che inibiscono la maturazione di altri follicoli), il progesterone (che impedisce le contrazioni uterine e sostiene l'endometrio) ed altri ancora (tra cui inibina, prolattina e pronenina).
Dal punto di vista anatomico tali strutture costituiscono tre sedi di shunt e permettono di saltare distretti ad alta resistenza e a basso flusso: 1) Dotto venoso di Aranzio, comunicazione vascolare tra vena ombelicale e vena cava inferiore che permette a quantit variabili di sangue di saltare il fegato. 2) Forame ovale, (comunicazione interatriale) il sangue che arriva allatrio destro pu direttamente passare nellatrio e quindi nel ventricolo sinistro . 3) Dotto di Botallo, collega direttamente l'arteria polmonare con l'aorta discendente escludendo la circolazione polmonare.
Lapparato circolatorio fetale raggiunge lo sviluppo anatomico definitivo alla 10masettimana di et gestazionale. Il feto a 6-7 settimane ha una frequenza cardiaca di 160-170 battiti per minuto (bpm), mentre alla nascita di 130 140 bpm. Il centro cardioregolatore molto sensibile alle variazioni di pressione parziale di ossigeno, di conseguenza la frequenza cardiaca fetale rappresenta un precoce sistema di allarme per l'identificazione dell'ipossia in atto.
Nella circolazione fetale si hanno distretti ad alto flusso ed a bassa resistenza (placenta) e distretti a basso flusso e ad elevata resistenza (polmone e fegato). Questa resistenza e la presenza degli shunt fanno si che il flusso del sangue nei polmoni fetali non superi mai l'8-10% della gittata cardiaca. I ventricoli destro e sinistro del cuore, a causa dell esistenza dei due particolari canali vascolari , foro ovale e dotto arterioso, lavorano in parallelo per pompare in aorta sangue ben ossigenato proveniente dalla placenta attraverso la vena ombelicale . La circolazione fetale estremamente complessa: tutte le modificazione anatomo-funzionali sono finalisticamente programmate per affrontare condizioni fisiologiche di ipossia come il travaglio di parto .
Il sangue ossigenato della placenta arriva al feto attraverso la vena ombelicale. Questa dopo esser penetrata attraverso l'ombelico nel corpo fetale, si suddivide in due rami: uno va a irrorare il fegato mentre l'altro 50% del sangue della vena ombelicale (saturato all80% in O2) non attraversa il fegato ma lo shunta tramite il Dotto venoso di Aranzio,
sfociando nella vena cava inferiore, nella quale fluisce anche il sangue deossigenato proveniente dagli arti inferiori riducendo cos la saturazione al 70% circa. Attraverso la vena cava inferiore, il sangue penetra nellatrio dx. Latrio dx fetale, in corrispondenza dello sbocco della vena cava inferiore, presenta una formazione (crista dividens o valvola di Eustachio) che convoglia la corrente sanguigna verso il setto interatriale, dove presente il foro ovale che mette in comunicazione i due atri. Una volta attraversato il forame ovale,questo sangue con una elevata tensione di O2, passa dallatrio al ventricolo sinistro, saturato in O2 al 70%, passa nel tratto ascendente dellaorta e da qui va ad irrorare i vasi cerebrali e degli arti superiori perci il cuore e il cervello possono giovarsi di maggiore ossigenazione rispetto agli organi della parte bassa del corpo. Nellatrio sinistro giunge anche il sangue che proviene dai polmoni mediante le quattro vene polmonari. Dalla parte superiore del corpo il sangue, notevolmente meno ossigenato, ritorna, mediante la vena cava superiore all'atrio dx e da questo, attraverso la valvola tricuspide piuttosto che il forame ovale, fluisce nel ventricolo dx. Dal ventricolo dx, attraverso larteria polmonare, una piccola quantit di sangue arriva ai polmoni del feto (circa il 10% a causa delle elevate resistenze del piccolo circolo), mentre la maggior parte attraverso il dotto di Botallo, si riversa nell'aorta discendente,la saturazione in O2 del sangue nellaorta discendente e nelle arterie seguenti valutabile attorno al 60%. Di conseguenza i vasi che originano dallarco aortico ,che vascolarizzano la testa e gli arti superiori, contengono sangue con una tensione di O2 superiore a quella presente nel tratto dellaorta discendente. Una parte di questo sangue va ad irrorare la parte inferiore del corpo, per poi rientrare nella vena cava inferiore attraverso il circolo venoso refluo, l'altra parte passa nelle arterie ombelicali e raggiunge la placenta. E' importante sottolineare come nell'organismo fetale nessun apparato irrorato da sangue esclusivamente arterioso, in quanto il sangue arterioso proveniente dalla placenta per mezzo della vena ombelicale si mescola: 1) nella vena cava inferiore, con il sangue venoso proveniente dalla parte inferiore del corpo attraverso la vena cava inferiore stessa e con il
sangue convogliato dal sistema portale mediante le vene sovraepatiche; 2) nell'atrio destro, con il sangue venoso proveniente dalla met superiore del corpo (la commistione solo parziale); 3) nell'atrio sinistro, dopo aver attraversato l'atrio destro ed il foro Ovale, si mescola allo scarso sangue venoso proveniente dalle vene polmonari; 4) nell'aorta, dopo lo sbocco del dotto di Botallo. Il sangue fluente in aorta si ripartisce per il 60% in placenta e per il 40% agli altri organi. Esiste una maggiore affinit dell Hb fetale per lossigeno che compensa la bassa saturazione in O2 del sangue fetale. Poich nella circolazione fetale si hanno distretti ad alto flusso ed a bassa resistenza (placenta) e distretti a basso flusso e ad elevata resistenza (polmone e fegato). Le resistenze arteriolari polmonari sono cos elevate che il flusso ematico polmonare ridotto tanto da non superare il 7-8 % della gittata cardiaca totale. Nella circolazione sistemica fetale la resistenza al flusso ematico bassa fisiologicamente a causa della alta capacitanza placentare. La bassa PaO2 sistemica fetale (circa 25 mmHg) insieme alla produzione locale di prostaglandine, mantiene pervio il dotto arterioso fetale. A causa delle elevate resistenze polmonari, il sangue proveniente dal ventricolo dx scorre da dx a sin : dallarteria polmonare, attraverso il dotto arterioso, nellaorta. Nel feto la pressione atriale sinistra relativamente bassa a causa del ridotto ritorno ematico polmonare , mentre la pressione atriale destra relativamente alta per il notevole ritorno ematico dalla placenta; la differenza di pressione tra i due atri mantiene pervio il foro ovale e permette al sangue di passare dallatrio dx al sinistro. Alla nascita, dopo i primi atti respiratori, che determinano laumento del flusso ematico polmonare, si verifica una profonda modificazione a livello della circolazione: - le resistenze arteriolari polmonari cadono improvvisamente come
risultato della vasodilatazione derivante dallespansione polmonare, dallaumentata PaO2, e dalla ridotta PaCO2, infatti lintroduzione daria determina a livello alveolare uninterfaccia aria-liquido che favorisce il collasso alveolare; queste forze sono contrastate dalle forze elastiche delle costole e della parete toracica. Di conseguenza cade la pressione interstiziale polmonare, determinando un ulteriore aumento del flusso ematico attraverso i capillari polmonari. Quando il flusso ematico polmonare si stabilizza, il ritorno venoso polmonare aumenta e la pressione in atrio sinistro si innalza. Lintroduzione daria fa aumentare la PaO2 , determinando la costrizione delle arterie ombelicali, il flusso ematico placentare si riduce o cessa del tutto e si riduce il ritorno ematico allatrio destro. In tal modo la pressione atriale destra si riduce, aumenta la pressione atriale sinistra : il risultato la chiusura del forame ovale. Subito dopo la nascita dunque le resistenze sistemiche superano quelle polmonari e si ha un inversione rispetto alla situazione fetale. La direzione del flusso ematico attraverso il dotto arterioso pervio si inverte, creando uno shunt ematico sinistro-destro denominato CIRCOLAZIONE DI TRANSIZIONE Questa situazione persiste subito dopo la nascita (quando aumenta il flusso ematico polmonare e si verifica la chiusura funzionale del foro ovale) fino a circa 24h di vita, quando si ha la chiusura del dotto arterioso. Il sangue proveniente dallaorta che entra nel dotto arterioso e nei suoi vasa vasorum ha unalta PaO2 che, insieme alle variazioni del metabolismo delle prostaglandine, determina una vasocostrizione e la chiusura del dotto arterioso. Al momento della chiusura del dotto arterioso si instaura la circolazione di tipo adulto: i due ventricoli iniziano a pompare in serie e non esistono pi shunt maggiori tra la circolazione polmonare e sistemica. Durante i primi giorni di vita, in caso di distress respiratorio neonatale, si pu avere il ritorno ad una circolazione di tipo fetale: lasfissia ,con ipossia e ipercapnia, causa la vasocostrizione delle arteriole polmonari e la
dilatazione del dotto arterioso con inversione dei processi sopra descritti e con la realizzazione di uno shunt dx- sin attraverso il dotto arterioso nuovamente pervio e/o il forame ovale riaperto. Di conseguenza il neonato presenta una grave ipossiemia, condizione questa denominata ipertensione polmonare persistente o circolazione polmonare persistente (senza, ovviamente, circolazione placentare).
Displasia Congenita dellAnca Complesso di anomalie di sviluppo e di conformazione dei componenti articolari, i quali, per la conseguente incongruenza e per effetto dei movimenti, vengono a perdere i normali rapporti reciproci. Sotto questa definizione vengono inclusi tutti i diversi gradi di alterato sviluppo dellarticolazione coxo-femorale la cui precisa caratterizzazione risulta in rapporto al metodo di indagine utilizzato ai fini diagnostici . Epidemiologia attualmente l'incidenza viene stimata tra 4,5 e 5 per 1000 nati. L'affezione prevale nettamente nel sesso femminile (rapporto M/F=1:6), pi spesso monolaterale (75% dei casi) ed i frequente a sinistra. Eziopatogenesi E' tipicamente multifattoriale: fattori meccanici: presentazione podalica: sintende: un bambino in situazione longitudinale (con il suo asse longitudinale parallelo allasse longitudinale dellutero) ma con il podice (sedere e/o gambe e piedi), e non la testa, che si affaccia in basso allingresso del canale del parto. Oligoidramnios: un patologia che vede la presenza di poco liquido amniotico e pu essere dovuta ad un ritardo di crescita intrauterino oppure ad un forte stress materno oppure ancora alla scarsa assunzione di liquidi. Malformazioni congenite muscoloscheletriche, vizi di posizione intrauterina, abnormi sollecitazioni articolari lassit legamentosa: secondaria verosimilmente a fattori ormonali (maggior secrezione di estrogeni); ipertono muscolare dei flessori e degli adduttori; fattori genetici: la familiarit stata dimostrata in circa il 25-30% dei casi. Diagnosi Le indagini utili per una diagnosi precoce della DCA prevede:
l'esame clinico che presenta una sensibilit variabile dal 35 al 60% in rapporto anche all'esperienza dell'esaminatore Le manovre diagnostiche idonee all'esame clinico sono: Manovra di Ortolani: si pratica con paziente supino, sdraiato su un piano rigido, adbucendo delicatamente le cosce, flesse a formare un angolo di 90 con il bacino e le gambe. Le dita dell'esaminatore, appoggiate in corrispondenza del grande trocantere e con il pollice sul piccolo trocantere, esercitano contemporaneamente una pressione in senso mediale e verso l'alto. La testa femorale, se dislocata, torna a occupare la cavit acetabolare, facendo percepire uno scatto (scatto d'entrata) all'operatore: se presente, il segno di Ortolani indice di lussazione; Manovra di Barlow : a paziente supino, con le mani posizionate come sopra detto sulle cosce flesse e in posizione di semi-abduzione , l'esaminatore adduce delicatamente le cosce stesse, esercitando con il palmo della mano appoggiato sul ginocchio una lieve pressione verso il basso e, con il pollice nel piccolo trocantere, verso l'esterno. La testa femorale, in caso di anca lussabile, pu abbandonare la cavit acetabolare e, superando il cercine glenoideo, provocare lo scatto d'uscita: il riscontro di questo segno indice di anca lussabile. Le manovre di Ortolani e Barlow devono essere sempre praticate nel primo esame obiettivo del neonato e in seguito ripetute, ricordando tuttavia che esse non sono pi significative dopo i 2 mesi, in quanto successivamente la lassit articolare si riduce, mentre aumenta la tensione degli adduttori. In questa fase pi tardiva, pu essere utilizzata la manovra di Galeazzi, che si esegue ponendo il bambino supino con le anche e le ginocchia flesse: in caso di lussazione, compare un accorciamento apparente del femore, in quanto le due ginocchia risultano disallineate. L'esame ecografico ha una specificit e una sensibilit che si avvicina al 100% eper tanto viene applicato in modo sistematico come test di screening. Va praticato: - all'et di 8-12 settimane, in tutti i neonati; - nel primo mese di vita, nei soggetti con esame clinico positivo alla nascita e/o con fattori di rischio di anamnisi,
- comunque entro il terzo mese - Il metodo pi diffuso per lo studio ecografico dell'anca del neonato quello morfologico di Graf, che consente, in maniera riproducibile, alcune misurazioni sulle immagini ottenute, tali da definire una precisa stadiazione di ciascuna anca studiata, cui corrispondono una situazione anatomopatologica e l'indirizzo prognostico e terapeutico. L'esame radiografico (Rx bacino per anche) non significativo nel neonato, divenendo attendibile solo verso il 4 mese.
PIEDE TORTO CONGENITO Il piede torto congenito (PTC) una deformit gi presente alla nascita, caratterizzata dalla deviazione degli assi anatomici del piede tra di loro e rispetto a quelli della gamba con conseguente modificazione dei punti di appoggio. Il termine piede torto congenito comprende un gruppo di malformazioni del piede di entit variabile che hanno come caratteristica comune una deviazione degli assi anatomici con conseguente modificazione dei normali punti di appoggio ed alterazione della funzione. Eziopatogenesi Leziologia incerta anche se sono state avanzate varie teorie come quella genetica, quella embrionaria e quella meccanica. Secondo la teoria genetica, lalterazione agirebbe sullo sviluppo del piede in epoca embrionaria non consentendo il fisiologico processo di maturazione. Secondo la teoria embrionaria esistono dei fattori esterni ambientali che possono determinare larresto di sviluppo del piede. La teoria meccanica prevede lesistenza di svariate condizioni uterine (briglie amniotiche, oligoidramnios, cordone ombelicale, neoplasie uterine, ecc) o fetali (microsomia, parti gemellari, ecc) in grado di determinare un alterato rapporto tra contenente (utero) e contenuto (feto). In questi casi pi opportuno parlare di malposizione che di malformazione congenita e la prognosi sicuramente migliore. Il PTC presenta una incidenza maggiore nei maschi rispetto alle femmine (rapporto 3:1); nel 50% dei casi bilaterale, si pu presentare come
deformit isolata o associata ad altre come torcicollo miogeno, lussazione congenita di ginocchio, displasia congenita danca, della quale ne rappresenta spesso lelemento spia. Leredo-familiarit dimostrata nel 15% dei casi ed frequente il suo riscontro nel contesto di osteodisplasie genotipiche e sindromi dismorfiche dello scheletro. Ha tendenza a recidivare sino allet di 5-7 anni. Diagnosi Clinicamente la deformit facilmente riconoscibile gi dalla nascita anche se laffinamento delle tecniche di ecografia ostetrica consente di fare diagnosi gi in epoca prenatale. La prognosi correlata al grado di deformit e alla precocit del trattamento terapeutico. E importante distinguere il piede torto idiopatico, non associato a cause specifiche, da quello secondario, legato ad altre malattie quali artrogriposi, distrofie muscolari, spina bifida ecc. Il PTC idiopatico costituisce la stragrande maggioranza dei casi, e colpisce 1,24 su 1000 nati. Classificazione Vengono distinte pi variet: piede equino-varo-addotto-supinato (85% dei casi), talo-valgo (10%) e metatarso-addotto (5%)e piede equino-valgo. In generale, quando si parla di piede torto congenito ci si riferisce sempre alla variet pi frequente; il piede si presenta in equinismo, ovvero in flessione plantare con appoggio esclusivamente sullavampiede, in varismo, con lasse longitudinale del retropiede deviato allinterno rispetto alla gamba, in supinazione ed in adduzione con conseguente rotazione interna della superficie plantare e deviazione dellavampiede verso linterno. Inizialmente le alterazioni sono a carico dei tessuti molli (tendini, capsule, legamenti), che posteriormente ed internamente si presentano retratti; solo successivamente, con il persistere dellalterazione dei normali rapporti degli abbozzi cartilaginei del piede, in assenza di adeguata terapia, si verifica linteressamento del tessuto osseo ed il conseguente appoggio sulle superficie laterale con grave danno funzionale alle strutture anatomiche pi prossimali (ginocchio, anca e colonna) ed alla
deambulazione. Piede equino varo-supinato-addotto E' l'anomalia congenita del piede pi frequente, con un'incidenza da 1 a 4 su 1000 nati; spesso bilaterale. Nel 10% dei casi associato ad altre malformazioni, in particolare con la lussazione congenita dell'anca.
VEDI QUADERNO
La diagnosi si basa esclusivamente sul quadro clinico, avendo lesame radiografico, almeno inizialmente, un valore limitato dalla presenza di cartilagine che nei primi anni di vita extrauterina non si ancora ossificata. La radiologia convenzionale, comunque, pu fornire informazioni utili, cos come la risonanza magnetica, riguardo la morfologia delle singole ossa mentre lindagine ecografica consente una valutazione dinamica del piede torto. Dal punto di vista classificativo, a seconda della possibilit di correggere il piede torto e in base allentit angolare del varismo, si distinguono tre gradi: I grado: la malformazione facilmente correggibile ed il piede forma sul piano frontale un angolo mediale maggiore di 90 rispetto allasse longitudinale della tibia; II grado: la malformazione risulta difficilmente correggibile ed il piede, invece, forma sul piano frontale un angolo mediale di 90 rispetto allasse longitudinale della tibia; III grado: la malformazione si presenta incorreggibile ed il piede forma sul piano frontale un angolo mediale inferiore di 90 rispetto allasse longitudinale della tibia.
Terapia La prognosi e correlata al grado di deformit e alla precocit del trattamento terapeutico.
Il trattamento conservativo, almeno inizialmente, ma pu divenire cruento se il risultato funzionale non soddisfacente (appoggio plantigrado non ottimale, scarsa mobilit, o presenza di sintomatologia dolorosa): esso si basa sullesecuzione di modellamenti manuali a tappe, tendenti a correggere la deformit e, sul confezionamento di apparecchi gessati femoro-podalici che devono essere rinnovati settimanalmente almeno per le prime 7-10 settimane. Tali manovre correttive devono essere graduali per evitare lo schiacciamento dei nuclei di accrescimento, consentendo nello stesso tempo ladattamento delle strutture vasculonervose alle nuove posizioni. Il periodo utile per eventuali interventi chirurgici deve iniziare non appena ci si rende conto che la deformit non cede al modellamento manuale. Il trattamento cruento varia da interventi semplici sulle parti molli che possono interessare solo il tendine di Achille o estendersi alle articolazioni posteriori e/o mediali del piede. Gli interventi sullo scheletro sono riservati a piedi torti trascurati o alle recidive. A fine trattamento obbligatorio lutilizzo di tutori e calzature ortopediche per prevenire la recidiva, temibile e possibile complicanza. Il trattamento del piede torto congenito ha subito nel corso degli anni notevoli miglioramenti. Fino agli anni cinquanta stato universalmente accettato lapproccio esclusivamente chirurgico, quale per esempio quello della capsulotomia posteriore secondo Kite, basato sullapertura delle articolazioni sotto-astragaliche, della tibio-tarsica e della astragalocalcaneare. La svolta decisiva verso un trattamento pi adeguato e meno invasivo, si avuta dopo la seconda met degli anni cinquanta, quando un chirurgo ortopedico argentino, Ignacio Ponseti, vissuto ad Iowa City, ha sviluppato un metodo efficace ed economico. Secondo Ponseti, il trattamento del piede torto congenito pu essere intrapreso, se possibile, subito dopo la nascita. Nella maggior parte dei casi, la malformazione pu essere corretta in 6 settimane circa grazie a brevi e delicate manipolazioni con cadenza settimanale, seguiti dalla applicazione di 6-7 apparecchi gessati femoro-podalici a ginocchia flesse. Il ricorso alla chirurgia limitato ad una tenotomia percutanea del tendine di Achille, necessaria per ultimare la correzione dellequinismo; ultimata questa fase al piede si esegue immobilizzazione con apparecchio gessato per ulteriori 6 settimane. Il grado di correzione raggiunto viene conservato successivamente da un tutore che mantiene il piede in abduzione e va
indossato durante la notte fino ad unet variabile tra i 2 e i 4 anni.
Amelia: assenza totale dellarto Focomelia: assenza del segmento prossimale dellarto Emimelia trasversale : assenza della met distale dellarto RIFLESSI DEL NEONATO Moro : limprovvisa estensione del capo provoca prima lestensione e poi la flessione delle gambe e delle braccia . Et di comparsa: nascita Et di scomparsa: 4-6 mesi Origine : Nuclei vestibolari del tronco Grasp : Ponendo un dito sul palmo della mano del neonato si ottiene una flessione delle dita sul palmo Et di scomparsa: 4-6 mesi Origine : Nuclei vestibolari del tronco Suzione : uno stimolo tattile vicino alla bocca provoca la suzione Et di comparsa: nascita Et di scomparsa: > 6 mesi Origine : sistema Trigeminale Incurvatura del tronco provocata da stimolazione sul margine ventrale . Et di comparsa: nascita Et di scomparsa: 6-9 mesi Origine : Midollo spinale Piazzamento : Il bambino appoggia il piede sul lettino quando il dorso del piede viene in contatto con il bordo del lettino.
Et di comparsa: nascita Et di scomparsa: 4-6 mesi Origine : corteccia Estensione crociata : una gamba tenuta saldamente in estensione e il dorso e la pianta del piede stimolati: sequenza di flessione, estensione e adduzione seguita da movimento a ventaglio delle dita del piede dellaltra gamba. Et di comparsa: nascita Et di scomparsa: 4-6 mesi Origine : Midollo spinale Tonico del collo : a bambino supino , facendo girare la testa si ha unestensione omolaterale del braccio e della gamba Et di comparsa: nascita Et di scomparsa: 4-6 mesi Origine : Nuclei vestibolari del tronco Paracadute: Spingendo lateralmente il bambino seduto, questi estende il braccio omolaterale in senso protettivo. Et di comparsa: 6-8 mesi Et di scomparsa: mai Origine : Nuclei vestibolari del tronco Landau: Con il bambino tenuto alla cintola e sospeso , lestensione del collo provoca estensione delle braccia e delle gambe. Et di comparsa: 6-8 mesi Et di scomparsa: 15-24 mesi Origine : Tronco
LEQUILIBRIO ACIDO-BASE L'equilibrio acido-base un processo dinamico che ha il compito di mantenere il pH dei liquidi organici entro i range della normalit. Il meccanismi preposti a questo scopo sono 3: Tempo di azione Frazioni di secondo 1-15 minuti ore-giorni
1) Sistemi tampone acido-base 2) Polmoni: Ventilazione 3) Reni: eliminazione di urina acida o alcalina
1) I sistemi tampone, sono presenti nei compartimenti intra ed extracellulari, che si oppongono alle variazioni del pH del mezzo. Il sistema acido carbonico/bicarbonato copre il 53% della capacit tampone dell'organismo. Il bicarbonato si lega agli ioni H formando un sale neutro e acido carbonico. L'acido carbonico si scinde in acqua e anidride carbonica che viene eliminata dal polmone attraverso la ventilazione. Il sistema tampone bicarbonato/acido carbonico il pi importante per tre motivi fondamentali : uno, perch presente in quantit maggiori rispetto agli altri; due, perch il pi ubiquitario (fluido interstiziale, plasma, eritrociti, cellule, ossa); tre, perch lunico sistema che ha due vie di sfogo: una, rapida, attraverso i polmoni trasformandosi in CO2 (che viene eliminata immediatamente in pochi minuti) e laltra trasformandosi in bicarbonato
ed idrogenioni, i quali ultimi vengono eliminati con il rene. Il fondamentale segreto del suo successo che lacido carbonico lunico (tra tutti i sistemi tampone) ad avere una scappatoia allesterno trasformandosi in qualche cosa di volatile (CO2), mentre lacqua residua non ha pi valore dal punto di vista dellequilibrio acido-base. Il rene collabora bene, per pi lento ad entrare in azione, ed impiega almeno 8-12 ore solo per dare inizio alla sua azione (se fosse solo per il rene moriremmo tutti nelle fasi acute). Una volta avviato il suo compenso, per, esso rimane stabile ed il suo contributo determinante, in quanto se non ci fosse nel rene il recupero dei bicarbonati si assisterebbe al loro completo consumo in pochi giorni. 2) meccanismo respiratorio svolge un intervento rapido, eliminando Co2 mediante modificazioni della ventilazione alveolare, che a loro volta si realizzano in base a valori del pH e della pCO2. 3) meccanismo renale costituisce l'intervento pi lento e si avvale dei processi di escrezione e di riassorbimento dei bicarbonati, di escrezione dei fosfati inorganici, dell'ammoniaca e degli acidi organici.
Nel neonato l'omeostasi dell'equilibrio acido-base riflette la progressiva maturazione dei meccanismi implicati nella sua regolazione: meccanismo respiratorio: gli scambi alveolo-capillari di O2 e CO2 sono possibili solo quando con la maturazione polmonare, si realizzata un'adeguata circolazione polmonare. meccanismo renale: il rene del neonato non subito in grado di assolvere le sue funzioni di eliminazione dei radicali acidi e di risparmio dei bicarbonati. Soprattutto nel pretermine la soglia renale ai bicarbonati pi bassa e l'eliminazione dell'acidit titolabile da parte del tubulo renale scarsa.
DISTURBI DELL'OMEOSTASI ACIDO-BASE Acidosi respiratoria
E' caratterizzata da diminuzione del pH arterioso (< 7.3) ed elevazione della concentrazione ematica di CO2. E' causata da tutte le condizioni in cui si ha ipoventilazione. L'accumulo di CO2 altera il sistema acido carbonico/bicarbonato con aumento dell'acidit ematica. CAUSE 1. Ipoventilazione da cause di origine nervosa o paresi dei muscoli respiratori 2. Ostacolo alla ventilazione ( x ostruzione delle vie aeree ) 3. Insufficienza respiratoria acuta e cronica ( x malattie toraco polmonari come: pneumotorace, polmoniti massive o edema polmonare ) 4. Cause iatrogene ( assunzione di narcotici e anestetici ) MECCANISMI DI COMPENSO Quando i sistemi tampone non riescono a riportare alla norma il valore del pH del sangue, sia la riduzione di questo che laumento della pCO2 determinano uno stimolo alla ventilazione, che viene amplificato anche dalla ridotta pO2 del sangue arterioso che tramite i chemocettori periferici attiva sui centri respiratori che rispondono inducendo iperventilazione polmonare. Nel momento in cui il compenso ventilatorio polmonare diventa inadeguato, interviene unulteriore possibilit di compenso da parte dellepitelio tubulare del rene che: 1. incrementa leliminazione di idrogenioni 2.maggiore riassorbimento di bicarbonato La conseguenza che il rene produce urina fortemente acida e fa aumentare la concentrazione ematica di bicarbonato. SEGNI CLINICI - Disturbi dello stato di coscienza fino al coma - Irrequietezza - Tachipnea e Dispnea - Cefalea SEGNI DI LABORATORIO - pCO2 - pH
- bicarbonati - Anion gap normale ALCALOSI METABOLICA Condizione metabolica caratterizzata da un aumento del pH ed incremento plasmatico dei bicarbonati. Subentra in conseguenza di uneccessiva perdita di idrogenioni o di un eccessiva ritenzione o somministrazione di alcali. CAUSE 1. Associata a diminuzione di H20 e Cloro per: -perdita di succhi gastrici (per vomito persistente e drenaggio gastrico; oltre agli H+ con il vomito si perdono anche K +, Cl-, Na + e H20). -Terapia diuretica ( riduce il riassorbimento prossimale di sodio e di cloro) -Alcalosi post-ipercapnia 2. Associata ad iperattivit del corticosurrene (con aumento degli ormoni corticosteroidi: diminuisce il potassio e aumenta il metabolismo anaerobico): -Sindrome di Cushing -Aldosteronismo primario 3. Deplezione potassica grave: quando viene perduto il potassio, sodio e idrogenioni si spostano nel distretto intercellulare per rimpiazzarlo. Ci causa alcalosi extracellulare 4. Introduzione eccessiva di basi MECCANISMI DI COMPENSO - Azione dei sistemi tampone (apporto di H+ nel compartimento extracellulare) - Compenso respiratorio: laumento dei bicarbonati provoca ipoventilazione - Compenso renale: aumento di escrezione dei bicarbonati e ne diminuisce il riassorbimento SEGNI CLINICI - vomito - debolezza muscolare e crampi
- gravi aritmie SEGNI DI LABORATORIO del pH, della pCO2 arteriosa e dei bicarbonati di cloro e potassio
Potrebbero piacerti anche
- Circolazione FetaleDocumento2 pagineCircolazione FetaledanielaNessuna valutazione finora
- 3 - Circolazione FetaleDocumento1 pagina3 - Circolazione FetaleRomina CasagrandeNessuna valutazione finora
- Circolazione FetaleDocumento1 paginaCircolazione FetaleGaia BorraccesiNessuna valutazione finora
- Il CuoreDocumento5 pagineIl CuoreScuola primaria "Santa Chiara d'Assisi"Nessuna valutazione finora
- Il FegatoDocumento7 pagineIl FegatoNicola BombaceNessuna valutazione finora
- APPARATIDocumento37 pagineAPPARATIWEFsNessuna valutazione finora
- PediatriaDocumento163 paginePediatriaMimmo Colella100% (1)
- Apparato Circolatorio Sanguigno Riassunto ScrittoDocumento13 pagineApparato Circolatorio Sanguigno Riassunto ScrittoStephanie KondeNessuna valutazione finora
- Sistema CardiovascolareDocumento11 pagineSistema CardiovascolareBruce WiiNessuna valutazione finora
- FluodinamicaDocumento9 pagineFluodinamicaSara CascioNessuna valutazione finora
- Apparato Cardio Circolatorio NeonatoDocumento29 pagineApparato Cardio Circolatorio NeonatoGraziana DellisantiNessuna valutazione finora
- 17 Anatomia 03-04-14Documento7 pagine17 Anatomia 03-04-14SandroNessuna valutazione finora
- Embriologia CardiovascolareDocumento6 pagineEmbriologia CardiovascolaremenafabNessuna valutazione finora
- Cuore PDFDocumento13 pagineCuore PDFNicla MontingelliNessuna valutazione finora
- Circolazione SanguignaDocumento2 pagineCircolazione Sanguignaao oniNessuna valutazione finora
- Sistema CardiocircolatorioDocumento41 pagineSistema Cardiocircolatorioeliafuma03Nessuna valutazione finora
- Anatomia PDFDocumento10 pagineAnatomia PDFFlavio BizzarriNessuna valutazione finora
- AnatomiaDocumento204 pagineAnatomiaelisabettuccia058Nessuna valutazione finora
- Apparato CircolatorioDocumento3 pagineApparato CircolatorioPopovici PavelNessuna valutazione finora
- PLACENTA InserireDocumento18 paginePLACENTA InserireandreaNessuna valutazione finora
- FisiologiaDocumento18 pagineFisiologiaGabriele BalloNessuna valutazione finora
- Toni Soffi CardiaciDocumento4 pagineToni Soffi CardiacibvincenzoNessuna valutazione finora
- Apparato CircolatorioDocumento5 pagineApparato CircolatorioAndrea FortiNessuna valutazione finora
- Sistema CircolatorioDocumento9 pagineSistema CircolatorioannaritagloriaNessuna valutazione finora
- SCIENZEDocumento4 pagineSCIENZEandrea.mandolesiNessuna valutazione finora
- Apparato CircolatorioDocumento4 pagineApparato CircolatorioLuigi BorgeseNessuna valutazione finora
- 2021 Farmacia Cardiovascolare 2 13 16 AprileDocumento67 pagine2021 Farmacia Cardiovascolare 2 13 16 AprileChiara ArdauNessuna valutazione finora
- Vena PortaDocumento3 pagineVena Portaalessan9Nessuna valutazione finora
- Di Nino Alessia, VA, L'apparato CardiocircolatorioDocumento5 pagineDi Nino Alessia, VA, L'apparato CardiocircolatorioAlessia Di NinoNessuna valutazione finora
- Sistema Nervoso, Encefalo e Nervi CraniciDocumento10 pagineSistema Nervoso, Encefalo e Nervi CraniciFrancesco FalconieriNessuna valutazione finora
- Il CuoreDocumento18 pagineIl CuorepiliNessuna valutazione finora
- Sbobine Anatomia 1Documento66 pagineSbobine Anatomia 1giorgiocaresanaNessuna valutazione finora
- FEGATODocumento2 pagineFEGATOGiulia TestinoNessuna valutazione finora
- L'apparato CircolatorioDocumento5 pagineL'apparato CircolatorioEileen Moni BidinNessuna valutazione finora
- Sistema Nervoso e Vascolarizzazione TestaDocumento56 pagineSistema Nervoso e Vascolarizzazione TestaSofia CoppiardiNessuna valutazione finora
- La Circolazione SanguignaDocumento4 pagineLa Circolazione SanguignaManuela MarraNessuna valutazione finora
- Il Sistema VascolareDocumento21 pagineIl Sistema VascolareNicolò Gino CoratoNessuna valutazione finora
- Fisiologia Apparato Cardio-CircolatorioDocumento53 pagineFisiologia Apparato Cardio-Circolatoriomgrazya89Nessuna valutazione finora
- Sistema Cardio CircolatorioDocumento18 pagineSistema Cardio Circolatoriosabah mihratNessuna valutazione finora
- Apparato Respiratorio e CardiovascolareDocumento29 pagineApparato Respiratorio e CardiovascolareColorado Express YTNessuna valutazione finora
- Appunti UrologiaDocumento29 pagineAppunti UrologiaMatteo Gidgio MeloniNessuna valutazione finora
- Apparato CircolatorioDocumento5 pagineApparato CircolatorioErmes IulianoNessuna valutazione finora
- (PDF - ITA) Manuale Di CardiologiaDocumento352 pagine(PDF - ITA) Manuale Di CardiologiaAlessio Sola75% (8)
- Vena Cava InferioreDocumento2 pagineVena Cava InferioreAlessandro ZadraNessuna valutazione finora
- Sistema CirculatorioDocumento8 pagineSistema CirculatorioJusta MemeNessuna valutazione finora
- Apparato CircolatorioDocumento10 pagineApparato CircolatorioPeter OlumataNessuna valutazione finora
- Apparato CardiocircolatorioDocumento9 pagineApparato CardiocircolatoriomannaggeppettoNessuna valutazione finora
- Vascolare Anatomia IIDocumento11 pagineVascolare Anatomia IIGianmarcoFiorentiniNessuna valutazione finora
- Un Sistema Per Nutrire e Depurare Il CorpoDocumento5 pagineUn Sistema Per Nutrire e Depurare Il CorpoGiuliaNessuna valutazione finora
- Viscerale Lezione 1 Parte 3Documento9 pagineViscerale Lezione 1 Parte 3Antonio GarNessuna valutazione finora
- Apparato RiproduttoreDocumento5 pagineApparato RiproduttoreLucia LisciNessuna valutazione finora
- Fisiopatologia Del Circolo e Del Sistema VasaleDocumento13 pagineFisiopatologia Del Circolo e Del Sistema VasaleCaterina RizzoNessuna valutazione finora
- 13 Lezione - Anatomia e Fisiologia Del CuoreDocumento19 pagine13 Lezione - Anatomia e Fisiologia Del Cuoresono bruttoNessuna valutazione finora
- Apparato CardiocircolatorioDocumento53 pagineApparato Cardiocircolatorioalessandro ricciNessuna valutazione finora
- L'apparato Circolatorio PDFDocumento10 pagineL'apparato Circolatorio PDFAntonio BevilacquaNessuna valutazione finora
- Lezione 1 FisiologiaDocumento5 pagineLezione 1 FisiologiaElettra Di NoceraNessuna valutazione finora
- Apparato CircolatorioDocumento7 pagineApparato CircolatorioMichele CasiniNessuna valutazione finora
- Valutazione Ecografica Dei Testicoli e Degli EpididimiDocumento26 pagineValutazione Ecografica Dei Testicoli e Degli Epididimiprimularossa1961Nessuna valutazione finora
- Sarò mamma! - Igiene e consigli prima, durante e dopo il partoDa EverandSarò mamma! - Igiene e consigli prima, durante e dopo il partoNessuna valutazione finora
- Zanzare in Appenino - I culicidi di alta quota in provincia di ModenaDa EverandZanzare in Appenino - I culicidi di alta quota in provincia di ModenaNessuna valutazione finora
- (Yoga) La Pratica Della Terapia Del DigiunoDocumento28 pagine(Yoga) La Pratica Della Terapia Del DigiunoMattia Crema Mahavir Anand50% (2)
- Christiaan BarnardDocumento5 pagineChristiaan BarnardpizzaNessuna valutazione finora
- Linee Guida INPS Accertamenti Stati Invalidanti PDFDocumento147 pagineLinee Guida INPS Accertamenti Stati Invalidanti PDFrsueuropawoolf8793Nessuna valutazione finora
- Materiale Ferri - GrassiDocumento195 pagineMateriale Ferri - GrassiAldo Di CristofaroNessuna valutazione finora
- (Shiatsu) Meridiani PrincipaliDocumento12 pagine(Shiatsu) Meridiani Principaliastrovane72Nessuna valutazione finora