Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Sali PDF
Caricato da
Giorgia SolesTitolo originale
Copyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Sali PDF
Caricato da
Giorgia SolesCopyright:
Formati disponibili
I NOMI DEI SALI
I sali sono composti prevalentemente binari e ternari, ma possono essere formati
anche da quattro o più elementi. Vediamo le regole relative ai casi più semplici e
ricorrenti.
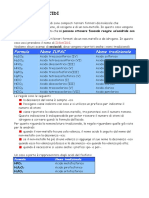
I NOMI DEI SALI BINARI
Nella tabella sottostante vengono riportati i nomi IUPAC e quelli tradizionali; questi
ultimi un po’ meno intuitivi:
Formula Nome IUPAC Nome tradizionale
KBr Bromuro di potassio Bromuro di potassio
BaBr2 Dibromuro di bario Bromuro di bario
Cr2S3 Trisolfuro di dicromo Solfuro cromico
SnCl4 Tetracloruro di stagno Cloruro stannico
SnCl2 Dicloruro di stagno Cloruro stannoso
Nella nomenclatura IUPAC si aggiunge la desinenza –uro al nome del secondo elemento
della formula e si usano i soliti prefissi. Anche nella nomenclatura tradizionale si
aggiunge la desinenza –uro al nome del non-metallo e si usano le desinenze –oso e –ico
per il metallo.
Per risalire dal nome IUPAC di un sale binario alla sua formula:
si scrive prima il simbolo del metallo e poi quello del non-metallo
si individuano gli indici in base ai prefissi.
Per risalire dal nome tradizionale di un sale binario alla sua formula:
occorre ricordare le valenze del metallo e scegliere quella appropriata in base
alla desinenza –oso o -ico
occorre ricordare anche la valenza del non-metallo in base alla formula
dell’idracido da cui formalmente deriva: la valenza del non-metallo equivale al
numero di atomi di idrogeno
I NOMI DEI SALI TERNARI
Formula Nome IUPAC Nome tradizionale
BaSO4 Tetraossosolfato(VI) di bario Solfato di bario
Zn3(PO4)2 Tetraossodifosfato(V) di zinco Fosfato di zinco
Fe(NO3)2 Triossodinitrato(V) di ferro(II) Nitrato ferroso
Fe(NO3)3 Triossotrinitrato(V) di ferro(III) Nitrato ferrico
NaClO Monossoclorato(I) di sodio Ipoclorito di sodio
CuNO2 Diossonitrato(III) di rame (I) Nitrito rameoso
KClO3 Triossoclorato(V) di potassio Clorato di potassio
Mg3(BO3)2 Triossodiborato(III) di magnesio Borato di magnesio
Per la nomenclatura IUPAC:
la desinenza del sale diventa –ato in quanto quella dell’ossiacido è sempre –ico;
si aggiunge il nome del metallo e, quando è necessario, la sua valenza.
Per la nomenclatura tradizionale:
la desinenza del sale è –ito quando il nome dell’ossiacido finisce con –oso,
mentre è –ato quando il nome dell’ossiacido termina con –ico;
si aggiunge il nome del metallo con l’eventuale desinenza –ico oppure –oso a
seconda della valenza maggiore o minore.
Potrebbero piacerti anche
- NOMENCLATURADocumento9 pagineNOMENCLATURAnicolepesce01Nessuna valutazione finora
- Lezione1 Stechiometria Nomenclatura ChimicaDocumento21 pagineLezione1 Stechiometria Nomenclatura ChimicaLeo Bursese100% (1)
- Nomenclatura Composti InorganiciDocumento4 pagineNomenclatura Composti InorganiciSerena MarrazzoNessuna valutazione finora
- 3) SALI TERNARI EserciziDocumento3 pagine3) SALI TERNARI Esercizicorrado corradi0% (1)
- NomenclaturaDocumento13 pagineNomenclaturaAleCastelliNessuna valutazione finora
- Lezione Di Chimica N. 4Documento5 pagineLezione Di Chimica N. 4the andrix splatterNessuna valutazione finora
- NomenclaturaDocumento17 pagineNomenclaturaermelinda memoliNessuna valutazione finora
- Nomenclatura TotaleDocumento36 pagineNomenclatura TotaleRoberta BasiricòNessuna valutazione finora
- Nomenclatura Chimica: Appunti DiDocumento19 pagineNomenclatura Chimica: Appunti Dihaconep181Nessuna valutazione finora
- 4) COMPOSTI INORGANICI EserciziDocumento4 pagine4) COMPOSTI INORGANICI Esercizicorrado corradiNessuna valutazione finora
- 3 Nomenclatura 2021Documento14 pagine3 Nomenclatura 2021serenaNessuna valutazione finora
- Nomenclatura Di Base Chimica Per IngegneriaDocumento13 pagineNomenclatura Di Base Chimica Per IngegneriaVu D TrevorNessuna valutazione finora
- Nomenclatura Molecole InorganicheDocumento25 pagineNomenclatura Molecole InorganicheLorenzo GregorisNessuna valutazione finora
- Ripasso Nomenclatura TradizionaleDocumento3 pagineRipasso Nomenclatura TradizionaleAlessio SargentiniNessuna valutazione finora
- 2) IDROSSIDI, OSSIACIDI, IDRACIDI EserciziDocumento3 pagine2) IDROSSIDI, OSSIACIDI, IDRACIDI Esercizicorrado corradiNessuna valutazione finora
- F4 UvoifevgujdxfyvyukcvyukfeqguvkfequykvfecygiqkDocumento63 pagineF4 Uvoifevgujdxfyvyukcvyukfeqguvkfequykvfecygiqkjacoponavari2004Nessuna valutazione finora
- Nomenclatura Composti ChimiciDocumento21 pagineNomenclatura Composti ChimiciKnabodinalioNessuna valutazione finora
- Nomenclatura ChimicaDocumento63 pagineNomenclatura ChimicaDaniele CaglieroNessuna valutazione finora
- La Nomenclatura ChimicaDocumento5 pagineLa Nomenclatura ChimicaAlex SeveroniNessuna valutazione finora
- Antichi Simboli ChimiciDocumento20 pagineAntichi Simboli Chimicigerri74okNessuna valutazione finora
- Nomenclatura Dei Composti BinariDocumento4 pagineNomenclatura Dei Composti Binarinicolacaddeo07Nessuna valutazione finora
- Nomenclatura Compuşilor ChimiciDocumento9 pagineNomenclatura Compuşilor Chimicicondecuse100% (2)
- AcidiDocumento2 pagineAcidiAlvaro SoleroNessuna valutazione finora
- Nomenclatura ZanicchelliDocumento28 pagineNomenclatura ZanicchelliAndrea GregoNessuna valutazione finora
- Nomenclatura InorganicaDocumento10 pagineNomenclatura InorganicaLucaNessuna valutazione finora
- nuovi_esercizi_nomenclaturaDocumento8 paginenuovi_esercizi_nomenclaturanicolacaddeo07Nessuna valutazione finora
- NomenclatureDocumento3 pagineNomenclatureAndy ZanoliNessuna valutazione finora
- Nomenclatura ChimicaDocumento19 pagineNomenclatura Chimicaapi-253266324Nessuna valutazione finora
- Nomenclatura Tradizionale e SistematicaDocumento2 pagineNomenclatura Tradizionale e SistematicaMichelangelo Mastrorocco De Grandis67% (3)
- Elementi Composti NomenclaturaDocumento7 pagineElementi Composti NomenclaturaTed SukuboNessuna valutazione finora
- Chimica NomenclaturaDocumento7 pagineChimica NomenclaturaJUVE NAPOLI 2-0 E' FINITA FORZA GIUVENessuna valutazione finora
- Esercizi NomenclaturaDocumento10 pagineEsercizi NomenclaturaAlessandro PratiNessuna valutazione finora
- Nomenclatura InorganiciDocumento11 pagineNomenclatura InorganiciFrancesco Berry BerardiniNessuna valutazione finora
- Tavola Per La Nomenclatura Dei Composti Chimici (Tradizionale e IUPAC) Nome Compos Ti F. Chimica Nomenclatura Trad. Nomenclatura IUPAC Oss. Note e EsDocumento2 pagineTavola Per La Nomenclatura Dei Composti Chimici (Tradizionale e IUPAC) Nome Compos Ti F. Chimica Nomenclatura Trad. Nomenclatura IUPAC Oss. Note e Esnicole vitaNessuna valutazione finora
- Appunti Di Chimica Inorganica Per Il Liceo ScientificoDocumento3 pagineAppunti Di Chimica Inorganica Per Il Liceo ScientificoBelinda AbbruzzeseNessuna valutazione finora
- NomenclaturaDocumento16 pagineNomenclaturaSant NientNessuna valutazione finora
- Esercizi TotaliDocumento19 pagineEsercizi TotaliSARA FERRANTENessuna valutazione finora
- ChimicaDocumento8 pagineChimicaStella SelmaniNessuna valutazione finora
- La NomenclaturaDocumento63 pagineLa NomenclaturaromersadavideNessuna valutazione finora
- 2 nomenclaturaIIDocumento30 pagine2 nomenclaturaIIBiagio CastronovoNessuna valutazione finora
- Nomenclatura ChimicaDocumento8 pagineNomenclatura ChimicaDaniele CenedaNessuna valutazione finora
- La Nomenclatura (Chimica)Documento9 pagineLa Nomenclatura (Chimica)Federico MazzolaniNessuna valutazione finora
- Zanichelli Chimica Intorno Sintesi10Documento2 pagineZanichelli Chimica Intorno Sintesi10dmfra08Nessuna valutazione finora
- Valitutti Soluzioni Esercizi 82074 c14Documento6 pagineValitutti Soluzioni Esercizi 82074 c14marco poloNessuna valutazione finora
- 13) Idruri, Idracidi e Sali BinariDocumento3 pagine13) Idruri, Idracidi e Sali BinariShizuITANessuna valutazione finora
- Acidi TernariDocumento2 pagineAcidi TernariVeltro da CorvaiaNessuna valutazione finora
- La Nomenclatura InorganicaDocumento5 pagineLa Nomenclatura InorganicaSimona StefanelliNessuna valutazione finora
- NomenclaturaDocumento32 pagineNomenclaturaMarta DomenighiniNessuna valutazione finora
- ESERCIZI NomenclaturaDocumento2 pagineESERCIZI NomenclaturavikingdeathNessuna valutazione finora
- Appunti Di Scienze (Classe Seconda)Documento47 pagineAppunti Di Scienze (Classe Seconda)Liceo F. Vercelli100% (1)
- Esercizi ChimDocumento6 pagineEsercizi ChimrosagiuliaNessuna valutazione finora
- NOMENCLATURADocumento41 pagineNOMENCLATURAcelesteNessuna valutazione finora
- Lezione 1. Nomenclatura ChimicaDocumento57 pagineLezione 1. Nomenclatura ChimicaRagne FranciscoNessuna valutazione finora
- Domande Teoria Chimica GenDocumento5 pagineDomande Teoria Chimica GenAnonymous v3Tif9qQ2Nessuna valutazione finora
- Nomenclatura IUPACDocumento2 pagineNomenclatura IUPACEpiNessuna valutazione finora