Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
MDSAP Completo (4) Marzo 21
Caricato da
Jessica Rubí SuárezTitolo originale
Copyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
MDSAP Completo (4) Marzo 21
Caricato da
Jessica Rubí SuárezCopyright:
Formati disponibili
Documento No.
:
TÍTULO DE LA POLÍTICA: ENFOQUE MDSAP AU P0002.005
DE AUDITORÍA MDSAP Fecha de Revisión:
2020-09-01
ENFOQUE DE AUDITORÍA
MDSAP AU P0002.005 1 Página
Tabla de Contenidos
PREFACIO 5
VISIÓN GENERAL 6
SECUENCIA DE AUDITORÍA 6
REALIZACIÓN DE LA AUDITORÍA 9
NAVEGANDO LA REALIZACIÓN DE LA AUDITORÍA 10
TERMINOLOGÍA 11
ANEXOS 11
CICLO DE AUDITORÍA MDSAP 12
CAPÍTULO 1: GESTIÓN 18
TAREA 1 – SGC PLANEACIÓN, IMPLEMENTACIÓN, CAMBIOS Y MANUAL DE CALIDAD 18
TAREA 2 – REPRESENTANTE DE LA DIRECCIÓN 21
TAREA 3 – POLÍTICA Y OBJETIVOS DE CALIDAD 22
TAREA 4 – ESTRUCTURA ORGANIZACIONAL, RESPONSABILIDAD, AUTORIDAD, RECURSOS 23
TAREA 5 – ALCANCE DE LA SUBCONTRATACIÓN 24
TAREA 6 – COMPETENCIA Y CAPACITACIÓN DEL PERSONAL 25
TAREA 7 – PLANEACIÓN Y REVISIÓN DE LA GESTIÓN DE RIESGOS 26
TAREA 8 – CONTROL DE DOCUMENTOS Y REGISTROS 27
TAREA 9 – REVISIONES DE LA DIRECCIÓN 29
TAREA 10 – DISTRIBUCIÓN DE DISPOSITIVOS CON AUTORIZACIÓN DE MERCADO ADECUADOS 30
TAREA 11 – COMPROMISO DE LA ALTA DIRECCIÓN CON LA CALIDAD 32
CAPÍTULO 2: AUTORIZACIÓN DE COMERCIALIZACIÓN Y REGISTRO DE INSTALACIÓN 33
TAREA 1 – SOLICITUD PARA LA AUTORIZACIÓN DE COMERCIALIZACIÓN DEL DISPOSITIVO Y REGISTRO DE
33
INSTALACIÓN
TAREA 2 – EVIDENCIA DE AUTORIZACIÓN O APROBACIÓN DE COMERCIALIZACIÓN 38
TAREA 3 – NOTIFICACIÓN DE CAMBIOS A DISPOSITIVOS COMERCIALIZADOS O AL SGC 41
CAPÍTULO 3: MEDICIÓN, ANÁLISIS Y MEJORA 46
TAREA 1 – PROCEDIMIENTOS PARA LA MEDICIÓN, ANÁLISIS Y MEJORA DE LA EFECTIVIDAD DEL SGC Y
47
CONFORMIDAD DEL PRODUCTO
TAREA 2 – FUENTES DE DATOS DE CALIDAD 48
TAREA 3 – INVESTIGACIÓN DE NO CONFORMIDAD 50
TAREA 4 – INVESTIGACIÓN DE NO CONFORMIDAD POTENCIAL 51
TAREA 5 – CORRECCIÓN, ACCIÓN CORRECTIVA Y ACCIÓN PREVENTIVA 52
TAREA 6 – EVALUACIÓN DE CAMBIO DE DISEÑO COMO RESULTADO DE ACCIÓN CORRECTIVA O
53
PREVENTIVA
TAREA 7 – EVALUACIÓN DE CAMBIO DE PROCESO COMO RESULTADO DE ACCIÓN CORRECTIVA O
54
PREVENTIVA
TAREA 8 – IDENTIFICACIÓN Y CONTROL DE PRODUCTO NO CONFORME 55
TAREA 9 – ACCIÓN RELATIVA A PRODUCTO NO CONFORME DESPUÉS DE LA ENTREGA 56
TAREA 10 – AUDITORÍA INTERNA 57
TAREA 11 – INFORMACIÓN PROPORCIONADA PARA LA REVISIÓN DE LA DIRECCIÓN 58
TAREA 12 – EVALUACIÓN DE LA INFORMACIÓN DE LA FASE POST-PRODUCCIÓN, INCLUYENDO QUEJAS 59
TAREA 13 – COMUNICACIÓN CON PARTES EXTERNAS INVOLUCRADAS EN QUEJAS 62
TAREA 14 – EVALUACIÓN DE QUEJAS PARA REPORTE DE EVENTOS ADVERSOS 63
TAREA 15 – EVALUACIÓN DE PROBLEMAS DE CALIDAD PARA NOTIFICACIONES DE ADVERTENCIA 63
TAREA 16 – COMPROMISO DE LA ALTA DIRECCIÓN PARA EL PROCESO DE MEDICIÓN, ANÁLISIS Y MEJORA 65
MDSAP AU P0002.005 2 Página
CAPÍTULO 4: EVENTOS ADVERSOS DE DISPOSITIVOS MÉDICOS Y REPORTES DE
66
NOTIFICACIÓN
TAREA 1 – NOTIFICACIÓN DE EVENTOS ADVERSOS 66
TAREA 2 – NOTIFICACIÓN DE AVISOS DE ADVERTENCIA 72
CAPÍTULO 5: DISEÑO Y DESARROLLO 76
TAREA 1 – IDENTIFICACIÓN DE DISPOSITIVOS SUJETOS A PROCEDIMIENTOS DE DISEÑO Y DESARROLLO;
77
DOCUMENTACIÓN TÉCNICA
TAREA 2 – SELECCIÓN DE UN PROYECTO COMPLETO DE DISEÑO Y DESARROLLO 78
TAREA 3 – PLANEACIÓN DE DISEÑO Y DESARROLLO 79
TAREA 4 – IMPLEMENTACIÓN DEL PROCESO DE DISEÑO Y DESARROLLO 80
TAREA 5 – ENTRADA DE DISEÑO Y DESARROLLO 81
TAREA 6 – INTEGRIDAD, COHERENCIA Y FALTA DE AMBIGÜEDAD DE LA ENTRADA DE DISEÑO Y
83
DESARROLLO
TAREA 7 – SALIDA DE DISEÑO Y DESARROLLO Y VERIFICACIÓN DEL DISEÑO 84
TAREA 8 – ACTIVIDADES DE GESTIÓN DE RIESGOS APLICADAS A TRAVÉS DEL PROYECTO DE DISEÑO Y
86
DESARROLLO
TAREA 9 – VERIFICACIÓN DE DISEÑO O VALIDACIÓN DE DISEÑO PARA CONFIRMAR LA EFECTIVIDAD DE
88
LAS MEDIDAS DE CONTROL DE RIESGO
TAREA 10 – VALIDACIÓN DE DISEÑO 89
TAREA 11 – EVALUACIÓN CLÍNICA Y / O EVALUACIÓN DE LA SEGURIDAD Y DESEMPEÑO DEL DISPOSITIVO
90
MÉDICO
TAREA 12 – DISEÑO Y DESARROLLO DE SOFTWARE 91
TAREA 13 – CAMBIO DEL DISEÑO Y DESARROLLO 92
TAREA 14 – REVISIÓN DEL DISEÑO 94
TAREA 15 – REVISIÓN DEL IMPACTO DE LOS CAMBIOS DEL DISEÑO Y DESARROLLO EN DISPOSITIVOS
94
PREVIAMENTE HECHOS Y DISTRIBUIDOS
TAREA 16 – TRANSFERENCIA DE DISEÑO 96
TAREA 17 – COMPROMISO DE LA ALTA DIRECCIÓN PARA EL PROCESO DE DISEÑO Y DESARROLLO 97
CAPÍTULO 6: CONTROLES DE PRODUCCIÓN Y SERVICIO 98
TAREA 1 – PLANEACIÓN DEL PROCESO DE PRODUCCIÓN Y SERVICIO 99
TAREA 2 – SELECCIÓN DEL PROCESO(S) DE PRODUCCIÓN Y SERVICIO 101
TAREA 3 – CONTROLES PARA LA IMPLEMENTACIÓN DE PROCESO(S) SELECCIONADO(S) DE PRODUCCIÓN Y
101
SERVICIO
TAREA 4 – CONTROL DE LA LIMPIEZA DEL PRODUCTO 102
TAREA 5 – INFRAESTRUCTURA 103
TAREA 6 – AMBIENTE DE TRABAJO 104
TAREA 7 – IDENTIFICACIÓN DE PROCESOS SUJETOS A VALIDACIÓN 105
TAREA 8 – VALIDACIÓN DE PROCESO 106
TAREA 9 – VALIDACIÓN DEL PROCESO DE ESTERILIZACIÓN 108
TAREA 10 – MONITOREO Y MEDICIÓN DE LA CONFORMIDAD DEL PRODUCTO 109
TAREA 11 – CONTROL, OPERACIÓN Y MONITOREO DEL PROCESO DE PRODUCCIÓN Y SERVICIO;
110
CONTROLES DE RIESGO
TAREA 12 – COMPETENCIA DEL PERSONAL 111
TAREA 13 – CONTROL DEL MONITOREO Y MEDICIÓN DEL DISPOSITIVO 112
TAREA 14 – ANÁLISIS DEL IMPACTO DEL MONITOREO Y MEDICIÓN DE DISPOSITIVOS FUERA DE
113
ESPECIFICACIONES
TAREA 15 – VALIDACIÓN DEL SOFTWARE UTILIZADO PARA EL CONTROL DEL PROCESO DE PRODUCCIÓN Y
114
SERVICIO
TAREA 16 – EXPEDIENTE MAESTRO DEL DISPOSITIVO 115
TAREA 17 – REGISTRO DE PRODUCCIÓN; EVIDENCIA DEL CUMPLIMIENTO DE DISPOSITIVOS LIBERADOS 117
TAREA 18 – TRAZABILIDAD APLICABLE A DISPOSITIVOS IMPLANTABLES, DE SOPORTE DE VIDA O DE
118
SOSTENIMIENTO DE VIDA
TAREA 19 – IDENTIFICACIÓN DEL ESTATUS DEL PRODUCTO 120
TAREA 20 – PROPIEDAD DEL CLIENTE 121
MDSAP AU P0002.005 3 Página
TAREA 21 – ACTIVIDADES DE ACEPTACIÓN 121
TAREA 22 – IDENTIFICACIÓN, CONTROL Y DISPOSICIÓN DE PRODUCTOS NO CONFORMES 123
TAREA 23 – RETRABAJO DE PRODUCTOS NO CONFORMES 125
TAREA 24 – PRESERVACIÓN DEL PRODUCTO 126
TAREA 25 – REVISIÓN DE LOS REQUISITOS DEL CLIENTE, REGISTROS DE DISTRIBUCIÓN 127
TAREA 26 – ACTIVIDADES DE INSTALACIÓN 128
TAREA 27 – ACTIVIDADES DE SERVICIO 128
TAREA 28 – CONTROLES DE RIESGO APLICADOS AL TRANSPORTE, INSTALACIÓN Y SERVICIO 130
TAREA 29 – COMPROMISO DE LA ALTA DIRECCIÓN PARA EL PROCESO DE PRODUCCIÓN Y SERVICIO 131
CAPÍTULO 7: COMPRAS 132
TAREA 1 – PLANEACIÓN DE LAS ACTIVIDADES RELATIVAS A PRODUCTOS COMPRADOS Y PROCESOS
133
SUBCONTRATADOS
TAREA 2 – SELECCIÓN DEL EXPEDIENTE DE PROVEEDOR PARA AUDITORÍA 134
TAREA 3 – PROCEDIMIENTO PARA EL CONTROL DE PRODUCTOS COMPRADOS Y PROCESOS
134
SUBCONTRATADOS
TAREA 4 – EXTENSIÓN DE LOS CONTROLES APLICADOS AL PROVEEDOR Y AL PRODUCTO COMPRADO;
135
CRITERIOS DE SELECCIÓN; EVALUACIÓN Y REEVALUACIÓN DEL PROVEEDOR
TAREA 5 – SELECCIÓN DEL PROVEEDOR EN BASE A LA HABILIDAD PARA SATISFACER LOS REQUISITOS
136
ESPECÍFICOS DE COMPRAS
TAREA 6 – REGISTROS DE LA EVALUACIÓN DEL PROVEEDOR 139
TAREA 7 – CONTROLES EFECTIVOS SOBRE PROVEEDOR Y PRODUCTOS 140
TAREA 8 – VERIFICACIÓN DE LA ADECUACIÓN DE LA INFORMACIÓN DE COMPRAS, REQUISITOS
ESPECÍFICOS DE COMPRAS Y ACUERDO ESCRITO SOBRE NOTIFICACIÓN DE CAMBIOS, ANTES DE LA 141
COMUNICACIÓN CON EL PROVEEDOR
TAREA 9 – INFORMACIÓN DOCUMENTADA DE COMPRAS Y REQUISITOS ESPECÍFICOS DE COMPRAS 143
TAREA 10 – VERIFICACIÓN DE PRODUCTOS COMPRADOS 144
TAREA 11 – CONTROL DE ACTIVIDADES DE COMPRAS COMO FUENTE DE DATOS DE CALIDAD PARA EL
145
PROCESO DE MEDICIÓN, ANÁLISIS Y MEJORA
TAREA 12 – COMPROMISO DE LA ALTA DIRECCIÓN PARA EL PROCESO DE COMPRAS 146
ANEXO 1 – AUDITORÍA DE PRODUCTO / PROCESO RELATIVO A TECNOLOGÍAS Y
147
DOCUMENTACIÓN TÉCNICA
ANEXO 2 – AUDITORÍA DE REQUERIMIENTOS PARA DISPOSITIVOS MÉDICOS ESTÉRILES 155
ANEXO 3 – EVENTOS ADVEROS DE DISPOSITIVOS MÉDICOS Y REFERENCIA A PROCESO
160
RÁPIDO DE REPRTE DE NOTIFICACIONES
ANEXO 4 – REQUISITOS PARA ACUERDOS ESCRITOS 163
RESUMEN DE CAMBIOS DESDE LA REVISIÓN PREVIA 172
MDSAP AU P0002.005 4 Página
Prefacio
La intención del Programa de Auditoría Única de Dispositivos Médicos (MDSAP, por sus siglas en
inglés) es permitir que los auditores competentes de las Organizaciones de Auditoría (AOs, por sus
siglas en inglés) reconocidas por el MDSAP realicen una auditoría única del sistema de gestión de
calidad de una organización de dispositivos médicos que satisfaga los requisitos de las autoridades
reguladoras de Dispositivos Médicos participantes en el programa MDSAP.
Las auditorías realizadas bajo el programa MDSAP se basarán en procesos, se centrarán en varios
procesos definidos, un método definido para vincular esos procesos y se construirán sobre una
base de requisitos para la gestión de riesgos.
Uso de este documento
Este documento contiene instrucciones específicas para realizar auditorías bajo el programa
MDSAP. Incorpora una secuencia de auditoría, instrucciones para auditar cada proceso específico
e identifica vínculos que resaltan las interacciones entre los procesos.
Un cuadro rojo enfatiza las interrelaciones de procesos específicos y las actividades relevantes de
Gestión de Riesgos, si está viendo una versión en color del documento, o en recuadros grises si se
está viendo una versión en blanco y negro. Una fuente “Azul” enfatiza la integración de la Gestión
de Riesgos.
Esta revisión del documento combina el modelo de auditoría MDSAP y los documentos
complementarios del proceso, anteriormente separados, en un solo documento que contiene
detalles adicionales sobre cada proceso auditado; así como orientación para evaluar la
conformidad de cada proceso. En forma electrónica, la barra de navegación facilita el acceso
rápido a las Tareas relevantes. El usuario puede crear sus propios marcadores para navegar
rápidamente a varias secciones.
MDSAP AU P0002.005 5 Página
Visión General
El diseño del proceso de auditoría del Programa de auditoría única de dispositivos médicos
(MDSAP) tiene como objetivo garantizar que una sola auditoría proporcione una cobertura eficiente
pero completa de los requisitos reglamentarios. Estos requisitos incluyen; Dispositivos médicos -
Sistemas de gestión de la calidad - Requisitos para fines reglamentarios (ISO 13485: 2016), los
requisitos del Sistema de gestión de la calidad de los Procedimientos de evaluación de la
conformidad de las Regulaciones Australianas sobre productos terapéuticos (dispositivos médicos)
(TG (MD) R Sch3), Buenas Prácticas de Fabricación Brasileñas (RDC ANVISA 16/2013), la
Ordenanza japonesa sobre normas para el control de fabricación y el control de calidad de
dispositivos médicos y reactivos de diagnóstico in vitro (Ordenanza ministerial MHLW No. 169), la
Regulación del sistema de calidad (21 CFR Parte 820), y requisitos específicos de las autoridades
reguladoras de dispositivos médicos que participan en el programa MDSAP.
Secuencia de Auditoría
El diseño y desarrollo de la secuencia de auditoría MDSAP permite una realización lógica,
enfocada y eficiente de una auditoría. La secuencia de auditoría MDSAP sigue un enfoque de
proceso y tiene cuatro procesos principales: proceso de gestión, proceso de medición, análisis y
mejora, proceso de diseño y desarrollo y un proceso de controles de producción y servicio con
enlaces al proceso de apoyo para compras.
La definición de cada proceso incluye un propósito y un resultado que son indicadores del
desempeño del proceso. Cada Autoridad Reguladora participante espera que la gestión de riesgos
sea la base de los cinco procesos que son los requisitos de un sistema de gestión de la calidad
para las organizaciones de dispositivos médicos.
El proceso de auditoría de MDSAP tiene dos procesos de apoyo adicionales: Autorización de
comercialización de dispositivos y Registro de instalación y Notificación de Avisos de Advertencia y
Eventos Adversos de Dispositivos Médicos. Estos procesos son necesarios para cumplir con los
requisitos específicos de las autoridades reguladoras del MDSAP participantes.
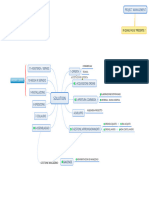
El diagrama de flujo que se muestra en la Figura 1 ilustra la secuencia de auditoría de MDSAP y
las interrelaciones. El diseño del enfoque de auditoría MDSAP requiere la auditoría de los procesos
MDSAP primarios en la siguiente secuencia: (1) Gestión (2) Medición, análisis y mejora (3) Diseño
y desarrollo, y (4) Procesos de control de producción y servicio. La auditoría del proceso de
Compras se realiza en conjunto con el proceso de Medición, Análisis y Mejora, el proceso de
Diseño y Desarrollo y el proceso de Controles de Producción y Servicio.
El diseño e implementación del sistema de gestión de calidad de una organización de dispositivos
médicos es una decisión estratégica de la organización de dispositivos médicos. A través de este
sistema, puede cumplir con los requisitos de las jurisdicciones reguladoras participantes de una
manera que sea apropiada para el tamaño de la organización de dispositivos médicos, los
procesos empleados y los productos suministrados. El sistema de gestión de calidad de la
organización de dispositivos médicos no necesita implementar ciertos procesos (por ejemplo,
Diseño y Desarrollo) si la regulación permite la exclusión o no aplicación del proceso. Las
organizaciones auditoras no están obligadas a auditar dichos procesos. Sin embargo, si la
organización de dispositivos médicos opta por subcontratar cualquier proceso relacionado con el
diseño y / o fabricación de dispositivos médicos del que la organización de dispositivos médicos
MDSAP AU P0002.005 6 Página
tiene la responsabilidad, estos procesos siguen siendo responsabilidad de la organización de
dispositivos médicos. El sistema de gestión de calidad de la organización de dispositivos médicos
debe implementar controles para monitorear y mantener la calidad del producto de los proveedores
y los procesos suministrados.
Las jurisdicciones participantes del MDSAP tenían la intención de promover un programa único de
auditorías que tenga en cuenta todos sus requisitos para los sistemas de gestión de la calidad. Por
lo tanto, incluir los requisitos reglamentarios de todas las jurisdicciones participantes del MDSAP es
un requisito predeterminado para la participación de una organización de dispositivos médicos en
el programa. Los titulares de la autorización de comercialización pueden haber utilizado
previamente una fuente alternativa de evidencia para demostrar el cumplimiento de los requisitos
reglamentarios de una jurisdicción. El suministro de un producto a la jurisdicción de una Autoridad
Reguladora del MDSAP participante requiere que el auditor incluya los requisitos reglamentarios
relevantes en el alcance de una auditoría.
Sin embargo, además de las exclusiones y no aplicaciones permitidas por ISO13485, la
organización de dispositivos médicos puede excluir los requisitos de los mercados donde la
organización de dispositivos médicos no tiene la intención de suministrar el producto. El alcance de
la auditoría y los criterios de auditoría deben tener en cuenta cualquier exclusión o no aplicación
justificada. Cuando una organización de dispositivos médicos reclama una exclusión de los
requisitos de un mercado objetivo, el auditor debe tener cuidado al aplicar la orientación
proporcionada en los procesos MDSAP. Es posible que algunos requisitos no sean aplicables.
Los dispositivos médicos regulados para su uso en estudios clínicos previos a la comercialización
bajo programas de acceso especial, exenciones de uso humanitario y programas de dispositivos de
investigación están fuera del alcance de una auditoría MDSAP típica. La fabricación y distribución
de un dispositivo que se suministre bajo un programa de tipo de acceso especial puede estar
sujeta a partes de los requisitos reglamentarios incluidos en el MDSAP. Se anima a las
organizaciones auditoras a que se pongan en contacto con la autoridad reguladora pertinente que
participa en el MDSAP para cualquier pregunta o aclaración.
MDSAP AU P0002.005 7 Página
Procesos de
Enfoque de
Auditoría
Gestión de Riesgos Figura 1
Autorización de
Comercialización de
Gestión Dispositivo y Registro
de Instalación
Medición // Eventos Adversos de
Dispositivo Médico y
Análisis y Mejora Reporte de
Notificaciones de
Advertencia
Autorización de
Diseño y Desarrollo Comercialización de
Dispositivo y Registro
de Instalación
Producción y
Provisión del
Servicio
Compras
Nota: Si bien existe una secuencia de auditoría prescrita para los procesos del MDSAP, los
auditores pueden auditar las tareas dentro de un proceso dado en cualquier secuencia para
permitir una auditoría eficiente y eficaz.
La secuencia de auditoría debe seguirse tal como se diseñó, sin embargo, bajo ciertas
circunstancias, incluido el número y la calificación de los auditores asignados a una auditoría, la
cantidad desigual de información asociada con los procesos específicos del cliente y el tipo de
actividad que se lleva a cabo, la aplicación rigurosa de la secuencia de auditoría puede impedir el
uso eficiente del tiempo de auditoría y crear problemas con la planificación de la auditoría. En estos
casos, se permiten excepciones juiciosas a la secuencia de auditoría siempre que exista una
justificación suficiente y se respeten los elementos centrales del Enfoque de auditoría de MDSAP,
MDSAP AU P0002.005 8 Página
incluidos los vínculos entre los procesos y las selecciones de muestras definidas y basadas en
riesgos.
Ejemplos de excepciones razonables:
Auditar la medición, el análisis y la mejora y la gestión al mismo tiempo para asignar mejor
el tiempo de auditoría para una actividad de múltiples auditores.
Iniciar la auditoría de un proceso MDSAP de seguimiento, como Producción o Diseño,
cuando se haya recopilado suficiente información mediante la revisión de los elementos
centrales en Medición, Análisis y Mejora y Gestión y procesos de apoyo, Autorización de
comercialización de dispositivos y Registro de instalaciones y Informe de avisos de aviso y
eventos adversos del dispositivo, pero antes de la finalización completa de estos procesos.
Permitir que un experto, como un experto en técnicas de esterilización específicas,
comience a revisar estos procesos y áreas específicas del cliente.
En todos los casos de estos ajustes, se debe prestar la debida atención a la comunicación dentro
de la auditoría para que estas decisiones se vuelvan a evaluar según sea necesario a medida que
se recopile información adicional a lo largo de la auditoría y se tomen las acciones apropiadas si
esta información altera la viabilidad de estos cambios.
Los ajustes específicos de la auditoría a la secuencia de auditoría del MDSAP deben
documentarse capturados en el informe de auditoría junto con la justificación adecuada.
Realización de la Auditoría
Durante la auditoría del sistema de gestión de la calidad de la organización de dispositivos
médicos, tal como se identifica en los procesos del MDSAP, se le pedirá al equipo de auditoría que
tenga en cuenta los "vínculos". Para que el sistema de gestión de la calidad de una organización
de dispositivos médicos funcione eficazmente, necesita identificar y gestionar numerosos procesos
interrelacionados (vinculados) de acuerdo con la cláusula 4.1.2 (c) de la norma ISO 13485: 2016.
El resultado de un proceso a menudo forma directamente la entrada de otros procesos, o las
actividades de un proceso de apoyo son relevantes para otros procesos. La secuencia de auditoría
del MDSAP y las tareas de auditoría incluyen vínculos para recordar al equipo de auditoría las
interacciones entre los procesos. Por ejemplo, los vínculos ayudan a los auditores a realizar las
selecciones adecuadas al pasar al siguiente proceso (por ejemplo, utilizar información del proceso
de Medición, Análisis y Mejora para seleccionar un proyecto de diseño y revisarlo cuando
corresponda).
Una auditoría de los procesos del sistema de gestión de la calidad de la organización de
dispositivos médicos tiene como objetivo evaluar hasta qué punto la organización de dispositivos
médicos está aplicando los principios de gestión de riesgos al definir sus actividades. La
implementación del enfoque de los controles basado en el riesgo es un aspecto integral del sistema
de gestión de calidad de una organización de dispositivos médicos y es responsabilidad de la alta
dirección proporcionar el compromiso y los recursos necesarios para este esfuerzo. La
implementación efectiva del enfoque basado en el riesgo generalmente comienza junto con el
proceso de diseño y desarrollo, avanza a través de la realización del producto, incluida la selección
de proveedores, considera la retroalimentación del monitoreo posterior a la comercialización y
continúa hasta el momento en que se da de baja el producto. Las decisiones basadas en riesgos
ocurren a lo largo de los diversos procesos del sistema de gestión de la calidad, y cada
MDSAP AU P0002.005 9 Página
organización de dispositivos médicos debe implementar el enfoque basado en riesgos, así como la
gestión de riesgos en la realización del producto, con una determinación de cuánto riesgo residual
es aceptable para garantizar que los dispositivos médicos cumplan con los requisitos seguridad y
rendimiento y requisitos reglamentarios.
Navegando la Realización de la Auditoría
Cada proceso de auditoría de MDSAP requerirá que el equipo de auditoría realice tareas de
auditoría para determinar si se logran los resultados y los propósitos del proceso. Cada tarea del
proceso de auditoría incluye referencias a Cláusulas y Regulaciones que incluyen; la (s) cláusula
(s) ISO 13485: 2016 aplicables, la (s) sección (s) correspondiente (s) de los requisitos del Sistema
de Gestión de Calidad de los Procedimientos de Evaluación de la Conformidad de las
Regulaciones de Productos Terapéuticos (Dispositivos Médicos) de Australia (TG (MD) R Sch3),
Buenas Prácticas de Fabricación Brasileñas (RDC ANVISA 16/2013), Ordenanza Japonesa sobre
normas para el control de fabricación y control de calidad de dispositivos médicos y reactivos de
diagnóstico in vitro (Ordenanza ministerial MHLW No. 169), la Regulación del sistema de calidad
(21 CFR 820) y cualquier requisito exclusivo que pertenece a una autoridad reguladora participante
del MDSAP. Estas referencias se han proporcionado para ayudar a los auditores a garantizar que
los requisitos de todas las autoridades reguladoras participantes del MDSAP se aborden durante la
auditoría.
Muchas tareas de auditoría requieren la verificación de la disponibilidad y el control de la
documentación y los registros específicos del regulador MDSAP. Estas tareas tienen una
referencia de Cláusula y Regulación a ISO 13485: 2016 cláusula 4.2.1, ya que la documentación
del sistema de gestión de calidad debe incluir documentación especificada por los requisitos
regulatorios aplicables (regulaciones, prácticas administrativas y políticas) [4.2.1 (e)]. Cuando un
requisito reglamentario se relaciona con la documentación requerida por otras cláusulas más
específicas de ISO 13485: 2016, la organización auditora debe hacer referencia a la cláusula más
específica al registrar los hallazgos de no conformidad. Para ser coherente con la norma ISO
13485: 2016, también se recuerda al equipo de auditoría que aplique el concepto de que “cuando
se requiere documentar un requisito, también se requiere establecerlo, implementarlo y
mantenerlo” 1.
La organización de dispositivos médicos debe demostrar su capacidad para proporcionar
dispositivos médicos que cumplan sistemáticamente con los requisitos reglamentarios y del cliente.
Durante la auditoría, es importante que los auditores sean conscientes de cualquier caso en el que
la organización de dispositivos médicos demuestre incumplimiento de alguno de los requisitos de la
norma ISO 13485: 2016, o parte de los requisitos enumerados en las actividades y tareas de
auditoría, y que estos las no conformidades se registran con el debido detalle. Se debe prestar
especial atención a la posible interrelación de las no conformidades observadas. Por ejemplo, los
hallazgos de auditoría tanto en los controles de compra como en las actividades de aceptación
pueden indicar una No Conformidad significativa porque el control sobre los proveedores y los
productos que suministran depende de una combinación eficaz de estas dos actividades, y las
deficiencias en una u otra pueden afectar la calidad del dispositivo terminado.
Siempre que una tarea de auditoría MDSAP requiera que un auditor verifique la identificación y
documentación de un requisito en la documentación del SGC, esta verificación debe realizarse
como parte de la preparación previa a la auditoría y la revisión de la documentación, según sea
práctico, para minimizar el tiempo de auditoría en el sitio y para aumentar la familiaridad del auditor
con el SGC de la organización de los Dispositivos Médicos.
MDSAP AU P0002.005 10 Página
1
ISO 13485:2016 – Cláusula 0.2
Terminología
El término "dispositivo" se utiliza en todos los procesos de MDSAP. Con el fin de aplicar los
procesos del MDSAP, y para acomodar matices en los sistemas regulatorios de las Autoridades
Reguladoras participantes, el uso del término "dispositivo" es para referirse a cualquier producto
que sea capaz de funcionar como un dispositivo médico, sea o no está empaquetado, etiquetado o
esterilizado. En algunas jurisdicciones, dicho producto se define como un "dispositivo terminado".
En otras jurisdicciones, un dispositivo terminado es aquel que está destinado a ser utilizado como
dispositivo médico y se encuentra en una etapa en la que el producto está listo para ser
comercializado o puesto en servicio por la organización de dispositivos médicos cuyo nombre
aparece en el etiquetado.
El término organización de dispositivos médicos en este documento pretende ser una referencia a
la definición en ISO 9000: 2016-Cl 3.2.1 y como se usa en ISO 13485: 2016. Un "fabricante" es un
tipo específico de organización de dispositivos médicos que se define de diversas maneras en las
regulaciones de las autoridades reguladoras participantes.
Un “producto” o “servicio”2 comprado u obtenido de otro modo es un producto o servicio
subcontratado. Además, un "proveedor" es cualquier persona que sea independiente del sistema
de gestión de calidad de la organización de dispositivos médicos. Esto incluye un proveedor que
puede ser parte de la misma corporación que la organización de dispositivos médicos pero que
opera bajo un sistema de gestión de calidad separado de la organización de dispositivos médicos
auditada. Para mayor aclaración, si un proveedor no es parte del alcance de auditoría interna de la
organización de dispositivos médicos, entonces el proveedor está bajo un sistema de gestión de
calidad separado. Las corporaciones o empresas que tienen políticas y procedimientos
corporativos de calidad no necesariamente colocan a todas las divisiones o grupos bajo el mismo
sistema de gestión de la calidad. Por lo tanto, una división o grupo puede ser proveedor de otra
división o grupo dentro de la misma corporación / empresa cuando no está dentro del alcance del
mismo sistema de gestión de la calidad. El control de los proveedores que forman parte de la
misma corporación y que no forman parte del SGC de la organización de dispositivos médicos
auditada es similar a la forma en que se controlan los proveedores externos. Por lo tanto, para los
propósitos del MDSAP y según sea necesario, una Organización de Auditoría tiene la discreción de
auditar a los proveedores externos de una organización de dispositivos médicos, incluidos los
proveedores corporativos. La organización de dispositivos médicos debe tener controles
adecuados sobre los procesos subcontratados que brindan dispositivos médicos y servicios
relacionados que cumplan constantemente con los requisitos reglamentarios aplicables y del
cliente.
Proveedores Críticos:
Para propósitos de MDSAP, “proveedores críticos” incluyen, pero no se limitan a:
• Aquellas entidades que proporcionan a la organización dispositivos terminados, es decir,
un dispositivo, o accesorio de cualquier dispositivo, que sea adecuado para su uso o capaz
de funcionar, esté o no esté empacado, etiquetado o esterilizado;
• Proveedores de productos, incluyendo servicios, que impacten a las salidas de diseño que
son esenciales para el funcionamiento adecuado del dispositivo; y
• Proveedores de productos y servicios que requieren validación de proceso.
Anexos
MDSAP AU P0002.005 11 Página
El Anexo 1 contiene información específica del país en cuanto a las expectativas para la auditoría
de tecnologías relacionadas con productos / procesos (distintas de la esterilización - Ver Anexo 2) y
la auditoría de la documentación técnica como parte de la ejecución de las Tareas de Auditoría.
2
GHTF/SG3/N17:2008 - Quality Management System – Medical Devices – Guidance on the Control of Products and Services Obtained from Suppliers
El Anexo 2 contiene información sobre la expectativa de auditoría de los requisitos para
dispositivos médicos estériles.
El Anexo 3 contiene una tabla que muestra un resumen de los plazos para Reporte de
Notificaciones de Advertencia e informes individuales de eventos adversos en las jurisdicciones
participantes del MDSAP.
El Anexo 4 contiene orientación específica de cada país sobre las expectativas de varios tipos de
acuerdos escritos con fines regulatorios.
Ciclo de Auditoría MDSAP
El Programa de auditoría única de dispositivos médicos se basa en un ciclo de auditoría de tres (3)
años. La Auditoría Inicial, también conocida como la "Auditoría de Certificación Inicial" es una
auditoría completa del sistema de gestión de calidad (SGC) de una organización de dispositivos
médicos que consta de una Auditoría de Etapa 1 (17021-1:2015 - Cl 9.3.1.2) y una Auditoría de
Etapa 2 (17021-1:2015 - Cl 9.3.1.3). La Auditoría inicial es seguida por una Auditoría de Vigilancia
parcial (17021-1:2015 - Cl 9.6.2.2) en cada uno de los siguientes dos (2) años y una Re-auditoría
completa, también conocida como “Auditoría de Recertificación” (17021-1:2015 - Cl 9.6.3.2) en el
tercer (3er) año. Una auditoría de recertificación también puede incluir una auditoría de Etapa 1 si
ha habido cambios significativos en el SGC que no se han evaluado adecuadamente de otra
manera.
Las auditorías especiales (17021-1:2015 - Cl 9.6.4.2), las auditorías realizadas por las autoridades
reguladoras y las auditorías no anunciadas son auditorías extraordinarias potenciales que pueden
ocurrir en cualquier momento dentro del ciclo de auditoría.
Nota: No todas las autoridades reguladoras participantes del MDSAP requieren, o hacen uso de,
documentos de certificación relacionados con el SGC de una organización de dispositivos médicos.
Los términos “certificación” y “recertificación” aparecen en este documento para mantener la
coherencia con la terminología utilizada en ISO / IEC 17021-1:2015 Evaluación de la conformidad -
Requisitos para los organismos que proporcionan auditoría y certificación de sistemas de gestión.
El ciclo de auditoría de un sistema de gestión de la calidad para dispositivos médicos estériles
debe incluir una evaluación integral del control de la esterilidad del dispositivo, generalmente
durante la auditoría inicial / recertificación. La auditoría de vigilancia, en ausencia de cambios que
afecten significativamente el control de esterilidad, puede limitarse a la verificación de la
implementación adecuada de los parámetros validados del proceso; actividades de control y
seguimiento; y lanzamiento del producto final. Si bien algunas actividades de auditoría se pueden
realizar de forma remota (por ejemplo, revisión del informe de validación del proceso de
esterilización), las actividades remotas por sí solas no pueden garantizar de manera efectiva el
control integral de los procesos de esterilización del dispositivo. El resultado de dichas actividades
de revisión remota debe servir como entrada para la auditoría in situ y debe incorporarse o
adjuntarse al informe de auditoría del MDSAP. La evaluación fuera del sitio de los controles de
esterilidad del producto no debe impedir que el equipo de auditoría en el sitio siga las pistas de
auditoría, incluidas las pistas de auditoría que requieren la revisión de documentos que se habían
evaluado previamente de forma remota.
MDSAP AU P0002.005 12 Página
Durante el curso del ciclo de auditoría, todas las familias de productos y los procesos importantes
deben evaluarse cuando sea posible.
La selección de muestras durante las auditorías para obtener evidencia de conformidad o no
conformidad con los criterios de auditoría del MDSAP puede basarse en estadísticas o en juicios.
Se prefiere el muestreo basado en juicios utilizando pistas de auditoría de una tarea o proceso para
informar la selección de muestras en otras tareas o procesos. Cuando sea posible, los auditores
deben seleccionar muestras de registros que representen a todas las jurisdicciones participantes
del MDSAP aplicables a la auditoría.
Auditoría Inicial (Auditoria de Certificación Inicial)
La auditoría "Inicial", también conocida como "Certificación inicial", consta de una auditoría de
Etapa 1 y Etapa 2.
Etapa 1 – Revisión de la documentación, evaluación de la preparación para la auditoría de la Etapa
2, etc.
Se debe realizar una auditoría Etapa 1 de acuerdo con la Cláusula 9.3.1.2 de ISO / IEC 17021-1:
2015 y todas las tareas del Proceso de Auditoría MDSAP y los requisitos reglamentarios aplicables.
Desde la perspectiva del MDSAP, los propósitos principales de una auditoría Etapa 1 son (1)
determinar si la documentación del SGC requerida por ISO 13485:2016 - Cláusulas 4.2.1 y otros
requisitos de documentación MDSAP aplicables se han definido y documentado adecuadamente;
(2) evaluar la preparación de la organización de dispositivos médicos para una auditoría Etapa 2;
(3) proporcionar un enfoque para planificar una auditoría Etapa 2; y (4) recopilar información sobre
el alcance del sistema de gestión de la calidad y otros aspectos de la organización de dispositivos
médicos.
Partes de una auditoría Etapa 1 (por ejemplo, revisión de la documentación) se pueden realizar en
un sitio que no sea el sitio (s) de la organización de dispositivos médicos que busca la certificación
inicial.
El resultado de la auditoría Etapa 1 ayudará a la Organización de Auditoría reconocida por el
MDSAP a determinar si la organización de dispositivos médicos está preparada para someterse a
una auditoría Etapa 2. La Organización de Auditoría deberá determinar la mejor manera de realizar
las tareas de la Etapa 1 y la Etapa 2 con respecto a la documentación externa y la revisión de
registros y las verificaciones en el sitio. Por lo tanto, partes de una auditoría de la Etapa 1 (por
ejemplo, revisión de la documentación) se pueden realizar en un sitio que no sea el sitio (s) de la
organización de dispositivos médicos que busca la certificación inicial. En la práctica, se pretende
que la organización auditora pueda combinar elementos de la etapa 1 y la etapa 2 para permitir
una única visita in situ para la auditoría inicial o una nueva auditoría de la organización de
dispositivos médicos.
Etapa 2 - Evaluación de la implementación y efectividad del SGC
Se debe realizar una auditoría Etapa 2 de acuerdo con la Cláusula 9.3.1.3 de ISO / IEC 17021-1:
2015 y utilizando todas las tareas del Proceso de Auditoría MDSAP aplicables.
El propósito de una auditoría Etapa 2 es determinar si se han implementado todos los requisitos
aplicables de ISO 13485:2016 y los requisitos reglamentarios relevantes de las autoridades
reguladoras participantes. Los objetivos de la auditoría de la etapa 2 deben incluir específicamente
una evaluación de:
la eficacia del SGC de la organización de dispositivos médicos que incorpora los requisitos
reglamentarios aplicables;
MDSAP AU P0002.005 13 Página
tecnologías relacionadas con productos / procesos (por ejemplo, moldeo por inyección,
esterilización);
documentación técnica del producto adecuada en relación con los requisitos
reglamentarios pertinentes; y,
la capacidad de la organización de dispositivos médicos para cumplir con estos requisitos.
Como parte del logro de estos objetivos, el auditor debe verificar que la organización de
dispositivos médicos mantenga evidencia objetiva suficiente y confiable para demostrar que sus
dispositivos cumplen con los principios esenciales de seguridad, desempeño y efectividad y
cualquier otro requisito reglamentario identificado en las tareas de auditoría. Esta verificación es
para asegurar que la documentación y los registros requeridos por las regulaciones nacionales de
las Autoridades Reguladoras participantes estén presentes, actualizados y completos. El auditor
debe esperar que la documentación y los registros se mantengan para demostrar el cumplimiento
continuo de los requisitos reglamentarios durante la fase posterior a la comercialización del ciclo de
vida del dispositivo.
Se realizará una auditoría Etapa 2 en todos los sitios que se registrarán en el certificado. (Por lo
tanto, cualquier sitio que sea relevante para el sistema de gestión de calidad de la organización de
dispositivos médicos pero que haya sido auditado fuera del sitio, no debe registrarse en el
certificado).
Auditorías de Vigilancia
(1ª y 2ª Auditorías de Vigilancia):
Se debe realizar una Auditoría de Vigilancia de acuerdo con la Cláusula 9.6.2.2 de ISO / IEC
17021-1:2015 y la cláusula 9.6.2 de IMDRF / MDSAP WG / N3:2016 y utilizando las tareas del
Proceso de Auditoría MDSAP aplicables.
El propósito de una serie de auditorías de vigilancia es asegurar que todos los requisitos aplicables
de ISO 13485:2016 y los requisitos regulatorios relevantes de las autoridades reguladoras
participantes sean auditados durante el ciclo de un programa de auditoría de tres años para la
organización de dispositivos médicos. Los objetivos de la auditoría de vigilancia durante el ciclo de
auditoría deben incluir específicamente la evaluación de:
la eficacia del SGC de la organización de dispositivos médicos que incorpora los requisitos
reglamentarios aplicables.
la capacidad de la organización de dispositivos médicos para cumplir con estos requisitos;
y
tecnologías relacionadas con productos / procesos nuevos o modificados; y,
documentación técnica nueva o modificada del producto en relación con los requisitos
reglamentarios pertinentes.
Además, las auditorías de vigilancia deben incluir una revisión de los problemas relacionados con
la seguridad y eficacia de los dispositivos médicos desde la última auditoría, como quejas, informes
de problemas, Reportes de Vigilancia y Retiros / Correcciones de Campo / Notificaciones de
Advertencia.
Estos objetivos permiten que la organización de auditoría reconocida por el MDSAP mantenga la
confianza de que el SGC continúa cumpliendo los requisitos entre las reevaluaciones (auditorías de
recertificación). El auditor debe esperar nuevamente que la documentación y los registros se
mantengan para demostrar el cumplimiento continuo de los requisitos reglamentarios durante la
fase posterior a la comercialización del ciclo de vida del dispositivo.
MDSAP AU P0002.005 14 Página
Las auditorías de vigilancia no requieren una auditoría Etapa 1 a menos que se hayan producido
cambios significativos desde la última auditoría. Por ejemplo, cuando hay cambios en el SGC
asociados con nueva legislación o cambios legislativos, o si la Organización de Auditoría lo
considera necesario.
No es necesario que cada auditoría de vigilancia individual del ciclo cubra todos los requisitos del
MDSAP. Sin embargo, como mínimo, cada auditoría de vigilancia debe abordar lo siguiente (según
corresponda):
a) Una revisión de los cambios en la organización de dispositivos médicos, su SGC o sus
productos, desde la auditoría anterior.
Nota: los cambios pueden requerir aplicaciones regulatorias.
b) Las tareas del proceso de auditoría de MDSAP que se enumeran en la tabla del
Apéndice 1 de MDSAP AU P0008 - Procedimiento de determinación del tiempo de
auditoría.
Nota: Cuando haya indicadores de no conformidades existentes o potenciales en los
datos, u otra información observada durante una auditoría de vigilancia que sugiera
que dichas no conformidades no han sido tratadas adecuadamente por el SGC de la
organización de dispositivos médicos, una auditoría del Proceso de Diseño y
Desarrollo y / o el Proceso de Controles de Producción y Servicio debe enfocarse en
aquellos indicadores de no conformidades existentes o potenciales.
Nota: Si la primera auditoría de vigilancia incluye el Proceso de Diseño y Desarrollo, la
segunda vigilancia debe incluir el Proceso de Controles de Producción y Servicio (o
viceversa) a menos que otros indicadores de no conformidades existentes o
potenciales dicten lo contrario.
c) Confirmación de que la organización de dispositivos médicos cuenta con arreglos para
mantener actualizada la documentación técnica de todos los dispositivos (ver Anexo
1).
d) El uso de marcas y referencias a la certificación.
Se proporciona orientación sobre la selección de muestras de datos para la auditoría de los
procesos en a) y b) anteriores dentro de las tareas relevantes de esos Procesos de Auditoría
MDSAP. La selección debe limitarse a los datos que sean relevantes para los procesos en a) y b)
anteriores.
Re-auditoría (Auditorías de Recertificación)
Se debe realizar una nueva auditoría (auditoría de recertificación) de acuerdo con la cláusula 9.6.3
de la norma ISO / IEC 17021-1:2015 y utilizando todas las tareas del proceso de auditoría de
MDSAP aplicables.
El propósito de una nueva auditoría es confirmar la relevancia, aplicabilidad e idoneidad continuas
del SGC de la organización de dispositivos médicos (en su conjunto), para satisfacer todos los
requisitos aplicables de ISO 13485:2016 y los requisitos reglamentarios relevantes de las
autoridades reguladoras participantes, con respecto al alcance de la certificación. Los objetivos de
la auditoría de recertificación deben incluir específicamente la evaluación de:
la eficacia del SGC de la organización de dispositivos médicos que incorpora los requisitos
reglamentarios aplicables
tecnologías relacionadas con productos / procesos (por ejemplo, moldeo por inyección,
esterilización)
MDSAP AU P0002.005 15 Página
documentación técnica adecuada del producto en relación con los requisitos
reglamentarios pertinentes
el cumplimiento continuo de estos requisitos por parte de la organización de dispositivos
médicos.
Las reevaluaciones no requieren una auditoría Etapa 1 a menos que se hayan producido cambios
significativos desde la última auditoría. Por ejemplo, cuando hay cambios en el SGC asociados con
nueva legislación o cambios legislativos, o si la Organización de Auditoría lo considera necesario.
Si ha habido cambios significativos en el SGC, las organizaciones de auditoría deben revisar la
documentación que implementa esos cambios de acuerdo con la Cláusula 9.6.3.1.3 de 17021-
1:2015. Las reevaluaciones pueden ser más breves que las auditorías iniciales mediante un
muestreo selectivo y focalizado.
Como parte del logro de los objetivos de una nueva auditoría, un auditor debe verificar los
requisitos de ISO / IEC 17021-1:2015 Cláusula 9.6.3.2.1, y lo siguiente, cuando corresponda:
Una revisión de los informes de auditoría del MDSAP para el ciclo de auditoría actual. Es
decir, los preparados desde la auditoría inicial o la reevaluación anterior.
Una revisión de los cambios en la organización de dispositivos médicos, el SGC o los
productos desde la auditoría de vigilancia anterior.
Un seguimiento de las correcciones y / o acciones correctivas derivadas de los hallazgos
de la auditoría MDSAP anterior, de cualquier tipo.
Una revisión de la efectividad e idoneidad del SGC de la organización de dispositivos
médicos durante el ciclo de auditoría actual.
Todas las tareas del proceso de auditoría de MDSAP aplicables.
La auditoría de los procesos y el muestreo deben centrarse en lo siguiente (en función del riesgo):
diseños nuevos o modificados y nuevos productos.
No conformidades potenciales y existentes previamente identificadas.
procesos nuevos o modificados.
zonas no cubiertas suficientemente durante el período de vigilancia.
Durante una auditoría de recertificación, la organización auditora deberá auditar todos los sitios que
están registrados en el certificado. (Por lo tanto, cualquier sitio que sea relevante para el sistema
de gestión de calidad de la organización de dispositivos médicos pero que haya sido auditado fuera
del sitio, no debe registrarse en el certificado).
Auditorías Especiales
Las auditorías especiales son auditorías extraordinarias en el sentido de que no forman parte del
ciclo de auditoría planificado. Estas auditorías solo deben usarse cuando sea necesario y deben
centrarse en elementos específicos del SGC de la organización de dispositivos médicos.
Las auditorías especiales pueden incluir auditorías realizadas en respuesta a una solicitud de
extensión al alcance de una certificación existente, para determinar si la extensión se puede
otorgar o no o como auditorías con poca antelación realizadas para investigar quejas
potencialmente importantes, o si se proporciona información específica. motivos para sospechar no
conformidades graves de los dispositivos, o por otros motivos.
Se pueden realizar auditorías con poca antelación a solicitud y bajo la dirección de las autoridades
reguladoras participantes del MDSAP o según el criterio de la Organización Auditora.
Las auditorías especiales deben realizarse de acuerdo con los requisitos aplicables de ISO / IEC
17021-1:2015 Cláusula 9.6.4, así como cualquier requisito adicional de la Organización de
MDSAP AU P0002.005 16 Página
Auditoría reconocida por el MDSAP y / o las autoridades reguladoras participantes del MDSAP
(cuando corresponda).
Deben utilizarse auditorías especiales para abordar, según corresponda:
La necesidad de ampliar el alcance de la auditoría o certificación de la organización de
dispositivos médicos para incluir productos nuevos o modificados entre auditorías
programadas regularmente.
Falta de supervisión por parte de la Organización Auditora reconocida por el MDSAP. Por
ejemplo, debido a un tiempo de auditoría insuficiente, una constitución inadecuada del
equipo de auditoría, etc.
Dar seguimiento a problemas específicos de post-comercialización. Por ejemplo, para una
queja potencialmente significativa.
Dar seguimiento a los hallazgos importantes de una auditoría MDSAP anterior.
A solicitud de una autoridad reguladora participante del MDSAP (en base a una asignación
específica).
Realizar auditorías de proveedores según lo dicte la autoridad reguladora o la política de la
Organización de Auditoría.
Una Organización de Auditoría que realiza una auditoría especial a solicitud de la Autoridad
Reguladora reconocida deberá presentar el informe de auditoría a la Autoridad Reguladora
reconocida dentro de los 15 días a partir del último día de la auditoría.
Auditorías No Anunciadas
Otro tipo de auditoría especial es la auditoría no anunciada. Las autoridades reguladoras
participantes del MDSAP requieren que las organizaciones auditoras realicen auditorías sin previo
aviso en circunstancias en las que se hayan detectado no conformidades de alto grado. Consulte
IMDRF / MDSAP WG / N3 Final: 2016 (2ª edición) para conocer los criterios.
Auditorías realizadas por Autoridades Reguladoras
Las autoridades reguladoras participantes del MDSAP también pueden realizar auditorías en
cualquier momento y por una variedad de razones que incluyen (1) "Con causa justificada" debido
a la información obtenida por la autoridad reguladora, (2) como seguimiento de los hallazgos de
una auditoría anterior, y (3) confirmar la implementación efectiva de los requisitos del MDSAP por
parte de las organizaciones auditoras reconocidas por el MDSAP.
El propósito de las auditorías realizadas por las autoridades reguladoras es garantizar la
supervisión adecuada de las actividades de auditoría de una organización de auditoría MDSAP
reconocida, como un medio alternativo de evaluar a las organizaciones de dispositivos médicos
que han sido identificadas como que llevan a cabo procesos de fabricación de alto riesgo y no han
sido auditadas adecuadamente, cuando sea suficiente. Los detalles sobre los procesos auditados
no se han incluido en un informe de auditoría, o cuando hay un historial de bajo cumplimiento con
los requisitos reglamentarios o del SGC.
MDSAP AU P0002.005 17 Página
Capítulo 1 – Gestión
La intención del proceso de gestión es proporcionar recursos adecuados para las actividades de
diseño, fabricación, garantía de calidad, distribución, instalación y servicio de dispositivos; asegurar
que el sistema de gestión de la calidad funcione de manera adecuada y eficaz; y supervisar el
sistema de gestión de la calidad y realizar los ajustes necesarios. Un sistema de gestión de la
calidad que se ha implementado eficazmente y se supervisa para identificar y abordar los
problemas existentes y potenciales tiene más probabilidades de producir dispositivos médicos que
funcionen según lo previsto.
El representante de la dirección es responsable de garantizar que los requisitos del sistema de
gestión de la calidad se hayan definido, documentado, implementado y mantenido de manera
eficaz. Antes de la auditoría de un proceso, puede ser útil entrevistar al representante de la
administración (o su designado) para obtener una descripción general del proceso y una idea del
conocimiento y comprensión de la administración del proceso.
El proceso de Gestión es el primer proceso que se audita según la secuencia de auditoría del
MDSAP.
Auditando el Proceso de Gestión
Propósito: El propósito de auditar el proceso de Gestión es verificar que la alta dirección garantice
que se ha establecido y mantenido un sistema de gestión de calidad adecuado y eficaz. Los
procesos de gestión deben reevaluarse al final de la auditoría para determinar si la alta dirección
ha demostrado el compromiso necesario para un sistema de gestión de la calidad eficaz que se ha
comunicado al personal.
Resultados: Como resultado de la auditoría del proceso de Gestión, la evidencia objetiva mostrará
si la organización de dispositivos médicos tiene:
A) Procesos identificados necesarios para el sistema de gestión de la calidad, su aplicación
en toda la organización de dispositivos médicos y su secuencia e interacción.
B) Procedimientos e instrucciones definidos, documentados e implementados para asegurar
el desarrollo y mantenimiento de un sistema de gestión de la calidad eficaz.
C) Se establecieron objetivos de calidad en las funciones y niveles relevantes dentro de la
organización de dispositivos médicos consistentes con la política de calidad y se aseguró
de que se revisen periódicamente para verificar su idoneidad
MDSAP AU P0002.005 18 Página
D) Determinó los criterios y métodos necesarios para asegurar la operación y control de los
procesos del sistema de gestión de la calidad, incluida la identificación y gestión de
procesos interrelacionados.
E) Comprometió el personal y los recursos adecuados para la infraestructura al sistema de
gestión de la calidad.
F) Asignó responsabilidad y autoridad al personal y estableció la estructura organizacional
para asegurar que los procesos que aseguran la calidad no se vean comprometidos.
G) Planificación de la gestión de riesgos realizada y revisión continua de la eficacia de las
actividades de gestión de riesgos para garantizar que se establezcan políticas,
procedimientos y prácticas para analizar, evaluar y controlar el riesgo.
H) Aseguró la efectividad continua del sistema de gestión de la calidad y sus procesos.
I) Estableció un sistema de gestión de la calidad que sea capaz de producir dispositivos que
sean seguros, efectivos y adecuados para su uso previsto.
Enlaces a Otros Procesos:
Medición, Análisis y Mejora; Diseño y Desarrollo; Compras; Controles de Producción y Servicio;
Autorización de Comercialización de Dispositivos y Registro de Instalación
Tarea 1 – SGC Planeación, Implementación, cambios y Manual de Calidad
Confirmar que la planificación del sistema de gestión de la calidad se lleva a cabo para
asegurar que todos los procesos requeridos son identificados, documentados,
implementados, monitoreados y mantenidos para cumplir con los requisitos aplicables y
alcanzar los objetivos de calidad.
Verificar que los cambios en el sistema de gestión de la calidad se gestionan para mantener
la conformidad del sistema de gestión de la calidad y de los dispositivos producidos.
Verificar que se ha documentado un manual de calidad.
Cláusula y Regulación:
ISO: 13485:2016: 4.1.1, 4.1.2, 4.1.3, 4.2.2, 4.1.4, 5.4.2;
TGA: TG (MD)R Sch3 P1 1.4 (4);
ANVISA: RDC ANVISA 16/2013: 2.1, 5.6;
MHLW / PMDA: MHLW MO169: 5, 7, 14;
FDA: 21 CFR 820.20]
Requisitos adicionales específicos del país:
Ninguno.
Evaluación de la conformidad:
Sistema de Gestión de Calidad
Los fabricantes de dispositivos médicos están obligados a establecer un sistema de gestión de la
calidad (incluyendo procedimientos e instructivos del sistema de calidad) adaptado a las funciones
MDSAP AU P0002.005 19 Página
reglamentarias asumidas por el fabricante y los dispositivos médicos que están fabricando o
diseñando. El sistema de gestión de la calidad del fabricante debe aplicar correctamente todos los
requisitos aplicables de los dispositivos médicos - Sistemas de gestión de la calidad - Requisitos
para fines reglamentarios (ISO 13485: 2016), los requisitos del Sistema de Gestión de la Calidad
de los Procedimientos de Evaluación de la Conformidad del Reglamento Australiano de Productos
Terapéuticos (MD) R Sch3), las Buenas Prácticas de Fabricación del Brasil (RDC ANVISA
16/2013), la Ordenanza de QMS japonesa (MHLW MO 169), el Reglamento del Sistema de Calidad
(21 CFR Part 820) y los requisitos específicos de las autoridades reguladoras de dispositivos
médicos que participan en el programa MDSAP, así como otros controles necesarios para asegurar
que sus dispositivos terminados, el diseño y los procesos de fabricación, y todas las actividades
relacionadas con las especificaciones aprobadas.
Procedimientos e instructivos del Sistema de Calidad:
La organización puede referirse a éstos como documentos de nivel 1. Por lo general, son
documentos de alto nivel, no relacionados con el producto y no relacionados con el proceso, y
normalmente se encuentran en el Manual de Calidad. Estos procedimientos e instructivos pueden
contener información sobre la secuencia e interacción de diversos procesos del sistema de gestión
de calidad. Se espera que cuando la norma especifica que se requiere documentar un determinado
proceso, también se requiere establecerlo, implementarlo y mantenerlo. 3 El Manual de Calidad
consiste en esbozar la estructura de la documentación y describir la interacción de procesos (por
ejemplo, los procesos para identificar no conformidades y correcciones y los procesos para
investigar las no conformidades para determinar la causa raíz y las acciones correctivas).
Planeación del Sistema de Gestión de la Calidad:
La planeación de la calidad se ocupa del diseño e implementación del sistema de gestión de la
calidad. Dicha planificación ocurre típicamente durante el desarrollo e implementación inicial de un
sistema de calidad, pero también ocurre cuando hay cambios en la política de calidad, objetivos de
calidad, SGC y requisitos reglamentarios, o cuando los cambios son necesarios para que el SGC
continúe siendo efectivo. La planificación de la calidad a este nivel no debe confundirse con la
planificación de calidad descrita en la cláusula 7.1 de la norma ISO 13485: 2016.
La evidencia de la planificación del sistema de calidad debe incluir al menos documentos que
identifiquen y registren las entradas y salidas de la planificación del sistema de calidad. También
puede estar disponible un procedimiento para la planificación del sistema de calidad.
Las entradas para la planificación de la calidad pueden incluir:
Política de Calidad.
Objetivos de Calidad.
Normas del Sistema de Gestión de la Calidad (por ejemplo, ISO 13485: 2016).
Los Requisitos Regulatorios.
Requisitos Específicos del Producto (por ejemplo, mantenimiento, instalación, etc.).
Estrategias de Mitigación del Riesgo (por ejemplo, capacitación de los usuarios).
Cambios Requeridos (por ejemplo, identificados durante las Auditorías o Revisiones de la
Dirección).
Los resultados de la planificación de la calidad pueden incluir, entre otros:
Una descripción de los procesos del SGC y sus entradas, salidas, secuencias e
interacciones.
El manual de calidad y los procedimientos asociados.
Un análisis de las deficiencias.
MDSAP AU P0002.005 20 Página
Identificación o recursos necesarios para implementar el SGC.
Identificación de las competencias y la formación necesarias para aplicar el SGC.
Implementación y Planes de Acción.
La planificación del sistema de gestión de la calidad también debe utilizarse cuando se contemplan
o se requieren cambios en el sistema de gestión de la calidad para garantizar la conformidad
permanente del SGC.
3
ISO 13485:2016 – Cláusula 0.2
Enlaces
Medición, Análisis y Mejora; Diseño y Desarrollo; Compras; Controles de Producción y Servicio;
Autorización de Comercialización de Dispositivos y Registro de Instalación
Durante la auditoría, siempre que se identifique un cambio, verifique que la organización de
dispositivos médicos haya implementado los controles de cambio adecuados.
Tarea 2 – Representante de la Dirección
Confirmar que la alta dirección ha documentado el nombramiento de un representante de la
dirección.
Verificar que las responsabilidades del representante de la dirección incluyen asegurar que
los requisitos del sistema de gestión de la calidad se establezcan y mantengan
efectivamente, informen a la alta dirección sobre el desempeño del sistema de gestión de la
calidad y aseguren la promoción de los requisitos reglamentarios en toda la organización.
Cláusula y Regulación:
ISO: 13485:2016: 5.5.2;
TGA: TG (MD) R Sch3 P1 1.4 (5)(b)(ii);
ANVISA: RDC ANVISA 16/2013: 2.2.5;
MHLW/PMDA: MHLW MO169:16;
FDA: 21 CFR 820.20 (b)
Requisitos adicionales específicos del país:
Ninguno.
Evaluación de la conformidad:
Representante de la Dirección
MDSAP AU P0002.005 21 Página
Es importante confirmar que la alta dirección ha nombrado a un representante de la dirección y que
las responsabilidades y autoridades del representante de la dirección han sido definidas,
documentadas e implementadas. El nombramiento del representante de la dirección debe ser
documentado.
Confirmar Nombramiento
La organización puede documentar el nombramiento de un representante de la dirección en un
organigrama, un Manual de Calidad, un memorando al archivo, una descripción de posición u otra
manera apropiada. El nombramiento del representante de la dirección puede hacerse por nombre o
título.
Evaluar la responsabilidad y la autoridad
Confirmar que el representante de la dirección ha establecido la responsabilidad y la autoridad para
asegurar que el sistema de gestión de la calidad es efectivamente definido, documentado,
implementado y mantenido. El representante de la dirección también debe haber establecido la
responsabilidad y la autoridad para informar a la alta dirección sobre el desempeño del sistema de
gestión de la calidad.
La confirmación se puede realizar entrevistando al representante de la dirección y la alta dirección
y revisando el Manual de Calidad, la descripción de posición del representante de la dirección o
documentos similares.
Otros ejemplos
Ejemplos adicionales de evidencia de las responsabilidades y autoridades del representante de la
dirección pueden incluir:
Autorización de firma para cambios en procedimientos, procesos, diseños, etc.
Autoridad para actuar en nombre de la alta dirección durante la auditoría.
Autorización para poner productos o procesos en espera.
Responsabilidad para las funciones de la Gestión de la Auditoría de Calidad.
Responsabilidad para contribuir a actividades de Acciones Correctivas y Preventivas,
Manejo de Quejas y Manejo de Productos No Conformes, etc.
Formación
Cuando las actividades realizadas personalmente por el representante de la dirección dan lugar a
una determinación de si el producto cumple con los requisitos, incluidos los requisitos
reglamentarios, el representante de la dirección debe ser competente para llevar a cabo dichas
actividades. En tales casos, verificar que la formación y la experiencia incluyan los requisitos
reglamentarios pertinentes.
Enlaces
Ninguno
Tarea 3 – Política y Objetivos de Calidad
Verificar que se han establecido una política y objetivos de calidad en las funciones y
niveles pertinentes dentro de la organización de Dispositivos Médicos.
Asegurar que los objetivos de calidad sean mensurables y coherentes con la política de
calidad.
Confirmar que se toman las medidas apropiadas para alcanzar los objetivos de calidad.
MDSAP AU P0002.005 22 Página
Cláusula y Regulación:
ISO: ISO 13485:2016: 5.3, 5.4.1;
TGA: TG (MD)R Sch3 P 1 1.4 (5) (a);
ANVISA: RDC ANVISA 16/2013: 2.2.1;
MHLW/PMDA: MHLW MO169: 12, 13;
FDA: 21CFR 820.20 (a)
Requisitos adicionales específicos del país:
Ninguno.
Evaluación de la conformidad:
Política de calidad
Una política de calidad es el compromiso de una o más declaraciones de las intenciones de la
organización y la dirección con respecto al cumplimiento de los requisitos acordados. La alta
dirección debe establecer la política de calidad y asegurar que se establezcan objetivos de calidad
que sean consistentes con la política de calidad. La alta dirección debe asegurarse de que la
política de calidad se entienda y se comunique a todos los niveles de la organización. Una
evaluación de si el sistema de calidad de la organización está cumpliendo con la política y los
objetivos de calidad establecidos debe ser un tema abordado durante las revisiones de la dirección.
Objetivos de calidad
Una forma eficaz de determinar si se han aplicado objetivos de calidad es pedir ejemplos de
objetivos de calidad y el estado de estos objetivos. Típicamente, un objetivo de calidad se expresa
como un objetivo o meta mensurable. Un ejemplo del objetivo de calidad de una organización
podría ser "que todos los componentes esenciales cumplan con las especificaciones con una tasa
de fiabilidad definida o mejor".
Para lograr este objetivo, la organización tendrá que identificar, evaluar y aprobar proveedores
confiables o traer la fabricación de ese componente a las propias instalaciones (in-house).
Enlaces
Ninguno
Tarea 4 – Estructura Organizacional, Responsabilidad, Autoridad, Recursos
Revisar la estructura organizacional del fabricante y los documentos relacionados para
verificar que incluyan provisiones para responsabilidades, autoridades (por ejemplo,
representante de la dirección), personal, recursos para infraestructura, competencias y
capacitación para asegurar que el personal tenga la competencia necesaria para diseñar y
fabricar dispositivos de conformidad con las disposiciones previstas y los requisitos
reglamentarios aplicables.
Cláusula y Regulación:
ISO: ISO 13485:2016: 5.1, 5.5.1, 5.5.2, 6.1, 6.2;
TGA: TG (MD)R Sch3 P1 1.4 (5) (b);
MDSAP AU P0002.005 23 Página
ANVISA: RDC ANVISA 16/2013: 2.2.2, 2.2.3. 2.2.4, 2.3;
MHLW/PMDA: MHLW MO169: 10, 15, 16, 21, 22, 23; 21
FDA: CFR 820,20 (b), 820.25
Requisitos adicionales específicos del país:
Ninguno.
Evaluación de la conformidad:
Responsabilidad y autoridad
Los métodos para completar esta tarea de auditoría incluyen revisar el organigrama y solicitar
preguntas de autoridad y responsabilidad. Las responsabilidades y las autoridades de varios
individuos dentro de la organización también se describen típicamente en el Manual de Calidad,
Descripciones y Perfiles de Puestos.
Recursos
La alta dirección es responsable de asegurar que los recursos necesarios para mantener un
sistema eficaz de gestión de la calidad se proporcionan. Los recursos incluyen dinero, equipo,
suministros y personal. Un método para confirmar que se dispone de recursos adecuados es pedir
al representante de la dirección que proporcione varios ejemplos de solicitudes recientes para
diferentes tipos de recursos y describa los resultados de estas solicitudes.
Enlaces
Ninguno
Tarea 5 – Alcance de la Subcontratación
Determinar el alcance de la subcontratación de procesos que puedan afectar la conformidad
del producto con los requisitos especificados y verificar la documentación adecuada de los
controles en el Sistema de Gestión de Calidad.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.1.5, 4.2.1;
TGA: TG (MD)R Sch3 P1 1.4 (5) (b) (iii), (d) (ii);
ANVISA: RDC ANVISA 16/2013: 2.5;
MHLW/PMDA: MHLW MO169: 5, 6;
FDA: 21 CFR 820.50
Requisitos adicionales específicos de cada país:
Australia (TGA):
Las condiciones de la autorización de comercialización (inclusión de ARTG) requieren que los
patrocinadores australianos lleven a cabo algunas actividades regulatorias que incluyen; manejo de
quejas del cliente (Ley s 41FN, Reg 5.8), la gestión y comunicación de archivos técnicos /
documentación técnica (Ley s 41FN (3)), reporte de eventos adversos (Ley s 41FN, Reg 5.7),
MDSAP AU P0002.005 24 Página
realización de retiros (Parte 4-9) ), asegurando que el nombre y la dirección del Patrocinador se
proporcionen con el dispositivo (Reg 10.2), el almacenamiento de dispositivos (Act s 41FN, Reg
5.9), el mantenimiento de registros de quejas y distribución (Act s 41FN, Reg 5.10), informe anual
durante un período inicial de tres años, de información específica a la TGA (ACT s41FN, Reg 5.11)
para dispositivos de Clase AIMD, Clase III y Clase IIb que son implantables, información sobre el
suministro de IVD específicos (Act s41FN, Reg 5.12) , asegurándose de que no se suministren
algunos dispositivos que contravengan la Parte 2 de los estándares de Venenos.
Algunos patrocinadores también brindan servicios para la instalación y el mantenimiento de un
dispositivo en nombre del fabricante y, en consecuencia, deben ser tratados como proveedores del
fabricante.
Cuando un requisito reglamentario para un patrocinador se cruza con un requisito reglamentario o
un requisito de ISO13485 para el fabricante, la actividad se tratará como una actividad
subcontratada y se documentará en el SGC del fabricante. Consulte también la Tarea 5, Compras.
El requisito de la Regulación 10.2 para “asegurar que el nombre y la dirección del Patrocinador se
proporcionen con el dispositivo de tal manera que el usuario del dispositivo pueda identificar
fácilmente al Patrocinador” es solo una obligación del Patrocinador. Esta actividad no necesita
estar incluida en la documentación del SGC del fabricante, sin embargo, los arreglos para el
suministro de esta información deben ser divulgados en el acuerdo escrito entre el fabricante y el
patrocinador. En los casos en que una actividad realizada por el Patrocinador también incluya la
provisión de información requerida por el Principio Esencial 13 (Etiquetas e Instructivo de Uso), o
13A (tarjetas de implantes del paciente y folletos), el Fabricante debe tratar al Patrocinador como
proveedor de esa actividad.
El Patrocinador no necesita ser tratado como un proveedor si el alcance del sistema de gestión de
calidad del Fabricante incluye el sitio y las actividades del Patrocinador. La supervisión de las
actividades exigidas por la legislación que deben realizar los patrocinadores debe estar claramente
documentada en el SGC e incluida en los planes de auditoría interna.
Canadá (HC):
Verificar que las funciones y responsabilidades de los corresponsales regulatorios, importadores,
distribuidores o proveedores de un servicio estén claramente documentadas en el sistema de
gestión de calidad de la organización y sean calificadas y controladas como proveedores, según
proceda.
Evaluación de la conformidad:
Subcontratación
La mayoría de las organizaciones subcontratan al menos algunos productos (incluidos los
servicios) que afectan la capacidad del dispositivo médico de ajustarse a los requisitos
especificados. Algunas organizaciones subcontratan la mayoría de los productos. Durante la
entrevista del representante de la dirección, determinar hasta qué punto la organización
subcontrata los procesos esenciales para el buen funcionamiento del dispositivo médico terminado.
El desempeño del proceso y la conformidad del producto, incluyendo el desempeño del producto
suministrado, deben ser incluidos en la revisión de la revisión. La organización del Dispositivo
Médico debe garantizar el control de los productos y procesos de subcontratados que afectan la
conformidad del producto con los requisitos especificados.
Enlaces
Compras
MDSAP AU P0002.005 25 Página
Durante la auditoría del proceso de compras de la organización del dispositivo médico, asegurar de
que la dirección ha asegurado el nivel adecuado de control sobre los proveedores, incluyendo una
evaluación de la relación entre los productos suministrados y el riesgo del producto.
Tarea 6 – Competencia y Capacitación del Personal
Confirmar que la organización del dispositivo médico ha determinado las competencias
necesarias para el personal que realiza trabajos que afectan la calidad del producto,
proporcionado una capacitación adecuada y concientizó al personal sobre la relevancia e
importancia de sus actividades en la calidad del producto y el logro de los objetivos de
calidad.
Asegurar que se mantengan registros de la capacitación y las competencias.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 6.2;
ANVISA: RDC ANVISA 16/2013: 2.2.3, 2.2.4, 2.3;
MHLW/PMDA: MHLW MO169: 6, 22,23, 25.4;
FDA: 21 CFR 820.20 (b) (2), 820.25
Requisitos adicionales específicos de cada país:
Brasil (ANVISA):
Confirmar que el fabricante se asegure de que cualquier consultor que brinda orientaciones sobre
diseño, compra, fabricación, envasado, etiquetado, almacenamiento, instalación o mantenimiento
de dispositivos médicos tiene la calificación adecuada para realizar dichas tareas. Dichos
consultores serán contratados como proveedores de servicios formales, de acuerdo con los
controles de compra definidos por el fabricante [RDC ANVISA 16/2013: 2.3.3].
Evaluación de la conformidad:
Capacitación
Se puede realizar una revisión de los registros de capacitación de los empleados para asegurarse
de que han sido capacitados con respecto a la política y objetivos de calidad de la organización. En
particular, esto debe hacerse para los empleados involucrados en operaciones claves que afectan
la realización y la calidad del producto.
Durante la auditoría del proceso de Control de Producción y Servicios, asegurar de que los
empleados que participan en operaciones claves que afectan la realización del producto y la
calidad del producto han recibido capacitación en sus tareas específicas, así como en la política y
objetivos de calidad.
Cuando sea apropiado, revisar los registros de capacitación para los empleados cuyas actividades
han contribuido a procesar las No Conformidades.
Enlaces
Controles de Producción y Servicio
Tarea 7 – Planeación y Revisión de la Gestión de Riesgos
MDSAP AU P0002.005 26 Página
Verificar que la dirección se ha comprometido y tiene responsabilidad en la planificación
general de la gestión de riesgos, incluida la revisión continua de la efectividad de las
actividades de gestión de riesgos, asegurando que las políticas, procedimientos y prácticas
se establezcan y documenten para analizar, evaluar y controlar el riesgo del producto
durante la realización del mismo.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.1.2 (b), 7.1;
TGA: TG (MD)R Sch1 P1 2;
ANVISA: RDC ANVISA 16/2013: 2.4;
MHLW/PMDA: MHLW MO169: 26;
FDA: 21 CFR 820.30 (g)
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Compromiso con la Gestión de Riesgos
Confirmar que la alta dirección ha demostrado su compromiso con el proceso de gestión de riesgos
asegurando la provisión de recursos adecuados y la asignación de personal calificado para las
actividades de Gestión de Riesgos. Las decisiones basadas en el riesgo ocurren a lo largo de los
diversos procesos del sistema de gestión de la calidad. La alta dirección es responsable de definir
y documentar la política para determinar los criterios de aceptabilidad del riesgo. Además, asegurar
de que la alta dirección revise la idoneidad del proceso de gestión de riesgos. Esta revisión puede
ser parte de la revisión de la dirección. Los riesgos previamente no identificados descubiertos
durante la producción y la postproducción del Dispositivo Médico pueden indicar la necesidad de
mejorar el proceso de gestión de riesgos. Cada organización debe decidir la medida en que el
riesgo es aceptable.
Cuando proceda, evaluar el papel de la alta dirección cuando se toman decisiones basadas en el
riesgo que parecen justificar niveles de riesgo que no cumplen con los criterios de aceptación de
riesgo previamente establecidos por la organización.
La Gestión del Riesgo generalmente comienza en conjunción con el proceso de planificación del
diseño y desarrollo en un momento del desarrollo cuando los resultados del análisis de riesgo
pueden afectar el proceso de diseño. Durante la auditoría del proceso de diseño y desarrollo,
evaluar el compromiso de la alta dirección con las actividades de gestión de riesgos. La evidencia
del compromiso con la gestión de riesgos puede incluir la implementación de controles nuevos o
más estrictos, controles externos (por ejemplo, controles adicionales relacionados con el
proveedor) o cambios de diseño para mantener un nivel aceptable de riesgo de producto
Enlaces
Diseño y Desarrollo
Tarea 8 – Control de Documentos y registros
Verificar que los procedimientos han sido definidos, documentados e implementados para
el control de documentos y registros de origen interno y externo requeridos por el sistema
de gestión de calidad.
MDSAP AU P0002.005 27 Página
Confirmar que la organización de Dispositivos Médicos conserva los registros y al menos
una copia obsoleta de los documentos controlados durante un período de tiempo por lo
menos equivalente a la vida útil del dispositivo, pero no menos de dos años a partir de la
fecha de liberación del producto.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.1.4, 4.2.1, 4.2.4, 4.2.5;
TGA: TG (MD)R Sch3 P1 1.4 (4);
ANVISA: RDC ANVISA 16/2013: 3.1;
MHLW / PMDA: MHLW MO169: 5, 6, 8, 9;
FDA: 21 CFR 820.40, 820.180
Requisitos adicionales específicos de cada país:
Australia (TGA):
Confirmar que la documentación y los registros del Sistema de Gestión de Calidad en relación con
un dispositivo descrito en TG(MD)R Sch3 P1 1.9 son conservados por el fabricante durante al
menos 5 años.
Tener en cuenta que las condiciones de la autorización de comercialización (inclusión de ARTG)
requieren que los patrocinadores australianos de IVD Clase III / AIMD, Clase IIb o Clase 4
implantables mantengan registros de distribución y registros de información relacionada con
cualquier mal funcionamiento o deterioro en las características o desempeño de un dispositivo, o
cualquier insuficiencia en el diseño, fabricación, etiquetado, instrucciones de uso o materiales
publicitarios de un dispositivo, o cualquier uso de acuerdo con, o contrario al uso previsto por el
fabricante de un dispositivo, que haya dado lugar a cualquier queja o problema en relación con el
dispositivo, por un período de hasta 10 años. (Reg 5.10).
Estos requisitos deben reflejarse en el acuerdo escrito entre el patrocinador australiano y el
fabricante y también pueden estar identificados en los procedimientos del fabricante.
Brasil (ANVISA):
Verificar que los registros de cambios incluyan una descripción del cambio, la identificación de los
documentos afectados, la firma del (de los) individuo (s) aprobador (es), la fecha de aprobación y
cuándo el cambio entre en vigencia [RDC ANVISA 16/2013: 3.1.5].
Confirmar que el fabricante mantiene una Lista Maestra de los Documentos Aprobados y efectivos
[RDC ANVISA 16/2013: 3.1.5].
Verificar que los registros y documentos electrónicos tengan copias de seguridad [RDC ANVISA
16/2013: 3.1.6].
Japón (MHLW):
Confirmar que la documentación y los registros del Sistema de Gestión de la Calidad en relación
con un dispositivo se conservan durante los siguientes períodos (5 años para los registros de
capacitación y la documentación). [MHLW MO169: 8.4, 9.3, 67, 68].
(1) 15 años para los “Dispositivos Médicos necesarios para el control de mantenimiento
especialmente diseñado” [o un año más de la vida útil de los productos cuando la vida útil o la
fecha de caducidad (en adelante denominada simplemente "vida útil") más un año supere 15 años].
(2) 5 años para los productos distintos de los “Dispositivos Médicos necesarios para el control de
mantenimiento especialmente diseñado” (o un año más de la vida útil de los productos cuya vida
útil más un año supere los 5 años).
MDSAP AU P0002.005 28 Página
Nota: El “Dispositivo Médico necesario para el control de mantenimiento especialmente diseñado”
se define a continuación en PMD Ley 2.8:
Un dispositivo médico designado por el Ministerio de Salud, Trabajo y Bienestar después de oír la
opinión del Consejo de Asuntos Farmacéuticos y Sanidad Alimentaria, como aquellos cuyo riesgo
potencial para el diagnóstico, el tratamiento o la prevención de la enfermedad es significativo sin un
control adecuado, ya que este tipo de equipo requiere conocimientos de expertos y la habilidad en
el examen de mantenimiento e inspección, reparación y otros manejos.
Estados Unidos (FDA):
Verificar que los registros y documentos electrónicos tengan copias de seguridad [21 CFR
820.180].
Evaluación de la conformidad:
Implementación de procedimientos de documentos y registros
Confirmar que la organización del Dispositivo Médico ha definido, documentado e implementado
procedimientos para el control de documentos y registros del Sistema de Gestión de Calidad. La
evidencia de que estos controles son efectivos puede ser comprobada a través de la auditoría de
los otros procesos del sistema de gestión de calidad. Por ejemplo, la evidencia de que el proceso
de control de documentos es ineficaz podría ser la observación de los procedimientos obsoletos
que se están utilizando o que los registros necesarios no están disponibles.
Asegurar de mantener al menos una copia de documentos controlados obsoletos.
Enlaces
Ninguno
Tarea 9 – Revisiones de la Dirección
Verificar que los procedimientos de Revisión por la Dirección se han documentado, se están
llevando a cabo revisiones de la dirección a intervalos planificados y que incluyen una
revisión de la idoneidad y efectividad de la política de calidad, los objetivos de calidad y el
sistema de gestión de calidad para asegurar que el sistema de gestión de calidad cumple
con todos los requisitos regulatorios aplicables.
Cláusula y Regulación:
ISO: ISO 13485: 2016: 5.6;
TGA: TG (MD)R Sch3 P1 1.4 (5) (b) (iii) (f);
ANVISA: RDC ANVISA 16/2013: 2.2.6;
MHLW/PMDA: MHLW MO169: 18, 19, 20;
FDA: 21 CFR820.20 (c)
MDSAP AU P0002.005 29 Página
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Verificar la implementación de los procedimientos de Revisión de la Dirección
Es importante verificar que la organización de Dispositivos Médicos ha documentado e
implementado procedimientos eficaces de revisión de la gestión. La alta dirección debe revisar la
idoneidad, adecuación y efectividad del sistema de gestión de calidad de la organización de
Dispositivos Médicos a intervalos definidos y con suficiente frecuencia para asegurar que el
sistema de gestión de calidad cumple con los requisitos aplicables de los dispositivos médicos –
Sistemas de Gestión de Calidad – Requerimientos para propósitos regulatorios (ISO 13485:2016),
Buenas Prácticas de Fabricación Brasileñas (RDC ANVISA 16/2013), la Ordenanza Japonesa de
QMS (MHLW MO 169), la Regulación del Sistema de Calidad (21 CFR Parte 820) y los requisitos
específicos de las autoridades regulatorias de dispositivos médicos que participan en el Programa
MDSAP además de la propia política y objetivos de calidad establecidos por la organización de
Dispositivos Médicos. Las fechas y los resultados de las revisiones de la dirección deben ser
documentados. Estos requisitos de documentación deben incluirse en el procedimiento de revisión
de la dirección.
Otros requisitos comúnmente vistos en los procedimientos de revisión de la dirección incluyen una
agenda fija de temas a discutir (con flexibilidad para los temas únicos de la agenda que se
agregarán), los asistentes necesarios que deben participar en la revisión dela dirección y cómo los
elementos de acción resultantes de la revisión de la dirección se deben abordar y participar en el
proceso de Medición, Análisis y Mejora cuando sea necesario. Garantizar que la política y los
objetivos de calidad se han revisado para que continúen siendo adecuados y que se hayan
identificado cambios en los requisitos regulatorios.
Otros requisitos comúnmente vistos en los procedimientos de revisión de la gestión incluyen una
agenda fija de temas a discutir (con flexibilidad para los temas únicos de la agenda que se
agregarán), los asistentes necesarios que deben participar en la revisión de gestión y cómo los
elementos de acción resultantes del examen de gestión se deben abordar y participar en el
proceso de Medición, Análisis y Mejora cuando sea necesario. Asegurar que la política de calidad y
los objetivos se han revisado para su idoneidad continua y que se han identificado cambios en los
requisitos reglamentarios. Otras entradas para la revisión de la dirección incluyen los resultados de
auditorías internas y externas, retroalimentación de los clientes, el desempeño del proceso y la
conformidad del producto, el estado de las acciones preventivas y correctivas, las acciones de
seguimiento de las revisiones de la dirección previas, los cambios que podrían afectar el sistema
de gestión de la calidad y las recomendaciones de mejora.
Durante la auditoría del proceso de Medición, Análisis y Mejora, confirmar cuando sea necesario
que los elementos de acción resultantes de la Revisión de la Dirección sean considerados para
Acciones Correctivas o Preventivas.
Enlaces
Medición, Análisis y Mejora
MDSAP AU P0002.005 30 Página
Tarea 10 – Distribución de Dispositivos con Autorización de Mercado
Adecuados
Confirmar que la organización del Dispositivo Médico ha definido e implementado controles
para garantizar que sólo los dispositivos que han recibido la autorización de
comercialización apropiada se distribuyen o se ofrecen de otra manera para la distribución
comercial en los mercados aplicables.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.1.1, 4.2.1, 5.2, 7.2.1, 7.2.3
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Responsabilidades y autoridades del personal
Durante la auditoría del proceso de Gestión, verificar que la organización del Dispositivo Médico ha
identificado y documentado las responsabilidades de los empleados y el personal para asegurar
que la información apropiada de registro, listado, licencias, notificación e información para
aprobación sea presentada adecuadamente a las autoridades regulatorias o representantes
autorizados (por ejemplo, Patrocinador Australiano) en el MDSAP.
Verificar que la organización del Dispositivo Médico ha identificado y documentado las
responsabilidades y autoridades del personal responsable de implementar los controles para
asegurar que los dispositivos sólo se distribuyen en las jurisdicciones participantes de MDSAP
donde se han obtenido autorizaciones de mercado.
Verificar que estas obligaciones están siendo realizadas por personal competente.
Controles para garantizar la autorización de mercado apropiada
Verificar que la organización del Dispositivo Médico ha identificado, documentado e implementado
controles para asegurar que sólo los dispositivos que han recibido autorización de comercialización
se distribuyen o se ofrecen para su distribución comercial en las jurisdicciones MDSAP
participantes donde la organización pretende suministrar el producto.
Los controles pueden incluir, pero no se limitan a:
Procesos de control de cambios que garanticen que los cambios se evalúan por su impacto
en las autorizaciones de comercialización existentes;
Procedimientos y / o Instructivos de Trabajo que identifiquen claramente las jurisdicciones
en las cuales los productos pueden ser vendidos;
Separar los números de parte de los dispositivos, por jurisdicciones;
Revisión de las órdenes de compra para asegurar los requerimientos del cliente y recibe
solamente producto con la apropiada acreditación del mercado;
Revisión de las prácticas y materiales de ventas y marketing (incluidas las páginas de
Internet) para asegurar que el producto se promueve sólo para mercados en los que el
producto mantiene una apropiada acreditación de mercado;
Segregación de dispositivos terminados en áreas de almacenamiento y envío, por
jurisdicciones;
MDSAP AU P0002.005 31 Página
Reglas de negocio en el software para evitar la aceptación de órdenes de compra donde
no hay autorización de comercialización;
Lenguaje específico en los acuerdos de distribución que limitan los dispositivos que
pueden ser distribuidos en ciertas jurisdicciones;
Materiales de marketing específicos para la jurisdicción (catálogos, sitios web, etc.);
La disponibilidad de información precisa sobre las autorizaciones de comercialización
obtenidas por jurisdicción.
La eficacia de estos controles se puede verificar, por ejemplo:
Entrevistar personal de ventas y personal de atención al cliente;
Entrevistar personal en transporte y distribución;
Software de ERP / Desafío de Ventas;
Revisión de los acuerdos de distribución;
Revisión del material de marketing;
Revisar registros de distribución y / o registros de DHR contra listas de autorizaciones
válidas de mercado.
La verificación de la efectividad de estos controles debe ser específica del (de los) identificador (es)
del dispositivo (por ejemplo, el número de modelo) que figuran en la (s) autorización (es) de
comercialización. Debe seleccionarse una amplia muestra que abarque muchos productos y
jurisdicciones, en particular al revisar los registros de distribución.
Con el fin de prepararse para esta tarea de auditoría, los equipos de auditoría deben asegurarse de
que tienen listas actuales de las autorizaciones de mercado de la organización, así como los
nombres de todos los representantes autorizados en las jurisdicciones MDSAP antes de entrar en
el sitio.
La apropiada aplicación de los procesos de registro, listado, licencias, notificación y aprobación y la
exactitud de la información para la Autorización de Comercialización de Dispositivos para su
presentación a Autoridades Regulatorias o representantes autorizados (por ejemplo, Patrocinador
Australiano) que participan en el MDSAP serán verificados bajo la Autorización de
Comercialización del Dispositivo y el proceso de Registro de Instalaciones. Una revisión preliminar
de la autorización de comercialización de dispositivos y del registro de instalaciones puede hacerse
durante la auditoría del proceso de Gestión, seguida de una cobertura completa para dispositivos
médicos específicos seleccionados para revisión bajo el proceso de Diseño y Desarrollo.
Enlaces:
Autorización de Comercialización de Dispositivos y Registro de Instalación
Tarea 11 – Compromiso de la Alta Dirección con la Calidad
A la conclusión de la auditoría debe decidirse si la Alta Dirección ha demostrado el
compromiso necesario para garantizar que se ha establecido y se mantiene un sistema de
gestión de la calidad adecuado y eficaz y si la eficacia del sistema ha sido comunicada a
personal.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.1.1, 4.1.4, 5.1, 5.5.3;
ANVISA: RDC ANVISA 16/2013: 2.1, 2.2.1;
MHLW/PMDA: MHLW MO169: 5, 10, 17;
FDA: 21 CFR 820.20 (a), 820.5
MDSAP AU P0002.005 32 Página
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Auditoría de los otros procesos
Durante la auditoría de los otros procesos del MDSAP, el equipo de auditoría tendrá la oportunidad
de evaluar si la administración se está llevando a cabo apropiadamente, sus responsabilidades; si
la política de calidad es entendida, implementada y mantenida en todos los niveles de la
organización; si se están proporcionando los recursos necesarios para mantener un sistema eficaz
de gestión de la calidad; si el representante de la dirección tiene las responsabilidades y
autoridades necesarias; la adecuación de la estructura organizacional; y si las revisiones de la
dirección y las auditorías de calidad son efectivas, etc.
Recordar que un sistema de gestión de la calidad que ha sido implementado efectivamente,
monitoreado para identificar y abordar problemas existentes y potenciales, y tiene un proceso
integrado de Gestión de Riesgos que utiliza la toma de decisiones basada en el riesgo es más
probable que produzca Dispositivos Médicos que funcionen como se pretende.
Enlaces
Ninguno
Capítulo 2 – Autorización de Comercialización y Registro de
Instalación
El proceso de Autorización de Comercialización de Dispositivos y Registro de Instalación puede ser
auditado como un enlace del proceso de Gestión y / o el proceso de Diseño y Desarrollo.
Auditando el Procesos de Autorización de Comercialización y Registro de
Instalación
Propósito: El propósito de la auditoría del proceso de Autorización de Comercialización de
Dispositivos y Registro de Instalación es verificar que la organización del Dispositivo Médico ha
realizado las actividades apropiadas en relación con la autorización de comercialización de
dispositivos y el registro de instalación con las autoridades regulatorias que participan en el
MDSAP.
Resultados: Como resultado de la auditoría del proceso de Autorización de Comercialización de
Dispositivos y Registro de Instalación, la evidencia objetiva mostrará si la organización del
Dispositivo Médico ha:
A) Cumplido con los requisitos para registrar y / o licenciar instalaciones de dispositivos.
B) Enviado Información listada de dispositivos a las autoridades regulatorias cuando sea
aplicable.
C) Obtenido Autorización de comercialización del dispositivo en las jurisdicciones apropiadas.
D) Preparado para la evaluación de los cambios (cuando proceda), y obtenida autorización de
comercialización para cambios en los dispositivos o en el sistema de gestión de la calidad
que requieran la modificación de la autorización de comercialización existente.
Enlaces
MDSAP AU P0002.005 33 Página
Gestión: Diseño y Desarrollo
Tarea 1 – Solicitud para la Autorización de Comercialización del Dispositivo
y Registro de Instalación
Verificar que la organización del Dispositivo Médico ha cumplido con los requisitos
regulatorios para registrar y / o licenciar las instalaciones del dispositivo y enviar
información de lista de dispositivos en las jurisdicciones apropiadas donde la organización
comercializa o distribuye sus dispositivos.
Evaluación de la conformidad:
En algunas jurisdicciones, la Autorización de Comercialización de Dispositivos es responsabilidad
del importador / Titular de la Autorización de Comercialización / Patrocinador. Sin embargo, la
autorización de comercialización sólo puede ser apropiada si el fabricante y el importador cumplen
las obligaciones que les han impuesto la legislación pertinente, incluidas las obligaciones mutuas
(por ejemplo, las comunicaciones relativas a la retroalimentación, la notificación de eventos
adversos y la gestión de avisos y retiros).
Previo a una auditoría, una organización de auditoría debe investigar independientemente la
identidad y la gama de productos, instalaciones e importadores (por ejemplo, importador, titular de
la autorización de comercialización, patrocinador, etc.) conocidos por la Autoridad Regulatoria de
cada jurisdicción donde la organización del Dispositivo Médico pretende suministrar el producto.
Verificar en o antes de la auditoría que los requisitos regulatorios para registrar y / o licenciar las
instalaciones del dispositivo y registrar información de lista de dispositivos se hayan aplicado
apropiadamente por la Organización del Dispositivo Médico para cada acuerdo de la Organización
del Dispositivo Médico / importador. Tener en cuenta que algunos Importadores / Titulares de la
Autorización de Comercialización / Patrocinadores pueden haber proporcionado información a las
Autoridades Regulatorias indicando que una Organización del Dispositivo Médico es el "fabricante
legal" aunque el mismo se considere inapropiadamente como un Fabricante de Equipo Original o
un Fabricante de Dispositivo Original. Una revisión del etiquetado del producto que se suministra a
una jurisdicción particular puede ayudar a determinar si se han aplicado procesos apropiados de
autorización de comercialización.
Se debe prestar especial atención a los casos en los que se comercializan productos en
jurisdicciones del MDSAP en las que no se ha otorgado la autorización de comercialización. Esto
puede ser evidente a través de la auditoría de otros procesos, como Diseño y Desarrollo.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.1.1, 4.2.1, 5.2, 7.2.1, 7.2.3
Requisitos específicos del país:
Australia (TGA):
El fabricante de un dispositivo médico es la persona responsable del diseño, la producción, el
embalaje y el etiquetado del dispositivo antes de suministrarlo a nombre de la persona, sea o no la
persona u otra persona que actúe en su nombre, que realiza esas operaciones.
Los importadores australianos (Patrocinadores) están obligados a incluir (registrar) dispositivos
médicos de fabricantes no australianos en el Registro Australiano de Bienes Terapéuticos (ARTG).
Los patrocinadores deben registrar a los fabricantes que representan y obtener un ID de cliente
MDSAP AU P0002.005 34 Página
para el fabricante, el cual debe ser asignado por la TGA. Un fabricante de un dispositivo médico es
también la persona que, con el fin de suministrar el dispositivo a nombre de una persona, realiza
una o más de las siguientes acciones utilizando productos confeccionados: ensambla, empaqueta,
procesa, reacondiciona, etiqueta el dispositivo o asigna un propósito diferente mediante el uso de
etiquetas, instrucciones de uso, publicidad o documentación técnica (TG Act s41BG).
Los importadores australianos (patrocinadores) deben incluir (registrar) dispositivos médicos de
fabricantes no australianos en el Registro Australiano de Productos Terapéuticos (ARTG). Los
patrocinadores deben registrar a los fabricantes que representan y obtener una identificación de
cliente y una identificación de ubicación para el fabricante de la TGA.
Para ayudar al Patrocinador Australiano, los Fabricantes, que están suministrando productos al
mercado australiano y eligen participar en el MDSAP, deben realizar lo siguiente para demostrar
que han cumplido con las obligaciones de los Fabricantes que desean suministrar a Australia;
Clasificar el dispositivo utilizando las reglas de clasificación australianas.
Identificar a partir del Reglamento de productos terapéuticos (dispositivos médicos) de
2002, un procedimiento de evaluación de la conformidad australiano que se aplicará de
acuerdo con la clasificación del dispositivo.
Seleccione un término GMDN relevante.
Obtener una auditoría MDSAP de su SGC y la documentación técnica de su dispositivo de
acuerdo con este Enfoque de auditoría, para demostrar que se han aplicado los requisitos
del SGC del procedimiento de evaluación de la conformidad seleccionado.
Preparar una Declaración Australiana de Conformidad de acuerdo con los requisitos del
Procedimiento de Evaluación de la Conformidad que se ha aplicado [TG (MD) R Sch 3 P1
Cl 1.8].
Firmar un acuerdo por escrito con el Patrocinador. Consultar el Anexo 4 para obtener
orientación sobre las funciones y responsabilidades del patrocinador australiano y un
fabricante extranjero.
Nota: Si el fabricante elige participar en el MDSAP por cualquier motivo y el
producto se suministra al mercado Australiano, los requisitos para el SGC en
un procedimiento de evaluación de la conformidad relevante deben incluirse
en el alcance de la auditoría realizada por una organización auditora
reconocida del MDSAP.
Nota: Los patrocinadores deben proporcionar al fabricante información en
relación con las obligaciones del fabricante en virtud de un procedimiento de
evaluación de la conformidad e información sobre si los dispositivos cumplen
con los Principios Esenciales [TG Act 41FN (3) (e)].
Referirse a:
o La Ley de Bienes Terapéuticos de 1989.
Parte 4-2 - Principios esenciales y estándares de dispositivos médicos.
Parte 4-3 - Procedimientos de evaluación de la conformidad.
Parte 4-5 - Inclusión de productos sanitarios en el Registro.
Parte 4-9 - Notificación Pública y Retiro de Dispositivos Médicos.
Capítulo 5 – Publicidad.
o Reglamento sobre productos terapéuticos (Dispositivos Médicos) 2002.
Parte 5 - División 5.2 – Condiciones.
Anexo 1 - Principios Esenciales.
MDSAP AU P0002.005 35 Página
Anexo 2 - Reglas de Clasificación.
Anexo 3 - Procedimientos de Evaluación de la Conformidad.
Brasil (ANVISA):
Fabricante significa cualquier persona que diseña, fabrica, ensambla o procesa dispositivos
terminados, incluyendo aquellas que sólo realizan procesos de esterilización, etiquetado y
envasado [RDC ANVISA 16/2013: 1.2.9].
Para un fabricante nacional, confirmar que el establecimiento cuenta con la autorización de
ANVISA para la fabricación de dispositivos médicos (AFE - Autorización de Funcionamiento da
Empresa). Para los fabricantes nacionales e internacionales, verificar que los productos ya
distribuidos en el mercado brasileño estén registrados / notificados con ANVISA [Ley Federal
Brasileña nº 6360/76].
Según la legislación Brasileña, la certificación de Buenas Prácticas de Fabricación (GMP) es un
requisito previo para el registro de dispositivos médicos. Por lo tanto, la inspección del sitio de la
instalación precede a la solicitud de registro del dispositivo. Los dispositivos médicos sujetos a
notificación no necesitan el certificado GMP, pero aún no están certificados, sus fabricantes deben
cumplir con los requisitos GMP.
Registro / Notificación de Dispositivos Médicos:
La autorización de comercialización del equipo será solicitada a ANVISA por el fabricante nacional
o importador (representante legal) formalmente establecido en Brasil. El registro es un proceso
integral de autorización de mercado, aplicado a dispositivos médicos de las clases III y IV, [ANVISA
RDC nº 36/2015, RDC nº 40/2015].
La notificación es un proceso simplificado de autorización de mercado, aplicado a las clases de
dispositivos médicos I y II, [ANVISA RDC nº 36/2015, RDC nº 40/2015]. El registro es válido por 10
años, mientras que la notificación no tiene fecha de vencimiento. La renovación del registro se
solicitará en el tiempo definido en la Ley brasileña 6360/1976.
Licencia de establecimiento:
El fabricante nacional: estará autorizado por ANVISA, como mínimo, como fabricante de
dispositivos médicos. Esta licencia incluye autorización para almacenar y distribuir dispositivos
médicos.
Importador: el importador es considerado el representante legal del fabricante internacional en
Brasil y estará autorizado por ANVISA para importar, almacenar y distribuir dispositivos médicos.
En el caso de la subcontratación del almacenamiento, el importador no necesita autorización para
esta actividad.
Canadá (HC):
Fabricante se refiere a una persona que vende un dispositivo médico bajo su propio nombre, o bajo
una marca de fábrica o de comercio, diseño, nombre comercial u otro nombre o marca propiedad o
controlada por la persona y que es responsable de diseñar, fabricar, ensamblar, etiquetar,
empaquetar, renovar o modificar el dispositivo, o asignarle un propósito, ya sea que esas tareas
sean realizadas por esa persona o en su nombre [CMDR 1].
Ninguna persona podrá importar o vender un dispositivo médico de Clase II, III o IV a menos que el
fabricante del dispositivo tenga una licencia con respecto a ese dispositivo o, si el dispositivo
MDSAP AU P0002.005 36 Página
médico ha sido sometido a un cambio descrito en la sección 34, una licencia modificada del
dispositivo médico [CMDR 26].
El fabricante del dispositivo médico presentará al Ministerio una solicitud de licencia de un
dispositivo médico en un formato establecido por el Ministerio [CMDR 32].
Una solicitud de licencia de un dispositivo médico deberá incluir una copia de un certificado del
sistema de gestión de calidad que certifique que el sistema de gestión de calidad bajo el cual se
fabrica el producto médico (clase II) o diseñado y el fabricante (clase III o IV) cumplen con el
Estándar Nacional de Canadá CAN/CSA-ISO 13485: 2016. [CMDR 32(2)(f); 32(3)(j); 32 (4) (p)].
Japón (MHLW):
"Titular de la autorización de comercialización" significa una persona que reside en Japón y se le
concede una licencia de comercialización de un gobierno prefectural [PMD Ley 23-2.1].
Aplicación o notificación para la comercialización
Dispositivos médicos de clase 2, clase 3 y clase 4, excepto los especificados por el requisito del
PMD Ley 23-2-23.1.
El Titular de la Autorización de Comercialización deberá enviar una “Solicitud de Aprobación de
Comercialización” a PMDA para obtener la autorización para comercializar un dispositivo médico
en Japón. [PMD Act 23-2-5.1].
El Titular de la Autorización de Comercialización también deberá presentar una “Solicitud de
Auditoría QMS” a PMDA, cuando no tenga un Certificado QMS vigente para el dispositivo. [PMD
Act 23-2-5.6, 7].
Para Dispositivos Médicos de clase 2 y clase 3 que están especificados por el requisito de PMD
Act 23-2-23.1, el Titular de la Autorización de Comercialización deberá presentar una "Solicitud de
Certificación de Comercialización" a un Organismo de Certificación Registrado (RCB) para obtener
la autorización para comercializar un dispositivo médico en Japón. [PMD Act 23-2-23.1].
Una "Solicitud de Auditoría del SGC" también será presentada a un RCB por la persona, cuando la
persona no cuente con un certificado válido del SGC para el dispositivo. [PMD Ley 23-2-23.3, 4].
Dispositivo Médico de Clase 1.
El titular de la autorización de comercialización presentará ante PMDA una "notificación de
comercialización" para la clase 1 en Japón [PMD Ley 23-2-12].
Un dispositivo médico de clase 1 no necesita ningún certificado del SGC para su comercialización.
Registro de Instalación (Sitio de Fabricación Registrado)
Un sitio de fabricación de dispositivos médicos que lleva a cabo uno de los procedimientos de
fabricación designados, a continuación, enumerados, deberán registrarse:
a) Diseño principal,
b) Ensamble principal,
c) Esterilización, y
d) Almacenamiento interno antes de la liberación final.
El sitio se denomina "Sitio de Fabricación Registrado". Tiene que presentar una solicitud a PMDA
para su registro por sí mismo [Ley PMD 23-2-3.1, 23-2-4].
MDSAP AU P0002.005 37 Página
Estados Unidos (FDA):
21 CFR 807 – Registro de Establecimiento y Clasificación de Dispositivos para Fabricantes e
Importadores Iniciales de Dispositivos.
Establecimiento significa un lugar de negocios bajo una dirección en una ubicación física general
en la que un dispositivo es fabricado, ensamblado o procesado de otra manera.
Propietario u operador significa la corporación, subsidiaria, compañía afiliada, sociedad o
propietario directamente responsable de las actividades del establecimiento registrado.
El propietario u operador debe registrar el establecimiento y enviar información de listada a la
Administración de Drogas y Alimentos (FDA, por sus siglas en inglés) para aquellos dispositivos en
distribución comercial, independientemente de la clasificación.
Los requisitos de registro y catálogo deben pertenecer a cualquier persona que:
Inicia o desarrolla especificaciones para un dispositivo que va a ser fabricado por una
segunda persona para su distribución comercial por la persona que inicia las
especificaciones;
Fabrica para la distribución comercial un dispositivo para sí mismo o para otra persona;
independientemente de si el fabricante coloca el dispositivo en una distribución comercial o
devuelve el dispositivo al cliente;
Re-empaca o re-etiqueta un dispositivo;
Actúa como importador inicial, excepto los importadores iniciales que pueden cumplir su
obligación de catalogar para cualquier dispositivo para el cual no iniciaron o desarrollaron
las especificaciones para el dispositivo o re-embalar o re-etiquetar el dispositivo
presentando el nombre y la dirección del fabricante.
Fabrica componentes o accesorios que están listos para ser utilizados para cualquier
propósito relacionado con la salud y están envasados o etiquetados para su distribución
comercial para tal fin;
Esteriliza o hace de otro modo un dispositivo para o en nombre de un desarrollador de
especificaciones o cualquier otra persona;
Actúa como establecimiento de un expediente de quejas; o
Es un establecimiento de dispositivos situado en una zona de comercio exterior
Enlaces
Gestión
Durante la auditoría del proceso de Gestión, confirme que la Alta Dirección conoce y ha hecho los
arreglos para la autorización de comercialización del dispositivo y el registro de la instalación.
Tarea 2 – Evidencia de Autorización o Aprobación de Comercialización
Confirmar que la organización ha recibido autorización o autorización de comercialización
adecuada en las jurisdicciones regulatorias donde la organización comercializa sus
dispositivos.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.1.1, 4.2.1, 5.2, 7.2.1, 7.2.3
MDSAP AU P0002.005 38 Página
Requisitos específicos del país:
Australia (TGA):
La autorización de comercialización (inclusión en el Registro Australiano de Productos
Terapéuticos [ARTG]) se otorga al Patrocinador Australiano. El Patrocinador no puede solicitar la
autorización de comercialización hasta que el Fabricante haya completado un procedimiento de
evaluación de la conformidad que sea relevante para la Clase del dispositivo. Los fabricantes no
australianos deberán ayudar al Patrocinador a través del suministro de información para respaldar
una solicitud de autorización de comercialización y para cumplir con las condiciones relevantes
para el suministro continuo. Un Patrocinador recibe un Certificado de Inclusión en ARTG para
identificar los productos a los que se les ha otorgado la autorización de comercialización. Los
productos con autorización de comercialización pueden identificarse a partir de la base de datos
ARTG de cara al público.
Normalmente, un Patrocinador no tiene permitido importar, suministrar, exportar o fabricar (en
Australia) un dispositivo médico a menos que; el dispositivo cumple con los principios esenciales, el
fabricante ha aplicado un procedimiento de evaluación de conformidad relevante y el patrocinador
ha incluido el dispositivo en el ARTG. Una exención para permitir la importación y el suministro
puede ser aprobada y otorgada al Patrocinador por la TGA, en los casos en que la TGA esté
convencida de que el dispositivo se utilizará bajo un esquema de ensayo clínico o el acceso
especial o esquemas de prescriptores autorizados. Una aprobación de exención puede contener
condiciones en relación con la fabricación del producto. El fabricante debe verificar con el
patrocinador australiano si se han aplicado tales condiciones a la aprobación de la exención.
Un fabricante debe mantener una lista de sus patrocinadores australianos y los productos que esos
patrocinadores han incluido en el registro australiano de productos terapéuticos.
Los procedimientos de un fabricante deben garantizar que el producto no se libere para su
suministro al mercado australiano a menos que el patrocinador haya recibido un "Certificado de
inclusión en el Registro Australiano de Productos Terapéuticos", que identifique cada tipo de
dispositivo médico que ha sido aprobado para su suministro. al mercado australiano [TG Act
s41FJ], o el Patrocinador tiene una exención relevante (TG Act Part 4-7).
Como parte de una solicitud de autorización de comercialización, un Patrocinador se compromete a
cumplir con ciertos requisitos que se identifican en s41FD - “Materias a certificar”. Estos asuntos
incluyen el establecimiento de un acuerdo escrito con el fabricante sobre el suministro de
información y el establecimiento de canales de comunicación efectivos para las actividades
posteriores a la comercialización. Ver el Anexo 4 para obtener más orientación.
Brasil (ANVISA):
En Brasil existen dos tipos de autorización comercial, registro y notificación:
La autorización de mercado del dispositivo será solicitada a ANVISA por el
fabricante o importador nacional (representante legal) formalmente establecido en
Brasil. El registro es un proceso integral para la autorización de comercialización,
MDSAP AU P0002.005 39 Página
que se aplica a los dispositivos médicos de las clases III y IV. [ANVISA RDC nº
36/2015, RDC nº 40/2015].
La notificación es un proceso de autorización de comercialización simplificado, que
se aplica a todos los productos sanitarios de las clases I y II. [ANVISA RDC nº
36/2015, RDC nº 40/2015] El registro es válido por 10 años, mientras que las
notificaciones no tienen fecha de vencimiento - la renovación del registro se
solicitará en el tiempo definido en la Ley Brasileña 6360/1976.
Canadá (HC):
Ninguna persona importará ni venderá un Dispositivo Médico de Clase II, III o IV a menos que el
fabricante del dispositivo posea una licencia con respecto a ese dispositivo o, si el dispositivo
médico ha sido sometido a un cambio descrito en la sección 34, una licencia de Dispositivo Médico
modificado [CMDR 26].
Japón (MHLW):
Cualquier persona que tenga la intención de comercializar un producto médico de rehabilitación,
deberá tener una licencia de comercialización otorgada por el gobierno de la prefectura. Esta
persona se llama "Titular de la Autorización de Comercialización" (MAH, por sus siglas en inglés) y
debe residir en Japón [PMD Ley 23-2.1]. La persona tiene que presentar una Solicitud de
aprobación / certificación de comercialización (dispositivos médicos de clase 2, 3 o 4) o una
Notificación de comercialización (dispositivo médico de clase 1) para obtener autorización de
comercialización para el dispositivo médico. Ninguna persona comercializará un dispositivo médico
en Japón, a menos que el titular de la autorización de comercialización del dispositivo haya
obtenido la autorización de comercialización [Ley PMD 23-2-5.1, 23-2-23.1, 23-2-12].
Estados Unidos (FDA):
21 CFR 807.81-Notificación previa al mercado:
Cada persona que debe registrar su establecimiento de conformidad con 807.20 debe presentar
una notificación previa a la comercialización a la Administración de Alimentos y Medicamentos al
menos 90 días antes de proponer comenzar la introducción o entrega para su introducción en el
comercio interestatal para la distribución comercial de un dispositivo destinado a uso humano que
cumple con alguno de los siguientes criterios:
1) El dispositivo se está introduciendo en la distribución comercial por primera vez; es decir, el
dispositivo no es del mismo tipo que, o no es sustancialmente equivalente a, (i) un
dispositivo en distribución comercial antes del 28 de mayo de 1976, o (ii) un dispositivo
introducido para distribución comercial después del 28 de mayo de 1976, que
posteriormente ha sido reclasificado en clase I o II.
2) El dispositivo se está introduciendo en la distribución comercial por primera vez por una
persona que requiere el registro.
21 CFR 814 - Aprobación previa al mercado
MDSAP AU P0002.005 40 Página
Se requiere una aprobación previa a la comercialización para cualquier dispositivo clase III de la
FDA que no estaba en el mercado (introducido o entregado para su introducción en el comercio
para distribución comercial) antes del 28 de mayo de 1976, y no es sustancialmente equivalente a
un dispositivo en el mercado antes del 28 de mayo. 1976, o a un dispositivo comercializado por
primera vez en, o después de esa fecha, que ha sido clasificado en clase I o clase II.
Enlaces
Gestión; Diseño y Desarrollo
Durante la auditoría del proceso de Gestión del Diseño y Desarrollo, asegurar de que la Alta
Dirección conozca los requisitos para la autorización de comercialización del dispositivo y el
registro de la instalación, y que estos se tengan en cuenta al diseñar el dispositivo.
Confirmar que la Alta Dirección obtenga la autorización de comercialización en las jurisdicciones
correspondientes antes de la distribución comercial del dispositivo.
Tarea 3 – Notificación de Cambios a Dispositivos Comercializados o al SGC
Verificar que la organización del Dispositivo Médico haya identificado los cambios en los
dispositivos comercializados o el Sistema de Gestión de Calidad que requieren notificación
a las autoridades regulatorias.
El equipo de auditoría debe prestar especial atención a las situaciones observadas en la
auditoría del proceso de Diseño y Desarrollo (específicamente cambios de diseño) que
pueden requerir notificación a las jurisdicciones en las que se comercializan los
dispositivos modificados.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.1.1, 4.2.1, 5.2, 7.2.1, 7.2.3, 7.3.9
Requisitos específicos del país:
Australia (TGA):
El fabricante debe notificar a su organismo auditor sobre:
Un cambio propuesto en su SGC, incluido el nombre de la ubicación del fabricante.
Un cambio propuesto para los proveedores críticos o los bienes y servicios que brindan.
Un cambio propuesto a un proceso de fabricación validado.
Un cambio propuesto en los tipos de dispositivos médicos a los que se aplicará el sistema.
Para la Clase III o AIMD, un cambio propuesto en el diseño, rendimiento previsto, usuario
previsto, embalaje, condiciones de almacenamiento o transporte de un dispositivo.
Los cambios deben ser evaluados por la Organización Auditora para determinar si se requiere una
auditoría especial para verificar la integridad continua del sistema de gestión de la calidad, o si la
verificación del cambio puede ocurrir en la próxima auditoría de rutina. La organización auditora
MDSAP AU P0002.005 41 Página
también debe verificar la adecuación continua de la documentación técnica como resultado del
cambio (ver Anexo 1).
Si el fabricante es titular de un certificado de evaluación de la conformidad de TGA, también se
requiere que el fabricante notifique a la TGA de estos cambios, antes de la implementación. En el
caso de cambios que el fabricante o el solicitante no considere sustanciales, deben notificarse a la
TGA en el momento de la recertificación de un certificado de evaluación de la conformidad
existente, incluido dentro del alcance de otra solicitud de evaluación de la conformidad o puesto a
disposición del auditor durante la próxima auditoría in situ; lo que ocurra antes.
Ejemplos de cambios sustanciales que pueden requerir notificación a la TGA incluyen, entre otros,
los siguientes:
Nombre y / o dirección del Fabricante.
Alcance de las instalaciones de fabricación existentes, incluidas las etapas de fabricación.
Adición o eliminación de una instalación de fabricación junto con actividades asociadas.
Proceso de fabricación crítico (por ejemplo, un proceso de recubrimiento de medicamentos,
un método de esterilización, etc.).
Proveedor crítico y / o alcance relevante.
Tipo de procedimiento de evaluación de la conformidad.
Categoría de dispositivo.
Diseño de productos (por ejemplo, materiales para dispositivos médicos, almacenamiento,
vida útil y empaque).
Información que se debe proporcionar con un dispositivo médico (por ejemplo, el propósito
previsto del dispositivo en los Instructivos de Uso, eliminación de advertencias,
contraindicaciones u otra información relacionada con la seguridad, etc.).
Referir a:
Reglamento de 2002 sobre productos terapéuticos (dispositivos médicos)
Regulación 3.5 - Dispositivos médicos fabricados fuera de Australia.
Anexo 3 - El procedimiento de evaluación de la conformidad relevante elegido por el
fabricante.
Nota: Una entrada en el Registro Australiano de Productos Terapéuticos (inclusión) a nombre del
Patrocinador Australiano está en vigor hasta que se cancele.
Brasil (ANVISA):
Los cambios que involucren dispositivos médicos ya aprobados por ANVISA, se someterán a una
nueva aprobación [Ley brasileña nº 6360/76 -Art. 13]. Los cambios / modificaciones que se deben
presentar son aquellos clasificados como cambios significativos, que afectan:
las características de seguridad y efectividad, incluidas las medidas para comunicar
información (por ejemplo, riesgo residual).
identificación del dispositivo o su fabricante o sitio de fabricación.
indicación de uso, incluido su objetivo, tipo de paciente (adulto, pediátrico, recién nacido) o
entorno que se utilizará (doméstico, hospitalario, ambulancia, etc.).
clasificación del dispositivo.
especificaciones técnicas del dispositivo, incluida la composición y otras características
operativas / técnicas / físicas.
método de fabricación.
Los ejemplos de modificaciones que pueden requerir una nueva presentación (lista enunciativa
mas no limitativa) incluyen, entre otros, los siguientes:
MDSAP AU P0002.005 42 Página
Método de esterilización;
Material estructural / composición;
Fabricante nuevo o adicional;
Método de fabricación;
Sitio de fabricación;
Parámetros de funcionamiento o condiciones de uso;
Características de seguridad del paciente o del usuario;
Material de embalaje de barrera estéril;
Reclamaciones de estabilidad o caducidad;
Diseño;
Etiquetas e instrucciones de uso (si la modificación es con respecto a la información);
Nombre comercial;
Indicación de uso;
Nueva versión de software;
Presentación comercial;
Inclusión de un nuevo dispositivo en una familia de dispositivos médicos ya aprobados;
Inclusión de nuevos accesorios.
Canadá (HC):
Si el fabricante propone realizar uno o más cambios, el fabricante presentará al Ministerio, en
un formato establecido por el mismo, una solicitud de modificación de licencia de dispositivo
médico que incluya la información y los documentos establecidos en la sección 32 que son
relevantes para el cambio [CMDR 34].
Todo fabricante de un dispositivo médico autorizado deberá, anualmente antes del 1 de
noviembre y en una forma autorizada por el Ministerio, proporcionar al mismo una declaración
firmada por el fabricante o por una persona autorizada para firmar en nombre del fabricante
describiendo cualquier cambio en la información y documentos suministrados por el fabricante
con respecto al dispositivo, distintos de los que se presentan en la sección 34 o 43.1 [CMDR
43].
Si el titular de una licencia de dispositivo médico interrumpe la venta del dispositivo médico en
Canadá, el licenciatario deberá informar al Ministerio dentro de los 30 días posteriores a la
interrupción, y la licencia se cancelará en el momento en que se informe al Ministerio [CMDR
43 (3))].
Sujeto a la sección 34, si se emite un certificado de Sistema de Gestión de Calidad nuevo o
modificado con respecto a un dispositivo médico con licencia, el fabricante del dispositivo
deberá presentar una copia del certificado al Ministerio dentro de los 30 días posteriores a su
expedición [CMDR 43.1].
Japón (MHLW):
Un cambio a un dispositivo médico aprobado / certificado por PMDA / un organismo de
certificación registrado puede requerir que el titular de la autorización de comercialización
presente una nueva solicitud, una solicitud de cambio o una notificación de cambio [PMD Ley
23-2-5.1, 23-2-5.11, 23-2-5.17, 23-2-23.1, 23-2-23.6, 23-2-23.7].
MDSAP AU P0002.005 43 Página
Los cambios que requieren la aplicación o la notificación son aquellos que afectan directamente
la seguridad y efectividad del dispositivo y / o la identidad sustancial del hecho aprobado
durante la aprobación / certificación de comercialización.
El sitio de fabricación registrado se comunicará con el titular de la autorización de
comercialización sobre el cambio cuando el sitio de fabricación registrado planifique dichos
cambios, de modo que el titular de la autorización de comercialización pueda tomar las
medidas reglamentarias necesarias mencionadas anteriormente [MHLW MO169; 29].
Los ejemplos de cambios que pueden requerir una aplicación o una notificación incluyen, pero
no se limitan, entre otros, los siguientes:
Diseño;
Composición;
Materia prima;
Método de esterilización;
Método de fabricación;
Sitio de fabricación;
Características de seguridad del paciente o del usuario;
Parámetros de funcionamiento o condiciones de uso;
Indicación de uso;
Tiempo de Vida;
Especificación de rendimiento;
Estados Unidos (FDA):
21 CFR 807 – Establecimiento del registro y listado de dispositivos para fabricantes e
importadores iniciales de dispositivos:
Actualizar la información de la lista de dispositivos durante cada junio y diciembre o, a su
discreción, en el momento en que se produzca el cambio. Las condiciones que requieren
actualización e información para enviar para cada una de estas actualizaciones son las
siguientes:
Si un propietario u operador introduce en la distribución comercial un dispositivo
identificado con un nombre de clasificación que no figura actualmente en la lista del
propietario u operador.
Si un propietario u operador interrumpe la distribución comercial de todos los
dispositivos en la misma clase de dispositivo
Actualizar el registro si hay cambios en la propiedad individual, estructura corporativa o de
sociedad, o ubicación en el momento del registro anual, o por carta si los cambios ocurren en
otro momento. Esta información debe enviarse dentro de los 30 días de dichos cambios. Los
cambios en los nombres de los funcionarios y / o directores de la (s) corporación (es) deben
presentarse ante el corresponsal oficial del establecimiento y deben ser entregados a la
Administración de Alimentos y Medicamentos al recibir una solicitud por escrito de esta
información.
MDSAP AU P0002.005 44 Página
21 CFR 807.81 – Notificación previa al mercado:
Se requiere una nueva aplicación completa 510 (k) para cambios o modificaciones a un
dispositivo existente, donde las modificaciones podrían afectar significativamente la seguridad
o efectividad del dispositivo, o el dispositivo se comercializará para una indicación nueva o
diferente. Todos los cambios en las indicaciones de uso requieren la presentación de un 510
(k).
Los ejemplos de modificaciones que pueden requerir una presentación 510 (k) incluyen, mas
no se limitan, entre otros, los siguientes:
Método de esterilización
Material estructural
Método de fabricación
Parámetros de funcionamiento o condiciones de uso
Características de seguridad del paciente o del usuario
Material de embalaje de barrera estéril
Reclamaciones de estabilidad o caducidad
Diseño
21 CFR 814.39 - Suplementos de PMA
Después de que la FDA aprueba un PMA, el solicitante debe presentar un suplemento de PMA
para su revisión y aprobación por la FDA antes de realizar un cambio que afecte la seguridad o
eficacia del dispositivo para el cual el solicitante tiene un PMA aprobado. Mientras que la carga
para determinar si se requiere un suplemento es principalmente del titular de PMA, los cambios por
los cuales un solicitante debe presentar un suplemento de PMA incluyen, pero no se limitan a, los
siguientes tipos de cambios si afectan la seguridad o efectividad del dispositivo:
Nuevas indicaciones para el uso del dispositivo.
Cambios de etiquetado.
El uso de una instalación o establecimiento diferente para fabricar, procesar o empacar el
dispositivo.
Cambios en los procedimientos de esterilización.
Cambios en el empaque.
Cambios en el rendimiento o especificaciones de diseño, circuitos, componentes,
ingredientes, principio de funcionamiento o diseño físico del dispositivo.
Extensión de la fecha de vencimiento del dispositivo en base a los datos obtenidos con un
protocolo de prueba de estabilidad o esterilidad nuevo o revisado que no ha sido aprobado
por la FDA.
Un solicitante puede realizar un cambio en un dispositivo después de que la FDA apruebe
un PMA para el dispositivo sin presentar un suplemento de PMA si el cambio no afecta la
seguridad o eficacia del dispositivo y el cambio se informa a la FDA en informes periódicos
posteriores a la aprobación requeridos como condición a la aprobación del dispositivo, por
ejemplo, un cambio editorial en el etiquetado que no afecte la seguridad o efectividad del
dispositivo.
MDSAP AU P0002.005 45 Página
Enlaces
Diseño y Desarrollo
Durante la auditoria del proceso de Diseño y Desarrollo, el equipo de auditoría debe confirmar que
la organización ha considerado los requisitos reglamentarios para la autorización de
comercialización del dispositivo y el registro de la instalación; y ha cumplido con estos requisitos
antes de comercializar el dispositivo cambiado en las jurisdicciones regulatorias aplicables.
Capítulo 3: Medición, Análisis y Mejora
Una de las actividades más importantes del sistema de gestión de la calidad es la identificación de
las causas existentes y potenciales de los problemas de calidad y del producto. Dichas causas
deben identificarse para que se puedan llevar a cabo acciones correctivas o preventivas
adecuadas y efectivas. Estas actividades se llevan a cabo bajo el proceso de Medición, Análisis y
Mejora.
El propósito del proceso de Medición, Análisis y Mejora de una organización de dispositivos
médicos es recopilar y analizar información, identificar e investigar las causas existentes y
potenciales de los problemas del producto y la calidad, y tomar acciones correctivas o preventivas
apropiadas y efectivas para prevenir la recurrencia o ocurrencia. Es esencial que una organización
de dispositivos médicos verifique o valide estas acciones, comunique las actividades de acciones
correctivas y preventivas a las personas responsables, proporcione información relevante para la
revisión de la gerencia y documente estas actividades. Estas actividades ayudarán a la
organización de dispositivos médicos a lidiar de manera efectiva con los problemas de calidad y
productos existentes o potenciales, prevenir su recurrencia y / u ocurrencia, y prevenir o minimizar
fallas de dispositivos u otros problemas de calidad.
El Representante de la Dirección es responsable de garantizar que los requisitos del sistema de
gestión de la calidad se hayan definido, documentado, implementado y mantenido de manera
eficaz. Antes de la auditoría de un proceso, puede ser útil entrevistar al representante de la
dirección (o su designado) para obtener una descripción general del proceso y una idea del
conocimiento y la comprensión de la dirección del proceso.
El proceso de Medición, Análisis y Mejora es el segundo proceso principal que se audita según la
secuencia de auditoría del MDSAP. Cuando corresponda, la información sobre las no
conformidades del dispositivo o del sistema de gestión de la calidad identificadas observadas
durante la auditoría del proceso de Medición, Análisis y Mejora debe usarse para tomar decisiones
MDSAP AU P0002.005 46 Página
en cuanto al diseño de proyectos o cambios de diseño para evaluar durante la auditoría del
proceso de Diseño y Desarrollo, proveedores a evaluar durante la auditoría del proceso de
Compras, y los procesos para revisar durante la auditoría del proceso de Controles de Producción
y Servicio.
Auditando el Proceso de Medición, Análisis y Mejora
Propósito: El objetivo de auditar el proceso de Medición, Análisis y Mejora es verificar que los
procesos del fabricante aseguren que la información relacionada con los productos, procesos o el
sistema de gestión de calidad sea recolectada y analizada para identificar no conformidades reales
o potenciales relativas a un producto, proceso o sistema de calidad real, que los problemas y
problemas potenciales son investigados, y que se toman medidas correctivas y acciones
preventivas apropiadas y efectivas.
Resultados: como resultado de la auditoría del proceso de Medición, Análisis y Mejora, la
evidencia objetiva mostrará si la organización del Dispositivo Médico ha:
A) Definido, documentado e implementado procedimientos para la medición, análisis y mejora
que abordan los requisitos del estándar del sistema de gestión de la calidad y la
participación de las Autoridades regulatorias de MDSAP.
B) Identificado, analizado y monitoreado fuentes apropiadas de datos de calidad para
identificar no conformidades o posibles no conformidades y determinado la necesidad de
una acción correctiva o preventiva.
C) Asegurado investigaciones que se llevan a cabo para identificar la (s) causa (s) subyacente
(s) de no conformidades y posibles no conformidades, cuando sea posible.
D) Implementado la acción correctiva apropiada para eliminar la recurrencia o acción
preventiva para prevenir la ocurrencia de no conformidades del producto o del sistema de
calidad, proporcional a los riesgos asociados con las no conformidades o posibles no
conformidades encontradas
E) Revisado la efectividad de la acción correctiva y la acción preventiva.
F) Utilizado información del análisis de producción y datos de calidad de postproducción para
mejorar el análisis del riesgo del producto, según corresponda.
Enlaces
Diseño y Desarrollo; Controles de Producción y Servicio; Compras; Eventos Adversos de
Dispositivos Médicos y Reporte de Notificaciones de Advertencia; Gestión
Tarea 1 – Procedimientos para la Medición, Análisis y Mejora de la
Efectividad del SGC y Conformidad del Producto
MDSAP AU P0002.005 47 Página
Verificar que se hayan establecido y documentado los procedimientos de medición, análisis
y mejora que abordan los requisitos del estándar del sistema de gestión de la calidad y de
las autoridades regulatorias.
Confirmar que la organización del Dispositivo Médico mantiene e implementa
procedimientos para monitorear y medir la conformidad del producto durante la realización
del producto, así como procedimientos que proporcionan mecanismos de retroalimentación
para proporcionar advertencias tempranas de problemas de calidad y la implementación de
acciones correctivas y acciones preventivas.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 8.1, 8.2.1, 8.2.6, 8.5;
TGA: TG(MD)R Sch3 P1 1.4(3)(a), (b), (5)(b)(iii), (f);
ANVISA: RDC ANVISA 16/2013: 5.3.1, 7.1, 7.2;
MHLW/PMDA: MHLW MO169: 6, 54, 55, 58, 62, 63, 64;
FDA: 21 CFR 820.100(a)
Requisitos adicionales específicos del país:
Brasil (ANVISA):
Verificar que el fabricante se haya asegurado de que la información sobre problemas de calidad o
productos no conformes se disemine adecuadamente a quienes están directamente involucrados
en el mantenimiento de la calidad del producto y para prevenir la ocurrencia de dichos problemas
[RDC ANVISA 16/2013: 7.1.1.6].
Estados Unidos (FDA):
Los procedimientos de verificación aseguran que la información relacionada con problemas de
calidad o productos no conformes se disemine a aquellos directamente responsables de garantizar
la calidad de dicho producto o la prevención de problemas [21 CFR 820.100 (a) (6)].
Confirmar que los procedimientos proveen la presentación de información relevante sobre los
problemas de calidad identificados, así como las acciones correctivas y preventivas, para la
revisión de la dirección [21 CFR 820.100 (a) (7)].
Evaluación de la conformidad:
Procedimientos
Cada organización debe establecer y mantener procedimientos para analizar datos e implementar
acción correctiva y acción preventiva. Los procedimientos deben incluir requisitos para:
Análisis de retroalimentación, conformidad con los requisitos del producto, características y
tendencias de procesos y productos (incluidas las oportunidades para la acción
preventiva), y la conformidad de proveedores.
Revisar las no conformidades, incluidas las quejas de los clientes.
Evaluar la necesidad de acción para prevenir la recurrencia o la ocurrencia de no
conformidades.
Registrar los resultados de cualquier investigación y de las medidas adoptadas.
Identificar la (s) acción (es) necesaria (s) para corregir y prevenir la recurrencia o la
ocurrencia de producto no conforme y otros problemas de calidad.
MDSAP AU P0002.005 48 Página
Asegurar de que la acción sea efectiva y no afecte negativamente al dispositivo terminado.
Implementar y registrar cambios en los métodos y procedimientos necesarios para corregir
y prevenir problemas de calidad identificados.
Asegurar que la información relacionada con problemas de calidad o productos no
conformes se disemine a aquellos directamente responsables de asegurar la calidad de
dicho producto o la prevención de tales problemas.
Tarea 2 – Fuentes de Datos de Calidad
Determinar si se han identificado y analizado fuentes apropiadas de datos de calidad de
acuerdo con un procedimiento documentado para usar el uso de métodos estadísticos
válidos (cuando corresponda) para la entrada en el proceso de medición, análisis y mejora,
incluidas quejas de los clientes, comentarios, registros de servicio, devueltos productos,
hallazgos de auditorías internas y externas, no conformidades de auditorías e inspecciones
regulatorias, y datos del monitoreo de productos, procesos, productos no conformes y
proveedores.
La información del análisis de los datos de calidad de la organización debe usarse para
informar la decisión del equipo de auditoría en cuanto a los registros de quejas específicos
para revisar en la Tarea 12, y los productos y procesos para auditar durante los procesos de
Diseño y Desarrollo, Controles de Producción y Servicio y Compras.
Cláusula y Regulación:
ISO: ISO 13485:2016: 7.5.4, 8.1, 8.2.1, 8.2.6, 8.4;
TGA: TG(MD)R Sch3 P1 1.4(3)(a), (b), (5)(b)(iii), (f);
ANVISA: RDC ANVISA 16/2013: 7.1.1.1, 9.1;
MHLW/PMDA: MHLW MO169: 43, 54, 55, 58, 61;
FDA: 21 CFR 820.100(a)
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Fuentes de datos de calidad
Quejas, registros de actividades de aceptación y concesiones, no conformidades identificadas en
auditorías internas, registros de servicios, aceptabilidad del producto suministrado y desempeño
del proveedor, y datos presentados en la revisión de la administración son fuentes de datos de
calidad comunes que son útiles para identificar problemas de calidad, entre otros.
Algunas fuentes de datos de calidad que pueden ser útiles para identificar problemas potenciales
son las actividades de aceptación, como las pruebas de componentes, en proceso o de
dispositivos terminados; monitoreo ambiental y control estadístico de procesos (CEP). Los
resultados de las actividades de aceptación pueden indicar una tendencia desfavorable que puede
dejar desatendida y provocar la no conformidad del producto.
Durante la auditoría del proceso de Medición, Análisis y Mejora, se recomienda que el (los) auditor
(es) revise (n) el informe de auditoría anterior si existe uno para la organización. Si esta
información está disponible, el equipo de auditoría debe usar la información en el informe al
seleccionar algunas fuentes de datos de calidad para revisar durante la auditoría. Por ejemplo, si
los registros del servicio fueron revisados durante la auditoría anterior y la organización manejó los
datos de manera apropiada, el equipo de auditoría puede desear seleccionar una fuente de datos
diferente para su revisión durante la auditoría. Sin embargo, si el documento de auditoría anterior.
MDSAP AU P0002.005 49 Página
Sin embargo, si la auditoría anterior documentó que los datos de los registros del servicio no se
ingresaron adecuadamente en el proceso de Medición, Análisis y Mejora, el equipo de auditoría
debería considerar revisar nuevamente los registros del servicio para determinar si la deficiencia
previa fue efectivamente abordada:
Seleccionar algunas fuentes de datos de calidad.
Determinar si los datos de estas fuentes se ingresaron en el proceso de Medición, Análisis
y Mejora de la organización para su análisis y si la información fue completa, precisa e
ingresada de manera oportuna.
Tener en cuenta los problemas de calidad que aparecen en más de una fuente de datos.
Por ejemplo, las no conformidades del dispositivo observadas en las reclamaciones deben
compararse con las no conformidades similares observadas durante el análisis de la
organización de los datos de otras fuentes de datos, como informes de rechazo de
productos o informes de productos o procesos no conformes.
Esta comparación ayudará a la organización del Dispositivo Médico y al equipo de auditoría a
comprender el alcance completo del problema de calidad.
Análisis de datos
Una organización del Dispositivo Médico debe usar datos de una variedad de fuentes de datos de
calidad para identificar las causas de los productos existentes y los problemas de calidad. No todas
las organizaciones tendrán las mismas fuentes de datos de calidad. Por ejemplo, los registros de
servicio y los informes de instalación son fuentes de datos de calidad que pueden no encontrarse
en todas las organizaciones de Dispositivos Médicos.
A medida que el equipo de auditoría realiza la auditoría, determine qué fuentes de datos de calidad
ha identificado la organización del Dispositivo Médico. El equipo de auditoría también determinará
si las fuentes identificadas por la organización del Dispositivo Médico son apropiadas y si la
organización del Dispositivo Médico está analizando datos de calidad de estas fuentes para
identificar problemas existentes del producto, así como problemas existentes dentro de su sistema
de calidad.
Más adelante en la evaluación del proceso de Medición, Análisis y Mejora, el equipo de auditoría
tomará muestras de datos de calidad en bruto para determinar cómo la organización del Dispositivo
Médico analizó los datos de calidad y respondió a los resultados de su análisis.
Una organización de Dispositivo Médico también debe usar datos de una variedad de fuentes de
datos de calidad para identificar las causas de posibles problemas de productos y calidad. La
organización debe buscar tendencias u otras indicaciones de problemas potenciales antes de que
los problemas realmente ocurran. La organización puede optar por realizar análisis de dispositivos
de la competencia, incluida la revisión de avisos de asesoramiento relacionados con dispositivos
de la competencia, para determinar si podrían ocurrir no conformidades similares en los
dispositivos de la organización de Dispositivo Médico.
Determinar si la organización de Dispositivo Médico puede identificar problemas potenciales de
productos y calidad que pueden requerir una acción preventiva.
Una organización de Dispositivos Médicos tiene la flexibilidad de utilizar cualquier método de
análisis que sea apropiado para identificar las causas existentes y potenciales de productos no
conformes u otros problemas de calidad. Sin embargo, una organización debe usar una
metodología estadística apropiada cuando sea necesario para detectar problemas recurrentes de
calidad.
MDSAP AU P0002.005 50 Página
Una organización de Dispositivo Médico también debe usar herramientas estadísticas apropiadas
cuando sea necesario utilizar una metodología estadística. No debe hacer un mal uso de las
estadísticas para minimizar el problema o evitar abordar el problema.
Enlaces
Compras
Durante la auditoría del proceso de Medición, Análisis y Mejora, el equipo de auditoría puede
encontrar datos que involucran no conformidades del producto, incluidas las quejas que involucran
dispositivos terminados, donde la causa subyacente del problema de calidad se remonta a un
producto suministrado.
Durante la auditoría del proceso de Compras, el equipo de auditoría debe considerar seleccionar
proveedores para auditar que tengan indicadores de acciones correctivas de no conformidades con
los componentes o procesos suministrados.
Tarea 3 – Investigación de No Conformidad
Determinar si las investigaciones se llevan a cabo para identificar la (s) causa (s)
subyacente (s) de las no conformidades detectadas, cuando sea posible.
Confirmar que las investigaciones son proporcionales al riesgo de la no conformidad.
Cláusula y Regulación:
ISO: ISO 13485:2016: 8.5.2;
TGA: TG(MD)R Sch3 P1 1.4(3)(a), (b), (5)(b)(iii), (f), TG(MD)R Sch1 P1 2;
ANVISA: RDC ANVISA 16/2013: 2.4, 6.5.1, 7.1.1.2;
MHLW/PMDA: MHLW MO169: 63;
FDA: 21 CFR 820.100 (a)(2)
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Investigaciones de No Conformidades
Las organizaciones deben definir e implementar un proceso para las investigaciones. El proceso
debe consistir en un enfoque estructurado y basado en el riesgo (en un Sistema de Calidad
maduro) destinado a determinar la causa raíz o subyacente de un problema de calidad. Los
criterios deben definirse para determinar cuándo es necesaria una investigación y el alcance de la
investigación. La investigación debe basarse en un plan pre-aprobado u otro enfoque definido, se
deben definir cronogramas, se deben asignar roles y responsabilidades, y el curso de acción debe
evaluarse cuando no se puede determinar la causa subyacente. Los resultados de la investigación
deben registrarse. La profundidad de la investigación de la organización de un proceso, producto u
otra no conformidad del sistema de calidad debe ser acorde con la importancia y el riesgo de la no
conformidad. El proceso para determinar el alcance de una investigación puede estar relacionado
con el sistema de gestión de riesgos de la organización de Dispositivos Médicos y los resultados de
diseño esenciales para el correcto funcionamiento del dispositivo.
Una corrección no es lo mismo que una acción correctiva.
MDSAP AU P0002.005 51 Página
Para que una organización de Dispositivos Médicos tome una acción correctiva (es decir, medidas
tomadas para evitar la recurrencia de una no conformidad existente), se debe realizar una
investigación para determinar la causa de la no conformidad. A menudo, una organización de
Dispositivos Médicos solo realizará una corrección para manejar el problema inmediato (por
ejemplo, re-etiquetar una gran cantidad de dispositivos terminados mal etiquetados). Determinar la
causa del lote de dispositivos terminados mal etiquetados es más difícil y puede pasarse por alto.
Siempre que sea posible, la organización de Dispositivos Médicos debe identificar la causa
subyacente o las causas de la no conformidad para que se puedan tomar las medidas correctivas
apropiadas.
Seleccionar registros
Al seleccionar registros de investigaciones para revisar, tener en cuenta el riesgo de la no
conformidad con el producto o proceso. Seleccionar los registros de las investigaciones donde la
no conformidad tiene un mayor riesgo de afectar negativamente la capacidad del dispositivo
terminado para cumplir con sus productos de diseño esenciales o la no conformidad afecta la
seguridad y eficacia del producto.
Enlaces
Ninguno
Tarea 4 – Investigación de No Conformidad Potencial
Determinar si las investigaciones se llevan a cabo para identificar la (s) causa (s)
subyacente (s) de no conformidades potenciales, cuando sea posible.
Confirmar que las investigaciones son proporcionales al riesgo de la no conformidad
potencial.
Cláusula y Regulación:
ISO: ISO 13485:2016: 8.5.3;
TGA: TG(MD)R Sch3 P1 1.4(3)(a), (b), (5)(b)(iii), (f), TG(MD)R Sch1 P1 2;
ANVISA: RDC ANVISA 16/2013: 2.4, 7.1.1.1;
MHLW/PMDA: MHLW MO169: 64; 21
FDA: CFR 820.100(a)(2)
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Investigaciones de no conformidades potenciales
La profundidad de la investigación de la organización de Dispositivos Médicos sobre no
conformidades potenciales en procesos productos u otras no conformidades del sistema de calidad
deben ser acorde con el riesgo de la no conformidad si ocurriera. El proceso para determinar el
alcance de una investigación puede estar relacionado con el sistema de gestión de riesgos de la
organización de Dispositivos Médicos y los resultados esenciales para el correcto funcionamiento
del dispositivo.
MDSAP AU P0002.005 52 Página
Seleccionar registros
Al seleccionar registros de investigaciones para revisar, tener en cuenta el riesgo de la no
conformidad potencial con el producto o proceso. Seleccionar los registros de las investigaciones
donde la no conformidad potencial tiene un mayor riesgo de afectar negativamente la capacidad
del dispositivo terminado para cumplir con sus resultados de diseño esenciales o la no conformidad
potencial podría afectar la seguridad y la eficacia del producto.
Enlaces
Ninguno
Tarea 5 – Corrección, Acción Correctiva y Acción Preventiva
Confirmar que las correcciones, acciones correctivas y acciones preventivas fueron
determinadas, implementadas, documentadas, efectivas y que no afectaron adversamente
los dispositivos terminados.
Asegurar de que la acción correctiva y la acción preventiva sean apropiadas para el riesgo
de las no conformidades o posibles no conformidades encontradas.
Cláusula y Regulación:
ISO: ISO 13485:2016: 8.2.1, 8.2.5, 8.3.1,8.5.2, 8.5.3;
TGA: TG(MD)R Sch1 P1 2, TG(MD)R Sch3 P1 1.4(3)(a), (b), (5)(b)(iii), (f);
ANVISA: RDC ANVISA 16/2013: 2.4, 6.5, 7.1.1.3, 7.1.1.4, 7.1.1.5;
MHLW/PMDA: MHLW MO169: 55, 57, 60, 63, 64;
FDA: 21 CFR 820.100(a)(3), 820.100 (a)(4),820.100(a)(6), 820.100(b)
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Determinar el alcance de las acciones
Las acciones correctivas tomadas por una organización de Dispositivos Médicos pueden variar
según la situación.
Las acciones correctivas están destinadas a corregir y también prevenir la recurrencia no solo de
productos no conformes, sino también de prácticas deficientes, como una capacitación inadecuada.
Al desarrollar acciones correctivas para abordar productos no conformes, la organización del
Dispositivo Médico debe considerar correcciones con respecto a los productos afectados,
distribuidos o no. Las correcciones y las acciones correctivas deben ser proporcionales al riesgo
asociado con la no conformidad.
El equipo de auditoría puede encontrar situaciones donde se ha identificado un problema de
calidad, pero la Alta Dirección de la organización de Dispositivos Médicos ha decidido no llevar a
cabo acciones correctivas. Confirmar que la decisión de la organización de Dispositivos Médicos de
no tomar medidas correctivas se haya tomado utilizando una toma de decisiones basada en el
riesgo adecuada, incluida la determinación de que el dispositivo terminado cumple con los criterios
de aceptabilidad del riesgo.
Determinar la efectividad de las acciones
MDSAP AU P0002.005 53 Página
Durante la auditoría del proceso de Medición, Análisis y Mejora, revisar los mecanismos mediante
los cuales la organización de Dispositivos Médicos evaluó la efectividad de las acciones correctivas
y preventivas. Comparar los registros de acciones correctivas y acciones preventivas de mayor y /
o mayor riesgo con los análisis de datos de calidad y productos de la organización de Dispositivos
Médicos, como los resultados de tendencias. Buscar problemas o tendencias de productos o de
calidad que continuaron o comenzaron después de la implementación de las acciones. Esto puede
indicar que las acciones correctivas o preventivas no fueron efectivas.
Revise cómo la organización de Dispositivos Médicos ha determinado que las acciones no afectan
negativamente a los dispositivos terminados.
Enlaces
Eventos adversos de dispositivos médicos y Reportes de Notificaciones de Advertencia
Determinar si alguna de las acciones correctivas de la organización requiere informar a las
autoridades MDSAP participantes.
Tarea 6 – Evaluación de Cambio de Diseño como Resultado de Acción
Correctiva o Preventiva
Cuando una acción correctiva o preventiva da como resultado un cambio en el diseño,
verificar que cualquier nuevo peligro y cualquier nuevo riesgo se evalúan en el proceso de
gestión de riesgos.
Cláusula y Regulación:
ISO: ISO 13485:2016: 7.1, 7.3.9;
TGA: TG(MD)R Sch1 P1 2;
ANVISA: RDC ANVISA 16/2013: 2.4, 4.1.10;
MHLW/PMDA: MHLW MO169: 26, 36;
FDA: 21 CFR 820.30(i), 820.30(g)
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Cambio de Diseño
Completar esta tarea de auditoría puede implicar vínculos con otros subsistemas. Verificación y
validación son elementos importantes para asegurar que las acciones correctivas y preventivas que
resultan en los cambios de diseño son efectivos y no introducen nuevos peligros.
Enlaces
Diseño y Desarrollo
Si la acción correctiva o preventiva implica cambiar el diseño, los controles de diseño deberán
aplicarse al cambio cuando corresponda.
Cuando sea necesario, confirmar que los controles de diseño fueron aplicado al cambio de acuerdo
con los procedimientos de la organización de Dispositivos Médicos.
MDSAP AU P0002.005 54 Página
Además, los cambios de diseño deben evaluarse en el proceso de gestión de riesgos de la
organización de Dispositivos Médicos para garantizar que los cambios no introduzcan nuevos
peligros.
Tarea 7 – Evaluación de Cambio de Proceso como Resultado de Acción
Correctiva o Preventiva
Cuando una acción correctiva o preventiva da como resultado un cambio en el proceso,
confirmar que el cambio del proceso se evalúa para determinar si sek introducen nuevos
riesgos para el producto.
Verificar que el fabricante haya realizado la revalidación de los procesos cuando
corresponda.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.1.2, 4.1.4, 4.1.6, 4.2.1, 7.1, 7.5.2, 7.5.6, 7.5.7;
TGA: TG(MD)R Sch1 P1 2; Sch3 P1 1.5(4);
ANVISA: RDC ANVISA 16/2013: 2.4, 5.6, 7.1.1.4;
MHLW/PMDA: MHLW MO169: 5, 6, 26, 45, 46;
FDA: 21 CFR 820.100(a)(4), 820.100(a)(5), 820.70(b), 820.75(c)
Requisitos adicionales específicos del país:
Australia (TGA):
Confirmar que el procedimiento del fabricante para hacer frente a cambios sustanciales en un
proceso crítico (por ejemplo, esterilización, procesamiento de materiales de origen animal,
procesamiento de materiales de origen microbiano o recombinante o procesos que incorporan una
sustancia medicinal en un dispositivo médico) requiere que el fabricante notifique la Organización
de Auditoría de sus planes antes de implementar un cambio en un proceso crítico. La Organización
de Auditoría debe evaluar el cambio propuesto antes de la implementación por parte del
Fabricante, para determinar si los requisitos del procedimiento de evaluación de la conformidad
relevante aún se cumplirán después del cambio. [TG (MD) R Sch3 P1 1,5 (2)].
Si el fabricante también es titular de un certificado de evaluación de conformidad de TGA, también
se requiere que el fabricante notifique a la TGA de estos cambios, antes de la implementación.
Canadá (HC):
Verificar que el fabricante tenga un proceso o procedimiento para identificar un "cambio
significativo" en un dispositivo de clase III o IV. Verificar que la información sobre "cambios
significativos" se presente en una solicitud de modificación de licencia de dispositivo médico
[CMDR 1, 34].
Japón (MHLW):
Confirmar que cuando el sitio de fabricación registrado planea realizar un cambio significativo en
los procesos de fabricación (por ejemplo, cambio de sitio de esterilización, cambio de sitio de
fabricación), el sitio de fabricación registrado notifica al titular de la autorización de comercialización
para para que el titular de la autorización de comercialización pueda realizar las acciones
regulatorias pertinentes [MHLW MO169: 29].
Evaluación de la conformidad:
MDSAP AU P0002.005 55 Página
Cambios de proceso
Completar esta tarea de auditoría puede implicar vínculos con otros procesos del sistema de
gestión de calidad. Los procesos de producción requieren al menos algún grado de calificación,
verificación o validación. Si el cambio involucra un proceso validado, revisar la evaluación de la
organización del cambio del proceso para determinar si es necesaria la revalidación.
Para los cambios en los procesos de producción que realizan los proveedores, el equipo de
auditoría debe considerar seleccionar a esos proveedores para la evaluación durante la auditoría
del proceso de Compras. En los casos en que la organización de Dispositivos Médicos realiza un
cambio en un proceso validado realizado por un proveedor, el equipo de auditoría debe evaluar si
se requiere una nueva validación. Si se requiere una nueva validación de los procesos de
producción, confirmar que los resultados muestran que el proceso cumple con el resultado
planificado.
Enlaces
Controles de Producción y Servicio, Compras
Si la acción correctiva o preventiva implica cambiar un proceso de producción, el equipo de
auditoría debe considerar seleccionar este cambio para la evaluación durante la auditoría de los
Controles de Producción y Servicio.
Tarea 8 – Identificación y Control de Producto No Conforme
Verificar que los controles estén en su lugar para garantizar que el producto que no cumpla
con los requisitos del producto se identifique y controle para evitar su uso o entrega
involuntarios.
Confirmar que se realizó, justificó y documentó una disposición apropiada y que se notificó
a cualquier parte externa responsable de la No Conformidad.
Cláusula y Regulación:
ISO: ISO 13485:2016: 8.3.1, 8.3.2;
TGA: TG(MD)R Sch3 P1 1.4(5)(b)(iii);
ANVISA: RDC ANVISA 16/2013: 6.5, 7.1.1.6;
MHLW/PMDA: MHLW MO169: 60;
FDA: 21CFR 820.90(a)
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Producto no conforme
El equipo auditor debe revisar los procedimientos y controles para prevenir la distribución
involuntaria de Producto No Conforme. El (los) auditor (es) pueden elegir seleccionar una muestra
de registros que involucren Producto No Conforme que estaban en existencia o devueltos para
revisar cómo se aplicaron los procedimientos y controles para controlar el Producto No Conforme.
Confirmar que la organización ha establecido y mantenido procedimientos que definen la
responsabilidad de la revisión y la autoridad para la disposición del producto no conforme, así
como la ejecución del proceso de revisión y disposición. La disposición del producto no conforme
debe documentarse.
MDSAP AU P0002.005 56 Página
El equipo de auditoría puede encontrar situaciones en las que la Alta Dirección de la organización
haya decidido autorizar el uso de productos no conformes bajo concesión. La documentación debe
incluir la justificación para el uso del producto no conforme y la firma de la (s) persona (s) que
autorizan el uso. Confirmar que la decisión de la organización de utilizar un producto no conforme
bajo concesión se ha realizado utilizando una toma de decisiones basada en el riesgo adecuada,
incluida la determinación de que el dispositivo terminado cumple con los requisitos especificados.
Tener en cuenta los casos en que el uso de productos no conformes en concesión ha llevado a que
los dispositivos no cumplan con las especificaciones.
Seleccionar registros
Al seleccionar registros de productos no conformes para revisar, tener en cuenta el riesgo de no
conformidad para el dispositivo terminado y el paciente o usuario. Seleccionar registros de
productos no conformes para revisar dónde la no conformidad tiene un mayor riesgo de afectar
negativamente la capacidad del dispositivo terminado para cumplir con sus productos de diseño
esenciales o la no conformidad afecta la seguridad y eficacia del producto.
Enlaces
Ninguno
Tarea 9 – Acción relativa a Producto No Conforme después de la Entrega
Confirmar que cuando se detecta un producto no conforme después de la entrega o el uso,
se toman las medidas adecuadas acordes con el riesgo o los riesgos potenciales de la no
conformidad.
Cláusula y Regulación:
ISO: ISO 13485:2016: 8.3.3, 8.5.2;
TGA: TG(MD)R Sch1 P1 2, TG(MD)R Sch3 P1 1.4(3)(a), (b), (5)(b)(iii), (f);
ANVISA: RDC ANVISA 16/2013: 2.4, 7.1.1.8;
MHLW/PMDA: MHLW MO169: 60, 63;
FDA: 21 CFR 820.100(a)
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Control y acción basados en el riesgo
Durante esta tarea de auditoría, confirmar que la organización ha determinado el control y las
acciones que se deben tomar sobre los productos no conformes detectados después de la entrega
o el uso, en proporción con el riesgo asociado con una falla del producto.
Si bien puede no ser necesario que la organización retire el producto no conforme de distribución
como parte de las acciones identificadas necesarias para corregir e impedir la reaparición del
problema, confirmar que la decisión se toma usando una justificación de riesgo adecuada.
Enlaces
Eventos adversos de Dispositivos Médicos Y Reportes de Notificaciones de Advertencias
Si la organización de Dispositivos Médicos ha realizado acciones de campo en productos ya
distribuidos, confirmar que las autoridades regulatorias apropiadas de MDSAP han sido notificadas,
si es necesario.
MDSAP AU P0002.005 57 Página
Tarea 10 – Auditoría Interna
Verificar que las auditorías internas del sistema de gestión de calidad se realicen de acuerdo
con los arreglos planificados y procedimientos documentados para garantizar que el
sistema de gestión de calidad cumpla con los requisitos establecidos del SGC y los
requisitos regulatorios aplicables, y para determinar la eficacia del sistema de calidad.
Confirmar que las auditorías internas incluyan disposiciones para el entrenamiento e
independencia del auditor sobre las áreas auditadas, correcciones, acciones correctivas,
actividades de seguimiento y verificación de acciones correctivas.
Cláusula y Regulación:
ISO: ISO 13485:2016: 6.2, 8.2.4;
TGA: TG(MD)R Sch3 P1 1.4(5)(b)(iii);
ANVISA: RDC ANVISA 16/2013: 7.3;
MHLW/PMDA: MO169: 22, 23, 56;
FDA: 21 CFR 820.22, 820.100
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Auditorías internas
Las auditorías internas son exámenes sistemáticos e independientes del sistema de gestión de
calidad de una organización que se realizan a intervalos definidos y con suficiente frecuencia para
determinar si las actividades del sistema de gestión de calidad y los resultados de tales actividades
cumplen con los procedimientos del sistema de gestión de calidad. Las auditorías internas también
deben determinar si estos procedimientos se implementan de manera efectiva y si son adecuados
para lograr los objetivos del sistema de gestión de calidad.
Auditores
Las auditorías internas se llevarán a cabo de acuerdo con los procedimientos establecidos por
personas debidamente capacitadas que no tienen responsabilidad directa por los asuntos
auditados. Si es posible, entrevistar a los auditores y preguntar cómo se realizan las auditorías,
cuánto duran las auditorías, qué documentos se revisan normalmente, etc.
Requisitos
Los procedimientos de auditoría interna generalmente incluyen requisitos para las calificaciones del
auditor, los requisitos para la frecuencia de las auditorías, las áreas funcionales específicas que se
auditarán y los planes de auditoría (o el requisito de establecer planes de auditoría antes de la
auditoría). Los procedimientos también deben incluir requisitos para:
cómo deben comunicarse, abordarse y seguirse las actividades y los resultados de la
auditoría (incluida una nueva auditoría, si es necesario) y,
cómo se documentarán las actividades de auditoría.
Revisión y documentación
MDSAP AU P0002.005 58 Página
La Alta Dirección tiene la responsabilidad de los asuntos auditados debe revisar el informe de la
auditoría de calidad. Deben documentarse las fechas y los resultados de todas las auditorías de
calidad (y las re-auditorías subsiguientes, si es necesario), así como también cualquier acción
correctiva o preventiva resultante de las auditorías internas.
Enlaces
Gestión
Durante la auditoría del proceso de gestión, el equipo auditor debe confirmar que el resultado de
las auditorías internas son una entrada para la Revisión de la Dirección.
TAREA 11 – INFORMACIÓN PROPORCIONADA PARA LA REVISIÓN DE LA DIRECCIÓN
Determinar si la información relevante sobre el producto no conforme, las no conformidades
del sistema de gestión de la calidad, las correcciones, las acciones correctivas y las
acciones preventivas se han informado a la Alta Dirección para su Revisión por la Dirección.
Cláusula y Regulación:
ISO: ISO 13485: 2016: 5.6.2;
TGA: TG (MD) R Sch3 P1 1,4 (5) (b) (iii);
ANVISA: RDC ANVISA 16/2013: 2.2.6, 7.1.1.7;
MHLW/PMDA: MO169: 19;
FDA: 21 CFR 820.100 (a) (7)
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Revisión por la Dirección
Durante el desempeño de esta tarea de auditoría, los auditores pueden optar por seleccionar una
medida correctiva o preventiva significativa reciente y determinar qué registros o información sobre
el evento se presentaron para la Revisión por la Dirección.
Enlaces
Gestión
Durante la auditoría del proceso de Gestión, el equipo de auditoría debería haber confirmado que
el estado de las acciones correctivas y preventivas es un aporte a la Revisión por la Dirección.
Durante la auditoría del proceso de Medición, Análisis y Mejora, determinar que la Alta Dirección
conoce los problemas de calidad de mayor riesgo, así como las acciones correctivas y preventivas
significativas, cuando sea necesario.
Tarea 12 – Evaluación de la Información de la Fase Post-Producción,
incluyendo Quejas
Confirmar que la organización de Dispositivos Médicos ha hecho arreglos efectivos para
adquirir experiencia de la fase de posproducción, manejo de quejas e investigación de la
causa de las no conformidades relacionadas con avisos de notificación con provisión de
retroalimentación en el proceso de Medición, Análisis y Mejora.
MDSAP AU P0002.005 59 Página
Seleccionar los registros de quejas para su revisión que representen el mayor riesgo para el
usuario o que tengan el mayor impacto en la capacidad del dispositivo para cumplir con sus
resultados de diseño esenciales.
Verificar que la información del análisis de producción y los datos de calidad de
posproducción se consideraron para mejorar el análisis del riesgo del producto, según
corresponda.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 7.2.3, 7.5.4 (a), 8.2.1, 8.2.2;
TGA: TG(MD)R Sch1 P1 2, Sch3 P1 1.4(3), 1.4(5)(b)(iii) &1.4(5)(f);
ANVISA: RDC ANVISA 16/2013: 7.2;
HC: CMDR 57-58;
MHLW/PMDA: MO169: 6, 29, 43, 55, 62.6;
FDA: 21 CFR 820.198
Requisitos adicionales específicos del país:
Australia (TGA):
Verificar que la organización de Dispositivos Médicos tenga procedimientos para un sistema de
post-comercialización que incluya una revisión sistemática de la experiencia de posproducción (por
ejemplo, de; grupos de usuarios expertos, encuestas de clientes, quejas de clientes y reclamos de
garantía, información de servicio y reparación, revisiones de literatura, publicaciones -Ensayos
clínicos de producción, comentarios de los usuarios que no sean quejas, esquemas de registro y
seguimiento de dispositivos, reacciones de los usuarios durante la capacitación, informes de
eventos adversos). La investigación debe realizarse de manera oportuna para garantizar que el
Patrocinador australiano pueda cumplir con los plazos de notificación de eventos adversos o la
implementación de avisos (retiros) [TG (MD) R Sch3 P1 1.4 (3) (a)].
Nota: En Australia, la realización de un retiro es responsabilidad del Patrocinador australiano de
acuerdo con el Procedimiento Australiano de Retiro Uniforme de Productos Terapéuticos.
Brasil (ANIVISA):
Verificar que cada fabricante haya establecido y mantenga procedimientos para recibir, examinar,
evaluar, investigar y documentar quejas. Dichos procedimientos deben garantizar que:
Las quejas son recibidas, documentadas, analizadas, evaluadas, investigadas y
documentadas por una unidad designada formalmente;
Cuando corresponda, las quejas se deben informar a la autoridad sanitaria competente;
Las quejas deben ser examinadas para determinar si una investigación es necesaria.
Cuando no se realiza una investigación, la unidad debe mantener un registro que incluya la
razón por la cual no se realizó la investigación y el nombre del responsable de esa
decisión;
Cada fabricante debe examinar, evaluar e investigar todas las quejas que involucren
posibles no conformidades del producto. Cualquier reclamo por muerte, lesión o amenaza
a la salud pública debe ser revisado, evaluado e investigado inmediatamente.
Los registros de la investigación deben incluir:
Nombre del producto;
Fecha de recepción de la queja;
Cualquier número de control utilizado;
Nombre, dirección y número de teléfono del demandante;
Naturaleza de la queja;
Datos y resultados de investigación, incluidas las medidas adoptadas [RDC ANVISA
16/2013: 7.2].
MDSAP AU P0002.005 60 Página
Canadá (HC):
Verificar que el fabricante mantenga registros de los problemas informados relacionados con las
características de rendimiento o seguridad de un dispositivo, incluidas las quejas de los
consumidores recibidas por el fabricante después de que el dispositivo se vendió por primera vez
en Canadá y todas las medidas adoptadas por el fabricante en respuesta a los problemas
referentes a las quejas [CMDR Sección 57].
Verificar que el fabricante haya establecido e implementado procedimientos documentados que le
permitan llevar a cabo una investigación efectiva y oportuna de los informes de problemas a través
de las quejas de los clientes, y llevar a cabo un retiro del dispositivo eficaz y oportuno [CMDR
Sección 58].
Japón (MHLW / PMDA):
Confirmar que la persona que opera el Sitio de fabricación registrado ha determinado e
implementado un acuerdo efectivo para comunicarse con el titular de la autorización de
comercialización japonesa en relación con la retroalimentación de los clientes, incluidas las quejas
de los clientes y avisos de notificación [No.169: 29].
Estados Unidos (FDA):
Verificar que los procedimientos hayan sido definidos, documentados e implementados para recibir,
revisar y evaluar quejas por parte de una unidad designada formalmente. Los procedimientos
deben asegurar que:
Todas las quejas se procesan de manera uniforme y oportuna.
Las quejas orales se documentan a la recepción.
Las quejas se evalúan para determinar si la queja representa un evento que se debe
reportar a la FDA.
Cada fabricante debe revisar y evaluar todas las quejas para determinar si es necesaria una
investigación. Cuando no se realiza ninguna investigación, el fabricante debe mantener un registro
que incluya el motivo por el cual no se realizó ninguna investigación y el nombre del individuo
responsable de la decisión de no investigar.
Cualquier queja sobre la falla del dispositivo, etiqueta o empaque para cumplir con cualquiera de
sus especificaciones debe ser revisada, evaluada e investigada, a menos que tal investigación ya
haya sido hecha para una queja similar y no sea necesaria otra investigación.
Cualquier queja que represente un evento que debe ser reportado a la FDA debe ser revisada,
evaluada e investigada por un individuo designado y debe mantenerse en una porción separada de
los archivos de quejas o debe estar claramente identificada. Los registros de la investigación deben
incluir una determinación de:
Si el dispositivo no cumplió con las especificaciones.
Si el dispositivo se estaba utilizando para el tratamiento o el diagnóstico.
La relación, si la hay, del dispositivo con el incidente o evento adverso informado.
Cuando se realiza una investigación, la unidad formalmente designada debe mantener un registro
de la investigación. El registro de la investigación debe incluir:
El nombre del dispositivo.
La fecha en que se recibió la queja.
Cualquier identificador único (UDI, por sus siglas en inglés), o código de producto universal
(UPC, por sus siglas en inglés) o cualquier otra identificación de dispositivo y número (s) de
control utilizado (s).
MDSAP AU P0002.005 61 Página
El nombre, la dirección y el número de teléfono del demandante.
La naturaleza y los detalles de la queja.
Las fechas y resultados de la investigación.
Cualquier acción correctiva tomada.
Cuando la unidad designada formalmente del fabricante se encuentra en un sitio separado del
establecimiento de fabricación, la (s) queja (s) investigada (s) y el (los) registro (s) de la
investigación deben ser razonablemente accesibles para el establecimiento de fabricación [21 CFR
820.198].
Evaluación de la conformidad:
Evaluación de datos de postproducción
Durante la revisión de las fuentes de datos de calidad que sirven como entradas para el proceso de
Medición, Análisis y Mejora, el equipo de auditoría puede optar por revisar las quejas y la
retroalimentación de los clientes. Confirmar que las quejas se manejan según lo requerido por las
autoridades regulatorias participantes de MDSAP. Las quejas pueden ser una importante fuente de
información con respecto a los problemas de calidad y, a menudo, son indicativos de que los
dispositivos distribuidos (o su empaque o etiquetado) no cumplen con los requisitos especificados.
Seleccionar registros
Un método para analizar las quejas y retroalimentación de los clientes es revisar el análisis de los
datos de las quejas y seleccionar uno o más modos de falla de las quejas, preferiblemente los
modos de falla asociados con un mayor riesgo para el paciente o el usuario. Una vez que el
equipo de auditoría ha seleccionado los modos de falla de queja, el auditor (es) puede seleccionar
una muestra de quejas de esos modos de falla y confirmar que las quejas se manejan de manera
apropiada, incluida la investigación y la implementación de medidas correctivas cuando sea
necesario.
Gestión de riesgos
La información de las fuentes de postproducción, incluidas las quejas y retroalimentación de los
clientes, puede proporcionar información importante para las actividades de gestión de riesgos
para el dispositivo. En particular, los riesgos previamente no identificados descubiertos durante el
monitoreo posterior a la producción pueden indicar la necesidad de mejorar el proceso de gestión
del riesgo o pueden indicar la necesidad de cambios en el diseño. Además, sobre la base de los
datos de calidad de posproducción, la organización de Dispositivos Médicos puede optar por
promulgar controles nuevos o más estrictos para mantener un nivel aceptable de riesgo del
producto.
Enlaces
Eventos Adversos de Dispositivos Médicos y Reportes Notificación; Diseño y Desarrollo; Controles
de Producción y Servicio
Durante la revisión de quejas y retroalimentación del cliente, confirmar que los informes de
dispositivos médicos individuales se hicieron a las autoridades regulatorias apropiadas cuando sea
necesario.
La información proveniente de la revisión de las fuentes de posproducción, incluidas las quejas y
los informes de vigilancia posteriores a la comercialización, debe orientar al equipo auditor en la
selección de diseños para revisar y procesos de producción para auditar.
MDSAP AU P0002.005 62 Página
Tarea 13 – Comunicación con Partes Externas involucradas en Quejas
Cuando la investigación determine que las actividades fuera de la organización
contribuyeron a una queja del cliente, verificar que los registros muestren que se
intercambió información relevante entre las organizaciones involucradas.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.1.5, 7.4.1, 8.3.1;
ANVISA: RDC ANVISA 16/2013: 7.1.1.6;
MHLW/PMDA: MO169: 5, 37, 60;
FDA: 21 CFR 820.100(a)(6)
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Quejas y no conformidades atribuidas al producto suministrado
Confirmar que la información relacionada con problemas de calidad o productos no conformes,
incluidas las quejas, se difunde a los responsables directos de garantizar la calidad del producto.
Esto incluye instancias donde la investigación revela que la causa subyacente de la queja o
producto no conforme se relaciona con el producto suministrado. La organización de Dispositivos
Médicos debe notificar al proveedor sobre el problema de calidad y tomar las medidas correctivas
apropiadas cuando sea necesario. El incumplimiento de una organización externa para
proporcionar productos que cumplan con los requisitos especificados puede descalificarlos como
un proveedor aceptable o aprobado.
Enlaces
Compras
Durante la auditoría del proceso de Medición, Análisis y Mejora, si las no conformidades
significativas están relacionadas con el producto suministrado, el equipo de auditoría debe
considerar seleccionar a esos proveedores para la evaluación durante la auditoría del proceso de
Compras de la organización de Dispositivos Médicos.
Tarea 14 – Evaluación de Quejas para Reporte de Eventos Adversos
Verificar que la organización de Dispositivos Médicos ha definido y documentado
procedimientos para la evaluación de quejas para reportes de Eventos Adversos.
Confirmar que las decisiones de no informar las quejas se tomaron de acuerdo con los
procedimientos establecidos y una justificación documentada.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1,7.2.3, 8.2.3;
TGA: TG(MD)R Sch3 P1 1.4(3)(c);
ANVISA: RDC ANVISA 16/2013: 7.1.1.8, RDC ANVISA 67/2009;
HC: CMDR 59-61.1;
MHLW/PMDA: MO169: 6, 29, 62;
FDA: 21 CFR 803
Requisitos adicionales específicos del país:
MDSAP AU P0002.005 63 Página
Consultar el proceso de MDSAP Eventos Adversos del Dispositivo Médico y Reportes de
Notificaciones de Advertencia.
Evaluación de la conformidad:
Informes individuales de eventos adversos
Un resultado de las actividades asociadas con el proceso de Medición, Análisis y Mejora, como el
manejo de quejas, puede ser la notificación de eventos adversos individuales a las autoridades
regulatorias en las que se comercializa el dispositivo. Cuando corresponda, seleccionar los
registros de quejas que cumplan con los criterios para informar y confirmar los informes
apropiados, así como si la información se proporcionó a la autoridad regulatoria. Asegurar de que
los informes de eventos adversos individuales contengan información precisa mediante la
comparación de los informes presentados con la denuncia asociada y la investigación de la queja.
Los eventos reportables suelen ser una importante fuente de datos de calidad de proceso de
Medición, Análisis y Mejora, ya que estos eventos indican que el dispositivo terminado ha causado
la muerte, lesiones graves o un mal funcionamiento de tal manera que, si se repitiera el mal
funcionamiento, el resultado podría ser muerte o lesión grave. Cualquier muerte, incluso si la
organización de Dispositivos Médicos lo atribuye a un error del usuario, se considera que tiene un
riesgo potencialmente alto asociado. Confirmar que los eventos reportables se evaluaron para la
acción correctiva cuando sea necesario.
Enlaces
Ninguno
Tarea 15 – Evaluación de Problemas de Calidad para Notificaciones de
Advertencia
Confirmar que el fabricante ha hecho arreglos efectivos para la evaluación oportuna de los
problemas de calidad que involucran productos distribuidos para la posible emisión e
implementación de notificaciones de advertencia.
Seleccionar registros para la revisión de problemas de calidad que fueron evaluados para la
posible emisión de a de advertencia (incluir registros donde se tomó la decisión de no emitir
un aviso de advertencia, así como registros de decisión de emitir avisos de advertencia) y
evaluar si la organización ha tomado las medidas adecuadas. basado en el riesgo y
documentado la justificación.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 7.2.3, 8.3.3;
TGA: TG(MD)R Sch3 P1 1.4(3)(c);
ANVISA: RDC ANVISA 16/2013: 7.1.1.8, RDC ANVISA 23/2012;
HC: CMDR 63-65.1;
MHLW/PMDA: MO169: 6, 29, 60;
FDA: 21 CFR 806
Requisitos adicionales específicos del país:
Consultar el proceso de MDSAP Eventos Adversos del Dispositivo Médico y Reportes de
Notificaciones de Advertencia.
Evaluación de la conformidad:
Notificaciones de Advertencia
MDSAP AU P0002.005 64 Página
Un resultado de las actividades asociadas con el proceso de Medición, Análisis y Mejora, incluido
el manejo de quejas y el descubrimiento de un producto no conforme que se ha distribuido, puede
ser la determinación de si es necesaria una acción de asesoramiento. Cuando corresponda,
seleccionar los problemas de calidad que se evaluaron para posibles acciones de asesoramiento y
evaluar si se tomaron las acciones adecuadas y las decisiones de la organización se justificaron,
en función del riesgo del problema de calidad para los usuarios del dispositivo. Esto puede incluir
evaluar si la organización determinó adecuadamente el alcance del problema de calidad. Por
ejemplo, si la organización determinó que un producto se distribuye en tres jurisdicciones MDSAP,
pero el aviso de advertencia solo se emitió en una jurisdicción MDSAP, el equipo de auditoría debe
determinar si la organización tiene una justificación documentada adecuada para el alcance de la
acción de asesoramiento.
Los problemas de calidad que llevaron a una Notificación de Advertencia son a menudo una fuente
importante de datos de calidad para el proceso de acciones correctivas, ya que estos eventos son
indicativos de que el dispositivo terminado no cumple con los requisitos especificados y tiene el
potencial de riesgo irrazonable para el usuario. Confirmar que los problemas de calidad que
resultaron en Notificaciones de Advertencia fueron evaluados para acción correctiva. Si se tomaron
medidas correctivas, evaluar el mecanismo por el cual la organización aseguró que la acción es
efectiva y no afecta negativamente la capacidad del dispositivo para cumplir con los requisitos
especificados. Si no se tomaron medidas correctivas para los problemas de calidad asociados con
una corrección, remoción o Notificaciones de Advertencia, revisar los fundamentos de la
organización para no emprender acciones correctivas y confirmar que la decisión es apropiada
utilizando un proceso de toma de decisiones basado en el riesgo.
Decisiones de no informar una corrección, eliminación o Notificación de Advertencia
El equipo de auditoría puede encontrar instancias donde la organización ha realizado actividades
que implican la emisión de Avisos de Notificación sin notificar a las autoridades regulatorias en los
mercados en los que se comercializa el dispositivo. En estas situaciones, revisar los fundamentos
de la organización para no informar estas acciones y asegurar de que la razón sea apropiada.
Verificar que los registros de la acción se mantengan.
Enlaces
Ninguno
Tarea 16 – Compromiso de la Alta Dirección para el Proceso de Medición,
Análisis y Mejora
Determinar, en base a la evaluación del proceso de Medición, Análisis y Mejora global, si la
Alta Dirección proporciona el compromiso necesario para detectar y abordar las no
conformidades de los sistemas de gestión de calidad, así como de los productos, y
garantiza la idoneidad y efectividad continuas del sistema de gestión de la calidad.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.1.3, 5.2, 8.1, 8.5.1;
ANVISA: RDC ANVISA 16/2013: 2.2.1;
MHLW/PMDA: MO169: 5, 11, 54, 62
Requisitos adicionales específicos del país:
Ninguno
MDSAP AU P0002.005 65 Página
Enlaces
Ninguno
Capítulo 4: Eventos Adversos de Dispositivos Médicos y Reportes
de Notificación
El proceso de Notificación de Eventos Adversos y Reportes de Notificación de Dispositivos
Médicos puede auditarse como un enlace del proceso de Medición, Análisis y Mejora.
Auditando los Eventos Adversos de Dispositivos Médicos y Reportes de
Notificación
Propósito: El objetivo de auditar los Eventos adversos de dispositivos médicos y los Reportes de
Notificaciones de Advertencia es verificar que los procesos de la organización de Dispositivos
Médicos aseguren que los eventos adversos y notificaciones de advertencia relacionados con los
dispositivos médicos individuales sean informados a las autoridades regulatorias dentro de los
plazos requeridos.
MDSAP AU P0002.005 66 Página
Resultados: Como resultado de la auditoría de los Eventos adversos de dispositivos médicos y el
proceso de avisos de notificación, la evidencia objetiva mostrará si la organización del Dispositivo
Médico ha:
A) Definido procesos para garantizar que los eventos adversos individuales relacionados con
el dispositivo se informan a las autoridades regulatorias según sea necesario.
B) Asegurado de que las notificaciones de advertencia son informadas a las autoridades
regulatorias y a los representantes autorizados cuando sea necesario.
C) Mantenido registros apropiados de los eventos adversos individuales relacionados con los
dispositivos y avisos de notificación.
Enlaces a Otros Procesos:
Medición, Análisis y Mejora.
Tarea 1 – Notificación de Eventos Adversos
Verificar que la organización de Dispositivos Médicos cuenta con un proceso para
identificar eventos relacionados con el dispositivo que pueden cumplir con los criterios de
informe definidos por las autoridades regulatorias participantes.
Verificar que el proceso de quejas tenga un mecanismo para revisar cada queja a fin de
determinar si se requiere un informe a una autoridad regulatoria.
Confirmar que los procesos de la organización de Dispositivos Médicos cumplen los plazos
requeridos por cada autoridad regulatoria donde se comercializa el producto.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 7.2.3, 8.2.2, 8.2.3;
Requisitos específicos del país:
Australia (TGA):
Los fabricantes deben implementar un sistema de postcomercialización que incluya disposiciones
para el informe de eventos adversos, por ejemplo: Regulaciones de Bienes Terapéuticos
(Dispositivos Médicos) 2002 Anexo 3 Parte 1 Cláusula 1.4 (3) (c) (i). En vista del acuerdo escrito
entre los fabricantes y el patrocinador australiano [TG Act 41FD], los eventos deben ser informados
por el fabricante a la TGA, o al patrocinador de manera oportuna para garantizar que un
patrocinador pueda cumplir sus obligaciones de presentación de informes conforme a la
Regulación de Bienes Terapéuticos (Dispositivos Médicos) Regla 5.7:
Verificar que el fabricante u otra persona que está al tanto de un evento que represente
una seria amenaza a la salud pública proporciona información tan pronto como sea
posible. El patrocinador debe informar el evento dentro de un plazo de 48 horas.
Verificar que el fabricante u otra persona que está al tanto de un evento que condujo a la
muerte o un deterioro grave en el estado de salud de un paciente, usuario u otra persona
proporciona información tan pronto como sea posible. El patrocinador debe informar el
evento dentro de un plazo de 10 días.
Verificar que el fabricante u otra persona está al tanto de un evento cuya repetición puede
conducir a la muerte o un deterioro grave en el estado de salud de un paciente, un usuario
u otra persona, brinde información tan pronto como sea posible. El patrocinador debe
informar el evento dentro de un período de 30 días.
MDSAP AU P0002.005 67 Página
Nota: Un evento que conlleve una amenaza grave para la salud humana es un peligro que surge
de una falla sistemática de los dispositivos o un evento u otra ocurrencia que puede provocar la
muerte o lesiones graves.
Nota: los eventos adversos pueden ser informados en línea a TGA, por el fabricante o el
patrocinador, en:
https://www.tga.gov.au/reporting-problems
Nota: Es una condición de los patrocinadores australianos de los dispositivos Clase AIMD, Clase III
e Implantables Clase IIb que brinden tres informes anuales consecutivos al TGA luego de la
inclusión del dispositivo en el ARTG. Los reportes anuales vencen el 1 de octubre de cada año. Los
reportes deben ser para el período del 1 de julio al 30 de junio. El informe debe incluir:
No. ARTG.
Nombre del producto.
No (s) de Modelo.
Número suministrado en Australia.
Número suministrado en todo el mundo (los números deben incluir dispositivos que son
iguales pero que se suministran con nombre diferente en otra jurisdicción).
Número de quejas en Australia.
Número de quejas en todo el mundo.
Número de eventos adversos y tasas de incidentes en Australia (tasa = N.º de eventos /
No. Suministrado x 100 = Tasa%).
Número de eventos adversos y tasas de incidentes en todo el mundo.
Una lista de las quejas más comunes y todos los eventos adversos.
Informe de incidente del dispositivo (DIR, por sus siglas en inglés) número de esos eventos
adversos informados a TGA.
Notificación regulatoria / acción correctiva por el fabricante.
Nota: Los patrocinadores australianos deben proporcionar a los fabricantes toda la información
que pueda ayudar al fabricante para cumplir con las obligaciones de un procedimiento de
evaluación de la conformidad (por ejemplo, información en relación con los eventos adversos)
[TG (MD) R Reg 5.8].
Brasil (ANVISA):
Verificar que un sistema de vigilancia post-mercado sea establecido e implementado en la
organización de Dispositivos Médicos e integrado en el Sistema de Calidad, con procedimientos y
flujos de trabajo establecidos para asegurar la identificación correcta e inmediata de eventos
adversos, la realización de investigaciones y el uso de los resultados para mejorar la seguridad y
eficacia del dispositivo cuando sea necesario [RDC ANVISA 67/2009 - Art. 6º].
Para los fabricantes nacionales (también se aplica a los representantes legales en Brasil): verificar
que la Alta Dirección haya designado a un profesional como responsable del sistema de vigilancia
posterior al mercado. Esta designación debe estar documentada [RDC ANVISA 67/2009 - Art. 5º].
Verificar que la organización de Dispositivos Médicos tenga mecanismos para procesar y registrar
quejas, realizar investigaciones y proporcionar retroalimentación directamente al denunciante, o en
MDSAP AU P0002.005 68 Página
el caso de un fabricante internacional, a su representante legal en Brasil, según sea necesario
[RDC ANVISA 67/2009 - Art. 6º, Art. 7º, Art. 9º].
Verificar que la organización de Dispositivos Médicos haya notificado a la autoridad regulatoria
sobre los problemas asociados con sus dispositivos, incluidos los eventos adversos (críticos o no
críticos), cualquier defecto técnico identificado con respecto a los productos ya comercializados,
cualquier cosa que pueda poner en riesgo la salud pública o casos de falsificación [RDC ANVISA
67/2009 - Art. 8º].
Para el fabricante internacional, verificar que el representante legal en Brasil tenga conocimiento de
la ocurrencia de la posibilidad de muerte, riesgo grave para la salud pública o casos de
falsificación, asociados con sus productos exportados a Brasil [RDC ANVISA 67/2009 - Art. 8º].
Canadá (HC):
Regulaciones de Dispositivos Médicos SOR / 98-282, Sección 59-61.1:
Verificar que el fabricante y el importador de un dispositivo médico presenten un informe preliminar
y final al ministerio sobre cualquier incidente que ocurra dentro o fuera de Canadá que involucre un
dispositivo vendido en Canadá.
a) Relacionado con la falla del dispositivo o el deterioro en su efectividad o cualquier
inadecuación en su etiquetado o en sus instrucciones de uso.
b) Ha llevado a la muerte o al deterioro grave del estado de salud de un paciente, usuario u
otra persona, o podría hacerlo si ocurriera [CMDR 59].
Verifique que el fabricante u otra persona que tenga conocimiento de un evento que ocasionó la
muerte o un deterioro grave del estado de salud de un paciente, usuario u otra persona, brinde
información en un informe preliminar dentro de los 10 días posteriores a que la persona tenga
conocimiento del evento u ocurrencia [CMDR 60 (1) (a) (i)].
Verificar que el fabricante u otra persona que tenga conocimiento de un evento cuya recurrencia
pueda provocar la muerte o un deterioro grave del estado de salud de un paciente, usuario u otra
persona, proporcione información en un informe preliminar dentro de los 30 días posteriores a que
la persona se da cuenta del evento u ocurrencia [CMDR 60 (1) (a) (ii)].
Nota: El requisito de informar incidentes que cumplan con los requisitos de la sección 59. (1) que
ocurran fuera de Canadá no se aplica a menos que el fabricante haya indicado, a una agencia
reguladora del país en el que ocurrió el incidente, la intención del fabricante de tomar medidas
correctivas. acción, o a menos que la agencia reguladora haya requerido que el fabricante tome
una acción correctiva. [CMDR 59. (2)].
Verificar que el fabricante haya hecho arreglos efectivos para enviar informes preliminares al
Ministerio y que los informes contienen [CMDR 60 (2)]:
El identificador de cualquier dispositivo médico que sea parte de un sistema, kit de prueba,
grupo de dispositivos médicos, familia de dispositivos médicos o familia de grupos de
dispositivos médicos;
Si el informe está hecho por:
MDSAP AU P0002.005 69 Página
el fabricante: el nombre y la dirección de ese fabricante y de cualquier importador
conocido, y el nombre, título y números de teléfono y facsímil de un representante del
fabricante para contactar para cualquier información relacionada con el incidente, o
el importador del dispositivo: el nombre y la dirección del importador y del fabricante y el
nombre, título y números de teléfono y facsímil de un representante del importador para
contacto para cualquier información relacionada con el incidente;
La fecha en que el incidente llamó la atención del fabricante o importador;
Los detalles conocidos con respecto al incidente, incluida la fecha en que ocurrió el
incidente y las consecuencias para el paciente, usuario u otra persona;
El nombre, la dirección y el número de teléfono, si se conoce, de la persona que reportó el
incidente al fabricante o importador;
La identidad de cualquier otro dispositivo o accesorio médico involucrado en el incidente, si
se conoce;
Los comentarios preliminares del fabricante o importador con respecto al incidente;
El curso de acción, incluida una investigación, que el fabricante o importador propone para
seguir con respecto al incidente y un calendario para llevar a cabo cualquier acción
propuesta y para presentar un informe final; y
Una declaración que indique si se ha realizado un informe anterior al Ministerio con
respecto al dispositivo y, de ser así, la fecha del informe.
Si un informe preliminar requerido por la sección 60 se presenta al Ministerio y / o Importador,
verificar que el fabricante haya presentado un informe final al Ministerio por escrito de acuerdo con
el cronograma establecido en CMDR 60 (2) (h) y el informe final contiene [CMDR 61 (1)]:
una descripción del incidente, incluyendo el número de personas que han experimentado
un deterioro grave en el estado de su salud o que han muerto;
una explicación detallada de la causa del incidente y una justificación de las acciones
tomadas con respecto al incidente; y
cualquier acción tomada como resultado de la investigación, que puede incluir:
aumento de la vigilancia posterior al mercado del dispositivo,
acción correctiva y preventiva con respecto al diseño y fabricación del dispositivo, y retiro
del dispositivo.
Si los informes requeridos por las secciones 60 y 61 son presentados al Ministerio por el
importador, verificar que el fabricante ha informado al Ministerio por escrito y que los informes que
presentarían el fabricante y el importador han presentado eran idénticos y que el fabricante ha
permitido al importador preparar y enviar reportes al Ministerio en nombre del fabricante [CMDR
61.1].
Japón (MHLW):
Los titulares de la autorización de comercialización deben implementar actividades de seguridad
posteriores al mercado de conformidad con los requisitos reglamentarios nacionales (japoneses)
además de los requisitos de SGC.
Las personas que operan los sitios de fabricación registrados no están obligadas a informar
cualquier evento adverso directamente a una autoridad regulatoria, pero deberán informar al titular
de la autorización de comercialización cualquier evento adverso que cumpla con los criterios
especificados por la Ordenanza para la aplicación de la Ley PMD Artículo 228-20.2 al titular de la
autorización de comercialización [MHLW MO169: 62.6].
MDSAP AU P0002.005 70 Página
Verificar que la persona que opera el Sitio de Fabricación Registrado proporcione eventos que
cumplan los siguientes criterios definidos por la Ordenanza para la Aplicación de la Ley PMD
Artículo 228-20.2 (ver abajo), al Titular de la Autorización de Comercialización de manera oportuna.
Los siguientes eventos de mal funcionamiento que pueden causar o pueden haber
causado daños a la salud:
Evento serio (nacional y extranjero).
Evento no grave no etiquetado (doméstico).
Los siguientes eventos de mal funcionamiento que pueden causar o pueden haber
causado daños a la salud:
Evento serio (nacional y extranjero).
Evento no grave no etiquetado (doméstico).
Cualquier medida adoptada para prevenir la aparición o la expansión del peligro para la
salud pública en relación con un dispositivo médico que se comercializa en países
extranjeros y es equivalente al que se comercializada en Japón. La acción incluye, pero no
se limita a:
Suspensión de fabricación, importación o venta,
Retiro del Mercado, y
Abolición.
Informe de estudio que indica:
Posibilidad de evento de cáncer y otras enfermedades graves, lesiones o muerte causadas
por el mal funcionamiento de un dispositivo médico (nacional y extranjero), o por
enfermedades infecciosas derivadas del uso de un dispositivo (nacional y extranjero),
Tasa significativa de ocurrencia, cambio de evento, etc. causado por el mal funcionamiento
de un dispositivo médico (nacional y extranjero),
Cambio significativo en la tasa de ocurrencia de enfermedades infecciosas causadas por el
uso de un dispositivo médico (nacional y extranjero) y,
El hecho de que un dispositivo médico es menos efectivo de lo que se afirma cuando se
aprueba.
Estados Unidos (FDA):
21 CFR 803: Reporte de dispositivos médicos
Determinar si el fabricante ha desarrollado un proceso para informar incidentes a la FDA que
involucran muertes relacionadas con dispositivos, lesiones graves y fallas reportables que ocurren
dentro y fuera de los Estados Unidos si el mismo dispositivo o uno similar se comercializa en los
Estados Unidos.
Confirmar que el fabricante haya desarrollado, mantenido e implementado procedimientos escritos
de Reportes de Dispositivos Médicos (MDR, por sus siglas en inglés) para lo siguiente:
MDSAP AU P0002.005 71 Página
Procesos internos que proporcionan:
Identificación, comunicación y evaluación oportuna y efectiva de eventos que pueden estar
sujetos a los requisitos de MDR;
Un proceso o procedimiento de revisión estandarizado para determinar cuándo un evento
cumple con los criterios para informar; y
Transmisión oportuna de informes completos de dispositivos médicos a la FDA.
Requisitos de documentación y mantenimiento de registros para:
Información que se evaluó para determinar si un evento era denunciable;
Todos los informes de dispositivos médicos y la información enviada a la FDA
Procesos que garantizan el acceso a la información que facilita un seguimiento y auditoría
oportunos.
Verificar que los informes se realicen dentro de los 30 días calendario posteriores al día en que el
fabricante reciba o tenga conocimiento de la información, de cualquier fuente, que razonablemente
sugiera que un dispositivo que se comercializa puede haber causado o contribuido a una muerte o
lesión grave:
Confirmar que los archivos MDR del fabricante contienen lo siguiente:
Información (o referencias a información) relacionada con el evento adverso, incluida toda
la documentación de las deliberaciones y los procesos de toma de decisiones utilizados
para determinar si una muerte relacionada con el dispositivo, una lesión grave o un mal
funcionamiento fue o no reportable a la FDA.
Copias de todos los formularios MDR y otra información relacionada con el evento enviada
a la FDA.
Si un dispositivo ha funcionado mal y es probable que este dispositivo o un dispositivo similar que
se comercialice cause o contribuya a la muerte o lesiones graves, si el mal funcionamiento se
repitiera, los informes resumidos trimestrales son aceptables para la mayoría de los códigos de
producto del dispositivo.
Si el fabricante mantiene archivos de eventos MDR como parte del archivo de quejas, asegúrese
de que el fabricante haya identificado de manera prominente estos registros como eventos
reportables MDR. La FDA no considerará que un informe MDR presentado cumple con 21 CFR
803 a menos que el fabricante evalúe un evento de acuerdo con los requisitos del sistema de
gestión de calidad. Confirme que el fabricante haya documentado y mantenido en los archivos de
eventos MDR una explicación de por qué el fabricante no presentó o no pudo obtener la
información requerida por 21 CFR 803, así como los resultados de la evaluación de cada evento.
Comparar la información presentada en el informe del dispositivo médico individual con la
información contenida en la queja asociada y confirmar que el informe del dispositivo médico
contiene toda la información relacionada con el evento que el fabricante conoce razonablemente.
Verificar que el fabricante haya enviado informes a la FDA a más tardar 5 días hábiles después del
día en que el fabricante tenga conocimiento de que:
Un evento reportable de MDR requiere una acción correctiva para evitar un riesgo irrazonable
de daño sustancial a la salud pública. El fabricante puede tener conocimiento de la necesidad
de tomar medidas correctivas a partir de cualquier información, incluido cualquier análisis de
tendencias; o
MDSAP AU P0002.005 72 Página
La FDA ha presentado una solicitud por escrito para la presentación de un informe de 5 días.
Si el fabricante recibe dicha solicitud por escrito de la FDA, el fabricante debe enviar, sin más
solicitudes, un informe de 5 días para todos los eventos posteriores de la misma naturaleza
que involucren dispositivos sustancialmente similares para el período de tiempo especificado
en la solicitud por escrito. La FDA puede extender el período de tiempo establecido en la
solicitud original por escrito si la FDA determina que es en interés de la salud pública.
Verificar que el fabricante haya enviado informes complementarios en el plazo de un mes desde la
obtención de la información que no se envió en un informe inicial.
Confirmar que los informes de dispositivos médicos incluyen el identificador de dispositivo único
(UDI, por sus siglas en inglés) que aparece en la etiqueta del dispositivo o en el paquete del
dispositivo.
Los informes de dispositivos médicos enviados a la FDA deben enviarse electrónicamente a través
del Electronic Submissions Gateway (ESG) utilizando eSubmitter o AS2 Gateway-to-Gateway
utilizando el software HL7 ICSR XML.
Enlaces
Medición, Análisis y Mejora
Los informes de eventos adversos individuales son una forma de retroalimentación y deben
analizarse según corresponda para las tendencias que requieren mejoras o acciones correctivas.
Durante la auditoría del proceso de Medición, Análisis y Mejora, confirmar que la organización haya
considerado eventos adversos individuales y tendencias de eventos adversos en el análisis de
datos.
Tarea 2 – Notificación de Avisos de Advertencia
Verificar que los Avisos de Advertencia sean informados a las autoridades regulatorias
cuando sea necesario y que cumplan con los plazos y los requisitos de mantenimiento de
registros establecidos por las autoridades regulatorias participantes.
Cláusula y Regulación:
ISO: ISO 13485: 2016: 4.2.1, 7.2.3, 8.2.3, 8.3.3
Requisitos específicos del país:
Australia (TGA):
Los fabricantes deben implementar un sistema de post-comercialización que incluya disposiciones
para la recuperación de dispositivos, por ejemplo, Regulaciones de Productos Terapéuticos
(Dispositivos Médicos) 2002 Anexo 3 Parte 1 Cláusula 1.4 (3) (c) (ii). En vista del acuerdo escrito
entre los Fabricantes y el Patrocinador australiano [TG Act 41FD] (ver Anexo 4), el Fabricante debe
informar a la TGA o al Patrocinador de las retiros propuestas de manera oportuna para garantizar
que un Patrocinador pueda cumplir con sus obligaciones de notificación [Regulación 5.7 de
Productos Terapéuticos (Dispositivos Médicos), Parte 4-9 de la Ley de Productos Terapéuticos y el
Procedimiento Uniforme de Retiro de Productos Terapéuticos (URPTG)].
Nota: Se puede encontrar más información sobre los requisitos australianos de avisos de aviso y
recuperación de dispositivos en https://www.tga.gov.au/recalls
Nota: Los patrocinadores australianos deben proporcionar a los fabricantes cualquier información
que ayude al fabricante a cumplir con las obligaciones de un procedimiento de evaluación de la
MDSAP AU P0002.005 73 Página
conformidad (por ejemplo, información relacionada con la recuperación de dispositivos) [TG (MD) R
Reg 5.8].
Brasil (ANVISA):
Verificar que los procedimientos y flujos de trabajo se establecieron para identificar cuándo son
necesarias las acciones de campo (retiros y correcciones), de acuerdo con el sistema de calidad y
sistema de vigilancia post-mercado de la organización [RDC ANVISA 67/2009 -Art. 6º; RDC
ANVISA 23/2012 – Art. 1º, Art. 5º].
Verificar que la organización de Dispositivos Médicos conserve registros sobre las acciones de
campo realizadas, incluidas aquellas que no necesitan ser informadas a las autoridades
regulatorias [RDC ANVISA 23/2012 – Art. 4º; Art. 6º, Art. 10, Art. 11, Art. 16].
Para los fabricantes nacionales (también se aplica a los representantes legales en Brasil): verificar
que la organización ha enviado a la autoridad regulatoria los informes solicitados, según la
regulación brasileña [RDC ANVISA 23/2012– Art. 10, Art. 11].
Verificar que la organización de Dispositivos Médicos haya realizado acciones de campo basadas
en evidencia potencial o concreta de que su producto no cumple con los requisitos esenciales de
seguridad y efectividad [RDC ANVISA 23/2012 – Art. 4º, Art. 6º, Art. 7º, Art. 13, Art. 14, Art. 15].
Para los fabricantes nacionales (también se aplica a los representantes legales en Brasil): verificar
que la organización de Dispositivos Médicos haya realizado acciones de campo cuando lo requiera
la autoridad regulatoria [RDC ANVISA 23/2012 – Art. 6º].
Para los fabricantes nacionales (también se aplica a los representantes legales en Brasil): verificar
que la organización notificó a la autoridad regulatoria sobre las acciones de campo, de acuerdo con
los requisitos y plazos establecidos por la normativa brasileña [RDC ANVISA 23/2012 – Art. 7º, Art.
8º].
Para los fabricantes internacionales, verificar que el representante legal en Brasil conocía la
ocurrencia de acciones de campo realizadas en productos exportados a Brasil [RDC ANVISA
67/2009 – Art. 8º].
Canadá (HC):
Reglamentaciones de Dispositivos Médicos SOR / 98-282, Sección 63 - 65.1:
Verificar que el fabricante y el importador de un dispositivo médico, en o antes de realizar un retiro
del mercado de un dispositivo, proporcionen al ministerio la siguiente información [CMDR 64]:
a) el nombre del dispositivo y su identificador, incluido el identificador de cualquier dispositivo
médico que sea parte de un sistema, kit de prueba, grupo de dispositivos médicos, familia
de dispositivos médicos o familia de grupo de dispositivos médicos;
b) el nombre y la dirección del fabricante e importador, y el nombre y la dirección del
establecimiento donde se fabricó el dispositivo, si es diferente de la del fabricante;
c) el motivo del retiro, la naturaleza del defecto o posible defecto y la fecha y circunstancias
bajo las cuales se descubrió el defecto o posible defecto;
d) una evaluación del riesgo asociado con la defectuosidad o posible defecto;
e) el número de unidades afectadas del dispositivo que el fabricante o importador:
i. fabricó en Canadá,
ii. importó a Canadá, y
iii. vendió en Canadá.
MDSAP AU P0002.005 74 Página
f) el período durante el cual el fabricante o importador distribuyó las unidades afectadas del
dispositivo en Canadá;
g) el nombre de cada persona a quien el fabricante o importador le vendió el dispositivo
afectado y la cantidad de unidades del dispositivo vendidas a cada persona;
h) una copia de cualquier comunicación emitida con respecto al retiro;
i) la estrategia propuesta para llevar a cabo el retiro, incluida la fecha para comenzar el retiro,
información sobre cómo y cuándo se informará al Ministerio del progreso del retiro y la
fecha propuesta para su finalización;
j) la acción propuesta para prevenir una recurrencia del problema; y
k) el nombre, el título y el número de teléfono del representante del fabricante o importador
para contactarse con respecto a cualquier información relacionada con el retiro.
Verificar que tan pronto como sea posible después de la finalización del retiro, el fabricante y el
importador informen al ministerio los resultados del retiro y la acción tomada para prevenir una
recurrencia del problema [CMDR 65].
Si los informes requeridos por las secciones 64 y 65 son presentados al Ministerio por el
importador, verificar que el fabricante haya informado al Ministerio por escrito que los informes que
el fabricante y el importador presentarían son idénticos y que el fabricante ha permitido que el
importador prepare y presente informes al Ministerio en nombre del fabricante [CMDR 65.1].
Japón (MHLW):
Los titulares de la autorización de comercialización deben reportar avisos de notificación a las
autoridades regulatorias [Ley 6811 de PMD].
Confirmar que la persona que opera el sitio de fabricación registrado ha determinado e
implementado un acuerdo efectivo para comunicarse con el titular de la autorización de
comercialización en relación con los avisos de notificación [MHLW MO169: 29].
Nota: Las personas que operan en los Sitios de fabricación registrados no están obligadas a
informar directamente a la autoridad regulatoria ningún aviso de notificación, sino que deben
comunicarse con el titular de la autorización de comercialización para que puedan tomar las
medidas reglamentarias necesarias.
Estados Unidos (FDA):
21 CFR 806: Dispositivos médicos; Informes de correcciones y eliminaciones.
Verificar que el fabricante tenga un proceso implementado para notificar a la FDA en el caso de
acciones relacionadas con correcciones y remociones de dispositivos y para mantener registros de
esas correcciones y eliminaciones.
Verificar que el informe escrito a la FDA de cualquier corrección o remoción iniciada para reducir un
riesgo para la salud o remediar una violación de la Ley de Alimentos, Medicamentos y Cosméticos
de EE.UU., se informa dentro de los 10 días hábiles posteriores al inicio de la corrección o
eliminación. Confirmar que el informe contiene el identificador de dispositivo único (UDI, por sus
siglas en inglés) que aparece en la etiqueta del dispositivo o en el paquete del dispositivo, o el
identificador del dispositivo, código de producto universal (UPC, por sus siglas en inglés), modelo,
catálogo o número de código del dispositivo y el lote de fabricación o número de serie del
dispositivo u otro número de identificación.
Confirmar que el fabricante mantiene registros de cualquier corrección y eliminación que no sea
necesario informar a la FDA (por ejemplo, correcciones y remociones realizadas para corregir una
infracción menor de la Ley de Alimentos, Medicamentos y Cosméticos de EE. UU., o sin riesgo
para la salud). Confirmar que los registros de correcciones y eliminaciones que no se deben
MDSAP AU P0002.005 75 Página
informar contienen el identificador único de dispositivo (UDI, por sus siglas en inglés) que aparece
en la etiqueta del dispositivo o en el paquete del dispositivo, o el identificador del dispositivo, código
de producto universal (UPC, por sus siglas en inglés), modelo, catálogo o código número del
dispositivo y el lote de fabricación o número de serie del dispositivo u otro número de identificación.
Enlaces:
Medición, Análisis y Mejora
Las correcciones y eliminaciones son indicativas de que el producto o proceso no cumple con los
requisitos especificados o los resultados planificados y la no conformidad no fue detectada antes
de la distribución. Cuando no se cumplen los requisitos especificados o los resultados planificados,
se deben tomar medidas correctivas y correctivas según sea necesario.
Durante la auditoría del proceso de Medición, Análisis y Mejora, confirmar que la organización haya
tomado una corrección apropiada con respecto a los dispositivos ya distribuidos, y haya tomado las
medidas correctivas apropiadas para evitar la recurrencia de la (s) afección (es) que causó la no
conformidad.
Capítulo 5: Diseño y Desarrollo
El propósito del proceso de Diseño y Desarrollo es controlar el proceso de diseño y asegurar que
los dispositivos satisfagan las necesidades del usuario, los usos previstos y los requisitos
especificados. Atención a la planificación de diseño y desarrollo, identificando entradas de diseño,
desarrollando salidas de diseño, verificando que las salidas de diseño cumplan con las entradas de
diseño, validando el diseño, controlando los cambios de diseño, revisando los resultados de
diseño, transfiriendo el diseño a producción y compilando los registros apropiados. asegurar que
los diseños resultantes satisfagan las necesidades del usuario, los usos previstos y los requisitos.
MDSAP AU P0002.005 76 Página
El representante de la dirección es responsable de garantizar que los requisitos del sistema de
gestión de la calidad se hayan definido, documentado, implementado y mantenido efectivamente.
Antes de la auditoría de cualquier proceso, entrevistar al representante de la dirección (o persona
designada) para obtener una descripción general del proceso y una idea del conocimiento por parte
de la dirección, así como el entendimiento del proceso.
La auditoría del proceso de Diseño y Desarrollo seguirá a la auditoría del proceso de Medición,
Análisis y Mejora según la secuencia de auditoría de MDSAP. La información sobre las no
conformidades del producto o del sistema de calidad observadas durante la auditoría del proceso
de Medición, Análisis y Mejora debe ser considerada al tomar decisiones sobre los proyectos de
diseño y desarrollo, incluyendo cambios de diseño resultantes de acciones correctivas, para ser
revisados durante la auditoría del proceso de Diseño y Desarrollo.
La revisión del proceso de Diseño y Desarrollo también brindará la oportunidad de evaluar cómo la
organización ha utilizado las actividades de gestión de riesgos para garantizar que las aportaciones
del diseño sean integrales y satisfagan las necesidades del usuario, para confirmar que las
medidas de control de riesgos que se planificaron se implementaron en el diseño; para verificar que
las medidas de control de riesgo sean efectivas para controlar o reducir el riesgo.
Además, la revisión de las actividades de diseño y desarrollo ayudará al equipo de auditoría
durante la auditoría del proceso de Compras de la organización porque el o los auditores tienen la
oportunidad de seleccionar proveedores para su revisión cuyas actividades están asociadas con un
mayor riesgo para el producto o cuyas actividades son críticas a los productos de diseño
esenciales. La revisión de las actividades de diseño y desarrollo también proporciona información
para ayudar al equipo de auditoría a realizar una evaluación final del proceso de gestión al finalizar
la auditoría.
Auditando el Proceso de Diseño y Desarrollo
Propósito: El objetivo de la auditoría del proceso de Diseño y Desarrollo es verificar que la
organización de Dispositivos Médicos establezca, documente, implemente y mantenga controles
para garantizar que los dispositivos médicos satisfagan las necesidades del usuario, los usos
previstos y los requisitos especificados.
Resultados: Como resultado de la auditoría del proceso de Diseño y Desarrollo, la evidencia
objetiva mostrará si la organización de Dispositivos Médicos ha:
A) Definido, documentado e implementado procedimientos para asegurar que los dispositivos
médicos son diseñados de acuerdo a los requerimientos especificados.
B) Planeado efectivamente el diseño y desarrollo de un dispositivo.
C) Establecido mecanismos, incluida la revisión sistemática, para abordar requisitos
incompletos, ambiguos o conflictivos.
D) Determinado los requisitos impuestos internamente o externamente para la seguridad, la
función y el rendimiento para el uso previsto, incluidos los requisitos regulatorios, la gestión
de riesgos y los requisitos de factores humanos.
E) Verificado que las salidas de diseño satisfacen los requisitos de entrada de diseño.
F) Identificado y mitigado, en la medida de lo posible, los riesgos asociados con el dispositivo,
incluido el software del dispositivo.
G) Asegurado de que los cambios en el diseño del dispositivo están controlados, los riesgos
asociados con el cambio de diseño se identifican y mitigan, en la medida de lo posible, y
que el dispositivo continuará funcionando según lo previsto.
H) Realizado la validación del diseño para asegurar que los dispositivos se ajusten a las
necesidades del usuario y el uso previsto.
MDSAP AU P0002.005 77 Página
I) Confirmado que el diseño está correctamente traducido a métodos y procedimientos de
producción.
Enlaces a otros procesos:
Compras; Controles de Producción y Servicio; Medición, Análisis y Mejora; Autorización de
Comercialización de Dispositivos y Registro de Instalación
Tarea 1 – Identificación de Dispositivos sujetos a Procedimientos de Diseño
y Desarrollo; Documentación Técnica
Verificar que se hayan identificado aquellos dispositivos que, por reglamento, están sujetos
a procedimientos de diseño y desarrollo. (Ver Anexo 1).
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.1.1, 4.2.1, 7.1, 7.3.10;
TGA: TG(MD)R Regs Division 3.2;
MHLW/PMDA: MO169:5, 6, 26;
FDA: 21 CFR 820.30(a)
Requisitos adicionales específicos del país:
Australia (TGA):
Cuando un fabricante aplica TG(MD)R Regs Division 3.2 y selecciona los procedimientos de
evaluación de la conformidad de Aseguramiento de Calidad Total [TG (MR) R Apéndice 3, Parte1],
los procedimientos para el diseño y desarrollo deben estar disponibles.
Además, para todas las clases de dispositivos, debe seguirse la orientación proporcionada para la
auditoría de la documentación técnica en el Anexo 1 a fin de garantizar la disponibilidad de pruebas
objetivas que demuestren el cumplimiento de los Principios Esenciales de Seguridad y
Rendimiento.
Brasil (ANVISA):
De acuerdo con las legislaciones brasileñas, no hay excepción al control de diseño.
Si las actividades de diseño se subcontratan, verificar que el fabricante tenga un registro maestro
de dispositivo completo para el dispositivo y registros de la transferencia de diseño a la producción
[RDC ANVISA 16/2013: 4.1.7, 4.2].
Canadá (HC):
Con respecto a los dispositivos de Clase II que no están sujetos a controles de Diseño y Desarrollo,
verificar que el fabricante tenga evidencia objetiva para establecer que los dispositivos de Clase II
cumplen con los requisitos de seguridad y efectividad de la sección 10 a 20 [CMDR 9, 10 a 20].
Japón (MHLW):
Los dispositivos de clase 1 no están obligados a cumplir con los requisitos de MHLW MO169: 30-
36, que son equivalentes al requisito de diseño y desarrollo en ISO13485 [MHLW MO169: 4.1].
Evaluación de la conformidad:
MDSAP AU P0002.005 78 Página
Ausencia de actividad de diseño
El equipo de auditoría puede encontrar situaciones en las que la organización de Dispositivos
Médicos no ha completado ningún proyecto de diseño, no tiene proyectos de diseño en curso o
planificados, y no ha realizado ningún cambio de diseño (es decir, no ha habido actividad de
diseño). Como mínimo, verificar que la organización de Dispositivos Médicos mantenga un
procedimiento de cambio de diseño definido y documentado. Una organización de Dispositivos
Médicos también puede haber definido y documentado otros procedimientos de control de diseño.
Para ese tipo de organización de Dispositivos Médicos, una organización de Dispositivos Médicos
sin actividad de diseño, que no incluye cambios de diseño, evaluar los procedimientos que la
organización de Dispositivos Médicos ha implementado. El equipo de auditoría puede proceder a la
auditoría del siguiente proceso.
Actividades de diseño subcontratadas
En los casos en que las actividades de diseño (desarrollo y cambios) sean completamente
subcontratadas por la organización de Dispositivos Médicos, el equipo auditor debe verificar (como
mínimo) que los controles y registros relacionados con la transferencia de diseño a producción han
sido determinados y que la línea de producción implementada en el sitio del fabricante cumple con
los requisitos de producción establecidos durante el diseño y desarrollo del dispositivo.
En estos casos, la organización de Dispositivos Médicos deberá asegurarse de que el
subcontratista cumpla con los requisitos de diseño y desarrollo, establecidos por - Sistemas de
gestión de calidad - Dispositivos médicos - Requisitos para fines regulatorios (ISO 13485:2016), los
requisitos del Sistema de gestión de calidad de la Evaluación de conformidad Procedimientos de
las Regulaciones de Bienes Terapéuticos Australianos (Dispositivos Médicos) (TG (MD) R Sch3),
Buenas Prácticas de Fabricación Brasileñas (RDC ANVISA 16/2013), Ordenanza QMS Japonesa
(MHLW MO 169), Regulación del Sistema de Calidad (21 CFR Parte 820) y cualquier otro requisito
específico de las autoridades regulatorias de dispositivos médicos que participen en el programa
MDSAP.
Enlaces
Compras
Si la organización de Dispositivos Médicos subcontrata actividades de diseño y desarrollo, o
cualquier parte del diseño y desarrollo, confirmar que la organización de Dispositivos Médicos trata
a la organización subcontratada como proveedor, ha calificado adecuadamente y mantiene el
control del proveedor, comunica los requisitos al proveedor, incluidos los requisitos regulatorios, y
tiene arreglos para verificar que las actividades de diseño y desarrollo satisfagan esos requisitos.
Tarea 2 – Selección de un Proyecto Completo de Diseño y Desarrollo
Seleccione un proyecto de diseño y desarrollo completo (cuando corresponda) para su
revisión.
Criterios de prioridad para la selección:
1. Quejas o problemas conocidos con un dispositivo en particular.
2. Riesgo del producto.
3. Cambios de diseño recientes, en particular cambios de diseño realizados para corregir
problemas de calidad asociado con el diseño del dispositivo
4. Edad de diseño (preferir la más reciente).
5. Diseños que no han sido auditados recientemente.
MDSAP AU P0002.005 79 Página
Enlaces
Medición, Análisis y Mejora
En este punto de la auditoría, el equipo de auditoría ya habrá revisado el proceso de Medición,
Análisis y Mejora. Si los auditores notaron acciones correctivas que resultaron en cambios de
diseño, o notaron las no conformidades del producto que se han atribuido al diseño del dispositivo,
el equipo de auditoría debería considerar seleccionar esos diseños para su revisión.
El equipo de auditoría debe ser particularmente consciente de cómo los problemas de calidad
identificados del proceso de Medición, Análisis y Mejora están relacionados con aspectos
específicos del diseño y desarrollo del dispositivo. Por ejemplo, si los auditores revisan quejas
relacionadas con una característica de seguridad del dispositivo que no funciona según lo previsto,
el equipo de auditoría debe considerar seleccionar para revisar la verificación de diseño de esa
característica de seguridad y determinar si se confirmaron métodos de control de riesgo efectivos.
Tarea 3 – Planeación de Diseño y Desarrollo
Verificar que el proceso de diseño y desarrollo esté planificado y controlado.
Revisar el plan de diseño para el proyecto de diseño y desarrollo seleccionado para
comprender las actividades de diseño y desarrollo; incluyendo las etapas de diseño y
desarrollo, las actividades de revisión, verificación, validación y transferencia de diseño que
son apropiadas en cada etapa; y la asignación de responsabilidades, autoridades e
interfaces entre los diferentes grupos involucrados en el diseño y desarrollo.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 7.1, 7.3.2;
TGA: TG(MD)R Sch3 P1 Cl 1.4(4) &(5)(c);
ANVISA: RDC ANVISA 16/2013: 4.1.2, 4.1.11;
MHLW/PMDA: MO169: 6, 26, 30;
FDA: 21 CFR 820.30(b), 820.30(j)
Requisitos adicionales específicos del país:
Australia (TGA):
Verificar que la planificación efectiva para el diseño y desarrollo esté documentada, generalmente
como parte de un Plan de Calidad [TG(MD)R Sch3 P1 Cl 1.4(4)].
Canadá (HC):
Verificar que los fabricantes de dispositivos de Clase IV mantengan un plan de calidad que
establezca las prácticas de calidad específicas, los recursos y la secuencia de actividades
relevantes para el dispositivo [CMDR 32].
Evaluación de la conformidad:
Revisión del Plan de Diseño
Revisar el plan de diseño para el proyecto seleccionado para comprender el diseño del diseño y
actividades de desarrollo, incluidas las responsabilidades e interfaces asignadas.
El plan de diseño del proyecto seleccionado puede ser utilizado por el equipo auditor como una
hoja de ruta para la revisión del proyecto.
MDSAP AU P0002.005 80 Página
Los planes pueden variar según el tipo o el tamaño del proyecto. Algunos planes de diseño se
pueden expresar como diagramas de flujo simples, o para proyectos más grandes, se pueden usar
Gantt o gráficos de técnicas de evaluación de programas (PERT). Los planes no tienen que
mostrar las fechas de inicio o finalización de las actividades cubiertas. Sin embargo, los planes
deben definir la responsabilidad de la implementación del diseño y las actividades de desarrollo y
describir las interfaces con diferentes grupos o actividades.
Esperar ver la interacción entre los departamentos de investigación y desarrollo, marketing,
regulación, fabricación y calidad. El equipo de auditoría también podría ver una interfaz con las
compras, los instaladores y los servidores. Cuando las instituciones externas (por ejemplo,
universidades o centros de investigación y desarrollo) participan en las actividades de diseño y
desarrollo, también deben definirse las interfaces entre la organización de Dispositivos Médicos y
esas instituciones externas.
Los planes de diseño y desarrollo pueden cambiar mientras evoluciona el proceso de diseño y
desarrollo; sin embargo, todos los cambios en el plan deben estar documentados y aprobados.
Enlaces
Ninguno
Tarea 4 – Implementación del Proceso de Diseño y Desarrollo
Para los registros de diseño y desarrollo del dispositivo seleccionados, verifique que los
procedimientos de diseño y desarrollo se hayan establecido y aplicado.
Confirmar que los procedimientos de diseño y desarrollo abordan las etapas de diseño y
desarrollo, revisión, verificación, validación, transferencia de diseño y cambios de diseño.
Cláusula y Regulación:
ISO: ISO 13485: 2016: 4.2.1, 7.3.1, 7.3.10;
TGA: TG (MD) R Sch3 P1 Cl 1,4 (4) y (5) (c);
ANVISA: RDC ANVISA 16/2013: 4.1.1;
MHLW/PMDA: MO169: 6, 30;
FDA: 21 CFR 820.30 (a), 820.30 (j)
Requisitos adicionales específicos del país:
Estados Unidos (FDA):
Verificar que los procedimientos de entrada de diseño contengan un mecanismo para abordar los
requisitos incompletos, ambiguos o conflictivos [21 CFR 820.30 (c)].
Evaluación de la conformidad:
Revisión de procedimientos
Los procedimientos de diseño y desarrollo establecen la estructura, proporcionan el marco y
respaldan el proceso de Diseño y Desarrollo de la organización de Dispositivos Médicos. El
objetivo de auditar los procedimientos es determinar si la organización cuenta con ese marco. Si
los procedimientos no han sido definidos y documentados, o son deficientes, los dispositivos de la
organización pueden no satisfacer las necesidades del usuario y el uso previsto.
Al realizar esta tarea de auditoría, el equipo de auditoría debe revisar los procedimientos de la
organización y verificar que los procedimientos satisfagan los requisitos de los dispositivos
médicos: - Sistemas de gestión de calidad - Dispositivos médicos - Requisitos para fines
MDSAP AU P0002.005 81 Página
regulatorios (ISO 13485: 2016), los requisitos del Sistema de gestión de calidad de la Evaluación
de conformidad Procedimientos de las Regulaciones de Bienes Terapéuticos Australianos
(Dispositivos Médicos) (TG (MD) R Sch3), Buenas Prácticas de Fabricación Brasileñas (RDC
ANVISA 16/2013), Ordenanza QMS Japonesa (MHLW MO 169), Regulación del Sistema de
Calidad (21 CFR Parte 820) y cualquier otro requisito específico de las autoridades regulatorias de
dispositivos médicos que participen en el programa MDSAP. Por ejemplo:
Verificar que el procedimiento de entrada de diseño incluye un mecanismo para abordar
requisitos incompletos, ambiguos o conflictivos.
Verificar que el procedimiento de salida asegura que se identifiquen las salidas esenciales.
Verificar que el procedimiento de revisión de diseño garantiza que cada revisión de diseño
incluya a una persona que no tenga responsabilidad por la etapa de diseño que se está
revisando.
Requerimiento Mínimo
Si la organización de Dispositivos Médicos no tiene proyectos de diseño en curso o planificados, no
ha realizado ningún cambio de diseño, asegurar que, como mínimo, la organización de Dispositivos
Médicos mantenga procedimientos de cambio de diseño definidos y documentados.
Enlaces
Ninguno
Tarea 5 – Entrada de Diseño y Desarrollo
Verificar que las entradas de diseño y desarrollo se establecieron, revisaron y aprobaron; y
que abordan los requisitos funcionales, de rendimiento y seguridad del cliente, el uso
previsto, los requisitos regulatorios aplicables y otros requisitos, incluidos los que surgen
de factores humanos, esenciales para el diseño y el desarrollo.
Verificar que cualquier riesgo y medida de mitigación de riesgos identificados durante el
proceso de gestión de riesgos se usen como una entrada en el proceso de diseño y
desarrollo.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 5.2, 7.2.1, 7.3.3, 8.2.1;
TGA: TG(MD)R Sch1 P1 2, Sch3 P1 Cl 1.4(2) &(5)(c), Sch 3 P1 1.4(3)(a) &(b)
ANVISA: RDC ANVISA 16/2013: 2.4, 4.1.3, 4.1.11;
HC: CMDR 10-20, 21-23, 66, 67,68;
MHLW/PMDA: MO169: 6, 11, 27, 31;
FDA: 21 CFR820.30(c), 820.30(g)
Requisitos adicionales específicos del país:
Australia (TGA):
Verificar que el fabricante haya identificado los Principios Esenciales relevantes que se aplican al
dispositivo médico [TG (MD) R Sch1 Essential Principles].
Verificar que el fabricante haya tenido en cuenta los comentarios de posproducción como una
entrada para monitorear y mantener los requisitos del producto y mejorar los procesos de
realización del producto.
Estados Unidos (FDA):
MDSAP AU P0002.005 82 Página
Para el (los) dispositivo (s) seleccionado (s), verifique que la organización tenga el permiso de
comercialización [510 (k)] apropiado o la aprobación previa al mercado (PMA, por sus siglas en
inglés) si distribuye los dispositivos en los Estados Unidos [21 CFR 807].
Evaluación de la conformidad:
Entradas de diseño
Las entradas son los requisitos físicos y de rendimiento de un dispositivo que se utilizan como base
para el diseño del dispositivo. Las entradas deben ser documentadas y aprobadas por el personal
apropiado. El equipo auditor debe revisar las fuentes utilizadas para desarrollar las entradas y
determinar que los aspectos relevantes de los requisitos para el dispositivo fueron cubiertos. Estas
fuentes deben incluir las regulaciones relevantes donde se han definido los criterios de seguridad y
rendimiento (por ejemplo, requisitos de seguridad y eficacia o Principios Esenciales de Seguridad y
Rendimiento). Los ejemplos de aspectos relevantes incluyen:
el uso previsto, las características de rendimiento
el usuario previsto
la mitigación de riesgos
la biocompatibilidad, la compatibilidad con el entorno de uso previsto (incluida la
compatibilidad electromagnética)
el software
la protección radiológica
los factores humanos
la esterilidad.
Las organizaciones deben tener en cuenta el pensamiento actual de los expertos donde la
información publicada está disponible (por ejemplo, Estándares).
Los insumos de diseño también pueden relacionarse con los procesos de fabricación, en particular
donde se requiere la validación, revalidación, el monitoreo periódico de los parámetros críticos del
proceso o la implementación de controles específicos para asegurar la calidad del producto (por
ejemplo, esterilización, moldeo por inyección, control en la fuente o inactivación de agentes
transmisibles en materiales de origen animal o controles de BPF en la manipulación,
procesamiento o incorporación de una sustancia medicinal en un dispositivo médico).
Las entradas de diseño son la base de la verificación y validación del diseño; por lo tanto, las
entradas de diseño deben definirse y registrarse como requisitos formales que permitan la
confirmación de las salidas de diseño.
La información relevante para el diseño de entrada también puede provenir de datos de
postproducción o experiencia de dispositivos similares. Las quejas y los eventos adversos forman
un sistema de retroalimentación que puede ayudar a mejorar la calidad en los diseños nuevos y los
cambios en los diseños actuales.
Enlaces
Autorización de Comercialización de Dispositivos y Registro de Instalación
MDSAP AU P0002.005 83 Página
Confirmar que la organización de Dispositivos Médicos ha considerado los requisitos regulatorios
para el registro, listado, notificación y licencia; y ha cumplido con estos requisitos antes de
comercializar el dispositivo en las jurisdicciones regulatorias aplicables.
Tarea 6 – Integridad, Coherencia y Falta de Ambigüedad de la Entrada de
Diseño y Desarrollo
Confirmar que las entradas de diseño y desarrollo sean completas, no ambiguas y que no
entren en conflicto entre sí.
Cláusula y Regulación:
ISO: ISO 13485:2016: 7.3.3;
TGA: TG(MD)R Sch 3 Part 1.4(4),
ANVISA: RDC ANVISA 16/2013: 4.1.3;
MHLW MO169: 31; 21 CFR820.30(c)
Requisitos adicionales específicos del país:
Australia (TGA):
Confirmar que las entradas de diseño incluyen los Principios Esenciales relevantes [TG (MD) R -
Schedule 1].
Las soluciones adoptadas por el fabricante para el diseño y la construcción de un dispositivo
médico deben ajustarse a los principios de seguridad que se derivan del estado de la técnica
generalmente reconocido. [TG (MD) R - Sch 1 - EP2]. Los principios de seguridad generalmente se
identifican en normas reconocidas internacionalmente.
El cumplimiento de un estándar determinado no es obligatorio según la legislación australiana; sin
embargo, es una forma de demostrar el cumplimiento de los Principios Esenciales.
La TGA presumirá el cumplimiento de los Principios Esenciales relevantes si el Fabricante ha
aplicado, en su totalidad, un estándar relevante identificado en una Orden de Estándares de
Dispositivos Médicos. (Consultar el sitio web de TGA, por ejemplo, ISO 10993).
Si las normas relevantes no se han identificado como entradas de diseño, asegúrese de que el
fabricante haya documentado una justificación para explicar por qué se han aplicado alternativas
para demostrar el cumplimiento de los Principios Esenciales [TG (MD) R Sch3 Part 1.4 (5) (c) (iii)
(C)].
Evaluación de la conformidad:
Entradas de Diseño
Las entradas de diseño deben definirse y registrarse como requisitos verificables, aprobados por el
personal apropiado. Si la organización no cuenta con entradas de diseño precisas y completas, el
diseño final puede no satisfacer las necesidades del usuario y el uso previsto.
Un método común para que una organización confirme que las entradas de diseño para un
proyecto de diseño y desarrollo son completas, no ambiguas y que no están en conflicto entre sí es
realizar una revisión del diseño después de que se determinen los requisitos iniciales.
Enlaces
MDSAP AU P0002.005 84 Página
Ninguno
Tarea 7 – Salida de Diseño y Desarrollo y Verificación del Diseño
Revisar las especificaciones del dispositivo médico para confirmar que las salidas de
diseño y desarrollo sean rastreables y satisfagan los requisitos de entrada del diseño.
Verificar que se hayan identificado los productos de diseño y desarrollo esenciales para el
correcto funcionamiento del dispositivo médico.
Las salidas incluyen, pero no se limitan a:
especificaciones del dispositivo
especificaciones del proceso de fabricación
especificaciones del proceso de esterilización (si corresponde)
las pruebas de aseguramiento de calidad
etiquetado y el empaque del dispositivo.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 4.2.3, 7.3.4;
TGA: TG(MD)R Sch3 P1 Cl 1.4(5)(c);
ANVISA: RDC ANVISA 16/2013: 4.1.5, 4.1.4, 4.1.11;
MHLW/PMDA: MO169: 6, 32;
FDA: 21 CFR 820.30(d), 820.30(f)
Requisitos adicionales específicos del país:
Australia (TGA):
Si no se han aplicado las normas pertinentes, o no se han aplicado en su totalidad, asegurar que el
fabricante haya documentado una justificación para explicar por qué se han aplicado métodos
alternativos para demostrar el cumplimiento de los Principios Esenciales [TG (MD) R Sch3 Parte
1.4 (5) (c) (iii) (C)].
Para los dispositivos que incorporan una sustancia medicinal, verifique que la documentación
también identifique los datos que se derivarán de las pruebas realizadas en relación con la
sustancia y su interacción con el dispositivo [TG (MD) R Sch 3 Part 1.4 (5) (c) (v)].
Evaluación de la conformidad:
Salidas del Diseño
Los resultados del diseño son los productos de trabajo o entregables de una etapa de diseño. Los
resultados del diseño pueden incluir documentos como diagramas, dibujos, especificaciones y
procedimientos tanto para productos como para procesos. Las salidas de una etapa pueden
convertirse en entradas para la siguiente etapa. El resultado total del diseño terminado consta de
las especificaciones del dispositivo, su embalaje y etiquetado (incluidas las tarjetas de implante y
los folletos, cuando corresponda), los requisitos del sistema de gestión de la calidad, el proceso de
fabricación y, si procede, los requisitos de instalación y mantenimiento.
MDSAP AU P0002.005 85 Página
Durante esta etapa de diseño, se puede producir una gran cantidad de registros o resultados. Solo
deben conservarse las salidas aprobadas. Sin embargo, si una organización de dispositivos
médicos opta por conservar otros registros, con fines históricos o de otro tipo, puede hacerlo.
Salidas Esenciales
Se deben identificar las salidas que son esenciales para el correcto funcionamiento del dispositivo.
Normalmente, una organización de dispositivos médicos puede utilizar una herramienta de gestión
de riesgos para determinar los resultados esenciales. Para verificar que esto se haya hecho, el
auditor o los auditores pueden revisar el proceso de la organización de dispositivos médicos para
determinar cómo se identificaron los resultados esenciales y si se hizo de acuerdo con sus
procedimientos de diseño de resultados.
La identificación de productos esenciales puede influir en otras actividades del sistema de calidad.
Por ejemplo, el establecimiento de controles y tolerancias del proceso de fabricación, el grado de
controles de compra y las actividades de aceptación aplicadas a un proveedor o la prioridad y
profundidad de una investigación de fallas pueden verse influenciadas por si el componente
(ensamblaje, material, etc.) se considera una salida imprescindible para el correcto funcionamiento
del dispositivo.
Salidas de diseño para dispositivos estériles
El diseño y desarrollo de dispositivos médicos destinados a ser estériles debe garantizar la
compatibilidad del proceso de esterilización con el dispositivo, la compatibilidad del embalaje del
dispositivo y el proceso de esterilización, la capacidad del dispositivo para ser esterilizado o re
esterilizado, y (si corresponde), justificación para agregar el dispositivo a una familia de productos
cubierta por un proceso de esterilización validado.
Verificación de diseño
En la verificación de diseño, la organización de Dispositivos Médicos obtiene evidencia objetiva (es
decir, datos) de que los productos de diseño cumplen con las entradas de diseño. Una
organización de Dispositivos Médicos genera esta evidencia objetiva realizando actividades de
verificación tales como pruebas, mediciones y análisis. Estas actividades deben ser explícitas y
exhaustivas en su ejecución. Las actividades de verificación de una organización de Dispositivos
Médicos deben ser predictivas, no empíricas. En otras palabras, los criterios de aceptación deben
establecerse antes de la actividad de verificación. El establecimiento de criterios de aceptación
predeterminados se puede encontrar en un protocolo de verificación o documento similar. Durante
la revisión de las actividades de verificación del diseño, el auditor determinará si los datos de
verificación del diseño confirman que los productos de diseño cumplen con los requisitos de
entrada del diseño.
Técnicas de verificación
Los diseños complejos requerirán más y diferentes tipos de verificaciones que los diseños simples.
A veces, una organización de Dispositivos Médicos tiene que usar su propia experiencia para
desarrollar (en la empresa) una forma de verificar un aspecto particular de un diseño. Cualquier
enfoque seleccionado por una organización es aceptable siempre que proporcione evidencia
objetiva confiable de que el resultado cumplió con la entrada.
Elegir actividades de verificación para su revisión
Al llevar a cabo esta tarea de auditoría, seleccionar los registros generados a partir de las
actividades de verificación de diseño asociadas con una serie de entradas de diseño y productos
MDSAP AU P0002.005 86 Página
de diseño. La revisión de estos registros determinará si las salidas de diseño cumplen con los
requisitos de entrada de diseño. Cuando sea posible, seleccionar la documentación de las
actividades de verificación de diseño que están asociadas con productos que se consideran
esenciales para el correcto funcionamiento del dispositivo o están asociados con el mayor riesgo
para el usuario o el paciente.
Enlaces
Compras, Controles de Producción y Servicio
Durante la revisión de un proyecto de diseño, el equipo de auditoría debe tener en cuenta los
procesos de producción y los productos suministrados que son esenciales para el correcto
funcionamiento del dispositivo. Los procesos de producción pueden incluir no solo las instrucciones
de fabricación, sino también los controles internos, como el tipo y el alcance de las actividades de
aceptación, la calibración del equipo y los intervalos de mantenimiento, los controles ambientales y
los controles de personal. Para los proveedores que proporcionan productos y servicios
relacionados con las salidas de diseño esenciales, el grado de controles de compras necesarios es
acorde con el efecto del producto suministrado en el funcionamiento adecuado del dispositivo
terminado.
Durante las auditorías del proceso de Compras y del proceso de Controles de Producción y de
Servicio, el equipo de auditoría debe considerar revisar los procesos de producción y los productos
suministrados que tienen el mayor riesgo o el mayor efecto en los resultados de diseño esenciales.
Tarea 8 – Actividades de Gestión de Riesgos aplicadas a través del Proyecto
de Diseño y Desarrollo
Verificar que las actividades de gestión de riesgos estén definidas e implementadas para el
diseño y desarrollo de productos y procesos.
Confirmar que los criterios de aceptabilidad del riesgo se establezcan y cumplan a lo largo
del proceso de diseño y desarrollo.
Verificar que cualquier riesgo residual se evalúe y, cuando corresponda, se comunique al
cliente (por ejemplo, etiquetado, documentos de servicio, Notificaciones de Advertencia,
etc.).
Nota: En algunos casos, puede ser necesario que el fabricante realice un análisis de riesgo /
beneficio para justificar un riesgo que no puede mitigarse a un nivel aceptable. Además, puede
ser necesario auditar otros procesos (por ejemplo, controles de producción y servicio,
compras) para verificar que se cumplen los criterios de aceptabilidad del riesgo, se controla
o reduce el riesgo, y se comunica el riesgo residual si es necesario.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 7.1, 7.3.3, 7.3.4;
TGA: TG(MD)R Sch1 P1 2, Sch3 P1 Cl 1.4(5)(c)(iii);
ANVISA: RDC ANVISA 16/2013: 2.4, 4.1.11, RDC ANVISA 56/2001;
MDSAP AU P0002.005 87 Página
HC: CMDR 10, 11, 15, 16;
MHLW/PMDA: MO169: 6, 26, 31,32;
FDA: 21 CFR 820.30(g)
Requisitos adicionales específicos del país:
Brasil (ANVISA):
Verificar que el fabricante haya establecido y mantenga un proceso continuo de gestión de riesgos
que cubra todo el ciclo de vida del producto. Los posibles peligros deben identificarse tanto en
condiciones normales como de fallas, incluidas las que surgen de factores humanos. El riesgo
asociado con esos peligros se calculará. Los riesgos deben ser analizados, evaluados y
controlados, según sea necesario. Se evaluará la efectividad de los controles de riesgos
implementados [RDC ANVISA 56/2001, RDC ANVISA 16/2013: 2.4].
Estados Unidos (FDA):
Confirmar que el fabricante haya identificado los posibles peligros asociados con el dispositivo en
condiciones normales y de falla. Los riesgos asociados con los riesgos, incluidos los que resultan
de un error del usuario, deben calcularse en condiciones normales y de falla. Si se considera que
un riesgo es inaceptable, debe reducirse a niveles aceptables por los medios adecuados. Asegurar
de que los cambios en el dispositivo para eliminar o minimizar los riesgos no introducen nuevos
riesgos [21 CFR 820.30 (g); comentario de preámbulo 83].
Evaluación de la conformidad:
Gestión de riesgos
Cada organización de Dispositivos Médicos debe determinar cuánto riesgo es aceptable. El uso
real de cualquier dispositivo médico incluye alguna medida de riesgo para los usuarios o pacientes.
La determinación de un nivel aceptable de riesgo depende del uso previsto del dispositivo,
incluidos los problemas de salud específicos de la población de pacientes, la capacitación de los
usuarios involucrados y el entorno de uso. Por ejemplo, los pacientes pediátricos pueden tener
menos capacidad para detectar un mal funcionamiento del dispositivo. Un dispositivo utilizado por
los consumidores generalmente tiene menos supervisión médica que un dispositivo utilizado en un
entorno hospitalario. El objetivo de un programa de gestión de riesgos es garantizar que el
dispositivo sea tan seguro como sea posible y que la seguridad del dispositivo sea aceptable para
el uso previsto.
La administración efectiva de riesgos generalmente comienza en conjunto con el proceso de
diseño y desarrollo, continúa con la realización del producto, incluida la selección de proveedores,
y continúa hasta el momento en que se retira el producto. La gestión del riesgo debe iniciarse en
un punto temprano en el proceso de diseño y desarrollo. Esto incluye definir el uso previsto del
dispositivo, considerando el riesgo bajo uso normal y el mal uso razonablemente previsto.
Comenzar el proceso de gestión de riesgos después de que el diseño haya progresado más allá de
un punto donde las características razonables de mitigación de riesgos pueden incluirse en el
diseño puede conducir a dispositivos que no satisfacen las necesidades del cliente y los requisitos
de seguridad de la organización. Los registros de la gestión de riesgos deben demostrar que los
riesgos que se han identificado como inaceptables se han mitigado a un nivel aceptable.
MDSAP AU P0002.005 88 Página
Mitigación de riesgos
Hay una serie de mecanismos que se pueden utilizar para mitigar el riesgo del producto. Estos
mecanismos de mitigación de riesgos, en orden decreciente de efectividad, incluyen características
de seguridad inherentes en el diseño del dispositivo, medidas de protección en el diseño (por
ejemplo, alarmas) y notificaciones del usuario, (por ejemplo, advertencias etiquetadas).
Revisión de las actividades de gestión de riesgos
Durante la revisión del proyecto de diseño seleccionado, verifique que la gestión de riesgos se
inicie al principio del proceso de diseño y desarrollo. Confirmar que el proceso de gestión de
riesgos de la organización de Dispositivos Médicos implica la evaluación, el control y el monitoreo
proactivos del riesgo del producto, seguido de la respuesta reactiva a los datos de calidad que
indican un riesgo del producto nuevo o cambiante.
Enlaces
Ninguno
Tarea 9 – Verificación de Diseño o Validación de Diseño para Confirmar la
Efectividad de las Medidas de Control de Riesgo
Confirmar que la verificación del diseño y / o la validación del diseño incluye garantías de
que las medidas de control de riesgos son eficaces para controlar o reducir el riesgo.
Cláusula y Regulación:
ISO: ISO 13485:2016: 7.1, 7.3.6, 7.3.7;
TGA: TG(MD)R Sch1 P1 2, Sch3 P1 Cl 1.4(5)(c);
ANVISA: RDC ANVISA 16/2013: 2.4, 4.1.4, 4.1.8, 4.1.11;
HC: CMDR 10,11, 15, 16;
MHLW/PMDA: MO169: 26, 34, 35;
FDA: 21 CFR 820.30(f), 820.30(g)
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Verificación de las medidas de control de riesgos
Durante la revisión de las actividades de verificación de diseño para el proyecto de diseño elegido,
confirmar que las medidas de control de riesgo identificadas sean realmente efectivas para reducir
o controlar el riesgo. Por ejemplo, un diseño para un tubo de alimentación enteral puede tener un
conector único para evitar la posibilidad de una conexión incorrecta con otros tipos de dispositivos,
como los catéteres de succión. La verificación del diseño debe mostrar que es difícil o imposible
conectar dispositivos no relacionados al tubo de alimentación enteral.
Enlaces
Ninguno
MDSAP AU P0002.005 89 Página
Tarea 10 – Validación de Diseño
Verificar que los datos de validación de diseño y desarrollo muestran que el diseño
aprobado cumple con los requisitos para la aplicación especificada o los usos previstos.
Verificar que la prueba de validación de diseño se ajuste de acuerdo con la naturaleza y el
riesgo del producto y el elemento que se validan.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 7.3.7;
TGA: TG(MD)R Sch1 P1 2; Sch3 P1 Cl1.4(5)(d);
ANVISA: RDC ANVISA 16/2013: 2.4, 4.1.8, 4.1.11;
HC: CMDR 12, 18, 19; MHLW MO169: 6, 35;
FDA: 21 CFR 820.30(g)
Requisitos adicionales específicos del país:
Australia (TGA):
Para los dispositivos que contienen material sensible a la temperatura, las condiciones ambientales
deben considerarse para los requisitos específicos del país. Por ejemplo, las muestras de prueba
deben acondicionarse según ISTA 2A para cubrir la zona climática australiana (rango de
temperatura extrema -29°C-50°C) para la validación del empaque.
Evaluación de la conformidad:
Validación de diseño
La validación del diseño se realiza para proporcionar evidencia objetiva de que las especificaciones
de diseño (productos) se ajustan a las necesidades del usuario y los usos previstos. La validación
del diseño debe completarse antes de la distribución comercial del producto. Las actividades de
validación del diseño deben ser predictivas, no empíricas. En otras palabras, los criterios de
aceptación deben establecerse antes de la actividad de validación. El establecimiento de criterios
de aceptación predeterminados se puede encontrar en un protocolo de validación o documento
similar.
La validación del diseño se debe realizar bajo condiciones operativas definidas en unidades de
producción iniciales, lotes o lotes, o sus equivalentes. La validación del diseño debe asegurar que
los dispositivos se ajusten a las necesidades definidas del usuario y los usos previstos e incluye la
prueba de las unidades de producción bajo condiciones de uso reales o simuladas. Los resultados
de la validación del diseño, incluida la identificación del diseño, método (s), fecha e individuo (s)
que realizan la validación, deben registrarse.
Necesidades, entorno y usos
MDSAP AU P0002.005 90 Página
La validación del diseño debe abordar las necesidades de todas las partes relevantes, como el
paciente, el trabajador de la salud, el ingeniero biomédico y el empleado de almacenamiento. Se
debe tener en cuenta el entorno en el que se almacenará, transportará y utilizará el dispositivo.
La validación del diseño debe realizarse para cada uso previsto. La validación del diseño también
debe confirmar que se cumplen las necesidades del usuario y los usos previstos asociados con el
empaque y etiquetado del dispositivo. Estas salidas tienen implicaciones en los factores humanos
y, a menos que se tengan en cuenta adecuadamente durante la validación del diseño, pueden
afectar negativamente al dispositivo y su uso. Confirme que los datos de validación del diseño
muestran que el diseño aprobado cumplió con las necesidades predeterminadas del usuario y los
usos previstos. Los usos previstos deben incluir el propósito del dispositivo, el tipo de paciente
(adultos, pediatría o recién nacido) y el entorno en el que se transportará y utilizará el dispositivo
(uso doméstico, hospitales, ambulancias, etc.).
Enlaces
Ninguno
Tarea 11 – Evaluación Clínica y / o Evaluación de la Seguridad y Desempeño
del Dispositivo Médico
Verificar que las evaluaciones clínicas y / o la evaluación de la seguridad y el rendimiento
del dispositivo médico se hayan realizado como parte de la validación del diseño, si así lo
requieren las reglamentaciones nacionales o regionales.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 7.3.7;
TGA: TG(MD)R Reg 3.11, Sch3 P1 Cl 1.4(5)(c)(vii), Sch3 P8;
ANVISA: RDC ANVISA 16/2013: 4.1.8, 4.1.11, RDC ANVISA 56/2001;
HC: CMDR 12, 18, 19;
MHLW/PMDA: MO169: 6, 35;
FDA: 21 CFR 820.30(g)
Requisitos adicionales específicos del país:
Australia (TGA):
Verificar que los registros de la validación incluyan evidencia clínica según lo requerido por los
procedimientos de evidencia clínica [TG(MD) Sch3 P1 Cl 1.4(5)(c)(vii) and TG(MD) Sch3 P8].
Para obtener más información sobre las fuentes y los tipos de evidencia clínica y cómo se pueden
utilizar para demostrar el cumplimiento de los Principios Esenciales Australianos, los auditores
pueden consultar las pautas de evidencia clínica (dispositivos médicos).
Evaluación de la conformidad:
Evaluaciones clínicas y pruebas
La validación del diseño puede implicar la realización de algún tipo de evaluación clínica, incluidas
pruebas bajo condiciones de uso reales o simuladas. Las evaluaciones clínicas pueden implicar
estudios clínicos completos. Las evaluaciones clínicas también pueden consistir en otras
MDSAP AU P0002.005 91 Página
evaluaciones en un entorno clínico o no clínico, la provisión de evidencia histórica de que diseños
similares son clínicamente seguros o revisiones de literatura científica.
El equipo de auditoría debe limitar su revisión de evaluaciones clínicas para verificar si las
evaluaciones clínicas se han realizado como parte de la validación del diseño, cuando sea
necesario, y si la organización de Dispositivos Médicos ha establecido criterios de aceptación para
los resultados para validar el dispositivo y que los resultados obtenidos cumplen los criterios de
aceptación definidos.
Cuando corresponda, revisar las evaluaciones clínicas, si se realizan, para validar el diseño. El
equipo de auditoría debe confirmar que los datos de las evaluaciones clínicas demuestran que las
necesidades del usuario y los usos previstos para el dispositivo y su embalaje y etiquetado se
cumplieron.
Enlaces
Ninguno
Tarea 12 – Diseño y Desarrollo de Software
Si el dispositivo médico contiene software, verificar que el software esté sujeto al proceso
de diseño y desarrollo.
Confirmar que el software se incluyó en el proceso de gestión de riesgos.
Cláusula y Regulación:
ISO: ISO 13485:2016: 7.3.2, 7.3.10;
TGA: TG(MD)R Sch1 P1 2, Sch1 EP12.1;
ANVISA: RDC ANVISA 16/2013: 2.4, 4.1.8, 4.1.11;
HC: CMDR 20;
MHLW/PMDA: MO169: 30;
FDA: 21 CFR 820.30(g)
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Desarrollo de software
Muchos dispositivos están controlados al menos parcialmente por software. Algunos dispositivos
consisten casi en su totalidad en software. Para el software del dispositivo, confirmar que el
software es parte del plan de diseño y desarrollo del dispositivo. Deben definirse los requisitos del
ciclo de vida para el software del dispositivo médico, incluido el uso previsto.
Verificación de software
"Verificación de software" es un término que se usa a menudo para describir las pruebas del
software. Durante la revisión del desarrollo del software, confirmar que la organización de
Dispositivos Médicos haya llevado a cabo las actividades de verificación adecuadas. La verificación
a menudo se lleva a cabo mediante la realización de casos de prueba en la unidad, el subsistema y
los niveles de integración; así como pruebas funcionales del sistema.
MDSAP AU P0002.005 92 Página
La verificación del software puede incluir la prueba del producto de software instalado en el
hardware de destino. Al igual que con otros tipos de verificación de diseño, la verificación del
software es una actividad predictiva. Los criterios de aceptación deben determinarse antes de
realizar la prueba.
Los criterios de aceptación predeterminados a menudo se encuentran en un protocolo de
verificación o documento similar.
Confirmar que se han cumplido los criterios de aceptación predeterminados revisando los
resultados reales de las pruebas de software seleccionadas. Las actividades de gestión de riesgos
para el dispositivo y el software pueden ayudar a guiar al equipo de auditoría en cuanto a qué
pruebas de verificación implican las salidas de diseño esenciales del dispositivo y el software.
Validación de software
La validación de software es una "confirmación mediante examen y provisión de evidencia objetiva
de que las especificaciones de software se ajustan a las necesidades del usuario y los usos
previstos, y que los requisitos particulares implementados a través del software pueden cumplirse
consistentemente". Implica verificar el funcionamiento correcto del software en su real o entorno de
uso simulado, incluida la integración en el dispositivo final cuando corresponda. Las pruebas de la
funcionalidad del software del dispositivo en un entorno de uso simulado y las pruebas en el sitio
del usuario se incluyen generalmente como componentes de un programa de validación de diseño
general para un dispositivo automatizado de software.
El equipo de auditoría puede encontrar momentos en los que el software se ha instalado en sitios
de usuarios como parte de la validación, a menudo denominado "prueba beta". Las pruebas beta
pueden ser un método para confirmar que el dispositivo, incluido el software, cumpla con las
necesidades del usuario y los usos previstos.
Enlaces
Ninguno
Tarea 13 – Cambio del Diseño y Desarrollo
Verificar que los cambios de diseño y desarrollo se controlaron, verificaron (o validados en
su caso) y se aprobaron antes de la implementación.
Confirmar que cualquier riesgo nuevo asociado con el cambio de diseño se haya
identificado y mitigado en la medida de lo posible.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 4.2.3, 7.1, 7.3.9, 7.3.10; 8.2.1
TGA: TG(MD)R Sch1 P1 2, Sch3 P1 Cl 1.4(5)(f), Sch3 P1Cl1.5(4), Sch3 P1 1.4(3)(a) &(b)
ANVISA: RDC ANVISA 16/2013: 2.4, 4.1.4, 4.1.8, 4.1.10, 4.1.11, Ley Brasileña 6360/76 -Art. 13;
HC: CMDR 1, 34;
MHLW/PMDA: MO169: 6, 26, 36;
FDA: 21 CFR 820.30(i)
Requisitos adicionales específicos del país:
Australia (TGA):
Verificar que el fabricante tenga un proceso o procedimiento para notificar a la organización de
auditoría de un cambio sustancial en el proceso de diseño o la gama de productos que se
fabricarán [TG(MD)R Sch3 Cl 1.5].
MDSAP AU P0002.005 93 Página
Verificar que el fabricante tenga un proceso o procedimiento para identificar un cambio sustancial
propuesto para el diseño o el rendimiento previsto de un dispositivo de Clase AIMD o Clase III, y
notificar al organismo de evaluación antes de implementar el cambio [TG (MD) R Sch3 P1 Cl 1.6
(4)].
Si el fabricante también es titular de un certificado de evaluación de la conformidad de TGA,
también se requiere que el fabricante notifique a la TGA de estos cambios.
Verificar que el fabricante haya tenido en cuenta los comentarios de posproducción como una
entrada para monitorear y mantener los requisitos del producto y mejorar los procesos de
realización del producto.
Brasil (ANVISA):
Si el dispositivo médico evaluado ya está registrado / notificado con ANVISA, verificar que el
cambio de diseño se haya presentado correctamente y con prontitud a ANVISA para su
aprobación, cuando corresponda [Ley brasileña 6360/76 art. 13].
Canadá (HC):
Verificar que el fabricante tenga un proceso o procedimiento para identificar un "cambio
significativo" en un dispositivo médico de Clase III o IV. Verifique que la información sobre
"cambios significativos" se presente en una solicitud de modificación de licencia de dispositivo
médico [CMDR 1, 34].
Japón (MHLW):
Para el titular de la autorización de comercialización, confirme si el titular de la autorización de
comercialización ha presentado una nueva solicitud, una solicitud de cambio o una notificación de
cambio a PMDA / a un organismo de certificación registrado, cuando corresponda. [PMD Act 23-2-
5.1, 23-2- 5.11, 232-5.17, 23-2-23.1, 23-2-23.6, 23-2-23.7].
Para el sitio de fabricación registrado, confirmar si el sitio tiene un mecanismo para comunicarse
con el titular de la autorización de comercialización sobre las modificaciones del dispositivo, de
modo que el titular de la autorización de comercialización pueda tomar las medidas adecuadas. Si
se ha producido una modificación crítica del dispositivo médico en el sitio de fabricación registrado,
confirme si el sitio de fabricación registrado se ha comunicado con el titular de la autorización de
comercialización acerca del cambio [MHLW MO169: 29].
Estados Unidos (FDA):
Verificar que la organización de Dispositivos Médicos haya obtenido un nuevo 510 (k) o un
complemento a la aprobación previa al mercado si es necesario [21 CFR 807].
Evaluación de la conformidad:
Procedimientos
Una organización de Dispositivos Médicos puede tener procedimientos de control de cambios
separados para manejar los cambios de posproducción y preproducción, o una organización de
Dispositivos Médicos puede tener un procedimiento que maneje ambos.
Naturaleza del cambio
La documentación y el control de los cambios comienza cuando las entradas de diseño iniciales
son aprobadas y continúan durante la vida útil del producto. El control de cambio de diseño se
aplica a cambios en entradas o salidas como resultado de verificación de diseño o validación de
diseño, cambios en etiquetado o empaque, cambios para mejorar el rendimiento de un producto,
MDSAP AU P0002.005 94 Página
cambios de proceso (s) de producción y cambios que resultan de quejas de producto. El cambio
puede ser aceptable mientras esté controlado.
Registros
El control de los cambios no está completo hasta que los resultados de la revisión de los cambios y
cualquier actualización de las especificaciones del producto o los procesos modificados sean
documentados o modificados.
Comunicación y acciones consecuentes
Los cambios deben comunicarse efectivamente y los requisitos para cualquier acción consecuente
deben definirse (por ejemplo, capacitación o comunicación al personal de diseño o producción).
Enlaces
Proceso de Medición, Análisis y Mejora (si se realizó un cambio de diseño para corregir un
problema de calidad con el dispositivo); Autorización de Comercialización de Dispositivos y
Registro de Instalaciones
Durante la auditoría del proceso de Medición, Análisis y Mejora, los auditores pueden encontrar
acciones correctivas o preventivas que resultaron en cambios de diseño. Cuando la acción
correctiva o preventiva implica cambiar el diseño, confirmar que los controles de diseño se hayan
aplicado al cambio, de acuerdo con los procedimientos de la organización de Dispositivos Médicos.
Confirmar que estos cambios de diseño fueron efectivos para abordar los problemas de calidad o
posibles problemas de calidad identificados en acciones correc+tivas o preventivas. Además, el
cambio de diseño debe evaluarse en el proceso de gestión de riesgos de la organización de
Dispositivos Médicos para garantizar que los cambios no introduzcan nuevos riesgos. Algunos
cambios pueden requerir una revalidación cuando no es posible verificar que se hayan cumplido
los requisitos después de que se haya implementado el cambio.
El equipo de auditoría también debe confirmar que la organización de Dispositivos Médicos ha
considerado los requisitos reglamentarios para el registro, listado, notificación y licencia; y ha
cumplido con estos requisitos antes de comercializar el dispositivo cambiado en las jurisdicciones
regulatorias aplicables.
Tarea 14 – Revisión del Diseño
Verificar que las revisiones de diseño se llevaron a cabo en las etapas adecuadas según lo
requerido por el plan de diseño y desarrollo.
Confirmar que los participantes en las revisiones incluyan representantes de las funciones
relacionadas con la etapa de diseño y desarrollo que se está revisando, así como también
con el personal especializado que se necesite.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 7.3.2, 7.3.5;
TGA: TG(MD)R Sch3 P1 C1.4(5)(c)(i);
ANVISA: RDC ANVISA 16/2013: 4.1.6, 4.1.11;
MHLW/PMDA: MO169: 6, 30, 33;
FDA: 21 CFR 820.30(e)
Requisitos adicionales específicos del país:
Estados Unidos (FDA):
MDSAP AU P0002.005 95 Página
Verificar que los procedimientos aseguren que los participantes incluyan representantes de todas
las funciones relacionadas con la etapa de diseño que se revisa y una persona (s) que no tenga
responsabilidad directa por la etapa de diseño que se revisa, así como cualquier especialista
necesario [21 CFR 820.30 (e)].
Evaluación de la conformidad:
Revisiones de diseño
Las revisiones de diseño generalmente ocurren al final de cada etapa o fase de diseño o después
de la finalización de los hitos del proyecto. El número de revisiones de diseño puede variar, pero
como mínimo, se debe realizar una revisión formal. Las revisiones deben proporcionar
retroalimentación al equipo de diseño sobre problemas emergentes, evaluar el progreso del
proyecto de diseño y desarrollo, y confirmar que el diseño está listo para pasar a la siguiente fase
de desarrollo o para la transferencia a la fase de fabricación.
No es necesario tener reuniones totalmente convocadas para todas las revisiones de diseño. Para
diseños simples o cambios menores, las revisiones de escritorio y las aprobaciones pueden ser
adecuadas. Las revisiones de diseño deben incluir a un individuo que no tenga responsabilidad
directa por la etapa de diseño que se revisa y la representación de la fabricación para garantizar
que los productos de diseño y desarrollo se verifiquen como adecuados para la fabricación antes
de convertirse en especificaciones de producción finales.
Durante la revisión de las actividades de revisión de diseño para el proyecto de diseño
seleccionado, confirmar que las revisiones incluyeron a un individuo que no tuvo responsabilidad
directa por la etapa de diseño que se está revisando. El equipo de auditoría también debe
confirmar que los elementos de acción pendientes se están resolviendo o se han resuelto.
Enlaces
Ninguno
Tarea 15 – Revisión del Impacto de los Cambios del Diseño y Desarrollo en
Dispositivos Previamente Hechos y Distribuidos
Verificar que los cambios de diseño hayan sido revisados por el efecto en los productos
previamente realizado y entregado, y que se mantienen los registros de los resultados de la
revisión.
Cláusula y Regulación:
ISO: ISO 13485:2016: 7.3.9;
ANVISA: RDC ANVISA 16/2013: 4.1.10;
MHLW/PMDA: MO169: 36;
FDA: 21 CFR 820.30(i)
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Efectos en partes constituyentes y productos ya entregados
Hay situaciones en las que un cambio de diseño puede afectar las partes constituyentes. Por
ejemplo, un cambio a una porción desechable de un sistema de aspiración podría afectar la
MDSAP AU P0002.005 96 Página
capacidad del desechable para conectarse a la consola. Cuando sea necesario, asegurar de que el
cambio de diseño no afecte negativamente a los productos en distribución.
Enlaces
Ninguno
Tarea 16 – Transferencia de Diseño
Determinar si el diseño se transfirió correctamente a producción.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 4.2.3, 7.3.8;
ANVISA: RDC ANVISA 16/2013: 4.1.7, 4.1.9, 4.1.11, 4.2;
MHLW/PMDA: MO169: 6, 30;
FDA: 21 CFR 830.30(h)
Requisitos adicionales específicos del país:
Brasil (ANVISA):
Confirmar que el fabricante asegura que el diseño no se lanza para producción hasta su
aprobación por las personas asignadas por el fabricante y que las personas asignadas revisan
todos los registros requeridos al historial de diseño para asegurar que esté completo y el diseño
final sea compatible. con los planes aprobados, antes de su lanzamiento. Confirmar que esta
publicación, incluida la fecha y la firma manual o electrónica del responsable, esté documentada
[RDC ANVISA 16/2013: 4.1.9, 4.1.11].
Evaluación de la conformidad:
Transferir el diseño a producción
Durante esta fase, el diseño se traduce en especificaciones de producción. Esto puede tener lugar
en etapas o fases. El equipo de auditoría debe revisar cómo se transfirió el diseño del proyecto
seleccionado a las especificaciones de producción. Con base en la identificación de productos
esenciales y actividades de gestión de riesgos, revisar los elementos significativos de los procesos
de fabricación, incluidos los productos de los proveedores y las tolerancias establecidas para los
procesos, y compárelos con los productos de diseño aprobados que figuran en los registros de
diseño. Estas actividades pueden confirmar si el diseño se transfirió correctamente o no.
La transferencia de diseño es un proceso que puede iniciarse no solo al final del proceso de diseño
y desarrollo, sino que también puede iniciarse inmediatamente antes de las etapas de validación y
puede continuar a medida que evoluciona el diseño y el desarrollo. Esta iniciación temprana de la
transferencia de diseño es útil para que los procesos de producción y las validaciones de los
dispositivos se realicen correctamente y para permitir las correcciones durante el proceso. Al final,
el proceso de diseño y desarrollo se "finaliza" mediante una "transferencia de diseño final".
MDSAP AU P0002.005 97 Página
Enlaces
Controles de Producción y Servicio, Compras
Verificar que los procesos de producción para el dispositivo, incluida la validación del proceso (si es
necesario), se hayan definido, documentado e implementado. Confirmar que se han identificado los
peligros potenciales que podrían ser introducidos o exacerbados por el proceso de producción y
que se han establecido controles de producción. Los procesos de producción incluyen no solo las
instrucciones de fabricación, sino también los controles internos, como el tipo y el alcance de las
actividades de aceptación, la calibración del equipo y los intervalos de mantenimiento, los controles
ambientales y los controles de personal.
Confirmar que la organización de Dispositivos Médicos haya determinado el tipo y la extensión de
los controles del proveedor en función de la relación entre los productos y servicios suministrados y
el riesgo del producto.
Tarea 17 – Compromiso de la Alta Dirección para el Proceso de Diseño y
Desarrollo
Determinar, en base a la evaluación del proceso de diseño y desarrollo en general, si la Alta
Dirección brinda el compromiso necesario para el proceso de diseño y desarrollo.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.1.3, 5.1, 5.5.1;
TGA: TG(MD)R Sch3 P1 Cl 1.4(5)(b)(ii);
ANVISA: RDC ANVISA 16/2013: 2.2.1;
MHLW/PMDA: MO169: 5, 10, 15
Requisitos adicionales específicos del país:
Ninguno
Enlaces
Ninguno
MDSAP AU P0002.005 98 Página
Capítulo 6: Controles de Producción y Servicio
El propósito del proceso de Controles de producción y servicio es fabricar productos que cumplan
con las especificaciones. Desarrollar procesos que sean adecuados para producir dispositivos que
cumplan con las especificaciones, validar (o verificar completamente los resultados de) esos
procesos y monitorear y controlar esos procesos son todos pasos que ayudan a asegurar que el
resultado sea un dispositivo que cumpla con los requisitos especificados. Después de completar la
auditoría del proceso de Controles de Producción y de Servicio de la organización de Dispositivos
Médicos, el equipo de auditoría volverá al proceso de Administración para tomar una decisión final
sobre si la alta dirección asegura que se haya establecido y mantenido un sistema de gestión de
calidad adecuado y efectivo en la organización de Dispositivos Médicos.
Para cumplir con los requisitos de Controles de Producción y Servicio de Dispositivos Médicos -
Sistemas de gestión de la calidad - Requisitos para fines reglamentarios (ISO 13485:2016), los
requisitos del Sistema de Gestión de la Calidad de los Procedimientos de Evaluación de la
Conformidad del Reglamento Australiano de Productos Terapéuticos (MD) R Sch3), las Buenas
Prácticas de Fabricación Brasileñas (RDC ANVISA 16/2013), la Ordenanza de QMS Japonesa
(MHLW MO 169), el Reglamento del Sistema de Calidad (21 CFR Part 820) y los requisitos
específicos de las autoridades regulatorias de Dispositivos Médicos que participan en el programa
MDSAP, la organización de Dispositivos Médicos debe comprender cuándo podrían ocurrir
desviaciones de las especificaciones del dispositivo como resultado del proceso de producción o
del entorno.
El representante de la dirección es responsable de garantizar que los requisitos del sistema de
gestión de la calidad se hayan definido, documentado, implementado y mantenido efectivamente.
Antes de la auditoría de cualquier proceso de MDSAP, entrevistar al representante de la dirección
(o persona designada) para obtener una visión general del proceso y una idea del conocimiento y
la comprensión de la gestión del proceso.
La auditoría del proceso de Controles de Producción y Servicio seguirá la auditoría del proceso de
Medición, Análisis y Mejora y el proceso de Diseño y Desarrollo según la secuencia de auditoría de
MDSAP. La información que el equipo de auditoría haya aprendido sobre los dispositivos y las no
conformidades del sistema de gestión durante la auditoría del proceso de Medición, Análisis y
Mejora, así como los elementos de mayor riesgo y productos de diseño esenciales de los proyectos
de diseño revisados durante la auditoría del proceso de Diseño y Desarrollo utilizado para tomar
decisiones sobre los procesos de producción a ser revisados durante la auditoría del proceso de
Controles de Producción y Servicio.
Auditando el Proceso de Controles de Producción y Servicio
Propósito: El propósito de auditar el proceso de controles de producción y servicio (incluidas
pruebas, infraestructura, instalaciones, equipos y servicios) es verificar que los procesos de la
organización de Dispositivos Médicos sean capaces de garantizar que los productos cumplan con
las especificaciones.
Resultados: como resultado de la auditoría del proceso de controles de producción y de servicio,
la evidencia objetiva mostrará si la organización de Dispositivos Médicos ha:
MDSAP AU P0002.005 99 Página
A) Definido, documentado e implementado procedimientos para asegurar que los procesos de
producción y servicio sean planificados, desarrollados, conducidos, controlados y
monitoreados para asegurar la conformidad con los requisitos especificados.
B) Desarrollado el proceso de controles de producción y servicio acordes con el efecto
potencial del proceso sobre el riesgo del producto.
C) Asegurado que cuando los resultados de un proceso no pueden ser verificados por
monitoreo o medición subsiguientes, el proceso es validado con un alto grado de seguridad
de que el proceso logrará consistentemente el resultado planificado.
D) Implementado procedimientos para la validación de la aplicación de software para
procesos de producción y servicio que afectan la capacidad del producto para cumplir con
los requisitos especificados, incluida la validación del software utilizado en el sistema de
gestión de calidad.
E) Mantenido registros para cada lote de dispositivos médicos que proporciona información
para la rastreabilidad y confirmación de que el lote cumple con los requisitos especificados.
F) Implementado controles para proteger la propiedad del cliente, incluida la propiedad
intelectual, la información confidencial de salud y otras formas de propiedad del cliente que
se utilizan o incorporan en los productos.
Enlaces a otros procesos:
Gestión; Diseño y Desarrollo; Medición, Análisis y Mejora;
Compras
Tarea 1 – Planeación del Proceso de Producción y Servicio
Verificar que los procesos de realización del producto estén planificados, incluidos los
controles necesarios, las condiciones controladas y las actividades de gestión de riesgos
requeridas para que el producto cumpla con los usos especificados o previstos, los
requisitos reglamentarios y legales relacionados con el producto y (cuando corresponda)
requisitos del identificador único de dispositivo.
Confirmar que la planificación de la realización del producto es coherente con los requisitos
de los demás procesos del sistema de gestión de la calidad y se realiza teniendo en cuenta
los objetivos de la calidad.
Cláusula y Regulación:
ISO: ISO 13485:2016: 7.1, 7.2.1, 7.5.1;
TGA: TG(MD)R Sch 1 P1 2, Sch3 P1 Cl1.4(4), Sch3 P1 Cl1.4(5)(d) &(e);
ANVISA: RDC ANVISA 16/2013: 2.2.1, 2.4, 4.1.2, 4.1.7, 5.1;
MHLW/PMDA: MO169: 26, 27, 40;
FDA: 21 CFR 801, 820.30(b), 820.20(a), 820.30(h), 820.70(a), 830
Requisitos adicionales específicos del país:
Estados Unidos (FDA):
Confirmar que la organización de Dispositivos Médicos ha determinado la aplicabilidad de los
requisitos de identificador único de dispositivo según 21 CFR 801 y 21 CFR 830, ha obtenido los
identificadores únicos de dispositivo de una agencia emisora de UDI acreditada por la FDA y los
elementos de datos requeridos han sido ingresados en la Base Global Única de Datos de
Identificación de Dispositivo (GUDID, por sus siglas en inglés) [21 CFR 801, 830].
Evaluación de la conformidad:
MDSAP AU P0002.005 100
Página
Planificación
Al planear la realización del producto, la organización de Dispositivos Médicos debe determinar
según corresponda los objetivos y requisitos de calidad para el producto, los procesos, documentos
y recursos específicos del producto, los criterios para la aceptación del producto y las actividades
requeridas de verificación, monitoreo, inspección y prueba específico para el producto. La
planificación de la realización del producto a menudo comienza en el diseño y desarrollo del
producto, incluida la traducción del diseño en las especificaciones de producción.
La planificación de la realización del producto debe ser coherente con las estrategias de control de
riesgos y mitigación identificadas por la organización durante las actividades de gestión de riesgos.
Durante la auditoría, tener en cuenta los requisitos del producto que se relacionan con los
requisitos legales y regulatorios, los requisitos necesarios para que el producto cumpla con los
usos especificados o previstos, y los requisitos para un uso seguro y eficaz del producto. La
organización de Dispositivos Médicos debe garantizar sus procesos, y la supervisión de los
procesos, la inspección y las actividades de prueba se planifican y desarrollan para garantizar que
se cumplan estos requisitos.
Identificador Único de Dispositivo (UDI, por sus siglas en inglés)
Un UDI es una representación codificada de información especificada. Aparece en la etiqueta del
dispositivo, en el empaque o, en algunos casos, en el dispositivo. El UDI debe presentarse en dos
formas: texto plano fácilmente legible y formato de identificación automática y captura de datos (o
AIDC, por sus siglas en inglés). Muchos tipos de codificaciones que cumplen con AIDC están
disponibles y son permitidos siempre que puedan ingresarse en un registro electrónico de paciente
u otro sistema informático a través de un proceso automatizado.
Los requisitos de la regla generalmente están dirigidos a etiquetadores. El concepto de etiquetador
se define en 21 CFR 801.3.
Dos factores principales determinan si una parte es etiquetador: (1) un etiquetador hace que se
aplique una etiqueta a un dispositivo con la intención de que el dispositivo se distribuya
comercialmente sin ningún reemplazo o modificación subsecuente de la etiqueta, o (2)) un
etiquetador hace que una etiqueta sea reemplazada o modificada con la intención de que el
dispositivo se distribuya comercialmente.
Los fabricantes, fabricantes por contrato, distribuidores privados de etiquetas y ensambladores de
kits de conveniencia son los tipos más comunes de organizaciones que se consideran
etiquetadores. Se aplican algunas pequeñas excepciones, como agregar un nombre o información
de contacto a la etiqueta ya existente.
El programa UDI requiere que los etiquetadores trabajen con una agencia emisora acreditada por
la FDA para producir sus UDI. La agencia emisora proporciona una parte de la UDI para identificar
al etiquetador, además de proporcionar un formato compatible con los estándares para la
visualización de la UDI en texto simple y código AIDC de fácil lectura.
La regla UDI requiere que los etiquetadores de Dispositivos cumplan dos requisitos básicos: (1) los
Dispositivos deben llevar un UDI en la ubicación adecuada, (2) y ciertos elementos de datos deben
ingresarse en la Base Global Única de Datos de Identificación de Dispositivo (GUDID). El GUDID
es una base de datos mantenida por el equipo de UDI en la FDA que sirve como un repositorio
público para la información de dispositivos relacionados con UDI.
Según la regla UDI, todos los Dispositivos Médicos, independientemente de la clase (e incluidos los
dispositivos no clasificados) deben cumplir con los requisitos de la regla, a menos que esté cubierto
por una exención o discreción de ejecución.
MDSAP AU P0002.005 101
Página
Objetivos de Calidad
Los Objetivos de Calidad generalmente se expresan como un objetivo u objetivo mensurable. La
planificación de la realización del producto debe incluir la consideración de cómo los procesos de
producción, los criterios para la aceptación del producto y las actividades de verificación,
validación, monitoreo, inspección y prueba requeridas específicas para el producto lograrán los
objetivos de calidad. Confirmar que la organización de Dispositivos Médicos haya definido objetivos
de calidad para el dispositivo.
Enlaces
Gestión
Confirmar cuando sea necesario que los objetivos de calidad relacionados con el producto se
consideraron para su inclusión en la revisión de la dirección.
Tarea 2 – Selección del Proceso(s) de Producción y Servicio
Revisar los procesos de producción considerando los siguientes criterios.
Seleccionar uno o más procesos de producción para auditar.
Recordatorio: La información que el equipo de auditoría ha aprendido sobre las no conformidades
del dispositivo y del sistema de gestión de calidad durante la auditoría del proceso de Medición,
Análisis y Mejora, así como los elementos de mayor riesgo y resultados de diseño esenciales de
los proyectos de diseño revisados durante la auditoría del proceso de Diseño y Desarrollo debe de
ser utilizada para tomar decisiones sobre los procesos de producción que son revisados.
Criterios de prioridad para la selección:
1. Indicadores de acción correctiva y preventiva de problemas de proceso o
problemas potenciales.
2. Uso del proceso de producción para productos de mayor riesgo.
3. Uso de procesos de producción que impactan directamente en la capacidad del
dispositivo para cumplir con los Resultados Esenciales de Diseño.
4. Nuevos procesos de producción o nuevas tecnologías.
5. Uso del proceso en la fabricación de múltiples productos.
6. Procesos que operan en múltiples turnos.
7. Procesos no cubiertos durante auditorías previas.
Enlaces
Ninguno
Tarea 3 – Controles para la Implementación de Proceso(s) Seleccionado(s)
de Producción y Servicio
Para cada proceso seleccionado, determinar si el proceso de producción y servicio se
planifica y lleva a cabo bajo condiciones controladas que incluyen lo siguiente:
MDSAP AU P0002.005 102
Página
La disponibilidad de información que describe las características del producto.
La disponibilidad de procedimientos documentados, requisitos, instrucciones de
trabajo y materiales de referencia, medidas de referencia y criterios para mano de
obra.
El uso de equipo adecuado.
La disponibilidad y el uso de dispositivos de monitoreo y medición.
La implementación de monitoreo y medición de parámetros de proceso y
características del producto durante la producción.
La implementación de las actividades de liberación, entrega y posterior a la
entrega.
La implementación de operaciones definidas para etiquetado y empaquetado.
El establecimiento de requisitos documentados para cambios en métodos y
procesos.
Cláusula y Regulación:
ISO: ISO 13485:2016: 7.5.1, 8.2.5, 8.2.6;
ANVISA: TG (MD) R Sch3 P1 Cl1.4 (5) (d) y (e);
ANVISA: RDC ANVISA 16/2013: 3.1.3, 4.2, 5.1, 5.2, 5.3, 5.4, 5.6, 5.6.1; 5.6.2;
MHLW/PDMA: MO169: 40, 57, 58, 59;
FDA: 21 CFR 820.70 (a), 820.70 (b), 820.75, 820.120, 820.130
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Establecimiento de instrucciones de trabajo, procedimientos y procesos de producción
Los procesos de producción que pueden causar una desviación a la especificación de un
dispositivo y todos los procesos validados deben ser controlados y monitoreados. La planificación
de la producción incluye el establecimiento de procedimientos e instrucciones de trabajo para el
control y la supervisión de los procesos de producción, incluidos los controles del servicio cuando
sea necesario. Los procedimientos de control y monitoreo pueden incluir actividades de aceptación
de dispositivos terminados y en proceso, así como medidas de control ambiental y de
contaminación. El establecimiento de procedimientos e instrucciones de trabajo para controlar la
producción del dispositivo debe proporcionar los controles y las tolerancias necesarias para
garantizar que los dispositivos terminados cumplan con las especificaciones del producto.
Enlaces
Ninguno
Tarea 4 – Control de la Limpieza del Producto
Determinar si la organización de Dispositivos Médicos ha establecido requisitos
documentados para la limpieza del producto, incluida la limpieza previa a la esterilización,
los requisitos de limpieza, si se proporcionan no estériles, y si se eliminan los agentes del
proceso del producto si es necesario.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 4.2.3, 6.4.2, 7.5.2;
TGA: TG(MD)R Sch3 P1 Cl1.4(5)(d);
ANVISA: RDC ANVISA 16/2013: 5.1.3.1, 5.1.3.4, 5.1.5.3;
MDSAP AU P0002.005 103
Página
MHLW/PMDA: MO169: 6, 25, 41;
FDA: 21 CFR 820.70(c), 820.70(d), 820.70(e), 820.70(h)
Requisitos adicionales específicos del país:
Brasil (ANVISA):
Confirmar que se ha establecido un programa de control de plagas y donde los químicos se usan
como parte del programa de control de plagas, la compañía debe asegurarse de que no afecten la
calidad del producto [RDC ANVISA 16/2013: 5.1.3.4].
Verifique que el fabricante haya establecido y mantenga procedimientos y cronogramas de limpieza
para áreas de producción y almacenes, de conformidad con las especificaciones de producción
[RDC ANVISA 16/2013: 5.1.3.1].
Evaluación de la conformidad:
Requisitos de limpieza
El objetivo de establecer requisitos para la limpieza del producto es minimizar la contaminación del
dispositivo terminado y el entorno de fabricación. Los dispositivos estériles pueden requerir un
mayor nivel de control en términos de minimizar la carga biológica y la contaminación de partículas
a fin de asegurar que se cumpla el nivel de garantía de esterilidad deseado.
Cada organización de Dispositivos Médicos debe evaluar el grado de limpieza requerido para el
funcionamiento adecuado y el uso previsto del dispositivo terminado e implementar las medidas de
control necesarias. Los ejemplos de medidas de control incluyen, entre otros, procedimientos de
limpieza, controles ambientales (por ejemplo, salas limpias u otros entornos controlados), requisitos
para el atuendo y capacitación del personal. Cuando sea necesario, confirmar que la organización
de Dispositivos Médicos haya identificado los requisitos de limpieza para el dispositivo terminado y
los controles adecuados para lograr el nivel de limpieza requerido.
Agentes de proceso
Los agentes de proceso, también conocidos como materiales de fabricación, generalmente se
definen como materiales o sustancias utilizados para facilitar el proceso de fabricación, que están
presentes en los dispositivos terminados como un residuo o impureza. Ejemplos de agentes de
proceso incluyen agentes de limpieza, agentes de desmoldeo, aceites lubricantes, proteínas de
látex, residuos de esterilizantes, etc. La organización de Dispositivos Médicos debe evaluar los
agentes de proceso utilizados durante el proceso de fabricación cuando el agente de proceso
podría tener un efecto adverso en el producto. Durante el diseño del producto y el desarrollo del
proceso de fabricación, se debe considerar el efecto potencial de los agentes de proceso.
Si el equipo de auditoría encuentra situaciones en las que se utilizan agentes de proceso en la
fabricación del producto, y el agente de proceso podría tener un efecto adverso en el producto,
confirmar que la organización de Dispositivos Médicos ha tomado medidas efectivas para controlar
el agente de proceso de una manera acorde con el riesgo que el agente representa para el
dispositivo terminado. Por ejemplo, la organización de Dispositivos Médicos puede necesitar validar
un proceso de limpieza para asegurar que se extraiga el aceite de corte de un implante ortopédico
antes del empaque y la esterilización.
Enlaces
Ninguno
Tarea 5 – Infraestructura
MDSAP AU P0002.005 104
Página
Verificar que la organización de Dispositivos Médicos haya determinado y documentado los
requisitos de infraestructura para lograr la conformidad del producto, incluidos los edificios,
el espacio de trabajo, el equipo de proceso y los servicios de soporte.
Confirmar que los edificios, las áreas de trabajo y los servicios de soporte permitan que el
producto cumpla con los requisitos.
Verificar que existan requisitos documentados e implementados para el mantenimiento del
equipo de proceso que sean importantes para la calidad del producto, y que se mantengan
registros de mantenimiento.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 6.3, 7.5.1;
ANVISA: RDC ANVISA 16/2013: 5.1.2, 5.1.5;
HC: CMDR 14;
MHLW/PMDA: MO169: 6, 24, 40;
FDA: 21 CFR 820.70(g), 820.70(f)
Requisitos adicionales específicos del país:
Brasil (ANVISA):
Verificar que las instalaciones de fabricación estén configuradas para proporcionar los medios
adecuados para el flujo de personas [RDC ANVISA 16/2013: 5.1.2].
Evaluación de la conformidad:
Requisitos de infraestructura
La organización de Dispositivos Médicos es responsable de evaluar las instalaciones de fabricación
para garantizar que los edificios, los servicios públicos y el espacio permitan alcanzar la
conformidad del producto. La organización de Dispositivos Médicos es responsable de garantizar el
espacio adecuado para evitar confusiones y garantizar el manejo ordenado de los productos.
Enlaces
Ninguno
Tarea 6 – Ambiente de Trabajo
Verificar que los requisitos documentados se hayan establecido, implementado y mantenido
para:
salud, limpieza y vestimenta del personal que podría tener un efecto adverso en la
calidad del producto.
monitorear y controlar las condiciones del entorno de trabajo que pueden tener un
efecto adverso en la calidad del producto.
capacitación o supervisión del personal que debe trabajar en condiciones
ambientales especiales.
controlar el producto contaminado o potencialmente contaminado (incluidos los
productos devueltos) para evitar la contaminación de otros productos, el entorno
de trabajo o el personal.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 6.4;
TGA: TG(MD)R Sch1 P2 7.2, 8;
MDSAP AU P0002.005 105
Página
ANVISA: RDC ANVISA 16/2013: 5.1.3;
MHLW/PMDA: MO169: 6, 25;
FDA: 21 CFR 820.70(c), 820.70(d), 820.70(e)
Requisitos adicionales específicos del país:
Brasil (ANVISA):
Verificar que se utilicen estándares de bioseguridad, cuando corresponda [RDC ANVISA 16/2013:
5.1.3.6].
Evaluación de la conformidad:
Control de contaminación
La organización de Dispositivos Médicos es responsable de establecer y mantener procedimientos
para evitar la contaminación de productos, equipos y personal por sustancias que podrían afectar
negativamente el dispositivo. Si las medidas de control de la contaminación son necesarias para
cumplir con los requisitos especificados, es posible que se requieran procedimientos y calendarios
de limpieza y desinfección para garantizar que las medidas de control de la contaminación
funcionen correctamente. La organización de Dispositivos Médicos debe considerar la segregación
y descontaminación del producto devuelto.
Prácticas de personal
Las prácticas de personal deben abordar la salud, limpieza y vestimenta del personal si pueden
afectar negativamente la calidad del producto o el entorno de trabajo. En el caso de que se
requiera que el personal de mantenimiento o de otro tipo trabaje temporalmente bajo condiciones
ambientales especiales, estas personas deben estar debidamente capacitadas o supervisadas por
un individuo capacitado.
Enlaces
Ninguno
Tarea 7 – Identificación de Procesos sujetos a Validación
Determinar si los procesos seleccionados y los subprocesos han sido revisados, incluidos
los procesos subcontratados, para determinar si se requiere la validación de estos
procesos.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 4.1.6, 7.5.6;
TGA: TG(MD)R Sch1 P2 8.2, 8.3; Sch3 P1 1.4(5)(d);
ANVISA: RDC ANVISA16/2013: 5.5.2, 5.5.3;
MHLW/PMDA: MO169: 6, 45;
FDA: 21 CFR 820.75(a)
Requisitos adicionales específicos del país:
Brasil (ANVISA):
Verificar que los métodos analíticos, los sistemas auxiliares para producción y control ambiental
que pueden afectar negativamente la calidad del producto o el sistema de calidad, se validen,
revisen periódicamente y, cuando sea necesario, se revalidan de acuerdo con procedimientos
documentados [RDC ANVISA 16/2013: 5.5.2, 5.5 .3].
MDSAP AU P0002.005 106
Página
Estados Unidos (FDA):
Se requiere la validación del proceso para la esterilización, el procesamiento aséptico, el moldeo
por inyección y la soldadura [21 CFR 820.75; comentario de preámbulo 143].
Evaluación de la conformidad:
Validación del Proceso
Durante la planificación de la realización del producto, la organización de Dispositivos Médicos
debe determinar qué procesos de producción requieren validación y qué procesos pueden
verificarse. La validación del proceso puede aplicarse a los procesos que generan componentes,
subconjuntos o dispositivos terminados. La validación del proceso es necesaria para los procesos
donde los resultados del proceso no se pueden verificar completamente. Los procesos que no se
pueden verificar completamente incluyen procesos donde las pruebas clínicas o destructivas son
necesarias para mostrar que el proceso produjo el resultado deseado, donde la inspección y / o
prueba de rutina no examina los atributos de calidad esenciales para el correcto funcionamiento del
dispositivo terminado, o donde la rutina la prueba tiene sensibilidad insuficiente para verificar la
seguridad y eficacia deseadas del producto terminado.
Los ejemplos de procesos que requieren validación incluyen, pero no están limitados a
esterilización, procesamiento aséptico, soldadura y moldeo por inyección. Cuando corresponda,
confirmar que la organización de Dispositivos Médicos haya identificado los procesos que
requieren validación, incluidos los requisitos de validación para cualquier proceso subcontratado.
Al validar los procesos, las organizaciones deben tener en cuenta el pensamiento actual de los
expertos donde la información publicada está disponible (por ejemplo, a través de la aplicación de
las normas ISO para la validación de la esterilización).
Enlaces
Compras
El equipo de auditoría puede encontrar situaciones donde la organización de Dispositivos Médicos
subcontrata procesos que requieren validación.
Durante la revisión del proceso de Compras, revisar los controles que la organización de
Dispositivos Médicos ha instituido sobre los proveedores que realizan procesos validados. Esto
puede ser particularmente importante para los procesos validados de mayor riesgo realizados por
los proveedores, ya que el fabricante del dispositivo terminado no tiene control inmediato sobre
esos procesos.
Tarea 8 – Validación de Proceso
Verificar que el (los) proceso (s) seleccionado (s) haya (n) sido validado (s) de acuerdo con
procedimientos documentados si el resultado del proceso no puede verificarse
completamente o puede verificarse, pero es no.
Confirmar que la validación demuestra la capacidad de los procesos para conseguir
consistentemente el resultado planificado.
En caso de que se hayan producido cambios en proceso previamente validado, confirmar
que el proceso fue revisado y evaluado, y la revalidación se realizó cuando correspondía.
Cláusula y Regulación:
MDSAP AU P0002.005 107
Página
ISO: ISO 13485:2016: 4.2.1, 7.5.6;
TGA: TG(MD)R Sch1 P1 2(1), Sch3 P1 1.4(5)(d);
ANVISA: RDC ANVISA 16/2013: 1.2.18, 5.5.1;
MHLW/PMDA: MO169: 6, 45;
FDA: 21 CFR 820.75(a), 820.75(c)
Requisitos adicionales específicos del país:
Australia (TGA):
Confirmar que los métodos de validación tienen en cuenta el estado de la técnica generalmente
reconocida por el estándar (por ejemplo, Órdenes estándar del Dispositivo Médico – MDSO, ISO /
Estándares IEC, BP, EP, USP, etc.) [TG Act s41CB, TG (MD) R Sch 1 P1 2 (1)].
Evaluación de la conformidad:
Validación del proceso
Validación del proceso significa establecer mediante evidencia objetiva (es decir, datos) que un
proceso produce constantemente un resultado (por ejemplo, nivel de garantía de esterilidad) o que
el producto cumple con especificaciones predeterminadas. Recordar que el término "producto" se
aplica a los componentes y a los dispositivos en proceso, así como dispositivos terminados. Por lo
tanto, la validación del proceso puede aplicarse a procesos que generan componentes, dispositivos
en proceso o dispositivos terminados.
Procedimientos de validación de procesos
Algunas organizaciones tienen procedimientos generales de validación de procesos. Otras
organizaciones establecen procedimientos separados para cada estudio de validación de procesos
individual. Ambos métodos para establecer los procedimientos de validación del proceso son
aceptables.
Revisar una validación
Durante la revisión de un estudio de validación, determinar cuando sea aplicable, si:
Los instrumentos utilizados para generar los datos fueron calibrados y mantenidos
adecuadamente;
Se establecieron especificaciones predeterminadas de productos y procesos;
Los planes de muestreo utilizados para recolectar muestras de prueba se basan en una
lógica estadísticamente válida;
Los datos demuestran que las especificaciones predeterminadas se cumplieron de manera
consistente;
Se desafiaron los límites de tolerancia del proceso;
El equipo de proceso se instaló, ajustó y mantuvo correctamente;
Los instrumentos de monitoreo del proceso fueron calibrados y mantenidos
adecuadamente;
Los cambios en el proceso validado se impugnaron adecuadamente (si corresponde); y
Los operadores de proceso estaban debidamente calificados.
Alcanzar el resultado planificado
MDSAP AU P0002.005 108
Página
Las actividades de validación de procesos son predictivas, más que empíricas. Para un estudio de
validación del proceso para mostrar que el proceso logra el resultado planificado, los criterios de
aceptación deben ser establecidos antes de realizar la validación Los datos del estudio de
validación del proceso deben mostrar que los criterios de aceptación predeterminados se han
cumplido.
Evidencia de No Conformidades
Los estudios de validación de procesos también pueden proporcionar información valiosa sobre No
Conformidades del proceso o producto. Por ejemplo, el estudio de validación del proceso debe
demostrar no solo que el proceso puede producir un resultado o producto que cumple con las
especificaciones predeterminadas, sino también que el proceso producirá consistentemente un
resultado o producto que cumple con las especificaciones predeterminadas. Si las no
conformidades del proceso o del producto relacionadas con un proceso validado se encuentran a
un nivel superior de la tasa anticipada, puede indicar que el estudio de validación del proceso no
confirmó que el proceso podría producir consistentemente un resultado o producto que cumpla con
las especificaciones predeterminadas. A menos que la organización de Dispositivos Médicos lo
haya reconocido durante el estudio de validación del proceso, es posible que no hayan investigado
la causa de la inconsistencia del proceso.
Enlaces
Ninguno
Tarea 9 – Validación del Proceso de Esterilización
Si el producto se suministra estéril (ver Anexo 2):
Verificar que el proceso de esterilización esté validado, re-validado periódicamente, y los
registros de la validación están disponibles.
Verificar que los dispositivos vendidos en un estado estéril se fabriquen y esterilicen bajo
condiciones apropiadamente controladas.
Determinar si el proceso de esterilización y los resultados están documentados y son
trazables a cada lote de producto.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 7.5.5, 7.5.6, 7.5.7;
TGA: TG(MD)R Sch1 2(1) & 8.3, Sch3 P1 1.4(5)(d);
ANVISA: RDC ANVISA 16/2013: 5.1.6, 5.5;
HC: CMDR 17;
MHLW/PMDA: MO169: 6, 44, 45, 46;
FDA: 21 CFR 820.75, 820.184(d)
Requisitos adicionales específicos del país:
Australia (TGA):
Verificar que los métodos de validación de la esterilización tengan en cuenta el estado de la técnica
generalmente reconocido (por ejemplo, las Órdenes Estándar Australianas para Dispositivos
MDSAP AU P0002.005 109
Página
Médicos actuales - MDSO, ISO 11135, ISO 11137, Orden de Normas de Dispositivos Médicos
(Requisitos de Endotoxinas para Dispositivos Médicos) 2018) [TG(MD)R Sch1 P1 2 (1)].
Evaluación de la conformidad:
Validación de procesos de esterilización
Los procesos de esterilización incluyen métodos de esterilización terminal (como radiación y óxido
de etileno) así como métodos de procesamiento aséptico. Los procesos de esterilización deben ser
validados, con revalidación periódica según lo exijan las normas o requisitos establecidos por la
organización de Dispositivos Médicos.
Control de los procesos de fabricación de dispositivos destinados a ser estériles
Además de garantizar que los procesos de limpieza, envasado y esterilización estén validados, los
auditores deben asegurarse de que la organización de Dispositivos Médicos mantenga los
controles apropiados sobre lo siguiente:
Monitoreo de rutina y medición de los procesos de limpieza, empaque y
esterilización.
Criterios de aceptación de rutina de los procesos de limpieza, empaque y
esterilización.
(Re) calificación, (re) verificación, (re) calibración y mantenimiento de los
equipos de limpieza, empaque y esterilización.
Control ambiental de las áreas de producción (diseño y monitoreo de áreas
limpias).
Almacenamiento de piezas del dispositivo, componentes y material de
empaque.
Almacenamiento del producto estéril terminado y gestión de la vida útil.
Procesos de manejo para dispositivos no estériles para re-esterilización.
Enlaces
Ninguno
Tarea 10 – Monitoreo y Medición de la Conformidad del Producto
Verificar que el sistema para monitorear y medir las características del producto sea capaz
de demostrar la conformidad de los productos con los requisitos especificados.
Confirmar que ese riesgo del producto se considera en el tipo y alcance de las actividades
de monitoreo del producto.
Cláusula y Regulación:
ISO: ISO 13485:2016: 7.1, 7.5.1, 8.1, 8.2.6;
TGA: TG(MD)R Sch1 P1 2, Sch3 P1 1.4(5)(b) &(e);
ANVISA: RDC ANVISA 16/2013: 2.4, 5.1.1, 9.1;
MHLW/PMDA: MO169: 26, 40, 54, 58;
FDA: 21 CFR 820.70(a), 820.250(a)
Requisitos adicionales específicos del país:
Ninguno
MDSAP AU P0002.005 110
Página
Evaluación de la conformidad:
Sistemas de monitoreo
El objetivo general de monitorear los procesos y las características del producto durante la
producción es garantizar que los productos se ajusten a los requisitos especificados definidos y
aprobados durante el diseño y desarrollo del dispositivo. La organización de Dispositivos Médicos
tiene la flexibilidad de determinar los controles que son necesarios, acorde con el riesgo para el
dispositivo terminado si las características de los procesos o productos no cumplen los requisitos
especificados. Durante la auditoría de los procesos de producción, confirmar que las medidas de
control son adecuadas para detectar las No Conformidades de procesos o productos.
Enlaces
Ninguno
Tarea 11 – Control, Operación y Monitoreo del Proceso de Producción y
Servicio; Controles de Riesgo
Verificar que los procesos utilizados en la producción y el servicio estén adecuadamente
controlados, monitoreados, operados dentro de los límites especificados y documentados
en los registros de realización del producto.
Además, verificar que las medidas de control de riesgos identificadas por el fabricante para
los procesos de producción son implementados, monitoreados y evaluados.
Cláusula y Regulación:
ISO: ISO 13485: 2016: 7.1, 7.5.1, 8.1, 8.2.5;
TGA: TG (MD) R Sch1 P1 2, Sch3 P1 1,4 (5) (b) y (e);
ANVISA: RDC ANVISA 16/2013: 2.4, 5.1.1, 5.1.6, 8.2, 9.1;
MHLW/PMDA: MO169: 26, 40, 54, 57;
FDA: 21 CFR 820.70 (a), 820.75 (b), 820.250
Requisitos adicionales específicos del país:
Australia (TGA):
Ver Anexo 1
Evaluación de la conformidad:
Control y monitoreo de procesos
Los procesos que pueden causar una desviación de las especificaciones del dispositivo y los
procesos validados deben ser controlados y monitoreados. Los procedimientos de control y
monitoreo pueden incluir las actividades de aceptación de dispositivos terminados y en-proceso,
así como las medidas de control ambiental y de contaminación.
Comparar los procedimientos de monitoreo y aceptación del proceso contenidos o referenciados
dentro de los registros de especificaciones de producción con aquellos disponibles para el personal
de producción. Confirmar que los procedimientos disponibles para el personal de producción son
las revisiones aprobadas más recientes.
MDSAP AU P0002.005 111
Página
Mientras se esté en el área de producción, verificar que el edificio sea de diseño adecuado y
contenga suficiente espacio para realizar las operaciones necesarias. Además, verificar que los
resultados de las actividades de control y monitoreo demuestran que el proceso actualmente está
funcionando de acuerdo con procedimientos. Esto se puede hacer comparando las instrucciones
de trabajo con lo que realmente se está haciendo, comparar los criterios de aceptación del
producto con los resultados de la actividad de aceptación, revisar las cartas de control contra
requisitos especificados, etc.
Enlaces
Diseño y Desarrollo
Los resultados de diseño para un dispositivo incluyen documentos tales como diagramas, dibujos,
especificaciones, procedimientos, y los procesos de producción que son esenciales para la
fabricación adecuada del dispositivo. Los procesos de producción pueden incluir no solo las
instrucciones de fabricación, sino también controles internos, tales como el tipo y alcance de las
actividades de aceptación, calibración del equipo e intervalos de mantenimiento, controles
ambientales y controles de personal.
Durante la auditoría del Proceso Controles de Producción y Servicio, considerar revisar los
procesos de producción que tienen mayor riesgo o mayor efecto en los resultados esenciales de
diseño.
Tarea 12 – Competencia del Personal
Verificar que el personal sea competente para implementar y mantener los procesos en de
acuerdo con los requisitos identificados por la organización de Dispositivos Médicos.
Cláusula y Regulación:
ISO: ISO 13485:2016: 6.2;
ANVISA: RDC ANVISA 16/2013: 2.3.2;
MHLW/PMDA: MO169: 22;
FDA: 21 CFR 820.25, 820.70(d), 820.75(b)
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Entrenamiento y calificación de personal
Los procesos de producción deben ser realizados por personal adecuadamente capacitado. La
organización de Dispositivos Médicos debe establecer procedimientos para identificar las
necesidades de capacitación y garantizar que todo el personal esté capacitado para realizar
adecuadamente sus responsabilidades asignadas.
Esta capacitación debe estar documentada. Adicionalmente, el personal que realiza procesos
validados debe estar calificado.
MDSAP AU P0002.005 112
Página
Es responsabilidad de la Alta Dirección determinar qué calificaciones son necesarias para el
personal que realiza procesos validados.
Enlaces
Gestión
Durante la auditoría del Proceso Controles de Producción y de Servicio, asegurar de que los
empleados que están involucrados en operaciones clave que afectan la realización del producto y
la calidad del producto han sido entrenados en sus tareas específicas de trabajo, así como en la
política de calidad y objetivos.
Cuando sea apropiado, revisar los registros de entrenamiento para aquellos empleados cuyas
actividades han contribuido al proceso de No Conformidades.
Tarea 13 – Control del Monitoreo y Medición del Dispositivo
Confirmar que la organización de Dispositivos Médicos ha determinado los dispositivos de
monitoreo y medición necesarios para proporcionar evidencia de conformidad con los
requisitos especificados.
Verificar que el equipo de monitoreo y medición utilizado en el control de producción y de
servicio haya sido identificado, ajustado, calibrado y mantenido, y capaz de producir
resultados válidos.
Cláusula y Regulación:
ISO: ISO 13485:2016: 7.5.1, 7.6;
TGA: TG(MD)R Sch3 P1 1.4(5)(e);
ANVISA: RDC ANVISA 16/2013: 5.1.5, 5.4;
MHLW/PMDA: MO169: 40, 53;
FDA: 21 CFR 820.70(g), 820.72
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Mantenimiento y calibración
Mientras se revisa el proceso de producción seleccionado, tomar nota de piezas significativas de
equipos de proceso y piezas significativas de equipos de medición o prueba. Considerar
seleccionar equipo de proceso y de prueba que, si no se controla adecuadamente, podría causar
que los dispositivos no cumplan con los requisitos especificados; o producir resultados inexactos
MDSAP AU P0002.005 113
Página
que podrían conducir a no conformidades no reconocidas. Confirmar que el equipo de producción y
prueba seleccionado para su revisión es adecuado para su propósito previsto y capaz de dar
resultados válidos.
Revisar los procedimientos de mantenimiento, control y calibración (y registros) para el equipo
seleccionado para su revisión. La frecuencia inicial con la que se calibran y mantienen los equipos
de medición y prueba generalmente se basa en las recomendaciones del fabricante del equipo. A
medida que la organización gane experiencia con el equipo, la frecuencia de calibración y
mantenimiento se puede ajustar, de acuerdo con un fundamento documentado.
Exactitud y precisión
Cuando la exactitud y la precisión son un factor en la validez del resultado del equipo de medición,
la exactitud y precisión requeridas deben definirse durante la planificación de la realización del
producto para garantizar que el equipo sea adecuado y capaz de proporcionar resultados válidos.
Revisión de registros
Si el equipo de producción o el equipo de prueba se encuentra fuera de sus requisitos de
mantenimiento o calibración, verificar que la organización de Dispositivos Médicos realizó una
evaluación del efecto de la situación de fuera de tolerancia en los dispositivos en proceso,
terminados o liberados, en función del riesgo. Los registros y procedimientos de ajuste, calibración
y mantenimiento del equipo pueden proporcionar información sobre las no conformidades. Revisar
estos procedimientos y registros para determinar si los procedimientos inadecuados o el
incumplimiento de la organización de Dispositivos Médicos con los procedimientos adecuados
contribuyeron a la no conformidad. Por ejemplo, determinar si la falta de ajuste o mantenimiento del
equipo específico contribuyó a la producción de productos no conformes.
Enlaces
Ninguno
Tarea 14 – Análisis del Impacto del Monitoreo y Medición de Dispositivos
Fuera de Especificaciones
Confirmar que la organización de Dispositivos Médicos evalúa (y registra) la validez de las
mediciones anteriores cuando se determina que el equipo no cumple con los requisitos
especificados, y toma las medidas apropiadas sobre el equipo y cualquier producto
afectado.
Verificar que el control de los dispositivos de monitoreo y medición sea adecuado para
garantizar resultados válidos. Confirmar que los dispositivos de monitoreo y medición estén
protegidos contra daños o deterioro.
Cláusula y Regulación:
ISO: ISO 13485:2016: 7.6;
TGA: TG(MD)R Sch3 P1 1.4(5)(e);
ANVISA: RDC ANVISA 16/2013: 5.4;
MHLW/PMDA: MO169: 53;
FDA: 21 CFR 820.72(a)
Requisitos adicionales específicos del país:
MDSAP AU P0002.005 114
Página
Ninguno
Evaluación de la conformidad:
Control de dispositivos de monitoreo y medición
Las organizaciones deben mantener los controles de calibración, almacenamiento y manejo
adecuados para el equipo de medición, monitoreo y prueba utilizados en el desarrollo, la
producción, la instalación y el servicio del producto. La calibración debe ser trazable a un estándar
de medición nacional o internacional, si hay uno disponible. Si un proveedor proporciona servicios
de calibración, los controles del proveedor se aplicarán para garantizar que la calibración se realice
de manera competente. Los controles apropiados ayudarán a infundir confianza en los resultados
obtenidos del uso del equipo.
Procedimientos
Las organizaciones deben definir, implementar y mantener procedimientos para el control de los
dispositivos de monitoreo y medición. La organización de Dispositivos Médicos puede optar por
desarrollar políticas generales para el control de dispositivos de monitoreo y medición, junto con
procedimientos separados y más específicos para la calibración y el control reales de cada equipo.
Los procedimientos deben tener en cuenta los controles ambientales necesarios para que el equipo
produzca resultados válidos, así como los requisitos específicos de almacenamiento o
manipulación cuando sea necesario. Por ejemplo, un juego de soportes calibrados puede requerir
almacenamiento en una funda acolchada para mantener la exactitud y precisión requeridas.
Confirmar que la organización cuenta con los procedimientos y controles adecuados para preservar
el funcionamiento adecuado de los equipos de monitoreo, medición y prueba.
Cuando el equipo se encuentra fuera de tolerancia
La organización de Dispositivos Médicos puede descubrir que el equipo de monitoreo o medición
ya no se encuentra dentro de su tolerancia de ajuste o calibración. En estas situaciones, la
organización de Dispositivos Médicos debe evaluar y registrar la validez de los resultados de
medición anteriores y tomar las medidas apropiadas sobre el equipo y cualquier producto afectado.
Enlaces
Ninguno
Tarea 15 – Validación del Software utilizado para el Control del Proceso de
Producción y Servicio
Si el proceso seleccionado está controlado por software o si el software se usa en el equipo
de producción o en el sistema de gestión de calidad, verificar que el software esté validado
para el uso previsto.
La validación del software puede ser parte de la calificación del equipo.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.1.6, 7.5.6, 7.6;
ANVISA: RDC ANVISA 16/2013: 5.5.2;
MHLW/PMDA: MO169: 45, 53;
FDA: 21 CFR 820.70(i)
Requisitos adicionales específicos del país:
MDSAP AU P0002.005 115
Página
Ninguno
Evaluación de la conformidad:
Validación de Software de Producción y Sistema de Calidad
El software de control del proceso de producción (y cualquier otro software utilizado en el sistema
de calidad de la organización) debe validarse para su uso previsto de acuerdo con un protocolo
establecido. Si el proceso de producción que el equipo de auditoría seleccionó para revisión se
controla con software, revisar los documentos y registros de validación del software. Los
documentos y registros de validación de software deben incluir:
Un documento de requisitos de software que describe los usos previstos y las necesidades
del usuario asociadas con el software.
Un protocolo de validación establecido o documento similar que describa las actividades
necesarias para demostrar que se pueden cumplir los requisitos del software.
Registros de los resultados de las actividades de validación de software descritas en el
protocolo de validación de software o documento similar.
Registro que los cambios de software están controlados apropiadamente (cuando
corresponda).
Para el software del sistema de gestión de calidad comercial y el equipo de prueba o producción
controlado por software, puede que para el la organización de Dispositivos Médicos no sea posible,
práctico o necesario revisar el código del software o los diversos casos de prueba de verificación
del software que normalmente realizan. el fabricante del software o equipo. Sin embargo, la
organización de Dispositivos Médicos aún debe asegurarse de que el software pueda funcionar de
acuerdo con las necesidades del fabricante del dispositivo. La validación para confirmar que el
software cumple con las necesidades de la organización de Dispositivos Médicos debe realizarse
de acuerdo con un protocolo o documento similar con criterios de aceptación predeterminados.
Si se utilizan varios sistemas impulsados por software en el proceso de producción, asegurar de
evaluar el (los) sistema (s) con mayor probabilidad de tener un impacto en la capacidad del
dispositivo terminado de cumplir con los requisitos especificados. No todos los sistemas
impulsados por software utilizados en un proceso de producción necesitarán ser auditados durante
cada auditoría.
Enlaces
Ninguno
Tarea 16 – Expediente Maestro del Dispositivo
Determinar si la organización de Dispositivos Médicos ha establecido y mantenido un
archivo para cada tipo de dispositivo que incluye o hace referencia a la ubicación de las
especificaciones del dispositivo, las especificaciones del proceso de producción, los
procedimientos de aseguramiento de calidad, los requisitos de trazabilidad y las
especificaciones de empaquetado y etiquetado y cuando sea aplicable, los requerimientos
de instalación y servicio.
Confirmar que la organización de Dispositivos Médicos haya determinado el alcance de la
trazabilidad según el riesgo que presente el dispositivo en caso de que el dispositivo no
cumpla con los requisitos especificados.
Cláusula y Regulación:
ISO: ISO 13485: 2016: 4.2.1, 4.2.3, 7.1, 7.5.8, 7.5.9.1;
TGA: TG (MD) R Sch3 P1 1,4 (5) (c), (d), (e) & 1,9;
MDSAP AU P0002.005 116
Página
ANVISA: RDC ANVISA 16/2013: 1.2.26, 2.4, 4.2, 5.2, 6.4;
HC: CMDR 9 (2), 21 - 23, 52 - 56, 66 - 68;
MHLW/PMDA: MO169: 6, 26, 47, 48;
FDA: 21 CFR 820.65, 820.181
Requisitos adicionales específicos del país:
Brasil (ANVISA):
Verificar que el fabricante haya establecido y mantenga procedimientos para asegurar la integridad
y para evitar la mezcla accidental de etiquetas, instrucciones y materiales de empaque [RDC
ANVISA 16/2013: 5.2.2.1].
Confirmar que el fabricante se haya asegurado de que las etiquetas se diseñen, impriman y,
cuando corresponda, se apliquen de modo que permanezcan legibles y se adhieran al producto
durante el procesamiento, almacenamiento, manejo y uso [RDC ANVISA 16/2013: 5.2.2.2].
Canadá (HC):
Verificar que el fabricante mantenga evidencia objetiva de que los dispositivos cumplen con los
requisitos de seguridad y efectividad del CMDR [CMDR 9 (2)].
Verificar que los dispositivos vendidos en Canadá tengan etiquetas que cumplan con los requisitos
canadienses de inglés y francés y que contengan el nombre y la dirección del fabricante,
identificador del dispositivo, número de control (para dispositivos de Clase III y IV), contenido de
empaque, esterilidad, caducidad, uso previsto, instrucciones de uso y condiciones de
almacenamiento especiales [CMDR 21-23].
Verificar que el fabricante mantenga registros de distribución con respecto a un dispositivo que
permita una retirada completa y rápida del dispositivo del mercado [CMDR 52-56].
Estados Unidos (FDA):
Si se requiere un número de control para la rastreabilidad, confirmar que dicho número de control
esté o acompañe al dispositivo durante toda la distribución [21 CFR 820.120 (e)].
Evaluación de la conformidad:
Registros
Los registros requeridos para cada tipo o modelo de dispositivo incluyen documentos tales como
diagramas, dibujos, especificaciones y procedimientos asociados con el dispositivo, su
empaquetado y etiquetado; así como los requisitos del sistema de gestión de calidad y del proceso
de producción; y si corresponde, requisitos de instalación y servicio. Los documentos y registros
asociados con los procesos de producción pueden incluir no solo las instrucciones de fabricación,
sino también los controles internos, como el tipo y el alcance de las actividades de aceptación, la
calibración del equipo y los intervalos de mantenimiento, los controles ambientales y los controles
de personal.
Estos documentos y registros proporcionan los requisitos e instrucciones para la fabricación, el
etiquetado, el empaque y las pruebas adecuados del dispositivo para garantizar que se cumplan
MDSAP AU P0002.005 117
Página
los requisitos especificados durante la producción de cada lote de dispositivos. Para los
dispositivos que el equipo de auditoría ha seleccionado para revisar, confirmar que se hayan
establecido los registros requeridos.
Trazabilidad general
Es responsabilidad de la organización de Dispositivos Médicos establecer procedimientos para la
trazabilidad. Para los dispositivos que no están implantados y que no son de soporte vital o de
mantenimiento de la vida, la organización tiene la flexibilidad de determinar qué materias primas y
componentes deben ser trazables, acorde con el riesgo que presenta el dispositivo en caso de que
el componente no lo haga cumplir con los requisitos especificados.
Los sistemas de trazabilidad comúnmente incluyen elementos tales como procedimientos escritos
que describen el sistema de numeración de control que se utilizará, así como la documentación de
números de lote, números de control o números de serie que identifican el lote de componentes,
subconjuntos, dispositivos terminados, empaque y etiquetado para ayudar a su identificación en el
proceso de fabricación.
Enlaces
Diseño y Desarrollo
Durante el diseño y desarrollo del dispositivo, deberían haberse identificado los resultados
esenciales de diseño para el funcionamiento adecuado del dispositivo. Las materias primas, los
componentes y los subconjuntos deberían haber sido considerados para la trazabilidad si sus No
Conformidades pudieran resultar en que el dispositivo terminado no cumpliera con sus requisitos
específicos y funciones esenciales.
Tarea 17 – Registro de Producción; Evidencia del Cumplimiento de
Dispositivos Liberados
Determinar si la organización de Dispositivos Médicos ha establecido y mantenido un
registro de la cantidad fabricada y aprobada para la distribución de cada lote de dispositivos
médicos, el registro se verifica y se aprueba, el dispositivo se fabrica de acuerdo con el
archivo al que se hace referencia en la tarea 16 y si los requisitos para la liberación del
producto se cumplieron y documentaron.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 7.5.1, 7.5.8, 7.5.9.1, 8.2.6;
ANVISA: RDC ANVISA 16/2013: 3.2, 5.2, 6.4;
MHLW/PMDA: MO169: 6, 40, 47, 48, 58;
FDA: 21 CFR 820.120, 820.184
Requisitos adicionales específicos del país:
Brasil (ANVISA):
Verificar que el Registro Histórico del Dispositivo incluye o hace referencia a la siguiente
información: fecha de fabricación; componentes utilizados; cantidad fabricada; resultados de
inspecciones y pruebas; parámetros de procesos especiales; cantidad liberada para distribución;
etiquetado; identificación del número de serie o lote de producción; y liberación final del producto
[RDC ANVISA 16/2013: 3.2.1].
MDSAP AU P0002.005 118
Página
Verificar que la etiqueta no se haya liberado para su almacenamiento o uso hasta que una persona
designada haya examinado la etiqueta para verificar su exactitud. La aprobación, que incluye la
fecha, el nombre y la firma física o electrónica de la persona responsable, debe documentarse en
el Registro Histórico del Dispositivo [RDC ANVISA 16/2013: 5.2.2.3].
Estados Unidos (FDA):
Verificar que la etiqueta no se libere para su almacenamiento o uso hasta que una persona
designada haya examinado la etiqueta para verificar su exactitud, incluyendo, cuando corresponda,
el identificador de dispositivo único (UDI, por sus siglas en inglés) correcto o el Código de Producto
Universal (UPC, por sus siglas en inglés), fecha de caducidad, número de control, instrucciones de
almacenamiento, instrucciones de manejo y cualquier instrucción de procesamiento adicional [21
CFR 820.120 (b)].
Confirmar que la etiqueta se almacena de manera que proporcione una identificación adecuada y
evite confusiones. Verificar que las operaciones de etiquetado y empaquetado estén controladas
para evitar confusiones de etiquetado [21 CFR 820.120 (c) y (d)].
Verificar que la etiqueta y el etiquetado utilizados para cada unidad de producción, lote o kits estén
documentados en el registro del lote, así como cualquier número de control utilizado [21 CFR
820.120 (e), 820.184 (e)].
Evaluación de la conformidad:
Verificar la fabricación del dispositivo
Verificar que cada lote de dispositivos se haya fabricado de acuerdo con las especificaciones del
producto y la producción, teniendo en cuenta que, en algunos casos, un lote puede ser un único
dispositivo. Esta verificación debe incluir una revisión de los controles de compras y las actividades
de aceptación en recepción aplicadas a al menos un componente significativo o materia prima,
dispositivo en proceso o terminado, así como las actividades y resultados de aceptación, registros
de control ambiental y de contaminación (si corresponde) y planes de muestreo para procesos y
controles y monitoreo ambiental.
El registro de cada lote de dispositivos debe incluir, o hacer referencia a la ubicación de la siguiente
información:
Las fechas de fabricación;
La cantidad fabricada;
La cantidad liberada para su distribución;
Los registros de aceptación que demuestran que el dispositivo ha sido fabricado de
acuerdo con los arreglos planificados y las especificaciones del producto definidas;
La identificación primaria y el etiquetado utilizados para cada unidad de producción;
Cualquier identificación del dispositivo y número (s) de control utilizados, incluidos los
identificadores únicos del dispositivo cuando corresponda; y
Una disposición para indicar que el registro ha sido verificado y aprobado.
Determinar si hay problemas
Si, durante la realización de esta tarea de auditoría, el equipo auditor observa evidencia de que el
proceso está fuera del rango de aceptación de la organización de Dispositivos Médicos para los
parámetros de operación o de que existen No Conformidades del producto, confirmar que las No
Conformidades fueron manejadas adecuadamente, con aportes al proceso de Medición, Análisis y
Mejora cuando sea apropiado.
MDSAP AU P0002.005 119
Página
Enlaces
Ninguno
Tarea 18 – Trazabilidad aplicable a Dispositivos Implantables, de Soporte de
Vida o de Sostenimiento de Vida
Si la organización de Dispositivos Médicos fabrica dispositivos médicos implantables
activos o no activos, dispositivos que sostienen la vida o que sostienen (secundarios) la
vida, confirmar que el fabricante mantiene registros de trazabilidad de todos los
componentes, materiales y condiciones del ambiente de trabajo (si éstos pueden causar que
el dispositivo no satisface sus requisitos específicos) además de registros de la identidad
del personal que realiza cualquier inspección o prueba de estos dispositivos.
Confirmar que la organización de Dispositivos Médicos requiere que los agentes o
distribuidores de estos dispositivos mantengan registros de distribución y los ponga a
disposición para su inspección.
Verificar que la organización de Dispositivos Médicos registre el nombre y la dirección de
los consignatarios de envío de estos dispositivos.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 7.5.9.2, 8.2.6;
MHLW/PMDA: MO169: 6, 49, 59;
FDA: 21 CFR 820.65
Requisitos adicionales específicos del país:
Canadá (HC):
Verificar que el fabricante haya identificado los implantes del Anexo 2 y proporcione tarjetas de
registro de implantes con dispositivos o que emplee otro sistema adecuado aprobado por Health
Canada [CMDR 66-68].
Verificar que el fabricante de los dispositivos que figuran en el Anexo 2 de las Regulaciones de
Dispositivos Médicos mantenga registros de distribución de estos dispositivos, así como cualquier
información recibida en las tarjetas de registro de implantes relacionadas con estos dispositivos del
Anexo 2 [CMDR 54].
Estados Unidos (FDA):
Verificar que el fabricante haya implementado un sistema de seguimiento para los dispositivos para
los cuales el fabricante recibió una orden de seguimiento de la FDA. El sistema de seguimiento
debe garantizar que el fabricante pueda rastrear el dispositivo hasta el usuario final. El fabricante
debe realizar auditorías periódicas del sistema de seguimiento [21 CFR 821].
Evaluación de la conformidad:
Trazabilidad de dispositivos implantables, que sostienen la vida o que sostienen la vida
(secundarios)
Las organizaciones de Dispositivos Médicos que producen dispositivos terminados cuya falla
podría ocasionar lesiones graves o daños al usuario deben implementar un sistema de trazabilidad.
El sistema de trazabilidad debe permitir que cada lote de dispositivos terminados sea rastreado por
un número de control o un mecanismo similar en toda la cadena de distribución. Las
organizaciones también deben prever el control y la trazabilidad de los componentes y materiales
MDSAP AU P0002.005 120
Página
utilizados en la fabricación del dispositivo, así como la documentación de las condiciones de
fabricación cuando las condiciones de fabricación pueden hacer que el dispositivo terminado no
cumpla los requisitos especificados (por ejemplo, condiciones de cuarto limpio).
La organización de Dispositivos Médicos puede determinar qué componentes y materias primas
deben ser rastreables utilizando herramientas de gestión de riesgos, como el análisis de riesgos, o
mediante la identificación de los componentes y procesos utilizados para cumplir los resultados
esenciales del diseño del producto.
Seguimiento de Dispositivos Médicos
Algunas autoridades regulatorias que participan en el MDSAP tienen requisitos para rastrear
ciertos tipos de dispositivos para el usuario final. Para las autoridades regulatorias que tienen
requisitos de seguimiento, estos requisitos generalmente se aplican a un subconjunto pequeño de
dispositivos que son de mantenimiento vital o de mantenimiento vital (secundario), destinados a
implantarse por más de un año, o que la autoridad regulatoria considera que son de alto riesgo.
Si la organización de Dispositivos Médicos fabrica o distribuye un dispositivo que cumple con un
requisito de seguimiento, confirmar que la organización cuenta con los sistemas necesarios para
proporcionar el seguimiento de cada dispositivo al usuario final.
El sistema de seguimiento de la organización de Dispositivos Médicos debe ser revisado y auditado
periódicamente por la organización para confirmar que el sistema de seguimiento sea efectivo. El
sistema de seguimiento debe contener el identificador único del dispositivo (UDI, por sus siglas en
inglés), número de lote, número de modelo o número de serie del dispositivo u otro identificador
necesario para proporcionar un seguimiento efectivo de los dispositivos.
Enlaces
Ninguno
Tarea 19 – Identificación del Estatus del Producto
Verificar que la identificación del estado del producto sea adecuada para garantizar que solo
se despache, use o instale el producto que ha pasado las inspecciones y pruebas
requeridas.
Cláusula y Regulación:
ISO: ISO 13485:2016: 7.5.8;
ANVISA: RDC ANVISA 16/2013: 6.1.2, 6.4;
MHLW/PMDA: MO169: 47, 50;
FDA: 21 CFR 820.86
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Identificación
La identificación generalmente se define como la descripción del producto que lo distingue de otro
producto. Las organizaciones deben definir, documentar e implementar procesos para la
identificación y el control del producto, incluidos los componentes, agentes de proceso,
MDSAP AU P0002.005 121
Página
subconjuntos, dispositivos terminados, empaquetado y etiquetado. Esto se puede lograr mediante
el uso de números de parte, números de lote, números de orden de trabajo, cantidades, nombre
del proveedor, y otros medios. El alcance de las actividades de identificación debe basarse en la
complejidad y el riesgo del producto.
Enlaces
Ninguno
Tarea 20 – Propiedad del Cliente
Verificar que la organización de Dispositivos Médicos haya implementado controles para
identificar, verificar, proteger y salvaguardar las propiedades del cliente provistas para su
uso o incorporación en el producto.
Verificar que la organización de Dispositivos Médicos trata la información del paciente y la
información confidencial de salud como propiedad del cliente.
Cláusula y Regulación:
ISO: ISO 13485:2016: 7.5.10;
MHLW/PMDA: MO169: 51
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Protección de la propiedad del cliente
La organización de Dispositivos Médicos es responsable de salvaguardar la propiedad del cliente
mientras se encuentre bajo el control de la organización. Si alguna propiedad del cliente se pierde,
daña o no es adecuada para su uso, debe notificarse al cliente y mantenerse registros.
Enlaces
Ninguno
Tarea 21 – Actividades de Aceptación
Verificar que las actividades de aceptación aseguran la conformidad con las
especificaciones y están documentadas.
Confirmar que el alcance de las actividades de aceptación es proporcional al riesgo
planteado por el dispositivo.
Nota: las actividades de aceptación se aplican a cualquier componente, subconjunto o servicio
entrante, independientemente del acuerdo financiero o comercial de la organización de Dispositivos
Médicos con el proveedor.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 7.4.3, 7.5.8, 8.2.6;
MDSAP AU P0002.005 122
Página
TGA: TG(MD)R Sch1 P1 2, Sch3 P1 Cl1.4(5)(d);
ANVISA: RDC ANVISA 16/2013: 5.3.1, 5.3.2, 5.3.3, 5.3.4, 9.2;
MHLW/PMDA: MO169: 6, 39, 47,58, 59;
FDA: 21 CFR 820.80, 820.250(b)
Requisitos adicionales específicos del país:
Brasil (ANVISA):
Verificar que los planes de muestreo estén definidos y basados en una lógica estadística válida.
Cada fabricante debe establecer y mantener procedimientos para garantizar que los métodos de
muestreo sean adecuados para su uso previsto y se revisen regularmente. Una revisión de los
planes de muestreo debe considerar la ocurrencia de productos no conformes, informes de
auditoría de calidad, quejas y otros indicadores [RDC ANVISA 16/2013: 9.2].
Estados Unidos (FDA):
Verificar que el fabricante establezca y mantenga procedimientos para asegurar que los métodos
de muestreo sean adecuados para su uso previsto y que, cuando se produzcan cambios, se
revisen los planes de muestreo [21 CFR 820.250 (b)].
Evaluación de la conformidad:
Actividades reconocidas de aceptación
Se espera que las organizaciones definan, documenten e implementen sistemas y procedimientos
para las actividades de aceptación para verificar que los productos, incluidos los dispositivos
terminados, los dispositivos en proceso, los componentes, el empaque y el etiquetado cumplan con
los requisitos especificados. Las actividades de aceptación reconocidas incluyen, entre otras,
inspecciones, pruebas, revisión de certificados de análisis y auditorías de proveedores. Los
procedimientos y sistemas de aceptación efectivos afectan directamente la capacidad de una
organización para demostrar que el proceso y el producto cumplen con las especificaciones.
Durante la auditoría de las actividades de aceptación para los dispositivos seleccionados para la
auditoría, confirmar que la organización de Dispositivos Médicos haya definido procesos para las
actividades de aceptación en la recepción, en proceso y aceptación final. Determinar si las
actividades de aceptación se han implementado. Una forma de realizar esta tarea de auditoría es
revisar una muestra de registros de lotes y confirmar que las actividades de aceptación se han
documentado y que las actividades de aceptación muestran que se han cumplido los requisitos
especificados. Los registros deben identificar quién realizó las actividades de aceptación.
Se debe identificar el estado de aceptación de los dispositivos entrantes, en proceso y terminados.
La identificación del estado de aceptación debe mantenerse durante la fabricación, el empaque, el
etiquetado y, cuando corresponda, la instalación y el servicio para asegurar que solo se distribuya,
utilice o instale el producto que haya pasado las actividades de aceptación requeridas.
Actividades de aceptación que involucran a empresas relacionadas
El equipo de auditoría puede encontrar situaciones en las que la organización de Dispositivos
Médicos recibe productos recibidos de un afiliado financiero o corporativo. Es responsabilidad de la
organización de Dispositivos Médicos receptora realizar y registrar las actividades de aceptación
necesarias para garantizar que el producto recibido cumpla con los requisitos especificados, así
como aplicar los controles de compra necesarios al proveedor. Las actividades de aceptación y los
controles de compra se aplican a todos los productos recibidos desde fuera del fabricante final,
independientemente de si la transacción tiene lugar o no, e independientemente de la relación
corporativa o financiera del proveedor con la organización de Dispositivos Médicos.
MDSAP AU P0002.005 123
Página
Muestreo
El equipo de auditoría puede encontrar el uso del muestreo durante las actividades de aceptación.
Por ejemplo, una organización de Dispositivos Médicos puede elegir usar el muestreo para realizar
la aceptación de recepción en un gran lote de componentes entrantes. Cuando se utilizan, los
planes de muestreo deben escribirse y basarse en una lógica estadística válida y una metodología
basada en el riesgo.
Combinación de controles
Un concepto importante para recordar es que la calidad no puede inspeccionarse o probarse en
productos. Las organizaciones deben establecer una combinación adecuada de actividades de
aceptación y controles de compras para garantizar que los productos cumplan con los requisitos
especificados. El tipo y el alcance de las actividades de aceptación pueden basarse en parte en la
cantidad de controles de compras aplicados al proveedor, la capacidad demostrada del proveedor
para proporcionar productos de calidad y el impacto potencial del producto en el dispositivo
terminado, incluido el riesgo que el dispositivo presenta al paciente o usuario si no se cumplen los
requisitos especificados. Las organizaciones que llevan a cabo un control de calidad
exclusivamente dentro de la empresa aún deben evaluar la capacidad de los proveedores para
proporcionar productos aceptables.
Evidencia de actividades de aceptación inadecuadas
El equipo de auditoría puede encontrar instancias en las que el producto se haya considerado
aceptable al completar con éxito las actividades de aceptación, pero posteriormente se demuestra
que el producto no cumple con los requisitos especificados (es decir, falla del dispositivo que
genera la queja del producto). Esto puede indicar que las actividades de aceptación no son
suficientes para identificar las no conformidades. Confirmar que la organización de Dispositivos
Médicos ha tomado las medidas adecuadas para determinar la idoneidad de las actividades de
aceptación.
Enlaces
Compras; Diseño y Desarrollo
El equipo de auditoría debería considerar revisar los controles y requisitos de compra para los
proveedores de productos de mayor riesgo. El equipo auditor también debe considerar revisar los
controles y requisitos de compra para los proveedores de productos que se someten a actividades
de aceptación mínima en el fabricante del dispositivo, particularmente si el producto suministrado
se fabrica utilizando un proceso que requiere validación. Durante la revisión de las actividades de
aceptación, si el equipo de auditoría encuentra situaciones donde los registros de las actividades
de aceptación del producto suministrado revelan productos que no cumplen los requisitos
especificados, considerar seleccionarlos para su revisión durante la auditoría del proceso de
Compras de la organización.
El establecimiento de los controles de compras necesarios y las actividades de aceptación
requeridas es un resultado de diseño. El grado de los controles de compra necesarios y el alcance
de las actividades de aceptación deben basarse en el riesgo que plantea el producto que no
cumple con sus requisitos específicos y resultados de diseño esenciales.
Tarea 22 – Identificación, Control y Disposición de Productos No Conformes
MDSAP AU P0002.005 124
Página
Verificar que la identificación, control y disposición de los productos no conformes es
adecuada, en función del riesgo que la no conformidad representa para el dispositivo que
cumple sus requisitos específicos.
Cláusula y Regulación:
ISO: ISO 13485:2016: 7.5.8, 8.3;
TGA: TG(MD)R Sch1 P1 2, Sch3 P1 Cl1.4(5)(b);
ANVISA: RDC ANVISA 16/2013: 6.5.1, 6.5.2;
MHLW/PMDA: MO169: 47, 50, 60;
FDA: 21 CFR 820.60, 820.90(a), 820.86, 820.100(a)
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Procedimientos
El propósito de controlar el producto no conforme es evitar el uso involuntario y distribución de
productos no conformes, incluidos componentes, agentes de procesamiento, dispositivos en
proceso y dispositivos terminados. Confirmar que la organización de Dispositivos Médicos ha
definido e implementado procedimientos para la identificación, control, segregación, evaluación y
disposición de producto no conforme.
Manejo de productos no conformes
La organización de Dispositivos Médicos puede abordar el producto no conforme tomando medidas
para eliminar la No Conformidad detectada (por ejemplo, clasificar un lote entrante de
componentes para eliminar componentes que no cumplen con las especificaciones), autorizando
su uso, liberación o aceptación en concesión, o tomando acción para evitar su uso original previsto
(por ejemplo, permitir que los componentes o dispositivos se utilicen como unidades de
demostración en conferencias de marketing).
Hasta que se pueda hacer una disposición, la organización de Dispositivos Médicos debe tener un
proceso para identificar adecuadamente producto no conforme para evitar su uso accidental o no
autorizado. Un ejemplo es etiquetar y mover el producto no conforme a un recinto controlado lejos
del área de producción.
Si el producto no conforme se acepta bajo concesión, se deben mantener los registros de la
identidad de la persona que autoriza la concesión.
Si se ha detectado un producto no conforme después de que un producto se haya lanzado y
puesto en uso, la organización de Dispositivos Médicos debe considerar los riesgos asociados con
el dispositivo y puede necesitar considerar un aviso o retiro del mercado.
Evaluación del producto no conforme
La evaluación de una no conformidad debe incluir una determinación de la necesidad de una
investigación y notificación a las personas u organizaciones responsables de la no conformidad,
como un proveedor. Asegurar de que la organización de Dispositivos Médicos haya establecido
MDSAP AU P0002.005 125
Página
adecuadamente una interfaz / interacción entre los procesos para la identificación de productos no
conformes y los procesos para la acción correctiva. Estas interacciones deben ser evidentes en el
Manual de Calidad.
Enlaces
Medición, Análisis y Mejora
El equipo de auditoría debe tener en cuenta cualquier caso en el que la aceptación de productos no
conformes haya conducido a que los dispositivos terminados no cumplan con los requisitos
especificados. Esta información a menudo se puede encontrar en registros de actividades de
aceptación y registros de quejas.
Durante la revisión de las acciones correctivas y preventivas de la organización de Dispositivos
Médicos, los auditores pueden haber observado instancias en las que se encontró que los
productos no conformes eran la causa subyacente de los problemas de calidad y las quejas. El
equipo auditor debe considerar revisar el manejo y la evaluación de la organización de Dispositivos
Médicos de los productos no conformes que se determinó que eran la causa subyacente de los
problemas de calidad.
Asegurar de que el análisis de los datos relacionados con los productos no conformes se considere
como una entrada para el proceso de Medición, Análisis y Mejora de la organización de
Dispositivos Médicos y que se hayan implementado acciones correctivas o preventivas cuando sea
necesario.
Tarea 23 – Retrabajo de Productos No Conformes
Si es necesario volver a trabajar un producto, confirmar que la organización de Dispositivos
Médicos haya determinado los efectos adversos del retrabajo en el producto.
Verificar que el proceso de retrabajo se haya realizado de acuerdo con un procedimiento
aprobado, que los resultados de la revisión se hayan documentado y que el producto
retrabajado se haya vuelto a verificar para demostrar la conformidad con los requisitos.
Cláusula y Regulación:
ISO: ISO 13485:2016: 8.3.4;
ANVISA: RDC ANVISA 16/2013: 6.5.3;
MHLW/PMDA: MO169: 60;
FDA: 21 CFR 820.90(b)
Requisitos adicionales específicos del país:
MDSAP AU P0002.005 126
Página
Ninguno
Evaluación de la conformidad:
Retrabajando producto no conforme
El equipo de auditoría puede encontrar instancias donde la organización de Dispositivos Médicos
ha elegido abordar productos no conformes mediante el retrabajo del componente, subconjunto o
dispositivo terminado. La organización de Dispositivos Médicos debe contar con procedimientos
aprobados adecuados para abordar los productos no conformes destinados a retrabajo. El
producto retrabajado se debe volver a evaluar o volver a analizar para asegurarse de que cumpla
con sus requisitos originales especificados. El retrabajo debe estar documentado.
Tener en cuenta los casos en que la causa subyacente de los problemas de calidad, como las
quejas de que los dispositivos terminados no cumplen los requisitos especificados, se remonta a
los dispositivos que se han retrabajado. Esto puede ser una indicación de que el proceso de
retrabajo no fue adecuado para asegurar que el dispositivo terminado cumpla con las
especificaciones.
Además, el retrabajo de los productos fabricados utilizando procesos validados puede ser una
indicación de que el proceso no puede producir productos consistentemente que cumplan con los
requisitos especificados. Si el equipo de auditoría observa un patrón de productos retrabajados que
se fabrican utilizando un proceso validado, considerar revisar la validación del proceso para
confirmar que la organización de Dispositivos Médicos tiene datos que demuestren que el proceso
es efectivo, reproducible y estable; y que la organización de Dispositivos Médicos está operando el
proceso dentro de los parámetros validados.
Enlaces
Ninguno
Tarea 24 – Preservación del Producto
Verificar que se establezcan y mantengan procedimientos para preservar la conformidad del
producto y las partes constituyentes de un producto durante el procesamiento interno, el
almacenamiento y el transporte al destino previsto. Esta preservación abarca la
identificación, manejo, empaque, almacenamiento y protección, incluidos aquellos
productos con vida útil limitada o que requieren condiciones de almacenamiento especiales.
Cláusula y Regulación:
ISO: ISO 13485:2016: 7.5.8, 7.5.11;
TGA: TG(MD)R Sch1 P1 4&5;
ANVISA: RDC ANVISA 16/2013: 5.2.1, 6.1.1, 6.2.1;
HC: CMDR 14;
MHLW/PMDA: MO169: 47, 52;
FDA: 21 CFR 820.130, 820.140, 820.150, 820.160(a)
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
MDSAP AU P0002.005 127
Página
Asegurar un manejo adecuado
La organización de Dispositivos Médicos debe tener un sistema documentado que defina los
requisitos de manejo del producto en todas las etapas de fabricación para evitar confusiones,
daños y deterioro. Esto puede incluir requisitos específicos para el almacenamiento y envío para
garantizar la preservación del producto a su destino. Por ejemplo, es posible que un dispositivo de
diagnóstico in vitro deba almacenarse y enviarse en estado congelado para mantener la vida útil
adecuada de los reactivos. o las muestras de prueba pueden necesitar ser acondicionadas según
ISTA 2A para cubrir la zona climática australiana (rango de temperatura extrema -29°C-50°C) para
la validación del empaque. Estos requisitos de manejo deberían haberse tenido en cuenta durante
la planificación de la realización del producto para el dispositivo. Cuando sea necesario, confirmar
que se implementen las medidas de control necesarias para garantizar la conformidad del producto
con sus requisitos específicos.
Enlaces
Ninguno
Tarea 25 – Revisión de los Requisitos del Cliente, Registros de Distribución
Confirmar que la organización de Dispositivos Médicos realiza una revisión de los requisitos
del cliente, incluidos los requisitos de la orden de compra, antes del compromiso de la
organización de suministrar un producto a un cliente.
Verificar que la organización de Dispositivos Médicos mantenga la documentación requerida
por las autoridades regulatorias con respecto al mantenimiento de los registros de
distribución.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 5.2, 7.2.2, 7.5.9;
ANVISA: RDC ANVISA 16/2013: 6.3;
MHLW/PMDA: MO169: 6, 11, 28, 48, 49;
FDA: 21 CFR 820.160(a)
Requisitos adicionales específicos del país:
Brasil (ANVISA):
Verificar que el fabricante mantenga registros de distribución que incluyan o hagan referencia a: el
nombre y la dirección del consignatario, la identificación y cantidad de productos enviados, la fecha
de envío y cualquier control numérico utilizado para la trazabilidad [ANVISA RDC 6.3].
Canadá (HC):
Verificar que el fabricante mantenga registros de distribución que contengan información suficiente
para permitir la retirada completa y rápida del dispositivo médico del mercado [CMDR 52-53].
Verificar que los registros de distribución de un dispositivo sean retenidos por el fabricante de una
manera que permita la recuperación oportuna, durante el período más prolongado de (a) la vida útil
proyectada del dispositivo; y (b) dos años después de la fecha de envío del dispositivo [CMDR 55-
56].
MDSAP AU P0002.005 128
Página
Estados Unidos (FDA):
Verificar que el fabricante mantenga registros de distribución que incluyan o hagan referencia a la
ubicación del nombre y la dirección del consignatario inicial, la identificación y la cantidad de
dispositivos enviados; y cualquier número de control utilizado [21 CFR 820.160 (b)].
Evaluación de la conformidad:
Registros de distribución
La organización de Dispositivos Médicos debe mantener registros de distribución que incluyan o
hagan referencia a la ubicación del consignatario inicial, la identificación y cantidad de dispositivos
enviados, la fecha de envío y los números de control utilizados.
Enlaces
Ninguno
Tarea 26 – Actividades de Instalación
Si se requieren actividades de instalación, confirmar que se mantengan los registros de las
actividades de instalación y verificación.
Cláusula y Regulación:
ISO: ISO 13485:2016: 7.5.3;
ANVISA: RDC ANVISA 16/2013: 8.1;
MHLW/PMDA: MO169: 42;
FDA: 21 CFR 820.170
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Actividades de instalación
Cuando se debe instalar un dispositivo para un funcionamiento adecuado, la organización de
Dispositivos Médicos debe establecer procedimientos e instrucciones para garantizar una
instalación adecuada. Estas instrucciones deben estar disponibles para el personal que realiza la
instalación. Las actividades de instalación deben estar documentadas.
Determinar el alcance de la revisión
En ausencia de problemas de calidad identificados relacionados con la instalación del dispositivo
seleccionado, el equipo de auditoría puede optar por limitar la revisión del proceso de instalación a
confirmar que los procedimientos necesarios se encuentran en el lugar adecuado.
Enlaces
Ninguno
Tarea 27 – Actividades de Servicio
Determinar si las actividades de servicio se llevan a cabo y se documentan de acuerdo con
las instrucciones y procedimientos definidos e implementados.
MDSAP AU P0002.005 129
Página
Confirmar que los registros de servicio se utilizan como fuente de datos de calidad en el
proceso de Medición, Análisis y Mejora.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 7.5.4, 8.4;
ANVISA: RDC ANVISA 16/2013: 8.2;
MHLW/PMDA: MO169: 6, 43, 61;
FDA: 21 CFR 820.200
Requisitos adicionales específicos del país:
Brasil (ANVISA):
Confirmar que el fabricante haya establecido y mantenga procedimientos para asegurar que los
registros de las actividades de mantenimiento se mantengan con la siguiente información:
el producto atendido;
el número de control del producto atendido;
la fecha de finalización del servicio;
identificación del proveedor del servicio;
descripción del servicio realizado;
los resultados de las inspecciones y pruebas realizadas [RDC ANVISA 16/2013: 8.2.1].
Verificar que el fabricante revise periódicamente los registros de las actividades de servicio. En los
casos donde el análisis identifica tendencias que presentan peligro o registros que implican muerte
o lesiones graves, se debe iniciar una acción correctiva o preventiva [RDC ANVISA 16/2013: 8.2.2].
Estados Unidos (FDA):
Verificar que cada fabricante que recibe un informe de servicio que representa un evento que debe
ser reportado a la FDA como un informe de dispositivo médico automáticamente considera que el
informe es una queja [21 CFR 820.200 (c)].
Confirmar que los informes de servicio estén documentados e incluyan el nombre del dispositivo
revisado, cualquier identificador de dispositivo único (UDI, por sus siglas en inglés) o código de
producto universal (UPC, por sus siglas en inglés) y cualquier otra identificación de dispositivo y
número (s) de control utilizados y la fecha de servicio [21 CFR 820.200 (d)].
Evaluación de la conformidad:
Procedimientos
Cuando el servicio es un requisito específico, la organización de Dispositivos Médicos debe definir
y mantener procedimientos, instrucciones y procesos para realizar y verificar que las actividades de
servicio cumplan con los requisitos especificados.
Proceso de Servicio
Cuando las organizaciones implementan programas de servicio, la organización de Dispositivos
Médicos debe asegurarse de que los componentes utilizados para la reparación sean aceptables
para el uso previsto, los procedimientos de inspección y prueba estén disponibles, y el equipo de
prueba se mantenga adecuadamente para garantizar que los dispositivos con servicio funcionarán
según lo previsto después del servicio. El personal que realiza actividades de servicio debe tener la
capacitación adecuada.
MDSAP AU P0002.005 130
Página
El equipo de auditoría puede observar instancias donde ocurrieron no conformidades y / o se
recibieron quejas después del servicio del dispositivo. Esto puede indicar que la actividad del
servicio no se controló adecuadamente o que el personal de servicio no cuenta con el equipo, las
instrucciones o la capacitación adecuados para realizar el servicio requerido.
Análisis de informes de servicio
Los informes de servicio pueden ser una fuente importante de datos de calidad para la entrada en
el proceso de Medición, Análisis y Mejora de la organización. Cuando sea necesario, confirmar que
los datos relacionados con los informes de servicio se analicen para una posible acción correctiva o
acción preventiva. Los informes de servicio también se deben analizar para determinar si el evento
del servicio representa un evento adverso que debe notificarse a las autoridades regulatorias.
En algunos casos, las quejas del producto pueden ser registradas inicialmente por la organización
de Dispositivos Médicos como un informe de servicio. Por ejemplo, un usuario puede informar a la
organización de Dispositivos Médicos que un dispositivo de monitoreo de parámetros sanguíneos
del paciente no está funcionando correctamente y requiere servicio. Al recibir el dispositivo del
usuario por la función de servicio de la organización de Dispositivos Médicos, la función de servicio
observa que el motivo por el que el dispositivo de monitoreo no funciona es que un componente
esencial dentro del dispositivo falló prematuramente. Este informe de servicio debe ser considerado
por la organización de Dispositivos Médicos como una queja y analizado por la organización de
Dispositivos Médicos para determinar si un informe de un evento adverso debe ser presentado a
las autoridades regulatorias.
Enlaces
Medición, Análisis y Mejora
Durante la auditoría del proceso de Medición, Análisis y Mejora de la organización de Dispositivos
Médicos, el equipo de auditoría ya pudo haber confirmado que los datos de calidad del análisis de
las actividades de servicio se analizan para una posible acción correctiva o preventiva. Al revisar
los informes de servicio de la organización de Dispositivos Médicos, el equipo de auditoría debe
tener en cuenta los informes de servicio que parecen ser quejas de productos. Asegurar de que los
informes del servicio que parecen ser quejas se hayan abordado de forma adecuada.
En algunos casos, se puede encontrar un problema de calidad similar para un dispositivo en
particular en los informes de servicio y los registros de quejas. En estos casos, confirmar que la
organización de Dispositivos Médicos está tomando las correcciones y / o acciones correctivas
adecuadas considerando que se observa un problema de calidad similar en múltiples fuentes de
datos.
Tarea 28 – Controles de Riesgo aplicados al Transporte, Instalación y
Servicio
Cuando corresponda, verificar que las medidas de control y mitigación de riesgos se
apliquen al transporte, la instalación y el servicio, de acuerdo con las prácticas de gestión
de riesgos de la organización de Dispositivos Médicos.
Cláusula y Regulación:
ISO: ISO 13485:2016: 7.1, 7.5.1, 7.5.3, 7.5.4, 7.5.11;
TGA: TG(MD)R Sch1 P1 2&5;
MDSAP AU P0002.005 131
Página
ANVISA: RDC ANVISA 16/2013: 2.4;
MHLW/PMDA: MO169: 26, 40, 42, 43, 52;
FDA: 21 CFR 820.160(a), 820.170(a), 820.200(a)
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Control de riesgo
Los requisitos para la entrega, instalación y servicio de un dispositivo en particular ya deberían
haber sido evaluados y abordados por la organización de Dispositivos Médicos durante el diseño,
desarrollo y planificación para la realización del producto.
Si se identificaron medidas de control de riesgos que involucran la entrega, instalación y servicio
para un dispositivo en particular, confirmar que los procesos necesarios han sido implementados
para asegurar que las medidas de control de riesgo estén en su lugar. Por ejemplo, una
organización de Dispositivos Médicos puede haber identificado que para que un dispositivo de
imágenes médicas brinde imágenes precisas, el servicio debe ser realizado por personal
capacitado de acuerdo con instrucciones específicas.
Las medidas de control de riesgos pueden incluir advertencias en el dispositivo de imágenes de
que solo personal autorizado debe dar servicio al dispositivo y el diseño de una herramienta única
para acceder al interior del dispositivo que solo se proporciona al personal de servicio autorizado.
Enlaces
Ninguno
Tarea 29 – Compromiso de la Alta Dirección para el Proceso de Producción y
Servicio
Determinar, en base a la evaluación del proceso de control de producción y servicio en
general, si la Alta Dirección proporciona el compromiso necesario con el proceso de control
de producción y de servicio para asegurar que los dispositivos cumplan con los requisitos y
objetivos de calidad especificados.
Cláusula y Regulación:
ISO: ISO 13485:2016: 5.1, 5.2;
ANVISA: RDC ANVISA 16/2013: 2.2.1;
MHLW/PMDA: MO169: 10, 11
Requisitos adicionales específicos del país:
Ninguno
MDSAP AU P0002.005 132
Página
Enlaces
Ninguno
CAPÍTULO 7: COMPRAS
La intención del proceso de Compras es garantizar que los productos y servicios adquiridos,
subcontratados o recibidos de otra manera cumplan con los requisitos especificados. Se espera
que la organización de Dispositivos Médicos establezca y mantenga controles documentados para
planificar y realizar actividades de compras.
Los controles necesarios dependen del efecto del producto en la calidad, seguridad y efectividad
del dispositivo terminado. Los procesos de compra efectivos incorporan requisitos y
especificaciones de compra, la selección de proveedores aceptables en función de la capacidad de
los proveedores para proporcionar productos aceptables, la realización de actividades de
aceptación necesarias y el mantenimiento de los registros de calidad requeridos.
El Representante de la Dirección es responsable de garantizar que los requisitos del sistema de
gestión de calidad se hayan definido, documentado, implementado y mantenido efectivamente.
Antes de la auditoría de cualquier proceso de MDSAP, entrevistar al Representante de la Dirección
(o persona designada) para obtener una visión general del proceso y una idea del conocimiento y
la comprensión de la Alta Dirección acerca del proceso.
El proceso de Compras es integral para los otros procesos de la secuencia de auditoría de
MDSAP. A medida que se realiza la auditoría del proceso de medición, análisis y mejora de la
organización, proceso de diseño y desarrollo y controles de producción y servicio, el equipo auditor
debe evaluar el efecto que el producto adquirido tiene en la calidad del dispositivo terminado. El
equipo de auditoría debe usar información aprendida sobre no conformidades reales y potenciales
de productos y procesos durante la auditoría del proceso de Medición, Análisis y Mejora, elementos
de mayor riesgo y productos de diseño esenciales de los proyectos de diseño revisados durante la
auditoría del proceso de Diseño y Desarrollo, además de importantes procesos de producción y
productos subcontratados identificados durante la auditoría del proceso de Controles de
Producción y de Servicio para tomar decisiones sobre los archivos de evaluación de proveedores
para ser revisados durante la auditoría del proceso de Compras.
El proceso de Compras de la organización de Dispositivos Médicos puede ser revisado junto con el
proceso de Medición, Análisis y Mejora, el proceso de Diseño y Desarrollo, y el proceso de
Controles de Producción y de Servicio, teniendo en cuenta los vínculos del proceso de MSDAP. El
proceso de Compras debe considerarse un proceso crítico para aquellas organizaciones que
subcontratan actividades esenciales como el diseño, desarrollo y / o producción a uno o más
proveedores.
Auditando el Proceso de Compras
MDSAP AU P0002.005 133
Página
Propósito: El objetivo de auditar el proceso de compras es verificar que los procesos de la
organización de Dispositivos Médicos garanticen que los productos (por ejemplo, componentes,
materiales y servicios proporcionados por proveedores, incluidos contratistas y consultores)
cumplan con los requisitos de compra especificados, incluidos los requisitos del sistema de gestión
de calidad. Esto es particularmente importante para aquellas organizaciones que subcontratan
actividades como diseño y desarrollo y / o producción a uno o más proveedores, y cuando el
producto o servicio suministrado no puede verificarse mediante inspección (por ejemplo, servicios
de esterilización). Los proveedores incluyen aquellos proveedores de cualquier producto recibido
del exterior de la organización de Dispositivos Médicos, incluidas las afiliadas corporativas o
financieras, donde el producto tiene un efecto en la posterior realización del producto o en el
producto final.
Resultados: Como resultado de la auditoría del Proceso de Compras, la evidencia objetiva
mostrará si la organización de Dispositivos Médicos ha:
A) Definido, documentado e implementado Procedimiento para asegurar que los productos
adquiridos o suministrados de otro modo se ajusten a los requisitos de compra
especificados.
B) Establecido criterios para la selección, evaluación y reevaluación de proveedores en
función del tipo y la importancia del producto adquirido y el impacto del producto
suministrado en la posterior realización del producto o la calidad del dispositivo terminado.
C) Realizado la evaluación y selección de proveedores en función de la capacidad del
proveedor para cumplir con los requisitos especificados.
D) Asegurado la capacidad continua de los proveedores para proporcionar productos de
calidad que cumplan con los requisitos de compra especificados a través de la
reevaluación.
E) Determinado e implementado una combinación apropiada de controles aplicados a
proveedores junto con actividades de verificación de aceptación para garantizar la
conformidad con los requisitos del sistema de gestión de calidad y del producto, en función
del impacto del producto suministrado en el dispositivo terminado .
Enlaces a Otros Procesos:
Gestión; Diseño y Desarrollo; Medición, Análisis y Mejora; Controles de Producción y Servicio
Tarea 1 – Planeación de las Actividades relativas a Productos Comprados y
Procesos Subcontratados
Verificar que las actividades de planeación describen o identifican productos para comprar
y procesos para subcontratar, los requisitos especificados para los productos comprados,
los requisitos para comprar documentación y registros, los recursos de compra, las
actividades para la aceptación de productos comprados y la gestión de riesgos en la
selección de proveedores y compras.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.1.2, 4.1.3, 4.1.5, 7.1, 7.4.1, 7.4.2, 7.4.3;
TGA: TG(MD)R Sch1 P1 2, Sch3 P1 Cl1.4(5)(d)(ii);
ANVISA: RDC ANVISA16/2013: 2.5.1, 2.4;
MHLW/PMDA: MO169: 5, 26, 37, 38, 39;
FDA: 21 CFR 820.20, 820.50
MDSAP AU P0002.005 134
Página
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Planeación
Al planear la realización del producto, la organización de Dispositivos Médicos debe determinar,
según corresponda, los objetivos y requisitos de calidad para los productos comprados, los
procesos, documentos y recursos específicos de los productos comprados, los criterios para la
aceptación del producto comprado y la verificación, supervisión e inspección requeridas y las
actividades de prueba específicas para los productos comprados. La planificación de la realización
del producto a menudo comienza en el diseño y desarrollo del producto, incluida la traducción del
diseño en las especificaciones de producción. La traducción del diseño en las especificaciones de
producción incluye el establecimiento de requisitos específicos para el producto comprado.
Objetivos de calidad
Los objetivos de calidad generalmente se expresan como un objetivo o meta mensurable. La
planificación de la realización del producto debe incluir la consideración de cómo el producto
comprado, los criterios para la aceptación del producto comprado y las actividades requeridas de
verificación, monitoreo, inspección y prueba específicas para el producto adquirido alcanzarán los
objetivos de calidad.
Enlaces
Diseño y Desarrollo, Gestión
Durante la revisión de un proyecto de diseño, confirmar que la organización de Dispositivos
Médicos haya considerado el efecto del producto adquirido en los resultados de diseño esenciales.
Para los proveedores que proporcionan productos y servicios relacionados con los resultados de
diseño esenciales, el grado de controles de compras necesarios es acorde con el efecto del
producto suministrado en el funcionamiento adecuado del dispositivo terminado.
Durante la auditoría del proceso de Compras, confirmar, cuando sea necesario, que el grado de
control sobre los proveedores de productos comprados se haya realizado en función del riesgo que
representa el producto suministrado para la capacidad del dispositivo terminado de cumplir los
requisitos especificados.
Además, confirmar, cuando sea necesario, que los objetivos de calidad relacionados con el
producto adquirido se consideraron para su inclusión en la Revisión por la Dirección.
Tarea 2 – Selección del Expediente de Proveedor para Auditoría
Seleccionar uno o más archivos de evaluación del proveedor para auditar.
Criterios de prioridad para la selección:
MDSAP AU P0002.005 135
Página
1. Indicaciones de problemas con productos o procesos suministrados a partir de la auditoría
del proceso de Medición, Análisis y Mejora.
2. Proveedores de productos o procesos de mayor riesgo.
3. Proveedores que proporcionan productos o servicios que impactan directamente en los
resultados de diseño requeridos para el correcto funcionamiento del dispositivo.
4. Proveedores de procesos que requieren validación o revalidación.
5. Proveedores de productos o servicios recientemente aprobados.
6. Proveedores de productos o servicios utilizados en la fabricación de productos múltiples.
7. Proveedores de componentes o servicios no cubiertos durante auditorías anteriores.
Enlaces
Ninguno
Tarea 3 – Procedimiento para el Control de Productos Comprados y
Procesos Subcontratados
Verificar que se hayan establecido y documentado los procedimientos para asegurar que el
producto comprado cumple con los requisitos de compra.
Cláusula y Regulación:
ISO: ISO 13485:2016: 7.4.1;
TGA: TG(MD)R Sch3 P1 Cl1.4(5)(d)(ii);
ANVISA: RDC ANVISA 16/2013: 2.5.1;
MHLW/PMDA: MO169: 37;
FDA: 21 CFR 820.50
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Procedimientos
La organización de Dispositivos Médicos debe definir, documentar e implementar procedimientos
para asegurar que el producto comprado cumpla con los requisitos especificados. Estos
procedimientos comúnmente contienen información sobre los mecanismos por los cuales la
organización de Dispositivos Médicos categorizará a los proveedores en función del riesgo que
tiene el producto suministrado sobre la capacidad del dispositivo terminado para cumplir con los
requisitos especificados, los criterios que la organización de Dispositivos Médicos tiene para
evaluar a los proveedores, los medios de determinación de que un proveedor es aceptable, los
métodos para el monitoreo del proveedor, los requisitos para la reevaluación de los proveedores y
los medios por los cuales se puede determinar que un proveedor es inaceptable.
Es importante recordar que los requisitos para los controles de compra se aplican a todos los
productos recibidos de un proveedor por el cual la organización de Dispositivos Médicos tiene un
impacto en la realización del producto, si un pago ocurre o no, e independientemente de la
afiliación corporativa o financiera entre el proveedor y la organización de Dispositivos Médicos.
Enlaces
Ninguno
MDSAP AU P0002.005 136
Página
Tarea 4 – Extensión de los Controles Aplicados al Proveedor y al Producto
Comprado; Criterios de Selección; Evaluación y Reevaluación del Proveedor
Verificar que los procedimientos aseguran el tipo y el alcance del control aplicado al
proveedor y que el producto comprado depende del efecto del producto adquirido en la
realización posterior del producto o el producto final.
Verificar que los criterios para la selección, evaluación y reevaluación de proveedores se
hayan establecido y documentado.
Cláusula y Regulación:
ISO: ISO 13485:2016: 7.4.1;
ANVISA: RDC ANVISA 16/2013: 2.5.2, 2.5.3;
MHLW/PMDA: MO169: 37;
FDA: 21 CFR 820.50
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Alcance del control
El tipo y el alcance del control aplicado al proveedor deben tener en cuenta el efecto que el
producto suministrado tiene en el dispositivo terminado. Los procedimientos comúnmente
contienen métodos para clasificar a los proveedores, en función de la importancia del producto
suministrado para el correcto funcionamiento del dispositivo terminado y el historial pasado (si
corresponde) del proveedor.
Tener en cuenta las organizaciones que utilizan un enfoque de "talla única" para la gestión de sus
proveedores, ya que estos sistemas pueden no proporcionar la cantidad necesaria de evaluación y
supervisión sobre los proveedores de productos esenciales para el correcto funcionamiento del
dispositivo terminado.
Criterios de evaluación
La organización de Dispositivos Médicos debe definir, documentar e implementar procedimientos
que describan los criterios para la selección, evaluación y reevaluación de los proveedores. Los
procedimientos para la evaluación y selección de proveedores generalmente incluyen elementos
tales como los métodos por los cuales los proveedores serán evaluados y los medios y la
frecuencia con que se monitoreará el desempeño del proveedor.
La evaluación de los proveedores debe proporcionar un medio para evaluar la capacidad del
proveedor para suministrar productos que cumplan con los requisitos especificados. La
organización de Dispositivos Médicos puede evaluar la capacidad de un proveedor para suministrar
productos de calidad de varias maneras, que incluyen, entre otras, la realización de auditorías de
proveedores, inspecciones de primeros artículos, encuestas a proveedores y revisión del historial
pasado del proveedor en el suministro de un producto o servicio similar, si corresponde.
La organización de Dispositivos Médicos también puede optar por considerar la conformidad del
proveedor con los requisitos del sistema de gestión de calidad a través de certificaciones de
MDSAP AU P0002.005 137
Página
terceros; sin embargo, la certificación de terceros no debe confiarse exclusivamente en la
evaluación inicial de un proveedor.
Controles sobre proveedores de procesos de esterilización
Para los dispositivos destinados a ser estériles, la organización de Dispositivos Médicos debe
determinar los criterios que el proveedor debe cumplir para ser seleccionado, con respecto al
control de la esterilidad del dispositivo y realizar la selección y el seguimiento de los proveedores
teniendo en cuenta los criterios identificados.
Enlaces
Ninguno
Tarea 5 – Selección del Proveedor en base a la Habilidad para Satisfacer los
requisitos Específicos de Compras
Verificar que los proveedores se seleccionen en función de su capacidad para suministrar
productos o servicios de acuerdo con los requisitos especificados por la Organización de
Dispositivos Médicos.
Confirmar que el grado de control aplicado al proveedor es proporcional a la importancia del
producto o servicio suministrado en la calidad del dispositivo terminado, según el riesgo.
Verificar que se mantengan los registros de las evaluaciones de los proveedores.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 7.1, 7.4.1;
TGA: TG(MD)R Sch1 P1 2;
ANVISA: RDC ANVISA 16/2013: 2.3,3, 2.5.3, 2.4;
MHLW/PMDA: MO169: 6, 26, 37;
FDA: 21 CFR 820.50(a)
Requisitos adicionales específicos del país:
Australia (TGA):
Los procedimientos de evaluación de la conformidad requieren que un fabricante demuestre el
cumplimiento de los Principios Esenciales mediante la aplicación de un SGC. Por lo tanto, un
fabricante debe mostrar cómo se han aplicado los principios de gestión de riesgos durante el
diseño y la construcción, incluida la compra, para mitigar el riesgo. (EP 2 - TG (MD) R Sch1 P1 2).
Las condiciones de la autorización de comercialización (inclusión de ARTG) requieren que los
patrocinadores australianos lleven a cabo algunas actividades regulatorias que incluyen; manejo de
quejas del cliente (Act s 41FN, Reg 5.8), la gestión y comunicación de archivos técnicos /
documentación técnica (Ley s 41FN (3)), reporte de eventos adversos (Act s 41FN, Reg 5.7),
realización de retiros (Parte 4-9) ), asegurando que el nombre y la dirección del Patrocinador se
proporcionen con el dispositivo (Reg 10.2), el almacenamiento de dispositivos (Act s 41FN, Reg
5.9) y el mantenimiento de registros de quejas y distribución (Act s 41FN, Reg 5.10). Algunos
patrocinadores también brindan servicios para la instalación y el mantenimiento de un dispositivo
en nombre del fabricante. Cuando un requisito reglamentario para un Patrocinador se cruza con un
requisito reglamentario o un requisito de ISO13485 para el Fabricante, la actividad debe tratarse
como una actividad subcontratada y documentarse en el SGC del Fabricante. Verificar que el
Fabricante tenga controles de proveedores adecuados para mitigar el riesgo y asegurar que el
MDSAP AU P0002.005 138
Página
Patrocinador cumpla con las actividades subcontratadas incluidas en un acuerdo escrito [TG Act
41FN] para esas actividades.
Otras actividades que pueden subcontratarse al Patrocinador incluyen la presentación de
solicitudes en nombre del Fabricante a la TGA [TG Act s41EB], que representa al Fabricante en
interacciones con la TGA [TG Act s41FN (3)], como intermediario en las retiradas de productos.
[TG (MD) R Sch 3 - Parte 1: 1.4 (3)], en la notificación de cambios sustanciales a un tipo de
dispositivo médico (TG Act s41BE) que pueden requerir una variación a una entrada en el Registro
Australiano de Productos Terapéuticos (TG Act s9D), para la provisión de registros [TG (MD) R
Anexo 3 - Parte 1: 1.5, 1.9], u otros asuntos que puedan ser requeridos para permitir que el
Patrocinador cumpla con las condiciones de autorización de mercado [TG Act Parte 4- 5 Div 2].
El requisito de la Regulación 10.2 para “asegurar que el nombre y la dirección del Patrocinador se
proporcionen con el dispositivo de tal manera que el usuario del dispositivo pueda identificar
fácilmente al Patrocinador” es solo una obligación del Patrocinador. Esta actividad no necesita
estar incluida en la documentación del SGC del fabricante, sin embargo, los arreglos para el
suministro de esta información deben ser divulgados en el acuerdo escrito entre el fabricante y el
patrocinador. En los casos en que una actividad realizada por el Patrocinador también incluya la
provisión de información requerida por el Principio Esencial 13 (Etiquetas e IFU) o 13A (tarjetas de
implantes y folletos), el Fabricante debe tratar al Patrocinador como proveedor de esa actividad.
El Patrocinador no necesita ser tratado como un proveedor si el alcance del sistema de gestión de
calidad del Fabricante incluye el sitio y las actividades del Patrocinador. La supervisión de las
actividades de los patrocinadores debe estar claramente documentada en el SGC y debe incluirse
en los planes de auditoría interna.
Canadá (HC):
Verificar que cualquier corresponsal regulatorio utilizado por el fabricante se trate como un
proveedor y esté adecuadamente calificado.
Japón (MHLW):
Titular de la Autorización de Comercialización
Si el titular de la autorización de comercialización (MAH, por sus siglas en inglés) subcontrata
cualquier proceso que afecte la conformidad del producto con requisitos, a un sitio de fabricación
registrado (RMS, por sus siglas en inglés), entonces, verificar que el MAH haya realizado la
verificación necesaria de que el RMS tiene un Sistema de Gestión de Calidad apropiado. Si el sitio
de un proveedor es un sitio de fabricación registrado, entonces verificar que el MAH haya realizado
la verificación de que el proveedor tiene un sistema de gestión de calidad apropiado [MHLW
MO169: 65].
Sitio de Fabricación Registrado
Si el RMS ha tercerizado cualquier proceso que afecte la conformidad del producto con los
requisitos, a otro RMS, verificar que el RMS subcontratado haya realizado la verificación necesaria
de que el RMS subcontratado tenga un Sistema de Gestión de Calidad apropiado. Si el sitio de un
proveedor es un RMS, verificar que en los controles de compra del RMS se ha llevado a cabo la
verificación necesaria de que el proveedor posee un Sistema de Gestión de Calidad apropiado
[MHLW MO169: 65].
MDSAP AU P0002.005 139
Página
Evaluación de la conformidad:
Selección de proveedores
La selección de proveedores debe basarse en criterios definidos. Un concepto importante para
recordar es que la calidad no puede inspeccionarse o probarse en productos. Las organizaciones
de Dispositivos Médicos que decidan realizar el control de calidad del producto únicamente dentro
de la empresa deben evaluar la capacidad de los proveedores para proporcionar productos
aceptables.
Algunas organizaciones requieren que los proveedores mantengan varios tipos de certificaciones o
registros. Si bien los registros y las certificaciones de terceros pueden considerarse en las
evaluaciones de los proveedores, la organización no debe confiar exclusivamente en estos
métodos para realizar la evaluación inicial de los proveedores.
Para el (los) proveedor (es) que el equipo de auditoría ha elegido revisar, confirmar que la
selección de la organización del proveedor se basó en criterios definidos acordes con el riesgo
planteado, si el producto suministrado hace que el dispositivo terminado no cumpla con los
requisitos especificados.
Registros de evaluaciones de proveedores
La organización de Dispositivos Médicos debe mantener registros de la evaluación de la capacidad
del proveedor para cumplir con los requisitos especificados. Los registros deben incluir el
mecanismo por el cual se evaluó al proveedor, los resultados de la evaluación y la determinación
de si el proveedor se consideró aceptable.
Para los proveedores que el equipo de auditoría ha seleccionado, revisar la evaluación de parte de
la organización de Dispositivos Médicos de los proveedores. Confirmar que la evaluación se realizó
de acuerdo con los criterios definidos y es acorde con el efecto que el producto suministrado tiene
en los resultados esenciales del diseño.
Enlaces
Diseño y Desarrollo, Controles de Producción y de Servicio
El establecimiento de los controles de compras necesarios y las actividades de aceptación
requeridas es un resultado de diseño. El grado de los controles de compra necesarios y el alcance
de las actividades de aceptación deben basarse en el riesgo que plantea el producto que no
cumple con sus requisitos específicos y resultados esenciales de diseño.
Los auditores pueden encontrar situaciones donde la organización subcontrata procesos que
requieren validación.
Durante la revisión del proceso de Compras, revisar los controles que la organización de
Dispositivos Médicos ha instituido sobre los proveedores que realizan procesos validados. Esto
generalmente incluye confirmar que la organización de Dispositivos Médicos ha revisado los datos
de validación del proceso generados por el proveedor para garantizar que el proceso sea efectivo,
reproducible y estable. Esto puede ser particularmente importante para los procesos validados de
mayor riesgo realizados por los proveedores, ya que el fabricante del dispositivo terminado no tiene
control inmediato sobre esos procesos.
El equipo de auditoría también debería considerar revisar los controles y requisitos de compra para
los proveedores de productos que se someten a actividades de aceptación por parte de la
organización de Dispositivos Médicos.
MDSAP AU P0002.005 140
Página
Tarea 6 – Registros de la Evaluación del Proveedor
Verificar que la organización de Dispositivos Médicos mantenga controles efectivos sobre
los proveedores y el producto, de modo que se sigan cumpliendo los requisitos
especificados.
Cláusula y Regulación:
ISO: ISO 13485:2016: 7.4.1;
ANVISA: RDC ANVISA 16/2013: 2.5.3;
MHLW/PMDA: MO169: 37;
FDA: 21 CFR 820.50(a)
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Monitoreo del desempeño del proveedor
La organización de Dispositivos Médicos debe definir e implementar procesos para monitorear el
desempeño de los proveedores. El monitoreo del desempeño del proveedor no debe basarse
únicamente en consideraciones de costos o entregas a tiempo. El monitoreo de los proveedores
debe tomar en consideración el desempeño real del proveedor en términos de proporcionar
productos que cumplan con los requisitos especificados. Los ejemplos de actividades de
supervisión de proveedores pueden incluir, entre otros, nuevas auditorías de proveedores, análisis
estadísticos de los resultados de aceptación entrantes, supervisión de quejas y no conformidades
relacionadas con el producto suministrado, confirmación independiente del certificado de datos de
conformidad y consideración de las respuestas del proveedor a solicitudes de acción correctiva.
Para que el proveedor pueda mantener un estado como proveedor aceptable, el proveedor debe
ser capaz de suministrar productos que cumplan consistentemente con los requisitos especificados
por la organización de Dispositivos Médicos. Si el monitoreo del proveedor no demuestra que el
proveedor tiene la capacidad de proporcionar productos aceptables, la organización de Dispositivos
Médicos debe contar con los medios para emprender las acciones apropiadas, incluidas
actividades como solicitar medidas correctivas del proveedor y, en algunos casos, eliminar al
proveedor de los registros de proveedores aceptables.
Para los proveedores que el equipo de auditoría ha elegido revisar, confirmar que el monitoreo del
proveedor esté documentado y revisado por las personas adecuadas responsables de la selección
del proveedor. Tener especialmente en cuenta las instancias en las que el producto suministrado
ha causado quejas y / o no conformidades del producto. Verificar que la organización de
Dispositivos Médicos haya realizado el seguimiento adecuado del proveedor y tomado medidas
cuando sea necesario, como solicitar al proveedor que tome una medida correctiva.
Enlaces
Controles de Producción y Servicio, Medición, Análisis y Mejora
Se espera que las organizaciones definan, documenten e implementen sistemas y procedimientos
para las actividades de aceptación para verificar que los productos suministrados cumplan con los
requisitos especificados. Los procedimientos y sistemas de aceptación efectivos afectan
directamente la capacidad de una organización de Dispositivos Médicos para demostrar que los
productos suministrados cumplen con las especificaciones. Durante la auditoría del proceso de
Controles de Producción y de Servicio, confirmar que las actividades de aceptación apropiadas se
MDSAP AU P0002.005 141
Página
hayan implementado y monitoreado para asegurar que el producto recibido cumpla con los
requisitos especificados.
Además, se requiere que las organizaciones determinen, recopilen y analicen datos apropiados
para demostrar la capacidad de los proveedores de proporcionar productos aceptables. Durante la
auditoría del proceso de Medición, Análisis y Mejora, confirmar que el análisis de los datos de
desempeño del proveedor se haya realizado y se haya considerado para acciones correctivas o
preventivas cuando sea necesario.
Tarea 7 – Controles Efectivos sobre Proveedor y Productos
Confirmar que la reevaluación de la capacidad de los proveedores para cumplir con los
requisitos especificados se realice a intervalos consistentes con la importancia del producto
en el dispositivo terminado.
Cláusula y Regulación:
ISO: ISO 13485:2016: 7.4.1;
TGA: TG(MD)R Sch1 P1 2;
ANVISA: RDC ANVISA 16/2013: 2.5.2, 2.4;
MHLW/PMDA: MO169: 37;
FDA: 21 CFR820.50(a)
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Intervalos de reevaluación del proveedor
Las organizaciones deben implementar la combinación adecuada de evaluación de proveedores,
monitoreo de proveedores y actividades de aceptación para proporcionar la confianza necesaria en
la aceptabilidad del producto suministrado. Sin embargo, la evaluación del proveedor no es una
evaluación de "una sola vez". La organización de Dispositivos Médicos debe garantizar la
capacidad continua del proveedor para proporcionar productos que cumplan con los requisitos
especificados. La frecuencia de la reevaluación debe realizarse de acuerdo con los procedimientos
de la organización de Dispositivos Médicos y en intervalos consistentes con la importancia del
producto o servicio en el dispositivo terminado. La frecuencia de la reevaluación puede cambiar en
función de los problemas de calidad identificados con el producto suministrado.
Para el (los) proveedor (es) que el equipo de auditoría ha elegido revisar, confirmar que la
reevaluación del proveedor se realizó de forma acorde con el riesgo que representa el producto
suministrado para la capacidad del dispositivo terminado de cumplir con las especificaciones.
Enlaces
Medición, Análisis y Mejora
La frecuencia y el alcance de las actividades de reevaluación de proveedores pueden basarse, en
parte, en el desempeño del proveedor, como lo demuestran actividades tales como monitoreo
estadístico del proveedor, monitoreo de quejas y No Conformidades relacionadas con el producto
suministrado, y acciones correctivas o preventivas relacionado con el proveedor.
MDSAP AU P0002.005 142
Página
Tarea 8 – Verificación de la Adecuación de la Información de Compras,
Requisitos Específicos de Compras y Acuerdo Escrito sobre Notificación de
Cambios, antes de la Comunicación con el Proveedor
Verificar que la organización de Dispositivos Médicos asegura la adecuación de los
requisitos de compra de los productos y servicios que los proveedores deben proporcionar,
y define las actividades de gestión de riesgos y todas las medidas de control de riesgos
necesarias.
Confirmar que la organización de Dispositivos Médicos asegura la adecuación de los
requisitos de compra especificados antes de su comunicación al proveedor y que se
establece un acuerdo escrito con el proveedor en el que los proveedores deben notificar a la
organización sobre los cambios en el producto.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 7.4.2;
TGA: TG(MD)R Sch1 P1 2;
ANVISA: RDC ANVISA 16/2013: 2.4, 2.5.4, 2.5.6;
MHLW/PMDA: MO169: 6, 38;
FDA: 21 CFR 820.50(b)
Requisitos adicionales específicos del país:
Brasil (ANVISA):
Confirmar que las órdenes de compra sean aprobadas por una persona designada. Esta
aprobación, incluida la fecha y la firma, deberá documentarse [RDC ANVISA 16/2013: 2.5.4].
Evaluación de la conformidad:
Adecuación de la información de compra
La información de compras se proporciona comúnmente a los proveedores en documentos tales
como, entre otros, hojas de especificaciones, dibujos, contratos, órdenes de compra y acuerdos de
calidad. La cantidad de detalles requeridos en la información de compra debe ser acorde con el
efecto del producto suministrado en el rendimiento del dispositivo terminado.
Medidas de control de riesgos
La organización de Dispositivos Médicos es responsable de la calidad y el rendimiento del
dispositivo terminado. Los requisitos especificados para el dispositivo terminado no pueden
cumplirse a menos que las partes individuales del dispositivo terminado cumplan con las
especificaciones. Si bien el fabricante del dispositivo terminado puede requerir que el proveedor
adopte ciertas actividades de administración de riesgos para ayudar a garantizar la aceptabilidad
del producto entrante, la responsabilidad final del dispositivo terminado corre a cargo de la
organización de Dispositivos Médicos. La organización de Dispositivos Médicos es responsable de
identificar las medidas de control de riesgos que se requieren para el producto suministrado. Para
los proveedores que proporcionan productos y servicios relacionados con resultados esenciales de
diseño, el grado de las medidas necesarias de control de riesgos es acorde con el efecto del
producto suministrado en el funcionamiento adecuado del dispositivo terminado.
MDSAP AU P0002.005 143
Página
Algunos ejemplos de medidas de control de riesgos relacionadas con el producto suministrado
incluyen, pero no se limitan a, requerir que el proveedor use procedimientos de aseguramiento de
calidad aprobados por la organización de Dispositivos Médicos, el establecimiento de inspecciones
o pruebas del producto suministrado antes del envío a la organización de Dispositivos Médicos,
requiriendo que cada entrada el envío debe ir acompañado de un certificado de conformidad,
verificación periódica del certificado de conformidad por parte de un análisis de laboratorio de
tercería, implementación de actividades de aceptación en el fabricante del dispositivo terminado
basado en el riesgo que representa el producto suministrado para que el dispositivo terminado
cumpla con las especificaciones , y la verificación de los datos de validación por el fabricante del
dispositivo terminado para los procesos validados realizados por un proveedor.
Para los archivos de los proveedores que los equipos de auditoría han seleccionado para su
revisión, confirmar que las medidas de control de riesgos se hayan identificado cuando
corresponda y que las medidas de control de riesgos se hayan implementado y sean efectivas. Si
el (los) auditor (es) observan que el producto suministrado ha sido identificado como una causa
subyacente de quejas y No Conformidades, esto puede ser una indicación de que las medidas de
control de riesgo son inadecuadas o ineficaces.
Enlaces
Ninguno
Tarea 9 – Información Documentada de Compras y Requisitos Específicos de
Compras
Verificar que la organización de Dispositivos Médicos documente la información de compra,
incluidos, cuando corresponda, los requisitos para la aprobación del producto, los
procedimientos, los procesos, el equipo, la calificación del personal, los servicios de
esterilización y otros requisitos del sistema de gestión de la calidad.
Confirmar que los documentos y registros para la compra sean consistentes con los
requisitos de trazabilidad cuando corresponda.
Cláusula y Regulación:
ISO: ISO 13485:2016: 7.4.2, 7.5.9;
ANVISA: RDC ANVISA 16/2013: 2.3.3, 2.5.4, 2.5.5, 6.4;
MHLW/PMDA: MO169: 38, 48, 49;
FDA: 21 CFR 820.50(b), 820.65, 820.160
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Documentar información de compra
La información de compra debe describir el producto que se comprará, incluidos (cuando
corresponda) los requisitos para la aprobación de productos, procedimientos, procesos y equipos,
los requisitos para la calificación del personal y los requisitos del sistema de gestión de calidad
relacionados con el producto adquirido.
MDSAP AU P0002.005 144
Página
Siempre que sea posible, la información de compra debe contener un acuerdo en el que el
proveedor acuerde notificar a la organización de Dispositivos Médicos de los cambios en los
productos o servicios que puedan afectar la calidad del dispositivo terminado. La organización de
Dispositivos Médicos debe aprobar o rechazar estos cambios, en función del impacto del cambio
en los resultados esenciales de diseño del dispositivo terminado.
La información de compra puede registrarse en formato escrito o electrónico, pero debe estar
documentado.
Trazabilidad
Es responsabilidad de la organización de Dispositivos Médicos establecer procedimientos para la
trazabilidad. Para los dispositivos que no están implantados y que no son de soporte vital o de
mantenimiento de la vida, la organización de Dispositivos Médicos tiene la flexibilidad de
determinar qué materias primas y componentes deben ser trazables, acorde con el riesgo que
presenta el dispositivo en caso de que el componente no lo haga cumplir con los requisitos
especificados.
Las Organizaciones de Dispositivos Médicos cuya falla podría ocasionar lesiones graves o daños al
usuario, o que estén implantados o que sean de soporte vital o que mantengan la vida, deben
implementar un sistema de trazabilidad. El sistema de trazabilidad debe permitir que cada lote de
dispositivos terminados sea rastreado por un número de control o un mecanismo similar en toda la
cadena de distribución. Las organizaciones deben prever el control y la trazabilidad de los
componentes y materiales utilizados en la fabricación del dispositivo cuando estos puedan causar
que el dispositivo terminado no cumpla con los requisitos especificados.
La organización puede determinar qué componentes y materias primas deben ser trazables
utilizando herramientas de gestión de riesgos, como el análisis de riesgos, o mediante la
identificación de los componentes y procesos utilizados para cumplir los resultados esenciales de
diseño.
Enlaces
Ninguno
Tarea 10 – Verificación de Productos Comprados
Confirmar que la verificación (inspección u otras actividades) de los productos comprados
sea adecuada para garantizar que se cumplan los requisitos especificados.
Confirmar que la Organización de Dispositivos Médicos ha implementado una combinación
adecuada de controles aplicados al proveedor, la especificación de los requisitos de
compra y las actividades de verificación de aceptación que son proporcionales al riesgo del
producto suministrado en el dispositivo terminado.
Verificar que los registros de las actividades de verificación se mantienen.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.2.1, 7.1, 7.4.3;
TGA: TG(MD)R Sch1 P1 2, Sch3 1.4(5)(e);
ANVISA: RDC ANVISA 16/2013: 2.4, 2.5.2, 3.35.3.1, 5.3.2, 5.3.3;
MHLW/PMDA: MO169: 6, 26, 39;
FDA: 21 CFR 820.50, 820.80(b)
MDSAP AU P0002.005 145
Página
Requisitos adicionales específicos del país:
Brasil (ANVISA):
Verificar que el fabricante haya establecido y mantenga procedimientos para asegurar la retención
de componentes, materias primas, productos en proceso y productos devueltos hasta que se
hayan realizado y documentado las inspecciones, pruebas u otras verificaciones especificadas
[RDC ANVISA 16/2013: 5.3.3].
Evaluación de la conformidad:
Establecimiento de actividades de aceptación
La organización de Dispositivos Médicos debe establecer una combinación adecuada de
actividades de evaluación del proveedor y de aceptación en recepción para garantizar que los
productos y servicios, incluidos los servicios de esterilización, sean aceptables para su uso
previsto. Después de que un proveedor ha sido aprobado, se deben implementar las actividades de
aceptación necesarias para el producto suministrado. El grado de actividades de aceptación puede
variar según el tipo y la importancia del producto o servicio en la calidad del dispositivo terminado y
el alcance de las medidas realizadas por el proveedor para garantizar la aceptabilidad del producto.
Se espera que las organizaciones definan, documenten e implementen procesos y procedimientos
para las actividades de aceptación para verificar que los productos suministrados cumplan con los
requisitos especificados. Las actividades de aceptación reconocidas incluyen, entre otras,
inspecciones, pruebas, revisiones de certificados de análisis y auditorías de proveedores. Los
procedimientos y sistemas de aceptación efectivos afectan directamente la capacidad de una
organización de Dispositivos Médicos para demostrar que el proceso y el producto cumplen con las
especificaciones.
Es importante recordar que las actividades de aceptación se aplican a cualquier componente,
subconjunto o servicio entrante, independientemente de si el pago se realiza o no, y sin importar el
acuerdo financiero o comercial del fabricante con el proveedor.
Registros de actividades de verificación
Los registros de las actividades de verificación deben mostrar que el producto suministrado cumple
con los requisitos especificados. Si la organización de Dispositivos Médicos encuentra no
conformidades, confirmar que la organización haya manejado adecuadamente la No Conformidad
de acuerdo con los procedimientos establecidos de la organización de Dispositivos Médicos.
La organización de Dispositivos Médicos puede abordar el producto no conforme tomando medidas
para eliminar la no conformidad detectada (por ejemplo, clasificando un lote entrante de
componentes para eliminar componentes que no cumplen con las especificaciones), autorizando
su uso, liberación o aceptación en concesión, o tomando medidas para evitar su uso previsto
original (por ejemplo, permitir que los componentes se usen como ayudas de entrenamiento para
mostrar al personal de producción la diferencia entre un componente aceptable y no aceptable).
Para el (los) producto (s) suministrado (s), que el equipo de auditoría ha elegido revisar, confirmar
que se han mantenido los registros de las actividades de verificación. Una forma de realizar esta
tarea es solicitar una muestra de registros de verificación para el producto elegido y confirmar que
las actividades de aceptación se hayan documentado, incluida la documentación y la disposición
adecuada del producto No Conforme.
Enlaces
MDSAP AU P0002.005 146
Página
Controles de Producción y de Servicio
El equipo de auditoría puede encontrar instancias donde el producto se haya considerado
aceptable al completar con éxito las actividades de aceptación, pero posteriormente se demuestra
que el producto no cumple con los requisitos especificados (por ejemplo, falla del dispositivo debido
a un componente no conforme que ocasiona la queja del producto). Esto puede ser una indicación
de que las actividades de aceptación no son suficientes para identificar las no conformidades; o no
fueron conducidos apropiadamente.
Confirmar que la organización de Dispositivos Médicos ha tomado las medidas adecuadas para
determinar la idoneidad de las actividades de aceptación. Por ejemplo, la organización de
Dispositivos Médicos puede necesitar validar el método de prueba utilizado para la aceptación
entrante para garantizar que el método de prueba sea realmente capaz de identificar el producto
No Conforme.
Tarea 11 – Control de Actividades de Compras como Fuente de Datos de
Calidad para el proceso de Medición, Análisis y Mejora
Verificar que los datos de la evaluación de proveedores, las actividades de verificación y de
compras se consideren como una fuente de datos de calidad para la entrada en el Proceso
de Medición, Análisis y Mejora.
Cláusula y Regulación:
ISO: ISO 13485:2016: 8.4;
ANVISA: RDC ANVISA 16/2013: 7.1.1.1;
MHLW/PMDA: MO169: 61;
FDA: 21 CFR 820.100
Requisitos adicionales específicos del país:
Ninguno
Evaluación de la conformidad:
Recolección y análisis de datos
La organización de Dispositivos Médicos es responsable de garantizar que el producto
suministrado cumpla con los requisitos especificados. Además de la evaluación del proveedor, la
garantía de que el producto suministrado cumple con los requisitos especificados se logra con la
implementación de las actividades de aceptación apropiadas y el monitoreo de las quejas y no
conformidades asociadas con el producto adquirido. Los datos relacionados con las actividades de
aceptación y las no conformidades deben analizarse según corresponda para determinar la
necesidad de una acción correctiva o preventiva.
Enlaces
Medición, Análisis y Mejora
La organización de Dispositivos Médicos debe determinar las actividades de aceptación apropiadas
para el producto suministrado, basado en los resultados esenciales de diseño del dispositivo y el
riesgo que el dispositivo conlleva si no se cumplen los requisitos especificados. Confirmar cuando
sea necesario que el producto suministrado fue evaluado en cuanto al efecto en los resultados
esenciales de diseño del producto. Adicionalmente, verificar que las actividades de aceptación
MDSAP AU P0002.005 147
Página
apropiadas se implementaron en base al efecto potencial que el producto suministrado representa
para los resultados esenciales de diseño.
Se requiere que las organizaciones determinen, recopilen y analicen datos apropiados para
demostrar la capacidad de los proveedores de proporcionar productos aceptables. Durante la
auditoría del proceso de Medición, Análisis y Mejora, confirmar que el análisis de los datos de
desempeño de la evaluación del proveedor y las actividades de monitoreo del proceso del
proveedor se hayan realizado y considerado para la acción correctiva o preventiva cuando sea
necesario.
Tarea 12 – Compromiso de la Alta Dirección para el Proceso de Compras
Determinar, con base en la evaluación general de compra, si la Alta Dirección proporciona el
compromiso necesario para el proceso de compra.
Cláusula y Regulación:
ISO: ISO 13485:2016: 4.1.3, 4.1.5, 5.2;
ANVISA: RDC ANVISA 16/2013: 2.2.1;
MHLW/PMDA: MO169: 5, 11
Requisitos adicionales específicos del país:
Ninguno
Enlaces
Ninguno
ANEXO 1 – AUDITORÍA DE PRODUCTO / PROCESO RELATIVO A
TECNOLOGÍAS Y DOCUMENTACIÓN TÉCNICA
Propósito: Los requisitos para las Organizaciones de Auditoría en IMDRF / MDSAP WG /
N3FINAL: 2016 (Edición 2) incluyen, en la medida de lo posible durante las auditorías in situ y de
acuerdo con el sistema normativo aplicable, aspectos de evaluación que incluyen:
tecnologías relacionadas con productos / procesos (por ejemplo, moldeo por inyección,
esterilización); y
evidencia de documentación técnica adecuada del producto en relación con los requisitos
regulatorios pertinentes.
Se debe notar que:
IMDRF / MDSAP WG / N3FINAL: 2016 (Edición 2) no proporciona requisitos adicionales
para la certificación del producto (ISO / IEC 17065: 2012) o los requisitos de prueba del
producto (ISO / IEC 17025: 2005).
Lo siguiente está explícitamente excluido del alcance de IMDRF / MDSAP: WG / N3FINAL: 2016
(Edición 2) debido a la falta de convergencia regulatoria:
Las revisiones previas a la comercialización (por ejemplo, Exámenes de Dossier de
Diseño, Aplicaciones Premercado, Aplicaciones Shounin, Registro / Notificaciones de
Producto) típicamente realizadas por un especialista (s) de producto; y,
MDSAP AU P0002.005 148
Página
Las decisiones finales de seguridad y rendimiento / efectividad de un dispositivo médico
hechas por cualquier Autoridad Regulatoria.
Definiciones:
Documentación técnica
Evidencia documentada, normalmente una salida del sistema de gestión de calidad (SGC), que
demuestra el cumplimiento de un dispositivo con los requisitos regulatorios para productos y
procesos.
(Adaptado de IMDRF / MDSAP WG / N3FINAL: 2016 (Edición 2) - Sección 3.5)
Experto técnico:
Una persona que lleva a cabo las siguientes funciones en una auditoría:
evaluación de tecnologías relacionadas con productos / procesos;
evaluación de la documentación técnica;
evaluación del cumplimiento de los Reglamentos.
IMDRF / MDSAP WG / N3FINAL: 2016 (Edición 2)
Cláusula 7.1.2. Una Organización de Auditoría tendrá acceso al personal administrativo, técnico y
científico necesario con conocimientos técnicos y experiencia suficiente y adecuada en relación
con los dispositivos médicos y las tecnologías correspondientes.
Cláusula 7.1.5. Una Organización de Auditoría debe ser capaz de llevar a cabo todas las tareas
que se le asignan con el más alto grado de integridad profesional y la competencia técnica
requerida en el campo específico, ya sea que esas tareas sean llevadas a cabo por la misma
Organización de Auditoría o por en su nombre y bajo su responsabilidad.
Cláusula 9.2.4 – Los objetivos de auditoría de la Etapa 2 incluirán específicamente la evaluación
de:
la efectividad del SGC del fabricante que incorpora los requisitos de la normativa
regulatoria aplicable;
tecnologías relacionadas con productos / procesos (por ejemplo, moldeo por inyección,
esterilización);
documentación técnica adecuada del producto en relación con los requisitos regulatorios
pertinentes; y
la capacidad del fabricante para cumplir con estos requisitos.
Cláusula 9.3.2 - Los objetivos de la auditoría de la vigilancia durante el ciclo de auditoría incluirán
específicamente la evaluación de la efectividad del SG del fabricante que incorpora los requisitos
regulatorios aplicables y la capacidad del fabricante para cumplir con estos requisitos.
En adición:
tecnologías nuevas o modificadas relacionadas con productos / procesos (por ejemplo,
moldeo por inyección, esterilización); y
MDSAP AU P0002.005 149
Página
documentación técnica del producto nueva o modificada en relación con los requisitos
regulatorios pertinentes.
Cláusula 9.4.1 -Los objetivos de la auditoría de certificación incluirán específicamente la
evaluación de:
la eficacia del SGC del fabricante que incorpora los requisitos de la normativa regulatoria
aplicable.
tecnologías relacionadas con productos / procesos (por ejemplo, moldeo por inyección,
esterilización);
documentación técnica adecuada del producto en relación con los requisitos de los
reglamentos pertinentes; y
el continuo cumplimiento por parte del fabricante de estos requisitos.
ISO13485: 2016
Cláusula 4.2.3 – Expediente del Dispositivo Médico
Para cada tipo de dispositivo médico o familia de dispositivos médicos, la organización debe
establecer y mantener uno o más expedientes que contienen o hacen referencia a los documentos
generados para demostrar la conformidad con los requisitos de esta Norma Internacional y el
cumplimiento de los requisitos regulatorios aplicables.
El contenido del expediente (s) debe incluir, pero no está limitado a:
descripción general del dispositivo médico, uso / propósito previsto y etiquetado, incluidas
las instrucciones de uso;
especificaciones para el producto;
especificaciones o procedimientos de fabricación, embalaje, almacenamiento,
manipulación y distribución;
procedimientos para medir y monitorear;
según corresponda, requisitos para la instalación;
según corresponda, procedimientos para el servicio.
Cláusula 7.3.10 - Expedientes de Diseño y Desarrollo
La organización de Dispositivos Médicos debe mantener un expediente de diseño y desarrollo para
cada tipo de dispositivo médico o familia de dispositivos médicos. Este expediente incluirá o
referenciará los registros generados para demostrar la conformidad con los requisitos de diseño y
desarrollo, y los registros para los cambios de diseño y desarrollo.
Auditoría de Documentación Técnica
El expediente de dispositivo médico (ISO13485: 2016 Cl 4.2.3) y los expedientes de diseño y
desarrollo (ISO13485: 2016 Cl 7.3.10) deben contener o hacer referencia a documentos para
demostrar el cumplimiento de los requisitos de diseño y los requisitos regulatorios aplicables. Para
cumplir con los requisitos de N3 (Ed. 2), estos registros deben contener documentación técnica del
producto que incluya, entre otros:
MDSAP AU P0002.005 150
Página
Resultados del proceso de diseño y desarrollo, tales como: resultados de diseño, datos de
verificación de diseño con criterios de aceptación, datos de validación de diseño con
criterios de aceptación, un archivo de gestión de riesgos, análisis de factores humanos,
validación de software, etc.),
Resultados de diseño específicos, datos de verificación de diseño con criterios de
aceptación, datos de validación de diseño con criterios de aceptación para productos
donde una autoridad reguladora tiene expectativas específicas para el tipo de evidencia
para demostrar el cumplimiento de los requisitos regulatorios;
Entradas al proceso de controles de producción y servicio, tales como: especificaciones de
producción del dispositivo incluyendo dibujos apropiados, composición, formulación,
especificaciones de componentes y especificaciones de software;
Especificaciones para un proceso de producción que incluye las especificaciones
apropiadas del equipo, los métodos de producción, los procedimientos de producción y las
especificaciones del entorno de producción;
Procedimientos y especificaciones de aseguramiento de calidad, incluidos los criterios de
aceptación y el equipo de aseguramiento de calidad que se utilizará;
Especificaciones para el empaque y etiquetado, incluidos los métodos y procesos
utilizados;
Procedimientos y métodos para la instalación, el mantenimiento y el servicio;
Declaraciones específicas de jurisdicción (por ejemplo, una declaración de conformidad,
declaración sobre la presencia de sustancias específicas, lista de verificación de principios
esenciales, etc.).
La información puede ser una compilación de información documentada o, si los documentos que
constituyen la documentación técnica se mantienen por separado, puede ser un resumen que
incluya una referencia explícita a cada uno de estos documentos.
No se espera que los auditores evalúen completamente los datos que corroboran las decisiones
finales de seguridad y rendimiento / efectividad de un dispositivo médico hechas por cualquier
Autoridad Regulatoria. Sin embargo, se espera que el auditor aplique el modelo MDSAP para la
revisión de la Documentación Técnica cuando audite:
el proceso de diseño y desarrollo (consultar la Tarea de auditoría n.º 3 y siguientes, en el
capítulo 5 de los documentos MDSAP AU P0002 - Modelo de auditoría),
el proceso de controles de producción y servicio (consultar la Tarea de auditoría n.º 16, en
el capítulo 6 de los documentos MDSAP AU P0002 - Modelo de auditoría);
las declaraciones específicas de jurisdicción identificadas en el Proceso de Autorización de
Comercialización de Dispositivos y Registro de Instalación (consultar la tarea de auditoría
n.º 2, en el capítulo 2 de los documentos MDSAP AU P0002 - Modelo de auditoria).
El modelo de auditoría requiere que el auditor seleccione la documentación de diseño y la
documentación del proceso de fabricación para su revisión. La selección se basará en la
información recopilada anteriormente en la auditoría y teniendo en cuenta los riesgos (clasificación
de riesgo) asociados con el dispositivo, la novedad de la tecnología utilizada en el dispositivo y los
procesos de fabricación o métodos de esterilización asociados, junto con cualquier cambio al
dispositivo o procesos de fabricación asociados que han sido implementados por el fabricante
desde la última auditoría in situ, incluidos los cambios no informados controlados por el SGC. Se
debe realizar un mínimo de una revisión por auditoría. Se pueden realizar revisiones adicionales si
el tiempo lo permite o si el auditor sospecha que la documentación técnica previamente revisada
no es una muestra representativa. (Consultar tareas no. 2 en los capítulos 5 y 6).
MDSAP AU P0002.005 151
Página
Las auditorías de vigilancia también deben confirmar que el fabricante tenga los arreglos
establecidos para mantener la vigencia de la documentación técnica para todos los dispositivos.
Por ejemplo:
un procedimiento para revisar la vigencia de las normas relevantes y realizar análisis de
brechas según sea necesario;
un requisito para evaluar los cambios de diseño y la necesidad de más pruebas técnicas; y,
un plan para ensayos clínicos posteriores al mercado, cuando sea necesario, o revisiones
periódicas de literatura.
actualización de los documentos de gestión de riesgos (por ejemplo, niveles de ocurrencia
en el análisis de riesgos) basados en datos posteriores a la comercialización.
La siguiente tabla resume las tareas que un auditor de MDSAP utilizará para revisar la información
que constituye la Documentación Técnica.
Información Modelo de Auditoría: Proceso, Tarea #
Descripción general del Dispositivo Médico,
Diseño y Desarrollo, tarea # 5, 7
incluidas variantes y accesorios
Evidencia del cumplimiento de los requisitos
reglamentarios especificados para productos o
procesos.4
Evidencia de la inclusión de comentarios en la
Diseño y Desarrollo, tarea # 5, 7
gestión de riesgos para monitorear y mantener
los requisitos del producto, así como la
realización del producto o los procesos de
mejora.
Información que confirma que los productos de
diseño y desarrollo para el producto son
Diseño y Desarrollo, tarea # 7
trazables y satisfacen los requisitos de entrada
de diseño
Uso previsto e indicación de uso del dispositivo
Diseño y Desarrollo, tarea # 5, 7, 10, 11
médico
Etiquetado, (es decir, información que
acompaña a un dispositivo médico que se
encuentra en el dispositivo, su embalaje, las Diseño y Desarrollo, tarea # 1, 7, 8, 16
instrucciones de uso y en el material
promocional)
Autorización de Comercialización del
Confirmación de que el producto es un Dispositivo y Registro de Instalaciones, tarea #
dispositivo médico 1
Diseño y Desarrollo, tarea # 5
Autorización de Comercialización del
Dispositivo y Registro de Instalaciones, tarea #
Clasificación
1
Diseño y Desarrollo, tarea # 5
Expediente de Gestión de Riesgo Diseño y Desarrollo, tarea # 8
Datos preclínicos (estudios en modelos Diseño y Desarrollo, tarea # 10
animales, pruebas para respaldar el
cumplimiento de estándares relevantes,
pruebas de rendimiento técnico, etc.)
Evidencia clínica Diseño y Desarrollo, tarea # 11
Procesos de Fabricación Diseño y Desarrollo, tarea # 7, 16
Controles de Producción y Servicio, tarea # 3,
MDSAP AU P0002.005 152
Página
Información Modelo de Auditoría: Proceso, Tarea #
16
Diseño y Desarrollo, tarea # 16
Validación de Proceso Controles de Producción y Servicio, tarea # 7,
8, 9
Evidencia del cumplimiento de los requisitos Autorización de Comercialización del
reglamentarios especificados para la Dispositivo y Registro de Instalaciones, tarea #
autorización de comercialización. 1
Autorización de Comercialización del
Declaración de Conformidad Dispositivo y Registro de Instalaciones, tarea #
1
4
Por ejemplo, Australia - Principios esenciales, Canadá - Requisitos de seguridad y eficacia
Nota: esta tabla puede no abarcar exhaustivamente toda la información esperada en todas las
jurisdicciones.
Se espera que los auditores verifiquen:
la existencia y la coherencia de la información enumerada en esta tabla;
la aplicabilidad de esta información al dispositivo médico sujeto a autorización de
comercialización;
que los métodos implementados a lo largo del Diseño y Desarrollo para generar esta
información son sólidos y acordes con el riesgo asociado con el dispositivo médico;
que las conclusiones están fundamentadas.
Aunque no se espera que los auditores tomen decisiones finales de seguridad y efectividad
basadas en una revisión de la documentación técnica, si un auditor sospecha que existen
inquietudes de seguridad y efectividad del dispositivo, o si falta la evidencia que respalda el
cumplimiento de los requisitos de seguridad y eficacia, las observaciones deben describirse
explícitamente en el informe de auditoría. Si se sospecha una amenaza a la salud pública, se debe
enviar un aviso de comunicación de alerta temprana ("Notificación de 5 días de MDSAP") de
acuerdo con MDSAP AU P0027.001. Actividades y política de tiempo posterior a la auditoría.
La profundidad y el alcance de esta revisión deben ser acordes con la clasificación del dispositivo
médico, la novedad del uso previsto, la novedad de la tecnología o los materiales de construcción,
y la complejidad del diseño y / o la tecnología.
Expectativas de las Autoridades Regulatorias Participantes
Cada regulador participante puede tener diferentes requisitos para la revisión de la documentación
técnica y para la evaluación de la idoneidad de esa documentación técnica en la auditoría.
Si se identifican insuficiencias, las no conformidades se deben plantear de la manera normal,
utilizando la cláusula más específica y relevante de ISO13485, [consultar especialmente ISO
13485: 2016 §4.2.3 y §7.3.10] incluidos los planteados contra la documentación técnica en los
requisitos específicos del país [ver ISO 13485: 2016 §4.2.1.e, §7.2.1.c o §7.3.3.b]. Consultar GHTF
SG3 N19 para obtener más información sobre la clasificación de las no conformidades. Las NC de
la revisión de la documentación técnica se incluirán en el Formulario de Clasificación e Intercambio
de No Conformidad (MDSAP AU F0019.2)
En las siguientes secciones, se brinda más orientación sobre las expectativas para la evidencia del
cumplimiento de los requisitos regulatorios.
Requisitos adicionales específicos del país:
MDSAP AU P0002.005 153
Página
Australia - TGA
Auditoría de la Documentación Técnica:
La evaluación de los requisitos del producto para Australia Clase I (suministrado estéril), I (con una
función de medición), dispositivos médicos IIa y IIb, y Clase 1-3 IVD, es realizada por el regulador
sobre una base de muestreo antes de la autorización de comercialización; por lo tanto, se espera
que la revisión de la documentación técnica se realice en el contexto de la auditoría para aumentar
el conjunto de dispositivos muestreados y fortalecer el enfoque basado en el muestreo. La revisión
de la documentación técnica debe tomar en consideración las disposiciones de IMDRF / MDSAP
WG / N3 - 9.3.1. Esta documentación debe contener detalles suficientes para permitir una
evaluación de los datos y para demostrar:
cumplimiento del requisito; o
donde existe una norma apropiada, cumplimiento de los requisitos del Estándar relevante
que el fabricante ha elegido como medio para demostrar cumplimiento de los requisitos
regulatorios para productos y procesos.
En el caso de los dispositivos médicos de Clase III, Implantable Activo y de Diagnóstico In Vitro de
Clase 4 que han sido sometidos a un Examen de Diseño por separado de la auditoría del SGC, la
auditoría in situ debe garantizar que se mantenga la documentación técnica para estos
dispositivos.
La documentación técnica debe contener, o hacer referencia, evidencia del cumplimiento de los
Principios Esenciales y los siguientes requisitos. Una lista de verificación de Principios Esenciales 5,
aunque no es obligatoria, a menudo se utiliza como índice para identificar los Principios Esenciales
aplicables, cualquier método estándar o validado que se haya utilizado para demostrar el
cumplimiento, y una referencia al documento que contiene la evidencia del cumplimiento.
La evaluación de cada conjunto de documentación técnica seleccionada para el cumplimiento de
los Principios Esenciales, como mínimo, debe consistir en una revisión de:
Una descripción detallada del producto, incluido el uso previsto, el usuario previsto, la
clasificación del riesgo y el código de la Nomenclatura Global de Dispositivos Médicos
(GMDN, por sus siglas en inglés). Para dispositivos médicos IVD, la descripción también
debe incluir tipos de muestras, una lista de componentes del kit, la metodología y cualquier
instrumentación a ser utilizada;
la inclusión de información recopilada en los procesos de retroalimentación (por ejemplo,
quejas, informes de eventos adversos o retiradas para la corrección de productos) como
una entrada potencial en la gestión de riesgos para monitorear y mantener los requisitos
del producto, así como los procesos de realización o mejora del producto;
un índice de la compilación de documentos, o si la documentación no está recopilada, una
referencia a la documentación pertinente;
un archivo de gestión de riesgos (por ejemplo, seleccionar un riesgo particular y confirmar
que se ha gestionado de acuerdo con los requisitos de ISO 14971);
informe (s) seleccionado (s) de datos preclínicos y / o pruebas en banco (incluidos estudios
en modelos animales, pruebas para respaldar el cumplimiento de normas relevantes,
rendimiento técnico y pruebas de seguridad para seguridad eléctrica, seguridad mecánica,
seguridad radiológica, etc.) identificados por el fabricante como evidencia del cumplimiento
de los Principios Esenciales relevantes;
un informe de evaluación clínica seleccionado para confirmar que es actual y fue
preparado por un experto debidamente calificado;
MDSAP AU P0002.005 154
Página
cualquier otra documentación requerida para el tipo de dispositivo (por ejemplo, requisitos
especiales para dispositivos que incorporan sustancias medicinales o materiales de origen
animal);
la información que acompaña a un dispositivo (etiquetado, instrucciones de uso);
la declaración de conformidad (puede estar en un borrador para dispositivos de desarrollo)
que no tienen autorización de comercialización).
5
Como referencia, los fabricantes pueden optar por completar una Lista de verificación de
principios esenciales como una forma de indexar su evidencia de conformidad con los requisitos.
La lista de verificación no es obligatoria; sin embargo, proporciona una forma sucinta de identificar
la evidencia relevante. Una plantilla de muestra está disponible en http://www.tga.gov.au y
buscando "Lista de verificación de principios esenciales".
Brasil - ANVISA
Las regulaciones brasileñas exigen que ANVISA realice por completo el registro /autorización de
comercialización del producto para todas las clases de dispositivos médicos.
ANVISA espera que la Organización de Auditoría siga el Modelo de Auditoría para revisar la
documentación técnica, incluidos los requisitos específicos de Brasil definidos en el documento
MDSAP AU P0002.003 - Modelo de Auditoría. No hay requisitos adicionales para ser revisados
durante una auditoría MDSAP.
Canadá – Health Canada
La Oficina de Dispositivos Médicos de Health Canada ha asignado la responsabilidad de la revisión
de la documentación técnica a la División de Evaluación de Dispositivos. Para Health Canada el
MDSAP AU P0002.005 155
Página
objetivo de las auditorías llevadas a cabo por las organizaciones de auditoría de MDSAP es
determinar que los fabricantes que pretenden licenciar sus dispositivos en Canadá hayan
implementado un SGC de conformidad con los requisitos de la norma internacional ISO 13485 y la
Parte 1 de las regulaciones de dispositivos médicos canadienses. Del mismo modo, un titular de
una licencia de dispositivo médico debe mantener un SGC efectivo. Health Canada espera que las
Organizaciones de Auditoría confirmen durante sus auditorías que el fabricante mantiene evidencia
de seguridad y efectividad y no para determinar que los dispositivos sean seguros y efectivos.
Japón – MHLW / PMDA
La evaluación de los requisitos del producto se realiza antes de la autorización del mercado por
parte del regulador o los organismos de certificación registrados, por lo que la revisión de la
documentación técnica no se realiza en el contexto de la auditoría MDSAP como evaluación de la
conformidad con los Principios Esenciales de Seguridad y Rendimiento de los Dispositivos
Médicos.
Estados Unidos – FDA
Las regulaciones de dispositivos médicos de EEUU no requieren una documentación técnica como
se define en el presente documento, aunque la mayoría de los datos que componen la
documentación técnica son resultado directo del Expediente Histórico del Diseño (820.30 (j) y el
Expediente Maestro del Dispositivo (820.181).
ANEXO 2 – AUDITORÍA DE REQUERIMIENTOS PARA
DISPOSITIVOS MÉDICOS ESTÉRILES
Visión General: El control de la esterilidad de un dispositivo médico es el resultado de una serie
de procesos controlados que incluyen (pero no se limitan a):
Diseño y desarrollo:
a) requisitos de limpieza y esterilidad del dispositivo.
b) compatibilidad del dispositivo con el proceso de esterilización.
c) transporte, almacenamiento y presentación del dispositivo en el punto de uso.
d) compatibilidad del empaque del dispositivo con el proceso de esterilización.
e) capacidad del dispositivo para ser esterilizado o re-esterilizado.
f) requisitos de vida útil y vida del usuario del dispositivo.
g) fundamento para agregar el dispositivo a una familia de productos cubiertos por un
proceso de esterilización validado.
MDSAP AU P0002.005 156
Página
Controles de Producción y de Proceso, según corresponda:
a) validación del proceso de limpieza, empaque de barrera estéril y procesos de
esterilización.
b) monitoreo y medición de rutina de los procesos de limpieza, envasado y
esterilización.
c) criterios de aceptación de rutina de los procesos de limpieza, envasado y
esterilización.
d) (re) calificación, (re) verificación, (re) calibración y mantenimiento de los equipos
de limpieza, embalaje y esterilización.
e) control ambiental de las áreas de producción (diseño y monitoreo de áreas
limpias).
f) almacenamiento de partes del dispositivo, componentes y material de empaque.
g) almacenamiento del producto estéril terminado y gestión de la vida útil.
h) proceso de manipulación del dispositivo no estéril para la re-esterilización.
i) liberación de lotes de dispositivos con esterilización terminal.
Compras, dependiendo del producto o servicio adquirido:
a) Determinación de los criterios que el proveedor debe cumplir para ser
seleccionado, con respecto al control de la esterilidad del dispositivo.
b) Selección y monitoreo de proveedores considerando los criterios identificados.
c) Información de Compras.
d) Verificación del producto / servicio adquirido (y la documentación asociada).
Por lo tanto, la auditoría del control de la esterilidad de un dispositivo médico requiere un enfoque
holístico.
Competencias
Depende de la Organización de Auditoría determinar las competencias requeridas para lograr los
objetivos de la auditoría y asignar un equipo de auditoría competente. Sin embargo, la
Organización de Auditoría debe identificar auditores y / o expertos técnicos que tengan las
competencias identificadas a continuación. La siguiente tabla identifica las competencias
requeridas para auditar varios aspectos de la esterilización.
La auditoría de actividades y procesos que contribuyen a la esterilidad de un dispositivo médico
puede involucrar las siguientes competencias:
Microbiología:
a) Capacidad de evaluar la validación de los procesos y métodos de esterilización
independientemente de la disponibilidad de un estándar establecido (o la falta de dicho
estándar).
b) Capacidad de evaluar la validación de controles de contaminación ambiental y microbiana.
c) Capacidad para evaluar la validación de las actividades de envasado y los sistemas de
barrera estériles.
d) Una persona que se considere tener esta competencia probablemente tendrá la formación
como microbiólogo médico.
Sistemas de Envasado y Barrera Estéril:
MDSAP AU P0002.005 157
Página
a) Capacidad de evaluar la validación de actividades y procesos para sistemas de envasado y
barrera estéril.
Control Ambiental y de Contaminación:
a) Capacidad de evaluar la adecuación de los programas de control de contaminación
ambiental y microbiana.
Esterilización Rutinaria:
a) Capacidad de evaluar la validación de los procesos y métodos de esterilización cuando
existe un estándar establecido sobre el método que no sean procesos asépticos.
b) Capacidad de verificar la implementación de actividades y procesos de esterilización no
estándar previamente auditados por alguien que tenga la competencia en microbiología.
c) Capacidad para evaluar la implementación de actividades y procesos para sistemas de
envasado y barreras estériles previamente auditados por alguien que tenga la competencia
en empaque y los sistemas de barrera estéril o microbiológica.
d) Capacidad de evaluar la implementación de actividades de control ambiental y microbiano
previamente evaluadas por alguien que tenga la competencia en microbiología o control
ambiental y de contaminación.
Un auditor puede poseer varias de estas competencias.
La siguiente tabla resume las competencias requeridas para auditar los requisitos para dispositivos
médicos estériles:
Empaque y Control
Esterilización
Tema evaluado Microbiología Sistemas de Ambiental y de
Rutinaria
Barrera Estéril Contaminación
Proceso de √ √
esterilización (re)
MDSAP AU P0002.005 158
Página
Empaque y Control
Esterilización
Tema evaluado Microbiología Sistemas de Ambiental y de
Rutinaria
Barrera Estéril Contaminación
validación según
estándares bien
establecidos
(excluyendo
procesos
asépticos)
Proceso de
esterilización (re)
validación de
acuerdo con
normas menos
comunes, o el
uso de
esterilizante
√
menos común,
tecnologías de
esterilización,
métodos de
validación
(incluidos los
procesos
asépticos)
Validación del
proceso de
envasado y √ √
sistemas de
barrera estériles
Controles de
contaminación
√ √
ambiental y
microbiana
Implementación
rutinaria de
procesos de
esterilización de
acuerdo con √ √
procesos
validados
previamente
auditados
Implementación
rutinaria de
controles
ambientales y √ √ √
monitoreo
(incluido el
mantenimiento)
Implementación √ √ √
rutinaria de
actividades de
empaque de
acuerdo con
procesos
MDSAP AU P0002.005 159
Página
Empaque y Control
Esterilización
Tema evaluado Microbiología Sistemas de Ambiental y de
Rutinaria
Barrera Estéril Contaminación
previamente
validados
Auditoría de los Requisitos para Consideraciones de Esterilidad y Ciclo de Auditoría:
Todos los requisitos reglamentarios y de ISO 13485 para dispositivos médicos estériles deben
auditarse al menos una vez durante el ciclo de certificación. Si bien las Organizaciones de
Auditoría tienen flexibilidad para decidir cuándo se auditan estos requisitos durante el ciclo de
certificación, deben asegurarse de que los requisitos de esterilidad de un dispositivo hayan sido
auditados antes de incluir este dispositivo en el alcance de la certificación.
Todos los métodos de esterilización utilizados por un fabricante deben estar cubiertos durante todo
el ciclo de certificación.
Los objetivos para la auditoría de requisitos para dispositivos médicos estériles deben incluir, entre
otros, la verificación de que:
todos los procesos que contribuyen a la esterilidad de un dispositivo se controlan a través
del SGC de la organización y la validación se ha completado, según corresponda (por
ejemplo, limpieza, desinfección, procesamiento aséptico, sistemas de barrera estériles,
esterilización terminal, almacenamiento).
los criterios para la revalidación se definen y son seguidos, (por ejemplo, a una
periodicidad definida, después de cambios y tendencias significativos).
los procesos se implementan y monitorean para asegurar el cumplimiento de sus
parámetros validados.
se implementan y monitorean controles rutinarios de limpieza del producto y ambientales.
los resultados son consistentes de lote a lote.
los registros de lote (por ejemplo, un Expediente Histórico del Dispositivo) se mantienen
para cada lote de esterilización según un registro maestro de dispositivo aprobado.
la liberación del lote se realiza para cada lote de acuerdo con un procedimiento y por una
persona designada.
se observa un control adecuado de los proveedores cuando la esterilización se realiza de
forma externa (proceso definido para la selección de proveedores críticos definidos y
seguidos, acuerdos válidos, auditorías de proveedores, etc.).
En ausencia de cambios significativos con impacto potencial en el estado validado o nuevas
actividades de (re) validación desde la auditoría anterior, la auditoría debe centrarse en la revisión
de registros para determinar si se siguen los procesos validados, si se realiza la supervisión y si se
mantienen registros de lotes.
Si bien algunos aspectos se pueden auditar de forma remota (por ejemplo, revisión de la
documentación de validación del proceso de esterilización), la auditoría de los requisitos para los
dispositivos médicos estériles se debe realizar in situ.
El resultado de tales actividades de revisión remota debe servir como entrada para la auditoría in
situ y debe incorporarse o adjuntarse al informe de auditoría de MDSAP. La evaluación externa de
los controles de la esterilidad del producto no debe impedir que el equipo de auditoría en el sitio
siga pistas de auditoría, incluidos los registros de auditoría que requieren la revisión de los
documentos que previamente se habían evaluado de forma remota.
MDSAP AU P0002.005 160
Página
La auditoría de procesos para la validación de sistemas de esterilización y barrera estéril realizados
según estándares bien establecidos (por ejemplo, esterilización por vapor, irradiación gamma de 25
kGy, óxido de etileno en cámaras con liberación tradicional) puede ser realizada por alguien que
tenga la competencia microbiológica o la competencia en esterilización rutinaria.
La auditoría de una validación realizada según estándares menos comunes o utilizando
tecnologías / métodos de esterilización / esterilización menos común (por ejemplo, esterilización
con óxido de etileno en una bolsa, óxido de etileno en cámaras con liberación paramétrica,
esterilización por plasma, esterilización gamma de dosis baja) debe ser realizada por una persona
que tenga la competencia microbiológica. Esto también se aplica a la evaluación de la validación
del proceso aséptico o a la validación del proceso de esterilización de la seguridad microbiológica
de los dispositivos que incorporan sustancias, células, tejidos de origen animal o humano.
La implementación rutinaria de los procesos de esterilización según los estudios de validación
previamente auditados puede ser realizada por una persona que tenga la competencia de
esterilización rutinaria. Esto se aplica a todos los procesos de esterilización previamente validados
y auditados, incluidos los procesos realizados según estándares menos comunes, o el uso de
tecnologías de esterilización / esterilización / métodos de validación menos comunes.
Si los requisitos para dispositivos médicos estériles son auditados por separado por un auditor
competente o un experto técnico, esto deberá cubrir todos los requisitos aplicables y los resultados
de esta auditoría serán parte del informe de auditoría de MDSAP. Esto no debe impedir que el
equipo de auditoría de MDSAP siga las pistas en relación con los requisitos para dispositivos
médicos estériles. Las no conformidades que resulten de la auditoría de dispositivos médicos
estériles y los procesos de esterilización se calificarán de acuerdo con las políticas del MDSAP con
respecto a la calificación de las no conformidades.
ANEXO 3 – EVENTOS ADVEROS DE DISPOSITIVOS MÉDICOS Y
REFERENCIA A PROCESO RÁPIDO DE REPRTE DE
NOTIFICACIONES
La siguiente tabla está destinada a ser una guía de referencia rápida para los plazos para enviar
informes de eventos adversos individuales y avisos de advertencia. Esta tabla no sustituye el
conocimiento y la comprensión con respecto a los criterios que se deben informar en las
jurisdicciones participantes del MDSAP, ni sustituye la información contenida en la Auditoría con
Enfoque MDSAP Capítulo 4: Eventos Adversos de Dispositivos Médicos y Reportes de
Notificación.
MDSAP AU P0002.005 161
Página
Eventos Adversos Notificaciones de
Jurisdicción
Individuales Advertencia
El fabricante debe informar al El fabricante debe informar al
Patrocinador o al TGA, tan Patrocinador o al TGA, tan
pronto como sea posible, si un pronto como sea posible,
evento podría haber cualquier motivo técnico o
provocado la muerte o un médico de un mal
deterioro grave de la salud. funcionamiento o deterioro
que haya llevado a la retirada.
El patrocinador debe informar
en un plazo de 48 horas si un
evento representa una
amenaza para la salud
Australia pública.
El patrocinador debe informar
en un plazo de 10 días si un
evento provocó la muerte o un
deterioro grave de la salud.
El patrocinador debe informar
en un plazo de 30 días si un
evento podría provocar la
muerte o un deterioro grave
de la salud si se repitiera.
Debe informar dentro de las 5 días naturales desde la
72 horas en caso de muerte, decisión de iniciar la acción de
amenaza para la salud pública campo.
o falsificación.
Debe informar dentro de los
10 días en caso de eventos
adversos graves que no
impliquen la muerte y eventos
adversos no graves, cuya
reaparición tenga el potencial
de causar un evento adverso
grave a un paciente, usuario u
otra persona.
Brasil
Debe informar dentro de los
30 días en caso de un mal
funcionamiento que pueda
conducir a un evento adverso
grave.
Debe informar dentro de los
10 días en caso de muerte,
amenaza para la salud pública
o falsificación ocurrida en
otros países y asociada con
productos de salud
registrados a su nombre en
Brasil.
Canadá Para eventos que ocurren en En o antes de emprender el
MDSAP AU P0002.005 162
Página
Eventos Adversos Notificaciones de
Jurisdicción
Individuales Advertencia
Canadá: retiro.
10 días si el evento provocó la
muerte o deterioro grave de la
salud.
30 días si el evento pudiera
provocar la muerte o un
deterioro grave si el evento
volviera a ocurrir.
Para eventos que ocurren
fuera de Canadá:
Tan pronto como sea posible
después de que se tome la
decisión de tomar una acción
correctiva, o tan pronto como
sea posible después de que la
autoridad reguladora del país
en el que ocurrió el incidente
requiera que el fabricante
tome una acción correctiva.
Los sitios de fabricación Tan pronto como sea posible
registrados deben informar después de la acción.
cualquier evento adverso que
cumpla con los criterios
especificados por the
Ordinance for Enforcement
of PMD Act Article 228-20.2
al titular de la autorización de
comercialización lo antes
posible.
Japón
Los MAHs deben reportar
cualquier evento adverso
que cumpla con los criterios
especificados por the
Ordinance for Enforcement
of PMD Act Article 228-20.2
a la Agencia Regulatoria
dentro del plazo
especificado por la
ordenanza.
Estados Unidos 5 días calendario si la FDA ha 10 días hábiles desde el inicio
emitido un aviso de 5 días. de la corrección o remoción.
30 días calendario informes
de muerte o lesiones graves.
Se permiten informes
resumidos trimestrales para
informes de mal
MDSAP AU P0002.005 163
Página
Eventos Adversos Notificaciones de
Jurisdicción
Individuales Advertencia
funcionamiento para la
mayoría de los códigos de
productos.
ANEXO 4 – REQUISITOS PARA ACUERDOS ESCRITOS
Hay varias ocasiones en las que la interfaz entre una organización (por ejemplo, un fabricante
representado en la etiqueta de un producto y el responsable del diseño, producción,
acondicionamiento, etiquetado y actividades de seguimiento de la postproducción) y un proveedor
MDSAP AU P0002.005 164
Página
(una organización externa fuera del alcance del SGC de la organización), debe definirse en un
acuerdo escrito. Por ejemplo, de ISO 13485: 2016;
Cláusula 3.2 – un representante autorizado es una persona física o jurídica establecida dentro de
un país o jurisdicción que ha recibido un mandato por escrito del fabricante para actuar en su
nombre para tareas específicas con respecto a las obligaciones de este último en virtud de la
legislación de ese país o jurisdicción.
Cláusula 3.10 – Nota 1 a la entrada: un fabricante es responsable de garantizar el cumplimiento de
todos los requisitos reglamentarios aplicables a menos que esta responsabilidad sea impuesta
específicamente a otra persona por la autoridad reglamentaria dentro de esa jurisdicción. En
muchos casos, se necesitan acuerdos por escrito para establecer los arreglos entre un fabricante y
un representante autorizado para garantizar que el representante pueda cumplir con sus
obligaciones legales.
Cláusula 4.1.5 – requiere que los fabricantes sigan siendo responsables de la conformidad con los
requisitos reglamentarios aplicables para los procesos subcontratados. Los controles para estos
procesos deben incluir acuerdos de calidad escritos y ser proporcionales a la capacidad de la parte
externa para cumplir con los requisitos identificados en la Cláusula 7.4.
Cláusula 4.2.5 – requiere que los fabricantes definan e implementen métodos para proteger la
información médica confidencial contenida en los registros y para la retención y presentación de
cualquier registro de acuerdo con los requisitos reglamentarios. Los arreglos definidos en los
acuerdos con un Representante autorizado pueden garantizar la confidencialidad de la información
transmitida a un fabricante a través del representante en la recepción y registro de información
para el manejo de quejas y la retención de registros en poder del Representante autorizado.
Cláusula 5.2, 5.4.1, 5.5.2, 5.6.2, 7.2.1, 7.3.3, 7.3.7, 7.3.9 – los acuerdos escritos con los
representantes autorizados pueden ser una herramienta útil para garantizar que un fabricante y su
alta dirección están informados de los requisitos reglamentarios actuales y los cambios en las
jurisdicciones a las que se suministra el producto. Esta información puede proporcionar información
para algunas de las siguientes áreas, entre otras: objetivos de calidad, entradas de revisión por la
dirección, definición de los requisitos del cliente y controles de diseño y desarrollo.
Cláusula 7.2.3 – requiere que un fabricante se comunique con las autoridades reguladoras de
acuerdo con los requisitos regulatorios. En algunas jurisdicciones, el canal de comunicación es a
través del representante autorizado.
Cláusula 7.4.1, 7.4.2 – requiere que el fabricante aborde el incumplimiento de los controles de los
procesos subcontratados, con el proveedor y en cumplimiento de los requisitos reglamentarios. En
algunas jurisdicciones, el representante autorizado debe cumplir con los requisitos reglamentarios
pertinentes con la cooperación del fabricante.
Cláusula 7.5.9.1 – puede requerir que un representante autorizado participe en asegurar la
trazabilidad de un producto en la medida requerida por el fabricante.
Cláusula 8.2.1 – los requisitos reglamentarios pueden requerir que un fabricante incorpore
información de posproducción proporcionada por un representante autorizado para que se incluya
en un proceso de retroalimentación.
Cláusula 8.2.2 – puede ser necesario un acuerdo por escrito con un Representante Autorizado
para garantizar la recepción y el registro oportunos de la información para el manejo de quejas.
Cláusula 8.2.3 – requiere procedimientos documentados para la notificación a las autoridades
reguladoras cuando las quejas cumplen con los criterios de notificación especificados para eventos
adversos o la emisión de avisos. En algunas jurisdicciones, un representante autorizado en el país
MDSAP AU P0002.005 165
Página
realiza la notificación de estos eventos. Es necesario un acuerdo por escrito entre el fabricante y el
representante para establecer un canal de comunicación claro entre el fabricante y el regulador y
para garantizar el mantenimiento de registros de informes.
Cláusula 8.3.3 – requiere procedimientos para emitir Notificaciones de Advertencia de acuerdo con
los requisitos reglamentarios aplicables. En algunas jurisdicciones, se requiere que un
representante en el país coordine la aprobación y emisión de Notificaciones de Advertencian con la
autoridad reguladora local, mantenga registros de distribución que faciliten el retiro en esa
jurisdicción y, si es necesario, para coordinar un retiro bajo la supervisión de la autoridad
reguladora local. Es necesario un acuerdo por escrito entre el fabricante y el representante para
garantizar que el representante local pueda cumplir con sus responsabilidades legales y que las
responsabilidades sean claras en caso de un retiro del mercado.
Requisitos adicionales específicos del país:
Australia - TGA
Antes de obtener la autorización de comercialización, los patrocinadores australianos
(representantes autorizados en el país) deben "certificar asuntos" relacionados con el dispositivo y
su suministro, incluido el compromiso de celebrar acuerdos por escrito con un fabricante extranjero
para los asuntos que se especifican en las regulaciones. [TG Act - 41FD (e) y (g)]. (Los fabricantes
"legales" australianos que son responsables del diseño, la producción y el etiquetado, ya sea
realizado por su organización o en su nombre por otra organización, también son, por definición, un
patrocinador australiano).
Las condiciones posteriores para la autorización de comercialización incluyen el requisito de que el
Patrocinador continúe proporcionando información relacionada con la calidad, la seguridad y el
rendimiento del dispositivo a través de procedimientos y un acuerdo escrito establecido con el
fabricante en el extranjero. Esto incluirá información que solo está disponible del fabricante
extranjero del dispositivo que acepta la responsabilidad del diseño, producción, empaque y
etiquetado, etc. del dispositivo (TG Act - s41BG).
Los procedimientos de evaluación de la conformidad australianos también requieren que los
fabricantes extranjeros de dispositivos médicos suministrados en Australia se comprometan,
proporcionen registros (información, documentos y registros especificados en los Procedimientos
de Evaluación de la Conformidad) y notifiquen a la TGA o al Patrocinador de eventos específicos.
Estos requisitos de los Procedimientos de evaluación de la conformidad y las condiciones para la
autorización de comercialización imponen al Patrocinador la obligación legal de participar en los
procesos que, por lo general y en su totalidad, se tratan en el sistema de gestión de la calidad del
fabricante. Por ejemplo, algunos aspectos de los requisitos de ISO13485 para Notificaciones de
Advertencia (por ejemplo, retiros) son responsabilidad del Patrocinador. Por lo tanto, el fabricante
debe subcontratar estos requisitos al Patrocinador y, al hacerlo, convierte al Patrocinador en un
proveedor.
Al celebrar acuerdos por escrito, el Patrocinador y el Fabricante demuestran su compromiso de
cumplir con sus obligaciones y aclarar sus roles y responsabilidades legales dentro del marco
regulatorio Australiano para dispositivos médicos.
Los fabricantes y patrocinadores deben identificar los requisitos reglamentarios que son relevantes
para sus responsabilidades en virtud de la legislación (por ejemplo, ISO 13485:2016 Cl 4.1.1). La
siguiente tabla proporciona algunas pautas e identifica muchos de los requisitos clave que podrían
identificarse en un acuerdo escrito entre un fabricante extranjero y el patrocinador australiano. Las
MDSAP AU P0002.005 166
Página
partes de un acuerdo deben incorporar, según corresponda, los arreglos para cumplir con estos u
otros requisitos reglamentarios identificados, y pueden incluir los arreglos comerciales necesarios.
Esta tabla es un resumen de los requisitos, con la intención de crear conciencia sobre los roles y
responsabilidades que pueden necesitar aclaración en un acuerdo escrito. Esta es una guía y no
sustituye la referencia a ISO13485: 2016 o la legislación pertinente. Los patrocinadores y
fabricantes deben consultar la Ley de Productos Terapéuticos de 1989 (la Ley) y el Reglamento de
Productos Terapéuticos (Dispositivos Médicos) de 2002 (Reglamentos) para determinar todos los
requisitos aplicables.
Tener en cuenta que algunos requisitos y condiciones se aplican automáticamente por la Ley y los
Reglamentos. La TGA puede aplicar condiciones adicionales específicas sobre la fabricación y
suministro de un dispositivo médico en el momento de la autorización de comercialización, o más
tarde. Es posible que los acuerdos deban enmendarse para tener en cuenta cualquier condición
que posteriormente pueda afectar la relación entre el Patrocinador y el Fabricante.
Las referencias a secciones de la Ley están precedidas por una "s" [por ejemplo, s41FD]. Las
referencias a un reglamento del Reglamento van precedidas de una "r" [p. Ej. r5,8]. Las referencias
a la sección, parte o cláusula de un anexo del Reglamento están precedidas por "S", "P" y "Cl", p.
Ej. [S3 Cl1.8].
Papel del
Papel del
Requisito: Referencia(s): Patrocinador
Fabricante:
Australiano:
Solicitud de s41FC, Certificar los asuntos Proporcionar información al
enumerados en TG Act Patrocinador que le permita
Autorización de s41FD, s41FD, incluido un certificar los asuntos
Comercialización s41FH, procedimiento y un acuerdo identificados en TG Act
s41FI escrito con un fabricante s41FD.
extranjero para
proporcionar información
r5.2 del fabricante extranjero
Proporcionar la información
solicitada por la TGA en un
sobre el cumplimiento de aviso al Patrocinador si la
los Principios Esenciales y aplicación es seleccionada
la aplicación de un para una Auditoría de la
Procedimiento de Aplicación. (Ver también
Evaluación de la Reg 5.3).
Conformidad apropiado, a
la TGA, dentro de los 20
días posteriores a la Si lo solicita la TGA, ayudar
solicitud. al Patrocinador a
proporcionar una cantidad
razonable de muestras
dentro del plazo
especificado en el aviso.
Condiciones para la s41FN, Hacer arreglos que Ayudar al Patrocinador con
permitan que una persona los arreglos para permitir
Autorización de s41FO, autorizada de la TGA que la TGA ingrese a las
Comercialización s41JA, ingrese a las instalaciones instalaciones del
s41MP2, fuera de Australia donde Fabricante, o las de un
s41MPA2 una persona se ocupa de proveedor, para actividades
dispositivos médicos que de inspección.
s42B tienen autorización de
s42BAA mercado, con fines de Si lo solicita la TGA, ayudar
s42DD inspección, examen, al Patrocinador a
s42DJ medición, prueba, proporcionar una cantidad
muestreo, grabación de
s42DL (9) razonable de muestras
imágenes, etc. (Incluidas dentro del plazo
las instalaciones del especificado en el aviso.
r5.6 fabricante o las de un
MDSAP AU P0002.005 167
Página
r5.7, proveedor del fabricante). Asegurar de que el material
publicitario disponible para
r5.8,
Mantener procedimientos y Australia sea coherente con
r5.9 el propósito previsto del
acuerdos para garantizar
r5.10 que la información del dispositivo médico y la
r5.11, fabricante extranjero para obligación del Patrocinador
de cumplir con los
r8.1A corroborar el cumplimiento
de los Principios Esenciales requisitos publicitarios
r8.1 australianos.
y la aplicación de un
Procedimiento de
Evaluación de la Asegurar el suministro
Conformidad apropiado, o continuo de información
los cambios relevantes a la dentro de un plazo que
información suministrada permitirá al Patrocinador
previamente, pueda ser cumplir con sus
proporcionada a la TGA, obligaciones regulatorias.
dentro de los 20 días
posteriores a la solicitud. Asegurar de que la
información sobre
Brindar información a la problemas o quejas,
TGA y al fabricante que el proporcionada por el
patrocinador conozca en Patrocinador, sea una
relación con un dispositivo entrada para el proceso de
sobre cualquier mal retroalimentación del
funcionamiento o deterioro, fabricante.
insuficiencia o uso que
pueda conducir o podría Ayudar al Patrocinador a
haber llevado a la muerte cumplir con las condiciones
de un paciente o usuario de los registros, la
del dispositivo. , oa un fabricación, los principios
deterioro grave en su esenciales, etc. que
estado de salud (eventos puedan imponerse en el
adversos o casi eventos momento de la autorización
adversos) dentro de los de comercialización o
plazos prescritos (r5.7); después de la misma.
Proporcionar información a Brindar al Patrocinador
la TGA (dentro de los información relacionada
plazos prescritos - r5.7) y al con su obligación de
fabricante del que el notificar a la TGA sobre
patrocinador tenga eventos adversos, retiros /
conocimiento en relación avisos de advertencia,
con un dispositivo que se incumplimiento de los
relacione con una razón principios esenciales o la
técnica o médica de un mal validez de un documento
funcionamiento o deterioro de certificación relacionado
que pueda requerir un con el cumplimiento de los
aviso de advertencia o Principios Esenciales o la
retiro del mercado. un aplicación de
dispositivo que ha sido procedimientos de
distribuido; evaluación de la
conformidad; incluidos los
Cumplir con el requisito de requisitos del sistema de
notificar a la TGA de gestión de la calidad.
información que indique
que un documento de Asegurar de que el
certificación emitido Patrocinador conozca los
significa: requisitos del fabricante
cumplimiento de los para el almacenamiento y
principios esenciales; o transporte del dispositivo.
la aplicación de los
procedimientos de
evaluación de la Ayudar al Patrocinador con
conformidad pertinentes se la provisión de datos para
ha restringido, suspendido, un informe a la TGA como
revocado o ya no está en se describe en la Reg 5.11;
vigor. para dispositivos médicos
de Clase AIMD, Clase III,
Clase IIb que son
MDSAP AU P0002.005 168
Página
Proporcionar información a implantables o un IVD de
la TGA y al fabricante que Clase 4.
el patrocinador conozca en
relación con un dispositivo, Ayudar al Patrocinador con
que un dispositivo no la provisión de datos para
cumple con los Principios los IVD descritos en la Reg
Esenciales. 5.3 (1) (j), para un informe
descrito en la Reg 5.12.
Proporcionar al fabricante
de un dispositivo médico Informar al Patrocinador de
información relevante para: cualquier veneno que
las obligaciones del pueda estar presente en el
fabricante en virtud de los dispositivo como se
procedimientos de describe en Reg 5.13.
evaluación de la
conformidad; y si los
dispositivos médicos del Informar al Patrocinador de
fabricante cumplen con los información que indique
principios esenciales. que un certificado u otro
documento (que no sea un
certificado de evaluación de
Asegurar de que los conformidad emitido por
dispositivos cumplan con TGA u otro documento
las disposiciones aplicables emitido por TGA) que el
del Código de publicidad de Patrocinador usó para
productos terapéuticos y certificar asuntos bajo
otros requisitos relevantes s41FC (1) para significar:
(si los hubiera) en la (i) cumplimiento de los
legislación y que el material principios esenciales; o
publicitario sea coherente (ii) la aplicación de los
con el propósito previsto procedimientos de
por el fabricante. evaluación de la
conformidad pertinentes a
Asegurar de que un un producto;
anuncio no contenga una ha sido restringido,
declaración, representación suspendido, revocado o ya
gráfica o diseño que no está en vigor.
sugiera o insinúe que los
productos han sido Asegurar de que los
recomendados o registros de fabricación se
aprobados por un gobierno conserven y estén
o una autoridad disponibles durante un
gubernamental o en su período que sea al menos
nombre (incluido un la vida útil del dispositivo o
gobierno extranjero o una el período mínimo definido
autoridad gubernamental en los procedimientos de
extranjera), excepto en evaluación de la
esas circunstancias. conformidad australianos; 5
descrito en la legislación. años.
Brindar información al Asegurar de que la
fabricante sobre eventos responsabilidad de
que hayan dado lugar a mantener la disponibilidad
alguna queja o problema en de los registros de
relación con el dispositivo distribución y otros
del fabricante, por menor registros identificados en
que sea; r8.1A esté de acuerdo con
r8.1 esté acordada y
Cumplir con los requisitos verificada.
del fabricante para el
almacenamiento y
transporte del dispositivo.
Crear y mantener registros
contemporáneos de quejas,
eventos adversos, retiradas
y distribución de productos
y conservar los registros
durante los períodos
MDSAP AU P0002.005 169
Página
prescritos en las
Regulaciones (r5.10).
Cumplir con las
condiciones adicionales de
registros, fabricación,
principios esenciales, etc.,
específicamente impuestas
por la TGA en el momento
de, o con posterioridad, a la
autorización de
comercialización.
Para un dispositivo médico
de Clase AIMD, un
dispositivo médico de Clase
III, un dispositivo médico de
Clase IIb que es un
dispositivo médico
implantable o un dispositivo
médico de Clase 4 IVD,
proporcionar un informe a
la TGA como se describe
en la Reg 5.11.
Para los IVD descritos en la
Reg 5.3 (1) (j), proporcionar
un informe como se
describe en la Reg 5.12.
Asegurar de que no se
suministre un dispositivo en
Australia si el suministro
contraviene la Parte 2 de la
Norma de Venenos actual.
Asegurar de que los
registros de fabricación y
de distribución estén
disponibles para los
períodos definidos en la
Reg 8.1.
Notificación pública y 41KB Seguir las instrucciones del Ayudar al patrocinador
Procedimiento Uniforme de australiano a; cumplir con
Retiro de Dispositivos Retiro de Productos los requisitos descritos en
Médicos. Terapéuticos (URPRG, por el Procedimiento Uniforme
sus siglas en inglés) para de Retiro de Productos
tomar los pasos Terapéuticos (URPTG, por
especificados, de la sus siglas en inglés) para el
manera especificada y retiro de dispositivos,
dentro del período efectuar una notificación al
razonable que se público sobre los retiros del
especifique, para retirar mercado e informar a la
dispositivos médicos de TGA de la información
ese tipo que hayan sido relacionada con las
distribuidos, para publicar personas a las que se les
información especificada han suministrado los
para informar al público y dispositivos médicos.
notificar a la TGA la
información relativa a las
personas a las que se han
suministrado dispositivos
médicos.
Aplicación de los s41DA, Ayudar al fabricante del Cumplir con los
dispositivo a determinar la procedimientos de
Procedimientos de s41JA clase del dispositivo de evaluación de la
Evaluación de la acuerdo con las reglas de conformidad relevantes que
Conformidad y rP3 Div 3.2, clasificación australianas. son "obligaciones del
Solicitud de S3P1 Cl1.9, fabricante".
MDSAP AU P0002.005 170
Página
Información. S3P4 Cl4.8, Facilitar la provisión de los
registros del fabricante,
S3P5 Cl5.8 Clasificar un dispositivo.
incluidos, entre otros;
Registros para demostrar el
cumplimiento de los Aplicar un procedimiento de
principios esenciales, los CA apropiado para:
procedimientos de implementar un SGC
evaluación de la apropiado para la clase del
conformidad y cualquier dispositivo.
condición impuesta en el
momento de, o después de, Demostrar el cumplimiento
la concesión de la de los Principios Esenciales
autorización de relevantes para su uso en
comercialización el mercado australiano.
relacionada con las
actividades del fabricante,
Permitir que un funcionario
el cumplimiento de los
autorizado de la TGA entre
requisitos publicitarios, la
en las instalaciones del
seguridad y eficacia de los
fabricante y, mientras se
dispositivos. para el
encuentre en esas
propósito previsto, el
instalaciones, inspeccione
historial reglamentario de
las instalaciones y los
los dispositivos en otro
dispositivos médicos de
país, etc., cuando la TGA
cualquier tipo de acuerdo
solicite dichos registros.
con los requisitos de la
legislación.
Asegurar de que existan
arreglos para permitir que
Si lo solicita, proporcionar
la TGA controle el
documentación a una
funcionamiento y llevar a
persona autorizada
cabo inspecciones del
relacionada con
sistema de gestión de
dispositivos de un tipo
calidad del fabricante.
cubierto por el certificado
de CA emitido por TGA, o
Obtenga una Declaración al SGC del fabricante.
de Conformidad del
fabricante.
Permitir que la persona
autorizada copie los
Cuando la TGA haya documentos.
realizado un examen de
diseño, asegurar de que los
Hacer una declaración de
cambios en el diseño se
conformidad y
notifiquen a la TGA.
proporcionarla al
patrocinador australiano
Asegurar de que el para las solicitudes de
fabricante informe al autorización de
Patrocinador de los comercialización.
Eventos Adversos y Retiros
que deben informarse a la
Poner a disposición de
TGA.
TGA los registros
identificados en el
procedimiento de
evaluación de la
conformidad aplicado por el
fabricante, ya sea
directamente o a través del
patrocinador australiano.
Garantizar que los registros
de fabricación se
conserven y estén
disponibles durante un
período que sea al menos
la vida útil del dispositivo o
el período mínimo definido
en los procedimientos de
evaluación de la
conformidad australianos; 5
MDSAP AU P0002.005 171
Página
años.
Informar a la organización
de auditoría pertinente
(organismo de certificación)
de los cambios en el diseño
o SGC.
Comprometerse a informar
al Patrocinador o al TGA de
los eventos adversos o las
medidas tomadas para
recuperar / retirar
dispositivos del mercado.
Ensure reporting to the
relevant certification body
of a substantial change to
the system; or
change to the kinds of medical
devices to which the system is
to be applied.
Condiciones de los s41EJ Ayudar al fabricante del Además de las funciones
dispositivo de acuerdo con mencionadas anteriormente
Certificados de las reglas de clasificación para la "Aplicación de los
Evaluación de la australianas. procedimientos de
Conformidad emitidos evaluación de la
por la TGA. Facilitar la provisión de los conformidad".
registros del fabricante
solicitados por la TGA. Cooperar con la TGA en
(Si un fabricante elige una revisión de si se han
participar en el aplicado los requisitos de
Asegurar de que existan
MDSAP y está arreglos para permitir que un procedimiento de CA
suministrando la TGA controle el apropiado, incluyendo; la
aplicación de un SGC y el
productos a Australia, funcionamiento y lleve a
cabo inspecciones del cumplimiento de los
el Organismo principios esenciales de
sistema de gestión de
Autorizado debe calidad del fabricante. acuerdo con los requisitos
incluir los requisitos de la legislación.
de la jurisdicción Obtener una declaración de
australiana dentro del conformidad del Fabricante. Notificar a la TGA y a la
Organización de Auditoría
alcance de la de cualquier cambio
auditoría. Si el Cuando la TGA haya sustancial en el sistema de
fabricante también realizado un examen de gestión de calidad, la gama
diseño, asegurar de que los de productos cubiertos por
debe tener un cambios en el diseño se el SGC o cambios en el
Certificado de CA notifiquen a la TGA. diseño de los productos
emitido por TGA, las cubiertos por el certificado.
condiciones de ese Asegurar de que el
certificado también fabricante informa al Cumplir con cualquier
Patrocinador de los
deben aplicarse). condición adicional y
Eventos Adversos y Retiros relevante que se aplique a
que deben informarse a la un certificado de evaluación
TGA. de la conformidad cuando
se emita o se modifique
posteriormente.
Aclaración sobre el uso de MDSAP en Australia
La TGA reconoce formalmente los certificados MDSAP como un "documento de evaluación de la
conformidad" si se emite de acuerdo con MDSAP AU P0026 y hace referencia a los requisitos
MDSAP AU P0002.005 172
Página
reglamentarios de la jurisdicción australiana. La TGA utiliza estos documentos como evidencia del
cumplimiento de los requisitos del SGC de los procedimientos de evaluación de la conformidad
australianos en los casos en que la legislación no requiere que la TGA emita un Certificado de
evaluación de la conformidad - Ver Reg 4.1. Los certificados MDSAP se utilizan a menudo cuando
la Certificación EC alternativa no está disponible para dispositivos que no requieren un Certificado
de Evaluación de Conformidad emitido por TGA.
Para los dispositivos que requieren un Certificado de Evaluación de la Conformidad emitido por la
TGA, la TGA revisará los informes de auditoría MDSAP disponibles en busca de evidencia que
pueda respaldar un aplazamiento de una auditoría TGA programada.
Tener en cuenta que independientemente de cualquier vía que se haya utilizado, o se utilice, para
la autorización de comercialización en Australia, una organización de auditoría de MDSAP debe
incluir los requisitos de la jurisdicción australiana dentro del alcance de la auditoría de MDSAP si el
fabricante está suministrando el producto al australiano. Mercado.
Consultar el documento "Uso de pruebas de autorización de mercado de organismos reguladores /
de evaluación comparables en el extranjero para dispositivos médicos (incluidos los DIV)").
La Parte 4A de la Ley de Productos Terapéuticos de 1989 prevé que una organización constituida
en Australia sea reconocida como Organismo de Organismos de Evaluación de la Conformidad de
Australia (CAB) si satisface los criterios de evaluación. La legislación también establece
disposiciones para reconocer las evaluaciones de productos y las auditorías reglamentarias del
sistema de gestión de la calidad realizadas por los CAB australianos.
La legislación australiana reconoce por separado los informes y certificados de auditoría de
MDSAP como evidencia de un regulador extranjero comparable. Ver s41FDA (c) e instrumentos
relacionados.
Los procesos de evaluación utilizados para reconocer una organización de auditoría MDSAP no
califican a la organización para ser un organismo de evaluación de la conformidad australiano.
Brasil - ANVISA
No hay expectativas adicionales para la auditoría de acuerdos escritos durante una auditoría
MDSAP.
Canadá – Health Canada
No hay expectativas adicionales para la auditoría de acuerdos escritos durante una auditoría
MDSAP.
Japón – MHLW / PMDA
No hay expectativas adicionales para la auditoría de acuerdos escritos durante una auditoría
MDSAP.
Estados Unidos – FDA
No hay expectativas adicionales para la auditoría de acuerdos escritos durante una auditoría
MDSAP.
MDSAP AU P0002.005 173
Página
RESUMEN DE CAMBIOS DESDE LA REVISIÓN PREVIA
Prólogo / Uso de este documento
- Se agregó una declaración sobre la combinación del Enfoque de auditoría de MDSAP y el
Documento complementario, anteriormente documentos separados, en este documento
único.
- Se agregó una Declaración sobre programas de acceso especial.
Secuencia de Auditoría
- Se aclaró que el orden en el que se auditarán los procesos es fijo, sin embargo, la
secuencia de tareas de auditoría dentro de un proceso puede organizarse para permitir
una auditoría eficiente; Se aclaró que se permiten excepciones razonables para seguir la
secuencia de auditoría.
Realización de la Auditoría
- Se agregó un lenguaje aclaratorio en cuanto a la evaluación de la aplicación de los
principios de gestión de riesgos por parte de la organización de Dispositivos Médicos.
Navegando por la Secuencia de Auditoría
- Uso aclarado de la cláusula 4.2.1 (e) junto con los requisitos reglamentarios.
Terminología
- Se agregó lenguaje para "Organización de Dispositivos Médicos", proceso, producto o
servicio "subcontratado", "proveedores", "proveedores críticos", en todo el documento,
según corresponda.
Anexos
- Se modificó la referencia al Anexo 1.
- Introducción de dos nuevos anexos para resumir los requisitos específicos de cada país
para:
o informes de plazos para Eventos Adversos y Notificaciones de Advertencia.
o Acuerdos Escritos.
Ciclo de Auditoría de MDSAP
- Se agregó una declaración sobre las Auditorías de la Etapa 1 para las auditorías de
recertificación en ciertas circunstancias.
- Se agregó un párrafo sobre el muestreo durante las Auditorías.
Auditorías de Vigilancia
- Se agregó una referencia al Apéndice 1 de MDSAP AU P0008.
Proceso de Gestión
MDSAP AU P0002.005 174
Página
Tarea 1 – Evaluación de la conformidad
- Se agregó texto en el encabezado Procedimientos e Instrucciones del Sistema de Calidad
con respecto a las expectativas del término “documentado”.
- Texto agregado bajo el encabezado Planificación del sistema de gestión de la calidad con
respecto a la evidencia de la planificación del sistema de gestión de la calidad.
Tarea 5 – Texto agregado para el requisito específico del país de Australia:
- Referencia a EP13A para tarjetas de implantes de pacientes.
- Aclaración de la inclusión de las actividades de los patrocinadores en la auditoría interna
de la Organización de Dispositivos Médicos.
Proceso de Autorización de Comercialización de Dispositivos y Registro de Instalación
Tarea 1
- Trasladar los asuntos relacionados con los requisitos australianos para el acuerdo escrito
al Anexo 4.
- "Nota" a "Evaluación de la Conformidad"; se agregó texto en referencia a que se debe
prestar especial atención a los casos en los que los dispositivos se comercializan en
jurisdicciones donde no se ha otorgado la autorización de comercialización.
- Fechas de vencimiento corregidas para Brasil para registro y notificación.
Tarea 2
- Texto aclaratorio de los requisitos específicos de cada país de Australia.
- Fechas de vencimiento corregidas para Brasil para registro y notificación.
Tarea 3
- Se agregó texto dentro de la tarea para enfatizar el vínculo entre los cambios de diseño y
la necesidad de evaluar la Autorización de Comercialización.
- Se agregó texto al requisito específico del país de Australia con respecto a la notificación a
TGA de cambios en los casos en que el fabricante también posee un Certificado de
evaluación de conformidad de TGA.
- Se corrigió una referencia para Japón a la Ley PMD 23-2-5.12.
Autorización de Comercialización de Dispositivos y Registro de Instalación
- Se cambió "el fabricante debería" por "los fabricantes deben" mantener una lista de
patrocinadores australianos y los productos…
- Recordatorio adicional de que los patrocinadores deben tener un acuerdo por escrito con
los fabricantes.
Proceso de Medición, Análisis y Mejora
Tarea 2
- Se agregó una declaración de que la información del análisis de los datos de calidad de la
organización debe usarse para informar la decisión del equipo de auditoría en cuanto a
productos y procesos específicos a auditar durante los procesos de Diseño y Desarrollo,
Controles de Producción y Servicio y Compras.
MDSAP AU P0002.005 175
Página
Tarea 7
- Se corrigió el texto de los requisitos específicos del país para Australia, se agregó texto al
requisito específico del país de Australia con respecto a la notificación a TGA de cambios
en los casos en que el fabricante también posee un Certificado de evaluación de la
conformidad de TGA.
Tarea 12
Criterios agregados para la selección de quejas para revisión.
- Se agregaron sistemas de post comercialización como experiencia que se puede obtener
de la experiencia de post producción.
- Se agregaron "actividades de vigilancia posteriores a la comercialización" en la página
"Selección de registros".
- Se agregaron títulos de “Gestión de riesgos” a “Evaluación de la conformidad” para esta
tarea.
- Se agregó un texto que indica que la información de la revisión de las fuentes de post
producción, incluidas las quejas y los informes de vigilancia posteriores a la
comercialización, debe guiar al equipo auditor en la selección de diseños para revisar y
procesos de producción para auditar.
Tarea 14
- La tarea se reescribió para centrarse en la auditoría del proceso de la organización para
evaluar las quejas de posibles informes de eventos adversos individuales.
Tarea 15
- La tarea se reescribió para centrarse en la auditoría de los procesos de la organización
para evaluar problemas de calidad para posibles acciones de asesoramiento.
Proceso de Eventos Adversos y Notificaciones de Advertencia de Dispositivos Médicos
Tarea 1
- Se agregó una nota para Canadá sobre el requisito de informar los incidentes que cumplan
con los requisitos de la sección 59. (1) que ocurran fuera de Canadá no se aplica a menos
que el fabricante haya indicado, a una agencia reguladora del país en el que ocurrió el
incidente, la intención del fabricante. para tomar una acción correctiva, o a menos que la
agencia reguladora haya requerido que el fabricante tome una acción correctiva.
- Para Estados Unidos, asignación adicional para informes resumidos trimestrales para MDR
de mal funcionamiento.
Proceso de Diseño y Desarrollo
Tarea 5
- La retroalimentación de post producción se utilizará para mantener los requisitos del
producto y mejorar los procesos de realización del producto.
- En los encabezados "Evaluación de la Conformidad", "Entradas de Diseño", se agregó
texto que relaciona las Entradas de Diseño con los Procesos de Fabricación.
Tarea 7
MDSAP AU P0002.005 176
Página
- En el encabezado "Evaluación de la Conformidad”, “Resultados del Diseño", se agregó
texto que los resultados del diseño pueden incluir documentos como Diagramas, Dibujos,
Especificaciones y Procedimientos para Productos y Procesos.
Tarea 13
- Se agregó 8.2.1 como una cláusula relevante para Cambios de Diseño.
- Se agregó texto al requisito específico del país de Australia con respecto a notificar a TGA
de cambios en los casos en que el fabricante también posee un Certificado de Evaluación
de Conformidad de TGA.
Proceso de Controles de Producción y Servicio
Tarea 1
- En los encabezados "Evaluación de la conformidad", "Identificador Único de Dispositivo",
se eliminaron las fechas de introducción gradual para las clases de dispositivos.
Tarea 5
- Texto agregado para EP13A para tarjetas de implantes de pacientes para Australia.
Anexos
Anexo 1
Cambio de título para reflejar el contenido general de esta sección.
- Requisitos Generales para evaluar la documentación técnica - Se agregó un texto
aclaratorio para el resultado esperado del Control de Diseño para la Documentación
Técnica; y el seguimiento de la actualización de los documentos de Gestión de Riesgos.
- Requisito mínimo australiano para evaluar la documentación técnica – Se agregó la
inclusión de la información recopilada en los procesos de retroalimentación; y tarjetas de
implantes de pacientes.
Anexo 2
- Requisitos aclarados para calificar las no conformidades encontradas durante la Auditoría
de los Procesos de Esterilización.
Anexo 3
- Guía de Referencia Rápida para informar los plazos de Eventos Adversos y Avisos de
Advertencia.
Anexo 4
- Aclaración de cuándo se pueden requerir acuerdos escritos para respaldar los requisitos
reglamentarios y los temas que pueden necesitar ser incluidos.
MDSAP AU P0002.005 177
Página
Potrebbero piacerti anche
- GUIDA Fisica No Problem BDocumento128 pagineGUIDA Fisica No Problem BMatteo QuintilianiNessuna valutazione finora
- Controlli InterniDocumento31 pagineControlli InterniGiuseppe De FeoNessuna valutazione finora
- Sicurezza delle informazioni - Edizione 2022: Gestione del rischio - I sistemi di gestione - La ISO/IEC 27001:2022 - I controlli della ISO/IEC 27002:2022Da EverandSicurezza delle informazioni - Edizione 2022: Gestione del rischio - I sistemi di gestione - La ISO/IEC 27001:2022 - I controlli della ISO/IEC 27002:2022Nessuna valutazione finora
- SQS ITA-CAPITOLATO QUALITA' FORNITURE - Rev.4 Sett.'19Documento31 pagineSQS ITA-CAPITOLATO QUALITA' FORNITURE - Rev.4 Sett.'19ROBERTO SANTINO100% (1)
- Monitoraggio dei processi come sviluppo organizzativo e strumenti per la misurazioneDa EverandMonitoraggio dei processi come sviluppo organizzativo e strumenti per la misurazioneNessuna valutazione finora
- Uni en Iso 10012 2000 Requisiti Per I Processi e Le Apparecchiature Di Misurazione PDFDocumento28 pagineUni en Iso 10012 2000 Requisiti Per I Processi e Le Apparecchiature Di Misurazione PDFAnonymous nbPvDoH7i50% (2)
- Uni 11224 2011Documento30 pagineUni 11224 2011Anonymous 7QpTAoNessuna valutazione finora
- Esempio FPC PDFDocumento66 pagineEsempio FPC PDFDavide CaldiNessuna valutazione finora
- Manuale Di Revenue ManagementDocumento102 pagineManuale Di Revenue ManagementNicola SansoneNessuna valutazione finora
- BRC V7 It PDFDocumento132 pagineBRC V7 It PDFPaolo GeiNessuna valutazione finora
- Linee Guida Per La Classificazione e Gestione Del Rischio, La Valutazione Della Sicurezza Ed Il Monitoraggio Dei Ponti EsistentiDocumento90 pagineLinee Guida Per La Classificazione e Gestione Del Rischio, La Valutazione Della Sicurezza Ed Il Monitoraggio Dei Ponti EsistentiDaniele DominicNessuna valutazione finora
- Manuale Di Corretta Prassi IgienicaDocumento105 pagineManuale Di Corretta Prassi IgienicaStefano CarliNessuna valutazione finora
- 2001 11 21 - Procedure PDFDocumento98 pagine2001 11 21 - Procedure PDFMarco MarinoNessuna valutazione finora
- Manuale-Calcolo CM CMKDocumento102 pagineManuale-Calcolo CM CMKtestNessuna valutazione finora
- Manuale Qualita ItDocumento33 pagineManuale Qualita Itmatteo2009Nessuna valutazione finora
- Blow Press Calibration P-SL-T-044 - 00Documento12 pagineBlow Press Calibration P-SL-T-044 - 00aliNessuna valutazione finora
- Uni 10854 HaccpDocumento14 pagineUni 10854 Haccpmartello728Nessuna valutazione finora
- 02 Gestione Di Un Progetto in GMPDocumento115 pagine02 Gestione Di Un Progetto in GMPSee BeckNessuna valutazione finora
- Il Nuovo Regime Di Solvibilità - Solvency II - Pillar II e Processo ORSADocumento61 pagineIl Nuovo Regime Di Solvibilità - Solvency II - Pillar II e Processo ORSAGanugio MirianiNessuna valutazione finora
- Modelo Tecnico ProgamaDocumento156 pagineModelo Tecnico ProgamaYo VyNessuna valutazione finora
- Linee Guida Per Redazione Manuale Qualità Regione PDFDocumento54 pagineLinee Guida Per Redazione Manuale Qualità Regione PDFSimone GiorgiNessuna valutazione finora
- Circolare N. 1 - 2018 - Volume IDocumento342 pagineCircolare N. 1 - 2018 - Volume IeferraginaNessuna valutazione finora
- Manuale Deuclima VMC 300 S - Rev.1-20190515Documento50 pagineManuale Deuclima VMC 300 S - Rev.1-20190515Guidolol0% (1)
- BRC V6 enDocumento132 pagineBRC V6 enPaolo GeiNessuna valutazione finora
- Mic Um Si190300 HBL sw2-18 2-7 ItDocumento133 pagineMic Um Si190300 HBL sw2-18 2-7 ItJohny Ronald Gutierrez DelgadoNessuna valutazione finora
- 3 4 2005 - DispmediciDocumento68 pagine3 4 2005 - DispmediciRuger MonteNessuna valutazione finora
- Progettazione-Implementazione DWDocumento69 pagineProgettazione-Implementazione DWAndrea ArdentiNessuna valutazione finora
- Rischio Clinico Enrico Mazzoli SlideDocumento31 pagineRischio Clinico Enrico Mazzoli SlidegiudisNessuna valutazione finora
- Allegato1 C 1 5Documento60 pagineAllegato1 C 1 5enviro100% (1)
- Linee Guida Per Gli Audit Dei Sistemi Di Gestione Per La Qualità E/o Di Gestione AmbientaleDocumento38 pagineLinee Guida Per Gli Audit Dei Sistemi Di Gestione Per La Qualità E/o Di Gestione Ambientalel_47654558Nessuna valutazione finora
- 2020 10 Disposizioni e Istruzioni Attuazione DefDocumento133 pagine2020 10 Disposizioni e Istruzioni Attuazione DefPino MonopoliNessuna valutazione finora
- Tabella 2 2Documento11 pagineTabella 2 2Cosimo Damiano PetrachiNessuna valutazione finora
- Istruzione Operativa Per La Regolazione Tubi Raffreddamento ForniDocumento9 pagineIstruzione Operativa Per La Regolazione Tubi Raffreddamento FornialiNessuna valutazione finora
- Manuale HACCP 2020Documento216 pagineManuale HACCP 2020Riccardo PizzutoNessuna valutazione finora
- SCH130Documento10 pagineSCH130AntonioTirriNessuna valutazione finora
- P01 - Procedura Gestione Della DocumentazioneDocumento11 pagineP01 - Procedura Gestione Della DocumentazioneGiovanni AlbiNessuna valutazione finora
- Business Plan AEBDocumento55 pagineBusiness Plan AEBIvan PastoriniNessuna valutazione finora
- Rischio IT ClusitDocumento234 pagineRischio IT Clusitclaudio grazziNessuna valutazione finora
- Istruzione Operativa Per Ingrassagio Punti Macchina Sfl4-6 Sfl4-6 Machine Greasing Point Operating IstructionDocumento20 pagineIstruzione Operativa Per Ingrassagio Punti Macchina Sfl4-6 Sfl4-6 Machine Greasing Point Operating IstructionaliNessuna valutazione finora
- 07 Estrategia - Interaccio N Con Energi A Ele Ctrica (16 06 21)Documento55 pagine07 Estrategia - Interaccio N Con Energi A Ele Ctrica (16 06 21)Artemio Orlnado Melo MachucaNessuna valutazione finora
- Alg Il Monitoraggio Microbiologico Negli Ambienti LavoropdfDocumento91 pagineAlg Il Monitoraggio Microbiologico Negli Ambienti LavoropdfAndrea CarlucciNessuna valutazione finora
- AllegatoDocumento26 pagineAllegatoMarco MassaNessuna valutazione finora
- Hse ManualDocumento25 pagineHse ManualJOE SOSCNessuna valutazione finora
- 1 - Il Sistema AziendaDocumento25 pagine1 - Il Sistema AziendaDoriano PozziNessuna valutazione finora
- Mould Change P-SL-T-039 - 00Documento19 pagineMould Change P-SL-T-039 - 00aliNessuna valutazione finora
- Istruzione Operativa Sostituzione Cinghia Rotazione Platorelli E TensionamentoDocumento8 pagineIstruzione Operativa Sostituzione Cinghia Rotazione Platorelli E TensionamentoaliNessuna valutazione finora
- LineeGuida Montaggio SolaiDocumento66 pagineLineeGuida Montaggio SolaiElisabetta BolzoniNessuna valutazione finora
- Rischio Di Revisione Concetto Di Materiality Sistema Controllo InternoDocumento42 pagineRischio Di Revisione Concetto Di Materiality Sistema Controllo InternoStefano GualandrisNessuna valutazione finora
- Cei 62Documento26 pagineCei 62gandalf92Nessuna valutazione finora
- Y207 Machine Safety Guide It PDFDocumento144 pagineY207 Machine Safety Guide It PDFOscar GiacominNessuna valutazione finora
- Disciplinare Per La Produzione Di ConseveDocumento44 pagineDisciplinare Per La Produzione Di ConseveRoberto MontefuscoNessuna valutazione finora
- SOLUTIONDocumento1 paginaSOLUTIONFilippo RoaroNessuna valutazione finora
- Teoria Metodi Di Progettazione IndustrialeDocumento44 pagineTeoria Metodi Di Progettazione IndustrialetamaraNessuna valutazione finora
- Briocnc Mf904111123 Ita EngDocumento61 pagineBriocnc Mf904111123 Ita EngMwg WanNessuna valutazione finora
- Linee Guida Dichaiazione Rispondenza CNPIDocumento32 pagineLinee Guida Dichaiazione Rispondenza CNPIAndrea TomasselliNessuna valutazione finora
- Tesi Picco DamianoDocumento109 pagineTesi Picco DamianoJoe FalchettoNessuna valutazione finora
- 2016 It EgluiniDocumento205 pagine2016 It EgluiniFadi MagdiNessuna valutazione finora
- Iso 10725Documento44 pagineIso 10725AlessandroAbateNessuna valutazione finora
- Guida Di Buona Prassi Igienica: Per I Caseifici Di Azienda AgricolaDocumento132 pagineGuida Di Buona Prassi Igienica: Per I Caseifici Di Azienda AgricolaJorj JacksonNessuna valutazione finora
- Corso SIL Valvoliere IMQ - Progettazione HWDocumento24 pagineCorso SIL Valvoliere IMQ - Progettazione HWafricaNessuna valutazione finora