Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Formula Molecular y Empiica
Caricato da
Josselyn Bustillos Buenaño0 valutazioniIl 0% ha trovato utile questo documento (0 voti)
97 visualizzazioni6 pagineEste documento presenta la resolución de un ejercicio para determinar la fórmula empírica y molecular de un compuesto a partir de datos experimentales de combustión. Se calculan las masas de carbono, hidrógeno y oxígeno presentes y se obtiene la fórmula empírica C3H4O3. Sin embargo, al usar la masa molecular dada de 88, la fórmula molecular resultante C3H4O3 no coincide con la conocida del ácido ascórbico C6H8O6, lo que indica un error en el enunciado.
Descrizione originale:
explicacion
Titolo originale
formula molecular y empiica
Copyright
© © All Rights Reserved
Formati disponibili
PPT, PDF, TXT o leggi online da Scribd
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoEste documento presenta la resolución de un ejercicio para determinar la fórmula empírica y molecular de un compuesto a partir de datos experimentales de combustión. Se calculan las masas de carbono, hidrógeno y oxígeno presentes y se obtiene la fórmula empírica C3H4O3. Sin embargo, al usar la masa molecular dada de 88, la fórmula molecular resultante C3H4O3 no coincide con la conocida del ácido ascórbico C6H8O6, lo que indica un error en el enunciado.
Copyright:
© All Rights Reserved
Formati disponibili
Scarica in formato PPT, PDF, TXT o leggi online su Scribd
0 valutazioniIl 0% ha trovato utile questo documento (0 voti)
97 visualizzazioni6 pagineFormula Molecular y Empiica
Caricato da
Josselyn Bustillos BuenañoEste documento presenta la resolución de un ejercicio para determinar la fórmula empírica y molecular de un compuesto a partir de datos experimentales de combustión. Se calculan las masas de carbono, hidrógeno y oxígeno presentes y se obtiene la fórmula empírica C3H4O3. Sin embargo, al usar la masa molecular dada de 88, la fórmula molecular resultante C3H4O3 no coincide con la conocida del ácido ascórbico C6H8O6, lo que indica un error en el enunciado.
Copyright:
© All Rights Reserved
Formati disponibili
Scarica in formato PPT, PDF, TXT o leggi online su Scribd
Sei sulla pagina 1di 6
PRoFeBLoG.
es/jose
____________________________
Ejercicio de fórmula empírica y
fórmula molecular
Ejercicio de fórmula empírica y molecular
______________________________________________
_
AI quemar una muestra de 1,298 g de ácido ascórbico (vitamina
C) se forman 1,947 g de CO2 y 0,531 g de agua. Sabiendo que
dicho compuesto sólo contiene C. H y O. determina su fómula
empírica. Si su masa molecular es 88. ¿cuál es la fórmula
molecular?
• Determinar la masa de C en la muestra a partir de la masa de C contenida en
un mol de CO2 (44 g de CO2 contiene 12 g de C)
• 1,947 g CO2 · 12 g C / 44 g CO2 = 0,531 g C
• es la masa de C contenida en 1,947 g CO2 y por tanto contenida en la muestra
• Determinar la masa de H en la muestra a partir de la masa de H contenida en
un mol de H2O (18 g de H2O contiene 2 g de H)
• 0,531 g H2O · 2 g H / 18 g H2O = 0,059 g H
• es la masa de H contenida en 0,531 g H2O y por tanto contenida en la muestra
•
Ejercicio de fórmula empírica y molecular
______________________________________________
_
• La muestra de 1,298 g de ácido ascórbico contiene
• 0,531 g C
• 0,059 g H
• puesto que solamente contiene C H y O entonces la diferencia será la masa de
O contenida en la muestra (1,298 - 0,531 - 0,059) = 0,708 g O
• Expresamos estas masas (g) en cantidad de sustancia (mol)
• 0,531 g C = 0,044 mol C
• 0,059 g H = 0,059 mol H
• 0,708 g O = 0,044 mol O
Ejercicio de fórmula empírica y molecular
______________________________________________
_
• Dividimos estas cantidades por la más pequeña para encontrar la relación
entre ellas
• 0,044 mol C / 0,044 mol C = 1 mol C / mol C
•
• 0,059 mol H / 0,044 mol C = 1,34 mol H / mol C
• 0,044 mol O / 0,044 mol C = 1 mol O / molC
•
• Expresamos las relaciones anteriores en forma de números enteros,
multiplicando por 3 tendremos
• 3 mol C / mol C
• 4 mol H / mol C
• 3 mol O / mol C es decir la fórmula empírica es C3H4O3
Ejercicio de fórmula empírica y molecular
______________________________________________
_•Para encontrar la fórmula molecular: trabajamos con el valor de la masa
molecular de la sustancia
• M(ácido ascórbido)= 88
•
• M(C3H8O3)= 3·M(C)+4·M(H)+3·M(O)
• M(C3H8O3)= (3·12+4·1+3·16) =88
• puesto que coincide con el valor que aparece en el enunciado del problema
entonces tendremos que la fórmula molecular es C3H4O3
•
• Sin embargo, es sabido que la fórmula molecular
• del ácido ascórbico esC6H8O6
• por tanto debe de haber un error en el enunciado
PRoFeBLoG.es/jose
____________________________
Ejercicio de fórmula empírica y
fórmula molecular
Potrebbero piacerti anche
- Análisis Por CombustiónDocumento11 pagineAnálisis Por CombustiónDaniel MNessuna valutazione finora
- 2 - Formula Empirica y Molecular1Documento16 pagine2 - Formula Empirica y Molecular1Ramón Eliseo Flores EspinalNessuna valutazione finora
- Análisis Por CombustiónDocumento6 pagineAnálisis Por CombustiónMiguel RodriguezNessuna valutazione finora
- Universidad Nacional Mayor de San Marcos: Cálculos Básicos en QuímicaDocumento11 pagineUniversidad Nacional Mayor de San Marcos: Cálculos Básicos en QuímicaEnrique PuenteNessuna valutazione finora
- Fórmula empírica y cálculos químicosDocumento4 pagineFórmula empírica y cálculos químicosVictoria Mellinas AlvarezNessuna valutazione finora
- Formula Empirica y Porcentaje de ComposicionDocumento27 pagineFormula Empirica y Porcentaje de ComposicionDiana Jimenez MoralesNessuna valutazione finora
- Ejemplos de Composicion CentesimalDocumento14 pagineEjemplos de Composicion CentesimalTP M CovetNessuna valutazione finora
- Semana 6 Estequiom..Documento14 pagineSemana 6 Estequiom..Angelo RomanNessuna valutazione finora
- Formulas Empiricas y MolecularesDocumento18 pagineFormulas Empiricas y MolecularesYesenia GarciaNessuna valutazione finora
- Ficha de Trabajo en Casa FormulasDocumento2 pagineFicha de Trabajo en Casa FormulasBryan AmayaNessuna valutazione finora
- 9, NomenclaturaDocumento13 pagine9, Nomenclaturayuleidislara0428Nessuna valutazione finora
- Determinacion de Formulas Quimicas y MolecularesDocumento20 pagineDeterminacion de Formulas Quimicas y MolecularesBRYAN DANIEL ARAUJO GARAYNessuna valutazione finora
- C 11formulaempirica MolecularSept6Documento15 pagineC 11formulaempirica MolecularSept6Masumi YaiNessuna valutazione finora
- Tutoria 5Documento62 pagineTutoria 5Benjamin MuñozNessuna valutazione finora
- Aritmética QuímicaDocumento33 pagineAritmética QuímicaSantiago Ivan Pascual Panduro57% (7)
- Clase 4 Fórmula Molecular, Empírica %Documento7 pagineClase 4 Fórmula Molecular, Empírica %Fernando Clemente GarciaNessuna valutazione finora
- Fórmulas Empíricas y MolecularesDocumento4 pagineFórmulas Empíricas y MolecularesBruno David Cedillo Alaniz50% (2)
- Fórmulas empíricas y moleculares a partir de análisis químicosDocumento13 pagineFórmulas empíricas y moleculares a partir de análisis químicosArturo Vera PazNessuna valutazione finora
- Aritmética QuímicaDocumento43 pagineAritmética QuímicaAngellina Quiroz PeraltaNessuna valutazione finora
- Determinación de La Fórmula Empírica y MolecularDocumento7 pagineDeterminación de La Fórmula Empírica y MolecularjealcapaNessuna valutazione finora
- Ejerc Res Camb Materiales Proces QuimicosDocumento28 pagineEjerc Res Camb Materiales Proces Quimicosapi-3820155100% (1)
- Clase 2-2 Fórmulas QuímicasDocumento19 pagineClase 2-2 Fórmulas QuímicaschristianmolinaNessuna valutazione finora
- Problemas F Empirica MolecularDocumento58 pagineProblemas F Empirica MolecularRenato Diaz FrigerioNessuna valutazione finora
- QUIM002.Unidad II - EstequiometriaDocumento50 pagineQUIM002.Unidad II - EstequiometriaBárbara Reveco PérezNessuna valutazione finora
- 4 Clase Mol REC M.Atom M. Molec. VeterDocumento19 pagine4 Clase Mol REC M.Atom M. Molec. VeterAnonymous ETlAcinWrNessuna valutazione finora
- Fc3b3rmula EmpiricaDocumento5 pagineFc3b3rmula EmpiricaJose GMZNessuna valutazione finora
- Estequiometria IDocumento15 pagineEstequiometria IArlenis ArmuellesNessuna valutazione finora
- Tarea 10Documento5 pagineTarea 10Adrian LovonNessuna valutazione finora
- Cálculos estequiométricos y pureza de reacciones químicasDocumento6 pagineCálculos estequiométricos y pureza de reacciones químicasYessica QuintanaNessuna valutazione finora
- Aritmética QuímicaDocumento43 pagineAritmética QuímicaDeyman Becerra100% (2)
- Taller EstequiometriaDocumento16 pagineTaller EstequiometriaGloria LizarazoNessuna valutazione finora
- Cálculos estequiométricos y composición químicaDocumento8 pagineCálculos estequiométricos y composición químicaLedover Ledover LedoverNessuna valutazione finora
- Fórmulas Empíricas A Partir Del AnálisisDocumento84 pagineFórmulas Empíricas A Partir Del AnálisisBrayan Laitano Orellanos100% (1)
- Fórmula química: determinación de fórmulas empíricas y molecularesDocumento5 pagineFórmula química: determinación de fórmulas empíricas y moleculareseveNessuna valutazione finora
- Manual EsteqDocumento10 pagineManual EsteqTeresa SánchezNessuna valutazione finora
- Guía Estequiometria, El MOLDocumento4 pagineGuía Estequiometria, El MOLAngel Vicente Sanchez PilcoNessuna valutazione finora
- Analitica 4.5Documento2 pagineAnalitica 4.5Juan PabloNessuna valutazione finora
- Determinación de Formulas MolecularesDocumento7 pagineDeterminación de Formulas MolecularesMax Ferrol100% (1)
- Formulas Químicas y EstequiometríaDocumento17 pagineFormulas Químicas y EstequiometríaSan KanNessuna valutazione finora
- Relaciones de masa en reacciones químicasDocumento35 pagineRelaciones de masa en reacciones químicasAlejisBahamonNessuna valutazione finora
- Formula EmpiricaDocumento17 pagineFormula EmpiricacristianNessuna valutazione finora
- S7-Aritmética Química PDFDocumento31 pagineS7-Aritmética Química PDFAarón M. ReyesNessuna valutazione finora
- Ejercicios de EstequiometriaDocumento26 pagineEjercicios de EstequiometriaMaria SolanoNessuna valutazione finora
- PPP Unidad 3 - Estequiometria-3Documento38 paginePPP Unidad 3 - Estequiometria-3Cesar Caballero RamirezNessuna valutazione finora
- Comprension Porcentual de Un PresupuestoDocumento4 pagineComprension Porcentual de Un PresupuestoHenrry CifuentesNessuna valutazione finora
- Boletin Form Emp y Molec Gases y Disol - Ejemplos ResueltosDocumento8 pagineBoletin Form Emp y Molec Gases y Disol - Ejemplos ResueltosBraisNessuna valutazione finora
- Ejemplo Formula Empirica y MolecularDocumento3 pagineEjemplo Formula Empirica y MolecularJuan AndrésNessuna valutazione finora
- Ejercicios de Formula Empirica y Molecular PDFDocumento5 pagineEjercicios de Formula Empirica y Molecular PDFRoberto Jose CastañedaNessuna valutazione finora
- Fórmulas Empíricas y MolecularesDocumento10 pagineFórmulas Empíricas y MolecularesCARINANessuna valutazione finora
- Solución Ejercicio 61 de EstequiometrÍaDocumento2 pagineSolución Ejercicio 61 de EstequiometrÍajvc19538161Nessuna valutazione finora
- Guia 04 Estequiometria QUI080Documento13 pagineGuia 04 Estequiometria QUI080Alan John Andrades100% (2)
- 4.4.1.6.-Calculo % Composicion.Documento6 pagine4.4.1.6.-Calculo % Composicion.ALANNessuna valutazione finora
- Química Aritmética: Unidades, Mol, FórmulasDocumento56 pagineQuímica Aritmética: Unidades, Mol, FórmulasJorge Gavino Alomía100% (1)
- Estequiometría CompletoDocumento41 pagineEstequiometría CompletoJoako Jerez IbarraNessuna valutazione finora
- Recopilacion Examenes fq1bchDocumento8 pagineRecopilacion Examenes fq1bchCarlos XabierNessuna valutazione finora
- Ejercicio 7.60Documento3 pagineEjercicio 7.60Josselyn Bustillos BuenañoNessuna valutazione finora
- 10.-Ejercicio 7.52Documento3 pagine10.-Ejercicio 7.52Josselyn Bustillos BuenañoNessuna valutazione finora
- Catalogo Juegos Infantiles y Biosaludables 2016-2017Documento33 pagineCatalogo Juegos Infantiles y Biosaludables 2016-2017Josselyn Bustillos BuenañoNessuna valutazione finora
- 48 PDFDocumento85 pagine48 PDFAlberto PorrasNessuna valutazione finora
- Difusion en SolidosDocumento31 pagineDifusion en SolidosCarlos CoronadoNessuna valutazione finora
- TablasDocumento3 pagineTablasJosselyn Bustillos BuenañoNessuna valutazione finora
- Inyeccion ContinuaDocumento10 pagineInyeccion Continuajota_ovaNessuna valutazione finora
- Equilibrio de Fases PDFDocumento3 pagineEquilibrio de Fases PDFJosselyn Bustillos BuenañoNessuna valutazione finora
- NayeDocumento1 paginaNayeJosselyn Bustillos BuenañoNessuna valutazione finora
- LAMMPSDocumento2 pagineLAMMPSJosselyn Bustillos BuenañoNessuna valutazione finora
- 48 PDFDocumento85 pagine48 PDFAlberto PorrasNessuna valutazione finora
- Consulta AletasDocumento2 pagineConsulta AletasJosselyn Bustillos BuenañoNessuna valutazione finora
- Difusión de Tinta en Agar AgarDocumento4 pagineDifusión de Tinta en Agar AgarJosselyn Bustillos BuenañoNessuna valutazione finora
- Expo ArticuloDocumento3 pagineExpo ArticuloJosselyn Bustillos BuenañoNessuna valutazione finora
- Recursossantiago PDFDocumento6 pagineRecursossantiago PDFPaola Denise RiquelmeNessuna valutazione finora
- Prieto2019 en Es PDFDocumento15 paginePrieto2019 en Es PDFJosselyn Bustillos BuenañoNessuna valutazione finora
- BolIBM 18 PDFDocumento56 pagineBolIBM 18 PDFJosselyn Bustillos BuenañoNessuna valutazione finora
- BettyDocumento5 pagineBettyMaria Quequejana MamaniNessuna valutazione finora
- Laboratorio de Quimica - Osmosis PDFDocumento8 pagineLaboratorio de Quimica - Osmosis PDFJosselyn Bustillos BuenañoNessuna valutazione finora
- Dialnet Esterificacion 4902598 PDFDocumento8 pagineDialnet Esterificacion 4902598 PDFBianca LeyvaNessuna valutazione finora
- Contenido de AsignaturaDocumento7 pagineContenido de AsignaturaJosselyn Bustillos BuenañoNessuna valutazione finora
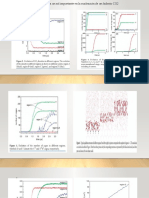
- Curvas de Reaccion en Funcion de La VelocidadDocumento2 pagineCurvas de Reaccion en Funcion de La VelocidadJosselyn Bustillos BuenañoNessuna valutazione finora
- Graficas para Analisis de Reacciones No CatalizadasDocumento1 paginaGraficas para Analisis de Reacciones No CatalizadasJosselyn Bustillos BuenañoNessuna valutazione finora
- Prieto2019 en Es PDFDocumento15 paginePrieto2019 en Es PDFJosselyn Bustillos BuenañoNessuna valutazione finora
- LessonPlanDiffusion 122115sm - En.esDocumento9 pagineLessonPlanDiffusion 122115sm - En.esJosselyn Bustillos BuenañoNessuna valutazione finora
- BolIBM 18 PDFDocumento56 pagineBolIBM 18 PDFJosselyn Bustillos BuenañoNessuna valutazione finora
- Determinación de cromo hexavalente en aguas por espectrofotometríaDocumento5 pagineDeterminación de cromo hexavalente en aguas por espectrofotometríaPatty BqqNessuna valutazione finora
- 1325-Texto Del Artículo-1907-1-10-20170927Documento10 pagine1325-Texto Del Artículo-1907-1-10-20170927Josselyn Bustillos BuenañoNessuna valutazione finora
- Esterificacion de Los Acidos Grasos Libres Del AceiteDocumento5 pagineEsterificacion de Los Acidos Grasos Libres Del AceiteAna Paula Castañeda CachayNessuna valutazione finora
- Recursossantiago PDFDocumento6 pagineRecursossantiago PDFPaola Denise RiquelmeNessuna valutazione finora
- Unidades Quimicas de MasaDocumento11 pagineUnidades Quimicas de MasaJOHAN PAREDES MENDIETANessuna valutazione finora
- TQ Prob 2012 4unidadesDocumento31 pagineTQ Prob 2012 4unidadeskobymaster090% (1)
- 0 - 02. Compuestos OrgánicosDocumento27 pagine0 - 02. Compuestos OrgánicosGdex ZiaNessuna valutazione finora
- Practica - 5 - Formula EmpíricaDocumento3 paginePractica - 5 - Formula EmpíricaalexNessuna valutazione finora
- Práctica QuímicaDocumento3 paginePráctica QuímicaJavi GuzmanNessuna valutazione finora
- Guia #13 Determinacion de La Formula Minima de Un CompuestoDocumento4 pagineGuia #13 Determinacion de La Formula Minima de Un CompuestoLucia MorenoNessuna valutazione finora
- Ejerc Res Camb Materiales Proces QuimicosDocumento28 pagineEjerc Res Camb Materiales Proces Quimicosapi-3820155100% (1)
- Practica Primer Parcial de Quimica GeneralDocumento5 paginePractica Primer Parcial de Quimica GeneralDaniel BernaNessuna valutazione finora
- Composición centesimal y fórmula molecularDocumento5 pagineComposición centesimal y fórmula molecularluis beltran MARCIAL PEREIRANessuna valutazione finora
- Diferencias Entre Mas Molar, Molecular y EmpricasDocumento5 pagineDiferencias Entre Mas Molar, Molecular y EmpricasRicardo Rivera MejiaNessuna valutazione finora
- Taller # 4 de Quimica Cie-ApiDocumento18 pagineTaller # 4 de Quimica Cie-ApiDILOPEZ100% (1)
- Tema EstequiometriaDocumento9 pagineTema EstequiometriaRony BrizuelaNessuna valutazione finora
- Ejercicios de Estequiometria 1Documento4 pagineEjercicios de Estequiometria 1Juan LópezNessuna valutazione finora
- Cadenas CarbonadasDocumento3 pagineCadenas CarbonadasJohn Michael VicentNessuna valutazione finora
- Átomos y moles: la unidad fundamental de la materiaDocumento30 pagineÁtomos y moles: la unidad fundamental de la materiaVR DanNessuna valutazione finora
- Guía 03 EstequiometríaDocumento7 pagineGuía 03 EstequiometríaKatherine Ordenes PintoNessuna valutazione finora
- Problemas EstequiometriaDocumento7 pagineProblemas EstequiometriaSuyapa PonceNessuna valutazione finora
- Movimiento 1º Bachillerato4Documento17 pagineMovimiento 1º Bachillerato4atravatraNessuna valutazione finora
- Composicion Centesimal PDFDocumento42 pagineComposicion Centesimal PDFMAJAPAU0% (1)
- A Partir de Las Siguiente Composición CentesimalDocumento30 pagineA Partir de Las Siguiente Composición CentesimalMarga Moncada67% (3)
- 3 Fórmulas QuímicasDocumento5 pagine3 Fórmulas Químicaslucrecia ʕ·ᴥ·ʔNessuna valutazione finora
- Fórmula empírica Mg oxidaciónDocumento6 pagineFórmula empírica Mg oxidaciónPieroNessuna valutazione finora
- Tema Balance de MateriaDocumento28 pagineTema Balance de MateriaMiguel Reza BurgaNessuna valutazione finora
- Estequiometría: Las leyes cuantitativas de las reacciones químicasDocumento14 pagineEstequiometría: Las leyes cuantitativas de las reacciones químicaspiratacoquiNessuna valutazione finora
- Estequiometría en Elementos y CompuestosDocumento56 pagineEstequiometría en Elementos y CompuestosGabriela Pazmiño-Armijos100% (1)
- Trabajo 4Documento15 pagineTrabajo 4Kareline BurgosNessuna valutazione finora
- Agenda Fórmula QuímicaDocumento15 pagineAgenda Fórmula Químicalola perezNessuna valutazione finora
- Formulas químicas y composición centesimalDocumento1 paginaFormulas químicas y composición centesimalIngrid Villalba GarciaNessuna valutazione finora
- Unidades Quimicas de MasaDocumento9 pagineUnidades Quimicas de MasaDrables Mejia100% (1)
- Modulo Final 2017 - QuimicaDocumento64 pagineModulo Final 2017 - QuimicaelverNessuna valutazione finora