Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
MDAtomo Merilin Oliv
Caricato da
Renderson Gonçalves0 valutazioniIl 0% ha trovato utile questo documento (0 voti)
245 visualizzazioni7 pagineModelos Atômicos são os aspectos estruturais dos átomos que foram apresentados por cientistas na tentativa de explicar o átomo e a sua composição.
Em 1808, o cientista inglês John Dalton propôs uma explicação para a propriedade da matéria. Trata-se da primeira teoria atômica que dá as bases para o modelo atômico conhecido atualmente.
Mas a constituição da matéria é motivo de estudos desde a antiguidade. Os pensadores Leucipo (500 a.C.) e Demócrito (460 a.C.) formularam a ideia de haver um limite para a pequenez das partículas. Afirmavam que elas se tornariam tão pequenas que não poderiam ser divididas. Chamou-se a essa partícula última de átomo – derivado de radicais gregos que, juntos, significam o que não se pode dividir.
Titolo originale
MDAtomoMerilinOliv
Copyright
© © All Rights Reserved
Formati disponibili
PPT, PDF, TXT o leggi online da Scribd
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoModelos Atômicos são os aspectos estruturais dos átomos que foram apresentados por cientistas na tentativa de explicar o átomo e a sua composição.
Em 1808, o cientista inglês John Dalton propôs uma explicação para a propriedade da matéria. Trata-se da primeira teoria atômica que dá as bases para o modelo atômico conhecido atualmente.
Mas a constituição da matéria é motivo de estudos desde a antiguidade. Os pensadores Leucipo (500 a.C.) e Demócrito (460 a.C.) formularam a ideia de haver um limite para a pequenez das partículas. Afirmavam que elas se tornariam tão pequenas que não poderiam ser divididas. Chamou-se a essa partícula última de átomo – derivado de radicais gregos que, juntos, significam o que não se pode dividir.
Copyright:
© All Rights Reserved
Formati disponibili
Scarica in formato PPT, PDF, TXT o leggi online su Scribd
0 valutazioniIl 0% ha trovato utile questo documento (0 voti)
245 visualizzazioni7 pagineMDAtomo Merilin Oliv
Caricato da
Renderson GonçalvesModelos Atômicos são os aspectos estruturais dos átomos que foram apresentados por cientistas na tentativa de explicar o átomo e a sua composição.
Em 1808, o cientista inglês John Dalton propôs uma explicação para a propriedade da matéria. Trata-se da primeira teoria atômica que dá as bases para o modelo atômico conhecido atualmente.
Mas a constituição da matéria é motivo de estudos desde a antiguidade. Os pensadores Leucipo (500 a.C.) e Demócrito (460 a.C.) formularam a ideia de haver um limite para a pequenez das partículas. Afirmavam que elas se tornariam tão pequenas que não poderiam ser divididas. Chamou-se a essa partícula última de átomo – derivado de radicais gregos que, juntos, significam o que não se pode dividir.
Copyright:
© All Rights Reserved
Formati disponibili
Scarica in formato PPT, PDF, TXT o leggi online su Scribd
Sei sulla pagina 1di 7
Teoria Atômica
1. Teoria de Dalton
2. Teoria de Thomson
3. Teoria de Rutherford
4. O modelo Atômico Atual
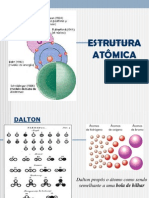
1. O Átomo na visão de Dalton
Em 1808, Dalton propôs a teoria do modelo atômico, onde o átomo é uma
minúscula esfera maciça, impenetrável, indestrutível, indivisível e sem carga.
Todos os átomos de um mesmo elemento químico são idênticos. Seu modelo
atômico foi chamado de modelo atômico da bola de bilhar.
Propriedades do átomo de Dalton:
Átomos de elementos diferentes possuem propriedades diferentes entre si.
Átomos de um mesmo elemento possuem propriedades iguais e de peso
invariável.
Átomos são partículas maciças, indivisíveis e esféricas formadoras da
matéria.
Nas reações químicas, os átomos permanecem inalterados.
2. O Átomo na visão de Thomson
O Modelo atômico de Thomson (1897) propunha então que o átomo não
fosse maciço (como havia afirmado John Dalton), mas sim um fluido com
carga positiva (homogêneo e quase esférico) no qual estavam dispersos
(de maneira homogênea) os elétrons. Podemos fazer a analogia desse
modelo atômico com um "Panetone" ou com um pudim recheado de uvas
passas, em que a massa do panetone seria positiva e as passas seriam as
partículas negativas.
O modelo proposto por Thomson ficou conhecido como o “Pudim de
Passas”.
3. O Átomo na visão de Rutherford
O modelo atômico de Rutherford, ficou conhecido como modelo
planetário do átomo. Segundo esta teoria, o átomo teria um núcleo
positivo, que seria muito pequeno em relação ao todo mas teria grande
massa e, ao redor deste, os elétrons, que descreveriam órbitas helicoidais
em altas velocidades, para não serem atraídos e caírem sobre o núcleo. A
eletrosfera - local onde se situam os elétrons - seria cerca de dez mil vezes
maior do que o núcleo atômico, e entre eles haveria um espaço vazio.
4. O modelo atômico atual
4.1. Partículas
4.2. Tabela Periódica
4.1 Partículas existentes no núcleo do
átomo
Se sabe que os elétrons possuem carga negativa, massa muito
pequena e que se movem em órbitas ao redor do núcleo atômico.
Os prótons possuem carga positiva, cuja massa é aproximadamente
superior 1837 vezes maior que a massa do elétron.
Os Nêutrons são partículas sem carga e possuem massa ligeiramente
superior aos prótons.
4.2 Tabela Periódica
A tabela periódica é uma ordenação sistemática dos elementos químicos
conhecidos.
Cada elemento se caracteriza por possuir um número de elétrons que se
distribuem nos diferentes níveis de energia do átomo correspondente.
Os níveis energéticos ou camadas, são denominados pelos símbolos K,
L, M, N, O, P e Q.
Cada camada possui uma quantidade fixa de elétrons. A camada mais
próxima do núcleo K, comporta somente dois elétrons; a camada L,
imediatamente posterior, oito, e assim sucessivamente.
Os elétrons da última camada (mais afastados do núcleo) são
responsáveis pelo comportamento químico do elemento, por isso são
denominados elétrons de valência.
Potrebbero piacerti anche
- Vírus e Suas Principais CaracterísticasDocumento35 pagineVírus e Suas Principais CaracterísticasRenderson GonçalvesNessuna valutazione finora
- Processos de Separação de MisturasDocumento37 pagineProcessos de Separação de MisturasRenderson GonçalvesNessuna valutazione finora
- As Regras de Nomenclatura Binomial de Lineu e Formas de Classificação BiológicaDocumento32 pagineAs Regras de Nomenclatura Binomial de Lineu e Formas de Classificação BiológicaRenderson GonçalvesNessuna valutazione finora
- Estados Físicos Da Matéria e Fatores Que Influenciam Na Mudança Dos Estados FísicosDocumento39 pagineEstados Físicos Da Matéria e Fatores Que Influenciam Na Mudança Dos Estados FísicosRenderson Gonçalves100% (1)
- Sistema Digestório e Suas Respectivas FunçõesDocumento24 pagineSistema Digestório e Suas Respectivas FunçõesRenderson GonçalvesNessuna valutazione finora
- Composicao Quimica Da Celula-EjaDocumento55 pagineComposicao Quimica Da Celula-EjaRenderson GonçalvesNessuna valutazione finora
- Classificação Dos Tecidos, Relacionando As Suas Funções e Localização Dos Tecidos para A Formação Dos ÓrgãosDocumento26 pagineClassificação Dos Tecidos, Relacionando As Suas Funções e Localização Dos Tecidos para A Formação Dos ÓrgãosRenderson GonçalvesNessuna valutazione finora
- 05excep - Es Leis de Mendel - AppDocumento5 pagine05excep - Es Leis de Mendel - AppRenderson GonçalvesNessuna valutazione finora
- Tabela Periódica - ExercíciosDocumento5 pagineTabela Periódica - ExercícioslindianecpNessuna valutazione finora
- 5º Teste 9ºDocumento2 pagine5º Teste 9ºCristina LopesNessuna valutazione finora
- Profº MIKAYLAN Surpresa 9º AnoDocumento2 pagineProfº MIKAYLAN Surpresa 9º AnoMikaylan SousaNessuna valutazione finora
- Eletrostática CompletaDocumento16 pagineEletrostática CompletaEmilson Moreira100% (1)
- Questões Sobre Atomística PDFDocumento18 pagineQuestões Sobre Atomística PDFZuanny Silva JucáNessuna valutazione finora
- 02r Carga Nuclear Efetiva-ResolvidoDocumento2 pagine02r Carga Nuclear Efetiva-ResolvidoAnderson Oliveira100% (2)
- Exercicios Isobaros IsotonosDocumento1 paginaExercicios Isobaros IsotonosLilian SilvaNessuna valutazione finora
- Extensivoenem Química Atomística 22-02-2019Documento10 pagineExtensivoenem Química Atomística 22-02-2019eng civil Paulo Vitor MedeirosNessuna valutazione finora
- Aula1Exerccio2 20160302223827Documento3 pagineAula1Exerccio2 20160302223827Neilton Batista GomesNessuna valutazione finora
- Constante de AvogadroDocumento8 pagineConstante de AvogadrolucastortelliNessuna valutazione finora
- Revisão - Modelos AtômicosDocumento2 pagineRevisão - Modelos AtômicosEversonNessuna valutazione finora
- Questoes de Massa Atomica e Massa MolecularDocumento5 pagineQuestoes de Massa Atomica e Massa MolecularKarina ChillcceNessuna valutazione finora
- 3.2 e 3.3 Estrutura Atómica e Ligação QuimicaDocumento53 pagine3.2 e 3.3 Estrutura Atómica e Ligação QuimicaPatrícia VieiraNessuna valutazione finora
- 2019 2020 Eq10 02 Teste Elem Quim Sua Organiz v1Documento9 pagine2019 2020 Eq10 02 Teste Elem Quim Sua Organiz v1ISLAMICO69Nessuna valutazione finora
- Questões Sobre Os Átomos - Prof. Adão Marcos Graciano Dos SantosDocumento4 pagineQuestões Sobre Os Átomos - Prof. Adão Marcos Graciano Dos SantosAdão Marcos GracianoNessuna valutazione finora
- Química NuclearDocumento35 pagineQuímica NuclearferpaesNessuna valutazione finora
- Teste - 3 9anoDocumento6 pagineTeste - 3 9anoCristina RodriguesNessuna valutazione finora
- Teste 1 8ºF Out015Documento4 pagineTeste 1 8ºF Out015migualexNessuna valutazione finora
- Química - Elementos QuímicosDocumento3 pagineQuímica - Elementos QuímicosCarrieFontaineNessuna valutazione finora
- O Que É ÁtomoDocumento5 pagineO Que É ÁtomoCristiane SoaresNessuna valutazione finora
- Aula 1-Estrutura AtômicaDocumento12 pagineAula 1-Estrutura AtômicaJonathan RamosNessuna valutazione finora
- Física - Pré-Vestibular Impacto - Eletrostática IDocumento2 pagineFísica - Pré-Vestibular Impacto - Eletrostática IFísica Qui100% (6)
- As 8 Partículas Subatômicas Mais Fundamentais Do Universo PDFDocumento5 pagineAs 8 Partículas Subatômicas Mais Fundamentais Do Universo PDFGustavo PradoNessuna valutazione finora
- TabelaDocumento53 pagineTabelaitalo jimenez100% (1)
- Aula 02 - Modelos At, Estrutura Atômica, Diagrama de Pauling e Semelhanças QuimicasDocumento18 pagineAula 02 - Modelos At, Estrutura Atômica, Diagrama de Pauling e Semelhanças QuimicasKarina GodarthNessuna valutazione finora
- Ficha Nº1Documento9 pagineFicha Nº1Rafael MarquesNessuna valutazione finora
- Grandezas Quimicas - PoligrafoDocumento5 pagineGrandezas Quimicas - PoligrafoRobson Passarinho100% (1)
- Química - Pré-Vestibular Impacto - AtomísticaDocumento2 pagineQuímica - Pré-Vestibular Impacto - AtomísticaQuímica Qui100% (1)
- Introdução A Química ExercíciosDocumento2 pagineIntrodução A Química ExercíciosDaniele Blanco CavalcantiNessuna valutazione finora