Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Amalgama Dental
Caricato da
Christopher Tomás CataláCopyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Amalgama Dental
Caricato da
Christopher Tomás CataláCopyright:
Formati disponibili
AMALGAMA DENTAL
DESARROLLO HISTORICO
Se desconoce quien fue la primera persona en utilizar la amalgama.
1765: Darget usa un compuesto de metales para obturar. 1818: Regnart usa un compuesto de metales de baja fusin (Pb, Sn, Bi) ms un 10% de Hg. 1818: Bell es el primero en usar amalgama en Gran Bretaa. 1826: Traveau usa limaduras de plata pura que mezclaba con Hg "pasta de Hg" 1833: los hermanos Crawcour desarrollaron en Inglaterra el denominado "mineral sucedaneum" basado en una mezcla de limaduras de monedas de Ag con Hg e introdujeron su uso en E.E.U.U.
1845: la Asociacin Americana de Cirujanos dentistas prescribe el uso de la amalgama debido a los graves accidentes que se producan por el Hg. 1850: supone el fin de la guerra de la amalgama porque sta se declara material inocuo para la salud. 1855: Tonwsend aadi Sn a partes iguales con la Ag en la aleacin, lo que mejoraba sensiblemente sus propiedades. 1881:Flagg cambi las propiedades de a aleacin introduciendo 65%de Ag, 35% de Sn y 5% de Cu. 1895: Black establece criterios y bases cientficas para la fabricacin de la amalgama. 1900: se utiliz la amalgama de cobre. 1908: Black recomienda proporciones diferentes a las de la actualidad. 65% de Ag, 28% de Sn, Cu y Zn, y dio lugar a las primeras amalgamas cientficamente desarrolladas.
1910: se realizan investigaciones desde el punto de vista clnico. 1919-1928: establecimiento de normas y especificaciones, se uniformaron los criterios de las aleaciones.
1925: Souder realiz estudios sobre las propiedades fsicas. 1929: la ADA estableci los lmites de cada uno de los componentes y se consiguieron preparados comerciales idnticos. 1936:Gayler realiz estudios sobre los aspectos clinicos de la amalgama. 1957: establecimiento de la FDI: se establecen las normas para el estudio de los materiales.
1962: Taylor y Demaree presenta la aleacin de partculas dispersas. 1963: Innes y Ygudelis emplean en la aleacin cantidades mas elevadas de cobre, aparece la aleacin de fase dispersa. 1973: Mahler observ que la amalgama de fase dispersa era superior clnicamente, porque no presentaba fase 2 y el ndice de fracturas marginales era menor, por eso comenzaron a llamarse aleaciones non fase 2.
1975: comienzan a fabricarse aleaciones de elevado contenido con Cu. 1983: las 2/3 partes de las aleaciones para amalgama son de elevado contenido en Cu.
AMALGAMA DENTAL
CONCEPTOS
- Aleacin: dcese de la mezcla de dos o ms metales para lo cual habremos de calentar por encima de su punto de fusin de los dos metales y dejarlo enfriar hasta alcanzar la temperatura ambiente.
- Sistema de aleacin: dcese de la mezcla de dos o ms metales en todas las combinaciones posibles. Por ejemplo, Au-Cu en distintas proporciones, dan aleaciones distintas; al conjunto de estas aleaciones se llama sistema de aleaciones. Si no los calentamos y los hacemos lquidos no se pueden mezclar entre s.
- Fase: es cualquier proporcin de un sistema fsicamente peculiar, homogneo en su estructura y separable de manera mecnica. Un sistema de aleaciones est formado por todas las fases o compuestos diferentes a que da lugar la mezcla de los metales en cuestin.
- Diagrama de fases o diagrama de equilibrio trmico del sistema de aleaciones: es la forma grfica de representar lo que sucede en un sistema de aleaciones, en el que se muestran las distintas fases que se pueden producir en funcin de los porcentajes de los componentes de la mezcla y la temperatura. Las fases se van nombrando segn el alfabeto griego en orden de aparicin: , y
Nota: slo se expresa la proporcin de uno de los elementos, el otro se obtiene restando al anterior.
Cmo obtener un diagrama de fases: Cogemos un metal y lo sometemos a una temperatura elevada y lo hacemos lquido. Posteriormente lo dejamos enfriar, as obtenemos una curva de enfriamiento.
Xs: punto de inflexin por debajo del cual los metales son slidos. Xl: punto de inflexin por encima del cual los metales son lquidos. Intervalo Xs- Xl: periodo de solidificacin.
La temperatura a partir de la cual un metal se hace lquido se llama T lquida (TI), y cuando la temperatura desciende el metal solidifica a una temperatura llamada T slida (Ts). Por encima de TI la aleacin es completamente lquido. Por debajo de Ts es completamente slida. En la aleacin contamos con un metal A y un metal B con concentraciones x e y. Las aleaciones no tiene un puntode fusin, sino un intervalo de fusin, asi que encontramos distintos intervalos de fusin dependiendo de las distintas concentraciones en las en las que se encuentren los metales:
Si juntamos todas las curvas de enfriamiento posibles al conjugar dos o ms metales, obtendremos un diagrama de fases:
Cuando una aleacin la calentamos por encima de su punto de fusin y luego la dejamos enfriar queda una aleacin slida la cual se puede dividir en:
1. Metales puros: es decir, que los metales sean insolubles en estado lquido y que al solidificar queden separados en capas distintas. No se ha conseguido unirlos. 2. Soluciones slidas: son aquellos miscibles en estado liquido. Los tomos de un metal se entremezclan con los del otro metal, de forma que los tomos de un metal se meten en la estructura del otro, es decir, no se combinan qumicamente. Los metales formarn cristales. Al diluirse puede suceder dos cosas, que los tomos del otro metal se siten entre los del primero o bien los sustituyan.
Por lo tanto tendremos dos tipos de cristales: Soluciones slidas intersticiales (SSI): los tomos del metal que se disuelve (soluto) ocupan espacios entre los tomos del disolvente (denominamos disolvente al metal cuya estructura cristalina permanece, y soluto al metal que se introduce en la estructura cristalina del otro) Ejemplo: Fe-C, uno de los tomos siempre es ms pequeo que el otro, ya que si no fuera as sera imposible introducirse dentro de la estructura. Solucin slida de sustitucin (SSS): en este caso los tomos del solvente ocupan los sitios de los tomos del disolvente; esto es debido a que el tamao atmico es similar. Ej: Au-Cu.
Nota: ./ S.S.I.: el tomo del soluto no ocupa el lugar del tomo del disolvente, sino que slo se mete dentro de la estructura del disolvente, pero sin sustituir un tomo por otro. Por eso el tamao de los tomos del soluto han de ser de menor tamao, porque si no, no cabran.
./ S.S.S.:EI tomo del soluto ocupa el lugar exacto del tomo del disolvente.
Al conseguir soluciones slidas obtendremos una serie de propiedades fsicas: Aumenta la dureza superficial Aumenta la resistencia Aumenta el lmite proporcional Disminuye la ductilidad
3. Mezcla eutctica: los metales al solidificar se hacen insolubles de forma que precipitan en finos cristales yuxtapuestos de uno y otro ntimamente mezclados y conservando su estructura, cosa que no suceda en las soluciones slidas. Esta mezcla tiene unas caractersticas: -Tienen una composicin definida: ocurre cuando mezclo un porcentaje concreto de un metal con otro porcentaje concreto del otro metal. -Temperatura de fusin constante. -Su punto de fusin es el ms bajo de todas las aleaciones que se puedan formar con los dos metales. La mezcla eutctica se consigue en el punto ms bajo donde contacta la lnea de los slidos con la de los lquidos (puede darse el caso de varios puntos pero nunca una lnea). Ej: en el sistema Ag-Cu de abajo la mezcla eutctica se consigue en el punto E, donde la plata se encuentra en un 71,9% Y el cobre al 28,1% cuando se alcanza una temperatura de 780C.
Diagrama de fase de equilibrio del sistema Ag-Cu.
, aleacin rica en Ag , aleacin rica en Cu La mezcla eutctica es la aleacin compuesta por un 71% de Ag y un 281% de Cu
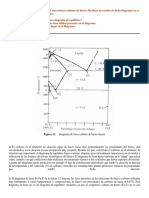
4. Compuestos intermetlicos: al solidificar los metales tienden al formar compuestos quimico, de manera que los tomos de uno no se distribuyen aleatoriamente entre los tomos del otro, sino que se distribuyen de manera definida y concreta. Diagrama de equilibrio del sistema Ag- Sn
- Punto D: es el punto del sistema intermetlico Ag3Sn (fase ) formada por el liquido y el rea superior) - Si Sn es mayor de 26,8% la fase es rica en Sn, la amalgama ser ms dbil a la corrosin. - Si Sn es menor de 26,8%, encontramos entonces una fase y .
METALOGRAFA
INTRODUCCIN La amalgama dental es un material con el que se hacen restauraciones de insercin plstica; para trabajarla se mezcla un polvo, compuesto por una aleacin de dos o ms metales, y un lquido, que es el mercurio (Hg), ste slo es slido a temperaturas significativamente ms bajas que la temperatura ambiente habitual. La masa plstica obtenida se inserta en una preparacin convenientemente realizada en un diente y, dentro de ella, adquiere estado slido
CONCEPTO DE AMALGAMA DENTAL Una aleacin se define como una mezcla de metales en la que un compuesto siempre es el Hg y el otro componente es otra aleacin de metales en la que tambin puede ir incorporado el mercurio.
CONCEPTO DE ALEACIN Es la aleacin de dos o ms metales con el Hg, la cual endurece a Ta ambiente dando lugar a una estructura cristalina. Los metales salvo el Hg se encuentran formando una aleacin metlica denominada aleacin para amalgama dental.
COMPONENTES DE LAS ALEACIONES PARA AMALGAMAS DENTALES Los componentes son cinco: Ag, Sn, Cu, Zn y Hg. Ag: elemento principal en cuanto a porcentaje de participacin en las aleaciones para amalgama dental. Es necesaria para asegurar una adecuada resistencia a la amalgama y asegura su rpido endurecimiento debido a los compuestos que va a formar con el Hg. en la fase de amalgamacin. Un exceso de Ag producira expansin. Sn: contribuye a la amalgamacin y el tiempo de endurecimiento. Un exceso de Sn por encima del 29% producira una excesiva contraccin de la mezcla, reducira la resistencia, prolongara el tiempo de fraguado con lo que aumentara la expansin retardada y las fracturas marginales Cu: se encuentra en amalgamas convencionales, y en cantidades inferiores a un 6% mejora las propiedades de resistencia y dureza, y sirve para mantener al Ag y Sn dentro de los porcentajes porcentajes normales en las amalgamas ricas en Cu, mejorando las propiedades fsicas y el comportamiento clnico. Zn: favorece el proceso de fabricacin industrial. La funcin principal del Zn en las amalgamas es actuar como desoxidante, proporciona amalgamas ms limpias con menor tendencia al ennegrecimiento. Sin embargo, presenta un importante inconveniente, y es que en presencia de humedad descompone el agua en H y O. El H2 forma burbujas que pueden expandir el bloque de la restauracin. Por todo ello no se recomienda utilizar amalgamas que lleven Zn en nios, ni restauraciones en las que no sea posible colocar un dique y aislarlas de la humedad. En Zinc se utilizan en cantidades muy pequeas (0,01%). La amalgama lleva como mnimo un 0'01% de Zn. Si lleva menos se dice que es una amalgama sin Zn.
Hg: en la aleacin sirve para preamalgamar un poco la mezcla, dndole una consistencia adecuada a la aleacin. Son pocas las aleaciones que llevan mercurio y, como ya se ha dicho, un exceso de mercurio provoca expansin.
CLASIFICACIN DE LAS ALEACIONES DE METALES 1. Por su composicin: Aleaciones convencionales Aleaciones de alto contenido en Cu Aleaciones con o sin Zn
2. Por la forma de sus partculas: Aleaciones de limaduras Aleaciones esferoidales Aleaciones mixtas
ALEACIONES CONVENCIONALES Se desarrollaron a a partir de los estudios de Black. Se corresponden a la especificacin nmero 1 de la ADA. Los metales los incorporamos a la aleacin de la siguiente manera: a. Ag: 65-70% b.Sn: 20-29% c.Cu: 0-6% d. Zn: 0-2% e. Hg: 0-3% La Ag y el Sn se incorporan juntos en forma de compuesto intermetlico Ag3Sn, en fase de su sistema de aleaciones. La forma de fabricarlo en fundir un 73% de Ag y un 27% de Sn. Lo calentamos por encima de su punto de fusin y lo dejamos enfriar lentamente por debajo de 480C obteniendo la fase . El Cu, por su parte, puede estar presente de dos maneras: - Disuelto en la aleacin, si es inferior al 2'5%. - En forma de compuestos CU3Sn en fase , y Cu6Sn5 en fase si est entre 2'5% y el 6%.
ALEACIONES DE ALTO CONTENIDO EN Cu Composicin: Ag: 60-70%
Sn: 15-30% Cu: >12% El Cu se introdujo en altas concentraciones en las aleaciones al observarse que produca amalgamas con mejores propiedades fsicas y comportamiento clnico. Este tipo de aleaciones se consiguen de dos maneras:
a.Aleaciones de fase dispersa: (12% de Cu) Se obtienen aadiendo 2/3 partes de aleacin convencional Ag-Sn en forma de compuesto intermetlico Ag3Sn, partculas que generalmente son irregulares, y una 1/3 parte de una mezcla eutctica de Ag-Cu en forma de partculas esferoidales (72% de Ag y 28% de Cu). Se denomina a estas aleaciones de fase dispersa debido a los dos tipos de partculas diferentes que las componen, y el contenido resultante de Cu est en torno al 12% del total de la aleacin. Fueron las primeras aleaciones de alto contenido en Cu que se fabricaron.
b.Aleaciones de composicin uniforme: Se obtienen fundiendo conjuntamente Ag, Sn y Cu en las proporciones antes mencionadas para obtener un bloque de aleacin, del que se obtendrn posteriormente partculas de idntica composicin.
ALEACIONES CON O SIN Zn Con Zn: >0'01 % en su composicin. Sin Zn:S 0'01 % en su composicin. El Zn provoca que las amalgamas sean menos plsticas y ms quebradizas. Por eso se usa en ese porcentaje tan escaso,un exceso provocara expansin. Se usa fundamentalmente como desoxidante por su afinidad al agua, dando aleaciones ms limpias.
ALEACIONES DE LIMADURAS Se obtienen por fresado de un lingote de aleacin, en el que se encuentran todos los metales que forman la aleacin en las proporciones determinadas. Segn el tamao de las limaduras se habla de: - Macrocorte - Corte medio - Microcorte
stas ltimas son las que mejores cualidades clnicas han demostrado al producir una mejor amalgacin, adems de proporcionar una mejor adaptacin de las partculas a las paredes cavitarias. Suelen ser de composicin convencional.
ALEACIONES ESFEROIDALES Se obtienen por atomizacin del metal que constituye la aleacin, fundido dentro de un recipiente que contiene un gas inerte. La aleacin solidifica en forma de pequeas gotas o esfrulas. Pueden ser de composicin convencional o ricas en Cu. Las aleaciones esferoidales ofrecen mejores propiedades mecnicas y comportamiento clnico que las de limaduras: - Requieren menos cantidad de Hg para amalgamarse - Experimentan un endurecimiento ms rpido, por lo que confieren una mayor resistencia inicial de la amalgama (disminuyendo as el ndice de fracturas de la amalgama que aparece en las primeras horas tras la colocacin) - Son adems menos susceptibles a las variables de manipulacin.
ALEACIONES MIXTAS Se corresponden con las denominadas aleaciones de fase dispersa de alto contenido en cobre. Se componen de: 2/3 partes de partculas de limaduras irregulares de composicin convencional 1/3 parte de esferoidales de eutctico Ag-Cu.
CONCEPTO DE AMALGAMA DENTAL Es la aleacin de uno o ms metales con el Hg, la cual endurece dando una estrutura cristalina. Estos metales salvo el Hg, se encuentran a su vez formando una aleacin metlica que se denomina aleacin para amalgama dental.
CLASIFICACIN SEGN EL NMERO DE COMPONENTES Binaria: Cu+ Hg Terciaria: Cu+ Hg+ Ag Cuaternaria: Cu+ Hg+ Ag+ Sn Primaria: Cu+ Hg+ Ag+ Sn+ Zn
REACCIONES DE AMALGAMACIN PARA AMALGAMAS DE COMPOSICiN CONVENCIONAL O DE BAJO CONTENIDO EN Cu
En estas aleaciones, la plata y el estao se encuentran predominantemente en forma del compuesto intermetlico Ag3Sn o fase , pudiendo haber pequeas cantidades de otras fases como la (3. Al mezclarse con el Hg, la Ag y el Sn se separan y el Hg reacciona con cada uno de estos elementos, dando lugar a la siguiente reaccin qumica expuesta de forma simplificada. + Ag3Sn + Hg ~ Ag3Hg4 + Sn8Hg + Ag3Sn 1 2
La fase del final queda porque el metal no se disuelve entero sino que siempre queda un ncleo metlico sin disolver porque no hemos metido Hg suficiente para que queden ncleos metlicos dentro sin disolver confiriendo una mayor resistencia y dureza. Cada compuesto forma la fase de su diagrama de equilibrio, y para diferenciarlos, llamamos: - partcula original Ag3Sn ~ fase (30-35%) - productos subderivados de Ag y Hg= Ag3Hg4 ~ fase 1 (60-70%), - productos subderivados del Sn y Hg = Sn8Hg ~fase 2 (1-10%)
Pueden adems encontrarse pequeas cantidades de fases Cu- Sn: Cu6Sn5~ fase Cu3Sn ~ fase
Al poner estas partculas de aleacin en estado slido en contacto con el Hg lquido, ste baa la superficie de las partculas y penetra en su interior parcialmente, comenzando su reaccin con los metales de la aleacin y dando lugar a las nuevas fases de reaccin 1 y 2,
producidas a costa de la parte ms externa de las partculas de aleacin original, cuyos ncleos internos que no han podido ser atacados por el Hg quedan intactos propiciando que siga existiendo fase . El resultado, por lo tanto, es una estructura nucleada, en la que las nuevas fases 1 y 2 recubren al ncleo que permanece intacto, o sea a la fase . La difusin del Hg al interior de las partculas da lugar a una disminucin de volumen de la mezcla que denominamos contraccin inicial. Al proceso por el cual se dan las reacciones qumicas que generan los nuevos compuestos se denomina cristalizacin y conduce al endurecimiento de la masa, ya que estos productos son slidos a temperatura ambiente.
Esta cristalizacin se produce de manera dendrtica o arborescente, ya que los productos de reaccin originan ramificaciones que suponen un aumento de volumen respecto a la masa original. A tal efecto se le denomina expansin inmediata para diferenciarla de otros procesos de expansin que pueden producirse en la amalgama posteriormente por otras causas.
Como la solubilidad de la Ag en el Hg es del 0'035% en peso y la del Sn es del 0'6%, los productos de la Ag precipitan primero ~ fase 1. Se saturan antes por tener una menor solubilidad. Los productos de Sn precipitan despus ~ fase 2, y como hay mayor cantidad de Ag que de Sn, la fase 1ser mayor y la denominaremos matriz porque atrapa a las partculas de la reaccin que quedan sin reaccionar. La fase 2 tambin ser matriz pero en menor medida. Una vez producida toda la reaccin, son las partculas las que les proporcionan las mejores propiedades a la amalgama. Por ello a mayor cantidad de partculas, mayor resistencia. En la amalgama final tambin pueden quedar productos derivados de la impureza de la fase y que tambin proporcionan dureza, pero en menor cantidad.
PROPIEDADES QUE OFRECEN LAS DISTINTAS FASES DE LA AMALGAMA Fase : es la que presenta un mejor comportamiento clnico, por sufrir poca variacin dimensional y tener buena resistencia compresiva y a la deformacin. Por lo tanto, siempre que exista una amalgamacin adecuada, a mayor fase , mejores propiedades tendr la amalgama resultante. En resumen, es la que aporta las buenas propiedades a una amalgama.
Fase 1: inferior en sus propiedades a la fase anterior, pero aceptable; presenta escasa susceptibilidad a la corrosin y su cristalizacin arborescente es la responsable de la expansin inmediata, -Tiene peores propiedades que -la anterior pero mejores que la 2. Fase 2: es la que ofrece peores cualidades. Es la ms dbil mecnicamente, y adems es muy susceptible a la corrosin ante el contacto con el medio bucal, lo que da lugar a que se separen el Sn y el Hg. De hecho, la resistencia de la fase 2 es un 10% de la que tiene la fase 1. El Hg seguir interactuando con la fase y original, dando lugar a nuevos productos de reaccin, fases 1 y 2, y adems ms matriz, que por su cristalizacin dar lugar a una nueva expansin, denominada expansin retardada. Esta expansin est localizada en la superficie de la obturacin, que es donde se va a producir la corrosin. Esta expansin da lugar a una extrusin fuera de los mrgenes de la cavidad, formndose una cua de amalgama no soportada, susceptible de fracturarse ante fuerzas masticatorias, dando lugar a la denominada fractura marginal. Esta relacin entre la corrosin y la fractura marginal fue establecida por Jorgensen en la denominada "teora de la expansin mercurioscpica" El Sn da lugar a diferentes productos de corrosin, fundamentalmente compuestos de oxgeno y cloro (Sn02, Sn4(OH)6CI2, etc). Estos productos de corrosin se depositan en la interfase diente-obturacin mejorando el sellado marginal y disminuyendo la filtracin. Con el paso del tiempo, la fase 1se transforma en 1, ms estable, lo que implica una liberacin de Hg que queda libre para seguir reaccionando y formar nuevas partculas 1 y 2. Todos estos fenmenos hacen que la amalgama no sea un material estable, sino que a lo largo del tiempo vaya sufriendo cambios que alteran su situacin inicial.
REACCIN DE AMALGAMACIN PARA LAS AMALGAMAS DE ALTO CONTENIDO EN Cu La gran diferencia de estas amalgamas, es que el Cu capta el Sn impidiendo que reaccione con el Hg y, por lo tanto, reduciendo de manera significativa la formacin de la nociva fase 1. Se produce una doble reaccin del Hg: 1. Por un lado con la Ag del eutctico Ag-Cu formando fase 1. 2. Por otro lado con la Ag de la fase y dando lugar tambin a fase 1. El Sn liberado de la fase , reacciona con el Cu del eutctico, por el que tiene gran afinidad, impidiendo la formacin de la fase 2 y generando las fases , , del sistema Cu-Sn. La fase 1 que se ha formado, lo ha hecho de forma simultnea a la fase y rodearn a las partculas del eutctico que han quedado sin consumir. Esta fase 1, al igual que en las amalgamas convencionales forma la matriz (debido al crecimiento arborescente. Las partculas que no se han consumido quedan envueltas en su estructura).
Por lo tanto no se puede hablar de amalgamas non 2 hasta pasada una semana de la amalgamacin. Durante aproximadamente 1 ao la amalgama no es estable porque la fase se transforma paulatinamente en fase , ms estable. La reaccin global al cabo de un ao, momento en que la amalgama se estabiliza, puede representarse as: Las fases resultantes son superiores en cualidades a las aleaciones convencionales. Estas amalgamas presentan:
Menor corrosin Menor expansin retardada Menor fractura marginal
Peor autosellado de la obturacin, al formarse menor cantidad de productos de corrosin, por lo que resulta importante utilizar selladores de interfase (barnices y adhesivos)
Potrebbero piacerti anche
- Capítulo 04 - Libertad, Razón y TradiciónDocumento2 pagineCapítulo 04 - Libertad, Razón y TradiciónejacobprNessuna valutazione finora
- LogicaDocumento5 pagineLogicaAna OrozcoNessuna valutazione finora
- La Teoria de La Anomia de MertonDocumento14 pagineLa Teoria de La Anomia de Mertongabriela1936Nessuna valutazione finora
- Iii Bim - Leng - 4to Año - Guia Nº2 - Los Vicios Del LenguajDocumento8 pagineIii Bim - Leng - 4to Año - Guia Nº2 - Los Vicios Del LenguajJosé Miguel Ojeda Pérez0% (2)
- Los Sofistas y Socrates L Jose GajateDocumento8 pagineLos Sofistas y Socrates L Jose GajateSr. LeonardoNessuna valutazione finora
- Metodo MayeuticoDocumento3 pagineMetodo MayeuticoCatalinaNessuna valutazione finora
- Ética y PolíticaDocumento4 pagineÉtica y Políticajuana100% (1)
- Hechos SocialesDocumento7 pagineHechos SocialesAntonio AguilarNessuna valutazione finora
- El Estado Del Derecho Antes de La Aparición de La Ley de Las 12 TablasDocumento19 pagineEl Estado Del Derecho Antes de La Aparición de La Ley de Las 12 TablasabimedinaNessuna valutazione finora
- Significado de MercantilismoDocumento17 pagineSignificado de MercantilismoJennie LaraNessuna valutazione finora
- El Pensamiento Politico de La Edad MediaDocumento10 pagineEl Pensamiento Politico de La Edad MediaLumaidNessuna valutazione finora
- Causas Internas y Externas Que Dieron Origen A La Guerra de Independencia de MéxicoDocumento2 pagineCausas Internas y Externas Que Dieron Origen A La Guerra de Independencia de MéxicoarmandonetNessuna valutazione finora
- TTeoría Del Estado (De Luca - Finocchiaro)Documento53 pagineTTeoría Del Estado (De Luca - Finocchiaro)julietabaronciniiNessuna valutazione finora
- Apuntes-Nuevos EscenariosDocumento101 pagineApuntes-Nuevos EscenariosAriel Guillermo BanduraNessuna valutazione finora
- Anomia social y participaciónDocumento18 pagineAnomia social y participaciónan91dres100% (1)
- 1 Resumen de Las Meditaciones Metafísicas de René DescarteDocumento3 pagine1 Resumen de Las Meditaciones Metafísicas de René DescarteDiego Olate100% (1)
- SÓCRATES Trabajo FinalDocumento12 pagineSÓCRATES Trabajo FinalMary Marca MamaniNessuna valutazione finora
- Legalidad y Legitimidad JavierDocumento4 pagineLegalidad y Legitimidad JavierJavier LuchettaNessuna valutazione finora
- Análisis de la Teoría del EstadoDocumento75 pagineAnálisis de la Teoría del EstadoBelenMéndezNessuna valutazione finora
- Pensamiento de La Escuela de MiletoDocumento2 paginePensamiento de La Escuela de MiletoKevin Correa67% (3)
- Glosario El Tercer Mundo y El Movimiento No AlineadoDocumento1 paginaGlosario El Tercer Mundo y El Movimiento No AlineadoAdriana SonoNessuna valutazione finora
- Diferendo Entre Colombia y Venezuela Por Golfo CoquivacoaDocumento20 pagineDiferendo Entre Colombia y Venezuela Por Golfo CoquivacoaJonathan GarzonNessuna valutazione finora
- Democracia y Lucha de Clases en La AntiguedadDocumento7 pagineDemocracia y Lucha de Clases en La Antiguedadcarolina guerreroNessuna valutazione finora
- La Filosofia Del Derecho Según HegelDocumento9 pagineLa Filosofia Del Derecho Según HegelAlicia Quiroz100% (1)
- Perspectiva Liberal Burguesa Antes de La Revolución FrancesaDocumento2 paginePerspectiva Liberal Burguesa Antes de La Revolución FrancesaJota RockeroNessuna valutazione finora
- Resumen de Proceso Juridico de Descubrimiento de America Diego FernandezDocumento9 pagineResumen de Proceso Juridico de Descubrimiento de America Diego FernandezFrancisca MoralesNessuna valutazione finora
- Teoria Del ValorDocumento10 pagineTeoria Del ValorPrPl Irán0% (1)
- Sistema de NormasDocumento3 pagineSistema de NormasManuel Bárcenas VNessuna valutazione finora
- Aproximación Historiográfica Al Concepto de Signo LingüísticoDocumento463 pagineAproximación Historiográfica Al Concepto de Signo LingüísticoGabrielaFrancescoliNessuna valutazione finora
- Feudalismo AbsolutismoDocumento5 pagineFeudalismo AbsolutismoSandra PassarelliNessuna valutazione finora
- Fin Del FeudalismoDocumento3 pagineFin Del FeudalismoJuanJesúsGarcíaGonzález0% (2)
- SOCIOLOGÍADocumento10 pagineSOCIOLOGÍAlorNessuna valutazione finora
- Ideas Políticas en RomaDocumento2 pagineIdeas Políticas en RomaAlejandra PeñuelaNessuna valutazione finora
- Aspectos Generales de La Logica: Operaciones ConceptuadorasDocumento7 pagineAspectos Generales de La Logica: Operaciones ConceptuadorasbecmanbecmanNessuna valutazione finora
- Tema 1 Introducción A La FilosofíaDocumento10 pagineTema 1 Introducción A La FilosofíaAlvaro Fal-conde DE AgueraNessuna valutazione finora
- Trabajo de Bases Romanisticas AvanceDocumento61 pagineTrabajo de Bases Romanisticas AvanceElizabeth Angeles Salvador100% (1)
- Contexto Histórico Hobbes y RosseauDocumento4 pagineContexto Histórico Hobbes y Rosseauparlatuto100% (1)
- Gobierno de CubaDocumento2 pagineGobierno de CubaCarlos Enrique AlaviNessuna valutazione finora
- Cuadro ComparativoDocumento7 pagineCuadro ComparativoGenesis CaballeroNessuna valutazione finora
- Egipto MonografiaDocumento17 pagineEgipto MonografiaIlen Mandarachi Escobar100% (1)
- V Los Comicios (Por Curias y Por Centurias)Documento7 pagineV Los Comicios (Por Curias y Por Centurias)jose moralesNessuna valutazione finora
- Cultura ToltecaDocumento3 pagineCultura ToltecaCBHNessuna valutazione finora
- Introducción a las bases filosóficas del positivismoDocumento15 pagineIntroducción a las bases filosóficas del positivismoMariangel MedinaNessuna valutazione finora
- Introduccion Al Derecho UsacDocumento30 pagineIntroduccion Al Derecho UsacdirizaacNessuna valutazione finora
- Monarquía Constitucional GBDocumento10 pagineMonarquía Constitucional GBcamila moncayoNessuna valutazione finora
- Diccionario Derecho Romano 1Documento6 pagineDiccionario Derecho Romano 1Darlin ZapanaNessuna valutazione finora
- MONARQUÍADocumento8 pagineMONARQUÍAAlejandro cordon100% (1)
- Derecho Romano Capitulo 5-6-7-8Documento30 pagineDerecho Romano Capitulo 5-6-7-8Anacari Caztiillo100% (1)
- Ensayo Sobre El Espiritu de Las LeyesDocumento16 pagineEnsayo Sobre El Espiritu de Las LeyesEduardo BolañosNessuna valutazione finora
- Piotr Sztompa. La Modernidad y Más Allá (Resumen)Documento9 paginePiotr Sztompa. La Modernidad y Más Allá (Resumen)jorge gonzalez100% (1)
- La División de PoderesDocumento16 pagineLa División de PoderesferNessuna valutazione finora
- Derecho FeudalDocumento26 pagineDerecho FeudalmigomismoNessuna valutazione finora
- Situación Indígena en El Periodo Colonial: Problemas y PerspectivasDocumento23 pagineSituación Indígena en El Periodo Colonial: Problemas y PerspectivasRodriguez Lucas50% (4)
- RevFranRevoluciónDocumento3 pagineRevFranRevoluciónEduardo José Berrocal Blandón100% (1)
- FeudalismoDocumento5 pagineFeudalismowamNessuna valutazione finora
- Contrato de Mutuo y ComodatoDocumento16 pagineContrato de Mutuo y ComodatoMARIELA ALEJANDRA OSORIO NATARENONessuna valutazione finora
- ANTOLOGIA El Humanismo y El RenacimientoDocumento55 pagineANTOLOGIA El Humanismo y El RenacimientoAngy CalivNessuna valutazione finora
- Elemntos de MetalurgiaDocumento5 pagineElemntos de MetalurgiahNessuna valutazione finora
- Aleaciones MetalicasDocumento6 pagineAleaciones Metalicasely.bayasNessuna valutazione finora
- Halitosis Fisiologia y EnfrentamientoDocumento8 pagineHalitosis Fisiologia y EnfrentamientoatzabiNessuna valutazione finora
- Accesorios - AlimentaciónDocumento3 pagineAccesorios - AlimentaciónChristopher Tomás CataláNessuna valutazione finora
- Guía de Ejército Guerreros Del CaosDocumento18 pagineGuía de Ejército Guerreros Del CaosAndrew AlbertNessuna valutazione finora
- Manifiesto Comunista PDFDocumento79 pagineManifiesto Comunista PDFJuan Carlos González GutiérrezNessuna valutazione finora
- El Señor de La Guerra de Marte Edición de La Biblioteca Marciana Cuentos de Edgar Rice Burroughs - Averigüe Por Qué Me Encanta!Documento2 pagineEl Señor de La Guerra de Marte Edición de La Biblioteca Marciana Cuentos de Edgar Rice Burroughs - Averigüe Por Qué Me Encanta!Christopher Tomás CataláNessuna valutazione finora
- RoqueDiaz VikingosDocumento5 pagineRoqueDiaz VikingosChristopher Tomás CataláNessuna valutazione finora
- Programa de Salud Dental Infantil de MurciaDocumento8 paginePrograma de Salud Dental Infantil de MurciaChristopher Tomás CataláNessuna valutazione finora
- Manejo Paciente OdontoDocumento7 pagineManejo Paciente OdontoChristopher Tomás CataláNessuna valutazione finora
- Trabajo 2 Jeansy Carrascal.......Documento9 pagineTrabajo 2 Jeansy Carrascal.......jeansy cararascalNessuna valutazione finora
- Guía de Acondicionamiento Superficial de Estructuras MetalícasDocumento28 pagineGuía de Acondicionamiento Superficial de Estructuras Metalícassalinov774Nessuna valutazione finora
- Nociones Generales Sobre Propiedades de Los MetalesDocumento24 pagineNociones Generales Sobre Propiedades de Los MetalesPaul TorresNessuna valutazione finora
- Mapa Mental Dream TeamDocumento6 pagineMapa Mental Dream TeamRodolfo RegaladoNessuna valutazione finora
- Qué Es El HierroDocumento4 pagineQué Es El HierroVeronica Ibarra100% (1)
- Lab de Tecnología de Materiales 2019-IDocumento68 pagineLab de Tecnología de Materiales 2019-IGustavo FloresNessuna valutazione finora
- Zinc y Sus AleacionesDocumento28 pagineZinc y Sus AleacioneseliaNessuna valutazione finora
- Madrid Científico. 1913, No. 767 PDFDocumento16 pagineMadrid Científico. 1913, No. 767 PDFAntonio BravoNessuna valutazione finora
- PRACTICA N 02 DE MECANICA DE FLUIDO JuevesDocumento30 paginePRACTICA N 02 DE MECANICA DE FLUIDO JuevesYvis Antonio Suarez PerezNessuna valutazione finora
- Anodizado de TitanioDocumento107 pagineAnodizado de TitanioLeon JimarezNessuna valutazione finora
- T3P2Documento4 pagineT3P2Adan BarreraNessuna valutazione finora
- PREGUNTAS DE REPASO MetalesDocumento5 paginePREGUNTAS DE REPASO MetalesZaida Briones SerenaNessuna valutazione finora
- Superaleaciones Base CobaltoDocumento4 pagineSuperaleaciones Base CobaltoKarinaFloresMorales100% (1)
- 01 - Cojinete - de Deslizamiento PDFDocumento9 pagine01 - Cojinete - de Deslizamiento PDFJuan Pablo AparicioNessuna valutazione finora
- Estructura de las Aleaciones y sus PropiedadesDocumento54 pagineEstructura de las Aleaciones y sus PropiedadesJulius CandelarioNessuna valutazione finora
- Hornos de Crisol 1Documento27 pagineHornos de Crisol 1JeanCarloNoreñaNessuna valutazione finora
- Sistemas EutecticosDocumento15 pagineSistemas EutecticosHelen Cárdenas HonoresNessuna valutazione finora
- Ejercicios PropuestosDocumento2 pagineEjercicios PropuestosGuadalupe LunaNessuna valutazione finora
- Efecto de Los Elementos AleantesDocumento11 pagineEfecto de Los Elementos AleantesArmando Mendieta HernandezNessuna valutazione finora
- Tema 4. Biomateriales MetálicosDocumento86 pagineTema 4. Biomateriales MetálicosAntonio Jimenez RecioNessuna valutazione finora
- Riesgos Higienicos en El Sector de La JoyeriaDocumento14 pagineRiesgos Higienicos en El Sector de La JoyeriaKaren Zugeidi Buitrago GarciaNessuna valutazione finora
- Demostracion de La Regla de La PalancaDocumento6 pagineDemostracion de La Regla de La PalancaMaría Argomedo ReyesNessuna valutazione finora
- Expo Aleaciones Al FinalDocumento141 pagineExpo Aleaciones Al FinalIlse GutierrezNessuna valutazione finora
- 2011 - Resol 1725 Protesico DentalDocumento19 pagine2011 - Resol 1725 Protesico Dentaldaian3012100% (1)
- Puntos Invariantes Hierro CarbonoDocumento2 paginePuntos Invariantes Hierro CarbonoLeo DonadoNessuna valutazione finora
- AmalgamaDocumento5 pagineAmalgamaJoOn BrightsideNessuna valutazione finora
- Aleaciones de Cobalto Cromo MolibdenoDocumento14 pagineAleaciones de Cobalto Cromo MolibdenoReginaldo Tr100% (1)
- Trabajo Todo Sobre El Acero y El FierroDocumento29 pagineTrabajo Todo Sobre El Acero y El FierroJuan Edgardo Farias BarretoNessuna valutazione finora
- Antologia 2017Documento59 pagineAntologia 2017Akira RyugujiNessuna valutazione finora
- Actividadd 1555469727Documento4 pagineActividadd 1555469727S'ammi L'ealNessuna valutazione finora