Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Clasificación y Fundamento de Análisis Volumétrico
Caricato da
Duck PatyTitolo originale
Copyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Clasificación y Fundamento de Análisis Volumétrico
Caricato da
Duck PatyCopyright:
Formati disponibili
Clasificacin y fundamento de anlisis volumtrico: Es el anlisis cuantitativo que busca medir el volumen de una solucin estndar o solucinnormal, necesario
para completar la reaccin especfica en una muestra sometida a examen.La solucin normal o estndar es aquella cuya concentracin o valor de reaccin por unidadde volumen es conocido. Valoraciones cido-base. Se efecta una reaccin de neutralizacin en la cual un cido reacciona con una cantidad equivalente de base. El valorante es siempre un cido o una base fuerte, siendo el analito una base o cido fuerte o dbil. Las curvas de valoracin se construyen representando el pH de la disolucin frente al volumen de reactivo aadido. Los indicadores utilizados suelen ser cidos o bases dbiles de intensos colores. Valoraciones de oxidacin-reduccin. En este tipo de valoraciones se produce una reaccin de transferencia de electrones entre el analito (sustancia a valorar) y el agente valorante. La reaccin que discurre entre ambos debe ser de cintica alta, puesto que de su velocidad depende la obtencin de buenos resultados. Por otra parte debe disponerse de un medio que permite observar el punto final de la valoracin. Estos indicadores pueden ser de muy diversos tipos, pero por lo general, son sustancias con caractersticas redox y cuya forma oxidada y reducida tienen diferente color. El valor del potencial normal del indicador tiene que estar entre los potenciales normales de los dos sistemas, para que viere cerca del punto de equivalencia de la valoracin. 9 Valoraciones de precipitacin. Estn basadas en reacciones en las que se forman compuestos de baja solubilidad. La mayora de los precipitados se forman lentamente lo que hace que se disponga de pocos agentes precipitantes para su aplicacin en valoraciones. Valoraciones de formacin de complejos. Los reactivos que forman complejos se utilizan ampliamente en la valoracin de cationes metlicos. Los ms empleados son compuestos orgnicos que tienen varios grupos donadores de electrones capaces de formar numerosos enlaces covalentes con iones metlicos. Como indicadores qumicos se utilizan colorantes orgnicos que forman quelatos coloreados con los iones metlicos. El negro de eriocromo T es de los ms utilizados, cuyos complejos con los iones metlicos son generalmente rojos, presentado un cambio de coloracin en funcin del pH del medio en el que se realice la valoracin puesto que la especie libre es roja/azul/naranja en funcin de que estemos a pH<6.3, 6.3<pH<11.6, y pH>11.6 respectivamente.
2.- importancia del manejo de disoluciones normales en el anlisis volumtrico. Es de suma importancia ya que este mtodo se utiliza para medir disoluciones liquidas, y se debe tener un concepto de lo que son las disoluciones normales para manejar bien este mtodo
3.- peso equivalente Peso equivalente: El peso equivalente de un elemento o compuesto es la cantidad del mismo que se combina o reemplaza a 8.000 partes de oxigeno o 1.008 partes de hidrogeno. El peso equivalente se expresa en gramos. *el peso equivalente de un elemento o compuesto se determina de acuerdo a los nmeros totales de equivalentes de los cationes o aniones, si se trata de una sal, cido o base, de acuerdo al numero de electrones ganados o perdidos por las sustancias de una reaccin o si es un metal de acuerdo al peso que es necesario para producir 11.2L de H2. *Peso equivalente de un acido. es igual a su peso molecular dividido por el numero de atomos de hidrgeno contenidos en su molcula y capaces de ser sustituidospor un metal. *Peso equivalente de una base. es igual a su peso molecular dividido por la valencia del metal o el numero de los grupos hidroxilos contenidos en la molcula de la base. 4.- Errores en una determinacin analtica. Error Absoluto : E = xi - xt (donde xt = valor verdadero o aceptado) Error Relativo : Er = xi -xt 100%
xt Errores Accidentales Prdida de parte de la muestra Contaminacin de la muestra Avera de algn instrumento Errores Sistematicos o Determinados Aquellos que pueden determinarse y probablemente evitarse o corregirse Errores aleatorios o indeterminados Errores fortuitos cuya magnitud y signo no pueden predecirse ni calcularse
5.- importancia de la estadstica en el anlisis qumico:
Bueno en general la importancia que tiene la estadstica en el anlisis qumico es muy esencial ya que con este y sus medidas de tendencia central, como media, varianza desviacin estndar, entre otras, ayuda a interpretar los datos obtenidos y si llegas a una respuesta sobre la investigacin
Potrebbero piacerti anche
- Cuestionario de Analitica (1) VolumetriaDocumento27 pagineCuestionario de Analitica (1) VolumetriasegundoNessuna valutazione finora
- Fundamentos Del Análisis VolumétricoDocumento19 pagineFundamentos Del Análisis VolumétricoLili GrandaNessuna valutazione finora
- Analisis de AguasDocumento7 pagineAnalisis de AguasAlexanderZuñigaGarciaNessuna valutazione finora
- Análisis VolumétricosDocumento3 pagineAnálisis VolumétricosRodrigo Mono Pinto100% (1)
- Titulaciones Complejometricas PDFDocumento10 pagineTitulaciones Complejometricas PDFJnr JhomarNessuna valutazione finora
- Valoración - Complexométrica - Tema4 - Química AnalíticaDocumento15 pagineValoración - Complexométrica - Tema4 - Química AnalíticaSenki93Nessuna valutazione finora
- Titulaciones Acido-Base y ComplejométricasDocumento22 pagineTitulaciones Acido-Base y ComplejométricasMartha CabreraNessuna valutazione finora
- Informacion DiapositivasDocumento3 pagineInformacion DiapositivasJEAN CARLOS TORRES POVEDANessuna valutazione finora
- Análisis volumétrico: Conceptos básicos de valoraciónDocumento12 pagineAnálisis volumétrico: Conceptos básicos de valoraciónDiana Calderon PazNessuna valutazione finora
- Tipos de Métodos de Análisis CuantitativoDocumento27 pagineTipos de Métodos de Análisis CuantitativoLaü Xï Giraldo0% (1)
- Análisis Volumétrico Ácido PDFDocumento3 pagineAnálisis Volumétrico Ácido PDFCarlos Humberto FloresNessuna valutazione finora
- Tarea4 Analisis CuantitativoDocumento11 pagineTarea4 Analisis CuantitativoMauricio Andrade0% (1)
- Ut 2 VolumetríasDocumento7 pagineUt 2 Volumetríasmario tiradoNessuna valutazione finora
- Practica Titulacion de HCL y NaohDocumento17 paginePractica Titulacion de HCL y NaohOscar MedinaNessuna valutazione finora
- Aplicaciones de La VolumetriaDocumento22 pagineAplicaciones de La VolumetriaElías Torres71% (7)
- Acido BaseDocumento12 pagineAcido BasedenissaNessuna valutazione finora
- Potenciometría de neutralizaciónDocumento9 paginePotenciometría de neutralizaciónJavier GamesrodriguezNessuna valutazione finora
- Informe 2 FinalDocumento18 pagineInforme 2 FinalCamila Isabel Sanchez FukushimaNessuna valutazione finora
- Cálculo y aplicaciones del factor gravimétricoDocumento5 pagineCálculo y aplicaciones del factor gravimétricoEmilio GutierrezNessuna valutazione finora
- Aplicaciones de La Gravimetria y VolumetriaDocumento8 pagineAplicaciones de La Gravimetria y Volumetriajesus abraham santamaria ruizNessuna valutazione finora
- Métodos VolumétricosDocumento8 pagineMétodos VolumétricosEmanuel MoralesNessuna valutazione finora
- CUESTIONARIODocumento2 pagineCUESTIONARIODennys ZavalaNessuna valutazione finora
- Informe Final de LectroquimicaDocumento19 pagineInforme Final de LectroquimicaEnrique Fernando Llaza TomayaNessuna valutazione finora
- Volumetría de NeutralizaciónDocumento69 pagineVolumetría de NeutralizaciónJhossy Aisha NyaNessuna valutazione finora
- Informe Laboratorio 4 Quimica BasicaDocumento28 pagineInforme Laboratorio 4 Quimica BasicaAndtimonNessuna valutazione finora
- Glosario Quimica AnaliticaDocumento19 pagineGlosario Quimica AnaliticaDiana Iraiz Mendoza MarquezNessuna valutazione finora
- Analisis VolumetricoDocumento3 pagineAnalisis VolumetricoCristian GomezNessuna valutazione finora
- Informe VolumetriaDocumento7 pagineInforme Volumetriarodrigo JulcaNessuna valutazione finora
- Quimica Analitica (Pal 12Documento15 pagineQuimica Analitica (Pal 12Bismarck Sernaque CordovaNessuna valutazione finora
- Tema 4Documento6 pagineTema 4Olga MartínezNessuna valutazione finora
- Analisis Cuantitativo y Cualitativo de AlcoholesDocumento28 pagineAnalisis Cuantitativo y Cualitativo de AlcoholesErick Villegas MayhuaNessuna valutazione finora
- Informe 6 Analisis Quimico Volumetria de NeutralizacionDocumento14 pagineInforme 6 Analisis Quimico Volumetria de NeutralizacionMARCO ANTONIO BOJORQUEZ PAUCARNessuna valutazione finora
- Marco Teoric1Documento20 pagineMarco Teoric1Kevin Mamani0% (1)
- Prelab 5 Volumetría de Compuestos de CoordinaciónDocumento4 paginePrelab 5 Volumetría de Compuestos de CoordinaciónYankarlo OrdoñezNessuna valutazione finora
- Cuestionario de VolumetriaDocumento8 pagineCuestionario de VolumetriaAlejandra Santiago0% (1)
- Titu Laci OnDocumento18 pagineTitu Laci OnKevin MamaniNessuna valutazione finora
- Clasificación Del A Análisis Químico CuantitativoDocumento10 pagineClasificación Del A Análisis Químico CuantitativoLuis Adalberto Santiago MelendezNessuna valutazione finora
- Análisis VolumétricoDocumento5 pagineAnálisis VolumétricoDaniel J BelloNessuna valutazione finora
- Informe 12 Valoracion de Un Alcali Vs Un AcidoDocumento6 pagineInforme 12 Valoracion de Un Alcali Vs Un AcidoCindy Villacis0% (2)
- Tema 1 Metodos Clasicos.,.Documento4 pagineTema 1 Metodos Clasicos.,.aanitahpNessuna valutazione finora
- Taller de Quimica Analitica para Entrega Por Parejas PDFDocumento7 pagineTaller de Quimica Analitica para Entrega Por Parejas PDFMARIANA ALVAREZ RESTREPONessuna valutazione finora
- Análisis volumétrico: determinación de concentraciones desconocidasDocumento17 pagineAnálisis volumétrico: determinación de concentraciones desconocidasCRISTOFER VICTOR VASCONSUELO EUGENIO100% (1)
- ANALISIS VOLUMETRICO TareaDocumento16 pagineANALISIS VOLUMETRICO TareaCRISTOFER VICTOR VASCONSUELO EUGENIONessuna valutazione finora
- Analitica 1Documento5 pagineAnalitica 1JAVIER NICOLAS CERON ROMERONessuna valutazione finora
- Titulación AcidoDocumento8 pagineTitulación AcidoLuciana Benavente ManriqueNessuna valutazione finora
- Indicadores Ácido BaseDocumento9 pagineIndicadores Ácido BaseDiegoo D'LunaNessuna valutazione finora
- Quimica AnaliticaDocumento18 pagineQuimica AnaliticaJossJossNessuna valutazione finora
- Tema 3 - Introd A La Volumetria 27-08-2012Documento56 pagineTema 3 - Introd A La Volumetria 27-08-2012josemaria0205940% (1)
- Práctica 5: Valoraciones Ácido-Base.Documento25 paginePráctica 5: Valoraciones Ácido-Base.Enrique DelgadoNessuna valutazione finora
- Técnicas analíticas alimentariasDocumento66 pagineTécnicas analíticas alimentariasSebastian ErassoNessuna valutazione finora
- Cap 7 VolumetríaDocumento22 pagineCap 7 VolumetríaJoshua Head100% (1)
- Volumetría de Neutralización UNSA (2) y OrecipitaciónDocumento142 pagineVolumetría de Neutralización UNSA (2) y OrecipitaciónAlejandro Zambrano50% (2)
- IntroducciónDocumento8 pagineIntroducciónJader Álvarez AcostaNessuna valutazione finora
- Valoracion CuantitativaDocumento12 pagineValoracion CuantitativaRosalynNeciosupRamosNessuna valutazione finora
- Soluciones y TitulacionDocumento8 pagineSoluciones y TitulacionAbel de Jesús RiveraNessuna valutazione finora
- Titulación RedoxDocumento4 pagineTitulación RedoxValle Salcedo RoyNessuna valutazione finora
- Práctica 6Documento16 paginePráctica 6Jesús B. PérezNessuna valutazione finora
- Cuestionario de VolumetriaDocumento8 pagineCuestionario de VolumetriaPau CasTañoNessuna valutazione finora
- De Prod Com 7 LmeDocumento12 pagineDe Prod Com 7 LmeAreelii Vaaldeez0% (1)
- Técnicas analíticas básicas: En el control de la calidad del agua según normatividadDa EverandTécnicas analíticas básicas: En el control de la calidad del agua según normatividadNessuna valutazione finora
- Los Sauces de Olimar - Propuestas bodas y eventos 2022/23Documento12 pagineLos Sauces de Olimar - Propuestas bodas y eventos 2022/23Lucas Garcia SanchezNessuna valutazione finora
- Pauta de Clasificacion Rocas Igneas Intrusivas y Extrusivas GeoRustonDocumento8 paginePauta de Clasificacion Rocas Igneas Intrusivas y Extrusivas GeoRustonCroSe VALORANTNessuna valutazione finora
- Actividades GymkanaDocumento6 pagineActividades GymkanaManuel Jalón RojasNessuna valutazione finora
- Presupuesto-184-19 Venta de Repuestos Municipalidad de Monzon - 290G-LC - 500 Horas ..Documento2 paginePresupuesto-184-19 Venta de Repuestos Municipalidad de Monzon - 290G-LC - 500 Horas ..Miguel Angel Perales GuerraNessuna valutazione finora
- Trabajo Hidro11Documento13 pagineTrabajo Hidro11Nelson AlarconNessuna valutazione finora
- Enfermedad Transmitida Por Alimentos F355Documento2 pagineEnfermedad Transmitida Por Alimentos F355Victor Mauricio Rengifo HurtadoNessuna valutazione finora
- Actividad 2Documento8 pagineActividad 2Lourdes MadridNessuna valutazione finora
- Desprendimiento Prematuro de Placenta Normalmente InsertaDocumento7 pagineDesprendimiento Prematuro de Placenta Normalmente InsertaJuanMallmaCartolinNessuna valutazione finora
- Conocimientos Tradicionales Relativos A La Biodiversidad PDFDocumento413 pagineConocimientos Tradicionales Relativos A La Biodiversidad PDFNuria NebotiNessuna valutazione finora
- Costos producción muebles maderaDocumento6 pagineCostos producción muebles maderaFabio Humberto Garcia MondragonNessuna valutazione finora
- Estrategia Geometalurgica en Flotacion GFLCDocumento19 pagineEstrategia Geometalurgica en Flotacion GFLCheniken79Nessuna valutazione finora
- SOLDADURADocumento27 pagineSOLDADURAEddy RolanNessuna valutazione finora
- Tesis RivasDocumento37 pagineTesis RivasKleyjarhCorreaNessuna valutazione finora
- Ficha 06 Identificamos Las Potencialidades de Nustra LocalidadDocumento2 pagineFicha 06 Identificamos Las Potencialidades de Nustra LocalidadElmer Aranda AltamiranoNessuna valutazione finora
- Aguirrefabian, Gestor - A de La Revista, 73-104-1-CEDocumento5 pagineAguirrefabian, Gestor - A de La Revista, 73-104-1-CEMARIA GOMEZNessuna valutazione finora
- Juegos de MesaDocumento19 pagineJuegos de Mesaeduardopineros100% (1)
- Campaña Lustria Conquista Del Nuevo Mundo 2004 EsDocumento20 pagineCampaña Lustria Conquista Del Nuevo Mundo 2004 EsSylcred TVNessuna valutazione finora
- Memoria DescriptivaDocumento37 pagineMemoria Descriptivayamilet839Nessuna valutazione finora
- Triptico Reserva Nacional MatsesDocumento2 pagineTriptico Reserva Nacional MatsesChayi ReyNessuna valutazione finora
- Monografia - Trastornos Metabolicos Del Recien NacidoDocumento13 pagineMonografia - Trastornos Metabolicos Del Recien NacidoEdward Escobar GarciaNessuna valutazione finora
- Macronutriente y MicronutrienteDocumento11 pagineMacronutriente y MicronutrienteAron Martinez TorresNessuna valutazione finora
- Trabajo en espacios confinadosDocumento8 pagineTrabajo en espacios confinadosNovita AguileraNessuna valutazione finora
- Cien Años de Soledad - Gabriel García M.Documento16 pagineCien Años de Soledad - Gabriel García M.Ulises Ronda lopezNessuna valutazione finora
- Practina N°1. Sistema de Generación de FríoDocumento23 paginePractina N°1. Sistema de Generación de FríoLiliana Llaure HuingoNessuna valutazione finora
- Amoxycol Is 366Documento2 pagineAmoxycol Is 366Yhimi YhanNessuna valutazione finora
- Control de Temperatura Del Cuarto FríoDocumento4 pagineControl de Temperatura Del Cuarto FríoCristhiam Alexis Serrano RicoNessuna valutazione finora
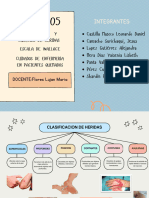
- Clasificacion de HeridasDocumento8 pagineClasificacion de HeridasLeonardo CastillaNessuna valutazione finora
- La Religión RomanaDocumento43 pagineLa Religión RomanaispnolascoNessuna valutazione finora
- Caso Turismo Baldeon - CalderonDocumento38 pagineCaso Turismo Baldeon - CalderonJhon Alex Baldeon CondoriNessuna valutazione finora
- Especificaciones Tecnicas para Aguas NegrasDocumento17 pagineEspecificaciones Tecnicas para Aguas NegrasmarioalonsofNessuna valutazione finora