Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Tipos de Catalizadores
Caricato da
Margoth PesantezTitolo originale
Copyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Tipos de Catalizadores
Caricato da
Margoth PesantezCopyright:
Formati disponibili
UNIVERSIDAD DE CUENCA
FACULTAD DE CIENCIAS QUÍMICAS
CARRERA DE INGENIERÍA QUIMICA
TALLER NO 3 / QUÍMICA GENERAL
TIPOS DE CATALIZADORES
Margoth Pesántez
Universidad de Cuenca, Facultad de Ciencia Químicas, Carrera de Ingeniería
Química.
Cuenca – Ecuador
Autor para correspondencia: joceline.pesantez@ucuenca.edu.ec
Fecha de recepción: 29-10-2018
“TIPOS DE CATALIZADORES”
INTRODUCCIÓN
La transformación de los reactivos en los productos de reacción es el resultado
de un conjunto de etapas, como la interacción de las moléculas con los centros donde
reside la actividad catalítica, el transporte de fluidos hasta llegar a ellos o las reacciones
que modifican la composición. Cada una de estas etapas se produce a una determinada
velocidad que es función de la naturaleza del proceso.
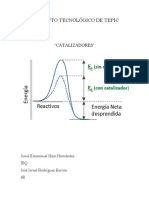
Un catalizador es una sustancia química, simple o compuesta, que modifica la
velocidad de una reacción química, interviniendo en ella, pero sin llegar a formar parte
de los productos resultantes de la misma, es decir aceleran una reacción al disminuir la
energía de activación o al cambiar el mecanismo de reacción.[ CITATION LaH85 \l 12298 ]
TIPOS DE CATALIZADORES:
Catalizadores homogéneos:
La catálisis homogénea tiene lugar cuando los reactivos y el catalizador se encuentran
en la misma fase, ya sea líquida o gaseosa.
o Catalizadores ácido-base
Este tipo de catalizadores agregan o quitan un protón a un reactivo y eso provoca que se
acelere la reacción.
En la catálisis ácida, el catalizador generalmente es un ion H+. En la catálisis básica,
-
generalmente es un ion (OH) .
UNIVERSIDAD DE CUENCA
FACULTAD DE CIENCIAS QUÍMICAS
CARRERA DE INGENIERÍA QUIMICA
TALLER NO 3 / QUÍMICA GENERAL
Por lo general, el catalizador ácido mas usado es el Ácido Sulfúrico (H2SO4).
o Catalizadores organometálicos por complejos de metales de
transición.
Los Compuestos Organometálicos son el resultado de la unión de diversos
metales con grupos orgánicos Alquilo (ejemplo: CH3-, Metil) y Arilo (ejemplo: C 6H5-,
Fenilo). Son muy empleados, especialmente los Metal-Alquilo, en las síntesis orgánicas.
Los compuestos organometálicos de aluminio están entre los catalizadores más
activos en procesos de síntesis de carbonatos cíclicos.
o Catalizadores biológicos
Por lo general este tipo de catalizadores son conocidos como enzimas y actúan
generalmente en todos los procesos bioquímicos que ocurren en los seres vivos.
Las enzimas son capaces de lograr que la reacción transcurra con actividades
muy superiores porque sus centros activos presentan ciertas características específicas.
Existen muchos puntos de contacto entre el catalizador y el substrato, se
producen cambios estructurales muy rápidos debido a la flexibilidad de la proteína para
facilitar la catálisis de la reacción y, finalmente, disponen de una sorprendente habilidad
para combinar efectos aparentemente incompatibles, como la simultaneidad de la
catálisis ácida y básica y de las interacciones hidrofóbicas e hidrofílicas. [ CITATION Art04
\l 12298 ]
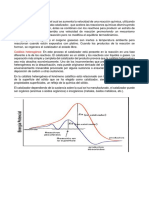
Catalizadores heterogéneos
La catálisis heterogénea se produce entre dos fases, por ejemplo: sólido-gas o líquido-
sólido.
Generalmente están hecho de metal y su función es incrementar el número de colisiones
exitosas que ocurren en una reacción y también pueden crear nuevos intermediarios de
la reacción o nuevos pasos en los mecanismos de la reacción.
UNIVERSIDAD DE CUENCA
FACULTAD DE CIENCIAS QUÍMICAS
CARRERA DE INGENIERÍA QUIMICA
TALLER NO 3 / QUÍMICA GENERAL
Los catalizadores heterogéneos son catalizadores que se encuentran en una fase
distinta que los reactivos. Por ejemplo, el catalizador podría estar en fase sólida
mientras que los reactivos están en fase líquida o gaseosa.
CONCLUSIONES
Para concluir, un catalizador es un agente es decir puede ser una sustancia o un
compuesto que actúa acelerando o retardando una reacción. Los catalizadores son muy
importantes en la fabricación, refinación, entre otros procesos. Por lo tanto, podemos
decir que un catalizador además de aumentar la velocidad de transformación, puede
favorecer o dificultar la formación de determinados productos finales.
BIBLIOGRAFÍA
Cuevas, R. (10 de Febrero de 2009). Clasificación de los Catalizadores. Obtenido de
http://depa.fquim.unam.mx/amyd/archivero/clasificacioncatalizadores_6456.pdf
La Habana. (1985). Quimica General. Editorial pueblo y educación.
Mendez, A. (13 de Septiembre de 2013). Catalizadores. Obtenido de
https://quimica.laguia2000.com/ecuaciones-quimicas/catalizadores
Romero, A. (2004). Catalizadores y procesos catalíticos. Obtenido de
http://www.rac.es/ficheros/discursos/dr_20080825_148.pdf
Potrebbero piacerti anche
- Modelamiento y casos especiales de la cinética química heterogéneaDa EverandModelamiento y casos especiales de la cinética química heterogéneaValutazione: 3 su 5 stelle3/5 (1)
- CatalizadorDocumento23 pagineCatalizadoralfredo pcNessuna valutazione finora
- CatalizadoresDocumento7 pagineCatalizadoresJOSU� EMMANUEL HAM HERN�NDEZ100% (1)
- Unidad V.catalisis en Sistemas Homogeneos y HeterogeneosDocumento19 pagineUnidad V.catalisis en Sistemas Homogeneos y Heterogeneosgreey escorciaNessuna valutazione finora
- Catalizadores No BiologicosDocumento9 pagineCatalizadores No BiologicosYuritziNessuna valutazione finora
- Unidad 4 Fisicoquimica 2Documento32 pagineUnidad 4 Fisicoquimica 2Adán Fonseca HernandezNessuna valutazione finora
- Investigacion CatalizadoresDocumento5 pagineInvestigacion CatalizadoresLeslie Priscila VelNessuna valutazione finora
- Catalizadores No BiológicosDocumento9 pagineCatalizadores No BiológicosYuritziNessuna valutazione finora
- Reactor Catalitico HeterogeneoDocumento21 pagineReactor Catalitico HeterogeneoHector Efrain Cortes MedinaNessuna valutazione finora
- Catalisis - Tapia Medina TeresitaDocumento19 pagineCatalisis - Tapia Medina TeresitaTeresita tapiaNessuna valutazione finora
- Ensayo Sobre Los CatalizadoresDocumento3 pagineEnsayo Sobre Los CatalizadoresBernardo SerpaNessuna valutazione finora
- Catalisis AmbientalDocumento13 pagineCatalisis AmbientalJhonatan MalaraNessuna valutazione finora
- Catálisis: IntegrantesDocumento34 pagineCatálisis: IntegrantesMARIA DE LA LUZ TORRES ZARATENessuna valutazione finora
- CatalisisDocumento21 pagineCatalisisBeatriz EchevarriaNessuna valutazione finora
- Catalizador HomogéneoDocumento4 pagineCatalizador HomogéneoJGerardo D Hernández100% (1)
- Practica CatalizadoresDocumento2 paginePractica CatalizadoresSarai Luz LuzNessuna valutazione finora
- CatálisisDocumento5 pagineCatálisisLEONARDO V�CTOR EUGENIO PACHAS QUISPENessuna valutazione finora
- Reunidad IvDocumento9 pagineReunidad IvLuis Fernando Carrizales CastilloNessuna valutazione finora
- Investigación U4Documento10 pagineInvestigación U4RmnNessuna valutazione finora
- Maria Veronica FisicoquimicaDocumento16 pagineMaria Veronica FisicoquimicaBrenda araujooNessuna valutazione finora
- LAB3 QMCDocumento5 pagineLAB3 QMCNikol Lopez ValdezNessuna valutazione finora
- CatálisisDocumento12 pagineCatálisisJC MosqueraNessuna valutazione finora
- CATALISISDocumento12 pagineCATALISISeduanllNessuna valutazione finora
- Marco Teorico)Documento24 pagineMarco Teorico)Jhoan BorhorquezNessuna valutazione finora
- Unidad IV. Investigación FisicoquímicaiiDocumento32 pagineUnidad IV. Investigación FisicoquímicaiiCarlos FernandoNessuna valutazione finora
- CatalisisDocumento14 pagineCatalisisLuciano Matías SalasNessuna valutazione finora
- Unidad 4 CatalisisDocumento35 pagineUnidad 4 CatalisisFrancis Xavier Santos Trinidad100% (2)
- Actividad 12. Reforzamiento y Preparación para Examen Parcial IIDocumento26 pagineActividad 12. Reforzamiento y Preparación para Examen Parcial IIFernando FariñasNessuna valutazione finora
- CatalizadoresDocumento22 pagineCatalizadoressofiaNessuna valutazione finora
- Mapas Conceptuales1.Pptx (Autoguardado)Documento10 pagineMapas Conceptuales1.Pptx (Autoguardado)Jhoan Borhorquez100% (1)
- 3 - Catálisis Homogénea UT 1Documento51 pagine3 - Catálisis Homogénea UT 1Cristina Clavijo100% (1)
- CATALISIS (Final2)Documento28 pagineCATALISIS (Final2)Liliana LiliNessuna valutazione finora
- Resumen de CatalisisDocumento5 pagineResumen de CatalisisLUIS ANGEL VAZQUEZ VALDOVINOSNessuna valutazione finora
- CatálisisDocumento3 pagineCatálisisAaron Huillcas SullcarayNessuna valutazione finora
- Cinetica Unidad 5Documento21 pagineCinetica Unidad 5David JuniorNessuna valutazione finora
- HoyDocumento3 pagineHoyJose Wenceslao Calcina TuniNessuna valutazione finora
- Catalizador - EcuRed PDFDocumento3 pagineCatalizador - EcuRed PDFYori Edison Vasquez SalamancaNessuna valutazione finora
- CATÁLISISDocumento6 pagineCATÁLISISAdrian GarciaNessuna valutazione finora
- Catalisis Refinacion y PetroquimicaDocumento11 pagineCatalisis Refinacion y PetroquimicaFatima Salvador0% (1)
- CatálisisDocumento3 pagineCatálisislaurarimaNessuna valutazione finora
- Unidad 4 Fisicoquimica2Documento56 pagineUnidad 4 Fisicoquimica2Martha C. ArroyoNessuna valutazione finora
- Catálisis de Las Reacciones QuímicasDocumento22 pagineCatálisis de Las Reacciones QuímicasElizabeth ChirinosNessuna valutazione finora
- Catalizadores de RefinacionDocumento27 pagineCatalizadores de RefinacionEdwin Pachacuti Apaza100% (1)
- CatalisisDocumento10 pagineCatalisisHector Junior AdamesNessuna valutazione finora
- Ordenado Tema Del Primer SeminarioDocumento22 pagineOrdenado Tema Del Primer SeminarioMadheleyn del Carmen Alvarez ArmasNessuna valutazione finora
- Tema Del Primer SeminarioDocumento21 pagineTema Del Primer SeminarioMadheleyn del Carmen Alvarez ArmasNessuna valutazione finora
- CatalisisDocumento19 pagineCatalisisEduardo OcelotlNessuna valutazione finora
- CatálisisDocumento11 pagineCatálisisDiĕgő ŔuĩzNessuna valutazione finora
- CATALIZADORESDocumento7 pagineCATALIZADORESStevens Gonzales RiosNessuna valutazione finora
- Unidad 4 CatalisisDocumento35 pagineUnidad 4 Catalisispoli040590Nessuna valutazione finora
- Trabajo de Reactores Semi-ContinuosDocumento13 pagineTrabajo de Reactores Semi-ContinuosHenny VargasNessuna valutazione finora
- Catalisis Soto Calixto Tello Barrera.0Documento16 pagineCatalisis Soto Calixto Tello Barrera.0Kevin Jholsin Soto CalixtoNessuna valutazione finora
- Tarea 4-Jorge PaduaDocumento6 pagineTarea 4-Jorge PaduaBig PoppaNessuna valutazione finora
- Qui MicaDocumento23 pagineQui MicaDanerNessuna valutazione finora
- Tarea 4-Jorge PaduaDocumento7 pagineTarea 4-Jorge PaduaBig PoppaNessuna valutazione finora
- Resumen Del Capitulo 10 de Fogler.Documento40 pagineResumen Del Capitulo 10 de Fogler.Ambar Fajardo100% (5)
- Catalizador o CatálisisDocumento6 pagineCatalizador o CatálisisMarxx Aponte EscalanteNessuna valutazione finora
- Practica 10 Cinetica Química de Una RX CatalizadaDocumento49 paginePractica 10 Cinetica Química de Una RX CatalizadaDanny GarcíaNessuna valutazione finora
- Taller 1Documento3 pagineTaller 1daniel ruizNessuna valutazione finora
- Cinetica QuimicaDocumento12 pagineCinetica QuimicaHedi Osca Miranda ipda PotosíNessuna valutazione finora
- Unidad 2 QUIMICADocumento50 pagineUnidad 2 QUIMICAMargoth PesantezNessuna valutazione finora
- Informe #4 Determinacion de PHDocumento5 pagineInforme #4 Determinacion de PHMargoth PesantezNessuna valutazione finora
- Informe #3 Tipos de Reacciones QuimicasDocumento5 pagineInforme #3 Tipos de Reacciones QuimicasMargoth PesantezNessuna valutazione finora
- Cuadro ComparativoDocumento2 pagineCuadro ComparativoMargoth PesantezNessuna valutazione finora
- Cuadro ComparativoDocumento2 pagineCuadro ComparativoMargoth PesantezNessuna valutazione finora
- Aplicaciones de Las Propiedades ColigativasDocumento5 pagineAplicaciones de Las Propiedades ColigativasMargoth PesantezNessuna valutazione finora
- Oficio Modelo para Solicitud de Parqueo de Estudiantes 2019Documento1 paginaOficio Modelo para Solicitud de Parqueo de Estudiantes 2019Margoth PesantezNessuna valutazione finora
- Geometria MolecularDocumento2 pagineGeometria MolecularMargoth PesantezNessuna valutazione finora
- Oxidacion de AminasDocumento5 pagineOxidacion de AminasEudoro TrejosNessuna valutazione finora
- Informe 4Documento7 pagineInforme 4Katherine Nevado ManriqueNessuna valutazione finora
- Práctica 2 Fisicoquímica FarmacéuticaDocumento6 paginePráctica 2 Fisicoquímica Farmacéuticaraul rojasNessuna valutazione finora
- Cinética QuímicaDocumento153 pagineCinética QuímicaGerman Van der OlguinNessuna valutazione finora
- EJERCICIOS DE CINÉTICA (Kiwi)Documento14 pagineEJERCICIOS DE CINÉTICA (Kiwi)Kelly RestrepoNessuna valutazione finora
- Tema 3 - Reacciones Redox-PLATAFORMA PDFDocumento39 pagineTema 3 - Reacciones Redox-PLATAFORMA PDFRakel Martinez AlonsoNessuna valutazione finora
- PEC-2 - 2021-2022 - Soluciones QO1Documento12 paginePEC-2 - 2021-2022 - Soluciones QO1chiralicNessuna valutazione finora
- Adición Oxidante y Eliminación ReductoraDocumento11 pagineAdición Oxidante y Eliminación ReductoraAna Gil QuirogaNessuna valutazione finora
- Importancia de Las EnzimasDocumento8 pagineImportancia de Las EnzimasInvierte tu TiempoNessuna valutazione finora
- 4° BIOLOGÍA PRUEBA Enzimas 2020Documento2 pagine4° BIOLOGÍA PRUEBA Enzimas 2020Danniel AlexisNessuna valutazione finora
- Practica N°7 Lili LpezDocumento9 paginePractica N°7 Lili LpezLili LopezNessuna valutazione finora
- LIQ IV Reporte 1Documento15 pagineLIQ IV Reporte 1Lily Roosevelt AyalaNessuna valutazione finora
- Ejercicios Recuperación Reacciones 2Documento6 pagineEjercicios Recuperación Reacciones 2Will CabasNessuna valutazione finora
- Sustitución Nucleofílica AcílicaDocumento2 pagineSustitución Nucleofílica AcílicaAna E. Hernández Cruz100% (1)
- Apuntes Tema3-Mecanismos de ReaccionDocumento43 pagineApuntes Tema3-Mecanismos de ReaccionCecilio GutierrezNessuna valutazione finora
- UNIDAD 5 Cinética QuímicaDocumento11 pagineUNIDAD 5 Cinética QuímicaSasha OlivaresNessuna valutazione finora
- Cinética Enzimática BBM 2018Documento45 pagineCinética Enzimática BBM 2018Karen CuencaNessuna valutazione finora
- Velocidad de Uvna ReacciónDocumento5 pagineVelocidad de Uvna ReacciónSophiaAltamiranoCarranza100% (1)
- Copia de ENZIMASDocumento5 pagineCopia de ENZIMASRafaella Ignacia Cortes ColomboNessuna valutazione finora
- 05-3 Inhibicion EnzimaticaDocumento22 pagine05-3 Inhibicion Enzimaticabrenda lopez linaresNessuna valutazione finora
- Repaso San Marcos Semana 04 - QuímicaDocumento7 pagineRepaso San Marcos Semana 04 - QuímicaSILVIA ROSARIO CHALCO MENDOZA0% (1)
- Resumen Catalizadores en La Industria Quimica.Documento6 pagineResumen Catalizadores en La Industria Quimica.Brayan Castañeda LopezNessuna valutazione finora
- Velocidad de ReacciónDocumento30 pagineVelocidad de ReacciónRicardo Bermeo MolinaNessuna valutazione finora
- Cinética Quimica y CatálisisDocumento106 pagineCinética Quimica y CatálisisErica SaniNessuna valutazione finora
- Solucion Del Ejercicio de Ractor Catalitico de Lecho FijoDocumento7 pagineSolucion Del Ejercicio de Ractor Catalitico de Lecho FijoKatia Gutierrez Gala100% (1)
- Tema: Estequiometría - : Problema: Al Calentar 245 G de Clorato de Potasio. Qué Peso de ODocumento4 pagineTema: Estequiometría - : Problema: Al Calentar 245 G de Clorato de Potasio. Qué Peso de OJOHAN ESTEBAN REMOLINA MORANessuna valutazione finora
- Capitulo 14 CineticaDocumento66 pagineCapitulo 14 CineticaFailmerNessuna valutazione finora
- Efectos de La TemperaturaDocumento11 pagineEfectos de La TemperaturaSinaí VictoriaNessuna valutazione finora
- REACCIONES QUIMICAS IpnDocumento14 pagineREACCIONES QUIMICAS IpnAraceli GarcíaNessuna valutazione finora
- Diseño de Reactores 1 (Solucionario)Documento6 pagineDiseño de Reactores 1 (Solucionario)Victor J. OreNessuna valutazione finora