Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Tema 10. Química Orgánica 2000-2009 (Extra)
Caricato da
joseluTitolo originale
Copyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Tema 10. Química Orgánica 2000-2009 (Extra)
Caricato da
joseluCopyright:
Formati disponibili
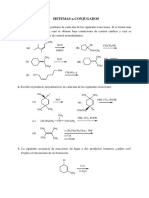
Complete y ajuste las siguientes reacciones orgánicas:
a) CH 3 CH 2 COOH CH 3 CH 2 OH
b) CH 3 CH CH 2 H 2
c) C4 H10 O2
QUÍMICA. 2000. JUNIO. EJERCICIO 4. OPCIÓN B
R E S O L U C I Ó N
a) CH3CH 2COOH CH3CH 2OH CH3CH 2COOCH 2CH3 H 2O
b) CH3CH CH 2 H 2 CH3CH 2CH3
13
c) C4 H10 O 2 4 CO 2 5 H 2O
2
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 1
Complete las siguientes reacciones e indique el tipo de reacción (adición, eliminación o
sustitución) a que corresponden.
a) CH 3CH CH 2 H 2O
b) C6 H6 (benceno) HNO3
H2SO4
c) CH3CHBrCH3
KOH
HBr
QUÍMICA. 2000. RESERVA 2. EJERCICIO 4. OPCIÓN B
R E S O L U C I Ó N
a) CH3CH CH 2 H 2O CH3CHOHCH3 (Adición)
b) C6H6 HNO3
H2SO4
C6H5 NO2 H2O (Sustitución)
c) CH3CHBrCH3
KOH
HBr CH3CH CH2 (Eliminación)
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 2
Complete las siguientes reacciones y ajuste la de combustión:
a) CH 3CH 3 Cl 2
Luz
b) C3 H8 O2
Calor
c) CH 3CH 2OH
H2SO4 ;Calor
QUÍMICA. 2000. RESERVA 3. EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
a) CH3CH3 Cl2
Luz
CH3CH2Cl HCl
b) C3H8 5O2
Calor
3CO2 4H2O
c) CH3CH2OH
H2SO4 ;Calor
CH2 CH2 H2O
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 3
Dados los siguientes compuestos orgánicos: CH 3CH 2CH 3 ; CH 3OH; CH 2 CHCH 3 . Indique
razonadamente:
a) ¿Cuál es soluble en agua?.
b) ¿Cuáles son hidrocarburos?.
c) ¿Cuál presenta reacciones de adición?.
QUÍMICA. 2000. SEPTIEMBRE. EJERCICIO 4. OPCIÓN B
R E S O L U C I Ó N
a) Metanol, ya que es una molécula polar con lo cual es soluble en agua.
b) Propano y propeno, ya que están formados por carbono e hidrógeno.
c) Propeno, ya que tiene un doble enlace.
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 4
Indique el tipo de hibridación que presenta cada uno de los átomos de carbono en las siguientes
moléculas: a) CH 3C CCH 3 ; b) CH 3CH CHCH 3 ; c) CH 3CH 2CH 2CH 3
QUÍMICA. 2001. RESERVA 1. EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
a) sp3,sp,sp, sp3;
b) sp3,sp2,sp2, sp3;
c) sp3,sp3,sp3, sp3
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 5
Complete las siguientes reacciones e indique el tipo al que pertenecen:
a) CH CH HCl
b) BrCH2 CH2Br KOH/ Etanol
2KBr
h
c) CH3CH2CH3 Cl 2 HCl
QUÍMICA. 2001. RESERVA 2. EJERCICIO 4. OPCIÓN B
R E S O L U C I Ó N
a) CH CH HCl CH 2 CHCl (Adición)
b) BrCH2 CH2Br
KOH/ Etanol
2KBr OHCH2 CH2OH (Sustitución)
h
c) CH3CH2CH3 Cl2 HCl CH3CH2CH2Cl (Sustitución)
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 6
Dadas las moléculas CH 4 , C2 H 2 , C2 H 4 , razone si las siguientes afirmaciones son verdaderas o
falsas: a) En la molécula C2 H 4 los dos átomos de carbono presentan hibridación sp 3 . b) El
átomo de carbono de la molécula CH 4 posee hibridación sp 3 . c) La molécula de C2 H 2 es
lineal.
QUÍMICA. 2001. RESERVA 3. EJERCICIO 2. OPCIÓN A
R E S O L U C I Ó N
a) Falsa. En el C 2 H 4 hay un doble enlace y los carbonos tienen hibridación sp 2
b) Cierta.
c) Cierta.
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 7
Complete las siguientes reacciones e indique de qué tipo son:
a) CH 3CH CH 2 HBr
h
b) CH 3CH 2CH 3 Cl 2
c) CH CH H2
Pt / Pd
QUÍMICA. 2001. RESERVA 3. EJERCICIO 4. OPCIÓN B
R E S O L U C I Ó N
a) CH3CH CH 2 HBr CH3CHBrCH3 (Adición electrófila)
h
b) CH3CH2CH3 Cl2 HCl CH3CH2CH2Cl (Sustitución)
c) CH CH H2
Pt / Pd
CH2 CH2 (Adición electrófila)
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 8
Las fórmulas moleculares de tres hidrocarburos lineales son: C3 H 6 , C4 H10 y C5 H12 . Razone si
son verdaderas o falsas las siguientes afirmaciones: a) Los tres pertenecen a la misma serie
homóloga. b) Los tres presentan reacciones de adición. c) Los tres poseen átomos de carbono
con hibridación sp 3 .
QUÍMICA. 2001. RESERVA 4. EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
a) Falsa. Ya que el C3H 6 es un alqueno y el C 4 H10 y C5 H12 son alcanos.
b) Falsa. Ya que el C 4 H10 y C5 H12 son alcanos y no dan reacciones de adición.
c) Cierta. Ya que los tres tienen carbonos con simples enlaces.
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 9
Complete las siguientes reacciones y ajuste la que corresponda a una combustión:
a) CH 3 CH CHCH 3 H 2
b) CH 3 CH 3 O2
h
c) CH4 Cl 2
QUÍMICA. 2002. JUNIO. EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
a) CH 3CH CHCH 3 H 2 CH 3CH 2 CH 2 CH 3
7
b) CH 3 CH 3 O 2 2 CO 2 3 H 2 O
2
h
c) CH 4 Cl 2 CH 3 Cl HCl
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 10
Los compuestos CH 3 CH 2 OH y CH 3 CH 2 CH 3 tienen masas moleculares similares. Indique,
justificando la respuesta:
a) Cuál tiene mayor punto de fusión.
b) Cuál de ellos puede experimentar una reacción de eliminación y escríbala.
QUÍMICA. 2002. RESERVA 1. EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
a) El etanol, porque posee enlaces de hidrógeno entre sus moléculas.
b) El etanol, puede deshidratarse, eliminando agua de su molécula para producir un alqueno: eteno.
H SO / H
CH3 CH 2 OH
2 4
CH 2 CH 2 H 2O
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 11
Dados los compuestos: 2-butanol, CH 3 CHOHCH 2 CH 3 , y 3-metilbutanol,
CH 3 CH(CH 3 )CH 2 CH 2 OH , responda, razonadamente, a las siguientes cuestiones:
a) ¿Son isómeros entre sí?
b) ¿Presenta alguno de ellos isomería óptica?
QUÍMICA. 2002. RESERVA 3. EJERCICIO 4. OPCIÓN B
R E S O L U C I Ó N
a) No, porque no tienen el mismo número de átomo de cada elemento. La fórmula molecular del 2-
butanol es C 4 H 10 O y la del 3 metil-1-butanol es C 5 H 12 O .
b) Sí, el 2-butanol , porque su segundo carbono es asimétrico. En el plano se pueden representar sus
enantiómeros de la forma:
H H
| |
CH 3 C CH 2 CH 3 CH 3 CH 2 C CH 3
y
| |
OH OH
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 12
a) Defina serie homóloga.
b) Escriba la fórmula de un compuesto que pertenezca a la misma serie homóloga de cada uno
de los que aparecen a continuación: CH 3 CH 3 ; CH 3 CH 2 CH 2 OH ; CH 3 CH 2 NH 2 .
QUÍMICA. 2002. RESERVA 4. EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
a) Serie homóloga es un conjunto de compuestos que, teniendo el mismo grupo funcional, cada uno
de ellos se diferencia del anterior en que posee un carbono más en la cadena carbonada.
b) Sólo hay que alargar la cadena carbonada en algún carbono:
Propano: CH 3 CH 2 CH 3
1-Butanol: CH 3CH 2 CH 2 CH 2 OH
Propilamina: CH 3 CH 2 CH 2 NH 2
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 13
Ponga un ejemplo de los siguientes tipos de reacciones:
a) Reacción de adición a un alqueno.
b) Reacción de sustitución en un alcano.
c) Reacción de eliminación de HCl en un cloruro de alquilo.
QUÍMICA. 2002. SEPTIEMBRE. EJERCICIO 4. OPCIÓN B
R E S O L U C I Ó N
a) CH 3CH CHCH 3 H 2 (Pt) CH 3CH 2 CH 2 CH 3
h
b) CH 4 Cl 2 CH 3 Cl HCl
c) CH 3CH 2 CH 2 CH 2 Cl KOH CH 3CH 2 CH CH 2 KCl H 2 O
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 14
Defina los siguientes conceptos y ponga un ejemplo de cada uno de ellos:
a) Serie homóloga.
b) Isomería de cadena.
c) Isomería geométrica.
QUÍMICA. 2003. JUNIO. EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
a) La que está constituida por un grupo de compuestos con la misma función y en la que cada
elemento se diferencia de otro en la longitud de la cadena carbonada.
b) La que presentan dos compuestos que sólo se diferencian en la cadena carbonada. Por ejemplo:
Butano: CH 3CH 2CH 2CH 3
Metilpropano CH 3CH(CH 3 )CH 3
c) La que pueden presentar algunos compuestos con doble enlace según tengan sustituyentes iguales
o no a un lado del plano nodal del doble enlace. Por ejemplo:
CH3 Cl
C=C
Cl CH3
Trans-2,3-diclorobut-2-eno
CH3 CH3
C=C
Cl Cl
Cis-2,3-diclorobut-2-eno
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 15
Complete las siguientes reacciones orgánicas e indique de qué tipo son:
a) CH3CH2CH2OH H2SO4 ,calor
H 2O
b) CH 3CH 2CH CH 2 HI
c) C6 H6 (benceno) HNO3
H2SO4
H 2O
QUÍMICA. 2003. RESERVA 1. EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
a) CH3CH2CH2OH
H2SO4 ,calor
CH3 CH CH 2 H 2O . (Eliminación)
b) CH3CH2CH CH2 HI CH 3CH 2CHICH 3 . (Adición electrófila)
c) C6 H6 (benceno) HNO3
H2SO4
C 6 H 5 NO 2 H2O . (Sustitución electrófila)
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 16
Explique uno de los tipos de isomería que pueden presentar los siguientes compuestos y
represente los correspondientes isómeros:
a) CH 3COCH 3
b) CH 3CH 2CH 2CH 3
c) CH 3CHFCOOH
QUÍMICA. 2003. RESERVA 2. EJERCICIO 4. OPCIÓN B
R E S O L U C I Ó N
a) Por ejemplo, de función: propanal. CH3CHO .
b) Por ejemplo, de cadena: metilpropano. CH3CH(CH3 )CH3
c) Por ejemplo, de posición: ácido 3-flúorpropanoico. CH2FCH 2COOH
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 17
Complete las siguientes reacciones orgánicas e indique de qué tipo son:
a) CH2 CH2 H2 Catalizador
b) CH3CH3 Cl 2
Luz
HCl
c) CH 3OH O2
QUÍMICA. 2003. RESERVA 3. EJERCICIO 4. OPCIÓN B
R E S O L U C I Ó N
a) CH 2 CH2 H2
Catalizador
CH 3CH 3 (Adición)
b) CH3CH3 Cl2
Luz
CH 3CH 2Cl HCl (Sustitución radicálica)
3
c) CH 3OH O 2 CO 2 2 H 2O (Combustión)
2
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 18
Dados los siguientes compuestos: CH 3COOCH 2CH 3 , CH 3CONH 2 , CH 3CHOHCH 3 y
CH 3CHOHCOOH
a) Identifique los grupos funcionales presentes en cada uno de ellos.
b) ¿Alguno posee átomos de carbono asimétrico? Razone su respuesta.
QUÍMICA. 2003. SEPTIEMBRE. EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
a)
CH3COOCH2 CH3 (Éster, acetato de etilo)
CH3CONH 2 (Amida, acetamida)
CH3CHOHCH3 (Alcohol, 2-propanol)
CH3CHOHCOOH (Alcohol y ácido, ácido 2-hidroxipropanoico)
b) En el carbono central del CH3CHOHCOOH hay unidos cuatro sustituyentes distintos (CH3-,
OH-, H- y COOH-) , luego éste será asimétrico.
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 19
Defina los siguientes conceptos y ponga un ejemplo de cada uno de ellos:
a) Isomería de función.
b) Isomería de posición.
c) Isomería óptica.
QUÍMICA. 2004. JUNIO. EJERCICIO 4. OPCIÓN B
R E S O L U C I Ó N
a) Dos compuestos son isómeros de función cuando, teniendo la misma fórmula molecular, presenta
cada uno una función distinta. Por ejemplo: etanol y dimetiléter.
b) Dos compuestos son isómeros de posición cuando, teniendo la misma fórmula molecular,
presenta cada uno un grupo característico en distinto carbono de l cadena carbonada. Por ejemplo:
1-butanol y 2-butanol.
c) Es aquella que presentan las sustancias que tienen al menos un carbono asimétrico, dando lugar a
dos isómeros ópticos (enantiómeros) que se diferencian en la distribución espacial de los cuatro
sustituyentes del carbono asimétrico. Por ejemplo, el ácido 2-hidroxipropanoico.
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 20
Complete las siguientes reacciones orgánicas e indique de qué tipo son:
a) CH4 Cl 2
Luz
b) CH2 CHCH3 H2
Catalizador
c) CH3 CH2 CH2 Br
KOH
EtOH
QUÍMICA. 2004. RESERVA 1. EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
a) CH4 Cl2
Luz
CH 3 Cl HCl (Sustitución radicálica)
b) CH2 CHCH3 H2
Catalizador
CH 3CH 2 CH 3 (Adicción electrófila)
c) CH3 CH2 CH2 Br
KOH
EtOH
CH 3 CH CH 2 KBr H 2 O (Eliminación)
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 21
Las fórmulas moleculares de tres hidrocarburos lineales son: C2 H 4 ; C3 H 8 y C4 H10 . Razone si
son verdaderas o falsas las siguientes afirmaciones:
a) Los tres pertenecen a la misma serie homóloga.
b) Los tres experimentan reacciones de sustitución.
c) Sólo uno de ellos tiene átomos de carbono con hibridación sp 2 .
QUÍMICA. 2004. RESERVA 2. EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
a) Falso. El primero es un alqueno (eteno) y el segundo y tercero son alcanos (propano y butano o
metilpropano).
b) Falso. Sólo los alcanos experimentan sustituciones por vía radicálica.
c) Cierto. La presenta el alqueno en los carbonos que forman el doble enlace.
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 22
Complete las siguientes reacciones e indique de qué tipo son:
a) CH 2 CH 2 Br2
b) CH 3 CH 3 O2
c) C6 H6 (benceno) Cl 2
AlCl 3
QUÍMICA. 2004. RESERVA 3. EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
a) CH2 CH2 Br2 CH 2 Br CH 2 Br (Adición electrófila)
7
b) CH 3CH 3 O 2 2 CO 2 3H 2O (Combustión)
2
c) C6 H6 (benceno) Cl2
AlCl3
C 6 H 5Cl HCl (Sustitución electrófila)
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 23
Dados los compuestos orgánicos: CH 3CH 3 ; CH 3OH y CH 2 CHCH 3 .
a) Explique la solubilidad en agua de cada uno de ellos.
b) Indique cuáles son hidrocarburos.
c) ¿Puede experimentar alguno de ellos reacciones de adición? En tal caso, escriba una.
QUÍMICA. 2004. SEPTIEMBRE. EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
a) Debido a la polaridad de la molécula de alcohol, (la molécula de metanol es tetraédrica con el
grupo hidroxilo en uno de los vértices y al ser el oxígeno tan electronegativo, crea un
desplazamiento electrónico en la misma dirigido hacia el átomo de oxígeno). Sólo el metanol será
soluble en agua.
b) El primero es un alcano (etano) y el tercero un alqueno (propeno).
c) El alqueno por poseer doble enlace. Por ejemplo:
CH2 CHCH3 H 2O CH 3CHOHCH 3
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 24
a) Escriba las estructuras de los isómeros de posición del n-pentanol (C5 H11OH) .
b) Represente tres isómeros de fórmula molecular C8 H18 .
QUÍMICA. 2005. JUNIO. EJERCICIO 4. OPCIÓN B
R E S O L U C I Ó N
a)
CH 3CH 2CH 2CH 2CH 2OH pentan-1-ol
CH 3CH 2CH 2CHOHCH 3 pentan-2-ol
CH 3CH 2CHOHCH 2CH 3 pentan-3-ol
b)
CH 3CH 2CH 2CH 2CH 2CH 2CH 2CH 3 octano
CH 3CH 2CH 2CH 2CH 2CH(CH 3 )CH 3 2 – metilheptano
CH 3CH 2CH 2CH 2CH(CH 3 )CH 2CH 3 3 – metilheptano
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 25
Complete las siguientes reacciones:
a) CH 3CH CH 2 HBr
b) CH 3CH 2CH 3 Cl 2
Luz
c) CH 3CH 2CH CH 2 H 2O
QUIMICA. 2005. RESERVA 2 EJERCICIO 4 OPCIÓN A
R E S O L U C I Ó N
a) CH3CH CH 2 HBr CH3CHBrCH3
h
b) CH3CH2CH3 Cl2 HCl CH3CH2CH2Cl
c) CH 3CH 2CH CH2 H2O CH3CH 2CHOHCH 3
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 26
Para el eteno (CH 2 CH 2 ) indique: a) La geometría de la molécula. b) La hibridación que
presentan los orbitales de los átomos de carbono. c) Escriba la reacción de combustión ajustada
de este compuesto.
QUIMICA. 2005. RESERVA 2 EJERCICIO 3 OPCIÓN B
R E S O L U C I Ó N
a) Triangular plana con ángulos de 120º.
b) Los átomos de carbono tienen hibridación sp 2 .
c) CH2 CH2 3O 2 2CO2 2H2O
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 27
Considere las siguientes moléculas:
CH 3CHOHCH 3 ; CH 3COCH 3 ; CH 3CONH 2 ; CH 3COOCH 3
a) Identifique sus grupos funcionales.
b) ¿Cuál de estos compuestos daría propeno mediante una reacción de eliminación?. Escriba la
reacción.
QUIMICA. 2005. RESERVA 3 EJERCICIO 4 OPCIÓN A
R E S O L U C I Ó N
a) CH 3CHOHCH 3 . Grupo alcohol.
CH 3COCH 3 . Grupo cetona.
CH 3CONH 2 . Grupo amida.
CH 3COOCH 3 . Grupo ester.
b) CH3CHOHCH3
H2SO4 ,calor
CH3 CH CH 2 H2O . (Eliminación)
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 28
Complete las siguientes reacciones y ajuste la de combustión:
a) CH 3CH 2CH 3 O 2
b) CH 3C CH HCl
c) CH 2 CHCH 3 H 2O
QUIMICA. 2005. RESERVA 4 EJERCICIO 4 OPCIÓN A
R E S O L U C I Ó N
a) CH 3CH 2CH 3 5O 2 3CO 2 4H 2O
b) CH 3C CH HCl CH 3CCl CH 2
c) CH 2 CHCH 3 H 2O CH 3CHOHCH 3
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 29
a) Defina carbono asimétrico.
b) Señale el carbono asimétrico, si lo hubiere, en los siguientes compuestos:
CH 3CHOHCOOH ,CH 3CH 2 NH 2 ,CH 2 CClCH 2CH 3 ,CH 3CHBrCH 2CH 3
QUÍMICA. 2005. SEPTIEMBRE. EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
a) Carbono asimétrico es aquel átomo de carbono que está unidos a 4 sustituyentes distintos.
b) Tienen carbonos asimétricos el CH3C*HOHCOOH y el CH3C*HBrCH2CH3
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 30
Utilizando un alqueno como reactivo, escriba:
a) La reacción de adición de HBr .
b) La reacción de combustión ajustada.
c) La reacción que produzca el correspondiente alcano.
QUÍMICA. 2006. JUNIO. EJERCICIO 4. OPCIÓN B
R E S O L U C I Ó N
a) CH3CH CH 2 HBr CH3CHBrCH3
9
b) CH3CH CH 2 O 2 3CO 2 3H 2O
2
c) CH3CH CH2 H 2 CH3CH2CH3
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 31
Razone las siguientes cuestiones:
a) ¿Puede adicionar halógenos un alcano?
b) ¿Pueden experimentar reacciones de adición de haluros de hidrógeno los alquenos?
c) ¿Cuáles serían los posibles derivados diclorados del benceno?
QUÍMICA. 2006. RESERVA 1. EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
a) Falso. Los alcanos no dan reacciones de adición.
b) Cierto. Por ejemplo: CH3 CH CH 2 HBr CH3 CHBr CH3
Regla de Markonikow: cuando un haluro de hidrógeno se adiciona a un alqueno asimétrico,
el hidrógeno entra en el carbono con mayor número de hidrógenos de los dos carbonos que portan
el doble enlace, y el halógeno entra en el otro.
c) El orto, meta y para diclorobenceno.
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 32
Señale el tipo de isomería existente entre los compuestos de cada uno de los apartados
siguientes:
a) CH 3CH 2CH 2OH y CH 3CHOHCH 3 .
b) CH 3CH 2OH y CH 3OCH 3 .
c) CH 3CH 2CH 2CHO y CH 3CH(CH 3 )CHO .
QUÍMICA. 2006. SEPTIEMBRE. EJERCICIO 4. OPCIÓN B
R E S O L U C I Ó N
a) Isomería de posición.
b) Isomería de función.
c) Isomería de cadena.
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 33
Para los siguientes compuestos: CH 3CH 3 ; CH 2 CH 2 y CH 3CH 2OH .
a) Indique cuál o cuáles son hidrocarburos.
b) Razone cuál será más soluble en agua.
c) Explique cuál sería el compuesto con mayor punto de ebullición.
QUÍMICA. 2007. JUNIO EJERCICIO 4. OPCIÓN B
R E S O L U C I Ó N
a) Los dos primeros, etano y eteno, son hidrocarburos ya que en su composición solamente aparece
carbono e hidrógeno. El tercero (etanol) es un alcohol.
b) El etanol es el más soluble en agua de los tres porque se trata de una molécula polar de forma que
las moléculas de agua (también polares) puede rodear a las moléculas de alcohol apareciendo
interacciones eléctricas entre los polos de ambos tipos de moléculas. Esto no es posible en las otras
dos moléculas que son apolares.
c) El compuesto de mayor punto de ebullición es el etanol ya que, a temperatura ambiente es
líquido, mientras que etano y eteno son gases. Esto es debido a los enlaces de hidrógeno (enlaces
intermoleculares) que se producen entre el átomo de oxígeno de una molécula de alcohol y el átomo
de hidrógeno de otra molécula de etanol. Estos enlaces o uniones entre moléculas hacen que sea
más difícil separarlas para pasar de estado líquido a gas y por tanto se necesitará una temperatura
(de ebullición) mayor.
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 34
Escriba:
a) Un isómero de cadena de CH 3CH 2 CH CH 2 .
b) Un isómero de función de CH 3OCH 2CH 3 .
c) Un isómero de posición de CH 3CH 2 CH 2CH 2COCH 3 .
QUÍMICA. 2007. RESERVA 1. EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
a) CH 3 C(CH 3 ) CH 2
b) CH 3 CH 2 CH 2OH
c) CH 3CH 2 CH 2COCH 2 CH 3
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 35
Indique los productos que se obtienen en cada una de las siguientes reacciones:
a) CH 3CH CH 2 Cl 2
b) CH 3CH CH 2 HCl
c) CH 3CH CH 2 O 2
QUÍMICA. 2007. RESERVA 2. EJERCICIO 4. OPCIÓN B
R E S O L U C I Ó N
a) CH 3CH CH 2 Cl 2 CH 3CHClCH 2Cl
b) Aplicamos la regla de Markovnikov
CH 3CH CH 2 HCl CH 3CHClCH 3
9
c) CH 3CH CH 2 O 2 3 CO 2 3H 2O
2
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 36
Escriba:
a) Dos hidrocarburos saturados que sean isómeros de cadena entre sí.
b) Dos alcoholes que sean entre sí isómeros de posición.
c) Un aldehído que muestre isomería óptica.
QUÍMICA. 2007. RESERVA 3. EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
a) Butano: CH 3CH 2CH 2CH 3 y metil propano: CH 3CH(CH 3 )CH 3
b) Propan-1-ol: CH 3CH 2CH 2OH y propan-2-ol: CH 3CHOHCH 3
c) 2-metilbutanal: CH 3CH 2CH(CH 3 )CHO
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 37
Complete las siguientes reacciones químicas:
a) CH 3CH 3 O 2
b) CH 3CHOHCH 3
KOH
etanol
c) CH CH 2 Br 2
QUÍMICA. 2007. RESERVA 4. EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
7
a) CH 3CH 3 O 2 2 CO 2 3H 2O
2
b) CH 3CHOHCH 3
KOH
e tan ol
CH 3CH CH 2 H 2O
c) CH CH 2Br2 CHBr2CHBr2
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 38
Indique el compuesto orgánico que se obtiene en las siguientes reacciones químicas:
a) CH 2 CH 2 Br2
b) C6 H6 (benceno) Cl 2
Catalizador
c) CH3CHClCH3 KOH
e tan ol
QUÍMICA. 2008. JUNIO EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
a) CH2 CH2 Br2 CH 2 Br CH 2 Br (Adición electrófila)
b) C6 H6 (benceno) Cl2
Catalizador
C 6 H 5 Cl HCl (Sustitución electrófila)
c) CH3 CHClCH3
KOH
e tan ol
CH 3 CH CH 2 HCl (Reacción de eliminación).
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 39
Dados los compuestos: (CH 3 ) 2 CHCOOCH 3 ; CH 3OCH 3 ; CH 2 CHCHO
a) Identifique y nombre la función que presenta cada uno.
b) Razone si presentan isomería cis-trans.
c) Justifique si presentan isomería óptica.
QUÍMICA. 2008. RESERVA 1 EJERCICIO 4 OPCIÓN B
R E S O L U C I Ó N
a) El primero es un éster (metilpropanato de metilo); el segundo es un éter (dimetiléter); el tercero
es un aldehido(propenal).
b) Ninguno tiene isomería cis-trans. El único que podría presentarla es el propenal por tener un
doble enlace, pero uno de los carbonos que lleva el doble enlace tiene los mismos sustituyente.
c) No, ya que ninguno tiene un carbono asimétrico.
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 40
Para el compuesto CH 3CH CHCH 3 escriba:
a) La reacción con HBr .
b) La reacción de combustión.
c) Una reacción que produzca CH 3CH 2CH 2CH 3
QUÍMICA. 2008. RESERVA 2 EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
a) CH 3CH CHCH 3 HBr CH 3CHBr CH 2CH 3
b) CH 3CH CHCH 3 6O 2 4CO 2 4H 2O
c) CH 3CH CHCH 3 H 2 (Pt) CH 3CH 2CH 2CH 3
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 41
Para cada compuesto, formule:
a) Los isómeros cis-trans de CH 3CH 2CH CHCH 3
b) Un isómero de función de CH 3OCH 2CH 3
c) Un isómero de posición del derivado bencénico C 6 H 4Cl 2
QUÍMICA. 2008. RESERVA 4. EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
a)
CH 3 CH 2 CH 3 CH 3 CH 2 H
CC CC
H H H CH 3
Cis penten-2-eno Trans penten-2-eno
b) Un isómero de un éter saturado puede ser un alcohol saturado, por ejemplo, cualquier propanol :
CH 3 CH 2 CH 2OH
c) Cualquiera de los tres posibles que se obtiene cambiando de posición los cloros en el anillo
bencénico.
Cl Cl Cl
Cl
Cl
Cl
1,2 dicloro benceno 1,3 dicloro benceno 1,4 dicloro benceno
u ó ó
orto diclorobenceno meta diclorobenceno para diclorobenceno
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 42
Indique el producto que se obtiene en cada una de las siguientes reacciones:
a) CH3CH CH2 Cl 2
b) CH 3CH CH 2 HCl
c) C 6 H 6 (benceno) HNO 3
2 4 H SO
QUÍMICA. 2008. SEPTIEMBRE. EJERCICIO 4. OPCIÓN B
R E S O L U C I Ó N
Las dos primeras son reacciones de adición electrófila al doble enlace y, sólo, se diferencian en que
en la primera reacción sólo se obtiene un producto, el 1,1-dicloropropano y en la segunda se pueden
obtener dos: el 1-cloropropano o el 2-cloropropano. Mayoritariamente, según la regla de
Markovnikov, se obtiene el segundo ya que el hidrógeno se une al carbono menos sustituido.
a) CH3CH CH2 Cl 2 CH 3CHClCH 2Cl .
b) CH3CH CH2 HCl CH 3CHClCH 3
c) C 6 H 6 (benceno) HNO 3 C 6 H 5 NO 2 H 2 O Isomería de cadena.
2 4H SO
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 43
Dados los compuestos CH 3OH,CH 3CH CH 2 y CH 3CH CHCH 3 , indique razonadamente:
a) Los que puedan presentar enlace de hidrógeno.
b) Los que puedan experimentar reacciones de adición.
c) Los que puedan presentar isomería geométrica.
QUÍMICA. 2009. JUNIO. EJERCICIO 4. OPCIÓN B
R E S O L U C I Ó N
El que puede presentar enlaces de hidrógeno es el metanol CH 3OH porque contiene un átomo muy
pequeño y electronegativo (el oxígeno) unido a un átomo de hidrógeno. Por tanto, se pueden
producir enlaces de hidrógeno entre el átomo de hidrógeno de una molécula el átomo de oxígeno de
otra molécula próxima.
b) Pueden dar reacciones de adición los alquenos y alquinos. Por tanto, el propeno CH 3CH CH 2
y el but-2-eno CH 3CH CHCH 3 pueden dar este tipo de reacción en el que el enlace doble
desaparece y se añaden a la molécula un par de átomos que pasan a enlazarse con cada uno de los
átomos de carbono que estaban unidos por el enlace doble (que pasa a ser enlace sencillo).
c) Las moléculas que pueden presentar isomería geométrica son las que presentan un enlace doble
en el que los carbonos presentan diferentes sustituyentes. En este caso se trata del but-2-eno ya que,
según la disposición espacial de los sustituyentes en los carbonos del doble enlace podemos
encontrarnos dos isómeros diferentes, el cis but-2-eno y el trans but-2-eno. Este tipo de isomería no
es posible en los otros dos compuestos.
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 44
Indique los compuestos principales que se obtienen cuando el propeno reacciona con:
a) Agua en presencia de ácido sulfúrico
b) Cloro
c) Cloruro de hidrógeno
Escriba las reacciones correspondientes
QUÍMICA. 2009. RESERVA 1. EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
a) CH 2 CH CH 3 H 2 O CH 3 CHOH CH 3
H SO
2 4
b) CH 2 CH CH 3 Cl 2 CH 2Cl CHCl CH 3
c) CH 2 CH CH 3 HCl CH 3 CHCl CH 3
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 45
a) Complete la reacción: 1mol CH CH 1mol Cl 2
b) Escriba la fórmula desarrollada de los isómeros que se forman.
c) ¿Qué tipo de isomería presentan estos compuestos?
QUÍMICA. 2009. RESERVA 3. EJERCICIO 4. OPCIÓN B
R E S O L U C I Ó N
a) 1mol CH CH 1mol Cl 2 CHCl CHCl
b)
c) Isomería cis-trans o geométrica
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 46
Complete las siguientes reacciones e indique el tipo al que pertenecen:
a) CH 3CH 3 O 2
b) CH 3CH 2OH
2 H SO
4
calor
c) C 6 H 6 (benceno) HNO 3
2 H SO
4
QUÍMICA. 2009. RESERVA 4. EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
7
a) CH 3CH 3 O 2 2 CO 2 3H 2O Combustión
2
b) CH 3CH 2OH CH 2 CH 2 H 2O
2 H SO
4
calor
Eliminación
c) C 6 H 6 (benceno) HNO 3 C 6 H 5 NO 2 H 2 O
2H SO
4
Sustitución.
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 47
Dado 1 mol de HC C CH 2 CH 3 escriba el producto principal que se obtiene en la reacción
con:
a) Un mol de H 2
b) Dos moles de Br 2
c) Un mol de HCl
QUÍMICA. 2009. SEPTIEMBRE. EJERCICIO 4. OPCIÓN A
R E S O L U C I Ó N
a) HC C CH 2 CH 3 H 2 CH 2 CH CH 2 CH 3
b) HC C CH 2 CH 3 2Br2 CHBr2 CBr2 CH 2 CH 3
c) HC C CH 2 CH 3 HCl CH 2 CCl CH 2 CH 3
TEMA 10. QUÍMICA ORGÁNICA 2000-2009 48
Potrebbero piacerti anche
- Quim T9 2005Documento7 pagineQuim T9 2005Carolina De la peña FernándezNessuna valutazione finora
- Quim T9 2021Documento7 pagineQuim T9 2021JURONessuna valutazione finora
- Quim T9 2008Documento6 pagineQuim T9 2008Ariana AndresNessuna valutazione finora
- Quim T9 2022Documento7 pagineQuim T9 2022Carolina De la peña FernándezNessuna valutazione finora
- Quim T9 2008Documento6 pagineQuim T9 2008JURONessuna valutazione finora
- Quim T9 2009Documento6 pagineQuim T9 2009JURONessuna valutazione finora
- Quim T9 2007Documento6 pagineQuim T9 2007JURONessuna valutazione finora
- Quim T9 2014Documento6 pagineQuim T9 2014Francisco IglesiasNessuna valutazione finora
- Quim T9 2020Documento7 pagineQuim T9 2020Carolina De la peña FernándezNessuna valutazione finora
- Ejercicios de Sintesis Organica: ) H (LuzDocumento8 pagineEjercicios de Sintesis Organica: ) H (Luzemily espinoza tamaraNessuna valutazione finora
- Ejercicios de Sintesis OrganicaDocumento10 pagineEjercicios de Sintesis Organicaemily espinoza tamaraNessuna valutazione finora
- Ejercicios de Quimica OrganicaDocumento19 pagineEjercicios de Quimica OrganicaFanny FloresNessuna valutazione finora
- 09 - Ejercicios de Química OrgánicaDocumento6 pagine09 - Ejercicios de Química OrgánicaKarglezNessuna valutazione finora
- Quimica-Organica - Doc IV ElectivoDocumento8 pagineQuimica-Organica - Doc IV ElectivoDiego Ignacio Parra ZentenoNessuna valutazione finora
- Ejercicios PAU de Quimica OrganicaDocumento8 pagineEjercicios PAU de Quimica OrganicaMiguel RuizNessuna valutazione finora
- TEMA 9 Química Orgánica 2000Documento6 pagineTEMA 9 Química Orgánica 2000LP JimeNessuna valutazione finora
- Quim T9 2004Documento6 pagineQuim T9 2004Carolina De la peña FernándezNessuna valutazione finora
- Selectividad Química Del CarbonoDocumento16 pagineSelectividad Química Del Carbonoorganica1Nessuna valutazione finora
- Alcoholes, Éteres y Fenoles (Ejercicios)Documento3 pagineAlcoholes, Éteres y Fenoles (Ejercicios)daniel arturo100% (1)
- Alcoholes, Éteres y Fenoles (Ejercicios)Documento3 pagineAlcoholes, Éteres y Fenoles (Ejercicios)daniel arturo83% (6)
- Ejercicios 01 - GeneralidadesDocumento6 pagineEjercicios 01 - GeneralidadesDeyanira LlaxaNessuna valutazione finora
- Quimica OrganicaDocumento13 pagineQuimica OrganicaIsabel MartinezNessuna valutazione finora
- Ejercicios ChireDocumento20 pagineEjercicios Chirethiara brenetNessuna valutazione finora
- Guia de Problemas QOII 2019 Parte 1Documento60 pagineGuia de Problemas QOII 2019 Parte 1Javier ArandaNessuna valutazione finora
- Ejercicios PAU de Quimica OrganicaDocumento6 pagineEjercicios PAU de Quimica Organicafergo1Nessuna valutazione finora
- Guia de CarboniloDocumento5 pagineGuia de CarboniloGaby BlancoNessuna valutazione finora
- Quimica OrganicaDocumento8 pagineQuimica OrganicaK'aren M'onroyNessuna valutazione finora
- Quim T9 2006Documento5 pagineQuim T9 2006Carolina De la peña FernándezNessuna valutazione finora
- Problemas QO I - H 7 - S Conjugados - JAGDocumento4 pagineProblemas QO I - H 7 - S Conjugados - JAGPedro MerinoNessuna valutazione finora
- 3-Problemas de Isomeria Con Solucions Novos PDFDocumento10 pagine3-Problemas de Isomeria Con Solucions Novos PDFjosemanuelpenaclasesNessuna valutazione finora
- ACIDOS CARBOXíLICOS (Ejercicios)Documento3 pagineACIDOS CARBOXíLICOS (Ejercicios)Zero MadsNessuna valutazione finora
- Practica 1Documento4 paginePractica 1Noemi JhoanNessuna valutazione finora
- Ejer Cici OsDocumento15 pagineEjer Cici OsAngel Jesus Méndez RamírezNessuna valutazione finora
- Tarea 11 Alquinos OrganicaDocumento7 pagineTarea 11 Alquinos OrganicaAlvarez Reyes YahirNessuna valutazione finora
- Taller 2 Quimica Organica II Ago Dic 2016 - AcidosDerivadosDocumento6 pagineTaller 2 Quimica Organica II Ago Dic 2016 - AcidosDerivadosFernanda BuilaNessuna valutazione finora
- PDFDocumento3 paginePDFSantos Agramonte RondoyNessuna valutazione finora
- Quimica 8Documento8 pagineQuimica 8ivcscribdNessuna valutazione finora
- Quimica PDFDocumento8 pagineQuimica PDFYhôrdhänNessuna valutazione finora
- HIDROCARBUROS (1ra Parte) (Ejercicios)Documento4 pagineHIDROCARBUROS (1ra Parte) (Ejercicios)nicol lara lopezNessuna valutazione finora
- HIDROCARBUROS (1ra Parte) (Ejercicios)Documento4 pagineHIDROCARBUROS (1ra Parte) (Ejercicios)Cindy Karina Ticlla Castro100% (1)
- Introduccion A La Quimica OrganicaDocumento4 pagineIntroduccion A La Quimica Organicadavicho_dodo0% (1)
- Ejercicios Unidad IDocumento5 pagineEjercicios Unidad Iomar pascualNessuna valutazione finora
- Problemas QO I - H 4 - Alquenos - JAGDocumento9 pagineProblemas QO I - H 4 - Alquenos - JAGPedro MerinoNessuna valutazione finora
- AlcanosDocumento2 pagineAlcanosPedro Nuñez SanchezNessuna valutazione finora
- Taller de NomenclaturaDocumento5 pagineTaller de NomenclaturaJuan Esteban Foronda ChicaNessuna valutazione finora
- Química Orgánica SelectividadDocumento9 pagineQuímica Orgánica SelectividadantlormonNessuna valutazione finora
- Quimica Organica ExamenDocumento36 pagineQuimica Organica ExamenangelNessuna valutazione finora
- Q - ASM - Dom - Sem 35Documento2 pagineQ - ASM - Dom - Sem 35andres ortizNessuna valutazione finora
- PEC - 2 - Curso - 12 - 13 EnunciadoDocumento4 paginePEC - 2 - Curso - 12 - 13 EnunciadoNatalia MartínNessuna valutazione finora
- Calapenshko-Q Runi Dom Sem6Documento5 pagineCalapenshko-Q Runi Dom Sem6José Carlos Torres VarillasNessuna valutazione finora
- 3Documento112 pagine3EzequielFernandoNessuna valutazione finora
- Balance de materia orientado a procesosDa EverandBalance de materia orientado a procesosNessuna valutazione finora
- Gasificación de briquetas de carbón con biomasa:: una alternativa energética sostenibleDa EverandGasificación de briquetas de carbón con biomasa:: una alternativa energética sostenibleNessuna valutazione finora
- Introducción a la química de los metales de transiciónDa EverandIntroducción a la química de los metales de transiciónNessuna valutazione finora
- Hidráulica para estudiantes de ingeniería agronómicaDa EverandHidráulica para estudiantes de ingeniería agronómicaNessuna valutazione finora
- Tema 9. Enlace Químico 2010-2016 (Clase)Documento35 pagineTema 9. Enlace Químico 2010-2016 (Clase)joseluNessuna valutazione finora
- Tema 8. La Estructura Del Átomo 2010-2016 (Clase)Documento41 pagineTema 8. La Estructura Del Átomo 2010-2016 (Clase)joseluNessuna valutazione finora
- (Extra) Tema 3. Redox 2000-2009 PDFDocumento81 pagine(Extra) Tema 3. Redox 2000-2009 PDFjoseluNessuna valutazione finora
- Arquitectura Y Energía Natural - Rafael Serra y Helena CochDocumento384 pagineArquitectura Y Energía Natural - Rafael Serra y Helena Cochal_herna2100% (5)
- Tema 9. Enlace Químico 2000-2009 (Extra)Documento48 pagineTema 9. Enlace Químico 2000-2009 (Extra)joseluNessuna valutazione finora
- Tema 10. Química Orgánica 2010-2016 (Clase)Documento34 pagineTema 10. Química Orgánica 2010-2016 (Clase)joseluNessuna valutazione finora
- (Extra) Tema 4. Equilibrio 2000-2009 PDFDocumento63 pagine(Extra) Tema 4. Equilibrio 2000-2009 PDFjoseluNessuna valutazione finora
- (Extra) Tema 2. Formulación Inorgánica y Orgánica 2000-2009 PDFDocumento120 pagine(Extra) Tema 2. Formulación Inorgánica y Orgánica 2000-2009 PDFjoseluNessuna valutazione finora
- Guía DocenteDocumento9 pagineGuía DocentejoseluNessuna valutazione finora
- Adolescentes y Consumo de Drogas PDFDocumento9 pagineAdolescentes y Consumo de Drogas PDFOHJNessuna valutazione finora
- (Clase) Tema 3 Redox 2010-2016 PDFDocumento10 pagine(Clase) Tema 3 Redox 2010-2016 PDFjoseluNessuna valutazione finora
- Preguntas A ResponderDocumento3 paginePreguntas A Responderjoselu100% (1)
- (Clase) Tema 2. Formulación Inorgánica y Orgánica 2010-2016 PDFDocumento82 pagine(Clase) Tema 2. Formulación Inorgánica y Orgánica 2010-2016 PDFjoseluNessuna valutazione finora
- Instrucciones para La Realización de La Práctica Sobre Personalidad y Diferencias IndividualesDocumento5 pagineInstrucciones para La Realización de La Práctica Sobre Personalidad y Diferencias IndividualesjoseluNessuna valutazione finora
- Guion RenalDocumento7 pagineGuion RenaljoseluNessuna valutazione finora
- Práctica RelajaciónDocumento9 paginePráctica RelajaciónjoseluNessuna valutazione finora
- DX y Tto ITS PDFDocumento87 pagineDX y Tto ITS PDFjoseluNessuna valutazione finora
- Fisiologia Pulmonar-GuiónDocumento7 pagineFisiologia Pulmonar-GuiónjoseluNessuna valutazione finora
- Tema 23 HEMOSTASIA (PROPIO) PDFDocumento3 pagineTema 23 HEMOSTASIA (PROPIO) PDFjoseluNessuna valutazione finora
- InformeDocumento1 paginaInformejoseluNessuna valutazione finora
- Fisiologia Cardiovascular GuiónDocumento13 pagineFisiologia Cardiovascular GuiónjoseluNessuna valutazione finora
- Tema 23 HEMOSTASIA (PROPIO) PDFDocumento3 pagineTema 23 HEMOSTASIA (PROPIO) PDFjoseluNessuna valutazione finora
- Tema 20, 21 y 22 Sangre, Inmunida (PROPIO) PDFDocumento15 pagineTema 20, 21 y 22 Sangre, Inmunida (PROPIO) PDFjoseluNessuna valutazione finora
- Tema 29 Fisiologia PropioDocumento11 pagineTema 29 Fisiologia PropiojoseluNessuna valutazione finora
- Fisiologia Pulmonar-GuiónDocumento7 pagineFisiologia Pulmonar-GuiónjoseluNessuna valutazione finora
- Temas Respiratorio Fisiologia PDFDocumento32 pagineTemas Respiratorio Fisiologia PDFjoseluNessuna valutazione finora
- Fisiologia Cardiovascular GuiónDocumento13 pagineFisiologia Cardiovascular GuiónjoseluNessuna valutazione finora
- Tema 20, 21 y 22 Sangre, Inmunida (PROPIO) PDFDocumento15 pagineTema 20, 21 y 22 Sangre, Inmunida (PROPIO) PDFjoseluNessuna valutazione finora
- Temas Cardiovascular Fisiologia PDFDocumento59 pagineTemas Cardiovascular Fisiologia PDFjoseluNessuna valutazione finora
- HidrocarburosDocumento5 pagineHidrocarburosguiddensNessuna valutazione finora
- Práctica 2 AlcanosDocumento2 paginePráctica 2 AlcanosAlondra LunaNessuna valutazione finora
- Tarea 2Documento4 pagineTarea 2mauricioNessuna valutazione finora
- HANDBOOK OF NATURAL GAS TRANSMISSION AND PROCESSING - En.esDocumento33 pagineHANDBOOK OF NATURAL GAS TRANSMISSION AND PROCESSING - En.esIntegridad de Equipos y Gestión de Activos NelcamNessuna valutazione finora
- Entrega Final PetrolCA 1Documento65 pagineEntrega Final PetrolCA 1Teddy naranjo castroNessuna valutazione finora
- Ap Equinoccio Sistemas de Filtrado de Agua OkDocumento21 pagineAp Equinoccio Sistemas de Filtrado de Agua Okapi-26992971Nessuna valutazione finora
- AlcanosDocumento2 pagineAlcanosLuis CastilloNessuna valutazione finora
- Petro Qui MicaDocumento83 paginePetro Qui MicaAngel ArielNessuna valutazione finora
- Catalogo Crunch Oil - 2021 - EspañolDocumento29 pagineCatalogo Crunch Oil - 2021 - EspañolNicolas FuentesNessuna valutazione finora
- Libro de Trabajo 4 Bryan Blas HuamaniDocumento8 pagineLibro de Trabajo 4 Bryan Blas HuamaniBryan Blas HuamaniNessuna valutazione finora
- Humedal El Burro 1Documento10 pagineHumedal El Burro 1Sebastián VegaNessuna valutazione finora
- Guia Quimica 11º I P 2016Documento21 pagineGuia Quimica 11º I P 2016Dar MendezNessuna valutazione finora
- Prueba Coef.2 QuimicaDocumento2 paginePrueba Coef.2 QuimicaFabian Alejando Santana LeivaNessuna valutazione finora
- Eco LlantasDocumento36 pagineEco LlantasCarlos Andres Pulido VelascoNessuna valutazione finora
- Anexo 4Documento10 pagineAnexo 4Jefferson puentes laraNessuna valutazione finora
- Tema 4a. AlcanosDocumento47 pagineTema 4a. AlcanosErnesto RuizNessuna valutazione finora
- Manual Mantenimiento TransformadoresDocumento121 pagineManual Mantenimiento TransformadoresRigoberto Urrutia100% (3)
- Remediacion de SuelosDocumento6 pagineRemediacion de SuelosMaria Nathalia Aragon SanchezNessuna valutazione finora
- Energia Y Minas: Normas LegalesDocumento3 pagineEnergia Y Minas: Normas LegalesINSTITUTO INADAPNessuna valutazione finora
- AsfaltenosDocumento0 pagineAsfaltenosHenry Gustavo Chaves GutiérrezNessuna valutazione finora
- Sistema BifuelDocumento17 pagineSistema Bifuelgay tragavergasNessuna valutazione finora
- CUESTIONARIODocumento4 pagineCUESTIONARIOAngie PradaNessuna valutazione finora
- Quimica OrganicaDocumento14 pagineQuimica OrganicaAnn Victoria Villagra100% (1)
- AlcanosDocumento6 pagineAlcanosANGHELY CELESTENessuna valutazione finora
- Formulacion y NomenclaturaDocumento77 pagineFormulacion y NomenclaturabegoscribdNessuna valutazione finora
- Grupos Funcionales-Quimica Organica 17.31.56Documento16 pagineGrupos Funcionales-Quimica Organica 17.31.56equipo xochiNessuna valutazione finora
- Quimica Iv Area 2Documento12 pagineQuimica Iv Area 2Altair PerezNessuna valutazione finora
- Reglamento Actividades de ComercializacionDocumento16 pagineReglamento Actividades de ComercializacionValeria PujosNessuna valutazione finora
- Medición EstáticaDocumento52 pagineMedición EstáticaDuran ElyNessuna valutazione finora
- HDS Hidrocarburos Contaminados APLDocumento1 paginaHDS Hidrocarburos Contaminados APLEstebanNessuna valutazione finora