Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Resumen Del Articulo Cientifico Modelación de Catálisis Enzimática Con Enzimas Alostéricas
Caricato da
VinicioBenalcazarTitolo originale
Copyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Resumen Del Articulo Cientifico Modelación de Catálisis Enzimática Con Enzimas Alostéricas
Caricato da
VinicioBenalcazarCopyright:
Formati disponibili
UNIVERSIDAD CENTRAL DEL ECUADOR
INGENIERIA QUIMICA
VINICIO BENALCAZAR Entrega: viernes, 20 de Mayo del 2016
RESUMEN DE ARTICULO CIENTIFICO REFERIDO A LA INGENIERIA QUIMICA
MODELACIÓN DE CATÁLISIS ENZIMÁTICA CON ENZIMAS ALOSTÉRICAS
Fuente [CITATION Cer16 \l 8192 ]
Investigadores
- Investigadores de la Universidad Autónoma Metropolitana Unidad Iztapalapa
Antecedentes
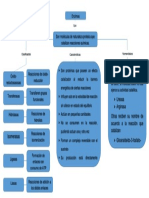
- Ciertas enzimas (llamadas alostéricas) que controlan la velocidad de rutas metabólicas
completas, tienen un mecanismo de regulación de su actividad catalítica por
acumulación de algún intermediario de la ruta metabólica.
- La enzima cataliza la condensación de carbamil-fosfato con aspartato para producir
Ncarbamil-L-aspartato y ortofosfato. Esta es una reacción inicial de la síntesis de las
pirimidinas componentes de los ácidos nucleicos.
Investigación
- Se investiga y compara un modelo de agentes con otros modelos cinéticos de la enzima
aspartato transcarbamilasa.
- La simulación realista de fenómenos biocatalíticos alostéricos depende de la
modelación del comportamiento cinético de la enzima. La cinética enzimática
basada en la forma cooperativa del complejo alostérico puede modelarse utilizando
interacciones entre agentes. La modelación con agentes permite la representación
de curvas de saturación sigmoidales, sin requerir los valores numéricos de
parámetros cinéticos necesarios en otros modelos cinéticos.
- Se analiza las reacciones y los modelos enzimáticos de :
o El sistema enzimático sin regulación alostérica
Según Chaplin
o Análisis molecular de la cinética enzimática alostérica
Según Monod
o Análisis Cinético de Hill
o Análisis basado en agentes de enzimas alostéricas y simulación de Monte Carlo
para reacciones enzimáticas alostéricas
o Modelaciones basada en agentes de reacciones enzimáticas
Resultados de la Investigación
- Se generó curvas para el análisis de saturación de sustrato hiperbólicas (enzimas no
alostéricas) grafico 1
- Curvas sigmoidales de saturación de sustrato (enzimas alostéricas) grafico 2
Grafico 1 Grafico 2
Conclusiones de la investigación
- La modelación basada en agentes representa adecuadamente el comportamiento cinético
de enzimas alostéricas.
- la comparación de los cálculos de actividad enzimática con resultados experimentales
de la enzima aspartato trascarbamilasa presenta una correspondencia aceptable.
Terminología
- Enzimas alostéricas
o Enzimas que presentan dos conformaciones diferentes, estables e
intercombertibles
o La forma inactiva presenta baja afinidad con el sustrato
o La forma activa presenta afinidad con el sustrato
- fenómenos biocatalíticos
o Reacciones catalíticas con agentes Biológicos
- Curvas de saturación sigmoidales
o Es una curva de saturación hiperbólica (características de fijación cooperativa de
ligandos a proteínas )
- La forma cooperativa del complejo alostérico
o Es una forma biológica causada por enzimas, y se realiza cuando una enzima
compleja alostérica se une a una unidad enzimática.
1 Bibliografía
Aranda , J., & Salgado, S. (2008). Revista Mexicana de Ingenieria Quimica. (Revista)
Recuperado el 18 de Mayo de 2016, de Universidad Autónoma Metropolitana Unidad
Iztapalapa.
Potrebbero piacerti anche
- ResumenDocumento2 pagineResumenDaiwa Yovana YAURICASA QUISPENessuna valutazione finora
- Tema 4. EnzimologíaDocumento3 pagineTema 4. EnzimologíaPaula MadridNessuna valutazione finora
- Clase Enzimas 2Documento42 pagineClase Enzimas 2adolfo moralesNessuna valutazione finora
- EnzimasDocumento22 pagineEnzimasMARIA PAOLA QUINTANA SISANessuna valutazione finora
- Bioquimica 2023 TP 02 Enzimas - Preguntas Domiciliarias BIOQUIDocumento8 pagineBioquimica 2023 TP 02 Enzimas - Preguntas Domiciliarias BIOQUIMati DPNessuna valutazione finora
- Enzimologia BasicaDocumento11 pagineEnzimologia BasicaLuis FallaNessuna valutazione finora
- Enzimología Tema 1bDocumento35 pagineEnzimología Tema 1bpabloNessuna valutazione finora
- CUESTIONARIODocumento11 pagineCUESTIONARIOClaudia PalmaNessuna valutazione finora
- Clase EnzimasDocumento55 pagineClase Enzimasadolfo moralesNessuna valutazione finora
- 6.enzimas. Generalidades. Medida ActividadDocumento64 pagine6.enzimas. Generalidades. Medida ActividadKaren Cuenca100% (1)
- Unidad 2Documento69 pagineUnidad 2Geréz JulioNessuna valutazione finora
- ME-Objetivos Enzimas RevDocumento20 pagineME-Objetivos Enzimas Revapi-369665675% (4)
- En ZimasDocumento267 pagineEn ZimasAnibal Izak Vazkez KamarenahNessuna valutazione finora
- Informe de Laboratorio AlbuminaDocumento5 pagineInforme de Laboratorio AlbuminaAlfredo El MuguNessuna valutazione finora
- Bbioquimica de Los Alimentos - Enzimas en Panaderia y ConfiteriaDocumento33 pagineBbioquimica de Los Alimentos - Enzimas en Panaderia y ConfiteriaHenry Oré Gutiérrez83% (6)
- Cuestionarios de BioquimicaDocumento33 pagineCuestionarios de Bioquimicameme.gdjgtxNessuna valutazione finora
- Tema 3. EnzimasDocumento34 pagineTema 3. Enzimastopo presidenteNessuna valutazione finora
- Biocápsula de EnzimasDocumento5 pagineBiocápsula de EnzimasLaura PomaresNessuna valutazione finora
- Tema 2.1 Enzimología ClínicaDocumento26 pagineTema 2.1 Enzimología ClínicaGuillermo LasarteNessuna valutazione finora
- Informe de Actividad EnzimaticaaaaaaDocumento22 pagineInforme de Actividad Enzimaticaaaaaalizbet perez mezaNessuna valutazione finora
- S5 Enzimas 2023Documento3 pagineS5 Enzimas 2023ValentinaNessuna valutazione finora
- Tema 5 - EnzimasDocumento9 pagineTema 5 - EnzimasJulian Jaramillo AngelNessuna valutazione finora
- Bioquimica Pendiente Tarea 3Documento3 pagineBioquimica Pendiente Tarea 3francisco riveraNessuna valutazione finora
- Cinética EnzimáticaDocumento12 pagineCinética EnzimáticaAbner Hernandez LopezNessuna valutazione finora
- F Tema 8. Enzimas.Documento31 pagineF Tema 8. Enzimas.David G dtortuagmail.comNessuna valutazione finora
- ENZIMIOLOGÍA - Obstetricia PDFDocumento65 pagineENZIMIOLOGÍA - Obstetricia PDFDerecho IcaNessuna valutazione finora
- Tema 5 (Enzimas) PDFDocumento9 pagineTema 5 (Enzimas) PDFPercya RochaNessuna valutazione finora
- Biocatalizador CompletoDocumento21 pagineBiocatalizador CompletoEnzon BritoNessuna valutazione finora
- Catálisis Enzimática y EspecificidadDocumento29 pagineCatálisis Enzimática y EspecificidadLissette GioannaNessuna valutazione finora
- Enzimas BioquimicaDocumento45 pagineEnzimas BioquimicaJcaminoNessuna valutazione finora
- ENZIMASDocumento8 pagineENZIMASBrenda Michelle Baños CedeñoNessuna valutazione finora
- Tema 2. Cinética EnzimáticaDocumento34 pagineTema 2. Cinética EnzimáticapabloNessuna valutazione finora
- Actividad EnzimaticaDocumento7 pagineActividad EnzimaticaAndres DelgadilloNessuna valutazione finora
- Unidad 2 - Tema 3 - Regulación de EnzimasDocumento31 pagineUnidad 2 - Tema 3 - Regulación de EnzimasMarianaNessuna valutazione finora
- EnzimasDocumento15 pagineEnzimasCandela RodriguezNessuna valutazione finora
- ENZIMASDocumento5 pagineENZIMASSebastián Camargo ReaNessuna valutazione finora
- Qué Es La Cinética EnzimáticaDocumento4 pagineQué Es La Cinética EnzimáticaJesús RGNessuna valutazione finora
- Guia 3 B1Documento9 pagineGuia 3 B1Victor Manuel Magana TrinidadNessuna valutazione finora
- Enzimas y CofactoresDocumento74 pagineEnzimas y CofactoresJeimykNessuna valutazione finora
- 08 EnzimasDocumento44 pagine08 EnzimasCarlos M. Guerra ANessuna valutazione finora
- Bioprocesos Preguntas Tipo ExamenDocumento4 pagineBioprocesos Preguntas Tipo Examenanthony minho Caballero IparraguirreNessuna valutazione finora
- Enzimas Reguladoras - Dra. GilDocumento35 pagineEnzimas Reguladoras - Dra. GilHinO - Arturo100% (1)
- Guía Actividad EnzimáticaDocumento15 pagineGuía Actividad EnzimáticaDaniela AdarmeNessuna valutazione finora
- EnzimasDocumento50 pagineEnzimasGato QuequeNessuna valutazione finora
- Resumen EnzimasDocumento5 pagineResumen EnzimasHisely Inuyasely Suárez RendónNessuna valutazione finora
- Conferencia 5.biocatalizadores. Regulación EnzDocumento45 pagineConferencia 5.biocatalizadores. Regulación EnzNoybNessuna valutazione finora
- TP 5 Enzimas ByBM 2023Documento28 pagineTP 5 Enzimas ByBM 2023valentina umbidezNessuna valutazione finora
- Actividad Enzimática (Modo de Compatibilidad) (Reparado)Documento17 pagineActividad Enzimática (Modo de Compatibilidad) (Reparado)Diego Joaquín RiveraNessuna valutazione finora
- Enzimas, Conversión de SustratoDocumento50 pagineEnzimas, Conversión de SustratomoncadaNessuna valutazione finora
- J Tarea Bioquimica 1Documento5 pagineJ Tarea Bioquimica 1Jessenia MaciasNessuna valutazione finora
- 04 - EnzimasDocumento12 pagine04 - Enzimascarlitaferreyra12Nessuna valutazione finora
- En ZimasDocumento4 pagineEn ZimasMaria GarciaNessuna valutazione finora
- Cinetica EnzimaticaDocumento3 pagineCinetica EnzimaticaNIDIA JULISSA ALCALDE CARDENASNessuna valutazione finora
- Enzimas 2Documento19 pagineEnzimas 2Eduardo FeriaNessuna valutazione finora
- Aspectos Generales y Propiedades de Las EnzimasDocumento37 pagineAspectos Generales y Propiedades de Las Enzimasronald stevn alvarez osorioNessuna valutazione finora
- E. ZimasDocumento15 pagineE. Zimasluis fernandoNessuna valutazione finora
- EnzimasDocumento8 pagineEnzimasDavid JimenezNessuna valutazione finora
- EnzimasDocumento13 pagineEnzimasMariana CastilloNessuna valutazione finora
- Cálculo de parámetros de rapidez en cinética química, cinética enzimática y catálisis heterogéneaDa EverandCálculo de parámetros de rapidez en cinética química, cinética enzimática y catálisis heterogéneaValutazione: 5 su 5 stelle5/5 (1)
- Tipos de Catalizadores Según Las Reaccione QuimicasDocumento3 pagineTipos de Catalizadores Según Las Reaccione QuimicasVinicioBenalcazarNessuna valutazione finora
- Proyecto Diseño PerfumeDocumento25 pagineProyecto Diseño PerfumeVinicioBenalcazarNessuna valutazione finora
- Destilacion Rellenos PDFDocumento24 pagineDestilacion Rellenos PDFVinicioBenalcazarNessuna valutazione finora
- Cambios MonetariosDocumento5 pagineCambios MonetariosVinicioBenalcazarNessuna valutazione finora
- Reacciones Quimicas, CCR y Proceso ClausDocumento19 pagineReacciones Quimicas, CCR y Proceso ClausVinicioBenalcazarNessuna valutazione finora
- Fundamentos Contabilidad de CostosDocumento4 pagineFundamentos Contabilidad de CostosVinicioBenalcazarNessuna valutazione finora
- Test de DegustacionDocumento1 paginaTest de DegustacionVinicioBenalcazarNessuna valutazione finora
- Deber FodaDocumento4 pagineDeber FodaVinicioBenalcazarNessuna valutazione finora
- Analisis Experimental de Un Sistema Dinamico de FiltracionDocumento4 pagineAnalisis Experimental de Un Sistema Dinamico de FiltracionVinicioBenalcazarNessuna valutazione finora
- Sistema de Almacenamiento de Lodos Peligrosos.Documento2 pagineSistema de Almacenamiento de Lodos Peligrosos.VinicioBenalcazarNessuna valutazione finora
- Matriz de Marco Logico o Matriz de PlanificaciónDocumento28 pagineMatriz de Marco Logico o Matriz de PlanificaciónVinicioBenalcazarNessuna valutazione finora
- Resumen Articulo CientificoDocumento2 pagineResumen Articulo CientificoVinicioBenalcazarNessuna valutazione finora
- Definicion de Paradigmas y 5 Ejm ParadigmasDocumento6 pagineDefinicion de Paradigmas y 5 Ejm ParadigmasVinicioBenalcazarNessuna valutazione finora
- Deber Ejercicios LibroDocumento19 pagineDeber Ejercicios LibroVinicioBenalcazarNessuna valutazione finora
- Resumen Articulo Cientifico Diamante Sintético de Distintos Colores PersonalizadoDocumento3 pagineResumen Articulo Cientifico Diamante Sintético de Distintos Colores PersonalizadoVinicioBenalcazarNessuna valutazione finora
- Ejemplos de Ciclo de Vida de ProductosDocumento11 pagineEjemplos de Ciclo de Vida de ProductosVinicioBenalcazarNessuna valutazione finora
- Concepto de Proyectos IndustrialesDocumento6 pagineConcepto de Proyectos IndustrialesVinicioBenalcazarNessuna valutazione finora
- Resumen Articulo Científico Procedimiento de Obtención de Fracciones de LípidosDocumento3 pagineResumen Articulo Científico Procedimiento de Obtención de Fracciones de LípidosVinicioBenalcazarNessuna valutazione finora
- Resumen Articulo Científico Método para La Obtención de Aceite Extravirgen de La Pulpa de AguacateDocumento3 pagineResumen Articulo Científico Método para La Obtención de Aceite Extravirgen de La Pulpa de AguacateVinicioBenalcazarNessuna valutazione finora
- Resumen Articulo Científico Composición y Proceso para Tratamiento de Aguas Residuales y Negras Obteniendo Agua PotableDocumento2 pagineResumen Articulo Científico Composición y Proceso para Tratamiento de Aguas Residuales y Negras Obteniendo Agua PotableVinicioBenalcazarNessuna valutazione finora
- Marco Teorico - Elaboración de Azucar en Polvo de Miel de AbejaDocumento3 pagineMarco Teorico - Elaboración de Azucar en Polvo de Miel de AbejaVinicioBenalcazarNessuna valutazione finora
- Resumen Articulo Cientifico Conversión HidrotérmicaDocumento3 pagineResumen Articulo Cientifico Conversión HidrotérmicaVinicioBenalcazarNessuna valutazione finora
- Resumen Articulo Cientifico Sistema para Lixiviación Solar en Pilas de MineralesDocumento3 pagineResumen Articulo Cientifico Sistema para Lixiviación Solar en Pilas de MineralesVinicioBenalcazarNessuna valutazione finora
- Resumen Articulo Científico Metodo Hidrometalúrgico para La Recuperación de ZincDocumento4 pagineResumen Articulo Científico Metodo Hidrometalúrgico para La Recuperación de ZincVinicioBenalcazarNessuna valutazione finora
- Articulo Cientifico CepasDocumento2 pagineArticulo Cientifico CepasVinicioBenalcazarNessuna valutazione finora
- RESUMEN ARTICULO CIENTIFICO BiopeliculasDocumento3 pagineRESUMEN ARTICULO CIENTIFICO BiopeliculasVinicioBenalcazarNessuna valutazione finora
- Informe 1-Benalcazar-Practica1-In - Reac.quim.1Documento9 pagineInforme 1-Benalcazar-Practica1-In - Reac.quim.1VinicioBenalcazarNessuna valutazione finora
- Ejercicios de ElectroquímicaDocumento8 pagineEjercicios de ElectroquímicaVinicioBenalcazarNessuna valutazione finora
- Corrosion Selectiva - ExposiciónDocumento25 pagineCorrosion Selectiva - ExposiciónVinicioBenalcazarNessuna valutazione finora
- Balanceada Por REDOX3Documento3 pagineBalanceada Por REDOX3Alejandra Mantilla100% (1)
- Instituto Politécnico Nacional: Laboratorio de Cinetica Y Reactores Homogeneos Titular: Edgar Ivan Hernandez CarvajalDocumento14 pagineInstituto Politécnico Nacional: Laboratorio de Cinetica Y Reactores Homogeneos Titular: Edgar Ivan Hernandez CarvajalFernandaa' SancheezNessuna valutazione finora
- Repaso San Marcos Semana 06 - QuímicaDocumento8 pagineRepaso San Marcos Semana 06 - QuímicaSILVIA ROSARIO CHALCO MENDOZANessuna valutazione finora
- Unidad I. Ejercicios (20-27943)Documento21 pagineUnidad I. Ejercicios (20-27943)Alexis GomezNessuna valutazione finora
- OrgII - Unidad - IV - Clase 1Documento19 pagineOrgII - Unidad - IV - Clase 1Juan V RamirezNessuna valutazione finora
- Informe Reloj de YODODocumento5 pagineInforme Reloj de YODOKevin ContrerasNessuna valutazione finora
- Tarea Unidad 4Documento5 pagineTarea Unidad 4octaviopozo andresauriaNessuna valutazione finora
- Condensación AldólicaDocumento6 pagineCondensación AldólicaLaura Valentina FernándezNessuna valutazione finora
- Guia de Trabajo Reacciones y Ecuaciones QuímicasDocumento4 pagineGuia de Trabajo Reacciones y Ecuaciones QuímicasJose HernandezNessuna valutazione finora
- Laboratorio 3Documento5 pagineLaboratorio 3Necker Chumbes EscobarNessuna valutazione finora
- CINÉTICA - iNFORME 10 FINALDocumento8 pagineCINÉTICA - iNFORME 10 FINALcamila barrera barrientosNessuna valutazione finora
- En ZimasDocumento47 pagineEn ZimasFelipe LavínNessuna valutazione finora
- HDT - Cinética EnzimáticaDocumento2 pagineHDT - Cinética EnzimáticaAle GarciaNessuna valutazione finora
- ESTUDIO CINETICO DE LA INVERSION DE LA SACAROSA - Informe 1 - 1 1Documento21 pagineESTUDIO CINETICO DE LA INVERSION DE LA SACAROSA - Informe 1 - 1 1Luciana Camila Olivera AguilarNessuna valutazione finora
- Presentación Trabajo de Química y Ciencia Ilustraciones Moléculas Verde TurquesaDocumento12 paginePresentación Trabajo de Química y Ciencia Ilustraciones Moléculas Verde TurquesaNuñez Damian SaraNessuna valutazione finora
- Marco Teorico - Reacciones RedoxDocumento13 pagineMarco Teorico - Reacciones RedoxLivia Prtl FlrsNessuna valutazione finora
- PB, CD, Ni Vs CuDocumento3 paginePB, CD, Ni Vs CuJeanzhito SweetNessuna valutazione finora
- Reporte 1. Equilibrio QuímicoDocumento18 pagineReporte 1. Equilibrio Químicocristian lopezNessuna valutazione finora
- Feria Cientifica Reloj de YodoDocumento21 pagineFeria Cientifica Reloj de YodoLuis Almarza OrellanaNessuna valutazione finora
- Tema 8 ENZIMAS Y CATÁLISISDocumento5 pagineTema 8 ENZIMAS Y CATÁLISISJohanna Castillo100% (1)
- Cinética EnzimáticaDocumento22 pagineCinética EnzimáticaMeybelin QuispeNessuna valutazione finora
- Factores Que Afectan La Actividad Enzimatica y Digestion Enzimatica Del AlmidonDocumento1 paginaFactores Que Afectan La Actividad Enzimatica y Digestion Enzimatica Del AlmidonPatty Soncco SonccoNessuna valutazione finora
- Bitacora P 2.4 BitácoraDocumento3 pagineBitacora P 2.4 BitácorarauljcNessuna valutazione finora
- Problemas de Cinetica y Reactores Fase Ii PDFDocumento13 pagineProblemas de Cinetica y Reactores Fase Ii PDFANDREA VANESSA ROJAS VARGASNessuna valutazione finora
- Anexo 3 QUIMICADocumento5 pagineAnexo 3 QUIMICAAcademia InternacionalNessuna valutazione finora
- Informe Rendimiento 8 DEFINITIVODocumento21 pagineInforme Rendimiento 8 DEFINITIVOWILLIAM ANDRES OVALLE VILLARRAGANessuna valutazione finora
- Cuadro EnzimasDocumento1 paginaCuadro Enzimascarlos0% (1)
- Cálculos EstequiométricosDocumento2 pagineCálculos Estequiométricoscarocamacho957321100% (2)
- Tema 1 CineticaDocumento60 pagineTema 1 CineticaChristian QC100% (1)
- Taller Reacciones QuímicasDocumento9 pagineTaller Reacciones QuímicasSebastian PedrozoNessuna valutazione finora