Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Trabajo Práctico de Laboratorio Destilación
Caricato da
Sofía A. SánchezDescrizione originale:
Copyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Trabajo Práctico de Laboratorio Destilación
Caricato da
Sofía A. SánchezCopyright:
Formati disponibili
Trabajo Práctico de Laboratorio N°3: Destilación
Objetivo de la práctica: llevar a cabo la purificación y separación de
compuestos orgánicos mediante un proceso de destilación
Destilación
La destilación es el método más común e importante para la purificación y
separación de líquidos. Este método se emplea para separar dos o más líquidos
miscibles de una mezcla, o para eliminar el disolvente de sustancias disueltas.
Hay varios tipos de destilaciones, entre ellas se destacan la simple y la
fraccionada, y por otro lado la por arrastre con vapor y a presión reducida.
Destilación simple:
El objetivo de la destilación es la separación de un líquido volátil de una sustancia
no volátil o la separación de líquidos con distintos puntos de ebullición. La destilación
simple se usa cuando la diferencia entre los puntos de ebullición de los componentes
es grande, mayor de 80ºC, o cuando las impurezas son sólidos disueltos en el líquido a
purificar. La destilación es ampliamente utilizada, por ejemplo, para recuperar
disolventes y para obtener agua destilada.
Para la destilación simple, normalmente se utiliza un aparato como el
representado en la figura 1, montado sobre dos soportes. Consta de un matraz de
destilación, provisto de un termómetro. El matraz descansa sobre una placa calefactora.
El matraz de destilación va unido a un refrigerante con camisa de refrigeración por la
que circula agua en contracorriente. Finalmente, el extremo inferior del refrigerante se
une a una alargadera que conduce el destilado al matraz colector.
Figura 1: Equipo de destilación simple
El líquido que se quiere destilar se pone en el matraz (que no debe llenarse
mucho más de la mitad de su capacidad) y se calienta con la placa calefactora. Cuando
se alcanza la temperatura de ebullición del componente más volátil comienza la
producción apreciable de vapor, condensándose parte del mismo en las paredes del
matraz. La mayor parte del vapor pasa a través de la tubuladura lateral de la cabeza de
destilación al refrigerante donde se condensa debido a la corriente de agua fría que
asciende por la camisa de este. El destilado (vapor condensado) escurre al matraz
colector.
Destilación fraccionada:
Si la diferencia que hay entre los puntos de ebullición es demasiado pequeña
para que una destilación simple resulte eficiente, es necesario recurrir a destilaciones
repetidas. En la práctica se emplea una columna fraccionada, a través de la cual la fase
de vapor y la fase condensada fluyen en direcciones opuestas. De tal manera que el
vapor a medida que asciende por la columna es cada vez más rico en el componente
más volátil.
La eficiencia de tales columnas se expresa en platos teóricos. Un plato teórico
se define como la unidad de la columna que tiene la misma eficacia en la separación
que una destilación simple y se expresa a menudo en centímetros de altura de la
columna.
Destilación por arrastre con vapor:
La destilación por arrastre con vapor es una técnica usada para separar
sustancias orgánicas insolubles en agua y ligeramente volátiles, de otras no volátiles
que se encuentran en la mezcla, como resinas o sales inorgánicas, u otros compuestos
orgánicos no volátiles.
Fundamento físico: ley de Dalton
Los vapores saturados de los líquidos inmiscibles siguen la Ley de Dalton sobre
las presiones parciales, que establece que: cuando el vapor de dos sustancias, que no
reaccionan entre sí, se mezcla a temperatura constante, cada vapor ejerce la misma
presión que ejercería si estuviera solo. Consecuentemente, la suma de las presiones de
cada gas (presiones parciales, P1, P2, … Pp), será igual a la presión total del sistema
(PT). Su expresión matemática es la siguiente:
PT = P1 + P2 + --- Pn
Al destilar una mezcla de dos líquidos inmiscibles entre sí, su punto de ebullición
será la temperatura a la cual la suma de las presiones de vapor parciales (es decir, PT)
iguala a la presión externa. Esta temperatura será inferior al punto de ebullición del
componente más volátil. Si uno de los líquidos es agua (destilación por arrastre con
vapor de agua) y si se trabaja a la presión atmosférica, se podrá separar un componente
de mayor punto de ebullición que el agua a una temperatura inferior a 100ºC. Esto es
muy importante cuando el compuesto se descompone al someterlo a elevadas
temperaturas (por ejemplo, su propia temperatura de ebullición). En general, esta
técnica se utiliza cuando los compuestos cumplen con las condiciones de ser volátiles,
inmiscibles en agua, tener presión de vapor baja y elevado punto de ebullición.
Aplicaciones Industriales: aceites esenciales
La destilación por arrastre con vapor se emplea con frecuencia para separar
aceites esenciales de tejidos vegetales. Los aceites esenciales son mezclas complejas
de hidrocarburos, terpenos, alcoholes, compuestos carbonílicos, aldehídos aromáticos
y fenoles y se encuentran en hojas, cáscaras o semillas de algunas plantas.
En el vegetal, los aceites esenciales están almacenados en glándulas,
conductos, sacos o en otros reservorios dentro del vegetal, por lo que es conveniente
desmenuzar el material para exponer esos reservorios a la acción del vapor de agua.
Los aceites esenciales son productos naturales aplicados en diferentes industrias como
la industria cosmética y farmaceútica.
Métodos: destilación por arrastre con vapor
Cuando se usa vapor saturado o sobrecalentado, generado fuera del equipo
principal, ya sea por una caldera, una olla de presión o un matraz adecuado, esta técnica
recibe el nombre de "destilación por arrastre con vapor" propiamente dicha.
También se puede usar el llamado "método directo", en el que el material está
en contacto íntimo con el agua generadora del vapor. En este caso, se ponen en el
mismo recipiente el agua y el material a extraer, se calientan a ebullición y el aceite
extraído es arrastrado junto con el vapor de agua hacia un condensador, que enfría la
mezcla, la cual es separada posteriormente para obtener el producto deseado.
Procedimiento experimental
Separación por destilación simple de una mezcla de sustancias
Esta experiencia consiste en la separación de una mezcla compuesta por una
solución acuosa de CuSO4 y cloroformo (punto de ebullición 61.2°C) y comprobar
mediante un indicador la pureza del líquido destilado.
Se monta el aparato de destilación según se indica en la figura 1. A continuación
se introducen en el matraz de destilación 50 ml de cloroformo y 150 ml de solución de
CuSO4.
Se enciende entonces la platina calefactora y se comienza a calentar la mezcla
contenida en el matraz, observando el incremento progresivo de temperatura en el
termómetro. A una temperatura próxima al punto de ebullición del cloroformo
(componente más volátil) se observará que se empieza a recoger destilado. Anotar
esta temperatura y recoger hasta que la temperatura de destilación se aproxime a los
100 °C (fracción 1) y colocarlos aparte en un tubo. Anotar la temperatura al acabar la
recolección de la fracción 1. Continuar la destilación y seguir recogiendo destilado
(fracción 2) hasta que apenas quede líquido en el matraz. Apagar entonces la platina
calefactora.
Informe de laboratorio:
Evaluar y describir los resultados obtenidos teniendo en cuenta las condiciones
en que se realizó la experiencia.
Potrebbero piacerti anche
- Eficiencia energética en las instalaciones de climatización en los edificios. ENAC0108Da EverandEficiencia energética en las instalaciones de climatización en los edificios. ENAC0108Nessuna valutazione finora
- Guia de Practicas Fisicoquímica I.Documento113 pagineGuia de Practicas Fisicoquímica I.Bryan Zavala PachecoNessuna valutazione finora
- Destilación SencillaDocumento4 pagineDestilación SencillaVARLODNessuna valutazione finora
- Guía 7-DestilaciónDocumento9 pagineGuía 7-DestilaciónkatherineNessuna valutazione finora
- TallerDocumento9 pagineTallerdavid esteban33% (3)
- Diagrama de Flujo para La Determinación de Azúcar en Bebidas CarbonatadasDocumento1 paginaDiagrama de Flujo para La Determinación de Azúcar en Bebidas CarbonatadasFranklin RiveraNessuna valutazione finora
- AlquenosDocumento18 pagineAlquenosChris Flores GonzalesNessuna valutazione finora
- Unidad 1-Química 4to AñoDocumento7 pagineUnidad 1-Química 4to AñoMarcosNessuna valutazione finora
- Guía 1 Equilibrio Iónico PDFDocumento7 pagineGuía 1 Equilibrio Iónico PDFeduarNessuna valutazione finora
- MetilanilinaDocumento23 pagineMetilanilinaBryan Roncal LlajarunaNessuna valutazione finora
- Teorico de Hidrocarburos Aromaticos Polinucleares 2017Documento35 pagineTeorico de Hidrocarburos Aromaticos Polinucleares 2017whiyeNessuna valutazione finora
- Determinacion de Agua en El AlcoholDocumento9 pagineDeterminacion de Agua en El AlcoholAaronNessuna valutazione finora
- Introducción. Arrastre de VaporDocumento2 pagineIntroducción. Arrastre de VaporAlejandro AlcántaraNessuna valutazione finora
- Aplicaciónes de La Fisicoquimica A La Petroquimica 1Documento9 pagineAplicaciónes de La Fisicoquimica A La Petroquimica 1Eduardo PicónNessuna valutazione finora
- Informe 3Documento6 pagineInforme 3Deyanira PoloNessuna valutazione finora
- Practic 3 Cambios Fisicos y QuimicosDocumento12 paginePractic 3 Cambios Fisicos y QuimicosAnibal0% (1)
- Extraccion Cafeina Quimica OrganicaDocumento2 pagineExtraccion Cafeina Quimica OrganicaSantiago MoralesNessuna valutazione finora
- Analisis Cualitativo Del Carbono Acabado PDFDocumento8 pagineAnalisis Cualitativo Del Carbono Acabado PDFJuan GarciaNessuna valutazione finora
- Hidrocarburos AromaticosDocumento14 pagineHidrocarburos AromaticosAlex UbagoNessuna valutazione finora
- Volumetrias y Volumetria de PrecipitacionDocumento51 pagineVolumetrias y Volumetria de PrecipitacionC'Denisse PalominoNessuna valutazione finora
- Cuál Es La Diferencia Entre Cristalización y PrecipitaciónDocumento2 pagineCuál Es La Diferencia Entre Cristalización y PrecipitaciónJennifer AlvinoNessuna valutazione finora
- Practico #8 Obtención de AmoníacoDocumento5 paginePractico #8 Obtención de AmoníacoMaruja Del Pópolo GrzonaNessuna valutazione finora
- Informe. Práctica 3Documento11 pagineInforme. Práctica 3Melina HernándezNessuna valutazione finora
- Informe de Propiedades Coligativas Completo G 2Documento11 pagineInforme de Propiedades Coligativas Completo G 2Nitgma DcNessuna valutazione finora
- Aislamiento de Limoneno A Partir de Cascaras de NaranjaDocumento4 pagineAislamiento de Limoneno A Partir de Cascaras de NaranjaLuz CasteleyroNessuna valutazione finora
- Práctica 7. Fenómenos Físicos y QuímicosDocumento3 paginePráctica 7. Fenómenos Físicos y QuímicosKariLu LittleFace100% (1)
- LAB 3 Fenol AguaDocumento2 pagineLAB 3 Fenol AguaSebastián MachucaNessuna valutazione finora
- Principales Factores Que Afectan A La SolubilidadDocumento3 paginePrincipales Factores Que Afectan A La SolubilidadJAIME ANDRES CARDOZO GONZALEZNessuna valutazione finora
- PROYECTO de DestilacionDocumento11 paginePROYECTO de DestilacionOrlanny Contreras Bautista100% (1)
- Marco TeoricoDocumento4 pagineMarco TeoricoAna Luz MoyaNessuna valutazione finora
- Resumen de Adición de Radicales y Reacciones.Documento13 pagineResumen de Adición de Radicales y Reacciones.Javier Aldair Ruiz AmadorNessuna valutazione finora
- Informe 3 - Extracción de La CafeínaDocumento5 pagineInforme 3 - Extracción de La CafeínaStephanie GabriellaNessuna valutazione finora
- Lab 1. Guia Extraccion de Cafeina de Te o CafeDocumento4 pagineLab 1. Guia Extraccion de Cafeina de Te o Cafejuan DavidNessuna valutazione finora
- EquilibrioDocumento14 pagineEquilibrioNatalia Arias Figueroa100% (1)
- Cuestionario de QuimicaDocumento20 pagineCuestionario de QuimicaNeil Edwin Alarcón RoseroNessuna valutazione finora
- Practica N°2 Extraccion y CromatografiaDocumento18 paginePractica N°2 Extraccion y CromatografiaLeonela SANessuna valutazione finora
- Practica 3 Cinetica.1Documento9 paginePractica 3 Cinetica.1Kenyaa CarolinaaNessuna valutazione finora
- Previo 2 Pruebas de Solubilidad en Disolventes OrgánicosDocumento4 paginePrevio 2 Pruebas de Solubilidad en Disolventes OrgánicosSophie Evans100% (2)
- TamizadosDocumento5 pagineTamizadosTatito CastiyopNessuna valutazione finora
- Lab. 6Documento7 pagineLab. 6Yeimy EstefanyNessuna valutazione finora
- INTRODUCCIÓNDocumento3 pagineINTRODUCCIÓNKatty Julieth Rangel GutierrezNessuna valutazione finora
- Informe de ExtracciónDocumento5 pagineInforme de ExtracciónJunnior Alejandro AcostaNessuna valutazione finora
- Practica 8Documento2 paginePractica 8Gabriela MerchanNessuna valutazione finora
- Guia de Laboratorio 1 Quimica OrganicaDocumento8 pagineGuia de Laboratorio 1 Quimica OrganicaJanice RomeroNessuna valutazione finora
- Informe Final - Reactividad de HidrocarburosDocumento7 pagineInforme Final - Reactividad de HidrocarburosLaura EscobarNessuna valutazione finora
- Informe de Laboratorio de Química Orgánica: Identificación de Sustancias y Propiedades Físicas ESPOLDocumento9 pagineInforme de Laboratorio de Química Orgánica: Identificación de Sustancias y Propiedades Físicas ESPOLCarolina Sánchez86% (7)
- COMBUSTIÓNDocumento4 pagineCOMBUSTIÓNDiego Sotelo0% (1)
- PRACTICA 5 - Destilacion SencillaDocumento9 paginePRACTICA 5 - Destilacion SencillaDeymis AlborNessuna valutazione finora
- Quimica Maceracion PracticaDocumento2 pagineQuimica Maceracion PracticaIvan SilvaNessuna valutazione finora
- Aldehidos y Cetonas. Sintesis y Reacciones.Documento12 pagineAldehidos y Cetonas. Sintesis y Reacciones.Belen Rocio Delmar Flores CaribauxNessuna valutazione finora
- Centrifugación Diferencial de Organelos CelularesDocumento4 pagineCentrifugación Diferencial de Organelos CelularesKatherine Ester Cortez VillaNessuna valutazione finora
- Secuencia Didáctica: Propiedades Periódicas de Los Elementos - PPTX Pegui.Documento6 pagineSecuencia Didáctica: Propiedades Periódicas de Los Elementos - PPTX Pegui.Emerson Man50% (2)
- Obtención de EtilenoDocumento3 pagineObtención de Etilenosantiago971226100% (1)
- Informe de Laboratorio Destilación FraccionadaDocumento11 pagineInforme de Laboratorio Destilación Fraccionadadanna gabriela pereira villanuevaNessuna valutazione finora
- Práctica de Laboratorio SaponificaciónDocumento3 paginePráctica de Laboratorio SaponificaciónZulema CastroNessuna valutazione finora
- Solubilidad y SolucionesDocumento5 pagineSolubilidad y SolucionesEdgar RomeroNessuna valutazione finora
- Laboratorio de DestilacionDocumento38 pagineLaboratorio de DestilacionNatalyNessuna valutazione finora
- PROYECTO Alcohol A Partir de Jugo de NaranjaDocumento8 paginePROYECTO Alcohol A Partir de Jugo de NaranjaAndy CondeNessuna valutazione finora
- Destilación Por Arrastre de VaporDocumento7 pagineDestilación Por Arrastre de VaporGary Robert Gunther Maidana100% (1)
- PrácticaDocumento8 paginePrácticaGamer RJNessuna valutazione finora
- Norma TSRDocumento5 pagineNorma TSRCesar Augusto Cruz CruzNessuna valutazione finora
- Informe Finalizado Actualizado PDFDocumento230 pagineInforme Finalizado Actualizado PDFGerardo MestasNessuna valutazione finora
- Proyecto UBVDocumento9 pagineProyecto UBVGabriel VivenesNessuna valutazione finora
- IPS E-Max ZirCADDocumento40 pagineIPS E-Max ZirCADjorgeNessuna valutazione finora
- Suministro y Desalojo Del Agua de La Ciudad de MéxicoDocumento17 pagineSuministro y Desalojo Del Agua de La Ciudad de MéxicoAngelus UtenaNessuna valutazione finora
- Taller Riesgo Quimico.Documento23 pagineTaller Riesgo Quimico.Lizette Vanessa PEREZ GOMEZNessuna valutazione finora
- Office de Planta 1Documento6 pagineOffice de Planta 1Gypsysoul AryamNessuna valutazione finora
- Foro Semana 1Documento3 pagineForo Semana 1Mary Valladares100% (1)
- Fenomenos Fisicos y QuimicosDocumento7 pagineFenomenos Fisicos y QuimicosOmar BisbalNessuna valutazione finora
- Cuaderno PracticoDocumento58 pagineCuaderno PracticoJensy Kimberlim Villanueva Tantalean100% (2)
- LISTOS INFORMES 5TO GRADO (3) LAPSO MARLON ListosDocumento8 pagineLISTOS INFORMES 5TO GRADO (3) LAPSO MARLON ListosmaximinoNessuna valutazione finora
- Pavimentos SilenciososDocumento42 paginePavimentos SilenciososHuber Adrian Cati ZeaNessuna valutazione finora
- Ciclo OtecDocumento4 pagineCiclo OtecLuigi MaguiñaNessuna valutazione finora
- Procedimiento de Uso de ComedoresDocumento10 pagineProcedimiento de Uso de ComedoresYAWARNessuna valutazione finora
- TRABAJO - FINAL - P&ID Tratamiento de Aguas ResidualesDocumento22 pagineTRABAJO - FINAL - P&ID Tratamiento de Aguas ResidualesOri ApazaNessuna valutazione finora
- Modelo PNT Oregano PDFDocumento82 pagineModelo PNT Oregano PDFCristian Alvarez HuillcaNessuna valutazione finora
- Maquinarias en La Industria de Bebidas GasificadasDocumento16 pagineMaquinarias en La Industria de Bebidas GasificadasAnderson Jhon ArgandoñaNessuna valutazione finora
- Recuperacion de Oro Pauchi MarcallaccDocumento32 pagineRecuperacion de Oro Pauchi MarcallaccFlores Valdivia NenaxinaiNessuna valutazione finora
- Ejercicios Principio de Arquimedes-201m0315Documento11 pagineEjercicios Principio de Arquimedes-201m0315Ernesto GamboaNessuna valutazione finora
- Física y Química 3º Eso Control 1 Solucionado 2012 - 2013Documento6 pagineFísica y Química 3º Eso Control 1 Solucionado 2012 - 2013mmfdez377Nessuna valutazione finora
- Examen Quinto Segundo BimDocumento8 pagineExamen Quinto Segundo BimcelekimmyNessuna valutazione finora
- Excavaciones OshasDocumento12 pagineExcavaciones OshasLudis Núñez BlancoNessuna valutazione finora
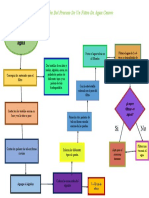
- Elaboración Del Proceso de Un Filtro de Agua CaseroDocumento1 paginaElaboración Del Proceso de Un Filtro de Agua Caserofamilia preciadoNessuna valutazione finora
- Taller de Jabones RitualizadosDocumento21 pagineTaller de Jabones RitualizadosShary Alcantara67% (3)
- Arcilla Resumida PDFDocumento10 pagineArcilla Resumida PDFFramSamtanaNessuna valutazione finora
- Equipos, Unidades y Reactivos de EIADocumento9 pagineEquipos, Unidades y Reactivos de EIAMafer SolizNessuna valutazione finora
- Tub. PVC SAGAR. Ficha TecnicaDocumento3 pagineTub. PVC SAGAR. Ficha Tecnicaarnold100% (1)
- Impactos Ambientales Proyecto 8 Semana 1 Decimo AñoDocumento5 pagineImpactos Ambientales Proyecto 8 Semana 1 Decimo AñoDennis TinocoNessuna valutazione finora
- P O SO: % 200kg X Fertilizante 100% X 256,41 KGDocumento27 pagineP O SO: % 200kg X Fertilizante 100% X 256,41 KGJavier De la CruzNessuna valutazione finora
- Noguera Henriquez Roberto Eduardo 2022Documento133 pagineNoguera Henriquez Roberto Eduardo 2022percy mendoza callupeNessuna valutazione finora