Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Ácidos y bases: teorías de Arrhenius, Brønsted-Lowry y Lewis
Caricato da
Yessica silvaDescrizione originale:
Titolo originale
Copyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Ácidos y bases: teorías de Arrhenius, Brønsted-Lowry y Lewis
Caricato da
Yessica silvaCopyright:
Formati disponibili
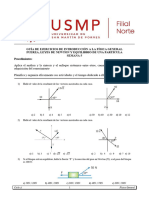
SEMANA 6 2018 – III
18/10/18
ACIDOS Y BASES d) I, IV y V e) todas
1. Según Arrhenius, Bronsted y Lowry, indique un
ácido triprótico y la base más débil. 10. Indique verdadero (V) o falso (F) según
I. H2CO3 II. HNO3 III. H3PO4 IV. Br-1 corresponda:
V. I –1
VI. Cl -1
( ) Un método práctico para obtener el ácido
a) II y V b) III y VI c) III y IV conjugado de una base Bronsted-Lowry es
d) II y IV e) III y V quitar un hidrógeno a la fórmula de la base
( ) Con respecto a la fuerza relativa del ácido
2. ¿Cuántas proposiciones son verdaderas? clórico y el ácido brómico se cumple:
I. El C6H6 es aprótico HClO3 HBrO3
II. El HS- es un anfótero. ( ) Con respecto a los oxiácidos del cloro, la
III. El NaOH 10–3 M es básico. fuerza de los ácidos disminuye como sigue:
IV. El HClO4 es más ácido que el H2SO4 HClO4 HClO3 HClO2 HClO
a) FFFV b) VVVV c) FFVV d) VVFF e) VVFV ( ) Una reacción Bronsted – Lowry también se
da en fase gaseosa:
3. Según su fuerza ácida, ¿cuál es incorrecta? NH3(g) + HCl(g) NH4Cl(g)
I. H2SO3 > H2SeO3 > H2TeO3 a) VFVF b) VVVV c) FVFV d) FFVV e) FVVV
II. H l > HBr > HCI > HF 11. Escriba las fórmulas de las especies químicas
III. CH4 > NH3 > H2O que faltan:
IV. HClO4 > HNO3 > H3PO4 I. HSO4- + ……… SO4-2 + NH4+
V. HClO3 > HClO2 > HClO II. PH3 + HCl ………… + Cl-
a) I y III b) III c) II d) IV y V e) I y IV III. HNO3 + ……… NO3 -
+ H3O+
IV. HCO3 + H2O ………… +
-
CO3-2
4. Sobre la teoría de los electrólitos, ¿cuántos son a) NH2 , PH4 , H2O , H3O
- + +
verdaderos? b) NH3 , PH4+ , OH- , H3O+
I. La solución de NaCl conduce electricidad. c) NH-2 , PH2- , H2O , OH-
II. Según Arrhenius, el grado de disociación d) NH3 , PH4+ , H2O , H3O+
depende de la concentración del electrolito. e) NH2+2 , PH4 , H2O , H3O+
III. El HCl(ac) es mejor conductor que el
CH3COOH. 12. Si para los siguientes ácidos oxácidos, la fuerza
IV. Al mezclar CS2 con C6H6, la mezcla es de acidez aumenta con el número de átomos de
conductora. oxígeno.
a) 0 b) c) 2 d) 4 e) 3 HClO < HClO2 < HClO3 < HClO4
Marque el orden creciente de fuerza básica para
5. ¿Qué sales disueltas en agua, hacen que su pH sus conjugados.
sea menor que 7? a) HClO2 < HClO3 < HClO < HClO4
I. NaHCO3, II. NH4NO3, III. NaBr b) HClO4 < HClO3 < HClO2 < HClO
a) I y II b) I y III c) II y III c) ClO4- < ClO3- < ClO2- < ClO-
d) solo I e) II d) ClO -
< ClO2- < ClO3- < ClO4-
e) ClO3 -
< ClO2- < ClO4- < ClO-
6. El soluto que aumenta el pOH del H2O será:
a) KCN b) NH4Cl c) Zn(OH)2 13. Respecto a la teoría de Lewis, marque
d) NaNO3 e) HCOOK verdadero (V) o falso (F):
( ) La reacción ácido-base implica la
7. ¿Qué sal o sales aumenta el pH del agua? transferencia de un par de electrones.
I. NaHCO3 II. NaHSO4 III. NaCl ( ) Los cationes de transición tienen tendencia a
IV. AlCl3 V. K3PO4 formar iones complejos, por lo cual son
a) todas b) I y V c) I, II y V ácidos
d) I. II, IV y V e) I, IV y V ( ) En las reacciones ácido-base de Lewis se
puede producir una sal.
8. Señale verdadero (V) o falso (F). ( ) Los ácidos son agentes electrofílicos y las
I. El NH3 y BH3 son bases de Lewis. bases son agentes nucleofílicos
II. El CO2 es ácido de Lewis y el agua es base a) VFVF b) FVVV c) FVFV
de Lewis. d) VVVV e) FFVV
III. Según Arrhenius la neutralización se 14. Del siguiente listado ¿Cuáles son sustancias
representa por H + + OH – H2O ácidas de Lewis?
IV. La siguiente reacción es ácido-base de Lewis 1) NO3- 2) NH4+ 3) BeBr2 4) SO3 5) AsH3
Ag+ + 2NH3 Ag(NH3)+2 a) 1, 2, 3 b) 2, 4, 5 c) 2, 3, 4
a) VFFV b) FFFF c) VVVV d) FVVV e) FVFV d) Sólo 1 y 5 e) Todos
9. Indique los pares ácido-base conjugados según 15. Respecto a la teoría Acido-Base de Arrhenius:
la teoría de Bronsted Lowry: I. Los ácidos aumentan la concentración de H+
I. H2CO3 , CO2 II. H2O , OH- III. H2SO3 , HSO3- en una solución acuosa
IV. OH- , O2- V. HCl , Cl2 II Las bases liberan OH- y neutralizan los ácidos
a) I y V b) II, III y IV c) II y III produciendo sal y agua.
Prof. Gerardo Santamaria
SEMANA 6 2018 – III
18/10/18
III. HI, H2SeO4 y NH3 son ácidos ( ) La oxidación y reducción ocurren en forma
IV.KOH, Ba(OH)2 y B(OH)3 son bases simultánea
Son incorrectas: ( ) El agente oxidante se oxida
a) Sólo I b) Sólo II c) I y II ( ) La forma reducida cede electrones
d) III y IV e) Todas ( ) El agente reductor se oxida.
a) VVFFF b) FFVVF c) VVFFV d) FVFFV e) FFFVF
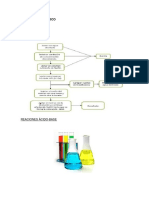
REACCIONES REDOX 7. ¿Completar las siguientes semireacciones de
1. Indique verdadero (V) o falso (F) de cada oxidación o reducción?
proposición respecto a las reacciones redox: I. S2 – ....................... S 8
I. La sustancia que se reduce transfiere II. P4 ...................... P3 –
electrones al que se oxida a) Oxidación; 12: reducción; 12
II. En la reducción se pierde electrones para que b) Oxidación; 16: reducción ;12
aumente el estado de oxidación (E.O) c) Reducción; 16: reducción; 12
III. El agente oxidante es la sustancia que se oxida d) Oxidación; 16: oxidación; 12
IV. Reacción intramolecular: Cuando se oxida y se e) Oxidación; 2: reducción 3
reduce elementos diferentes que pertenecen a 8. Colocar verdadero (V) o falso (F) donde
un solo reactante. corresponda:
a) FFVV b) FFFV c) VFFV d) VFFV e) FVFV I. Una sustancia se reduce si existe su agente
2. Se llama agente oxidante a la sustancia que reductor
se....................... y genera la................... que II. Una sustancia se oxida si existe su agente
se encuentra en ............................ oxidante
a) reduce – forma reducida – productos III. El agente reductor transfiere electrones al
b) oxida - forma reducida – productos agente oxidante
c) reduce - forma oxidada – productos IV. El agente oxidante y el agente reductor
d) oxida – forma oxidada - reactantes puede ser la misma sustancia
e) oxida – forma oxidada – productos a) FFFV b) FFVV c) VVFV d) VVVV e) VVVF
3. En cuál de las siguientes casos se genera 9. No es característica de una reacción redox:
reacción Redox a) El total de electrones perdidos es igual al
a) Al ingerir sal de Andrews después de una total de electrones ganados.
acidosis estomacal b) El proceso de oxidación es simultaneo con el
b) La formación de la lluvia ácida proceso de reducción.
c) La degradación anaeróbica hasta metano de c) Los átomos al transferir sus electrones se
una manzana oxidan y los que los reciben se reducen.
d) La precipitación del AgCl d) Se da por intercambio de iones.
e) Todas son redox e) Se puede tener dos o mas sustancias que se
4. Indique verdadero (V) o falso (F) de cada oxiden y reduzcan al mismo tiempo.
proposición respecto a las reacciones redox: 10. En la reacción química:
I. La sustancia que se reduce transfiere S + KOH K2SO3 + K2S + H2O
electrones al que se oxida Podemos afirmar:
II. En la reducción se pierde electrones para que I. El azufre se oxida II. El azufre se reduce
aumente el estado de oxidación (E.O) III. El K2S es la especie o forma reducida
III. El agente oxidante es la sustancia que se IV. La suma de coeficiente es 18
oxida V. Se trata de una dismutación
IV.Reacción intramolecular: Cuando se oxida y se a) I, II, III b) I, II, III, IV c) I, II, III, V d) Sólo
reduce elementos diferentes que pertenecen a II e) I y III
un solo reactante.
a) FFVV b) FFFV c) VFFV d) VFFV e) 11. En la ecuación química:
FVFV Cr2O3 + Na2CO3 + KNO3 Na2CrO4 + CO2 +
5. Son reacciones Redox: KNO2
I. Desprendimiento de hidrógeno cuando se Al dividir el coeficiente del agente oxidante entre
ataca un metal con ácido. el coeficiente del agente reductor se obtiene:
II. Desprendimiento de CO2 por descomposición a) 3 b) 0,33 c) 2 d) 0,5 e) 2/3
de ácido carbónico. 12. Igualar la siguiente ecuación:
III. Desprendimiento de CO2 por combustión del K2Cr2O7 +H2S+H2SO4 S +Cr2(SO4)3+K2SO4
metano +H2O
IV.Desplazamiento de un metal por otro metal Hallar la suma de los coeficientes
más activo. estequiométricos de las sustancias que se
V. Descomposición de un compuesto en sus disocian y las que se ionizan en agua:
elementos. a) 7; 3 b) 3; 7 c) 3 y 4
a) I, II, IV b) II, III, V c) I, II, III, V d) 2 y 3 e) 4; 3
d) I, III, IV, V e) Todos 13. A partir de la reacción:
6. Respecto a las reacciones redox indique FeCl2 + KMnO4 + HCl FeCl3 + MnCl2 + KCl +
verdadero (V) o falso (F) según corresponda: H2O
( ) Existe variación del estado de oxidación Hallar el valor de “x” con respecto a los
coeficientes de la reacción igualada.
Prof. Gerardo Santamaria
SEMANA 6 2018 – III
18/10/18
X = suma de coeficientes de las sales haloideas e) III, IV y V
suma de coeficientes de sales oxisales
a) 3/8 b) 4/5 c) 5/4 d) 1/12 e) 12/1 24. En la siguiente ecuación química; se puede
afirmar que:
14. De la siguiente ecuación: KMnO4 + C6H12O6 K2Cr2O7 + NO2 + HNO3 KNO3 + Cr(NO3)3 +
CO2 + MnO2 + K2CO3 + H2O. H2O
Indique la relación molar: a) El agente reductor es el HNO3
E = Coeficiente(oxidante + reductor)/forma b) El agente oxidante es el K2Cr2O7
reducida c) El agente oxidante es el cromo
a) 5/4 b) 4/5 c) 2/3 d) 3/2 e) 9/8 d) La sustancia que gana electrones es NO2
15. Luego de balancear la ecuación rédox, e) El agente oxidante es el HNO3
determine la relación molar que existe entre la 25. ¿Cuál de las proposiciones es incorrecta al
forma oxidada y la forma reducida, según: balancear por redox la reacción:
P2H4 PH3 + P4H2 P4 + KOH + H2O KH2PO2 + PH3
a) 2 b) 6 c) 2/3 d) 1/3 e) 1/6 a) es una reacción de dismutación
b) transfiere 12 electrones
16. Al balancear la siguiente ecuación química, c) su forma reducida es PH3
indique el coeficiente de la especie que se d) coeficiente del H2O es 3
oxida. e) e) de coeficiente en total es 12
Cr2O7-2 + SO3-2 + H+ Cr3+ + SO4-2 + 26. Balancear la siguiente ecuación e indica la
H2O relación molar: (Agente reductor /Agente
a) 1 b) 3 c) 2 d) 4 e) 6 oxidante) y suma de coeficientes de las
17. Para la reacción redox en medio básico: sustancias que se ionizan en agua.
S-2 + OH- + I2 SO4-2 + I- + H2O HNO3 + HMnO4 + KHSO4 K2S2O8 + Mn(NO3)2+
¿Cuál es el coeficiente de los iones hidroxilo? H2O
a) 4 b) 7 c) 8 d) 12 e) 18 a) 10, 5 b) 5, 6 c) 2, 5
18. Dada la siguiente ecuación química: d) 1/2, 6 e) 4, 8
Co+2 + OH- + ClO3- Co2O3 + Cl- + H2O 27. La suma de los coeficientes al balancear la
¿Cuántos moles de agente reductor se necesita siguiente ecuación es: KI + H2SO4K2SO4+ I2+
para generar 324 g de agua? H2S+ H2O
a) 9 b) 13 c) 16 d) 26 e) 20
a) 19 b) 29 c) 18 d) 12 e) 36 28. Al balancear la ecuación química:
19. Balancear la siguiente ecuación en medio ácido: AsO4-3 + I-1 + H+ AsO2-1 + I2 +
FeS + NO31- NO + SO42- + Fe3+ H2O
e indicar cuantas moles de agua, se obtienen por Indicar (V) Verdadero ó (F) Falso:
cada 6 moles de agente oxidante . ( ) El arseniato se oxida a arsenito
a) 1 b) 2 c) 4 d) 6 e) 12 ( ) Se forma 1 mol I2 por cada mol I-1
20. Balancear la siguiente reacción y determina el ( ) El coeficiente del agente reductor es 2
coeficiente del reductor en: ( ) La reacción ocurre en medio fuertemente
Cloruro férrico + ácido sulfhídrico Cloruro ácido.
ferroso + ácido clorhídrico + azufre a) VVVV b) VVFF c) FFVV d) FFVF e) VFVF
a) 5 b) 4 c) 3 d) 2 29. ¿Cuántas moles de H2SO4 debe agregarse
e) 1 para neutralizar completamente el medio básico
21. Luego de balancear en medio básico: en que se realiza la siguiente reacción?
MnO4- + I- + H2O MnO2 + IO3- + OH- . CrI3 + Cl2 CrO4 -2 + IO4 - + Cl - (medio básico)
Calcule el número de moles de forma reducida a) 2 b) 27 c) 64 d) 32 e) 128
por cada 5 moles de la forma oxidada. 30. Indique el coeficiente de los ión OH – que
a) 2 b) 3 c) 6 d) 8 e) 10 resultan de balancear la siguiente reacción: ClO -
22. La reacción en medio alcalino: Al + NO3- Cl2 + ClO3 -
[Al(OH)4]- + NH3 , tiene por coeficiente del agua a) 1 b) 2 c) 4 d) 5 e) 6
y del oxidrilo: 31. Balancee en medio ácido e indique la suma
a) 13 y 2 b) 10 y 6 c) 18 y 5 d) 24 y 5 e) de coeficientes: H2O2 + MnO4-1 O2 + Mn+2
13 y 6 a) 14 b) 16 c) 10 d) 28 e) 15
23. Al ajustar la semireacción en medio ácido; 32. Luego de balancear la siguiente reacción,
P4 H2PO4- , se observa que; señalar la suma de coeficientes de las especies
I. Se necesita 4 mol de H2O para producir 5 que no se ionizan en agua.
mol de electrones. C6H12O6 + NO3-1 H+ NO + CO2
II. Se generan 6 mol de H+ por cada mol de a) 12 b) 10 c) 13 d)18 e) 15
H2PO4- 33. Con la catáfila de la cebolla se puede limpiar
III. Se pierden 10 mol de e por cada mol P4 el oxido férrico (Fe2O3) que se forma en los
IV. La razón molar : e-/ H+ = 10/9 utensilios de cocina hechos de metal (cuchillos,
V. La razón molar : H2O / H+ = 2/3 cucharas, etc.) esto debido al oxalato de calcio
Las proposiciones verdaderas son: presente en la cebolla que puede reducir al ión
a) I, III y IV b) II, III, V c) I, II y V d) II, III Fe+3 del oxido, según:
y IV Fe2O3 + (C2O4)-2 CO2 + Fe
Prof. Gerardo Santamaria
SEMANA 6 2018 – III
18/10/18
Esta reacción se realiza adicionando unas gotas
de limón. Indique la suma de los coeficientes de
los reactantes:
a) 21 b) 11 c) 10 d)8 e) 6
34. En la reacción en medio alcalino: Al + NO3-
AlO2- + NH3 Es incorrecto decir:
a) El aluminio pierde electrones b) El nitrógeno
gana electrones c) La suma de todos los coef. es
32 d) La especie oxidada tiene coef. 8 e) El
aluminio es reductor
35. ¿Cuántas moléculas de H2O existen en la
ecuación química balanceada en medio ácido?
HS2O3-1 S+HSO4-1
a) 4 b) 1 c) 2 d) 3 e) 5
36. El coeficiente del C 2 en el balance de la
siguiente ecuación en un medio básico es:
C 2 C O3 C
a) 2 b) 3 c) 4 d) 5 e) 6
37. El ion triyoduro en solución se obtiene por
reacción del yodato y del ion yoduro en medio
ácido.
IO3-(ac) + I-(ac) I3- (ac)
Luego para determinar la cantidad de triyoduro
producido se le hace reaccionar con tiosulfato de
sodio en solución y los nuevos productos son el
ion yoduro y el ion tetratiosulfonato, según la
ecuación:
I3- + S2O32- I- + S4O62-
A partir de estas reacciones determine:
I. El número de moles de ion triyoduro
producidos por 1 mol de agente oxidante en
la primera reacción.
II. El número de moles de ion tetrationato
producidos por 1 mol de agente reductor, en
la segunda reacción.
a) 9;3 b) 24;3 c) 18;3 d) 24;0,5 e) 3;0,5
38. El tetróxido de diyodo (I2O4) reacciona con
hidroxido de sodio produciéndose yodato sódico,
yoduro de sodio, agua y O2 molecular. Luego de
escribir la ecuación química, señale la
proposición incorrecta:
a) Uno de los elementos se oxida y se reduce.
b) El NaIO3 no es la única forma oxidada.
c) Es una reacción redox intramolecular.
d) No constituye una reacción de dismutación.
e) El I2O4 solo actua como agente reductor.
39. El yodo molecular en medio básico se
autoxida-reduce a yodito y yoduro. Balancee la
ecuación y determine la relación:
N=Coeficiente OH-/Coeficiente de la forma
oxidada
a) 5 b) 6 c) 7 d) 8 e) 9
Prof. Gerardo Santamaria
Potrebbero piacerti anche
- Quimica PDFDocumento5 pagineQuimica PDFErik Apec CeoNessuna valutazione finora
- Sofia Pre2021.II 01Documento2 pagineSofia Pre2021.II 01JAIME REDOLFO YUPANQUINessuna valutazione finora
- 1er Seminario FISICADocumento12 pagine1er Seminario FISICAAntonio Montalvo CorreaNessuna valutazione finora
- Examende ConocimientoDocumento2 pagineExamende ConocimientoHernan Miranda RamosNessuna valutazione finora
- Química Estructura Materia con . Resume el tema central del documento que es la química y la estructura de la materia a nivel nanoscópicoDocumento66 pagineQuímica Estructura Materia con . Resume el tema central del documento que es la química y la estructura de la materia a nivel nanoscópicoIvonne Seminario AlejavoNessuna valutazione finora
- Formato Full PraxisDocumento5 pagineFormato Full PraxisHugo Cahuana YucraNessuna valutazione finora
- Teoría Semana 1Documento10 pagineTeoría Semana 1GABRIEL EDUARDO BARTOLO CARRANZANessuna valutazione finora
- Raz. Mate 1 PDFDocumento2 pagineRaz. Mate 1 PDFJOHA CORNEJONessuna valutazione finora
- Capítulo 01 Materia Energía - 1Documento1 paginaCapítulo 01 Materia Energía - 1Teofilo Donaires FloresNessuna valutazione finora
- Cinematica Graficas 2Documento4 pagineCinematica Graficas 2Luis SalazarNessuna valutazione finora
- 2013 IiDocumento94 pagine2013 IiRaul Leon Espinoza100% (1)
- Problemas Propuestos-La MateriaDocumento2 pagineProblemas Propuestos-La MateriaMATEO TAIPE TANIANessuna valutazione finora
- Semestral Unmsm - Química (Intro)Documento3 pagineSemestral Unmsm - Química (Intro)Camila EspinozaNessuna valutazione finora
- Anual Uni-Semana 20 FísicaDocumento19 pagineAnual Uni-Semana 20 Físicaalez cercaNessuna valutazione finora
- Capítulo 12 Soluciones 0Documento6 pagineCapítulo 12 Soluciones 0Teofilo Donaires FloresNessuna valutazione finora
- Caratulas UssDocumento16 pagineCaratulas UssRosa Maria Soriano TrujillanoNessuna valutazione finora
- Problemas - MateriaDocumento3 pagineProblemas - MateriaMATEO TAIPE TANIANessuna valutazione finora
- Quimica 2Documento34 pagineQuimica 2lalo92_1Nessuna valutazione finora
- Químicasemana 8 RepasoDocumento3 pagineQuímicasemana 8 RepasoYubel N. Lopez VasquezNessuna valutazione finora
- Semana 1 Estructura AtómicaDocumento2 pagineSemana 1 Estructura AtómicaJORGE LUIS VALDEZ CONDENANessuna valutazione finora
- Cap. MateriaDocumento2 pagineCap. MateriaWalter Silva SerranoNessuna valutazione finora
- Química Tema 06Documento8 pagineQuímica Tema 06Cesar CubasNessuna valutazione finora
- Fenómenos químicos y físicosDocumento2 pagineFenómenos químicos y físicosalvaroNessuna valutazione finora
- Quimica Semana 06Documento3 pagineQuimica Semana 06Alexis Chunga ReupoNessuna valutazione finora
- S1 QuímicaDocumento2 pagineS1 QuímicaCesar CubasNessuna valutazione finora
- 5to Grado de Secundaria Ciencias Ib-Ev - AngelDocumento79 pagine5to Grado de Secundaria Ciencias Ib-Ev - AngelAngel Alfredo Guillen UrrutiaNessuna valutazione finora
- Fracciones PDFDocumento2 pagineFracciones PDFCaleb Nuñes TafurNessuna valutazione finora
- Química reacciones químicasDocumento6 pagineQuímica reacciones químicasYessica silvaNessuna valutazione finora
- Seminario IIDocumento1 paginaSeminario IIPromedio SjlNessuna valutazione finora
- Análisis dimensional y representación de magnitudes físicasDocumento2 pagineAnálisis dimensional y representación de magnitudes físicasSilvioChávezNessuna valutazione finora
- SEM 1 Materia y Energia - Docx 1Documento3 pagineSEM 1 Materia y Energia - Docx 1Anonymous SxQLvCNessuna valutazione finora
- Gráficas Del Movimiento MecanicoDocumento7 pagineGráficas Del Movimiento Mecanicokarinxxxx50% (2)
- 2-Conceptos Generales 2012Documento7 pagine2-Conceptos Generales 2012Javier Andres Esteban MuñozNessuna valutazione finora
- Semana 4Documento4 pagineSemana 4Rodolfo Angel Carrillo VelasquezNessuna valutazione finora
- NOMENCLATURADocumento14 pagineNOMENCLATURAbaterod3Nessuna valutazione finora
- T7 - Números Racionales IiDocumento2 pagineT7 - Números Racionales IiOmar RamirezNessuna valutazione finora
- Análisis Vectorial 5°Documento3 pagineAnálisis Vectorial 5°Wilmer Flores CastroNessuna valutazione finora
- Unc Física - Tema 02 VectoresDocumento4 pagineUnc Física - Tema 02 VectoresManuel MecoNessuna valutazione finora
- Semana 3Documento5 pagineSemana 3Rodolfo Angel Carrillo VelasquezNessuna valutazione finora
- Propiedades de La MateriaDocumento2 paginePropiedades de La MateriaCarlos Alfonso Jara Benites100% (1)
- Formulación InorgánicaDocumento17 pagineFormulación InorgánicafinstrolNessuna valutazione finora
- Análisis dimensional en físicaDocumento4 pagineAnálisis dimensional en físicaVictorNessuna valutazione finora
- Semana 2.2 PDFDocumento8 pagineSemana 2.2 PDFRodolfo Angel Carrillo VelasquezNessuna valutazione finora
- Semana 13 PDFDocumento9 pagineSemana 13 PDFRodolfo Angel Carrillo VelasquezNessuna valutazione finora
- Boletín #1 (Repaso) UFNVDocumento57 pagineBoletín #1 (Repaso) UFNVKattlin CáceresNessuna valutazione finora
- Qi Academia - Materia y Energía I.Documento2 pagineQi Academia - Materia y Energía I.Maribel Condori MaqueraNessuna valutazione finora
- Nomenclatura Inorganica-2013Documento16 pagineNomenclatura Inorganica-2013CarNessuna valutazione finora
- Examen Admisión 2002 - IiDocumento6 pagineExamen Admisión 2002 - Iitreeblackshago3138Nessuna valutazione finora
- 1separataquimicacolegio 140330204752 Phpapp01Documento4 pagine1separataquimicacolegio 140330204752 Phpapp01Josue Marin PomaNessuna valutazione finora
- MPCLDocumento2 pagineMPCLcleverNessuna valutazione finora
- VECTORESDocumento10 pagineVECTORESEdwin GonzalesNessuna valutazione finora
- Física - Constantes Fundamentales. Unidades - GiancoliDocumento2 pagineFísica - Constantes Fundamentales. Unidades - GiancolidanielitoNessuna valutazione finora
- Química OrgánicaDocumento11 pagineQuímica Orgánicalantano3000Nessuna valutazione finora
- PROBLEMAS DE QUÍMICA FÍSICA Y QUÍMICADocumento3 paginePROBLEMAS DE QUÍMICA FÍSICA Y QUÍMICAMATEO TAIPE TANIANessuna valutazione finora
- Cepunt Sem01 Abril Agosto2007Documento3 pagineCepunt Sem01 Abril Agosto2007Ysrael NarvaezNessuna valutazione finora
- Repaso Quimicaa PreDocumento4 pagineRepaso Quimicaa PreRichard SolanoNessuna valutazione finora
- Cap 10 Reacciones Químicas 01Documento1 paginaCap 10 Reacciones Químicas 01Teo DonairesNessuna valutazione finora
- Ejercicios Balota 8Documento10 pagineEjercicios Balota 8Beny BarraNessuna valutazione finora
- Acidos y BasesDocumento7 pagineAcidos y BasesWilian Humberto Vargas FarfanNessuna valutazione finora
- Acidos y Bases NivelacionDocumento3 pagineAcidos y Bases NivelacionCarlosConstantinoNessuna valutazione finora
- planeamiento estratgico empresarialDocumento29 pagineplaneamiento estratgico empresarialYessica silvaNessuna valutazione finora
- POLINOMICA ELECTRICASDocumento14 paginePOLINOMICA ELECTRICASYessica silvaNessuna valutazione finora
- VALORIZACIÓN ARQUITECTURADocumento23 pagineVALORIZACIÓN ARQUITECTURAYessica silvaNessuna valutazione finora
- Guía de ejercicios - S5Documento8 pagineGuía de ejercicios - S5Yessica silvaNessuna valutazione finora
- Monografía sobre el Proyecto Hidráulico MajesDocumento5 pagineMonografía sobre el Proyecto Hidráulico MajesYessica silvaNessuna valutazione finora
- VALORIZACIÓN ARQUITECTURADocumento23 pagineVALORIZACIÓN ARQUITECTURAYessica silvaNessuna valutazione finora
- VALORIZACION SANITARIASDocumento19 pagineVALORIZACION SANITARIASYessica silvaNessuna valutazione finora
- Examen Final GBDocumento1 paginaExamen Final GBYessica silvaNessuna valutazione finora
- My Oral ProyectDocumento12 pagineMy Oral ProyectYessica silvaNessuna valutazione finora
- Análisis Sísmico EstáticoDocumento36 pagineAnálisis Sísmico EstáticoJULCA SILVA JOSE CARLOSNessuna valutazione finora
- Examen Parcial ANTISISMICADocumento2 pagineExamen Parcial ANTISISMICAMauricio PaicoNessuna valutazione finora
- Laboratorio Práctico N1Documento3 pagineLaboratorio Práctico N1Yessica silvaNessuna valutazione finora
- 066 Ca 71684732249 TEMA05 CUADRILATEROSPERUANO2023 OKOKDocumento3 pagine066 Ca 71684732249 TEMA05 CUADRILATEROSPERUANO2023 OKOKYessica silvaNessuna valutazione finora
- Pert CPMDocumento7 paginePert CPMJUAN CARLOS PERICHE CASTRONessuna valutazione finora
- Laboratorio 02Documento2 pagineLaboratorio 02Yessica silvaNessuna valutazione finora
- Vivienda unifamiliar - Cuadro de acabadosDocumento10 pagineVivienda unifamiliar - Cuadro de acabadosYessica silvaNessuna valutazione finora
- Listado de empleadosDocumento2 pagineListado de empleadosYessica silvaNessuna valutazione finora
- Cuenta BCPDocumento1 paginaCuenta BCPYessica silvaNessuna valutazione finora
- Examen Final - BDocumento2 pagineExamen Final - BYessica silvaNessuna valutazione finora
- Formula de Euler para Hallar El Pandeo de Una ColumnaDocumento4 pagineFormula de Euler para Hallar El Pandeo de Una ColumnaYessica silvaNessuna valutazione finora
- Las Tres GargantasDocumento1 paginaLas Tres GargantasYessica silvaNessuna valutazione finora
- Presentación y Sustentación Del 50% Avance Trabajo Caso AplicativoDocumento1 paginaPresentación y Sustentación Del 50% Avance Trabajo Caso AplicativoYessica silvaNessuna valutazione finora
- Drywall y falso techo: conceptos, usos y construcciónDocumento1 paginaDrywall y falso techo: conceptos, usos y construcciónYessica silvaNessuna valutazione finora
- Ley 1 Newton equilibrio fuerzasDocumento1 paginaLey 1 Newton equilibrio fuerzasYessica silvaNessuna valutazione finora
- Tabla de AcabadosDocumento3 pagineTabla de AcabadosYessica silvaNessuna valutazione finora
- METRADO ELECTRICAS - XLSX - METRADOS ELECTRICAS Local ComunalDocumento1 paginaMETRADO ELECTRICAS - XLSX - METRADOS ELECTRICAS Local ComunalYessica silvaNessuna valutazione finora
- Ingeniería romana: El Panteón de Agripa, cúpula de hormigón no armado más grande de la antigüedadDocumento1 paginaIngeniería romana: El Panteón de Agripa, cúpula de hormigón no armado más grande de la antigüedadYessica silvaNessuna valutazione finora
- Aprendizaje, regresión y hormigón con ML, SVR, GPR, RLA y ANNDocumento1 paginaAprendizaje, regresión y hormigón con ML, SVR, GPR, RLA y ANNYessica silvaNessuna valutazione finora
- Expo 4 Planeamiento AlexDocumento1 paginaExpo 4 Planeamiento AlexYessica silvaNessuna valutazione finora
- Libro1 (Recuperado Automáticamente)Documento1 paginaLibro1 (Recuperado Automáticamente)Yessica silvaNessuna valutazione finora
- Unidad # 4 Equilibrio QuimicoDocumento53 pagineUnidad # 4 Equilibrio QuimicoALEJANDRO ALONSO OCHOA VARGASNessuna valutazione finora
- Biorremediación de Arsénico Con Apoyo de Ingeniería GenéticaDocumento10 pagineBiorremediación de Arsénico Con Apoyo de Ingeniería GenéticaBreiner Yupanqui PecheNessuna valutazione finora
- Sssinforme de Empresa PiggisDocumento24 pagineSssinforme de Empresa Piggisvaleria japonNessuna valutazione finora
- VolumetríaDocumento17 pagineVolumetríaandyskywalkerNessuna valutazione finora
- Informe Pila VoltaicaDocumento4 pagineInforme Pila VoltaicaCarlosNessuna valutazione finora
- Matías Vargas Control 3Documento6 pagineMatías Vargas Control 3matias vargas apablazaNessuna valutazione finora
- Formación dNTPsDocumento4 pagineFormación dNTPsAngel HinojosaNessuna valutazione finora
- Reacciones Ácido-Base y RedoxDocumento9 pagineReacciones Ácido-Base y RedoxEL PAPUNessuna valutazione finora
- Electrólisis Del AguaDocumento11 pagineElectrólisis Del AguaBriggitte RodríguezNessuna valutazione finora
- ARTURO TOMAS MANSILLA JORDAN - Reporte 4 - Determinación de CenizasDocumento6 pagineARTURO TOMAS MANSILLA JORDAN - Reporte 4 - Determinación de CenizasArturo Mansilla JordanNessuna valutazione finora
- Bromo Por Electrolisis FinalDocumento9 pagineBromo Por Electrolisis FinalDimar Villarroel RNessuna valutazione finora
- ECUACIONES QUÍMICAS Y CÁLCULOSDocumento24 pagineECUACIONES QUÍMICAS Y CÁLCULOSKiara Marielen Salazar PaucarNessuna valutazione finora
- Análisis químico de compuestos orgánicos e inorgánicosDocumento67 pagineAnálisis químico de compuestos orgánicos e inorgánicosisabelNessuna valutazione finora
- Kahoot QuimicaDocumento3 pagineKahoot QuimicaAnonymous L1LsiwwnNessuna valutazione finora
- Gómez Espitia Diego Julian - Practica 4Documento5 pagineGómez Espitia Diego Julian - Practica 4DIEGO JULIAN GOMEZ ESPITIANessuna valutazione finora
- 6) Procedimiento Caracterización y Cuantificación ChosDocumento3 pagine6) Procedimiento Caracterización y Cuantificación ChosAnie SegoviaNessuna valutazione finora
- Clase 7 - Morfologia de Los Depositos Minerales - Principales Depositos Explotados - Rol Pirita PDFDocumento55 pagineClase 7 - Morfologia de Los Depositos Minerales - Principales Depositos Explotados - Rol Pirita PDFMaglio RamosNessuna valutazione finora
- Química InorgánicaDocumento15 pagineQuímica InorgánicaVictor TiconaNessuna valutazione finora
- Examen Bimestral 2 - Saco Oliveros - 4to Año - Belisario - Julio 2016Documento4 pagineExamen Bimestral 2 - Saco Oliveros - 4to Año - Belisario - Julio 2016Carmen Rosa Castro DíazNessuna valutazione finora
- GRUPO 6IM2 Lista de Los Potenciales de OxidaciónDocumento1 paginaGRUPO 6IM2 Lista de Los Potenciales de OxidaciónJulian PerezNessuna valutazione finora
- Tarea 6-Resolución QOIIDocumento6 pagineTarea 6-Resolución QOIISonya BarriosNessuna valutazione finora
- CaballaDocumento60 pagineCaballapaul darioNessuna valutazione finora
- Fao Gasificacion BiomasaDocumento110 pagineFao Gasificacion BiomasaCarlos J. Mateo100% (1)
- Ilovepdf Merged PDFDocumento63 pagineIlovepdf Merged PDFAlissa SerranoNessuna valutazione finora
- TP N°10 - ElectroquímicaDocumento24 pagineTP N°10 - ElectroquímicaMauricio ahumadaNessuna valutazione finora
- Cuestionario de Biología Sup Clase 5 - Jessica Minchala 3bgu BDocumento2 pagineCuestionario de Biología Sup Clase 5 - Jessica Minchala 3bgu BJessica MinchalaNessuna valutazione finora
- Lab10Documento10 pagineLab10Jaire MoroteNessuna valutazione finora
- UNIDAD QUÍMICA DE MASA PREU - FPDFDocumento2 pagineUNIDAD QUÍMICA DE MASA PREU - FPDFGerman MamaniNessuna valutazione finora
- Quimica Programa2013Documento23 pagineQuimica Programa2013Stephany AnReiiNessuna valutazione finora
- BioluminicenciaDocumento5 pagineBioluminicenciaMarina Ysabel Caceres MoranNessuna valutazione finora