Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Informe de Conductimetría y Potenciometria
Caricato da
Jorge Rosales0 valutazioniIl 0% ha trovato utile questo documento (0 voti)
272 visualizzazioni8 pagineInstrumental
Copyright
© © All Rights Reserved
Formati disponibili
PDF, TXT o leggi online da Scribd
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoInstrumental
Copyright:
© All Rights Reserved
Formati disponibili
Scarica in formato PDF, TXT o leggi online su Scribd
0 valutazioniIl 0% ha trovato utile questo documento (0 voti)
272 visualizzazioni8 pagineInforme de Conductimetría y Potenciometria
Caricato da
Jorge RosalesInstrumental
Copyright:
© All Rights Reserved
Formati disponibili
Scarica in formato PDF, TXT o leggi online su Scribd
Sei sulla pagina 1di 8
DETERMINACIÓN DE ÁCIDEZ TOTAL EN UNA MUESTRA DE
COMPOTA DE MANZANA – GERBER
POR TITULACIÓN POTENCIOMETRICA Y CONDUCTIMÉTRICA
Jorge Luis Rosales
Laboratorio de Química Analítica Instrumental – Departamento de Química
Facultad Experimental de Ciencias y Tecnología. Universidad de Carabobo
Profesores: José Jiménez y Daniel Pacheco.
Resumen
Las titulaciones potenciométricas y conductimétricas se realizan cuando no es posible la
detección del punto final, ya que no hay cambio de color (indicador). Para esta práctica, se
realizaron este tipo de titulaciones para determinar el porcentaje de acidez contenido en una
muestra de compota Heinz de pera. Para ello, se inició con el tratamiento de la muestra donde
se homogenizó en agua destilada y se trasvasó a un balón aforado llenando hasta la línea de
aforo. Posteriormente, se prepararon las soluciones como NaOH 0.01M por dilución y una
solución de ftalato ácido potásico (KPH) 0.01M, que se usó como patrón primario para la
estandarización del NaOH. Luego, se procedió con la titulación del ácido cítrico que es el
ácido predominante y utilizado como acidificante en la compota Heinz de pera. Utilizando
un pH-metro y un conductímetro, se midieron los valores de pH y la conductancia en cada
intervalo de adición de NaOH. Con estos valores, se realizaron las curvas de titulación
correspondientes a cada método, determinando los volúmenes equivalentes. Para finalizar,
se determinó la cantidad en gramos de ácido cítrico correspondiente a la alícuota de compota
y se obtuvo el porcentaje de acidez tanto por potenciometría y conductimetría de (0.0313 ±
0.0001) % y (0.0329 ± 0.0001) %, respectivamente.
Palabras claves: Titulación, Conductimetría, Potenciometría.
_________________________________________________________________________
INTRODUCCIÓN forma básica, se necesita al menos dos
unidades de pH para apreciar el cambio de
Tradicionalmente se han utilizado los
coloración de la solución. En la actualidad
indicadores para determinar el punto de
el avance tecnológico ha permitido que los
equivalencia en una valoración ácido-base.
alumnos puedan utilizar potenciómetros
Sin embargo, teniendo en cuenta la
de bajo coste y sea posible registrar
sensibilidad del ojo humano, en el mejor
fácilmente la variación del pH de la
de los casos cuando el color del indicador
disolución al ir añadiendo el agente
en la forma ácida es muy diferente al de la
valorante. La representación del pH frente
al volumen adicionado ilustra el proceso Experiencia n°2. Preparación de
de neutralización y permite una estimación soluciones.
muy precisa del punto final de la A partir de una solución de NaOH 0.1M,
valoración. mediante un proceso de dilución, se tomó
De igual manera, en el análisis cuantitativo una alícuota de 25ml para la preparación
son muy utilizadas las valoraciones de una solución de NaOH 0.01M.
conductimétricas. La conducción de una Seguidamente se pesaron (0.1021 ±
0.0001) g de ftalato ácido potásico en un
corriente eléctrica a través de una solución
beaker de 25ml, se disolvió con una
de un electrolito involucra la migración de
porción de agua destilada y se trasvasó a
especies cargada positivamente hacia el
un balón de (50 ± 0.05) ml llevando hasta
cátodo y especies cargadas negativamente la línea de aforo con agua destilada.
hacia el ánodo. Todos los iones
contribuyen al proceso de conducción, Experiencia n°3. Encendido de
pero la fracción de corriente transportada conductímetro y pH-metro.
por cada especie está determinada por su Para el uso de los equipos, se revisó que
concentración relativa y su movilidad ambos estuvieran en buenas condiciones.
inherente en el medio. Por otra parte, las El conductímetro tenía que poseer una
titulaciones conductimétricas en las que corriente estable, donde no se observaran
las mediciones de la conductancia se usan cambios radicales de valores. Por otra
para indicar el punto final de una reacción parte, se verificó que el electrodo del pH-
se puede aplicar a la determinación de una metro estuviera siempre húmedo ya sea, en
variedad de sustancias. una solución amortiguadora de pH
conocido o en una solución saturada de
METODOLOGÍA KCl.
Experiencia n°1. Preparación de la Experiencia n°4. Estandarización de la
muestra de compota de pera – Heinz. solución de NaOH 0.01M.
Se pesaron (15,0397 ± 0,0001) g de la Se trasvasaron, 10ml de la solución de
muestra de compota de pera - Heinz en un ftalato ácido potásico a una fiola y se
vaso de precipitado de 250ml. Luego, al adicionaron 3 gotas de fenolftaleína. En la
disolver en 50ml de agua destilada, se bureta, se colocó la solución de NaOH
agitó hasta homogenizar lo suficiente. Se 0.01M hasta la línea de aforo. Antes de
realizó un tratamiento térmico, calentando empezar la titulación se midió el pH de la
por unos 30 minutos aproximadamente. solución y se anotó el valor.
Para finalizar, mediante la filtración por Posteriormente se comenzó a titular, hasta
gravedad, se retiró todos los componentes observar un cambio de coloración en la
solidos presentes. La solución filtrada, se solución (de incoloro a rosado). Este
trasvasó a un balón aforado de 250ml y se proceso de realizó por duplicado.
completó hasta la línea de aforo con agua
destilada.
Experiencia n°5. Titulación Habitualmente, la titulación
potenciométrica y conductimétrica de la potenciométrica y conductimétrica se
compota realiza cuando no es posible la detección
del punto final de una valoración
Con el NaOH, previamente estandarizado,
empleando un indicador visual. Estos se
se tituló la compota agregando un volumen
consideran uno de los métodos más
de titulante sucesivo de 0.5 ml.
exactos, porque el potencial y la
Seguidamente, entre cada adición de
conductancia siguen el cambio real de la
titulante se agitaba la solución un agitador
actividad (titulación) y el punto final
magnético y se colocaban los electrodos
coincide directamente con el punto de
tanto del conductímetro como el de pH-
equivalencia [2].
metro dentro de la solución. Se anotaban
los valores obtenidos y se procedía con la En la práctica, se inició con la
titulación. La titulación se continuó hasta estandarización del NaOH 0.01M con una
observar un cambio notable en la solución patrón de Ftalato ácido potásico
conductancia y en el pH. Este proceso de (KPH) 0.01M. El ftalato es una sal con un
realizó por triplicado. hidrógeno ligeramente ácido, y se utiliza a
menudo como patrón primario en
ANÁLISIS DE RESULTADOS
valoración ácido-base porque es sólido,
La compota es un postre casero que estable al aire, por lo que es fácil pesar con
tradicionalmente esta hecho de manzana, precisión y además, no es higroscópico.
pero se hace igualmente de distintas frutas Para que la estandarización fuera más
(pera, melocotón, albaricoque, frutas rojas, rápida, se adicionaron 3 gotas de
entre otras) y posee una textura bastante fenolftaleína, a la solución de ftalato, que
espesa. Normalmente, en los estudios posee un punto de viraje entre 8.2 (rosado
potenciométricos y conductimétricos de muy claro) – 10 (magenta-rosado) [3]
soluciones no se requieren analizar (Reacción 1).
grandes procesos de preparaciones de
muestras como en el caso de los métodos
espectrofométricos, como por ejemplo en
la determinación de hierro por UV-
Visible. Estas, se pueden analizar en gran
cantidad de muestras líquidas y gaseosas
[1]. En el caso de las sólidas o muy
Figura 1A. Reacción 1. Ftalato ácido potásico
espesas, como la compota de pera, se con NaOH.
pueden preparar en solución y luego ser
estudiadas [1]. Por lo tanto, se realizó un Como se utilizaba NaOH, se observaría el
pre-tratamiento a la muestra de compota, punto final al observar el cambio de
donde se disolvió en agua destilada y se coloración. En este punto, se introducía el
filtró la misma para retirar el exceso de electrodo de vidrio del pH-metro para
componentes en estado sólido, como la obtener el valor de pH correspondiente a
pulpa. ese punto, dando un pH = 9.5 para ambas
estandarizaciones ya que se realizaron por
duplicado. Luego de estandarizar el NaOH
0.01M, se procedió con la titulación de la debida a los 3 grupos, carboxilos-COOH
compota de pera marca Heinz, midiendo que pueden perder un protón en las
en cada adición de titulante (NaOH) tanto soluciones (pKa1= 3.13, pKa2=4.76 y
el pH como su conductancia, con la pKa3=6.4) y cuando esto sucede, se
finalidad de determinar la acidez total. La produce el ión citrato que son buenos
reacción ocurrida se representa en reacción controladores del pH en soluciones básicas
2. [4].
C6H8O7 (ac) + 3NaOH (ac) = C6H5O7Na3 Al titular la compota Heinz de sabor pera,
(ac) + H2O (l) (Reacción 2). se obtuvieron los valores de pH y se
graficaron con respecto al volumen del
Generalmente para analizar la acidez de
titulante (NaOH) utilizado. (Figuras 2A,
una muestra que contiene trazas de frutas
3A, 4A. Hoja de cálculo, Titulación
es suficiente determinar la acidez titulable
Potenc. Compota). Como se puede
del ácido predominante [4]. La compota
observar, las curvas de titulación son
analizar es de pera, por lo que es de esperar
semejantes a la esperada a una titulación
que el ácido predominante sea el ácido
acido- base (Figura 1b).
málico (C4H6O5), que es un ácido de
origen natural que está presente en muchos
alimentos vegetales y sobre todo en frutas
como la manzana, pera, plátanos, entre
otros [5]. Sin embargo, este ácido llega ser
el ácido predominante si la muestra
analizar es la fruta directamente. En Figura 1b. Curva de titulación de ácido cítrico y
cambio, en productos procesados de frutas NaOH en un jugo de limón.
como la compota, el ácido predominante
es el ácido cítrico (C6H8O7, también Sin embargo, la concentración de ácido
denominado E-330, a nivel industrial) que cítrico mostrada en la figura 1 es mayor,
es uno de los aditivos más utilizados por la por lo que fue necesario un mayor
industria alimentaria, en dulces (como la volumen de NaOH para poder titularla. En
compota) se utiliza como acidulante y cambio, el ácido cítrico contenido en la
regulador de pH para lograr una óptima compota de pera es mucho menor pero se
gelificación [5]. logra observar la misma tendencia gráfica.
Los puntos volumétricos tomados para las
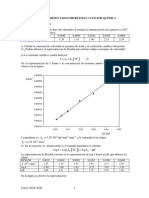
Para nuestro caso en particular, al titular el figuras 2A, 3A y 4A fueron escasos, lo que
ácido cítrico por potenciometría se debería hace que la curva de titulación no sea lo
obtener la figura 1b. En la curva de más pronunciada posible. A pesar de esto,
valoración del ácido cítrico, se gráfica el fue posible construir la curva de titulación
pH de este en función del volumen observando su punto de inflexión, que
titulante de NaOH 0.01M agregado. Se indicaba el punto de equivalencia. Para
observó que el pH aumentaba lograr determinar cuantitativamente el
progresivamente a medida que se le agrega punto de equivalencia, se aplicó el método
el NaOH. El salto de pH que se observa de la primera y segunda derivada. Para
corresponde a la neutralización total de los ΔpH
ello, se calculó la primera derivada
tres iones H+. La acidez del ácido cítrico es ΔV
realizando una diferencia entre los valores volumen, afectará la conductancia de la
de pH obtenidos y los volúmenes de solución dependiendo de si ocurren o no
titulante: reacciones química [2]. Si ocurre una
𝚫𝐩𝐇 (𝐩𝐇𝟐−𝐩𝐇𝟏)
reacción iónica, la conductancia puede
= (Ec. 1) aumentar o disminuir; en efecto, con el
𝚫𝐕 (𝐕𝟐−𝐕𝟏)
agregado de una base o ácido fuerte. Para
Y graficando, como se muestra en las este caso, al titular ácido cítrico-hidróxido
figuras 2B, 3B y 4B (Hoja de cálculo, de sodio, estamos en presencia de una
Titulación Potenc. Compota). El punto reacción ácido débil-base fuerte, el punto
máximo observado en estas gráficas, de equivalencia se evidencia a un pH≈7
reflejó el punto de equivalencia. No (Figura 1) y en el mismo la disolución es
obstante, se aplicó también el método de la básica, al sufrir hidrólisis el anión citrato
Δ2pH
segunda derivada , donde se obtenían de la sal, pues proviene de un ácido débil
Δ2V
los valores por diferencia de la primera y una base fuerte [2] (FIGURA).
derivada (Tablas 5, 6 y 7. Hoja de En la reacción 3, entre (C6H5O7)3- y H+, los
cálculo, Titulación potenc. Compota). iones de H+ son reemplazados por Na+
En este caso la representación gráfica de la durante la titulación. A medida que avanza
segunda derivada con respecto al volumen la titulación, la conductancia aumenta
del titulante debe alcanzar valor cero (0)
(Tablas 10, 11 y 12. Hoja de cálculo.
(corte con el eje X) en el punto de Titulación conduct compota) y esto es
equivalencia de la valoración (Figuras debido a que la conductancia de Na+ es
2C, 3C y 4C. Hoja de cálculo, Titulación mayor que la conductancia de H+ [2].
potenc. Compota). Para determinar con
mayor precisión el volumen de [(C6H5O7)3-].[H+] + [Na+].[OH-]
equivalencia, se seleccionaron los dos (reacción 3. Reacción iónica)
puntos que hacen corte con el eje X
El punto final, se determina en un gráfico
(Figuras 2D, 3D y 4D. Hoja de cálculo,
de conductancia o conductancia específica
Titulación potenc. Compota) obteniendo
en función al volumen del titulante
la pendiente y la intersección con el eje Y,
agregado (NaOH). Estas curvas de
se calculó el corte con el eje X, que
titulación tienen una variedad de formas,
representaba el volumen de equivalencia.
dependiendo del sistema químico. En
Con el volumen promedio de los general, están caracterizadas por porciones
volúmenes de equivalencias, determinados de líneas rectas con pendientes diferentes
en las curvas de titulación por el método a cada lado del punto de equivalencia [2]
de la segunda derivada, se logró calcular el (Figuras 5A, 5B y 5C. Hoja de cálculo.
% de acidez en la compota Heinz de pera Titulación conduct compota).
(Ec. 2) obteniendo un porcentaje de
Las mediciones conductimétricas ofrecen
(0.0313 ± 0.0001) %.
un medio adecuado para la determinación
En las titulaciones conductimétricas, el de puntos finales en titulaciones. Para
agregado de un electrolito a una solución establecer el punto final conductimétrico,
de otro electrolito, bajo condiciones que no se necesitaron suficientes mediciones
producen un cambio apreciable en el experimentales para definir la curva de
titulación. Se grafican los datos de éxito para titulaciones basadas en
conductancia en función del volumen de equilibrios relativamente desfavorables.
reactivo titulante. Posteriormente, se
CONCLUSIONES
extrapolan las dos porciones lineales y se
obtiene el punto de equivalencia en la Mediante curvas de titulaciones
intersección de ambas rectas (y1 = y2) [2] potenciométricas y
(Figuras 5A, 5B y 5C. Hoja de cálculo. conductimétricas, se determinó el
Titulación conduct compota). Al realizar volumen de equivalencia para
los cálculos, se obtuvo un volumen posteriormente determinar el % de
promedio y con ello el % de acidez de la acidez en la compota Heinz de
compota obteniendo un valor de (0.0329 ± pera.
0.0001) %. El porcentaje obtenido por la
Debido a que las reacciones no son titulación potenciométrica y
absolutamente completas, las curvas de conductimétrica fue, (0.0313 ±
titulación conductimétrica muestran 0.0001) % y (0.0329 ± 0.0001) %
invariablemente desviaciones con relación respectivamente.
a la linealidad rigurosa en la región del El ácido cítrico es el ácido
punto de equivalencia. Las regiones curvas predominante en la compota
se vuelven pronunciadas cuando la Heinz de pera, que es utilizado
reacción se hace menos favorable y como acidificante.
cuando la reacción resulta más diluida [2]. REFERENCIAS BIBLIOGRÁFICAS
Las porciones lineales se definen mejor a
través de mediciones suficientemente [1] – Valencia, Lina. Titulación
alejadas del punto de equivalencia para potenciométrica. Universidad Católica
que el efecto de los iones comunes impulse Andrés Bello, Guayana. 01-02-05, pág. 2.
la reacción más cerca de completarse; las [2] – Brunotti, Carlos y De Napoli,
mediciones en la proximidad del punto de Hernán. Titulación conductimétrica. Pág.
equivalencia, a diferencia de los métodos 6, 7 y 9. 06-05-16
potenciométricos, no tienen ningún
significado [6]. [3] – Chang, Raymond. Química,
equilibrios ácidos – bases y equilibrios de
Ciertamente, debido a la hidrólisis, solubilidad. Editorial McGraw Hill. 2010.
disociación o solubilidad del producto de Pág. 734-735.
reacción, los valores de la conductividad
medida en las cercanías del punto de [4] – Pittaluga, Augustin.Titulaciones
equivalencia no tienen sentido en la Potenciométricas. Instituto Superior de
construcción del gráfico, dado que la curva Buceo. Pág. 3
será redondeada en una o ambas ramas [6]. [5] – Riesgo, Alberto-Calderón, Cristina.
En contraste con los métodos Tu Mejor Versión, Nutrición y Dietética.
potenciométricos, que dependen de Disponible en:
observaciones en condiciones en las que la blog.nutritienda.com/ácidos/ última
reacción es menos completa, el análisis visita: 16/10/19
conductimétrico puede emplearse con
[6] – Fisconia, Marcos. Conductividad http://sgpwe.izt.uam.mx/files/users/uami/jp
Eléctrica en soluciones iónicas. n/Q._Inorganica/LABORATORIO/5_Conductiv
Laboratorio de química Inorgánica. idades_Electricas_en_Soluciones.pdf última
Disponible en: visita: 16/10/19
CÁLCULOS TÍPICOS
a) Determinación del volumen de alícuota para solución de NaOH 0.01M
(Dilución)
C1.V1 = C2.V2 (ec. 2)
𝑪𝟐. 𝑽𝟐
𝑪𝟏 =
𝑪𝟏
C1 = Concentración de NaOH 0.1M
V1 = Volumen de la alícuota a tomar (determinar)
C2 = Concentración de NaOH 0.01M
V2 = Volumen del NaOH de 250ml
b) Determinación de la masa de ftalato ácido potásico 0.01M
𝟎. 𝟎𝟏𝒎𝒐𝒍 𝟓𝟎𝒎𝒍 𝟏𝑳 𝒈𝒇𝒕𝒂𝒍𝒂𝒕𝒐
.( ).( ) (𝟐𝟎𝟒. 𝟐𝟑 )
𝑳 𝟏 𝟏𝟎𝟎𝟎𝒎𝒍 𝟏𝒎𝒐𝒍
c) Determinación de la concentración de ácido cítrico, utilizando los volúmenes
equivalentes obtenidos por potenciometría y conductimetría
Utilizando la ecuación 2. Se sustituyen los valores del volumen y se determinan las
concentraciones del ácido cítrico para cada método.
d) Para la determinación de los volúmenes de equivalencias, tanto para
potenciometría como conductimetría:
Se tomaban las ecuaciones de las rectas de cada gráfica y se igualaban despejando
x, que sería el volumen de equivalencia.
y1 = b1x + a1 ; y2 = b2x+ a2; igualando y1 = y2
b1x + a1 = b2x+ a2
𝒂𝟐 − 𝒂𝟏
𝒙=
𝒃𝟏 − 𝒃𝟐
e) Determinación del porcentaje de acidez:
𝒈 á𝒄𝒊𝒅𝒐 𝒄í𝒕𝒓𝒊𝒄𝒐 (𝒆𝒙𝒑𝒆𝒓𝒊𝒎𝒆𝒏𝒕𝒂𝒍𝒆𝒔)
%𝑨𝒄𝒊𝒅𝒆𝒛 = 𝒙𝟏𝟎𝟎 (ec. 3)
𝒈 𝒅𝒆 𝒎𝒖𝒆𝒔𝒕𝒓𝒂 𝒑𝒆𝒔𝒂𝒅𝒐
(Revisar Hoja de cálculo. Datos y cálculos de concentraciones)
Potrebbero piacerti anche
- Técnicas analíticas básicas: En el control de la calidad del agua según normatividadDa EverandTécnicas analíticas básicas: En el control de la calidad del agua según normatividadNessuna valutazione finora
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSDa EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSValutazione: 4.5 su 5 stelle4.5/5 (7)
- Manual S4aDocumento29 pagineManual S4aJesus Ormachea100% (1)
- Tutorial Caesar II TraducidoDocumento36 pagineTutorial Caesar II Traducidopablopasqualini18100% (2)
- Informe de Extraccion de CafeinaDocumento11 pagineInforme de Extraccion de CafeinaLiz GoCaNessuna valutazione finora
- Importancia de Los Costos en La Toma deDocumento4 pagineImportancia de Los Costos en La Toma deCeledonio Hernandez SanchezNessuna valutazione finora
- Lab - Volumetria ComplexometricaDocumento4 pagineLab - Volumetria ComplexometricaValentina Javiera Pinto Barreda50% (2)
- Informe de Laboratorio - Determinación de Fosfatos en BebidasDocumento8 pagineInforme de Laboratorio - Determinación de Fosfatos en BebidasFelipe ValenzuelaNessuna valutazione finora
- Practica Metodo NioshDocumento10 paginePractica Metodo NioshAudrey ArzateNessuna valutazione finora
- ProblemasDocumento2 pagineProblemasRolando Torres Pacheco0% (1)
- Laboratorio Sistemas TernariosDocumento19 pagineLaboratorio Sistemas Ternariosgustavo alzate patiñoNessuna valutazione finora
- Informe Pka Rojo de MetiloDocumento8 pagineInforme Pka Rojo de MetilomichNessuna valutazione finora
- Resultados y Análisis de Resultados - Espectrofotometría y PKaDocumento11 pagineResultados y Análisis de Resultados - Espectrofotometría y PKaJorge Luis FigueroaNessuna valutazione finora
- Taller 10 PH Acidos Poliproticos-2Documento2 pagineTaller 10 PH Acidos Poliproticos-2Andzhiita SaampeerNessuna valutazione finora
- Fico 2Documento20 pagineFico 2Adrian Quispe100% (1)
- PH de Mezcla de AcidosDocumento6 paginePH de Mezcla de AcidosDaniel PrepaNessuna valutazione finora
- INFORME LAB 7 TitulacionesDocumento11 pagineINFORME LAB 7 TitulacionesIsabella GiraldoNessuna valutazione finora
- Practica Acidos PoliproticosDocumento5 paginePractica Acidos PoliproticosJulio Cesar Jimenez BautistaNessuna valutazione finora
- Método QuelatométricoDocumento3 pagineMétodo QuelatométricoSharon Yanireth Castro PaganNessuna valutazione finora
- Informe 4. Titulaciones de Precipitación FINALxDocumento5 pagineInforme 4. Titulaciones de Precipitación FINALxCamiloNessuna valutazione finora
- Práctica 8 - Volumetría RedoxDocumento3 paginePráctica 8 - Volumetría RedoxLady GiraldoNessuna valutazione finora
- Redox Volumetria InformeDocumento12 pagineRedox Volumetria InformeAndrea HernandezNessuna valutazione finora
- LAB #2-3 Determinación Gravimétrica de CalcioDocumento6 pagineLAB #2-3 Determinación Gravimétrica de CalcioAna Soffia Gomez AriasNessuna valutazione finora
- Informe 2. Calibración Ley de BeerDocumento6 pagineInforme 2. Calibración Ley de BeerPau Toro100% (1)
- 09-Oxido-Reducción y AcidezDocumento14 pagine09-Oxido-Reducción y AcidezBorisJeanUsuriagaNessuna valutazione finora
- Informe 4. Valoracion PotenciometricaDocumento7 pagineInforme 4. Valoracion PotenciometricaAmarilla TCNessuna valutazione finora
- Analisis Cualitativo Marcha de CationesDocumento10 pagineAnalisis Cualitativo Marcha de CationesAna C. Ramirez0% (1)
- Informe N-5Documento4 pagineInforme N-5miguel concha ccanchiNessuna valutazione finora
- Determinación de Hierro (Practica Nº3) IMPRIMIRDocumento8 pagineDeterminación de Hierro (Practica Nº3) IMPRIMIRJean Pierre Cirilo SosaNessuna valutazione finora
- Analisis Elemental CualitativoDocumento10 pagineAnalisis Elemental CualitativoJulieth BecerraNessuna valutazione finora
- Informe de Valoración ConductométricaDocumento17 pagineInforme de Valoración ConductométricaNicole Melly HuertaNessuna valutazione finora
- Los Indicadores y Su Uso en El Analisis Quimico 3Documento8 pagineLos Indicadores y Su Uso en El Analisis Quimico 3rolalvgutNessuna valutazione finora
- Reporte Titulación Del Ácido Fuerte y Base FuerteDocumento9 pagineReporte Titulación Del Ácido Fuerte y Base FuerteErnesto Sanchez Soberane50% (2)
- Practica de ExtraccionDocumento26 paginePractica de ExtraccionJacqueline Velázquez JuarezNessuna valutazione finora
- Factores Que Deben Tomarse en Cuenta Al Momento de Elegir Un Método Analítico y Exponga Cada Factor.Documento4 pagineFactores Que Deben Tomarse en Cuenta Al Momento de Elegir Un Método Analítico y Exponga Cada Factor.Carolinamcr95Nessuna valutazione finora
- Reporte TermoquimicaDocumento8 pagineReporte TermoquimicaDiianaLauraMelendezNessuna valutazione finora
- Informe 3 Compuestos de CoordinacionDocumento5 pagineInforme 3 Compuestos de CoordinacionJoshua ShannonNessuna valutazione finora
- Capacidad Calorífica de Un CalorímetroDocumento6 pagineCapacidad Calorífica de Un Calorímetroソーダ エドゥアルドNessuna valutazione finora
- Examen-QA-06 02 2019Documento1 paginaExamen-QA-06 02 2019Noe FerrarisNessuna valutazione finora
- Informe Metodos Instrumentales de Analisis QuimicoDocumento4 pagineInforme Metodos Instrumentales de Analisis QuimicoGustavo Encina TroncosoNessuna valutazione finora
- CURVA TITULACION NH3 HCLDocumento2 pagineCURVA TITULACION NH3 HCLArmando MoraNessuna valutazione finora
- Método de Las Tangentes para La Determinación Del Punto de Final en Valoraciones PotenciométricasDocumento7 pagineMétodo de Las Tangentes para La Determinación Del Punto de Final en Valoraciones PotenciométricasAlejandro BritoNessuna valutazione finora
- Solucion Leccion 6Documento15 pagineSolucion Leccion 6DanielNessuna valutazione finora
- Extraccion Cafeina y Sintesis de Salicilato de IsoamiloDocumento2 pagineExtraccion Cafeina y Sintesis de Salicilato de IsoamiloHenry CarterNessuna valutazione finora
- Preparacion y Estandarizacion de SolucionesDocumento5 paginePreparacion y Estandarizacion de SolucionesErzaNessuna valutazione finora
- Calor Diferencial de Una Solución de Ácido BenzoicoDocumento15 pagineCalor Diferencial de Una Solución de Ácido BenzoicoAlejandro CarvelliNessuna valutazione finora
- Informe 1Documento26 pagineInforme 1Tatiana RodríguezNessuna valutazione finora
- Explicación Procedimiento YodometríaDocumento6 pagineExplicación Procedimiento YodometríaJulio Otarola Jimenez100% (2)
- Bombeo de Protones en Levaduras y Sus Procesos InhibitoriosDocumento8 pagineBombeo de Protones en Levaduras y Sus Procesos InhibitoriosDavid Colorado VegaNessuna valutazione finora
- Aplicaciones de Las Titulaciones de Neutralización (C)Documento7 pagineAplicaciones de Las Titulaciones de Neutralización (C)Necroz182100% (1)
- Practica 7y8 de Lab. Analitica.Documento21 paginePractica 7y8 de Lab. Analitica.FrankAbarcaNessuna valutazione finora
- Volumetria de NeutralizacionDocumento46 pagineVolumetria de NeutralizacionBruno ValverdeNessuna valutazione finora
- Informe - Valoración Acido Cítrico en Bebida ComercialDocumento14 pagineInforme - Valoración Acido Cítrico en Bebida ComercialAlexander Omar Capcha RiosNessuna valutazione finora
- Informe No. 9 - TITULACIONES REDOX MEDIANTE POTENCIOMETRÍA - OutputDocumento11 pagineInforme No. 9 - TITULACIONES REDOX MEDIANTE POTENCIOMETRÍA - OutputVanessa SánchezNessuna valutazione finora
- Determinación de La Constante de Equilibrio de Un IndicadorDocumento5 pagineDeterminación de La Constante de Equilibrio de Un IndicadorMaryjoseLeónNessuna valutazione finora
- Informe RefractometriaDocumento5 pagineInforme RefractometriaStefanny GuzmánNessuna valutazione finora
- Práctica 5 - Método MohrDocumento10 paginePráctica 5 - Método MohrJorgeLuisFR7Nessuna valutazione finora
- Determinación de La Constante de EquilibrioDocumento12 pagineDeterminación de La Constante de EquilibrioAndrea GonzálezNessuna valutazione finora
- GUIA DE PHDocumento2 pagineGUIA DE PHSilva Miguel ValeriaNessuna valutazione finora
- Mecanismo de Reacción Nylon 6,6Documento10 pagineMecanismo de Reacción Nylon 6,6ايفونكهرلمذبذبNessuna valutazione finora
- Volumetria de NeutralizacionDocumento14 pagineVolumetria de NeutralizacionEsperanza Mendoza100% (1)
- Ejercicios Parcial I Del Dos 2022Documento4 pagineEjercicios Parcial I Del Dos 2022Andres RamNessuna valutazione finora
- Informe Titulacion (TITULACION-ÁCIDO-BASE, MEDIDA DE PH)Documento6 pagineInforme Titulacion (TITULACION-ÁCIDO-BASE, MEDIDA DE PH)Juan Pablo Arias40% (5)
- Experiencia de Titulación Ácido - BaseDocumento8 pagineExperiencia de Titulación Ácido - BaseJorge RuizNessuna valutazione finora
- Informe de Conductancia de ElectrolitosDocumento5 pagineInforme de Conductancia de ElectrolitosJorge RosalesNessuna valutazione finora
- Determinación Del Área Específica de Un Sólido Mediante La Isoterma de Adsorción de Lagmuir Del Ácido Acético Del Carbón ActivadoDocumento4 pagineDeterminación Del Área Específica de Un Sólido Mediante La Isoterma de Adsorción de Lagmuir Del Ácido Acético Del Carbón ActivadoJorge RosalesNessuna valutazione finora
- Saponificación de Éster OrgánicoDocumento8 pagineSaponificación de Éster OrgánicoJorge RosalesNessuna valutazione finora
- Preparación Del Complejo de CobaltoDocumento10 paginePreparación Del Complejo de CobaltoJorge RosalesNessuna valutazione finora
- Informe de ADNDocumento2 pagineInforme de ADNJorge RosalesNessuna valutazione finora
- Informe de ADNDocumento4 pagineInforme de ADNJorge RosalesNessuna valutazione finora
- Informe de EnzimasDocumento8 pagineInforme de EnzimasJorge RosalesNessuna valutazione finora
- Informe de Servicio ComunitarioDocumento4 pagineInforme de Servicio ComunitarioJorge RosalesNessuna valutazione finora
- Informe de ADNDocumento4 pagineInforme de ADNJorge RosalesNessuna valutazione finora
- Estudio Del Comportamiento Químico de Los Elementos Boro y AluminioDocumento10 pagineEstudio Del Comportamiento Químico de Los Elementos Boro y AluminioJorge RosalesNessuna valutazione finora
- Informe de Complejos de CobreDocumento6 pagineInforme de Complejos de CobreJorge RosalesNessuna valutazione finora
- Titulación Por Formación de ComplejosDocumento15 pagineTitulación Por Formación de ComplejosJorge RosalesNessuna valutazione finora
- Biosíntesis de ProteínasDocumento4 pagineBiosíntesis de ProteínasJorge RosalesNessuna valutazione finora
- Aplicación Cromatografica en ProteínasDocumento4 pagineAplicación Cromatografica en ProteínasJorge RosalesNessuna valutazione finora
- Análisis Multivariante Empresa 2 PDFDocumento10 pagineAnálisis Multivariante Empresa 2 PDFJorge RosalesNessuna valutazione finora
- Informe de Titulación Fotométrica de Calcio en Agua de Pozo CORREGIDODocumento9 pagineInforme de Titulación Fotométrica de Calcio en Agua de Pozo CORREGIDOJorge RosalesNessuna valutazione finora
- Informe de Titulación Fotométrica de Calcio en Agua de PozoDocumento8 pagineInforme de Titulación Fotométrica de Calcio en Agua de PozoJorge RosalesNessuna valutazione finora
- Determinación de Ca CORREGIDO PDFDocumento9 pagineDeterminación de Ca CORREGIDO PDFJorge RosalesNessuna valutazione finora
- Informe de InstrumentalDocumento9 pagineInforme de InstrumentalJorge RosalesNessuna valutazione finora
- Determinación Del Pka Del Azul de Bromotimol Por EspectrofotometríaDocumento8 pagineDeterminación Del Pka Del Azul de Bromotimol Por EspectrofotometríaJorge RosalesNessuna valutazione finora
- Ensayo de Alta Gerencia EmpresarialDocumento4 pagineEnsayo de Alta Gerencia EmpresarialJorge RosalesNessuna valutazione finora
- Lenguaje de ProgramaciónDocumento5 pagineLenguaje de ProgramaciónYordan Sullca PalominoNessuna valutazione finora
- Problemas FlujoDocumento12 pagineProblemas FlujoJackNessuna valutazione finora
- Catalogo DepuradorasDocumento37 pagineCatalogo DepuradorasPaco PorrasNessuna valutazione finora
- 20142sfict034262 1 PDFDocumento52 pagine20142sfict034262 1 PDFByron100% (1)
- IC-Sem7-S14-Recipientes A PresionDocumento13 pagineIC-Sem7-S14-Recipientes A PresionBeltran GutierrezNessuna valutazione finora
- Tesltar Bombas de Vacio 2f 3 2f 10Documento1 paginaTesltar Bombas de Vacio 2f 3 2f 10Anonymous ZLmk6mPPnNessuna valutazione finora
- Atsa Del Sureste Catalogo Completo PDFDocumento159 pagineAtsa Del Sureste Catalogo Completo PDFOmar Perez SaldivarNessuna valutazione finora
- Informe Adsorcion 16Documento21 pagineInforme Adsorcion 16Angélica MontalvoNessuna valutazione finora
- Curso Refractario Cemento2Documento17 pagineCurso Refractario Cemento2keith ledezmaNessuna valutazione finora
- Infografía Final PDFDocumento1 paginaInfografía Final PDFDana SierraNessuna valutazione finora
- FT Per Pox 31 GelDocumento2 pagineFT Per Pox 31 Gelstark7Nessuna valutazione finora
- TEMA 2 - 2 Fatiga v3Documento61 pagineTEMA 2 - 2 Fatiga v3Ayrton Portilla EstradaNessuna valutazione finora
- 8.-Gestión de Simulacros - Nov2020Documento18 pagine8.-Gestión de Simulacros - Nov2020Shanti Adela Rueda MoscosoNessuna valutazione finora
- Sistema Distribución Vapor, PARTE 1Documento33 pagineSistema Distribución Vapor, PARTE 1Sergio RafaelNessuna valutazione finora
- Laboratorio - INSTALACIONES ELECTRICASDocumento4 pagineLaboratorio - INSTALACIONES ELECTRICASAndres LopezNessuna valutazione finora
- Examen de FisicaDocumento4 pagineExamen de FisicaDiegoNessuna valutazione finora
- Planimetria Con TeodolitoDocumento5 paginePlanimetria Con Teodolitojulio032125Nessuna valutazione finora
- Ficha Nemotecnica C.ADocumento2 pagineFicha Nemotecnica C.ANicole Stefany Mocha TorresNessuna valutazione finora
- Relación de Protocolos de PruebasDocumento2 pagineRelación de Protocolos de PruebasLady Robles MendozaNessuna valutazione finora
- VolvoDocumento3 pagineVolvoBarzola Soto OmarNessuna valutazione finora
- Punto 1 - Laura QuinteroDocumento3 paginePunto 1 - Laura QuinteroCamiloNessuna valutazione finora
- Curvas IDFDocumento3 pagineCurvas IDFFélix SantiagoNessuna valutazione finora
- Sistema PorticoDocumento5 pagineSistema PorticoRony Chavez CaceresNessuna valutazione finora
- Fti #005-2019-Gore - Puno-Potoni PDFDocumento15 pagineFti #005-2019-Gore - Puno-Potoni PDFivan tipula mamaniNessuna valutazione finora
- Cuadro Comparativo de Los Maestros de La CalidadDocumento1 paginaCuadro Comparativo de Los Maestros de La CalidadAlma Aragon MartinezNessuna valutazione finora
- Proyecto de Semana 2 Curso 1Documento6 pagineProyecto de Semana 2 Curso 1fsp443140Nessuna valutazione finora