Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
BBO
Caricato da
fabiolaCopyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
BBO
Caricato da
fabiolaCopyright:
Formati disponibili
La demanda biológica de oxígeno o demanda bioquímica de oxígeno (DBO) es un
parámetro que mide la cantidad de dioxígeno consumido al degradar la materia orgánica
de una muestra líquida.
Es la materia susceptible de ser consumida u oxidada por medios biológicos que contiene
una muestra líquida, disuelta o en suspensión. Se utiliza para medir propiamente el grado
de contaminación; normalmente se mide transcurridos cinco días de reacción (DBO5) y se
expresa en miligramos de oxígeno diatómico por litro (mg O2/l).
El método de ensayo se basa en medir el dioxígeno consumido por una
población microbiana en condiciones en las que se han inhibido los procesos
fotosintéticos de producción de dioxígeno en condiciones que favorecen el desarrollo de
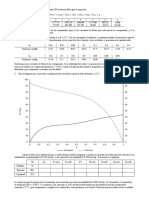
los microorganismos. La curva de consumo de dioxígeno suele ser al principio débil y
después se eleva rápidamente hasta un máximo sostenido, bajo la acción de la fase
logarítmica de crecimiento de los microorganismos.
Es un método aplicable en aguas continentales (ríos, lagos o acuíferos), aguas
negras, aguas pluviales o agua de cualquier otra procedencia que pueda contener una
cantidad apreciable de materia orgánica. Este ensayo es muy útil para la apreciación del
funcionamiento de las estaciones depuradoras.
No es aplicable, sin embargo, a las aguas potables, ya que al tener un contenido tan bajo
de materia oxidable la precisión del método no sería adecuada. En este caso se utiliza el
método de oxidabilidad con permanganato de potasio.
Según McKinney (1962), «El test de la DBO fue propuesto por el hecho de que
en Inglaterra ningún curso de agua demora más de cinco días en desaguar (desde su
nacimiento a su desembocadura). Así la DBO es la demanda máxima de dioxígeno que
podrá ser necesaria para un curso de agua inglés».
El método pretende medir, en principio, exclusivamente la concentración de contaminantes
orgánicos. Sin embargo, la oxidación de la materia orgánica no es la única causa del
fenómeno, sino que también intervienen la oxidación de los nitritos y de las sales
amoniacales, susceptibles de ser también oxidadas por las bacterias en disolución. Para
evitar este hecho se añade N-aliltiourea como inhibidor. Además, influyen las necesidades
de dioxígeno originadas por los fenómenos de asimilación y de formación de nuevas
células.
También se producen variaciones significativas según las especies de gérmenes, la
concentración de estos y su edad, y la presencia de bacterias nitrificantes y
de protozoos consumidores propios de dioxígeno que se nutren de las bacterias, entre
otras causas. Por todo ello este test ha sido constantemente objeto de discusión: sus
dificultades de aplicación, interpretación de los resultados y reproductibilidad se deben al
carácter biológico del método.
Índice
1Procedimiento de ensayo (método por dilución)
o 1.1Reactivos
o 1.2Procedimiento
o 1.3Expresión de los resultados
2Véase también
Procedimiento de ensayo (método por dilución)[editar]
El objeto del ensayo consiste en medir la cantidad de oxígeno diatómico disuelto en un
medio de incubación al comienzo y al final de un período de cinco días, durante el cual la
muestra se mantiene al abrigo del aire, a 20°C y en la oscuridad, para inhibir la eventual
formación de oxígeno por las algas mediante la fotosíntesis. Las condiciones de la medida,
en las que el agua a estudiar está en equilibrio con una atmósfera cuya presión y
concentración en oxígeno permanecen constantes, se acercan así a las condiciones reales
de la auto depuración de un agua residual.
Para su determinación se dispone de métodos de dilución y métodos instrumentales que
se derivan de métodos respirométricos que permiten seguir automáticamente la evolución
de la DBO en el curso de oxidación de las materias orgánicas contenidas en el agua.
Reactivos[editar]
Agua destilada
Agua residual urbana reciente
Solución fosfatos:
o Monohidrógenofosfato de sodio: 8,493 g
o Dihidrogenofosfato de potasio: 2,785 g
o Agua destilada hasta enrase a 1000 ml
Homogeneizar perfectamente la solución:
Solución de sulfato de magnesio de 20 g/l
Solución de cloruro de calcio de 25 g/l
Solución de cloruro de hierro de 1,5 g/l
Solución de cloruro de amonio de 2 g/l
Preparación del agua de dilución. Se prepara a partir de agua destilada introduciendo en
un recipiente:
Solución de fosfato…………………………5 ml
Solución de sulfato magnésico…………1 ml
Solución de cloruro cálcico………………1 ml
Solución de cloruro de hierro…………1 ml
Solución de cloruro amónico……………1 ml
Agua destilada hasta enrase a 1000 ml
Esta solución se mantiene a 20 °C y debe de airearse procurando evitar toda
contaminación por metales, materias orgánicas, oxidantes o reductores. Se detendrá la
aireación cuando la solución contenga 8 mg/l de oxígeno disuelto. Dejar en reposo durante
12 horas manteniendo el recipiente destapado. Añadir 5 ml de agua residual urbana por
litro de esta solución. Esta agua de dilución, deberá utilizarse dentro de las 24 horas
siguientes a su preparación.
Potrebbero piacerti anche
- UF1671 - Mantenimiento del entorno de plantas de tratamiento de agua y plantas depuradorasDa EverandUF1671 - Mantenimiento del entorno de plantas de tratamiento de agua y plantas depuradorasValutazione: 5 su 5 stelle5/5 (1)
- Mediciones de Carbono y OxigenoDocumento13 pagineMediciones de Carbono y OxigenoAnny EspinaNessuna valutazione finora
- Demanda Biológica de OxígenoDocumento3 pagineDemanda Biológica de OxígenoBobNessuna valutazione finora
- DBODocumento1 paginaDBOKarenAlorNessuna valutazione finora
- N AliltioureaDocumento2 pagineN AliltioureaFabian GomezNessuna valutazione finora
- Dbo UncDocumento6 pagineDbo UncWily ChavezNessuna valutazione finora
- Qué Es La DqoDocumento3 pagineQué Es La DqoEdwin Steven Romero RojasNessuna valutazione finora
- Resumen DBO, DQO, Caracteristicas de Aguas ResidualesDocumento3 pagineResumen DBO, DQO, Caracteristicas de Aguas ResidualesSandra ValeriaNessuna valutazione finora
- Demanda Bioquimica Del OxigenoDocumento19 pagineDemanda Bioquimica Del OxigenowillianNessuna valutazione finora
- Determinación de DBO-5Documento2 pagineDeterminación de DBO-5Joahan Anderson Estela Nuñez50% (2)
- Demanda Biológica de Oxígeno (Dbo)Documento3 pagineDemanda Biológica de Oxígeno (Dbo)Giovani QuirogaNessuna valutazione finora
- Demanda Biológica ODocumento7 pagineDemanda Biológica OMayli Milla AlegreNessuna valutazione finora
- DboDocumento4 pagineDboVictor Guzman PretellNessuna valutazione finora
- DBO-Microflora de Aguas ResidualesDocumento29 pagineDBO-Microflora de Aguas ResidualesRamón KyriosNessuna valutazione finora
- Guía de Laboratorio No. 5 OD y DBODocumento8 pagineGuía de Laboratorio No. 5 OD y DBOJuan Carlos SanabriaNessuna valutazione finora
- Lab4 DboDocumento16 pagineLab4 DboCarmen Sandoval33% (3)
- Universidad Nacional Del Santa Facultad de Ingeniería E. A. P. AgroindustrialDocumento15 pagineUniversidad Nacional Del Santa Facultad de Ingeniería E. A. P. AgroindustrialDannika SaavedraNessuna valutazione finora
- Determinacion de La Demanda Bioquímica de Oxígeno A Los 5 DíasDocumento3 pagineDeterminacion de La Demanda Bioquímica de Oxígeno A Los 5 DíasPatrizia Secce PerezNessuna valutazione finora
- Demanda Bioquimica de OxigenoDocumento18 pagineDemanda Bioquimica de OxigenoSamir SachaNessuna valutazione finora
- Método de Ensayo de Biodegradabilidad-EstudioDocumento3 pagineMétodo de Ensayo de Biodegradabilidad-Estudiohoneybee15Nessuna valutazione finora
- Demanda Bioquimica de OxigenoDocumento7 pagineDemanda Bioquimica de OxigenolobachevsNessuna valutazione finora
- Determinacion DboDocumento6 pagineDeterminacion DboZaimis Cancino DguezNessuna valutazione finora
- Demanda-Bioquimica-Del-Oxigeno TodoDocumento44 pagineDemanda-Bioquimica-Del-Oxigeno TodoLeonardo RuaroNessuna valutazione finora
- DBO5Documento17 pagineDBO5waldemar alejosNessuna valutazione finora
- Laboratorio #9 DBO5Documento5 pagineLaboratorio #9 DBO5lxndare musik mNessuna valutazione finora
- Presentación2 GRUPALDocumento18 paginePresentación2 GRUPALGaby MadridNessuna valutazione finora
- Dbo y DqoDocumento38 pagineDbo y DqoAndrea K Torres100% (1)
- Procesos Q y BDocumento5 pagineProcesos Q y BEllison Ardila VásquezNessuna valutazione finora
- Dbo5Documento20 pagineDbo5Juan PerezNessuna valutazione finora
- Practica 4 QADocumento4 paginePractica 4 QALennon CRNessuna valutazione finora
- DBODocumento15 pagineDBOAlex del ReyNessuna valutazione finora
- Determinación de Demanda Bioquímica de Oxigena (Dbo5) Del Río TitireDocumento17 pagineDeterminación de Demanda Bioquímica de Oxigena (Dbo5) Del Río TitireYudith LarijoNessuna valutazione finora
- LAB STAR Actividad Del VideoDocumento3 pagineLAB STAR Actividad Del VideoJaider Tordecilla VegaNessuna valutazione finora
- Dbo DqoDocumento8 pagineDbo Dqostefany alcivarNessuna valutazione finora
- Procesos MicrobianosDocumento3 pagineProcesos MicrobianosIriana MoreiraNessuna valutazione finora
- DBO5Documento21 pagineDBO5Peter Giancarlo Ramirez Tanta0% (1)
- Dbo, Dqo y Detergentes ExpDocumento35 pagineDbo, Dqo y Detergentes ExpGustavo Adolfo Hernandez GarciaNessuna valutazione finora
- 05-24-2019 053701 Am PRACTICA 5 Determinacion de La Demanda Bioquimica de Oxigeno (DBO)Documento7 pagine05-24-2019 053701 Am PRACTICA 5 Determinacion de La Demanda Bioquimica de Oxigeno (DBO)Ruth Mercado ChinchayNessuna valutazione finora
- TALLER EVAL - DETERMINAC DE LA - DBO Parte II-2425247-Vertim-LiqDocumento5 pagineTALLER EVAL - DETERMINAC DE LA - DBO Parte II-2425247-Vertim-LiqGABRIELA CAROLINA HIGIDIO FERRERNessuna valutazione finora
- Dbo - Informe 8 - AguasDocumento9 pagineDbo - Informe 8 - AguasAriel CuadroNessuna valutazione finora
- Aguas Residuales AmbDocumento10 pagineAguas Residuales Ambalexandra anahiNessuna valutazione finora
- GL-PL-25. Protocolo Dbo 5 PDFDocumento15 pagineGL-PL-25. Protocolo Dbo 5 PDFGBastidas BastidasNessuna valutazione finora
- Informe 7 - Dbo JPDocumento13 pagineInforme 7 - Dbo JPAnabel Roxana Fernandez RamirezNessuna valutazione finora
- Demanda Quimica de Oxigeno en Microbiologia de AguaDocumento39 pagineDemanda Quimica de Oxigeno en Microbiologia de AguaPaolo BarredaNessuna valutazione finora
- Repaso Lab Quimica 2Documento3 pagineRepaso Lab Quimica 2Valeria RondónNessuna valutazione finora
- Determinacion de OD, DBO5 EnviarDocumento4 pagineDeterminacion de OD, DBO5 EnviarELISABETH MUNOZ PISONessuna valutazione finora
- Laboratorio Dbo - AnalisisDocumento24 pagineLaboratorio Dbo - AnalisisMartin S. Lopez MogrovejoNessuna valutazione finora
- Dbo5-Exposicion FinalDocumento31 pagineDbo5-Exposicion Finalpfj5zn8bnbNessuna valutazione finora
- Agua ResidualesDocumento9 pagineAgua ResidualesWilian Ccapa HuanccoNessuna valutazione finora
- Determinación de Fluoruros, DQO, DBO.Documento4 pagineDeterminación de Fluoruros, DQO, DBO.Cristian Franco GalvánNessuna valutazione finora
- Contaminacion Del AguaDocumento14 pagineContaminacion Del AguaMark UsNessuna valutazione finora
- Practica 3. Demanda Bioquimica de Oxigeno (DBO5)Documento7 paginePractica 3. Demanda Bioquimica de Oxigeno (DBO5)Harley SinclairNessuna valutazione finora
- DboDocumento11 pagineDboJasmin LNNessuna valutazione finora
- Hoja de Reporte y Guias de Parametro in Situ - CampoDocumento23 pagineHoja de Reporte y Guias de Parametro in Situ - Campohjowar aguilarNessuna valutazione finora
- Demanda Bioquimica de OxigenoDocumento9 pagineDemanda Bioquimica de OxigenoDOUGLAS SÁNCHEZNessuna valutazione finora
- Tarea6 TDL Yamilet CarranzaDocumento5 pagineTarea6 TDL Yamilet CarranzaYAMILET CARRANZA BARRAGANNessuna valutazione finora
- TP0087 - DemandaBioquimicadeOxigeno - IdeamDocumento13 pagineTP0087 - DemandaBioquimicadeOxigeno - IdeamLUCHY43Nessuna valutazione finora
- DBO y DQODocumento8 pagineDBO y DQOJaime Andres QuimbayaNessuna valutazione finora
- Informe 6 - DQO y ODDocumento12 pagineInforme 6 - DQO y ODwendy sanchezNessuna valutazione finora
- Gl-pl-25. Protocolo Dbo 5Documento15 pagineGl-pl-25. Protocolo Dbo 5ana8816Nessuna valutazione finora
- Fosa Séptica o Tanque SépticoDocumento2 pagineFosa Séptica o Tanque SépticofabiolaNessuna valutazione finora
- Poblacion Censada Por Distritos Aqp Censo 2017Documento19 paginePoblacion Censada Por Distritos Aqp Censo 2017fabiolaNessuna valutazione finora
- 13.-Diseño Reactor UasbDocumento47 pagine13.-Diseño Reactor UasbMaria Victoria Torres LaraNessuna valutazione finora
- Reactores Anaerobios Digital Publicación Junio 2022Documento447 pagineReactores Anaerobios Digital Publicación Junio 2022fabiolaNessuna valutazione finora
- Tanque ImhoffDocumento2 pagineTanque ImhofffabiolaNessuna valutazione finora
- Poblacion EstablecimientosDocumento44 paginePoblacion EstablecimientosAlexanderChhNessuna valutazione finora
- VientoDocumento7 pagineVientofabiolaNessuna valutazione finora
- Historiadejauja 170603165229Documento7 pagineHistoriadejauja 170603165229fabiolaNessuna valutazione finora
- 1 CovDocumento3 pagine1 CovfabiolaNessuna valutazione finora
- Planta Trat Agua ResidualDocumento2 paginePlanta Trat Agua ResidualfabiolaNessuna valutazione finora
- Resumen Ejecutivo: - A.2 Ubicación Y Localización Del ProyectoDocumento45 pagineResumen Ejecutivo: - A.2 Ubicación Y Localización Del Proyectoronal mejia herreraNessuna valutazione finora
- AditivosDocumento1 paginaAditivosfabiolaNessuna valutazione finora
- Informe Final Geomorfologia PDFDocumento103 pagineInforme Final Geomorfologia PDFEduardo CesarNessuna valutazione finora
- Manejo Residuos SolidosDocumento2 pagineManejo Residuos SolidosfabiolaNessuna valutazione finora
- Consumo de AguaDocumento4 pagineConsumo de AguafabiolaNessuna valutazione finora
- EnsayoDocumento1 paginaEnsayofabiolaNessuna valutazione finora
- Construcción de Sistemas de AlcantarilladoDocumento1 paginaConstrucción de Sistemas de AlcantarilladofabiolaNessuna valutazione finora
- E. MeteorologicasDocumento2 pagineE. MeteorologicasfabiolaNessuna valutazione finora
- PreguntasDocumento1 paginaPreguntasfabiolaNessuna valutazione finora
- Decreto SupremoDocumento2 pagineDecreto SupremofabiolaNessuna valutazione finora
- Alcantarilla DoDocumento4 pagineAlcantarilla DofabiolaNessuna valutazione finora
- AditivosDocumento2 pagineAditivosfabiolaNessuna valutazione finora
- E. MeteorologicasDocumento2 pagineE. MeteorologicasfabiolaNessuna valutazione finora
- Disposiciones Complementarias Finales PrimeraDocumento2 pagineDisposiciones Complementarias Finales PrimerafabiolaNessuna valutazione finora
- IndicesDocumento21 pagineIndicesErick GonzalezNessuna valutazione finora
- LP Pavco Dic 4 2018 FinalDocumento40 pagineLP Pavco Dic 4 2018 FinalJhonnatan Fredy Gomez DominguezNessuna valutazione finora
- ÍNDICEDocumento1 paginaÍNDICEfabiolaNessuna valutazione finora
- Exp Lavado de FiltrosDocumento2 pagineExp Lavado de FiltrosfabiolaNessuna valutazione finora
- Especificaciones Tecnicas MinimasDocumento1 paginaEspecificaciones Tecnicas MinimasfabiolaNessuna valutazione finora
- Ensayo Taller Mecanico 2Documento18 pagineEnsayo Taller Mecanico 2Moises ChasiNessuna valutazione finora
- PRACTICA 1 Estabilidad de Comp Erik y DayDocumento7 paginePRACTICA 1 Estabilidad de Comp Erik y DayerikuribeNessuna valutazione finora
- Taller de InmunologiaDocumento19 pagineTaller de InmunologiaGaBriiela ViDalNessuna valutazione finora
- Tipos de Cableados Documento Final 1Documento11 pagineTipos de Cableados Documento Final 1Angie Vera MontielNessuna valutazione finora
- Ensayo 2 Bien Hecho Exposicion AvanzandoDocumento15 pagineEnsayo 2 Bien Hecho Exposicion AvanzandoRoy Perez LazoNessuna valutazione finora
- Informe N°3Documento7 pagineInforme N°3Antonio TelloNessuna valutazione finora
- Selección de Brocas - Jose BalcazarDocumento13 pagineSelección de Brocas - Jose BalcazarAlexander TenempaguayNessuna valutazione finora
- Prof. Julio LandinezDocumento31 pagineProf. Julio Landinezyonatan_mamani_10Nessuna valutazione finora
- Aashto T 90-16Documento10 pagineAashto T 90-16Waly OrtizNessuna valutazione finora
- Práctica 12 EcologíaDocumento4 paginePráctica 12 Ecologíadennie DominguezNessuna valutazione finora
- Concepto e Importancia de AbsorciónDocumento4 pagineConcepto e Importancia de AbsorciónKiara Odalis Tapia PardoNessuna valutazione finora
- Monografia Analitica Vitamina CDocumento16 pagineMonografia Analitica Vitamina CVictor David Fernandez PeñaNessuna valutazione finora
- Ley de HenryDocumento1 paginaLey de HenryGames RaRNessuna valutazione finora
- Ecologia InstrumentosDocumento10 pagineEcologia InstrumentosJasmin ZoteloNessuna valutazione finora
- Serie 90 11 14 y 16 Pies PDFDocumento16 pagineSerie 90 11 14 y 16 Pies PDFtaz1mxNessuna valutazione finora
- Kevin Campo 00209473 Informe 2 MacromoleculasDocumento11 pagineKevin Campo 00209473 Informe 2 MacromoleculasKevin CampoNessuna valutazione finora
- Intercambiador de Calor en La Industria LácteaDocumento2 pagineIntercambiador de Calor en La Industria Lácteabladimir zamora0% (1)
- Sentimientos ContradictoriosDocumento3 pagineSentimientos ContradictoriosIvan Ortiz LopezNessuna valutazione finora
- Listado de Puentes IIRSA NorteDocumento1 paginaListado de Puentes IIRSA NorteEduardo Mora Lazo100% (1)
- 10 APU PontonDocumento10 pagine10 APU PontonWashington CairaNessuna valutazione finora
- Eaton Jokey PDFDocumento8 pagineEaton Jokey PDFfabian cardenasNessuna valutazione finora
- El Intercambio de Gases en La RespiracionDocumento2 pagineEl Intercambio de Gases en La RespiracionDavixito André Gálvez FloresNessuna valutazione finora
- Guia Ejercicios Numero de OxidacionDocumento3 pagineGuia Ejercicios Numero de OxidacionjulianmardukNessuna valutazione finora
- Desarrollo de Ejemplo - Elementos de Cartografia TematicaDocumento7 pagineDesarrollo de Ejemplo - Elementos de Cartografia TematicaAna GabrielaNessuna valutazione finora
- Informe EbullicionDocumento4 pagineInforme EbullicionAlexis Peñafiel CafiaNessuna valutazione finora
- Proceso Industrial Elaboracion de La MantequillaDocumento23 pagineProceso Industrial Elaboracion de La MantequillaLalo Espino67% (3)
- Mezclas de Asfaltos y FillersDocumento2 pagineMezclas de Asfaltos y FillersNesFloresVelazquezNessuna valutazione finora
- Iveco Motor F1CDocumento191 pagineIveco Motor F1Cbhj67% (3)
- Los Chinos?Documento24 pagineLos Chinos?Ariana LuqueNessuna valutazione finora