Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Macla6 427 PDF
Caricato da
DanielleTitolo originale
Copyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Macla6 427 PDF
Caricato da
DanielleCopyright:
Formati disponibili
MACLA 6 XXVI R E U N iÓN ( S E M ) / XX R E U N iÓN (SEA) - 2006
INFLUENCIA DE LA FUERZA IÓNICA y LA
TEMPERATURA EN LA QUÍMICA SUPERFICIAL DE LA
E S MECTITA
M. ROZALÉN (1 ), P.Y. BRADY (2 ) Y F.J. HUERTAS (1 )
(1) Estación Experimental del Zaidin, eSIe, Granada, 1 8008, Spain . mlrozalen@eez . csic.es, jhuertas@eez . csic.es.
2( ) Sandia National Laboratories, Albuquerque, NM 871 85, USA. pvbrady@sandia.gov
INTRODUCCIÓN desorción de protones en función del pH, la fuerza iónica
( 0 . 1 , 0 . 0 1 Y 0.0 0 1 M KN0 3 ) y la temperatura (25, 50 Y
La química superficial de la esmectita ejerce un control 70°C). Los experimentos se llevaron a cabo mediante un
crítico sobre el ciclo de nutrición y contaminación en sue valorador automático METTLER DL 12 en suspensiones
los. Al mismo tiempo, las velocidades de disolución/pre de esmectita potásica utilizando una relación sólido/lí
cipitación de esmectita (propuesta como material de re quido de 20 gL-1, que fueron valoradas con soluciones de
lleno y barrera de ingeniería en almacenamientos de resi HCl 0.1 M Y KOH 0.1 M. Las suspensiones se agitaron de
d u o s n u c l e a r e s de a l t a a ctiv i d a d ) d e p e n d e n de l a forma continua y se burbujearon con N 2 durante toda la
naturaleza y número de especies presentes e n la superfi valoración para purgar la solución de CO2 . Normalmente
cie de la esmectita. Es por ello que existe un considerable se esperaron de 1 a 5 minutos entre cada adición de áci
inte r é s en compren d e r la quími c a s u p e r f i c i a l de l a do/base hasta que el pH se estabiliz a nuevamente. Se
esmectita, l o s procesos de meteorización y precipitación y considera el pH estable cuando cambia menos de 0.01 uni
la relación entre ambos. Teniendo en cuenta que la mayo dades por minuto. Cada rama de la valoración se realiza
ría estos procesos ocurren a temperaturas mayores de en un tiempo de 30 a 90 minutos. Las valoraciones a alta
25°C resulta de gran utilidad conocer cómo afecta este temperatura se llevaron a cabo sumergiendo la suspen
parámetro a la química superficial. s i ó n a r c i l l a / s o l u c i ó n en u n b a ñ o (o c a m i s a )
El obj eto de este estudio es identificar los sitios superfi termostatizada. Además s e realización valoraciones de
ciales activos y el comportamiento de la superficie de la soluciones de KN0 3 0 . 1 , 0.0 1 Y 0 . 0 0 1 M, sin esmectita,
esmectita en un amplio rango de pH evaluando el efecto para utilizarlas como referencia.
de la fuerza iónica y de la temperatura. Para controlar el efecto de la disolución de la esmectita
en el balance de protones se realizaron extracciones de 3
MATERIAL Y MÉTODOS mL de suspensión a pH 1, 2, 3, 1 0, 1 1 , 12 Y 13 durante las
valoraciones. Las soluciones se filtraron con un filtro de
Como material de partida se utilizó bentonita proce 0.2 Ilm y se analizaron mediante ICP-MS, para determinar
d e n t e del y a c i m i e n t o «L a S e r r a t a » ( C a b o d e G a ta, la concentración de Si, Al Y Mg liberado a la solución. Los
Almería). El material natural contiene aproximadamente resultados mostraron que la cantidad de protones consu
un 92% de esmectita y el resto son cuarzo, feldespatos, midos por la disolución del material es despreciable en el
plagioclasas, micas, calcita, anfíboles y vidrio volcánico. cálculo de la carga superficial.
Para este estudio se extrajo la fracción menor de 4 Ilm de El programa FITEQL (Westall, 1 982) fue usado para
esmectita mediante sedimentación y se saturó en potasio. ajustar las medidas de carga superficial y estimar los va
El material resultante corresponde a una esmectita (>99%) lores de las constantes de acidez de los sitios superficiales
con una capacidad de cambio de cationes (CEC) de 99.8 y la densidad total de sitios. Se utilizó un mo delo de
cmol(+) kg-1 y una fórmula estructural que corresponde a capacitancia constante, asumiendo tres tipos diferentes de
una montmorillonita: sitios superfici a l e s : las r e a cciones d o n o r/aceptor de
protones ocurren en los sitios con carácter ácido YOH (si
Ko.ss [A12.s4 Fe 3+0. 4s Mg1.12 1 [ Si 7.91 Alo.09l 0 20 (OH)4 tios silanol) y anfotérico XOH (aluminol) situados en los
bordes de los cristales de la esmectita, y las reacciones de
Sólo 0.76 iones K+ por fórmula unidad son intercambia intercambio de cationes H/K tienen lugar en los sitios
bles, lo cual indica la presencia de una pequeña proporción ZEH situados en el plano basal.
de láminas no hinchables. El estudio del agregado orientado
secado al aire y con etilén glicol, y la posterior simulación RESULTADOS Y DISCUSIÓN
con el programa NEWMOD, confirmaron que existen un
10% de láminas no hinchables. El área superficial externa del Las valoraciones obtenidas a 2 5 ° C, para una fuerza
material se determinó mediante isotermas de adsorción de iónica de 0.1, 0.01 Y 0.001 M de KN03, se han representa
nitrógeno (BET) resultando un valor de 1 1 1 m2 g-1 . do en la figura 1, donde se puede observar que la carga
Se llevaron a cabo valoraciones superficiales ácido/ superficial es positiva por debaj o de pH 7 debido al pro
base en modo continuo de la esmectita potásica en un ceso de adsorción de protones, y por encima de pH 7 la
amplio rango de pH ( 1 - 1 3 . 5 ) para medir la adsorción/ carga superficial es negativa debido al proceso de libera-
MACLA 6 Página 427
MACLA 6 XXVI R E UNiÓN (SE M) / XX R E UNiÓN (SEA) - 2006
----------
0.005 - -_. ..
0.0008 O O.01M
O O.01M -- m o de l 0.0007
-- model
0.004 t:.. O.1M
Ó. O.1M O O.OO1M 0.0006
0.003 0.0005
0.0004
0.002 - 0.0003
� 0.001 �
1/)
0.0002
0.0001
1/)
"O "O
(Q 0- --· ----····· .__ ._---.-
(Q O
"S 3 5 7 13
"S -0.0001 5 6 10
E
.§. -0.001 ";(; -0.0002
00
-0.0003
-0.002 "
-0.0004
-0.003 -0.0005
-0.0006
-0.004 -0.0007
-0.0008 j--------- .. ---.... .----.-----l,
-0.005· _··· -
pH
pH
Figura 1 : Datos experimentales para las valoraciones potenciométricas realizadas a 25°C a diferentes fuerzas iónicas.
Las líneas sólidas corresponden al modelo calculado con FITEQL.
ción de protones. En el intervalo de pH 7-8 .5 el efecto de L a s curvas son asimétricas respe cto al pH pznpc Y l a
la fuerza iónica es mínimo. Realmente se observa que las cinética de adsorción-desorción es m á s rápida e n medio
curvas están muy cerca unas de otras, de forma que pode alcalino y más lenta a pH< 7-8, lo que indica que el núme
mos concluir que la fuerza iónica solo tiene un pequeño ro total de sitios cargados negativa y positivamente es di
efecto en la adsorción/desorción de protones, lo cual es ferente según el rango de pH considerado. La forma de
similar a lo observado para otros filosilicatos. las curvas de valoración también sugiere la presencia de
Las curvas de valoración se entrecruzan en algunas zo múltiples sitios con diferentes características ácido-base.
nas lo que induce una dispersión en las constantes calcu Respecto al modelo se puede observar que los datos
ladas, lo cual ha sido observado por otros autores como experimentales y los calculados con el modelo (represen
Huertas et al., . ( 1 998) para caolinita . Sin embargo, si se tados con puntos y líneas sólidas respectivamente en la
excluyen los datos obtenidos a la fuerza iónica más baj a, figura 1 ) se ajustan muy bien entre pH 3-1 1 . A pH<3 Y
0 . 0 0 1 M, en la figura lb se puede ver que las curvas dis pH>l 1 los datos no se pudieron modelizar con FITEQL.
curren de forma paralela, desplazándose hacia valores En la tabla 1 s e muestran los valores ob teni d o s con
de pH más alcalinos a medida que disminuye la concen FITEQL para las constantes aparentes y la densidad de
tración de electrolito inerte, lo cual es consistente con lo sitios superficiales, considerando un modelo de 3 sitios.
o b t e n i d o p o r Av e n a y D e P a u l i ( 1 9 9 8 ) p a r a Estos muestran que los sitios aluminol son los predomi
montmorillonita sódica. E l p H del punto d e carga neta nantes, de forma que la superficie esta dominada por los
de protones cero (pHpznpcl corresponde al pH en el cual sitios >AIOH anfotéricos. La media obtenida para los si
la densidad de carga superficial de protones es igual a tios en los que ocurre el intercambio K/H obtenida con
cero. Los valores obtenidos (tabla 1 ) disminuyen confor el modelo es mucho menor que el número de sitios cal
me aumenta la fuerza iónica. Estos valores coinciden con culado a partir del valor de CEC (0.99 sitios nm-2 ) . Esta
el c a l c u l a d o p o r S t a n d l e r y S c h i n d l e r ( 1 9 9 3 ) p a r a diferencia ha sido observada por otros autores Zysset y
montmorillonita-Ca (pHpznp c 7 . 7 ) . E l aumento d e l Schindler ( 1 996), en el que la CEC determinada experi
pHpznpc e s debido a que conforme aumenta l a fu erza mentalmente en su trabajo es casi el doble del valor ajus
iónica también la concentración de K+ que compite con tado con el modelo. El motivo de esta discrepancia pue
los H+ por los grupos de carga permanente debidos a la de ser que el e quilibrio de intercambio catiónico no se
sustitución isomórfica. llega a alcanzar en los experimentos de valoración.
Fuerza T (OC) pK pK pK pK TAIOH TSiOH TZEH pHpZNPC
Iónica(M) AIOHz+ AIO- SiO ZEXH [sitios nrn-2] [sitios nrn-2] [sitios nm-2]
0.1 25 4.42 11.00 6.22 7.78 0.38 0.08 0.015 7.03
0.01 25 5.08 10.14 7.74 7.34 0.45 0.05 0.018 7.53
0.001 25 4.38 9.86 6.06 9.55 0. 35 0.10 0.018 7.70
0.01 50 3.31 11.28 5.40 8.34 0.54 0.11 0.022 7.39
0.01 70 2.00 11.50 5.85 7.79 0.51 0.11 0.020 7.20
Tabla 1 : Valores obtenidos con FITE QL para las constan tes de acidez y la dens idad de sitios superficiales de las valoraciones
potenciométricas ob tenidas .
MACLA 6 Página 428
MACLA 6 XXVI R E U N iÓN ( S E M ) / XX R E UNiÓN (S EA) - 2006
AlOH2+ AlO- SiO- K/H
�HO (kcal mol-1) 13.88 -6.32 9.19 -2.43
�So (cal mol-J) 36 .46 -41 .56 16.11 -23.13
Tabla 2: Resultados obtenidos para los parámetros termodinámicos de los procesos de adsorción en los diferen
tes sitios superficiales de la esmectita.
La constante de desprotonación de los grupos silanol afirmación es consistente con la observada por otros au
>SiOH (pKSiOH= 6.22 ) es del mismo orden que la obtenida tores para la adsorción de cationes en superficies de oxi
por otros autores para esmectitas y para Si0 2 . Por otro hidróxidos y filosilicatos en las que afirman que la ener
lado, los sitios aluminol parecen tener un carácter más gía de adsorción de los cationes tiene un valor cercano a
ácido en la esmectita (pKAIOH2 = 4.42 and pKA10-= 1 1.00) la energía de hidrólisis del catión (e.g., Brady (1 992) para
+
que en la y-A1 2 03 ' la adsorción de Cd y Pb en Si0 2 ) .
Los resultados de la tabla 1 indican un aumento del
número total de sitios superficiales con la temperatura, lo CONCLUSIONES
cual podría ser debido a la producción de bordes superfi
ciales con la temperatura (Brady et al., 1 996). A un pH - El efecto de la fuerza iónica en las valoraciones ácido/
dado un aumento de temperatura disminuye la cantidad base es reducido, como ocurre para otros filosilicatos
total de protones adsorbidos en la superficie y la pendien y óxidos simples. Las curvas de valoración discurren
te de las curvas de valoración disminuye . Este comporta aproximadamente de forma paralela, al contrario que
miento es contrario al observado por caolínita, (Brady et en el caso de caolinita y óxidos como Si0 2 y A12 03, don
al., 1 996); sin embargos estos autores afirman que el efec de se cruzan en uno o varios puntos .
to d e la temperatura sobre el p r o c e s o d e a d s o r ción/ - El pH del punto de carga neta de protones cero obteni
desorción de protones depende del mineral estudiado. do varía de forma lineal con el logaritmo de la fuerza
Como se ha observado p ara óxi dos e hidróxidos, el iónica, aumentando cuando esta disminuye.
pHpznpc disminuye cuando aumenta la temperatura (tabla - Al aumentar la temperatura disminuye el número to
1 ). Sin embargo el descenso en el pHpznpc es aparente ya tal de protones/hidroxilos adsorbidos en la superficie
que al aumentar la temperatura aumenta también la cons de la esmectita.
tante de disociación del agua. - El efecto de la temperatura en la adsorción de protones
A partir de las constantes de adsorción/desorción de es pequeño, de forma que la variación de los pK' s y el
protones se calcularon los parámetros termodinámicos del pH pznpc puede ser sólo aparente, puesto que estos cam
proceso; L'lH O y L'lSo, mediante la ecuación de Van't Hoff: bios se pueden deber a la variación de la energía de
hidratación del protón con la temperatura.
REFERENCIAS
Avena, M.J., De Paulí, c . P. (1 998). Journal of Colloid and
Interface Science 202, 1 95-204.
donde K es la constante termodinámica, L'l H O es la entalpía Brady, P.v. (1 992). Geochimica et Cosmochimica Acta 56,
de la reacción, R es la constante de los gases, T es la tem 2941 -2946.
peratura absoluta y L'lSo la entropía de la reacción. Los Brady, P. v., Cygan, R . T., Nagy, K . L . ( 1 996). Journal of
valores obtenidos se muestran en la tabla 2. Colloid and Interface Science 1 83, 356-364
Los valores de L'lHO para la reacción de disociación, para Huertas, F.L Chou, L., Wollast, R. (1 998). Geochimica et
todos los tipos de sitios superficiales, son bastante bajos, Cosmochimica Acta 62, 41 7-43 1.
lo que implica que la energía de adsorción de los protones Standler, M . , Schindler, P.W. ( 1 9 9 3 ) . Clays and Clay
en la superficie debe ser del orden d e su energía de Minerals, 41, 288-296.
hidratación (-261 kcal moI-l ) . Podemos concluir que los We stall, J . c . 1 9 8 2 . F I T E Q L . Report 8 2 - 0 1 , Chemistry
cambios en las constantes de adsorción debidos al aumen Dept., Oregon State University, Corvallis, Oregon.
to de temperatura están asociados a la variación de la Z y s s e t, M . , S c h i n d l e r, P.W. ( 1 9 9 6 ) . G e o ch i m i c a e t
constante de ionización del agua con la temperatura . Esta Cosmochimica Acta 60, 921-931.
MACLA 6 Página 429
Potrebbero piacerti anche
- Reporte Práctica 6Documento3 pagineReporte Práctica 6cristo JiménezNessuna valutazione finora
- Isoterma de TemkinDocumento19 pagineIsoterma de TemkinCancino Zamora Joan GloiserNessuna valutazione finora
- Análisis de La Microporosidad de Catalizadores de FCC: UímicaDocumento8 pagineAnálisis de La Microporosidad de Catalizadores de FCC: UímicaSam GuzmánNessuna valutazione finora
- Adsorcion Interfase Solido-LiquidoDocumento3 pagineAdsorcion Interfase Solido-Liquidojefe4100% (3)
- Adsorción de Líquidos en SólidosDocumento15 pagineAdsorción de Líquidos en Sólidosluisedo -Nessuna valutazione finora
- CrioscopíaDocumento5 pagineCrioscopíaFranco ChalacanNessuna valutazione finora
- Informe de AdsorcionDocumento14 pagineInforme de AdsorcionLauriza Giraldo HuamanNessuna valutazione finora
- AdsorciónDocumento9 pagineAdsorciónValentina Monroy GonzálezNessuna valutazione finora
- Tratamientos de Lodos de Galvanoplastia para La Recuperacion de Niquel y CromoDocumento12 pagineTratamientos de Lodos de Galvanoplastia para La Recuperacion de Niquel y CromoAlan BrañezNessuna valutazione finora
- Laboratorio 3. - Estequiometria de Una Reacción PDFDocumento22 pagineLaboratorio 3. - Estequiometria de Una Reacción PDFRojas GustavoNessuna valutazione finora
- Practica 16-Determinacion de Ionizacion de Un Electrolito DebilDocumento4 paginePractica 16-Determinacion de Ionizacion de Un Electrolito DebilAnonymous l2zWgdotbiNessuna valutazione finora
- Informe 7 Fisicoquímica II A y BDocumento12 pagineInforme 7 Fisicoquímica II A y Bgerson.santillanNessuna valutazione finora
- Recuperación de Antimonita A Partir de DesmontesDocumento16 pagineRecuperación de Antimonita A Partir de DesmontesAle HyztaNessuna valutazione finora
- Fuerza Iónica y CoeficienteDocumento12 pagineFuerza Iónica y CoeficienteMaria Angelica Oviedo TorresNessuna valutazione finora
- Adsorción de ácido oxálico en carbón vegetalDocumento18 pagineAdsorción de ácido oxálico en carbón vegetalLuisa MedinaNessuna valutazione finora
- Cinetica de Intercambio Ionico: Resina Amberlite IR 120 (H) Malla 30 Fecha Realizacion: 2 Noviembre 2016Documento5 pagineCinetica de Intercambio Ionico: Resina Amberlite IR 120 (H) Malla 30 Fecha Realizacion: 2 Noviembre 2016JuanAmayaNessuna valutazione finora
- ProblemasDocumento2 pagineProblemasdaniaNessuna valutazione finora
- Informe 7. Isoterma de Adsorcion WuuuDocumento13 pagineInforme 7. Isoterma de Adsorcion WuuumariaNessuna valutazione finora
- Informe de Laboratorio N°7 - Adsorción Del Ácido Acético Sobre Carbón ActivadoDocumento13 pagineInforme de Laboratorio N°7 - Adsorción Del Ácido Acético Sobre Carbón ActivadoMaycol Richard Leyva PatricioNessuna valutazione finora
- ElectrolitoDocumento8 pagineElectrolitoHanny Mirella Rojas RiveraNessuna valutazione finora
- Informe de Fuerza IónicaDocumento18 pagineInforme de Fuerza IónicaYesika AlmanzaNessuna valutazione finora
- ADSORCIONDocumento5 pagineADSORCIONDUVAN PETENessuna valutazione finora
- Practica N°4 - Análisis Cuantitativo de PermanganatoDocumento6 paginePractica N°4 - Análisis Cuantitativo de PermanganatoRuth jcNessuna valutazione finora
- 71 - Heriberto Bustamante - Sergio Castro - Estudio Sobre La Depresion de Calcocita La Flotacion de MolindenitaDocumento8 pagine71 - Heriberto Bustamante - Sergio Castro - Estudio Sobre La Depresion de Calcocita La Flotacion de MolindenitaRAMIRO FERNANDO MACHACA NEIRANessuna valutazione finora
- Muestreos de Agua en Localidad Del QuecheDocumento7 pagineMuestreos de Agua en Localidad Del Quechealondra.gaeteNessuna valutazione finora
- Conductividad de Soluciones Electroliticas - CompressDocumento15 pagineConductividad de Soluciones Electroliticas - CompressFABRICIO TELMO MATIAS MALCA SANCHEZNessuna valutazione finora
- Problemas TecnicasDocumento8 pagineProblemas TecnicasAsd SdfNessuna valutazione finora
- Analisis1examenes 4 y 5toDocumento11 pagineAnalisis1examenes 4 y 5toJavan ZaldivarNessuna valutazione finora
- Plantilla Informe Lab. Quimica AnaliticaDocumento5 paginePlantilla Informe Lab. Quimica AnaliticaSteven Agredo SanchezNessuna valutazione finora
- Relacion Entre La Hidratacionidesvitrificacion y El 6018Documento9 pagineRelacion Entre La Hidratacionidesvitrificacion y El 6018MarcosNessuna valutazione finora
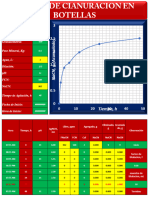
- Informe de Cianuracion en BotellaDocumento32 pagineInforme de Cianuracion en Botellajhoni88% (8)
- Seminario IV - Cinetica de Reacciones Gas Solido Reactivo JSDocumento3 pagineSeminario IV - Cinetica de Reacciones Gas Solido Reactivo JSTomii GonzalezNessuna valutazione finora
- Problemas de Aplicación Reactores IdealesDocumento4 pagineProblemas de Aplicación Reactores IdealesjorgeNessuna valutazione finora
- Estudio de La Cristalizacion Del Sulfato Calcico A 80°C Implicaciones en La Cristalizacion de La AnhidritaDocumento2 pagineEstudio de La Cristalizacion Del Sulfato Calcico A 80°C Implicaciones en La Cristalizacion de La AnhidritaJose Ronald CondoriNessuna valutazione finora
- Determinación Punto Isoeléctrico Fotocatalizador Mediante Potencial ZetaDocumento5 pagineDeterminación Punto Isoeléctrico Fotocatalizador Mediante Potencial ZetaHazael Ociel RFNessuna valutazione finora
- Conductimetría Serie 2 Agosto 2018Documento3 pagineConductimetría Serie 2 Agosto 2018Leif_Erikson_Nessuna valutazione finora
- Determinación de la estequiometría por MVCDocumento5 pagineDeterminación de la estequiometría por MVCeduardohk18Nessuna valutazione finora
- Formación de Radicales HidroxiloDocumento6 pagineFormación de Radicales HidroxiloeducobainNessuna valutazione finora
- 3) Diagramas-de-clasificación-R1R2-Streckeisen-1 PDFDocumento11 pagine3) Diagramas-de-clasificación-R1R2-Streckeisen-1 PDFKevinNessuna valutazione finora
- Crioscopía FinalDocumento5 pagineCrioscopía FinalNathaly FalconíNessuna valutazione finora
- Introduccion Del Carbono ActivadoDocumento4 pagineIntroduccion Del Carbono ActivadoCrhiiztiian RojjazNessuna valutazione finora
- PDF Informe Labn1 1 Corregido DLDocumento4 paginePDF Informe Labn1 1 Corregido DLLuisaNessuna valutazione finora
- VanessaMartinez APES 2016 DSC CuODocumento7 pagineVanessaMartinez APES 2016 DSC CuOVanessa Martinez RojasNessuna valutazione finora
- Laboratorio Nº1 Fisicoquimica I (Plancha 2)Documento13 pagineLaboratorio Nº1 Fisicoquimica I (Plancha 2)Jose FernandezNessuna valutazione finora
- Ing QcaDocumento104 pagineIng QcaAlicia QuezadaNessuna valutazione finora
- G5.II-Conductividad y Cinética ElectroquímicaDocumento3 pagineG5.II-Conductividad y Cinética Electroquímicamariasolruiz1984Nessuna valutazione finora
- Oxidación del ion yoduro con persulfato de amonioDocumento8 pagineOxidación del ion yoduro con persulfato de amonioKAREN ANDIA GUZMAN100% (1)
- Lixiviación de minerales de cobre: Fundamentos termodinámicos y cinéticosDocumento59 pagineLixiviación de minerales de cobre: Fundamentos termodinámicos y cinéticosARLEN SCOLY MAMANI ONSIHUAYNessuna valutazione finora
- ADSORCIONDocumento20 pagineADSORCIONKaylam Salazar LópezNessuna valutazione finora
- 21 Quimica Acosta Alfredo UnaDocumento17 pagine21 Quimica Acosta Alfredo UnaLuisa LopezNessuna valutazione finora
- Enunciado C4 - Grupo4Documento5 pagineEnunciado C4 - Grupo4Valeria NeiraNessuna valutazione finora
- Adsorción Ácido Oxálico CarbónDocumento7 pagineAdsorción Ácido Oxálico CarbónChiquinquira AnguloNessuna valutazione finora
- Guia de Problemas de Ejercicios (8) Reactores I: Universidad Tecnológica MetropolitanaDocumento2 pagineGuia de Problemas de Ejercicios (8) Reactores I: Universidad Tecnológica MetropolitanaMatias Ulloa SaavedraNessuna valutazione finora
- INFORME Fiqui Final AdsrocionDocumento20 pagineINFORME Fiqui Final AdsrocionedithNessuna valutazione finora
- Adsorción de Carbón ActivadoDocumento10 pagineAdsorción de Carbón ActivadoSusan BazanNessuna valutazione finora
- Examen Final 17 de Agosto de 2020Documento2 pagineExamen Final 17 de Agosto de 2020Mafer Mabel GalarzaNessuna valutazione finora
- Examen Final 17 de Agosto de 2020Documento2 pagineExamen Final 17 de Agosto de 2020marioNessuna valutazione finora
- Universidad Nacional Autónoma de México: Laboratorio de Cinética QuímicaDocumento11 pagineUniversidad Nacional Autónoma de México: Laboratorio de Cinética QuímicajessicaNessuna valutazione finora
- Problemas resueltos de Hidráulica de CanalesDa EverandProblemas resueltos de Hidráulica de CanalesValutazione: 4.5 su 5 stelle4.5/5 (7)
- Principios de Análisis de ConcordanciaDocumento16 paginePrincipios de Análisis de ConcordanciaDanielleNessuna valutazione finora
- 4 Practica 4 Segunda Ley de Newton - Documentos de Google PDFDocumento4 pagine4 Practica 4 Segunda Ley de Newton - Documentos de Google PDFDanielleNessuna valutazione finora
- Análisis Gravimétrico: Métodos y FundamentosDocumento42 pagineAnálisis Gravimétrico: Métodos y FundamentosBart SimpsomNessuna valutazione finora
- Tesis PDFDocumento219 pagineTesis PDFlibroscuentaspremiumNessuna valutazione finora
- Grupos Protectores en Química OrgánicaDocumento40 pagineGrupos Protectores en Química Orgánicafernandopessoa25Nessuna valutazione finora
- Regulación de La Expresión Génica en ProcariontesDocumento32 pagineRegulación de La Expresión Génica en ProcariontesBenjamin Padilla ParodiNessuna valutazione finora
- Teoria de Termodinamica - CengelDocumento12 pagineTeoria de Termodinamica - Cengelfedex_59Nessuna valutazione finora
- Equilibrio IonicoDocumento19 pagineEquilibrio IonicoSoraya Lorena Colque GómezNessuna valutazione finora
- Mobil Mining CoolantDocumento12 pagineMobil Mining CoolantValentina Andrea Gallardo CàceresNessuna valutazione finora
- Propiedades Nutritivas y Funcionales de La Mashua (Tropaeolum Tuberosum)Documento9 paginePropiedades Nutritivas y Funcionales de La Mashua (Tropaeolum Tuberosum)FrankJhoninoJFQuispeNessuna valutazione finora
- Reacciones químicas en disolución acuosaDocumento10 pagineReacciones químicas en disolución acuosaJosué Alessandro Bendezú OchoaNessuna valutazione finora
- 2.3 Identificación de Cationes Del Grupo Tercero: A. Ensayos para Confirmar Plomo (II)Documento3 pagine2.3 Identificación de Cationes Del Grupo Tercero: A. Ensayos para Confirmar Plomo (II)NAHOMI MARIE VILLAVICENCIO LLAMOJANessuna valutazione finora
- Causas de La SalinidadDocumento27 pagineCausas de La SalinidadCarol ladinoNessuna valutazione finora
- Creacion de Emprendimientos Solidarios1Documento139 pagineCreacion de Emprendimientos Solidarios1Ismael OsunaNessuna valutazione finora
- Solucionario química bimestral grado 4Documento3 pagineSolucionario química bimestral grado 4JAIRO JHOEL HUAMAN PEÑANessuna valutazione finora
- Contenido de HumedadDocumento10 pagineContenido de HumedadWalterFredyGutierrezCanazaNessuna valutazione finora
- Propiedades MalaquitaDocumento8 paginePropiedades MalaquitaBruno Cornejo del MarNessuna valutazione finora
- Acidos Nucleicos Power PointDocumento38 pagineAcidos Nucleicos Power PointBrayan PinazoNessuna valutazione finora
- Metabolismo de ProteínasDocumento18 pagineMetabolismo de Proteínas120384Nessuna valutazione finora
- Calor EspecificoDocumento14 pagineCalor EspecificoJahira PonceNessuna valutazione finora
- Manual de Radioprotección CROSDocumento35 pagineManual de Radioprotección CROSyuribeth hernandezNessuna valutazione finora
- Programa de monitoreo ambiental minería artesanalDocumento10 paginePrograma de monitoreo ambiental minería artesanalCarlos BartoloNessuna valutazione finora
- Práctica # 05 Separaciones FísicasDocumento6 paginePráctica # 05 Separaciones FísicasLuz Aurita García MenaNessuna valutazione finora
- Puentes de Fibra de CarbonoDocumento50 paginePuentes de Fibra de CarbonoReddy MChNessuna valutazione finora
- Determinacion de Cu y PB en CarneDocumento6 pagineDeterminacion de Cu y PB en CarneBryant VelasquezNessuna valutazione finora
- WPS precalificada SMAW variables esencialesDocumento6 pagineWPS precalificada SMAW variables esencialesJahir Morales100% (1)
- Tarea - 2 Fundamentacion-FarmacologiaDocumento8 pagineTarea - 2 Fundamentacion-FarmacologiaDayana MolinaNessuna valutazione finora
- Carbono Orgánico y Propiedades Del SueloDocumento29 pagineCarbono Orgánico y Propiedades Del SuelomolangoNessuna valutazione finora
- El Cemento PórtlandDocumento10 pagineEl Cemento PórtlandEduOliveraGuevaraNessuna valutazione finora
- Epitermal Intermedia Sulfuracion Maji PaulDocumento25 pagineEpitermal Intermedia Sulfuracion Maji PaulKath VasNessuna valutazione finora
- Agralco 2016Documento48 pagineAgralco 2016Miguel Raya FeriaNessuna valutazione finora
- Hidroxido de CalcioDocumento10 pagineHidroxido de CalcioD Ale VCNessuna valutazione finora
- Estructura Cristalina (V. Alcántara)Documento25 pagineEstructura Cristalina (V. Alcántara)Anonymous HZa6PcNessuna valutazione finora
- 3º ESO Unidad 4Documento18 pagine3º ESO Unidad 4Sara María Bello SalcedoNessuna valutazione finora
- 1CALCULO DE ESFUERZOS EN VIGAS Mejorado 2017Documento6 pagine1CALCULO DE ESFUERZOS EN VIGAS Mejorado 2017mercyNessuna valutazione finora
- (Acv-S08) Evaluación en Línea 07 (Ep) Quimica Inorganica 13126Documento7 pagine(Acv-S08) Evaluación en Línea 07 (Ep) Quimica Inorganica 13126Kevin SNNessuna valutazione finora