Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Informe 12 Quimica Analitica II
Caricato da
George Saavedra ZamoraCopyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Informe 12 Quimica Analitica II
Caricato da
George Saavedra ZamoraCopyright:
Formati disponibili
UNIVERSIDAD DE GUAYAQUIL
Facultad de Ciencias Químicas
Laboratorio de Química Analítica
Informe de Laboratorio Nº12
1. TEMA: Determinación porcentual de H2O2 en el agua oxigenada por yodometría
2. MARCO TEÓRICO
El yodo es un agente oxidante que se puede usar para titular agentes reductores
moderadamente fuertes. Por otro lado, el ion yoduro es un agente reductor suave, y
sirve como base para determinar agentes oxidantes fuertes.
Las titulaciones con I2 se llaman métodos yodimétricos. Estas titulaciones en general
se realizan en soluciones desde neutras o suavemente alcalinas (pH 8), hasta
débilmente ácidas. Si el pH es demasiado alcalino, el I2 se desproporcionará en hipo
yodato y yoduro:
I2 + 2OH- → IO- + I- + H2O
El yodo tiene una baja solubilidad en agua, pero el complejo I3- es muy soluble, de
modo que las soluciones de yodo se preparan disolviendo I2 en una solución
concentrada de yoduro de potasio:
I2 + I- → I-3
Por tanto, el I-3es realmente la especie que se usa en la titulación (D.Christian, 2009)
El ion yoduro es un agente reductor débil y reduce agentes oxidantes fuertes. Sin
embargo, no se usa como titulante, principalmente debido a la falta de un sistema
indicador visual adecuado, así como por otros factores, como la rapidez de la
TORRES JIMÉNEZ OSCAR ANDRÉS G1 C
reacción. Cuando se agrega un exceso de yodo a una solución de un agente
oxidante, se produce I2 en una cantidad equivalente al agente oxidante presente.
Por tanto, este I2 se puede titular con un agente reductor, y el resultado sería el
mismo que si se titulara directo el agente oxidante. El agente titulante que se usa es
tiosulfato de sodio. (Burns, 2011)
El punto final para las titulaciones yodo métricas se detecta con almidón. La
desaparición del color azul del almidón -I2 indica el final de la titulación. El almidón
no se agrega al principio de la titulación, cuando la concentración de yodo es alta.
En vez de esto, se agrega poco antes del punto final, cuando el color del yodo diluido
se vuelve amarillo pálido. Hay dos razones para esto: una es que el complejo yodo-
almidón sólo se disocia lentamente, y se tendría un punto final difuso si se adsorbiera
una gran cantidad de yodo en el almidón; la segunda razón es que gran parte de las
titulaciones yodométricas se realizan en un medio fuertemente ácido, y el almidón
tiende a hidrolizarse en solución ácida. (Harris, 2001).
En el método yodo métrico, se adiciona ioduro en exceso a la muestra de agua
oxigenada en medio ácido. El iodo liberado se titula con una solución de tiosulfato de
sodio (Na2S2O3) previamente valorada.
H2O2 + 2H+ + 2 I– → I2 + 2H2O
Reacción de titulación:
I2 + 2S2O32- → S4O62– + 2I-
La concentración de las soluciones de agua oxigenada comercial se expresa en
volúmenes, que indica el volumen de oxígeno (medido en mL o L) que, en
condiciones normales de presión y temperatura, pueden formarse por
TORRES JIMÉNEZ OSCAR ANDRÉS G1 C
descomposición del peróxido de hidrógeno contenido en una unidad de volumen de
muestra (también medida en mL o L). (GALLEGO PICÓ Alejandrina, 2013)
Se usa almidón como indicador de yodo. En una disolución que no tenga otra especie
coloreada, es posible ver el color de una disolución de I3-. Con almidón, el límite de
detección se puede rebajar en un factor de 10. En las yodimetrías, el almidón se
puede añadir al principio de la valoración La primera gota en exceso de I3-, después
del punto de equivalencia, colorea de azul oscuro la disolución. El almidón no debe
añadirse en estas reacciones, sino inmediatamente antes del punto de equivalencia
en la que se detecta visualmente por la decoloración del I3
Las soluciones estándar de yodo se pueden preparar pesando el yodo puro y
haciendo la dilución en un matraz volumétrico. El yodo se purifica mediante
sublimación y se adiciona a una solución concentrada de KI, la cual se pesa antes y
después de la adición del yodo. Sin embargo, es costumbre estandarizar la solución
con un estándar primario y el As2O3 es el que más se utiliza. En cuanto la
estandarización del tiosulfato de sodio, el estándar más obvio es el yodo puro, pero
rara vez se lo utiliza ya que resulta difícil manejarlo y pesarlo. Así que lo más común
es emplear un proceso yodométrico, un agente oxidante que liberara yodo a partir
de yoduro. (Douglas Skoog, 2015)
3. OBJETIVO GENERAL:
Determinar por método yodométrico el porcentaje de peróxido de hidrogeno
presente en el agua oxigenada.
4. OBJETIVOS ESPECÍFICOS:
Realizar la valorización del agua oxigenada con tiosulfato de sodio 0.1 N para la
determinación del valor real de nuestra muestra comercial.
Comprender la acción que produce el almidón para cambiar el color de nuestra
muestra en el punto final.
Realizar los cálculos estequiometricos para la determinación porcentual de
peróxido de hidrogeno presente en nuestra muestra.
TORRES JIMÉNEZ OSCAR ANDRÉS G1 C
TORRES JIMÉNEZ OSCAR ANDRÉS G1 C
5. MATERIALES, REACTIVOS Y EQUIPOS:
MATERIALES:
Soporte universal
Pipetas volumétricas
Vasos de precipitación
Auxiliar de pipeteo
1 matraz aforado de 500ml
3 Matraz Erlenmeyer
1 bureta de 50mL
1 embudo
1probeta
1Piseta
EQUIPOS:
Balanza analítica
Sorbona
REACTIVOS
Agua destilada, libre de CO2
Ácido sulfúrico diluido
Solución Tiosulfato de sodio 0,1N
Agua oxigena
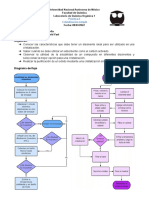
6. PROCEDIMIENTO:
En un matraz Erlenmeyer se toman de 5 a 20 mL de muestra para análisis.
Se agregan 20 mL de H2SO4 2N.
Adicionar 0.85 g de KI.
Guardar en la oscuridad durante 30 min.
Después de ese tiempo, valorar con Tiosulfato de sodio 0.1N. Hasta color
amarillo.
TORRES JIMÉNEZ OSCAR ANDRÉS G1 C
Agregar almidón y valorar con solución de Tiosulfato de sodio 0.1N.hasta
que se vuelva transparente.
7. RESULTADOS
Reacciones:
H2O2 + 3KI + 2H → I3- + 2H2O
I-3 + 2S2O32- → 3I- + S4O62-
PREPARACIÓN DE LA MUESTRA (CONSUMIR 10ML)
0.1003 eqq N𝑎2 𝑆2 𝑂3 1mol N𝑎2 𝑆2 𝑂3 1mol 𝐻2 𝑂2
× 0.010L x 𝑥
1L 1eqqN𝑎2 𝑆2 𝑂3 2mol N𝑎2 𝑆2 𝑂3
34𝑔𝐻2 𝑂2 100𝑚𝐿 𝐻2 𝑂2
× 𝑥 = 0.57 𝑚𝐿 𝐻2 𝑂2
1𝑚𝑜𝑙𝐻2 𝑂2 3𝑔𝐻2 𝑂2
VALORACIÓN 1
0.1103eqq N𝑎2 𝑆2 𝑂3 1mol N𝑎2 𝑆2 𝑂3 1mol 𝐻2 𝑂2
× 0.0178L x 𝑥
1L 1eqqN𝑎2 𝑆2 𝑂3 2mol N𝑎2 𝑆2 𝑂3
34𝑔𝐻2 𝑂2 100 𝐻2 𝑂2
× 𝑥 = 3.34% 𝐻2 𝑂2
1𝑚𝑜𝑙𝐻2 𝑂2 1𝑚𝐿𝐻2 𝑂2
8. ANÁLISIS DE RESULTADOS:
El porcentaje práctico que obtuvimos de H2O2 fue más bajo (3.34%) a la
presentación que hace la muestra cuyo porcentaje comercial es del 10%.
Nuestro consumo experimental nos dio 17.8mL además solo realizamos una
valoración por lo cual no se podrá sacar promedio ni coeficiente de variación.
TORRES JIMÉNEZ OSCAR ANDRÉS G1 C
9. CONCLUSIONES Y RECOMENDACIONES
CONLUSIONES:
Realizamos la valorización del agua oxigenada con tiosulfato de sodio 0.1 N
determinando que el valor real no coincide con el que expresa nuestra muestra
comercial.
Comprendimos que el cambio de color azul indica la presencia del ion yodo e
incluso puede indicar el punto final de una reacción.
Realizamos los cálculos estequiometricos determinando que el valor porcentual de
nuestra muestra fue de 3.34% esto pudo variar en el momento de que nuestra
muestra fue destapada.
RECOMENDACIONES:
Dejar reposar nuestra muestra el tiempo indicado para mejor resultado.
Colocar nuestra muestra en un sitio sin presencia de luz debido a que el yodo
se oxida con facilidad.
Utilizar una muestra totalmente nueva y sellada.
Es crucial el uso de papel aluminio para tapar nuestra muestra mientras se la
deja reposar.
10.
Bibliografía
Brown. (2011). Quimica. Pearson Educación.
Burns, R. A. (2011). Fundamentos de la Quimica. En F. d. Quimica. Mexico: PEARSON ISBN: 978-
607-32-0683-9.
Christian, G. (2009). QUIMICA ANALITICA. México: McGRAW-HILL ISBN-8429171312.
Douglas A. Skoog, D. M. (2014). fundamentos quimica analitica - novena edicion . España:
Publicado en inglés por Brooks/ISBN: 978-0-495-55828-6.
Harris, D. C. (2001). Análisis químico cuantitativo. Barcelona: ISBN: 9788429172225.
TORRES JIMÉNEZ OSCAR ANDRÉS G1 C
TORRES JIMÉNEZ OSCAR ANDRÉS G1 C
Potrebbero piacerti anche
- Informe 1 Identificacion de CarbohidratosDocumento5 pagineInforme 1 Identificacion de CarbohidratosMireya Parra67% (6)
- Marco TeóricoDocumento7 pagineMarco TeóricoFrank HurtadoNessuna valutazione finora
- LAb Metabolismo PRACTICA 2Documento5 pagineLAb Metabolismo PRACTICA 2Cesar GarciaNessuna valutazione finora
- Determinacion Gravimetrica de R2O3 en Un CementoDocumento4 pagineDeterminacion Gravimetrica de R2O3 en Un Cementofrancisco0% (1)
- Las Fichas Cómo Instrumentos de Trabajo en La Investigación DocumentalDocumento3 pagineLas Fichas Cómo Instrumentos de Trabajo en La Investigación DocumentalGeorge Saavedra ZamoraNessuna valutazione finora
- EjerciciosDocumento12 pagineEjerciciosAngie Nahomi Vega Pizarro50% (4)
- Practica 1 FactorizacionDocumento6 paginePractica 1 Factorizacionjesus neiraNessuna valutazione finora
- Volumetría de Formación de Complejos - EstudiantesDocumento8 pagineVolumetría de Formación de Complejos - EstudiantesAlejandra DíazNessuna valutazione finora
- Gravime. I.agr.20.Corregido ProblemaDocumento28 pagineGravime. I.agr.20.Corregido ProblemaDANIEL CHAVEZ MICHANessuna valutazione finora
- Grupo 4 AplicacionesPermanganometriaDocumento13 pagineGrupo 4 AplicacionesPermanganometriaHenny GabrielaNessuna valutazione finora
- Determinación de Cloruros en Una Muestra Acuosa Mediante Dos MetodosDocumento5 pagineDeterminación de Cloruros en Una Muestra Acuosa Mediante Dos MetodosximenaNessuna valutazione finora
- INFORME PRACTICA 3 CALOR DE DISOLUCION Y DE NEUTRALIZACION-comprimidoDocumento13 pagineINFORME PRACTICA 3 CALOR DE DISOLUCION Y DE NEUTRALIZACION-comprimidoDimar MontejoNessuna valutazione finora
- Volumetria de PrecipitacionDocumento4 pagineVolumetria de Precipitacion93arte50% (2)
- 09 Practica 7. Determinacion de ColesterolDocumento6 pagine09 Practica 7. Determinacion de ColesteroloscarNessuna valutazione finora
- Quimica Analitica Practica 03Documento8 pagineQuimica Analitica Practica 03Meléndez Meléndez John CharlesNessuna valutazione finora
- Prac-3-Determinacion de Acidez de La LecheDocumento7 paginePrac-3-Determinacion de Acidez de La LecheUchiha Frank No Hay Otro100% (1)
- Titulacion Por El Metodo de VolhardDocumento13 pagineTitulacion Por El Metodo de VolhardDanerNessuna valutazione finora
- Informe ArgentometriaDocumento5 pagineInforme ArgentometriaPaola JosefaNessuna valutazione finora
- Presentacion RedoxDocumento19 paginePresentacion RedoxPaola FloresNessuna valutazione finora
- Acido AcetilsalicilicoDocumento3 pagineAcido AcetilsalicilicoValentina SaenzNessuna valutazione finora
- Informe de Analitica Terminado Titulacion Potenciometrica PDFDocumento11 pagineInforme de Analitica Terminado Titulacion Potenciometrica PDFHabitaciones Para ParejasNessuna valutazione finora
- Qa2 TP3 Grupo5Documento5 pagineQa2 TP3 Grupo5Jonathan SeoNessuna valutazione finora
- Informe Completo de Determinación de Yodo en SalDocumento17 pagineInforme Completo de Determinación de Yodo en SalIsayana SozaNessuna valutazione finora
- AlcalinidadDocumento10 pagineAlcalinidadLore G AcostaNessuna valutazione finora
- Determinación de Hierro Por El Método de OrtofenantrolinaDocumento3 pagineDeterminación de Hierro Por El Método de OrtofenantrolinaBonnet HernándezNessuna valutazione finora
- Copia de Copia de Reporte-Práctica-1-LSO-1Documento4 pagineCopia de Copia de Reporte-Práctica-1-LSO-1Ana Sofia Padron SalasNessuna valutazione finora
- 04 Guía - Glicósidos CardiotónicosDocumento4 pagine04 Guía - Glicósidos CardiotónicosDiana Quiroga BuenaventuraNessuna valutazione finora
- Analisis Organico Primer ParcialDocumento42 pagineAnalisis Organico Primer ParcialManuel LoireNessuna valutazione finora
- Aplicación Analítica de La IodimetríaDocumento4 pagineAplicación Analítica de La IodimetríaEvelyn Paguay Carrillo100% (1)
- Practica 6Documento5 paginePractica 6miguelNessuna valutazione finora
- Determinación de Humedad Mediante Secado en EstufaDocumento5 pagineDeterminación de Humedad Mediante Secado en EstufaVanesa Lima LimaNessuna valutazione finora
- Práctica 1 - Etapa 1Documento5 paginePráctica 1 - Etapa 1Isabel LópezNessuna valutazione finora
- Experimento 8 PDFDocumento8 pagineExperimento 8 PDFLuïz A. Pinto Jr.Nessuna valutazione finora
- Cromatografía AzúcaresDocumento4 pagineCromatografía AzúcaresPatricia AmoresNessuna valutazione finora
- 11 Titulaciones Por Precipitación Mediante PotenciometríaDocumento2 pagine11 Titulaciones Por Precipitación Mediante PotenciometríaDavid Garcia0% (1)
- Deber de Polarimetría y Refractometría 28-12-2018Documento2 pagineDeber de Polarimetría y Refractometría 28-12-2018Farmacia Reina del Cisne100% (1)
- Marcha Sistematica para Cationes Sin El Empleo de h2sDocumento5 pagineMarcha Sistematica para Cationes Sin El Empleo de h2sKelly N Martinez AlmenteroNessuna valutazione finora
- Informe #4 Análisis PotenciometricoDocumento4 pagineInforme #4 Análisis PotenciometricoValee MartiinezNessuna valutazione finora
- Informe: Síntesis de Auxiliares de Formulación Síntesis de Estearato de Calcio y de MagnesioDocumento8 pagineInforme: Síntesis de Auxiliares de Formulación Síntesis de Estearato de Calcio y de MagnesioJorge Andrés Zambrano LeitónNessuna valutazione finora
- Practica de LipidosDocumento5 paginePractica de LipidosEsther SoledadNessuna valutazione finora
- PRACTICA 4 ANALISIS POR RETROVALORACION (Aspirina) PDFDocumento3 paginePRACTICA 4 ANALISIS POR RETROVALORACION (Aspirina) PDFDiana SalcedoNessuna valutazione finora
- Metodos Volumetricos IndirectosDocumento4 pagineMetodos Volumetricos IndirectosPabloSanchezNessuna valutazione finora
- Informe 6 Quimica AnaliticaDocumento10 pagineInforme 6 Quimica Analiticabianca leyvaNessuna valutazione finora
- Explicación Procedimiento YodometríaDocumento6 pagineExplicación Procedimiento YodometríaJulio Otarola Jimenez100% (2)
- Practica2dibenzalacetona Por La Condensación AldolDocumento2 paginePractica2dibenzalacetona Por La Condensación AldolYani TicasNessuna valutazione finora
- Determinación Yodométrica de Hipocloritos en Un BlanqueadorDocumento6 pagineDeterminación Yodométrica de Hipocloritos en Un BlanqueadorSandra Milena Saldarriaga SalazarNessuna valutazione finora
- Informe 4Documento19 pagineInforme 4laury suarezNessuna valutazione finora
- Valoracion Poteniometrica Con Acido FosforicoDocumento18 pagineValoracion Poteniometrica Con Acido FosforicoCinthya Knowles Gonzalez Rios100% (1)
- Laboratorio 4 5 6 7Documento3 pagineLaboratorio 4 5 6 7Wanda Polet Salvatierra Paz0% (3)
- CarbohidratosDocumento21 pagineCarbohidratoskatherin100% (1)
- Obtención Del YodoDocumento2 pagineObtención Del Yodojeniffer valverdeNessuna valutazione finora
- Preparaciones de Soluciones Amortiguadoras CompletoDocumento9 paginePreparaciones de Soluciones Amortiguadoras CompletoAbdielE.AraúzNessuna valutazione finora
- Determinacion de Cenizas (Digestion Húmeda)Documento3 pagineDeterminacion de Cenizas (Digestion Húmeda)Diana Fuentes Huerta0% (1)
- #1 Informe Titulación Ácido BenzoicoDocumento6 pagine#1 Informe Titulación Ácido BenzoicoSamuel Flores RamirezNessuna valutazione finora
- Tarea 4de Quimica Organica IIDocumento6 pagineTarea 4de Quimica Organica IILucía lorenaNessuna valutazione finora
- Practica 11 OrganicaDocumento8 paginePractica 11 OrganicaChe Zambrano BadilloNessuna valutazione finora
- Cationes Del Grupo II BDocumento10 pagineCationes Del Grupo II BNicolas MacasNessuna valutazione finora
- Imforme Determinación de Ácido CítricoDocumento8 pagineImforme Determinación de Ácido CítricoMaria MendozaNessuna valutazione finora
- Determinación de CalcioDocumento4 pagineDeterminación de CalcioDavid Cruz ZamoraNessuna valutazione finora
- BenzofenonaDocumento18 pagineBenzofenonadominicNessuna valutazione finora
- Practica 5Documento14 paginePractica 5Alvaro Cabrera DiazNessuna valutazione finora
- YodometriaDocumento13 pagineYodometriaCarla Villca Lopez100% (1)
- Practica n4Documento3 paginePractica n4Guido Taco MNessuna valutazione finora
- 4.2. - Problemas de TemperaturaDocumento11 pagine4.2. - Problemas de TemperaturaGeorge Saavedra ZamoraNessuna valutazione finora
- 4.2. - Problemas de TemperaturaDocumento11 pagine4.2. - Problemas de TemperaturaGeorge Saavedra Zamora0% (1)
- 1-6. - La Energía Deber CasaDocumento13 pagine1-6. - La Energía Deber CasaGeorge Saavedra ZamoraNessuna valutazione finora
- Dispersion de MicroorganismosDocumento33 pagineDispersion de MicroorganismosGeorge Saavedra ZamoraNessuna valutazione finora
- FitoquimicaDocumento9 pagineFitoquimicaGeorge Saavedra ZamoraNessuna valutazione finora
- Pensamiento Economico de AristotelesDocumento2 paginePensamiento Economico de AristotelesGeorge Saavedra ZamoraNessuna valutazione finora
- QUIMERISMO George SaavedraDocumento4 pagineQUIMERISMO George SaavedraGeorge Saavedra ZamoraNessuna valutazione finora
- Por Qué A La Gente No Le Gusta Ni Aporta para La LiteraturaDocumento1 paginaPor Qué A La Gente No Le Gusta Ni Aporta para La LiteraturaGeorge Saavedra ZamoraNessuna valutazione finora
- Balta Crisologo Rafael AnaniasDocumento123 pagineBalta Crisologo Rafael AnaniasAnonymous Ct05gTpvNessuna valutazione finora
- Guia de Bioquimica 2010 PDFDocumento98 pagineGuia de Bioquimica 2010 PDFrosa sanchezNessuna valutazione finora
- JuanOrdoñez Zullytorres Karoltorres Gabrielquintero Giselaguzmán AlejandracagueñasDocumento12 pagineJuanOrdoñez Zullytorres Karoltorres Gabrielquintero Giselaguzmán AlejandracagueñasVIVIAN ROCIO BARRETO CASTRONessuna valutazione finora
- Tabla de OxácidosDocumento2 pagineTabla de OxácidosJuan ValenzuelaNessuna valutazione finora
- Guion Metodologico 2o ParcialDocumento14 pagineGuion Metodologico 2o ParcialSolo ParaNessuna valutazione finora
- Rotulos ConsultoriosDocumento18 pagineRotulos ConsultoriosCDGBNessuna valutazione finora
- Tabla PeriodicaDocumento5 pagineTabla PeriodicaEddye Molina JaenNessuna valutazione finora
- Informe N°9 Acidos-BaseDocumento9 pagineInforme N°9 Acidos-BaseSKEICY NICOLL NAVARRO OLIVERANessuna valutazione finora
- Quimica Uno Cromatografia de Enlazamiento MetalicoDocumento5 pagineQuimica Uno Cromatografia de Enlazamiento MetalicoDaniel GarciaNessuna valutazione finora
- Qui MicaDocumento3 pagineQui MicaCarlos YagualNessuna valutazione finora
- Practica 2 Equipo 4 Flores Perez y Jimenez RodriguezDocumento4 paginePractica 2 Equipo 4 Flores Perez y Jimenez RodriguezGarcia Ortiz Juan PabloNessuna valutazione finora
- Taller NomenclaturaDocumento3 pagineTaller Nomenclaturaest.juan.dsanchezNessuna valutazione finora
- Yodometria y Permanganimetria - CARLOS ANTONIO PROMOTOR RODRIGUEZ - 200520Documento4 pagineYodometria y Permanganimetria - CARLOS ANTONIO PROMOTOR RODRIGUEZ - 200520CARLOS ANTONIO PROMOTOR RODRIGUEZNessuna valutazione finora
- Resinas BulkDocumento1 paginaResinas BulkMayra MoisenNessuna valutazione finora
- Informe de Laboratorio - CorrosiónDocumento9 pagineInforme de Laboratorio - CorrosiónArturo Camaño100% (1)
- Practica 5 CompletaDocumento19 paginePractica 5 CompletaHADID ESTEBAN MORALESNessuna valutazione finora
- GelatinaDocumento5 pagineGelatinaAlvaro RamosNessuna valutazione finora
- Cap 9 Lípidos 2023Documento43 pagineCap 9 Lípidos 2023anaiflorcitaNessuna valutazione finora
- Sosa CausticaDocumento2 pagineSosa CausticaAbrilNessuna valutazione finora
- MetabiomedDocumento4 pagineMetabiomedapi-216024326Nessuna valutazione finora
- Practica Disolventes ActivosDocumento6 paginePractica Disolventes Activosdevil_house4Nessuna valutazione finora
- Copia de 1. Pesar Una Cápsula de Porcelana Vacía, Limpia y Seca. 2. Añadir Aproximadamente 1,0 Gramo de Mezcla Compuesta de Arena, NaCl y Alcanfor.Documento5 pagineCopia de 1. Pesar Una Cápsula de Porcelana Vacía, Limpia y Seca. 2. Añadir Aproximadamente 1,0 Gramo de Mezcla Compuesta de Arena, NaCl y Alcanfor.juan sebastian carrillo castroNessuna valutazione finora
- 2da Expo (Gomez P.)Documento12 pagine2da Expo (Gomez P.)Jean Pierre Gerónimo FloresNessuna valutazione finora
- Quimica Organica INFORME ALDEHIDOS Y CETONASDocumento8 pagineQuimica Organica INFORME ALDEHIDOS Y CETONASZair AxelNessuna valutazione finora
- RxorgDocumento24 pagineRxorgWaldir Pumachari PurihuamanNessuna valutazione finora
- Examen - (ACV-S04) Evaluación en Línea 3 - EPDocumento5 pagineExamen - (ACV-S04) Evaluación en Línea 3 - EPJose Carranza VasquezNessuna valutazione finora
- ParteDocumento12 pagineParteFanny MazaNessuna valutazione finora
- Colegio Informático "San Juan de Vera": Conceptos GeneralesDocumento6 pagineColegio Informático "San Juan de Vera": Conceptos GeneralesSeree OcamposNessuna valutazione finora