Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
1 Obtencion Del Etilenglicol CD PDF
Caricato da
anon_22914928Titolo originale
Copyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
1 Obtencion Del Etilenglicol CD PDF
Caricato da
anon_22914928Copyright:
Formati disponibili
OBTENCION DEL ETILENGLICOL
Índice
1. OBJETIVOS
1.1. OBJETIVO GENERAL
1.2. OBJETIVOS ESPECIFICOS
2. FUNDAMENTO TEORICO
2.1. ANTECEDENTES
2.2. ETILENGLICOL
2.3. PROPIEDADES FISICAS Y QUIMICAS
2.3.1. PROPIEDADES FISICAS DEL ETILENGLICOL
2.3.2. PROPIEDADES QUIMICAS DEL ETILENGLICOL
2.3.2.1. OXIDACION
2.4. PRODUCCION
2.4.1. PRODUCCION INDUSTRIAL
2.4.1.1. OXIDO DE ETILENO
2.4.2. PRODUCCION RESUMIDA
2.5. USOS DE ETILENGLICOL}
2.6. TOXICIDAD
2.7. TOXICOCINETICA
3. MATERIALES Y REACTIVOS
4. PROCEDIMIENTO EXPERIMENTAL
5. CALCULOS Y RESULTADOS
6. CONCLUSIONES Y RECOMENDACIONES
7. BILBLIOGRAFIA
8. ANEXOS
OBTENCION DEL ETILENGLICOL 1
OBTENCIÓN DEL ETILENGLICOL
1. OBJETIVOS
1.1. OBJETIVO GENERAL
Sintetizar experimentalmente el etilenglicol a partir de etanol
1.2. OBJETIVOS ESPECIFICOS
Usar el equipo adecuado para cada parte de la reacción.
Efectuar experimentalmente, reacciones estudiadas en química orgánica ll.
Conocer métodos de identificación para el etilenglicol.
Realizar la ruptura del peryodato, sobre el etilenglicol, para obtener un
aldehído. Realizar la prueba de Fehling para comprobar la presencia del
aldehído
Conocer el componente esencial del cual se obtiene el etilenglicol.
Observar experimentalmente las características de los productos presentes
durante el proceso.
2. FUNDAMENTO TEORICO
2.1. ANTECEDENTES
Según la mayoría de las fuentes, el químico francés Charles-Adolphe Wurtz (1817-
1884) preparó el primer etilenglicol en 1856. Primero trató el "yoduro de etileno"
(C2H4I2) con acetato de plata y luego hidrolizó el "diacetato de etileno" resultante
con hidróxido de potasio. Wurtz nombró su nuevo compuesto como "glicol" porque
compartía cualidades tanto con el alcohol etílico (con un grupo hidroxilo) como con
la glicerina (con tres grupos hidroxilo). En 1859 Wurtz preparó etilenglicol a través
de la hidratación del óxido de etileno. No parece haber habido fabricación
comercial ni aplicación del etilenglicol antes de la Primera Guerra Mundial, cuando
OBTENCION DEL ETILENGLICOL 2
se sintetizó a partir de dicloruro de etileno en Alemania y se utilizó como un
sustituto del glicerol en la industria de explosivos.
2.2. ETILENGLICOL
El etilenglicol (sinónimos: etanodiol, glicol de etileno, glicol) es un compuesto
químico que pertenece al grupo de los dioles. Es un líquido transparente, incoloro,
ligeramente espeso como el almíbar y leve sabor dulce. Por estas características
organolépticas se suelen utilizar distintos colorantes para reconocerlo y así
disminuir las intoxicaciones por accidente. A temperatura ambiente es poco volátil,
pero puede existir en el aire en forma de vapor. Se fabrica a partir de la hidratación
del óxido de etileno (epóxido cancerígeno).
2.3. PROPIEDADES FISICAS Y QUIMICAS DEL ETILENGLICOL
2.3.1. PROPIEDADES FÍSICAS DEL ETILENGLICOL
OBTENCION DEL ETILENGLICOL 3
El etilenglicol es un líquido transparente, incoloro, inodoro, de sabor dulce. Es
higroscópico y completamente miscible con muchos disolventes polares, tales
como el agua, alcoholes, éteres de glicol, y acetona. Sin embargo, su solubilidad
es baja en solventes no polares, tales como el benceno, tolueno, dicloroetano, y
cloroformo.
Las siguientes son algunas de las propiedades físicas de etilenglicol:
Punto de ebullición a 101,3 kPa 197,60 ºC
Punto de fusión -13,00 ºC
Densidad a 20 ºC 1,1135 g / cm3
Índice de refracción, nD20 1,4318
Calor de vaporización a 101,3 kPa 52,24 kJ / mol
Calor de combustión 19,07 MJ / kg
Temperatura crítica 372ºC
Volumen crítico 6515,73 kPa
Presión crítica 0.186L / mol
Punto de inflamabilidad 111ºC
Temperatura de ignición 410ºC
OBTENCION DEL ETILENGLICOL 4
Límite explosivo inferior 3,20 vol%
Límite explosivo superior 53vol%
Viscosidad a 20 ºC 19.83 mPa · s
Coeficiente de dilatación cúbica a 20ºC 0,62 × 10-3 K-1
El etilenglicol es difícil de cristalizar; cuando se enfría, se forma una masa
altamente viscosa subenfriada, que finalmente solidifica para producir una
sustancia semejante al vidrio.
2.3.2. PROPIEDADES QUÍMICAS DEL ETILENGLICOL
Al igual que otros alcoholes el etilenglicol se somete a las reacciones típicas de
sus grupos hidroxilo. Aquí sólo consideraremos las características químicas
especiales y reacciones industrialmente importantes del etilenglicol. Los dos
grupos hidroxilo adyacentes permiten la ciclación, y la policondensación; uno o
ambos de estos grupos funcionales pueden, por supuesto, también reaccionan
para dar otros derivados.
2.3.2.1. OXIDACIÓN
El etilenglicol se oxida fácilmente por el oxígeno, ácido nítrico, y otros agentes
oxidantes para formar un número de aldehídos y ácidos carboxílicos. Los
productos típicos derivados de las funciones alcohólicas son glicolaldehıdo
(HOCH2 CHO), ácido glioxílico (HOCH2COOH), glioxal (CHOCHO), ácido glioxílico
(HCO- COOH), ácido oxálico (HOOCCOOH), formaldehído (HCHO) y ácido
fórmico (HCOOH). La variación de las condiciones de reacción puede conducir a
la formación selectiva de un producto de oxidación deseado. La oxidación en fase
gaseosa con aire en presencia de catalizadores de cobre es de importancia
industrial para la producción de glioxal. Escisión glicol se produce en solución
OBTENCION DEL ETILENGLICOL 5
ácida con agentes oxidantes, tales como el permanganato, peryodato, o
tetraacetato de plomo. La ruptura del enlace C-C produce principalmente
formaldehído, parte del cuales se oxida adicionalmente a ácido fórmico.
2.4. PRODUCCION
2.4.1. PRODUCCION INDUSTRIAL
Hidrólisis de Óxido de Etileno
Método de producción actual
Actualmente sólo se utiliza un método para la producción industrial de etilenglicol.
Este método se basa en la hidrólisis de óxido de etileno obtenido por oxidación
directa de etileno con aire o con oxígeno. El óxido de etileno se hidroliza
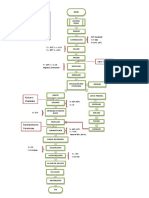
térmicamente a etilenglicol sin un catalizador. La Figura 1 muestra un esquema
simplificado de una planta de producción de etilenglicol por este método. La
mezcla óxido de etileno - agua se precalienta a alrededor de 200 ºC, por lo que el
óxido de etileno se convierte en etilenglicol. También se producen di-, tri- y tetra-
glicoles de polietileno, pero con rendimientos decrecientes respectivamente.
Figura 1. Diagrama de flujo para una planta de glicol
a) Reactor; b) la columna de secado; c) columna monoetilenglicol; d) columna de
dietilenglicol; e) columna de trietilenglicol; f) intercambiador de calor.
La formación de estos homólogos superiores es inevitable porque el óxido de
etileno reacciona con los etilenglicoles con más rapidez que con el agua; sin
OBTENCION DEL ETILENGLICOL 6
embargo, sus rendimientos pueden reducirse al mínimo si se utiliza un exceso de
agua - normalmente se emplea un exceso molar de 20 veces.. Aunque los valores
se determinaron mediante el uso de ácido sulfúrico como catalizador, también se
aplican como una buena aproximación para la reacción sin catalizador. Por lo
tanto, en la práctica casi el 90% del óxido de etileno se puede convertir en
monoetilenglicol, el 10% restante reacciona para formar homólogos superiores.
Se han descrito muchos catalizadores en la literatura que son capaces de
optimizar la selectividad o reducir la temperatura de reacción y el exceso de agua
requerida. Se sabe que los ácidos y bases aceleran la velocidad de reacción. La
cinética de la catálisis con ácidos y bases de la hidrólisis de óxido de etileno se
han investigado a fondo. La viabilidad industrial de la catálisis con columnas de
intercambio iónico en fase líquida y fase gaseosa ha sido probada. Aunque el uso
de catalizadores permite bajar la temperatura de reacción, la selectividad no fue
significativamente mayor. Además, el catalizador necesita ser separado y luego, o
bien ser devuelto a la mezcla de reacción o ser reemplazado. Como resultado de
estos inconvenientes, estos tipos de catálisis no han demostrado ser de uso
comercial. Sin embargo, varios catalizadores que mejoran la selectividad han sido
descritos en patentes; entre estos se incluyen molibdatos, vanadatos,
intercambiadores de iones, y compuestos orgánicos de antimonio. Sin embargo,
sus ventajas todavía no parecen justificar su utilización a escala industrial.
2.4.1.1. OXIDO DE ETILENO (OE).
El producto químico más importante derivado del etileno, que no es precursor de
polímeros, es el óxido de etileno. El OE es un gas tóxico a temperatura ambiente,
de Tb = 10,7 °C y Tf = -112 °C que forma mezclas explosivas con el aire. Es
soluble en agua en todas proporciones. Es un compuesto tóxico, inflamable y se
maneja líquido en recipientes a presión.
La producción mundial de este compuesto es de unos 14,5 millones de Tm/año. El
óxido de etileno se produce en instalaciones con capacidad superior a las 100.000
Tm/año. Actualmente el proceso de fabricación consiste en la oxidación directa del
etileno con una corriente de oxígeno utilizando catalizadores de plata. El oxígeno
se obtiene mediante una planta de fraccionamiento de aire. El catalizador contiene
OBTENCION DEL ETILENGLICOL 7
hasta un 15% en peso de plata, depositada en forma de capa fina sobre un
soporte inerte y poroso de alúmina (Al 2O3).
De los diversos productos secundarios derivados del óxido de etileno el más
importante es el etilenglicol. Es un líquido de Tb = 198 °C y Tf = -12 °C, soluble en
agua en todas proporciones. Es muy tóxico porque en el organismo se metaboliza
a ácido oxálico (HOOC-COOH). La producción mundial de etilenglicol es de
13,6x106 Tm. Se obtiene por adición de agua al óxido de etileno.
En el proceso industrial de fabricación se hace reaccionar el OE con agua en
exceso para evitar la formación de polímeros (10 veces en exceso molar).
La reacción puede llevarse a cabo en presencia de ácido sulfúrico como
catalizador a presión atmosférica y a 50-70 ºC, o bien sin catalizador a 200 ºC y de
20 a 40 atm. La selectividad es sólo del 90% y el rendimiento del 96%. La
fabricación de etilénglicol se realiza casi exclusivamente en un reactor acoplado al
de obtención de óxido de etileno por oxidación de etileno. La disolución resultante
se concentra por evaporación hasta el 70 %. El EG se purifica por destilación
fraccionada.
Posibles Mejoras y Desarrollos
El método de producción de glicol planteado anteriormente es el único con una
importancia industrial en la actualidad. Es un método simple, pero tiene algunos
inconvenientes importantes:
OBTENCION DEL ETILENGLICOL 8
1. La selectividad de la primera etapa - la producción de óxido de etileno - es
baja (alrededor de 80%).
2. La selectividad de la hidrólisis de óxido de etileno es baja - alrededor de
10% se convierte en di- y tri- etilenglicol.
3. El consumo de energía para la destilación de la gran cantidad de agua en
exceso es alta.
Por lo tanto, se ha llevado a cabo mucha investigación para mejorar este proceso.
La búsqueda de mejores catalizadores de plata es un objetivo para el punto 1. Los
puntos 2 y 3 deben ser considerados juntos, ya que una mayor selectividad para la
hidrólisis de óxido de etileno reduce automáticamente el exceso de agua
requerida.
2.3.2. PRODUCCIONES RESUMIDAS
El etilenglicol se produce a partir de etileno, mediante el compuesto
intermedio óxido de etileno. El óxido de etileno reacciona con agua produciendo
etilenglicol según la siguiente ecuación química.
C2H4O + H2O → HOCH2CH2OH
Esta reacción puede ser catalizada mediante ácidos o bases, o puede ocurrir en
un pH neutro a temperaturas elevadas. La mayor producción de etilenglicol se
consigue con un pH ácido o neutro en presencia de abundante agua. Bajo estas
condiciones, se puede obtener una productividad del 90%. Los principales
subproductos obtenidos son dietilenglicol, trietilenglicol, y tetraetilenglicol.
2.5. USOS DE ETILENGLICOL
Usos:
Anticongelante
Difusor de calor.
Con agua para impedir la congelación de motores y partes de los aviones
comerciales.
Para la fabricación de poliéster.
OBTENCION DEL ETILENGLICOL 9
Como Disolvente.
Para revelar fotografías.
Ingrediente de frenos hidráulicos.
Tintura de estampado.
Los usos del etilenglicol son varios debido a sus propiedades y estructura química.
Las mayores aplicaciones están en la industria automovilística y en aviación,
donde se utiliza como anticongelante del agua y como elemento para evitar el
hielo en las partes móviles.
Además, las aplicaciones del etilenglicol y sus usos en aviones favorecen el
deshielo, algo que lo hace muy adecuado a temperaturas inferiores a cero grados .
Otro uso es como disolvente de pintura. En la industria es utilizado en grandes
cantidades para disolver y eliminar las capas de pintura y evitar los restos de
tintes, también en plásticos.
En el campo de la fotografía el etilen-glicol sirve
como medio para el revelado.
Usos como anticongelante
Etilenglicol como anticongelantes, es posible que
esta aplicación sea la más conocida y extendida en
todo el mundo. Los usos del etilenglicol como
anticongelante son debidos a que tiene un punto de
ebullición alto.
En los climas fríos es necesario proteger los
automóviles y los vehículos de motor a combustión para evitar que el agua se
congele. Esta cambia de tamaño y puede romper las partes mecánicas, además
de bloquear el flujo del líquido. Mediante el uso de anticongelante con etilenglicol
es sencillo evitar la congelación.
¿Por qué se usa como refrigerante?
Porque no es corrosivo como otros materiales y sustancias e impide la
congelación. Además, al ser un líquido es capaz de lubricar y recorrer los
conductos necesarios sin importar que permanezca durante un tiempo inmóvil,
algo diferente a lo que sucede con otro anticongelante como es la sal.
2.6. TOXICIDAD
OBTENCION DEL ETILENGLICOL 10
La ingestión de cantidades muy altas de etilenglicol puede causar la muerte, en
tanto que cantidades mínimas pueden producir náusea, convulsiones, dificultad
para hablar, desorientación, y problemas en el corazón y el riñón. Los animales
hembras que sufrieron esta intoxicación por grandes cantidades de etilenglicol
tuvieron crías con defectos de nacimiento, mientras que los animales machos
experimentaron una disminución en el número de espermatozoides. Sin embargo,
estos efectos se observaron a niveles muy altos y no se espera que ocurran en
personas expuestas a niveles menores en sitios de residuos peligrosos.
El etilenglicol afecta a la química del organismo aumentando la cantidad de ácido,
lo que produce problemas metabólicos. La intoxicación se presenta como
depresión del sistema nervioso central e irritación en el sitio de absorción
inicialmente, seguido de acidosis metabólica e hipocalcemia.
Puede causar sordera, ceguera y puede dejar grandes secuelas cerebrales, y a
grandes dosis producir la muerte.
Es un disolvente orgánico con actividad nefrotóxica como se mencionó
anteriormente. Puede ocasionar necrosis tubular aguda que si no se trata a
tiempo, puede desencadenar una insuficiencia renal crónica y posteriormente la
muerte.
2.7. TOXICOCINETICA
Absorción: se absorbe eficazmente a través del tracto digestivo. Su absorción
respiratoria se ve dificultada por su acción irritante a ese nivel y su absorción
dérmica es escasa.
Biotransformación: el etilenglicol es oxidado por las mismas enzimas que
transforman el etanol y metanol (ADH (alcohol deshidrogenasa), MAOS(mono
amino oxidasas) y catalasas), formándose ácido glicólico (acidosis metabólica)
y ácido oxálico (metabolito final). El ácido oxálico tiene gran afinidad por
el calcio produciendo a nivel periférico una acumulación perivascular de oxalato de
calcio monohidratado, el cual posee forma de aguja, produciendo daño en estos
órganos.
Clínicamente puede manifestarse por una disminución del nivel de consciencia
(letargia), un estado comatoso (debido a la depresión del sistema nervioso central)
e insuficiencia renal aguda; se encuentra asociado a un desorden ácido-base
(específicamente por ácido glicólico) causando acidosis metabólica del tipo anión
gap (brecha aniónica), y osmolar elevados, pero si no se trabaja de forma rápida la
cantidad osmolar de intoxicación de etilenglicol será mucho menor, ya que el
etilenglicol al ser metabolizado deja menor cantidad disponible en niveles séricos,
disminuyendo esta medición y permitiendo dudar en el caso de pacientes que
puedan haber sufrido este tipo de intoxicación. Hay una disminución de la
OBTENCION DEL ETILENGLICOL 11
leucocitosis y aparición de cristales de oxalato de calcio monohidratado. No se
altera la concentración plasmática de sodio. Como fenómeno compensador al
estado de acidosis metabólica se desencadena un cuadro de hiperventilación con
excursiones respiratorias profundas (respiración de Kuss-Maul) disminuyendo la
presión parcial de CO2arterial y llevando a 99% de unión de oxígeno en
hemoglobina.
3. MATERIALES Y REACTIVOS
MATERIALES
Ítem Material Observación Cantidad
1 Pipeta graduada 10 mL 2
2 Pro pipetas 2
3 Balón redondo de 3 250 mL 1
bocas
4 Columna Vigreux 1
5 Cabeza de destilación 1
6 Tubo refrigerante 1
7 Mangueras y adaptaron 2
8 Alargadera 1
9 tubo recto de 15 cm 1
10 Matraz Erlenmeyer 250 mL 2
11 Vaso de precipitado 1000 mL 2
12 Tubo en U 1
13 tubos de ensayo 5
14 Gradilla 1
15 Termometro (Hg) 2
16 tapón de una entrada 5
17 Varilla de vidrio 1
18 Espátula 1
19 Vidrio Reloj 1
20 Piseta 1
21 Cepillo 1
22 Pinza de 3 dedos 4
23 Pinza Nuez 1
24 Embudo de 250 mL 1
decantación
25 Camisa calefactora 1
OBTENCION DEL ETILENGLICOL 12
REACTIVOS
Ítem Sustancia Formula Cantidad
1 Alcohol Etílico CH3CH2OH 20 mL
2 Ácido Sulfúrico H2SO4 5 mL
3 Agua de Cloro Cl2/H2O 20 mL
4 Hidróxido de Sodio NaOH 5g
5 Per yodato de Potasio KIO4 1g
6 Reactivo de Fehling
A/B
4. PROCEDIMIENTO EXPERIMENTAL
I. El primer paso a realizar en la síntesis de etilenglicol es deshidratar el
etanol para ello se debe armar un sistema como el mostrado en la fig. (1)
II. Mientras se mide 5 mL de ácido sulfúrico y se diluye en 5 mL de agua
destilada
III. Una vez armado el sistema se procede a la deshidratación del etanol
controlando la temperatura en 160 – 170 ºC
IV. El gas recolectado (eteno) pasara a burbujear en el matraz receptor
previamente cargado de 20 mL de agua de cloro esto para formar el 2
cloro etanol.
V. Es vital que al agregar el Hidróxido de Sodio al producto del paso IV esté
en una temperatura cercana a los bajo cero o en el mismo cero, esto para
asegurar que el Oxirano al tener un punto de ebullición de 10 ºC no se
evapore, dado también que es un gas toxico.
VI. Posteriormente se somete el mismo a una temperatura de no más de 30 ºC
para separar el Oxirano de posibles impurezas, además de que asi se
pueda hidrolizar con el agua acidulada, en el sistema mostrado en la fig.
(2).
VII. Una vez recolectado y formado el etilenglicol comprobar sus propiedades
químicas mediante las reacciones con Per yodato de potasio lo cual hace
que el glicol forme formaldehido y comprobar dicho grupo carbonilo con la
reacción de Fehling; cabe resaltar que al ser un glicol primario sus enlaces
son ligeramente ácidos y al reaccionar con un metal alcalino como el sodio
puede formas alcoholatos y esta sería otra forma de comprobar que la
sustancia obtenida es la deseada.
VIII. Registrar los datos experimentales.
OBTENCION DEL ETILENGLICOL 13
OBTENCION DEL ETILENGLICOL 14
5. CALCULOS, REACCIONES Y RESULTADOS
Reacciones Dadas:
Reacción #1
El proceso parte de 25 mililitros de etanol al 96% y 10 mililitros de solución de
ácido sulfúrico. Primeramente se calentó el ácido a 150 °C aproximadamente,
entonces, se añadió el etanol en el sistema para que sucediera su deshidratación.
H2O
t =170ºC
Etanol en medio de ácido sulfúrico caliente etileno + agua (deshidratación de
etanol).
Observaciones en la reacción:
- Se apreció el paso de gas por la columna de destilación y el refrigerante
hasta el recipiente colector, cerrado, con el agua de cloro.
- La temperatura se controló alrededor de los 170 °C.
- La reacción se dio por varios minutos, quedando un líquido oscurecido en el
balón.
Reacción #2
El gas generado fue a reaccionar con el agua de cloro.
Cl2/H2O HCl
Etileno + Agua de Cloro 2 Cloro Etanol + Ácido Clorhídrico
Observaciones en la reacción:
- El líquido (agua de cloro) cambia de color con la reacción dada.
OBTENCION DEL ETILENGLICOL 15
- El olor al abrir el sistema para la segunda etapa confirma la presencia del
etileno que no reacciona.
Reacción #3
Se utilizó el hidróxido de sodio en exceso para la reacción con el producto para
formar el óxido de etileno.
NaOH NaCl H2O
2 Cloro Etanol + Hidróxido de Sodio Óxido de etileno + Cloruro de Sodio + Agua
Observaciones en la reacción:
- Se presentó como reacción secundaria, la reacción entre el hidróxido de
sodio y el ácido clorhídrico, formándose agua y cloruro de sodio también.
- Se presentó la formación de precipitado, cloruro de sodio, el cual luego se
disolvió en el agua formada.
- Se sintió el olor característico del óxido de etileno con mucho cuidado.
Reacción #4
Se dejó calentar hasta los 30 °C el producto líquido, para que se separe el óxido
de etileno en forma gaseosa y pase a través del tubo en U hasta el recipiente con
agua acidulada con ácido sulfúrico para que se de la hidrólisis como reacción final.
H2SO4
H2O
Óxido de Etileno + Agua en Medio Ácido Etilenglicol
Observaciones en la reacción:
- El producto formado queda en conjunto con el agua acidulada en exceso,
ya que no se lo puede separar por destilación al ser su punto de ebullición
OBTENCION DEL ETILENGLICOL 16
superior a la del agua y además es soluble en agua al ser un compuesto
polar.
- Se observó el burbujeo en el líquido de partida, confirmándose la
separación del óxido de etileno del líquido para su posterior hidrólisis.
- Se formaron algunas pequeñas burbujas rojizas en el producto final.
- Se presentó el olor dulce característico del etilenglicol en el producto final.
Reacciones de Prueba:
Reacción 1:
Se pretendía utilizar ácido peryódico para la ruptura del enlace entre carbonos del
etilenglicol, entonces formando como producto 2 moles de formaldehido por cada
mol de etilenglicol, en una alícuota del producto final; sin embargo, no se disponía
de tal reactivo en laboratorio, entonces, se utilizó peryodato de potasio con el fin
de tener el radical peryodato en la reacción y esperando obtener el mismo
resultado:
-
IO4
2HCHO
Etilenglicol en medio de Peryodato 2 moles de Formaldehido
Observaciones de la reacción:
- Se observó un leve burbujeo en el líquido indicando que hubo reacción,
pero quedando precipitado por exceso del peryodato de potasio.
Reacción 2: Prueba de Fehling
HCHO + Cu2+ No Existe Reacción
Formaldehido + Cobre 2+ No reacciona
Observaciones de la reacción:
- La prueba de Fehling dio negativo, no se presentó cambios.
OBTENCION DEL ETILENGLICOL 17
En todo este proceso, no es posible obtener el rendimiento del proceso, ya que,
aunque se tengan los moles de partida, el rendimiento se desconoce por
desconocerse la composición del agua de cloro del laboratorio y además el
producto final está en medio de agua acidulada, de la cual, el producto buscado, el
etilenglicol, no pudo ser separado.
Análisis de Resultados
En la primera reacción, se utilizó un ácido diprótico, ya que este solo presta un
protón para que suceda la deshidratación del alcohol; en este punto, usar un ácido
como el ácido clorhídrico, no es conveniente, debido a que al donar un protón
este, queda un cloro libre, que puede influir en la reacción obteniéndose
resultados no esperados.
El problema de la primera reacción es que esta ocurre en el ácido calentado a 170
°C, lo cual hace que, al ingresar el etanol, además de etileno, pueda suceder la
destilación de algunos moles de etanol, además del agua formada, que puede salir
como vapor de agua. Para tratar de minimizar la salida de estos otros gases, se
trató poniendo la columna de destilación en contacto con hielo, de modo que la
temperatura de los gases baje más durante su paso por esta y pueda condensar
etanol, siguiendo su paso solamente el gas buscado; el problema de esto, es que
el hielo igualmente recibe calor y se derrite, poniendo en riesgo el equipo, por lo
cual ya no se consideró. Entonces, el producto formado con el agua de cloro no es
un producto puro, además del 2 cloro etanol, se presentó, posiblemente, el exceso
de agua de cloro, etanol destilado y agua. Al añadir el hidróxido de sodio, es
probable que este haya actuado sobre otros componentes además del que se
pretendía, por ello, se añadió un exceso; de todas formas, el rendimiento del
proceso se ve afectado ya con esto, lo cual lo consideramos cualitativamente. Se
mantuvo el producto con el epóxido en contacto con el hielo hasta armar el
sistema de la segunda etapa, ya que este tiene un punto de ebullición muy bajo,
superior a 0 grados pero inferior a la temperatura ambiente. El óxido de etileno se
separa aprovechando su punto de ebullición bajo, ya que el resto de componentes
del líquido tiene puntos de ebullición mucho mayores, entonces, se calentó hasta
30 °C la muestra, de modo que en forma de gas se separe el epóxido, lo cual se
apreció por el burbujeo en la muestra y por la presencia del gas en el tubo en U.
Una vez separado gas, este fue al recipiente con agua acidulada para su hidrólisis,
formándose entonces el etilenglicol, que era el producto principal buscado. El olor
característico de este confirmó su presencia. Se pretendió, como prueba, la
formación de un aldehído, el cual debería dar positivas las pruebas de aldehídos
conocidas; sin embargo, al no tener ácido peryódico en laboratorio, se usó
peryodato de potasio, ya que lo que nos importa del ácido peryódico es el radical
peryodato; sin embargo, la prueba de Fehling dio negativa en el supuesto
OBTENCION DEL ETILENGLICOL 18
formaldehido, pero sí se apreció reacción en la supuesta formación de este
aldehído. Lo que pudo haber sucedido es que se haya dado la reacción del
etilenglicol con el potasio presente, un metal; por lo cual, no se presentó el
formaldehido esperado en la prueba y por tanto la prueba de Fehling dio negativo.
6. CONCLUSIONES Y RECOMENDACIONES
En previas pruebas, no hubo un buen rendimiento debido a una mala interacción
con los reactivos con consecuencia en reacciones secundarias y fugas en el
sistema, a pesar de que hubo un control continuo de temperatura en la reacción;
ya que de este factor dependía la sintetizacion.
Todo el proceso fue de mucho cuidado, para sintetizar adecuadamente los
productos esperados; si bien en la práctica, en base a las pruebas realizadas no
existe un porcentaje de certeza de que se haya obtenido el etilenglicol, quizá como
recomendación si se le practicaba más ensayos a nuestra muestra de producto,
tendríamos más evidencia de que es el producto que deseábamos obtener,
además que nos podemos apoyar en la teoría. También considerando al olor,
viscosidad y manifestaciones que se mostraban, tampoco se puede evidenciar que
no se obtuvo el etilenglicol. A simple vista con la teoría tenemos el producto, ya
que cumple sus propiedades físicas, pero en las propiedades químicas es donde
no se obtuvo el producto ya que las pruebas no salieron efectivas.
Se aplicaron, no con mucha precisión, reacciones estudiadas, las que confirmaban
la presencia de etilenglicol, que no dieron resultados esperados debido a errores
en el sistema; como fuga de gases.
Es recomendable tener un sistema con selladuras de plastilina.
Se debe tener cuidado con el tratamiento del óxido de etileno ya que es un gas
toxico, es por eso que se trabajó con hielo, ya que muestra sus características
cancerígenas en estado gaseoso
7. BILBLIOGRAFIA
- Etilenglicol, https://es.wikipedia.org/wiki/Etilenglicol
- Etilenglicol, https://www.textoscientificos.com/quimica/etilenglicol
- Etilenglicol, usos, https://www.acidohialuronico.org/etilenglicol/
- Etoxido, https://www.eii.uva.es/organica/qoi/tema-05.php
OBTENCION DEL ETILENGLICOL 19
8. ANEXOS
OBTENCION DEL ETILENGLICOL 20
OBTENCION DEL ETILENGLICOL 21
OBTENCION DEL ETILENGLICOL 22
OBTENCION DEL ETILENGLICOL 23
OBTENCION DEL ETILENGLICOL 24
OBTENCION DEL ETILENGLICOL 25
SISTEMA ARMADO
OBTENCION DEL ETILENGLICOL 26
OBTENCION DEL ETILENGLICOL 27
OBTENCION DEL ETILENGLICOL 28
UNIVERSIDAD MAYOR DE
SAN ANDRES
OBTENCION
DEL
ETILENGLICOL
DOCENTE: Ing. Eduardo Invernizzi
AUXILIAR DE DOCENCIA: Univ. Hortencia Flores Mamani
MATERIA: Química Orgánica ll Laboratorio
CARRERA: Ingeniería Química
ESTUDIANTES:
- Bravo Loayza Luis Miguel
- Heredia Catacora José Ignacio
- Huanca Ramos Heidy Jovana
- Linares Laura Ximena
FECHA:
21 de noviembre de 2018
OBTENCION DEL ETILENGLICOL 29
Potrebbero piacerti anche
- CumenoDocumento6 pagineCumenoJoaquin Valdez FernandezNessuna valutazione finora
- Cc3b3mo Defenderse de Los Ataques Verbales 2Documento32 pagineCc3b3mo Defenderse de Los Ataques Verbales 2darloJDNessuna valutazione finora
- además de ser optimizado para al incluir palabras clave como reacciones químicas y reactoresDocumento6 pagineademás de ser optimizado para al incluir palabras clave como reacciones químicas y reactoresNatali CondeñaNessuna valutazione finora
- Ejercicio-2 BDM y BdEDocumento3 pagineEjercicio-2 BDM y BdEalba sarabiaNessuna valutazione finora
- Balance de Masa-2009Documento24 pagineBalance de Masa-2009Niche ChavezNessuna valutazione finora
- Coeficiente Total de Transferencia de Calor - TLV - Compañía Especialista en Vapor (America Latina)Documento6 pagineCoeficiente Total de Transferencia de Calor - TLV - Compañía Especialista en Vapor (America Latina)Luis Anselmo CastilloNessuna valutazione finora
- DBP DFP diagramas procesosDocumento42 pagineDBP DFP diagramas procesosMarcelaDenisseMuzzioNessuna valutazione finora
- Intercambiadores de CalorDocumento105 pagineIntercambiadores de CalorGladis tarifaNessuna valutazione finora
- Ev 2 PropiDocumento3 pagineEv 2 PropiandiesNessuna valutazione finora
- PLANTA-DE-TRATAMIENTO-DE - AguaDocumento10 paginePLANTA-DE-TRATAMIENTO-DE - AguaAndresNessuna valutazione finora
- Balances de materia en procesosDocumento2 pagineBalances de materia en procesosCamila EscobarNessuna valutazione finora
- Ejercicio PDFDocumento5 pagineEjercicio PDFZhakaDeVirgoNessuna valutazione finora
- Tarea 3Documento5 pagineTarea 3Uriel Fabián Del Río Félix100% (1)
- Investigacion Hidrodesalquilacion de ToluenoDocumento6 pagineInvestigacion Hidrodesalquilacion de ToluenoBetty SantiagoNessuna valutazione finora
- Ejercicios de Torres Agotamiento y EnriqueciminetoDocumento1 paginaEjercicios de Torres Agotamiento y EnriqueciminetoCristhian CarrizalesNessuna valutazione finora
- SÍNTESISDocumento17 pagineSÍNTESISGasersithoOnneNessuna valutazione finora
- Torre enfriadora agua condensadores 45°C 29°CDocumento7 pagineTorre enfriadora agua condensadores 45°C 29°CEduardo LeijaNessuna valutazione finora
- Balance de MateriaDocumento14 pagineBalance de MateriaKelly GCNessuna valutazione finora
- Curso Operaciones Unitarias I 9000 OperaDocumento22 pagineCurso Operaciones Unitarias I 9000 OperaCoorporacion Info tvNessuna valutazione finora
- 3 Determinacion de Coeficiente de Transferencia de Calor en Un Evaporador de Doble EfectoDocumento14 pagine3 Determinacion de Coeficiente de Transferencia de Calor en Un Evaporador de Doble EfectoFranco Guadalupe Castillo VegaNessuna valutazione finora
- Reactor So3Documento50 pagineReactor So3williamyc7Nessuna valutazione finora
- Celda de ArmfieldDocumento2 pagineCelda de ArmfieldLuisa TorresNessuna valutazione finora
- PROCESO DE OBTENCIÓN DE OLEFINAS POR CRAQUEO DE NAFTADocumento6 paginePROCESO DE OBTENCIÓN DE OLEFINAS POR CRAQUEO DE NAFTAWilliam Ledesma MascaroNessuna valutazione finora
- Informe Final de SimuDocumento56 pagineInforme Final de Simuirving_mendoza_58Nessuna valutazione finora
- Planta de FenolDocumento10 paginePlanta de FenolkatepiNessuna valutazione finora
- Ejercicios Del Punto de Pliegue PDFDocumento2 pagineEjercicios Del Punto de Pliegue PDFGilbert Rodriguez PalmaNessuna valutazione finora
- Problema 1Documento12 pagineProblema 1Kartel KalientitoxNessuna valutazione finora
- 6 1Documento3 pagine6 1Alejandra CuzcoNessuna valutazione finora
- Capit 7 P. ResueltosDocumento17 pagineCapit 7 P. ResueltosYerely OrtízNessuna valutazione finora
- Producción Industrial de AmoniacoDocumento6 pagineProducción Industrial de AmoniacoMagda CervantesNessuna valutazione finora
- Columnas de Rectificacion 23Documento25 pagineColumnas de Rectificacion 23Rodrigo Salinas HuamancondorNessuna valutazione finora
- Informe Rio AtoyacDocumento34 pagineInforme Rio AtoyacLa Zarzuela SantiagoNessuna valutazione finora
- NullDocumento114 pagineNullRafaela MontañoNessuna valutazione finora
- Apuntes OP3-Esxtracción y HumidificaciónDocumento32 pagineApuntes OP3-Esxtracción y HumidificaciónbeatrizNessuna valutazione finora
- Parcial FinalDocumento3 pagineParcial FinalSebastian OcampoNessuna valutazione finora
- Obtencion Industrial Del PropilenoDocumento3 pagineObtencion Industrial Del PropilenoCynthia Hernández AmpueroNessuna valutazione finora
- Examen 2do Parcial MNADocumento2 pagineExamen 2do Parcial MNAAlfredo AzcorraNessuna valutazione finora
- Guía10 - PRQ500 - 2PDocumento7 pagineGuía10 - PRQ500 - 2PJhoselyn Pijuan ViscarraNessuna valutazione finora
- Destilacion DiferencialDocumento12 pagineDestilacion DiferencialaddaNessuna valutazione finora
- Destilación de Amoníaco/Agua - Comparativa de Métodos de Dimensionamiento de TorreDocumento36 pagineDestilación de Amoníaco/Agua - Comparativa de Métodos de Dimensionamiento de TorreSANTIAGO FIUMENessuna valutazione finora
- Método de OndaDocumento9 pagineMétodo de OndaAna VelázquezNessuna valutazione finora
- Reacciones químicas en equilibrioDocumento6 pagineReacciones químicas en equilibrioSilvanaEscobedoNoveloNessuna valutazione finora
- 02 Ejerc EVAPORACIONDocumento2 pagine02 Ejerc EVAPORACIONCINTIA GOMEZ AUCEBIASNessuna valutazione finora
- Cortes de Petróleo: Análisis y CaracterizaciónDocumento2 pagineCortes de Petróleo: Análisis y CaracterizaciónLaura Torres100% (1)
- Método Ponchon-Savarit para calcular el número de platos en una columna de destilación fraccionadaDocumento11 pagineMétodo Ponchon-Savarit para calcular el número de platos en una columna de destilación fraccionadaJose Carlos RubiNessuna valutazione finora
- Banco de Preguntas Mecanica de FluidosDocumento5 pagineBanco de Preguntas Mecanica de FluidosSandra ColqueNessuna valutazione finora
- Producción de fenol: análisis de rutas de reacción y viabilidad económicaDocumento3 pagineProducción de fenol: análisis de rutas de reacción y viabilidad económicaSamantha OlveraNessuna valutazione finora
- Destilacion Por Lotes 2Documento20 pagineDestilacion Por Lotes 2Fernando PalominoNessuna valutazione finora
- Determinación de la AEPT, número de etapas teóricas y número de unidades de transferencia en una columna de destilación con rellenoDocumento13 pagineDeterminación de la AEPT, número de etapas teóricas y número de unidades de transferencia en una columna de destilación con rellenoJavier JulianNessuna valutazione finora
- Destilación FUGDocumento77 pagineDestilación FUGMarcos Condorí PacoNessuna valutazione finora
- CH3COOC2H5Documento3 pagineCH3COOC2H5lizNessuna valutazione finora
- Ecuacion Cinetica Del Alcohol Isopropilico PDFDocumento88 pagineEcuacion Cinetica Del Alcohol Isopropilico PDFJorgeReyesNessuna valutazione finora
- Determinación Del Coeficiente de Fugacidad de La Acetona en Fase Vapor y Fase Líquida (Final)Documento4 pagineDeterminación Del Coeficiente de Fugacidad de La Acetona en Fase Vapor y Fase Líquida (Final)Pipo Hernández100% (2)
- Ecología Proyecto III Canastas de PET FMADocumento7 pagineEcología Proyecto III Canastas de PET FMAJosee MaayaNessuna valutazione finora
- Capc3adtulo 10 Evaporadores PDFDocumento56 pagineCapc3adtulo 10 Evaporadores PDFclaudia tejada100% (1)
- Deshidratación Catalizada de D-Xilosa para La Obtención de FurfuralDocumento4 pagineDeshidratación Catalizada de D-Xilosa para La Obtención de FurfuralFernando HuarocNessuna valutazione finora
- Etil Engli ColDocumento15 pagineEtil Engli ColRoberto RamírezNessuna valutazione finora
- Obtencion Del Etilenglicol PDFDocumento13 pagineObtencion Del Etilenglicol PDFVeronica PatiNessuna valutazione finora
- Informe de Etilen GlycolDocumento34 pagineInforme de Etilen GlycolJenny Ojeda CastillonNessuna valutazione finora
- Obtención del etilenglicolDocumento13 pagineObtención del etilenglicolJosé Gregorio MartínezNessuna valutazione finora
- Curso Matlab 1Documento16 pagineCurso Matlab 1anon_22914928Nessuna valutazione finora
- Cuestionario 8 y 9Documento1 paginaCuestionario 8 y 9anon_22914928Nessuna valutazione finora
- Grupo7 CGDocumento17 pagineGrupo7 CGanon_22914928Nessuna valutazione finora
- Libro Cuali Tabla AnionesDocumento1 paginaLibro Cuali Tabla Anionesanon_22914928Nessuna valutazione finora
- Cuestionario 8 y 9Documento1 paginaCuestionario 8 y 9anon_22914928Nessuna valutazione finora
- Enfermedades Causadas Por El EstañoDocumento8 pagineEnfermedades Causadas Por El Estañoanon_229149280% (1)
- Grupo 5 ChichaDocumento2 pagineGrupo 5 Chichaanon_22914928Nessuna valutazione finora
- HepatitisDocumento9 pagineHepatitisanon_22914928Nessuna valutazione finora
- VitiligoDocumento6 pagineVitiligoanon_22914928Nessuna valutazione finora
- GLUCOLISISDocumento2 pagineGLUCOLISISanon_22914928Nessuna valutazione finora
- Optimización de Parámetros Del Proceso de Elaboración de Chicha de JoraDocumento18 pagineOptimización de Parámetros Del Proceso de Elaboración de Chicha de Joraatila117Nessuna valutazione finora
- Prevencion y Lucha Contra IncendiosDocumento68 paginePrevencion y Lucha Contra IncendiosxtusNessuna valutazione finora
- PLAGUCIDASDocumento55 paginePLAGUCIDASanon_22914928Nessuna valutazione finora
- PETROLERASDocumento30 paginePETROLERASanon_22914928Nessuna valutazione finora
- Prevencion y Lucha Contra IncendiosDocumento68 paginePrevencion y Lucha Contra IncendiosxtusNessuna valutazione finora
- Plomo... Parte 3Documento10 paginePlomo... Parte 3anon_22914928Nessuna valutazione finora
- Libro 1Documento11 pagineLibro 1anon_22914928Nessuna valutazione finora
- Proceso Elab Ind ChichaDocumento1 paginaProceso Elab Ind Chichaanon_22914928Nessuna valutazione finora
- GlucolisisDocumento9 pagineGlucolisisKathiinha MeeaawNessuna valutazione finora
- Tratamiento de Aguas para Consumo Directo PDFDocumento34 pagineTratamiento de Aguas para Consumo Directo PDFanon_22914928Nessuna valutazione finora
- GLUCOLISISDocumento2 pagineGLUCOLISISanon_22914928Nessuna valutazione finora
- 1er Comunicado1Documento5 pagine1er Comunicado1LNessuna valutazione finora
- Prevencion y Lucha Contra IncendiosDocumento68 paginePrevencion y Lucha Contra IncendiosxtusNessuna valutazione finora
- GlucolisisDocumento9 pagineGlucolisisKathiinha MeeaawNessuna valutazione finora
- GlucolisisDocumento9 pagineGlucolisisKathiinha MeeaawNessuna valutazione finora
- GlucolisisDocumento9 pagineGlucolisisKathiinha MeeaawNessuna valutazione finora
- Paredes V PDFDocumento90 pagineParedes V PDFanon_22914928Nessuna valutazione finora
- GlucolisisDocumento9 pagineGlucolisisKathiinha MeeaawNessuna valutazione finora
- GlucolisisDocumento9 pagineGlucolisisKathiinha MeeaawNessuna valutazione finora
- 4 LevadurasDocumento7 pagine4 LevadurasHeriberto Richard IllanesNessuna valutazione finora
- Balance de MateriaDocumento8 pagineBalance de MateriaJunior Anderson Espiritu ZavaletaNessuna valutazione finora
- Proyecto JabonDocumento6 pagineProyecto JabondanielNessuna valutazione finora
- Charles Adolphe Wurtz. Adriano CastroDocumento3 pagineCharles Adolphe Wurtz. Adriano CastroJOSE ADRIANO CASTRO BRAVONessuna valutazione finora
- Mecanismo de La Reacción de CannizzaroDocumento8 pagineMecanismo de La Reacción de CannizzaroKaterin Liliana Núñez PiñerezNessuna valutazione finora
- Unidad 2 (Q.o. 1s 2021 p.6 Fausac WDLR)Documento36 pagineUnidad 2 (Q.o. 1s 2021 p.6 Fausac WDLR)Panky Monteagudo RevolorioNessuna valutazione finora
- QUIMICA ORGANICA Semana 1Documento5 pagineQUIMICA ORGANICA Semana 1Jonatan Isaac100% (1)
- El SilicioDocumento2 pagineEl SilicioferprissNessuna valutazione finora
- Obtención de Anhídrido Ftálico A Partir de Acido Ftálico Con Calentamiento y Reflujo de Anhídrido AcéticoDocumento6 pagineObtención de Anhídrido Ftálico A Partir de Acido Ftálico Con Calentamiento y Reflujo de Anhídrido AcéticoHerman Ruiz CalderinNessuna valutazione finora
- Anexo 2Documento21 pagineAnexo 2Ivonne Stefany Bautista AyalaNessuna valutazione finora
- Informe 4 Quimica de AlimentosDocumento10 pagineInforme 4 Quimica de AlimentosYenny Rojas ShuanNessuna valutazione finora
- Minerales 48-51Documento21 pagineMinerales 48-51heydyNessuna valutazione finora
- Química orgánica II: Definición de términos claveDocumento23 pagineQuímica orgánica II: Definición de términos claveChrysNessuna valutazione finora
- A) ÁtomosDocumento5 pagineA) ÁtomosPriscila Gutierrez AldunateNessuna valutazione finora
- Codex PDFDocumento451 pagineCodex PDFMontes MarNessuna valutazione finora
- Eteres y EsteresDocumento13 pagineEteres y EsteresXimena Acevedo Moncada100% (1)
- Inventario Sustancias Químicas Construcciones MilDocumento2 pagineInventario Sustancias Químicas Construcciones MilDiego Alejandro Londoño ValenciaNessuna valutazione finora
- Propiedades de La Proteínas 1. Introducción: Guía de Práctica de Bioquímica AgroindustrialDocumento2 paginePropiedades de La Proteínas 1. Introducción: Guía de Práctica de Bioquímica AgroindustrialJulian VillanuevaNessuna valutazione finora
- Práctica 10Documento11 paginePráctica 10Sara L MartinezNessuna valutazione finora
- Cuadro Guia de Componentes de NPTDocumento4 pagineCuadro Guia de Componentes de NPTkateelithNessuna valutazione finora
- Taller Reactante Limite y ExcesivoDocumento13 pagineTaller Reactante Limite y ExcesivoMARIA FERNANDA CORREA SANCHEZNessuna valutazione finora
- FIP Valves Handbook 12-2017 ES LRDocumento52 pagineFIP Valves Handbook 12-2017 ES LROmar GuillenNessuna valutazione finora
- Reporte PracticaDocumento15 pagineReporte PracticaGil Castelán ÁngelNessuna valutazione finora
- Jose Buelvas Prueba Pec 11Documento3 pagineJose Buelvas Prueba Pec 11DONALDO RODRIGUEZ PEINADONessuna valutazione finora
- Instituto Politécnico Nacional: Reyes Reyes Perla GabrielDocumento9 pagineInstituto Politécnico Nacional: Reyes Reyes Perla GabrielAlejandro De GarcíaNessuna valutazione finora
- Primera Prueba Escrita de Materiales de Ingeniería: Completar o Resaltar La Respuesta Según CorrespondaDocumento2 paginePrimera Prueba Escrita de Materiales de Ingeniería: Completar o Resaltar La Respuesta Según Correspondaoscar chavez melgarejoNessuna valutazione finora
- Exposicion de Quimica Informe Aldehidos y CetonasDocumento16 pagineExposicion de Quimica Informe Aldehidos y CetonasVictoria AlbarranNessuna valutazione finora
- Sesión 5Documento41 pagineSesión 5Adrián Lume HuayllaniNessuna valutazione finora
- Estabilidad de compuestos de coordinación de Ni(IIDocumento8 pagineEstabilidad de compuestos de coordinación de Ni(IIDafne Aline Piña RuizNessuna valutazione finora
- NormaDocumento9 pagineNormayetzintlinNessuna valutazione finora