Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Hidrometalurgia
Caricato da
Eder RysCopyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Hidrometalurgia
Caricato da
Eder RysCopyright:
Formati disponibili
LIXIVIACIÓN DE MINERAL DE COBRE
Lixiviación Ácida De Mineral De Cobre.
Hidalgo Morales Claudia Karla, Reyes Muñoz Eder Alberto
Reséndiz Campos Arely Ximena, Ruelas López César Arturo
Resumen―
Palabras clave―
Lixiviación ácida, mineral oxidado de cobre, Malaquita, concentración lixiviada, tiempo óptimo, extracción, ácido
sulfúrico, sulfato de cobre (CuSO4), colorimetría.
I. INTRODUCCIÓN
Los procesos hidrometalúrgicos para la
disolución (lixiviación) de cobre se utilizan
sobre todo en minerales que contienen óxidos
de cobre, de baja ley y/o complejos, y en
menor escala o para tratar concentrados de
sulfuros.
Los minerales de óxidos de cobre pueden PRIMERA PARTE
lixiviarse por diversos métodos (in situ en las 0. Separar una muestra de aproximadamente
minas, en terreros, en montones, o en 5 gramos de mineral y enviarla al MEB para
tanques) dado que el cobre pasa fácilmente a su cuantificación por Rayos X y fotografía.
la solución. Los reactivos lixiviantes más 1. Observar al microscopio las partículas que
utilizados son ácidos diluidos (sulfúrico pueden contener Cu presentes en el mineral.
principalmente, Clorhídrico y nítrico 2. Preparar una solución de ácido sulfúrico
ocasionalmente), o bien soluciones alcalinas que contenga 50 g/L.
amoniacales de carbonato de amonio. Cuando 3. Transferir 100 mL de la solución lixiviante
se utiliza un ácido diluido la reacción química al vaso de reacción.
que ocurre durante el proceso de lixiviación 4. Adicionar cuidadosamente 10 g de mineral
de malaquita es (por ejemplo para ácido de Cu al frasco vial.
sulfúrico): 5. Homogeneizar la solución, durante 30
minutos agitando eventualmente y observar
Cu2(OH)2CO3(s)+2H2SO4(acu) 2CuSO4 (acu) + CO2 (g) + 3H2O (L)
cuidadosamente el experimento para
determinar las condiciones para la
Para estudiar el avance de esta reacción
cuantificación del proceso de lixiviación.
química en el laboratorio, es necesario
6. Separar el sólido y observarlo al
estimar las concentraciones de las diferentes
microscopio.
especies. La concentración de Cu 2+ en una
disolución acuosa puede determinarse
mediante la comparación colorimétrica.
II. PROCEDIMIENTO EXPERIMENTAL
30 de agosto 2018. Universidad Nacional Autónoma de México. 1
Facultad de Química. Departamento de Ingeniería Metalúrgica
LIXIVIACIÓN DE MINERAL DE COBRE
1. Observar al microscopio las partículas que 1. ¿Qué se observa durante la reacción
contenían Cu presentes en el mineral. entre la solución lixiviante y el mineral?
Comparar con la muestra original y dar
conclusiones. Se produce una reacción de forma
2. Tomar muestras del licor de lixiviación en burbujeante producto de la reacción entre el
los tiempos definidos a partir de la mineral y el ácido de la solución lixiviante.
experimentación de la etapa anterior.
3. Cuantificar el cobre contenido en las 2. ¿A partir de qué momento se presentó
muestras de licor de lixiviación por la disolución?, ¿fue constante?
comparación directa con las soluciones de
concentraciones conocidas de cobre. al momento de tomar la muestra en el primer
4.- Tomar dos muestras de 1ml cada una, tiempo de 2 minutos ya se presentaba una
aforar a 50 ml y enviar ambas muestras para ligera coloración en el tubo de ensaye, por lo
la determinación de Cu y Fe por Absorción que la disolución se presentó antes de ese
atómica. tiempo. Conforme aumentó el tiempo la
5.- Comparar los resultados obtenidos entre coloración fue haciéndose más fuerte pero sin
el colorímetro óptico y absorción atómica para ser constante.
cobre y determinar la precisión del
colorímetro. 3. Describa cualitativamente la variación
Equipo, material y reactivos de la concentración de cobre en la solución
con respecto al tiempo.
• 6 Frascos viales de 30 mL.
• 5 Embudos para filtración. La concentración fue haciéndose mayor
• 1 soporte universal. respecto al tiempo porque la coloración de la
• 1 soporte para embudos. disolución era más oscura. Al minuto 2
• 1 espátula. presentaba un azul verdoso muy pálido, sin
• 1 vidrio de reloj. embargo a los 25 minutos el azul verdoso era
• 1 pipeta graduada de 5 mL. más intenso que incluso podía notarse a
• 1 pipeta graduada de 10 mL. simple vista.
• 10 tubos de ensaye.
• 1 matraz erlenmeyer de 500 mL.
• 1 pro pipeta. 4. Si la lixiviación hubiese transcurrido
• Papel filtro. durante 3 horas ¿Cómo cambiarían los
• Solución de H2SO4. resultados obtenidos?
• Mineral.
• Microscopio menagráfico. La concentración de Cu disuelto hubiese sido
mayor, por lo que la disolución hubiera
RESULTADOS Y DISCUSIÓN presentado un color azul intenso al término
de las 3 horas ya que se habría dejado
reaccionar todo el ácido de la disolución con
la malaquita del mineral y esta le haría
Primera parte. cambiar
30 de agosto 2018. Universidad Nacional Autónoma de México. 2
Facultad de Química. Departamento de Ingeniería Metalúrgica
LIXIVIACIÓN DE MINERAL DE COBRE
5. Discutir el efecto que tiene sobre la 5
lixiviación la acidez y la agitación.
4
Fe [ppm]
La agitación de igual forma influye en la tasa 3
pH=0.5
de recuperación ya que este factor provoca 2
pH=2
que el ácido penetre en los poros de las 1
pH=1
partículas en disolución y reaccione de
0
manera más eficaz 0 50 100
Tiempo [min]
La acidez es importante ya que a más acidez
mayor recuperación de producto sin embargo REFERENCIAS.
en la industria no se emplean soluciones muy La recuperación de cobre mediante
ácidas debido al mayor gasto de insumos que lixiviación-extracción con disolventes
hacen que el proceso no sea económicamente electrólisis: hacia siglo XXI.
rentable. http://revistademetalurgia.revistas.csic.es/i
AGRADECIMIENTOS. ndex.php/revistademetalurgia/article/viewFi
Agradecimiento a Gustavo, ayudante de la le/818/829
materia del laboratorio de hidrometalurgia (fecha de consulta: 30/10/2018).
por la aclaración de dudas en el transcurso de
las sesiones experimentales. • F. R Morral. Metalurgia general, tomo 1. Ed:
Reverté S. A. Barcelona 1990.
8
7
6
Cu [ppm]
5
4 pH=0.5
3 pH=2
2
1 pH=1
0
0 50 100
Tiempo [min]
Lixiviación ácida de un concentrado de Cu (calcopirita)
con ácido clorhídrico y cloruro férrico (HCl y FeCl3).
Hidalgo Morales Claudia Karla, Reyes Muñoz Eder Alberto
Reséndiz Campos Arely Ximena, Ruelas López César Arturo
Resumen―
En el presente trabajo se muestran los resultados cualitativos y cuantitativos del estudio de la lixiviación ácida
de un mineral carbonato de cobre, Calcopirita, en función de la variación de la concentración lixiviada respecto
al tiempo. Se cuantificó de manera aproximada la cantidad de CuSO4 disuelto mediante la técnica de colorimetría.
30 de agosto 2018. Universidad Nacional Autónoma de México. 3
Facultad de Química. Departamento de Ingeniería Metalúrgica
LIXIVIACIÓN DE MINERAL DE COBRE
Palabras clave―
Lixiviación ácida, mineral oxidado de cobre, calcopirita, concentración lixiviada, tiempo óptimo, extracción, ácido
sulfúrico, sulfato de cobre (CuSO4), colorimetría.
Objetivos
1. Conocer las diferentes etapas de un proceso de lixiviación y proponer un modelo cinético para
la disolución de la calcopirita.
2. Estudiar y observar el efecto de la acidez en la lixiviación.
3. Estudiar el efecto de la temperatura, concentración, tamaño de partícula, velocidad de agitación,
presencia de una agente oxidante, etc. sobre la lixiviación de un concentrado de calcopirita
4.-Determinar la etapa limitante de la reacción de disolución y calcular el valor de la energía de
activación Ea.
Objetivos
Caracterización de un mineral de Cobre.
Realizar una lixiviación ácida al mineral Calcopirita.
Lixiviación ácida de un concentrado de Cu (calcopirita) con ácido sulfúrico (H2SO4).
Conocer las diferentes etapas de un proceso de lixiviación y proponer un modelo cinético para la
disolución de la calcopirita.
Estudiar el efecto de la temperatura, concentración, tamaño de partícula, velocidad de agitación,
presencia de una agente oxidante, etc sobre la lixiviación de un concentrado de calcopirita
I. INTRODUCCIÓN
La Lixiviación o disolución del metal (valor
metálico) y la precipitación o recuperación del Modelo de reacción:
metal disuelto, constituyen las dos
operaciones unitarias esenciales de la CuFeS2 + 2O2 + 4H2SO4 ↔
2CuSO4 + 2FeSO4
Hidrometalurgia. + 4S° + 4H2O
La lixiviación de concentrados de calcopirita
con ácido sulfúrico utilizada en minerales de Si la reacción química es la etapa
cobre de baja ley es un proceso relativamente determinante de la velocidad, la gráfica del
nuevo, el cual envuelve una reacción miembro izquierdo de la ecuación (1) Vs
heterogénea entre el solidó CuFeS2 y la tiempo dará una expresión lineal.
solución lixiviante (acuoso H2SO4).
Uno de los problemas con los que se [1-(1-∞)1/3] = Ks t (1)
encuentra el metalurgista, es la adquisición
de datos concernientes a la cinética de los Modelo de difusión:
procesos de lixiviación. En forma general, un
proceso de lixiviación ocurre en tres etapas: La reacción de difusión de reactivos acuosos
a) Etapa de la difusión de los reactivos a puede considerarse como:
través del solidó.
b) Etapa de la reacción química en la
a Asól + b Bac ↔
c Csól + productos solubles
superficie del solidó. El paso limitante es la difusión de reactivos
c) Etapa de la difusión de productos solubles acuosos a la interfase, o la difusión de
desde la superficie del sólido. productos solubles a partir de esta, si la
Con base en las condiciones experimentales, gráfica del miembro izquierdo de la ecuación
uno de estos pasos es el más lento y por tanto (2) Vs tiempo da una relación lineal.
es la etapa limitante de la lixiviación.
30 de agosto 2018. Universidad Nacional Autónoma de México. 4
Facultad de Química. Departamento de Ingeniería Metalúrgica
LIXIVIACIÓN DE MINERAL DE COBRE
[ (1- 2/3∞)-(1-∞)2/3 ] =Kd t (2)
In K = In A- Ea/RT (3)
Donde:
∞ = Fracción de partícula mineral que ha La ecuación 3 describe la variación de la
reaccionado en un tiempo t. constante de velocidad con la temperatura. La
Ks = Constante cinética para el modelo de reacción
gráfica de In K vs In 1/T proporciona una
de superficie.
relación lineal cuando una misma etapa es la
Kd = Constante cinética para el modelo de
limitante de la velocidad a la temperatura
difusión.
examinada. Un proceso puede cambiar su
mecanismo de control químico a bajas
temperaturas (Ea alta) a control por difusión a
altas temperaturas (Ea baja)
La energía de activación aparente Ea se
relaciona con el cambio de entalpía para la
etapa determinante, sin embargo, no es
suficiente para especificar la etapa lenta en
un proceso de lixiviación. Puede ser útil en la
interpretación de los datos cinéticos.
Un proceso controlado por difusión se
caracteriza por ser ligeramente dependiente
de la temperatura y proceso controlado por
reacción química, es altamente dependiente
de la temperatura. La Ea de un proceso
controlado por difusión de iones, es menor a
6 Kcal/mol. En el otro caso, la Ea es mayor a
10 Kcal/mol. Así para un proceso cuya Ea cae
dentro del intervalo de 6 a 10 Kcal/mol, la
distinción de la etapa limitante no es posible.
El valor de la energía de activación Ea puede
obtenerse del análisis de la ecuación de
Arrhenius, escrita en la forma logarítmica:
Procedimiento Experimental
Se realizarán los siguientes experimentos:
EQUIPO PRIMERA SESIÓN SEGUNDA SESIÓN TERCERA SESIÓN
30 de agosto 2018. Universidad Nacional Autónoma de México. 5
Facultad de Química. Departamento de Ingeniería Metalúrgica
LIXIVIACIÓN DE MINERAL DE COBRE
Ácido Sulfúrico 50g/l Ácido Sulfúrico 50g/l Ácido Clorhídrico 0.1N
Tamaño Estándar Tamaño DIFERENTE Tamaño Estándar
1 Temperatura ambiente Temperatura ambiente Temperatura ambiente
Agitación 4 Agitación 4 Agitación 4
Ácido Clorhídrico 0.1N
Ácido Sulfúrico 25g/l Ácido Sulfúrico 50g/l
Cloruro Férrico 0.01N
Tamaño Estándar Tamaño Estándar
2 Temperatura ambiente Temperatura 60°C
Tamaño Estándar
Temperatura ambiente
Agitación 4 Agitación 4
Agitación 4
Ácido Clorhídrico 0.1N
Ácido Sulfúrico 50g/l Ácido Sulfúrico 50g/l
Cloruro Férrico 0.1N
Tamaño Estándar Tamaño Estándar
3 Temperatura ambiente Temperatura ambiente
Tamaño Estándar
Temperatura ambiente
Agitación 8 Agitación NEUMÁTICA
Agitación 4
1. Preparar 1L de solución lixiviante de ácido sulfúrico y las indicadas de Ácido Clorhídrico y
Cloruro férrico
2 colocar el sistema de lixiviación.
3. Transferir 120 ml de la solución de ácido matraz de reacción.
4. Colocar el refrigerante, el termómetro y el tapón en el matraz y calentar hasta obtener la
temperatura de operación deseada, bajo agitación magnética. Tomar un mililitro de solución y un
mililitro de solución de H2SO4 al 10%, aforar a 50 mL con agua destilada y numerarla como
muestra cero.
5. Adicionar el mineral de calcopirita conservando la relación de % de sólidos en pesos de 10.
6. Tomar muestras de 2 a 5 mL de solución a los tiempos de 1, 3, 5, 7, 15, 23, 30 y 45 minutos,
filtrando y colectando en el correspondiente frasco vial, cada una de éstas. Tomar 1 mL de la
solución filtrada, transferirlo a un matraz aforado de 100 mL, adicionar 1 mL de H2SO4 al 10% y
aforar con agua destilada. Transferir las soluciones a frascos de plástico de 125 mL para el análisis
de Cu2+ y Fe2+ en solución por absorción atómica.
7. Filtrar la mezcla resultante, guardar la solución para su uso posterior en las prácticas de
extracción por solventes y
almacenar el sólido resultante en el recipiente • 1 termómetro.
correspondiente. • 1 matraz aforado de 500 mL.
• 3 matraces aforados de 100 mL.
• 1 pipeta graduada de 5 mL.
Equipo, material y reactivos • 1 pipeta graduada de 1 mL.
• 1 Recipiente para baño María. • 1 propipeta.
• 1 parrilla de calentamiento con agitación • 1 espátula.
magnética. • 1 pH-metro.
• 1 barra magnética. • Papel filtro.
• 1 matraz de 3 bocas de 500 mL. • 3 embudos de filtración.
• 3 tapones de Hule. • 1 soporte para embudos.
• 1 tapón de hule horadado para sujetar un • 2 soportes universales.
termómetro.
30 de agosto 2018. Universidad Nacional Autónoma de México. 6
Facultad de Química. Departamento de Ingeniería Metalúrgica
LIXIVIACIÓN DE MINERAL DE COBRE
• 30 frascos vial de 30 mL etiquetados de
manera clara y sistemática. Efecto de la agitación neumática
• 1 Refrigerante.
• 1 pizeta.
• Mineral de Calcopirita (concentrado de 3.- Graficar % extracción, [1-(1-∞)1/3], [(1-
flotación). 2/3∞) -(1-∞)2/3] contra tiempo y determinar
• Ácido sulfúrico (H2SO4). con las gráficas si el proceso está controlado
por la reacción química o difusión.
• Frascos viales de 50 mL
• Embudo para filtración. 4.- Graficar In K vs 1/T y determinar el valor
• 1 espátula. de la energía de activación de la reacción.
• 1 vidrio de reloj. 5.- Discutir los resultados obtenidos y definir
• tubos de ensaye. la etapa determinante de reacción.
• 1 matraz Erlenmeyer de 500 mL. 6.- Discutir el efecto que tienen sobre la
• 1 propipeta. lixiviación la acidez, la temperatura y la
• Solución de H2SO4. agitación.
• Microscopio
• Agua destilada.
Manejo de Resultados
1.- Determinar la concentración de Cu2+ y Fe3+
en cada muestra y determinar la fracción de
mineral disuelta para cada muestra.
∞ = [Cu2+]sol /[Cu2+]Tot. o por peso de
muestra. a) b)
2.- Construir las gráficas que Figura 1. Cantidad de mineral, utilizado para la
lixiviación a), frasco contenedor del mineral b)
muestren el efecto de las siguientes
variables en el proceso de lixiviación y
tanto para Cu como para Fe:
Efecto de la concentración de ácido.
Efecto del tamaño de partícula
Efecto de la Temperatura
Figura 2. Montaje del procedimiento experimental a
Efecto de la velocidad de agitación
Efecto del tipo de ácido
Efecto de la concentración de oxidante
30 de agosto 2018. Universidad Nacional Autónoma de México. 7
Facultad de Química. Departamento de Ingeniería Metalúrgica
LIXIVIACIÓN DE MINERAL DE COBRE
T ambiente.
Figura 3. Equipo para medir el pH usado en la
práctica.
Tablas 1a. y 1b. Resultados absorción
Figura 4. Frasco contenedor de Ácido sulfúrico atómica para el elemento Cu en ppm, y
resultados absorción atómica para el
elemento Fe en ppm
Equipo 1.
10
8
Cu [ppm]
6
4
2
0
0 20 40 60 80
Tiempo [min]
Figura 5. Disolución de cobre
F00 F05 F10
70
60
50
Fe [ppm]
40
30
20
10
0
0 20 40 60 80
Tiempo [min]
Figura 6. Filtración de residuos
30 de agosto 2018. Universidad Nacional Autónoma de México. 8
Facultad de Química. Departamento de Ingeniería Metalúrgica
LIXIVIACIÓN DE MINERAL DE COBRE
Determinación de energía de activación y mecanismo controlante.
Ejemplo de cálculo para la determinación de x.
Datos:
𝑚𝑔
𝑝𝑝𝑚 =
𝐿
5 gramos de mineral.
Alícuota de 1 ml.
50 ml de aforo.
𝐴𝑙í𝑐𝑢𝑡𝑜𝑡𝑎 1 𝑚𝑙 1
𝐹𝑎𝑐𝑡𝑜𝑟 𝑑𝑒 𝑑𝑖𝑙𝑢𝑐𝑖ó𝑛 = 𝐹𝐷𝑖𝑙 = = =
𝐴𝑓𝑜𝑟𝑜 50 𝑚𝑙 50
𝐶𝑜𝑛𝑐.𝑑𝑖𝑙𝑢𝑖𝑑𝑎 = 𝐶𝑜𝑛𝑐.𝑖𝑛𝑖𝑐 ∗ 𝐹𝐷𝑖𝑙
Despejando 𝐶𝑜𝑛𝑐.𝑖𝑛𝑖𝑐 , se obtiene:
𝐶𝑜𝑛𝑐.𝑑𝑖𝑙𝑢𝑖𝑑𝑎 𝐶𝑜𝑛𝑐.𝑑𝑖𝑙𝑢𝑖𝑑𝑎
𝐶𝑜𝑛𝑐.𝑖𝑛𝑖𝑐 = = 1 → 50 ∗ 𝐶𝑜𝑛𝑐.𝑑𝑖𝑙𝑢𝑖𝑑𝑎
𝐹𝐷𝑖𝑙
50
𝑚𝑎𝑠𝑎 = 𝐶𝑜𝑛𝑐.𝑖𝑛𝑖𝑐 ∗ 𝑉𝑜𝑙 = 50 ∗ 𝐶𝑜𝑛𝑐.𝑑𝑖𝑙𝑢𝑖𝑑𝑎 ∗ 100 𝑚𝑙 = 5000 𝑚𝑙 ∗ 𝐶𝑜𝑛𝑐.𝑑𝑖𝑙𝑢𝑖𝑑𝑎
𝑚𝑔
𝐶𝑜𝑛𝑐.𝑑𝑖𝑙𝑢𝑖𝑑𝑎 = 𝑝𝑝𝑚 =
𝐿
𝑚𝑔
𝑚𝑎𝑠𝑎 = 5000 𝑚𝑙 ∗ 𝐶𝑜𝑛𝑐.𝑑𝑖𝑙𝑢𝑖𝑑𝑎 ∗
1000 𝑚𝑙
1𝑔
5 ∗ 𝐶𝑜𝑛𝑐.𝑑𝑖𝑙𝑢𝑖𝑑𝑎 ∗ ( 3 ) 5 ∗ 𝐶𝑜𝑛𝑐.𝑑𝑖𝑙𝑢𝑖𝑑𝑎
10 𝑚𝑔
𝑋= =
𝑚𝑎𝑠𝑎𝑖𝑛𝑖𝑐𝑖𝑎𝑙 𝑚𝑎𝑠𝑎𝑖𝑛𝑖𝑐𝑖𝑎𝑙 ∗ 103
𝑔
Ejemplo para condición a Temperatura ambiente y concentración 50 ⁄𝑙 de H2SO4.
𝐶𝑜𝑛𝑐.𝑑𝑖𝑙𝑢𝑖𝑑𝑎 = 3.1 𝑝𝑝𝑚
5 ∗ 𝐶𝑜𝑛𝑐.𝑑𝑖𝑙𝑢𝑖𝑑𝑎 5 ∗ 3.1
𝑋= = = 0.0031
𝑚𝑎𝑠𝑎𝑖𝑛𝑖𝑐𝑖𝑎𝑙 ∗ 103 5 ∗ 103
30 de agosto 2018. Universidad Nacional Autónoma de México. 9
Facultad de Química. Departamento de Ingeniería Metalúrgica
LIXIVIACIÓN DE MINERAL DE COBRE
Tabla 5. Fracciones reaccionadas a partir del tiempo, en condiciones de Temperatura
𝒈
ambiente y concentración 50 ⁄𝒍 de H2SO4.
Tiempo [min] Cu Fe
0 0 0
1 0.0031 0.0015
3 0.0032 0.002
5 0.0033 0.0024
7 0.0038 0.0029
10 0.0037 0.0028
15 0.0039 0.003
30 0.0041 0.0038
Tabla 6. Fracciones reaccionadas a partir del tiempo, en condiciones a una temperatura de
𝒈
60°C y concentración 50 ⁄𝒍 de H2SO4.
Tiempo [min] Cu Fe
0 0 0
1 0.00701 0.00546
3 0.00807 0.00671
5 0.00817 0.00691
7 0.00924 0.00781
10 0.00761 0.00654
15 0.00866 0.00769
30 0.01048 0.00985
Para el modelo de reacción:
1
𝐾𝑠 𝑡 = [1 − (1 − 𝑥)3 ]
1
F (x) = [1 − (1 − 𝑥)3 ]
Discusión.
Contamos con los datos de la temperatura ambiente (25°C) y 60°C, estos analizaremos datos a
temperatura de 25°C. En estas temperaturas notamos un incremento constante de fracción
reaccionada en cada una de las especies, siendo las más altas en 30 minutos, logrando un
máximo de 0.0105 de fracción reaccionada de Cu y 0.0099 de fracción reaccionada de Fe. Estos
últimos se logran en la temperatura más alta, ya que en ese mismo tiempo a 25°C se tiene una
fracción reaccionada de 0.0041 de Cu y 0.0038 de Fe. La explicación de esto es que
termodinámicamente las temperaturas más altas favorecen la lixiviación de las especies, esto
también se vería favorecido en presiones altas.
Aunque las reacciones lucen poco significativas sabemos que el proceso de lixiviación es un
proceso lento y en ocasiones poco eficiente.
30 de agosto 2018. Universidad Nacional Autónoma de México. 10
Facultad de Química. Departamento de Ingeniería Metalúrgica
LIXIVIACIÓN DE MINERAL DE COBRE
Si analizamos por separado las reacciones de acuerdo con la concentración de FeCl2 notamos
comportamientos logarítmicos en cada una de las concentraciones del reactivo usado, tiene un
incremento considerable al inicio y después se vuelve menos notoria la concentración de Fe y Cu
en cada uno de los análisis.
Mencionamos que la concentración de mejor eficiencia para el Cu fue de 0.05 mientras que en Fe
fue de 0.1. Considerando esto podemos darle preferencia a la extracción de un mineral u otro.
Por las velocidades de reacción analizamos que se trata de un mecanismo difusivo.
Bibliografía
• C. B Gill. Nonferrous Extractive Metallurgy. 1980.
• F. R Morral. Metalurgia general, tomo 1. Ed: Reverte S. A. Barcelona 1990.
30 de agosto 2018. Universidad Nacional Autónoma de México. 11
Facultad de Química. Departamento de Ingeniería Metalúrgica
LIXIVIACIÓN DE MINERAL DE COBRE
Extracción por solventes. Equilibrio y cinética.
Hidalgo Morales Claudia Karla, Reyes Muñoz Eder Alberto
Reséndiz Campos Arely Ximena, Ruelas López César Arturo
Resumen―
Palabras clave
determinado por la aplicación de los
Objetivos diagramas de Mc Cabe-Thiele a las curvas
experimentales de extracción y despojo.
Trazar las isotermas de extracción y despojo Para obtener las curvas de equilibrio de
del sistema Cu-LIX-622. extracción (loading), el extractante orgánico
se adiciona a varias relaciones de volumen,
V ac (cte.) /V org, y se mezclan hasta alcanzar
Tiempo de realización de la práctica: 12 el equilibrio.
horas Una vez separadas, las fases son analizadas
para determinar el contenido de metal. Los
resultados de la fase acuosa se grafican sobre
Fundamentación la abscisa y los resultados de la fase orgánica
sobre la ordenada.
Los procesos de extracción por solventes son La isoterma de despojo se obtiene de la misma
utilizados en escala industrial en la extracción manera, manteniendo el volumen de la fase
y purificación de metales. El metal extraído orgánica (R2Cu) fijo y graficando los
(loading) puede regresarse o despojarse a la resultados de la fase orgánica en las abscisas
fase acuosa en forma concentrada y y los de la fase acuosa en las ordenadas.
purificada (stripping) ajustando las
condiciones de la solución para disminuir la
solubilidad del metal en la fase orgánica. Procedimiento Experimental
El proceso de extracción y purificación de Primera sesión.
cobre de las soluciones de lixiviación se
expresa: 1. Preparar 160 mL de solución de Cu2+ 1 g/L
a pH 2.2 (o utilizar licor de la lixiviación, medir
pH y ajustarlo si es necesario con
Extracción H2SO4/NaOH).
2 RH org + (Cu2+ + SO42-) ac ↔ R2Cu org
2. Preparar 125 mL de solución de LIX-
622/tolueno al 8 % en peso/v.
+(2 H+ +SO42-) ac 3. Transferir 30 mL de Solución de Cu2+ de 1
g/L a pH 2.2 a cada embudo de separación y
Despojo adicionar la fase orgánica a cada uno (60, 30,
15, 7.5, 3.75 mL), tapar y agitar los embudos
Las isotermas de extracción (loading) y durante 4 minutos. Separar las fases y
despojo (stripping) representan situaciones de colectar la acuosa para medir pH y preparar
equilibrio y predicen las condiciones óptimas muestras 1/50 para análisis de Cu2+. Incluir
para dichos procesos. el análisis de la muestra inicial de Cu2+ 1 g/L.
El número de pasos necesarios para alcanzar
una separación específica puede ser
30 de agosto 2018. Universidad Nacional Autónoma de México. 12
Facultad de Química. Departamento de Ingeniería Metalúrgica
LIXIVIACIÓN DE MINERAL DE COBRE
4. Numerar las muestras como E0, E1, E2, • 1 pipeta volumétrica de 2 mL.
E3, E4 y E5. • 1 pipeta volumétrica de 1 mL.
• 1 pipeta graduada de 10 mL.
Segunda sesión. • 1 soporte universal.
• 1 soporte para embudos.
1. Preparar 200 mL de solución de Cu2+ 8 g/L • 1 pH-metro.
a pH natural (tomar muestra para análisis). • 1 electrodo combinado para medir pH.
2. Preparar 200 mL de solución de LIX- • CuSO4. 5H2O.
622/tolueno al 8 % en peso/v. • H2SO4.
3. Poner en contacto en un embudo de • LIX-622.
separación las dos soluciones anteriores por • Tolueno.
4 minutos, separar las fases colectando la • Agua destilada.
fase orgánica cargada para el despojo y la fase
acuosa para el análisis de Cu2+ y medición de Resultados
pH.
4. Preparar 200 mL de una solución
conteniendo 150 g/L de H2SO4.
5. Transferir 50 mL de la fase orgánica
cargada con Cu2+ a cada embudo de
separación y agregar solución ácida de 150
g/L a cada uno (100, 50, 25, 10 y 5 mL). Agitar
durante 4 minutos, separar las fases y
colectar la fase acuosa para análisis de Cu2+.
Preparar muestras 1/50 para análisis de
Cu2+. Incluir el análisis de la muestra inicial
de Cu2+ 1 g/L (D00) y de la fase acuosa
Imagen1. %extracción en función del
residual del cargado de la fase orgánica (D0).
volumen de orgánico utilizado a los 4 min de
6. Numerar las muestras como D1, D2, D3,
agitación.
D4 y D5.
Tercera sesión.
Analizar y discutir los resultados obtenidos
durante la experimentación.
Equipo, material y reactivos
• 1 embudo de separación de 500 mL.
Imagen2. Isoterma de extracción con las
• 5 embudos de separación de 125 mL.
diferentes relaciones de volúmenes
• 1 matraz aforado de 500 mL.
trabajadas.
• 1 matraz aforado de 25 mL.
• 1 pipeta volumétrica de 25 mL.
• 1 Pipeta volumétrica de 10 mL.
• 1 pipeta volumétrica de 5 mL.
30 de agosto 2018. Universidad Nacional Autónoma de México. 13
Facultad de Química. Departamento de Ingeniería Metalúrgica
LIXIVIACIÓN DE MINERAL DE COBRE
Para la última imagen en donde se grafica el
porcentaje de extracción con respecto del
tiempo observamos que a volúmenes mayores
de orgánico como lo es el de 30 y 60 ml
obtenemos el mayor porcentaje de extracción
desde tiempos bajos, esto debido a que
tenemos mayor cantidad de orgánico libre
para atrapar el metal en el acuoso.
Imagen3. Relación del tiempo con la
extracción obtenida en cada relación de
Bibliografía
volúmenes.
• A. K. Biswas, Extractive Metallurgy of
Análisis de resultados.
Copper. Pergamon Press, 1980.
En el proceso de planta para la extracción de
• C. B Gill. Nonferrous Extractive Metallurgy.
cobre debemos conocer la relación de
1980.
volúmenes óptima para obtener el mayor
porcentaje de extracción de nuestro metal,
este análisis es necesario para poder obtener
el mejor rendimiento con el menor dinero
posible. Para este análisis se construyó la
isoterma de extracción en donde podemos
observar las concentraciones de acuoso vs la
concentración de acuoso, debido a que el
análisis de vía húmeda de la fase orgánica es
más complicado, esta última se sacó mediante
la diferencia de concentraciones una vez
conocida la del acuoso. Una vez trazada la
isoterma se trazó la gráfica de extracción
contra el volumen utilizado de orgánico, estos
valores solo se consideraron con 4 minutos de
agitación y en donde podemos observar que el
porcentaje más alto de extracción está
presente a los 10 ml de orgánico con 30 ml de
acuoso obteniendo un porcentaje de
extracción del 100%. Después de este
volumen observamos una pequeña caída
donde nuestra extracción decae hasta un
84.5% pero después en la relación 1:1
volvemos a obtener un 100% de extracción
por lo que esta caída la asociamos a errores
de medición en la concentración. Esto nos
dice que desde la relación 10ml orgánico y 30
ml acuoso obtenemos ya la mayor extracción
de nuestro electrolito cargado.
30 de agosto 2018. Universidad Nacional Autónoma de México. 14
Facultad de Química. Departamento de Ingeniería Metalúrgica
Potrebbero piacerti anche
- Informe de Laboratorio de Lixiviacion de Cobre Por AgitacionDocumento3 pagineInforme de Laboratorio de Lixiviacion de Cobre Por AgitacionAle SKNessuna valutazione finora
- Lixiviacion Acida de Un Mineral Oxidado de CobreDocumento6 pagineLixiviacion Acida de Un Mineral Oxidado de CobreCarlos Gallardo ReaNessuna valutazione finora
- Proceso Hidrometalúrgico de Lixiviación de Minerales Óxidos de Cobre (Percolación en Columna Con Ácido Sulfúrico)Documento8 pagineProceso Hidrometalúrgico de Lixiviación de Minerales Óxidos de Cobre (Percolación en Columna Con Ácido Sulfúrico)Marco Antonio MelgarejoNessuna valutazione finora
- Laboratorio HidrometalurgiaDocumento37 pagineLaboratorio HidrometalurgiaLeo Rodgers50% (4)
- Biolixiviacion EditarDocumento16 pagineBiolixiviacion EditarYOSSELY EMPERATRIZ AGAPITO HUAMANCHUMONessuna valutazione finora
- Práctica de Lixiviación de Cobre 2Documento5 paginePráctica de Lixiviación de Cobre 2CUELLAR RIZO JIMENA LIZETHNessuna valutazione finora
- Lixiviacion de Cobre Utilizando Bisulfato de Potasio PDFDocumento107 pagineLixiviacion de Cobre Utilizando Bisulfato de Potasio PDFgian danielNessuna valutazione finora
- Libro Metalurgia Alonso ArenasDocumento37 pagineLibro Metalurgia Alonso ArenasMaria AngelicaNessuna valutazione finora
- Informe Reloj de YODODocumento5 pagineInforme Reloj de YODOKevin ContrerasNessuna valutazione finora
- INFORME Lab.03 CAMBIOS FISICOS Y QUIMICOSDocumento22 pagineINFORME Lab.03 CAMBIOS FISICOS Y QUIMICOSrusbel chavarria moralesNessuna valutazione finora
- Practica-1-Inorg Alcalinos y Alcalinos TerreosDocumento15 paginePractica-1-Inorg Alcalinos y Alcalinos TerreosDanilo JaramilloNessuna valutazione finora
- Laboratorio Marcha Analitica Grupo IDocumento14 pagineLaboratorio Marcha Analitica Grupo IMarcela DavilaNessuna valutazione finora
- Reporte de Laboratorio 1 Equipo 1Documento15 pagineReporte de Laboratorio 1 Equipo 1Adriana Olvera RayónNessuna valutazione finora
- Práctica 2 Reacciones IónicasDocumento9 paginePráctica 2 Reacciones Iónicas202300010Nessuna valutazione finora
- Practica 04Documento3 paginePractica 04Lupita MarNessuna valutazione finora
- QM 344 Informe 1Documento4 pagineQM 344 Informe 1Roger RamosNessuna valutazione finora
- Articulo 4. Ciclo Del Cu.Documento8 pagineArticulo 4. Ciclo Del Cu.alberto barreraNessuna valutazione finora
- Ensayos Via SecaDocumento8 pagineEnsayos Via SecaVerónica Vanessa Medina GallegosNessuna valutazione finora
- Informe Laboratorio Lix CobreDocumento6 pagineInforme Laboratorio Lix CobreYoSoyCharlyeBobaryNessuna valutazione finora
- Resultados y Discusion Winkler 11Documento6 pagineResultados y Discusion Winkler 11OLVERY REVELONessuna valutazione finora
- Micro Cristales de Sulfuro by Franco ChalacanDocumento6 pagineMicro Cristales de Sulfuro by Franco ChalacanFranco ChalacanNessuna valutazione finora
- Hidrometalurgia Primera Parte 2019 PDFDocumento115 pagineHidrometalurgia Primera Parte 2019 PDFNicolas Ignacio Olivares MaturanaNessuna valutazione finora
- N 04lixiviación de Minerales de Oxido de Cobre YeisonDocumento18 pagineN 04lixiviación de Minerales de Oxido de Cobre YeisonAlex Joel Paredes LeyvaNessuna valutazione finora
- Informe 7 Flores PrietoDocumento9 pagineInforme 7 Flores Prietoivan gabriel flores prietoNessuna valutazione finora
- Fundamentos Del Proceso de TostaciónDocumento7 pagineFundamentos Del Proceso de Tostaciónfernando aguilera100% (1)
- Lixiviacion de Cobre PDFDocumento4 pagineLixiviacion de Cobre PDFalbertNessuna valutazione finora
- Volumetria de CuDocumento7 pagineVolumetria de CuJonás Correa PérezNessuna valutazione finora
- Identificacion de Sulfatos.Documento2 pagineIdentificacion de Sulfatos.Sofia Cortés OljicaNessuna valutazione finora
- Informe Lab Cinetica MioDocumento13 pagineInforme Lab Cinetica MioRodrigo AndradeNessuna valutazione finora
- PCM 3Documento11 paginePCM 3brandNessuna valutazione finora
- Lixiviacion de Minerales de CobreDocumento10 pagineLixiviacion de Minerales de CobreeduNessuna valutazione finora
- Lixiviacion AvanceDocumento6 pagineLixiviacion AvanceYudith Rosaluz Imata CondoriNessuna valutazione finora
- Informe #1 Organica I. Jesus Lopez, Ingrid Salas, Enrique YelaDocumento10 pagineInforme #1 Organica I. Jesus Lopez, Ingrid Salas, Enrique YelaIngrith Salas ErasoNessuna valutazione finora
- Practica 3. Coloides Del SueloDocumento25 paginePractica 3. Coloides Del SueloEliazar Valdez MartinezNessuna valutazione finora
- Manual de Prácticas de Metalurgia III PDFDocumento16 pagineManual de Prácticas de Metalurgia III PDFmartinNessuna valutazione finora
- Informe Practica 5 ENLACES QUIMICOSDocumento9 pagineInforme Practica 5 ENLACES QUIMICOSCesar Hernan Arcila SuarezNessuna valutazione finora
- Manual de Laboratorio de HidrometalurgiaDocumento31 pagineManual de Laboratorio de HidrometalurgiaYunn HdzNessuna valutazione finora
- Reporte 2 Formación de Fases y Velocidad de Reacciones QuímicasDocumento12 pagineReporte 2 Formación de Fases y Velocidad de Reacciones QuímicasLuis Mario BGNessuna valutazione finora
- Informe 7 - Reaccion de HidrocarburosDocumento7 pagineInforme 7 - Reaccion de HidrocarburosEvelyn Isabel Castillo100% (1)
- Articulo No 4Documento5 pagineArticulo No 4Catalina Luz TORRESNessuna valutazione finora
- Guia Laboratorio N°02-HidrometalurgiaDocumento10 pagineGuia Laboratorio N°02-HidrometalurgiaJesus Talledo BermudezNessuna valutazione finora
- PC Semana 9Documento6 paginePC Semana 9CESAR GAMBOA ANAYANessuna valutazione finora
- Laboratorio N°07Documento7 pagineLaboratorio N°07JADE COLQUE TORRESNessuna valutazione finora
- Laboratorio Presencial de Quimica 1Documento20 pagineLaboratorio Presencial de Quimica 1Esthefani MelendezNessuna valutazione finora
- S3-Practica 4-2021-08-09-IDocumento3 pagineS3-Practica 4-2021-08-09-IAshley SanchezNessuna valutazione finora
- Guia de Taller 7 - FlotaciónDocumento6 pagineGuia de Taller 7 - FlotaciónRoger Aristides Jimenez EspinozaNessuna valutazione finora
- Practica 8Documento6 paginePractica 8Ruano MadelynNessuna valutazione finora
- CineticadelixiviacionDocumento17 pagineCineticadelixiviacionFimm Nasca Metalurgia MinasNessuna valutazione finora
- Presentación Flotacion de MineralesDocumento20 paginePresentación Flotacion de MineralesIngrid MartinezNessuna valutazione finora
- Informe de Lab 9 de AbrilDocumento18 pagineInforme de Lab 9 de AbrilTHE RANGERNessuna valutazione finora
- 3.lixiviación Del CobreDocumento13 pagine3.lixiviación Del CobreAntonio RuizNessuna valutazione finora
- Práctica 3-4 LixiviaciónDocumento30 paginePráctica 3-4 LixiviaciónMichael CamachoNessuna valutazione finora
- Guia Solubilidad Sales MetálicasDocumento2 pagineGuia Solubilidad Sales MetálicasRobinson VelasquezNessuna valutazione finora
- Informe de Laboratorio - Laboratorio 3 - Estudio de Propiedades de La Materia-1Documento6 pagineInforme de Laboratorio - Laboratorio 3 - Estudio de Propiedades de La Materia-1Brandon Villalobos SolanoNessuna valutazione finora
- Instituto Politecnico Nacional Escuela Superior de Ingeniería Química E Industrias ExtractivasDocumento11 pagineInstituto Politecnico Nacional Escuela Superior de Ingeniería Química E Industrias ExtractivasJesús MezaNessuna valutazione finora
- Laboratorio 3 Cinetica de Flotacion (1) - 2Documento4 pagineLaboratorio 3 Cinetica de Flotacion (1) - 2Elizabeth LupacaNessuna valutazione finora
- Determinación de ClorurosDocumento6 pagineDeterminación de Clorurosmaria100% (1)
- El carbón: origen, atributos, extracción y usos actuales en ColombiaDa EverandEl carbón: origen, atributos, extracción y usos actuales en ColombiaValutazione: 4.5 su 5 stelle4.5/5 (2)
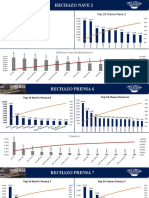
- General Paretos Nave 2Documento4 pagineGeneral Paretos Nave 2Eder RysNessuna valutazione finora
- Tesis I. M. 204 - Lascano Arias José MiguelDocumento215 pagineTesis I. M. 204 - Lascano Arias José MiguelEder RysNessuna valutazione finora
- Procesos FinalDocumento14 pagineProcesos FinalEder RysNessuna valutazione finora
- Manual de Practicas Electrometalurgía2019-1Documento22 pagineManual de Practicas Electrometalurgía2019-1Eder RysNessuna valutazione finora
- Electrodo Disco RotatorioDocumento4 pagineElectrodo Disco RotatorioEder RysNessuna valutazione finora
- Fpe Practica 1Documento6 pagineFpe Practica 1Eder RysNessuna valutazione finora
- Vector EsDocumento6 pagineVector EsEder RysNessuna valutazione finora
- MenagrafíaDocumento5 pagineMenagrafíaEder RysNessuna valutazione finora
- EEEP3 HfjdksDocumento3 pagineEEEP3 HfjdksEder RysNessuna valutazione finora
- Interjjhgjhgvalos de Confianza y Pruebas Djghjgjhe HipótesisDocumento3 pagineInterjjhgjhgvalos de Confianza y Pruebas Djghjgjhe HipótesisEder RysNessuna valutazione finora
- UnitecDocumento3 pagineUnitecEder RysNessuna valutazione finora
- Cantinflas Version CoolDocumento6 pagineCantinflas Version CoolEder RysNessuna valutazione finora
- Practica 5 Soluciones No ElectrolitosDocumento13 paginePractica 5 Soluciones No ElectrolitosEder RysNessuna valutazione finora
- PROPIEDADES COLIGATIVAS DextrosaDocumento3 paginePROPIEDADES COLIGATIVAS DextrosaEder RysNessuna valutazione finora
- Ejercicios de Quimica Organica 1 Estereoquim1Documento2 pagineEjercicios de Quimica Organica 1 Estereoquim1Eder RysNessuna valutazione finora
- Capítulo 104Documento22 pagineCapítulo 104Frank Huingo TelloNessuna valutazione finora
- Proyecto de InnovacionDocumento18 pagineProyecto de InnovacionGeorge Anderzon Victoriano RengifoNessuna valutazione finora
- Convocatoria Festival de Oratoria y DeclamaciónDocumento2 pagineConvocatoria Festival de Oratoria y DeclamaciónDayan Ferrufino FloresNessuna valutazione finora
- Microencapsulación de Aceites Esenciales para Su Aplicación Como Aditivo en Nutrición AvícolaDocumento1 paginaMicroencapsulación de Aceites Esenciales para Su Aplicación Como Aditivo en Nutrición AvícolaLuis Miguel Perez SolisNessuna valutazione finora
- 17 Aviso de Accidente de Trabajo IESSDocumento3 pagine17 Aviso de Accidente de Trabajo IESSJamil Valencia IntriagoNessuna valutazione finora
- Planteamiento Del Problema de InvestigaciónDocumento1 paginaPlanteamiento Del Problema de InvestigaciónharoldNessuna valutazione finora
- Cuadro Comparativo Proyecto de VidaDocumento2 pagineCuadro Comparativo Proyecto de VidaCamilo ToroNessuna valutazione finora
- Taller de S.P.Documento4 pagineTaller de S.P.julieth castilloNessuna valutazione finora
- Calendario Mano de ObraDocumento1 paginaCalendario Mano de ObraJOSE VENTURA ANGELESNessuna valutazione finora
- Ensayo de ConductismoDocumento6 pagineEnsayo de ConductismoKatherine Armijos71% (7)
- Derechos Sociales y de La Familia BS, 60,ººDocumento15 pagineDerechos Sociales y de La Familia BS, 60,ººRaquel AmoedoNessuna valutazione finora
- Guía Práctica de EncofradosDocumento200 pagineGuía Práctica de Encofradosergow100% (2)
- RM 092 2014 Mem DMDocumento51 pagineRM 092 2014 Mem DMalarcon_figmmNessuna valutazione finora
- Comite Equidad SalarialDocumento3 pagineComite Equidad SalarialCarlos G LayzaNessuna valutazione finora
- Violencia y Paz. LJADocumento3 pagineViolencia y Paz. LJAMahia RosarioNessuna valutazione finora
- El Delirio Del PlagioDocumento4 pagineEl Delirio Del PlagioAlberto SladognaNessuna valutazione finora
- LegumbresDocumento23 pagineLegumbresantonioNessuna valutazione finora
- Menu Detox 10 Dias Bajo en HistaminaDocumento11 pagineMenu Detox 10 Dias Bajo en HistaminaMaria HSNessuna valutazione finora
- Poeg PrimeroDocumento45 paginePoeg PrimeroyuliethperNessuna valutazione finora
- PROGRAMA Tiempo Ritmos BiologicosDocumento4 paginePROGRAMA Tiempo Ritmos BiologicosComo KarlaNessuna valutazione finora
- OPuOPr-informe S&H EngulianDocumento4 pagineOPuOPr-informe S&H EngulianDamianFrancucciNessuna valutazione finora
- Nota Urgencias 33Documento1 paginaNota Urgencias 33Luis NoriegaNessuna valutazione finora
- Triage HospitalarioDocumento33 pagineTriage HospitalarioRicardo Ramirez Vazquez100% (1)
- Determinacion de La Actividad EnzimaticaDocumento10 pagineDeterminacion de La Actividad EnzimaticaLUIS ERLIS OLIVARES PALMANessuna valutazione finora
- Manual Bomba en EspañolDocumento7 pagineManual Bomba en EspañolIpesa Gases MedicinalesNessuna valutazione finora
- Paralisis Cerebral Ataxica y AtetoideDocumento28 pagineParalisis Cerebral Ataxica y AtetoideJesus Calderon ValverdeNessuna valutazione finora
- Folleto Reconocimiento de ArbolesDocumento2 pagineFolleto Reconocimiento de ArbolesproyectopankoNessuna valutazione finora
- Conductores EléctricosDocumento20 pagineConductores EléctricosBetzy Florez RamirezNessuna valutazione finora
- Endoscopia de ColumnaDocumento31 pagineEndoscopia de ColumnaTOMASNOEL5100% (2)
- La Viuda La Monja y La CortesanaDocumento6 pagineLa Viuda La Monja y La CortesanaMónica Viviana DussetNessuna valutazione finora