Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
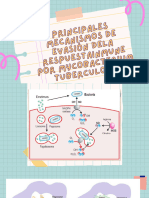
INFLAMASOMAS, Concepto y Componentes
Caricato da
Marijose Salas Vargas0 valutazioniIl 0% ha trovato utile questo documento (0 voti)
62 visualizzazioni5 pagineLos inflamasomas son complejos proteicos que actúan como sensores de patógenos e inician la respuesta inmune innata. Existen varios tipos de inflamasomas definidos por sus proteínas receptoras, incluyendo NLRP1, NLRP2, NLRC4 y NLRP3. El inflamasoma mejor caracterizado es NLRP3, el cual se activa por múltiples estímulos como especies reactivas de oxígeno mitocondrial y fosfolípidos, induciendo la maduración de citoquinas proinflamatorias a través de la caspasa-1.
Descrizione originale:
inflamasomas
Titolo originale
INFLAMASOMAS,Concepto y Componentes
Copyright
© © All Rights Reserved
Formati disponibili
DOCX, PDF, TXT o leggi online da Scribd
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoLos inflamasomas son complejos proteicos que actúan como sensores de patógenos e inician la respuesta inmune innata. Existen varios tipos de inflamasomas definidos por sus proteínas receptoras, incluyendo NLRP1, NLRP2, NLRC4 y NLRP3. El inflamasoma mejor caracterizado es NLRP3, el cual se activa por múltiples estímulos como especies reactivas de oxígeno mitocondrial y fosfolípidos, induciendo la maduración de citoquinas proinflamatorias a través de la caspasa-1.
Copyright:
© All Rights Reserved
Formati disponibili
Scarica in formato DOCX, PDF, TXT o leggi online su Scribd
0 valutazioniIl 0% ha trovato utile questo documento (0 voti)
62 visualizzazioni5 pagineINFLAMASOMAS, Concepto y Componentes
Caricato da
Marijose Salas VargasLos inflamasomas son complejos proteicos que actúan como sensores de patógenos e inician la respuesta inmune innata. Existen varios tipos de inflamasomas definidos por sus proteínas receptoras, incluyendo NLRP1, NLRP2, NLRC4 y NLRP3. El inflamasoma mejor caracterizado es NLRP3, el cual se activa por múltiples estímulos como especies reactivas de oxígeno mitocondrial y fosfolípidos, induciendo la maduración de citoquinas proinflamatorias a través de la caspasa-1.
Copyright:
© All Rights Reserved
Formati disponibili
Scarica in formato DOCX, PDF, TXT o leggi online su Scribd
Sei sulla pagina 1di 5
INFLAMASOMAS
CONCEPTO:
Los inflamasomas son complejos proteicos localizados en el citoplasma de las células,
que actúan como sensores y son mediadores del desarrollo de la inflamación. Existen
diferentes inflamasomas, pero todos ellos están relacionados con el reconocimiento de
patrones conservados de secuencias proteicas a través de los receptores tipo PPR, que
son receptores que reconocen patógenos. Estos últimos se subdividen en 4 categorías:
los receptores tipo Toll (TLRs), los receptores tipo RIG-I (derivado del inglés retinoic
acid-Inducible gene 1), los receptores de carbohidratos tipo lectina (CLRs) y los
receptores tipo NOD (derivado del inglés nucleotide-binding oligomerization domain)
Estos últimos conforman un grupo especializado de proteínas intracelulares presentes
en el citoplasma que se consideran esenciales para detectar patógenos e iniciar la
respuesta inmune innata. A los receptores tipo NOD de aquí en adelante los llamaremos
NOD-like receptor (NLR). Los NLRs están divididos en 3 subfamilias clasificadas de
acuerdo con los dominios de interacción con proteínas que poseen en la región amino
terminal: 1) NOD que consiste de 6 miembros diferentes –5 NOD y 1 CIITA (Class II
transactivator)–, 2) IPAF o NLRC, que está formado por 2 miembros, y 3) NLRP, del que
se reconocen 14 diferentes miembros
ELEMENTOS DEL INFLAMASOMA:
NLRP1
El NLRP1 también conocido como NALP1, es el sensor de las señales de
activación, de la respuesta inmune innata y está expresado en muchos tipos de
células inmunocompetentes en particular las células de Langerhans de la piel.
Sus variantes están asociadas a la susceptibilidad a padecer enfermedades
autoinmunes asociadas al vitíligo y enfermedades inflamatorias.
El inflamasoma NLRP1 es el único cuya proteína receptora contiene un dominio
PYD N-terminal y un CARD C-terminal, dos dominios de muerte que forman un
ramillete implicado en las interacciones homotípicas. En contraste con otras
proteínas NLRP, el dominio CARD de NLRP1 parece ser más esencial que el
PYD para el reclutamiento de procaspasa-1 y se ha demostrado que el NLRP1
se asocia directamente con procaspasa-1 a través de CARD en ausencia del
adaptador ASC, así también puede reclutar y activar la caspasa-5 a través del
mismo dominio. Además, en su región C-terminal se encuentra un dominio FIIND
(dominio con función por encontrar), el cual está ubicado entre el LRR y el
dominio CARDE.l NLRP1 y su homólogo murino Nlrpb1 tienen un dominio
NACHT que junto con el dominio FIIND facilitan la auto asociación. En ese
sentido, los experimentos de Finger demostraron que gracias al dominio FIIND,
el cual sufrió un proceso de auto proteólisis dentro de la proteína receptora
NLRP1, es lo que permitió que este receptor fuera capaz de responder y
ensamblar el inflamasoma NLRP1, en respuesta a la infección con PAMP’s de
distintos organismos. Luego de la escisión proteolítica de la proteína NLRP1 se
produjeron dos fragmentos poli peptídicos, los cuales permanecieron
autoasociados hasta que ocurrió el reclutamiento de la proteína ASC por el
dominio CARD del receptor NLRP1 que ya había sido procesado. Estos autores
también confirmaron que aparte de la asociación de la ASC con el sensor
citoplasmático NLRP1, la modificación postraduccional de la serina 1213 y el
residuo del aminoácido histidina 1186 presentes en el dominio FIIND de la
proteína NLRP1, era el evento molecular que dirigía la regulación en la activación
del inflamasoma NLRP1. El Nlrpb1 detecta la actividad proteolí- tica de la toxina
letal del ántrax (LeTx), mientras que el NLRP1 detecta tanto el LeTx como el
muramildipéptido (MDP) presente en micobacterias en presencia de ATP, sin
embargo se cree que la activación del NLRP1 por acción del muramil dipéptido
es indirecta ya que requiere de la interacción con la proteína NOD2 para unirse
al ATP y activar el inflamasoma, ya que se ha demostrado que la interacción de
NLRP1 con procaspasa-1 requiere de la presencia de NOD2.También se ha
demostrado que el inflamasoma NALP1 tiene un papel crucial en mediar la
expresión de las citoquinas inflamatorias durante la infección con Toxoplasma
gondii. Por otra parte, De Rivero y col. demostraron in vivo que el inflamasoma
NALP1 neuronal es un complejo multiproteico que consiste de la caspasa-1, la
caspasa-11, el NALP1, la proteína adaptadora ASC y la proteína adaptadora de
la apoptosis XIAP-1. Este inflamasoma tiene un inminente rol luego de la injuria
de la medula espinal de rata que activa la plataforma molecular que origina el
incremento de la caspasa-11 y de la proteína ASC, así como el procesamiento
de la caspasa-1 y la posterior maduración de la IL-1 y la IL-18 en un proceso
dependiente de la salida de iones K+. No obstante, Liu y col. previamente
reportaron que la activación del inflamasoma NALP1 recombinante en las
neuronas granulares del cerebelo resultó en la activación de la caspasa-3 con la
consiguiente apoptosis.
NLRP2
La proteína NLRP2 también conocida como NALP2, NBS1, PAN1 y PYFAF2, el
cual se expresa en diversos tipos de tejidos y órganos tales como el pulmón, la
placenta, el timo, los ovarios, el intestino, el corazón y el cerebro. Este
inflamasoma interactúa con el receptor P2X7 y de manera gradual forma un gran
poro en la membrana por el reclutamiento del hemicanal panexina-1, que permite
el ingreso de productos bacterianos como el lipopolisacárido (LPS) al citosol y la
subsecuente activación del inflamasoma NLRP2.Otro hallazgo en relación a esta
plataforma molecular es que también puede ser estimulado por la presencia de
interferones (IFN), y en el mismo orden de ideas Minkiewicz y col., explicaron
resultados relacionados con la activación de este inflamasoma en respuesta al
incremento en los niveles de ATP extracelular en los astrocitos corticales de
humanos, sin embargo aún faltan por describir las funciones ejercidas por el
NLRP2 en los procesos inflamatorios. Estudios previos de inhibición de la
actividad del NLRP2 por el agente uricosúrico probenecid y el antagonista del
receptor P2X7 azul brillante G (BBG), demostraron una disminución en los
niveles del inflamasoma NLRP2 y de la caspasa-1, y evidenciaron la importancia
de este complejo macromolecular en la respuesta inflamatoria del sistema
nervioso central y su utilidad como blanco quimioterapéutico ante lesiones
cerebrales originadas por una inflamación. Por otra parte Conti y col.,
argumentaron que la activación del TCR (receptor de las células T) por los
anticuerpos anti CD3, anti CD28 y los compuestos acetato forbol miristato (PMA)
e ionomicina indujeron la sobreexpresión el inflamasoma NLRP2 en las células
T, el cual a su vez inhibió la activación de los factores de transcripción NFAT,
AP-1 y NF-B. NLRC4 El inflamasoma NLRC4 o IPAF (factor de activación de
proteasa convertidor de interleuquina) contiene un receptor denominado NLRC4,
el cual es una proteína que pertenece a la familia NLR y contiene un dominio N-
terminal CARD que interactúa con el dominio CARD de la procaspasa, un
dominio central NOD y un dominio C-terminal LRR. Se ha demostrado que este
inflamasoma activa la caspasa-1, en respuesta a un dominio conservado en la
proteína bacteriana flagelina, así como al componente conservado tipo varilla del
sistema de secreción tipo III denominado PrgJ en Salmonella enterica Serotipo
Typhimurium ,sin embargo, Franchi y col. manifestaron que la activación del
inflamasoma NLRC4 requería de la presencia simultánea de un sistema de
secreción intacto tipo III (T3SS) o tipo IV (T4SS) necesario para el ingreso de los
factores de virulencia bacterianos y de pequeñas cantidades de flagelina; en
particular se ha demostrado que es una región en el extremo C-terminal de
flagelina la que activa el inflamasoma a través del receptor NLRC4. Para la
activación del inflamasoma NLRC4, en algunos casos requiere la presencia de
una segunda proteína NLR denominada NAIP5 (ejemplo: en respuesta a
Legionella pneumophila), la cual se cree que heterooligomeriza con NLRC4; la
proteína NAIP5 contiene tres dominios repetidos de la proteína inhibidora de la
apoptosis de baculovirus (BIR) en el N-terminal.
NLRP3
El inflamasoma mejor caracterizado es el NLRP3 y comparado con los
inflamasomas NLRC4, NLRP1 y AIM2, el NLRP3 es el único activado por
innumerables estímulos, el cual en condiciones de reposo se encuentra
localizado en el citosol celular. En la revisión realizada por Wen y col. (52), estos
autores señalaron que la mitocondria de la célula, cumple una función importante
en la activación del inflamasoma NLRP3, la cual se organiza en 2 categorías: La
primera es que la mitocondria es el andamiaje sobre el cual se ensambla el
complejo molecular denominado el inflamasoma NLRP3. La segunda es que la
proteína NLRP3 es activada por distintas moléculas efectoras producidas o
liberadas por la mitocondria tales como: las especies reactivas de oxígeno
mitocondrial, el ADN mitocondrial y el fosfolípido cardiolipina. Una vez que ocurre
la activación del inflamasoma NLRP3, se lleva a cabo una relocalización del
receptor NLRP3 que inicialmente se encontraba en reposo, desde el citosol hacia
la mitocondria, hecho demostrado a través del análisis de datos bioquímicos y
de imágenes de microscopia. La relocalización del receptor NLRP3 activado a la
mitocondria es llevado a cabo, con la participación de los 6 primeros residuos de
aminoácidos ubicados en el extremo N- terminal del dominio PYD de la proteína
NLRP3, el cual es esencial en la modulación y regulación óptima de la actividad
de este inflamasoma. De igual manera, Wen y col. manifestaron que otros
autores habían reportado que la interacción entre la proteína adaptadora de la
señalización antiviral y mitocondrial (MAVS) con el receptor NLRP3, era la
responsable de su asociación con la mitocondria en los macrófagos murinos
expuestos al ATP y la nigericina. El inflamasoma NLRP3 es un complejo de
señalización que activa la procaspasa-1 e induce el procesamiento de las
citoquinas inflamatorias dependientes de caspasa-1 (particularmente IL-1 e IL-
18). Este inflamasoma se encuentra en las células del sistema inmune innato
como los macrófagos y las células dendríticas. El inflamasoma NLRP3 está
constituido por la proteína receptora NLRP3 (también conocida como NALP3 y
criopirina), la ASC y la caspasa-1. La oligomerización de NALP3-ASC resulta en
el reclutamiento de la procaspasa-1 en el complejo, lo cual promueve el corte de
la misma en un mecanismo auto catalítico para generar el heterodí- mero activo
de caspasa-1 compuesto por dos subunidades activas. Estudios previos
sugirieron que NLRP3 está secuestrado por dos proteínas: la SGT1 (supresora
del alelo G2 del gen Skp1 homó- logo de la proteína p19 del ciclo celular) y la
HSP90 (proteína del choque térmico 90), en una conformación autoinhibitoria en
el estado de reposo; tras la estimulación del NLRP3 a través del dominio LRR,
éste experimenta una autooligomerización dependiente de ATP, mediada por su
dominio intermedio NOD, luego ocurre la interacción homotípica entre los
dominios N-terminal PYD del NLRP3 y la ASC y a continuación entre los
dominios CARD de la ASC y de la procaspasa-1 para formar un complejo de alto
peso molecular que conduce al y de colesterol, así como un número importante
de sustancias ambientales como la sí- lica, los asbestos y el adyuvante hidróxido
de aluminio, asimismo se ha encontrado que la exposición a la radiación
ultravioleta tipo B (UVB) o a sustancias químicas irritantes que causan
hipersensibilidad por contacto también inducen la respuesta dependiente del
inflamasoma. Las moléculas sensoras del inflamasoma conectan con la
caspasa-1 a través de la ASC. La ASC tiene un dominio pirina y un dominio para
el reclutamiento de la caspasa (CARD) e interacciona con las moléculas
sensoras proximales por el dominio pirina. El resultado es la conglomeración de
numerosos dímeros de ASC y mediante su dominio CARD atrae los monómeros
de procaspasa-1, para iniciar así la autoactivación heterotetramérica de la
caspasa-1. A su vez la caspasa-1 activa la pro-IL-1 y pro-IL-18 a sus formas
maduras.
AIM2
El inflamasoma AIM2, reconoce el ADN doble banda derivado de virus y de
bacterias patógenas en el citoplasma de los macrófagos infectados a través del
receptor ALR. ALR es un receptor citosólico perteneciente a la familia PYHIN
(familia de proteínas que contienen dominio pirina y dominio HIN), donde se
encuentra un dominio PYD N-terminal que media la interacción homotípica con
la ASC y en su C-terminal una o dos copias del dominio de unión a
oligonucleótido HIN-200, el cual puede unirse directamente al ADN del patógeno;
una vez oligomerizado el receptor con la proteína adaptadora ASC ocurre el
agrupamiento de la procaspasa-1 y su activación para producir la maduración de
las interleuquinas proinflamatorias IL-1 e IL-18. Los dominios HIN de esta familia
de proteínas, son exclusivos de los mamíferos y consisten en una serie aleatoria
de bolsillos de unión a oligonucleótidos y a oligosacáridos los cuales interactúan
con los ácidos nucleicos. Este tipo de inflamasoma ha demostrado ser esencial
para la defensa contra Francisella tularensis, F. novicida y Listeria
monocytogenes así como para citomegalovirus y vaccinia. El AIM2 también se
ha reportado como supresor de tumores y de las funciones que promueven la
aparición de estos tanto en mama como en colon y recto.
Potrebbero piacerti anche
- Fundamentos y técnicas básicas en biología molecularDa EverandFundamentos y técnicas básicas en biología molecularNessuna valutazione finora
- Transferencia de inmunidad en el binomio madre-cría: Estudio comparativo entre especiesDa EverandTransferencia de inmunidad en el binomio madre-cría: Estudio comparativo entre especiesNessuna valutazione finora
- 03 Que Son Los InflamasomasDocumento8 pagine03 Que Son Los InflamasomasLeon-lv Londoño100% (1)
- Receptores Citosólicos para Pamp y DampDocumento4 pagineReceptores Citosólicos para Pamp y DampPame FloresNessuna valutazione finora
- Seminario 2. Inmunidad Innata. Parte 2.Documento29 pagineSeminario 2. Inmunidad Innata. Parte 2.lilianabarbagallo.estilistaNessuna valutazione finora
- Reseñas: Inflamasomas: Mecanismo de Ensamblaje, Regulación y SeñalizaciónDocumento14 pagineReseñas: Inflamasomas: Mecanismo de Ensamblaje, Regulación y Señalizacióntenma1200Nessuna valutazione finora
- Fagocitosis y PRRDocumento4 pagineFagocitosis y PRRisrael tulcanazaNessuna valutazione finora
- El Papel de Los Receptores de Reconocimiento de Patrones en La Inmunidad InnataDocumento46 pagineEl Papel de Los Receptores de Reconocimiento de Patrones en La Inmunidad InnataKArdo23Nessuna valutazione finora
- La Enfermedad Del Sueño Tiene Sus Orígenes en La Región Afrotropical Del ContinenteDocumento4 pagineLa Enfermedad Del Sueño Tiene Sus Orígenes en La Región Afrotropical Del ContinentejordanNessuna valutazione finora
- Receptores CitosolicosDocumento33 pagineReceptores CitosolicosVanessa YapoNessuna valutazione finora
- Receptores SolublesDocumento6 pagineReceptores SolublesCarlitos AyalaNessuna valutazione finora
- PRRsDocumento3 paginePRRsOmar Adrian Hernandez JimenezNessuna valutazione finora
- Taller Sobre CitoesqueletoDocumento9 pagineTaller Sobre CitoesqueletoNatalie Rodriguez CortésNessuna valutazione finora
- Innata 2Documento46 pagineInnata 2henriquecastelanNessuna valutazione finora
- Exposición GrupalDocumento27 pagineExposición GrupalStephania SorianoNessuna valutazione finora
- Capítulo I - Respuesta Inmune. de La Fisiología A La MedicinaDocumento26 pagineCapítulo I - Respuesta Inmune. de La Fisiología A La Medicinaicaro chaineNessuna valutazione finora
- Papel de Los Receptores Tipo Toll en La Inmunidad InnataDocumento6 paginePapel de Los Receptores Tipo Toll en La Inmunidad InnataG-orgina Coello0% (1)
- Resumen - Generalidades Del Reconocimiento Por La Inmunidad InnataDocumento7 pagineResumen - Generalidades Del Reconocimiento Por La Inmunidad InnataRanciovichNessuna valutazione finora
- Inmunidad InnataDocumento22 pagineInmunidad InnataIsabellaNessuna valutazione finora
- Patologia y CausaDocumento7 paginePatologia y CausaAndrea K. CuelloNessuna valutazione finora
- Proceso de TranscripciónDocumento17 pagineProceso de TranscripciónKarina Alejandra Cervantes RoblesNessuna valutazione finora
- T4 InmunoDocumento21 pagineT4 InmunoCris SánchezNessuna valutazione finora
- 3 - PAMPs y RRPDocumento3 pagine3 - PAMPs y RRPGino MartinezNessuna valutazione finora
- Investigaciones InmunologiaDocumento15 pagineInvestigaciones InmunologiaErick Salazar ManzanoNessuna valutazione finora
- Actividad Receptores de PRRDocumento11 pagineActividad Receptores de PRRAndres PelayoNessuna valutazione finora
- Marco TeoricoDocumento46 pagineMarco TeoricoLiam RodriguezNessuna valutazione finora
- Presentacion Receptores Citosolicos y de MembranaDocumento41 paginePresentacion Receptores Citosolicos y de Membranaisabella vNessuna valutazione finora
- Respuesta InnataDocumento4 pagineRespuesta InnataAndrea Mariel PeñaNessuna valutazione finora
- Receptores Tipo Toll - TareasDocumento12 pagineReceptores Tipo Toll - TareasDayana Torrico VNessuna valutazione finora
- Receptores Tipo Toll - TareasDocumento12 pagineReceptores Tipo Toll - TareasDayana Torrico VNessuna valutazione finora
- Receptores Tipo Toll (TLR)Documento36 pagineReceptores Tipo Toll (TLR)Brenda Collantes VidalNessuna valutazione finora
- Paramyxoviridae TEXTODocumento28 pagineParamyxoviridae TEXTOSharon ReyesNessuna valutazione finora
- El Papel de Los TLR en La Activación de NeutrófilosDocumento6 pagineEl Papel de Los TLR en La Activación de NeutrófilosVic VargasNessuna valutazione finora
- Inflamación y Enfermedad de ParkinsonDocumento19 pagineInflamación y Enfermedad de Parkinsonjuan carlos muñozNessuna valutazione finora
- Receptores Del Tipo RIGDocumento7 pagineReceptores Del Tipo RIGReyner CovarrubiasNessuna valutazione finora
- Retroalimentación Area 2Documento22 pagineRetroalimentación Area 2Dove CameronNessuna valutazione finora
- Fichas 7Documento7 pagineFichas 7Noelita RiveraNessuna valutazione finora
- Papel Regulador Del ATPDocumento7 paginePapel Regulador Del ATPAlejandro DelgadoNessuna valutazione finora
- 169 Sistema Inmunitario Cutáneo PDFDocumento63 pagine169 Sistema Inmunitario Cutáneo PDFJ C Torres Formalab100% (1)
- LPS y Receptores Toll (MAOG)Documento13 pagineLPS y Receptores Toll (MAOG)miguel angel100% (3)
- 2do Parcial Medicina MolecularDocumento7 pagine2do Parcial Medicina MolecularAna Daniela Cruz ZarabiaNessuna valutazione finora
- Respuesta Inmune Innata - 1ra ParteDocumento18 pagineRespuesta Inmune Innata - 1ra Parteirving hilarioNessuna valutazione finora
- Mecanismos de Transcripcion.Documento41 pagineMecanismos de Transcripcion.Jhoe100% (1)
- 5 Simposios 105-340Documento89 pagine5 Simposios 105-340EDUARDO CARRILLO GODINEZNessuna valutazione finora
- HETERÓFILOSDocumento3 pagineHETERÓFILOSRosa Mezta DamisNessuna valutazione finora
- NEUROTROFINASDocumento6 pagineNEUROTROFINASSandra chopinNessuna valutazione finora
- 4.moleculas Del Sistema Inmunologico EspecificoDocumento66 pagine4.moleculas Del Sistema Inmunologico EspecificoGonzales Sanchez JoseNessuna valutazione finora
- Sepsis MaternaDocumento40 pagineSepsis MaternaAlberto BrunoNessuna valutazione finora
- Resumen - Clase Teórica de Virus Herpes Simplex y Varicela-ZósterDocumento4 pagineResumen - Clase Teórica de Virus Herpes Simplex y Varicela-Zósterapi-3697245100% (3)
- Receptores NKDocumento2 pagineReceptores NKToledo YamilaNessuna valutazione finora
- Inmunidad InnataDocumento14 pagineInmunidad InnataMelissa RodriguezNessuna valutazione finora
- Alonso, Neuropéptidos, Estrés y AlergiaDocumento16 pagineAlonso, Neuropéptidos, Estrés y AlergiaPC Marian RjNessuna valutazione finora
- Tarea S10 Histología MédicaDocumento8 pagineTarea S10 Histología MédicaNikola García RiveraNessuna valutazione finora
- Tema 5. Reconocimiento en La Inmunidad InnataDocumento5 pagineTema 5. Reconocimiento en La Inmunidad InnatalucisNessuna valutazione finora
- Sem1 InmunoDocumento79 pagineSem1 InmunoRicardo DanielNessuna valutazione finora
- El Proceso de Expresión Génica2Documento21 pagineEl Proceso de Expresión Génica2Erika PerezNessuna valutazione finora
- 572-Texto Del Artículo-1074-1-10-20190702 PDFDocumento10 pagine572-Texto Del Artículo-1074-1-10-20190702 PDFFernanda AltamiranoNessuna valutazione finora
- Inmunidad InnataDocumento38 pagineInmunidad InnataAnyello BuitragoNessuna valutazione finora
- NomenclaturaDocumento3 pagineNomenclaturaNadia Araya AvendañoNessuna valutazione finora
- La Genética en La ActualidadDocumento28 pagineLa Genética en La Actualidadeddy leonNessuna valutazione finora
- Consenso Psoriasis. Actualizacion 2019 14112019Documento22 pagineConsenso Psoriasis. Actualizacion 2019 14112019Giorjhian Erick Lomas ArenasNessuna valutazione finora
- Gui As Basadas en La Evidencia para El Manejo de La Psoriasis en Colombia - EsDocumento257 pagineGui As Basadas en La Evidencia para El Manejo de La Psoriasis en Colombia - Esdarturo67Nessuna valutazione finora
- Mehu100 U1 t9 Sindromes Mielodisplasicos GoldmanDocumento7 pagineMehu100 U1 t9 Sindromes Mielodisplasicos GoldmanMarijose Salas VargasNessuna valutazione finora
- Mehu100 - U1 - t9 - Sindromes Mielodisplasicos y Neoplasias RozmannDocumento5 pagineMehu100 - U1 - t9 - Sindromes Mielodisplasicos y Neoplasias RozmannMarijose Salas VargasNessuna valutazione finora
- Mehu100 U1 t9 Sindromes Mielodisplasicos GoldmanDocumento7 pagineMehu100 U1 t9 Sindromes Mielodisplasicos GoldmanMarijose Salas VargasNessuna valutazione finora
- Guias Clinica Psoariasis ChileDocumento19 pagineGuias Clinica Psoariasis ChileCarlos DNessuna valutazione finora
- 2.proteccion RadiologicaDocumento8 pagine2.proteccion RadiologicaMarijose Salas VargasNessuna valutazione finora
- Resultados y Discusión de ResultadosDocumento6 pagineResultados y Discusión de ResultadosMarijose Salas VargasNessuna valutazione finora
- Fisiología Tiroides y ParatiroidesDocumento43 pagineFisiología Tiroides y ParatiroidesMarijose Salas VargasNessuna valutazione finora
- Lectura Previa 2 - HCL ElectrónicaDocumento22 pagineLectura Previa 2 - HCL ElectrónicaMarijose Salas VargasNessuna valutazione finora
- Silabo - ParasitologíaDocumento12 pagineSilabo - ParasitologíaMarijose Salas Vargas100% (2)
- Marco TeoricoDocumento3 pagineMarco TeoricoMarijose Salas VargasNessuna valutazione finora
- Farmaco Informe IiiDocumento21 pagineFarmaco Informe IiiMarijose Salas VargasNessuna valutazione finora
- Tiroides - Doctor SalazarDocumento78 pagineTiroides - Doctor SalazarMarijose Salas VargasNessuna valutazione finora
- Clase Medula p2Documento44 pagineClase Medula p2Marijose Salas VargasNessuna valutazione finora
- Practicas de Lab. Morfofisiologia PDFDocumento91 paginePracticas de Lab. Morfofisiologia PDFMarijose Salas VargasNessuna valutazione finora
- Citogenética Humana Oncohematologia PDFDocumento8 pagineCitogenética Humana Oncohematologia PDFjhonandyramosNessuna valutazione finora
- Inmunidad Adaptativa y Presentacion de AntigenoDocumento34 pagineInmunidad Adaptativa y Presentacion de AntigenoAna Flores CahuayaNessuna valutazione finora
- Reacción en Cadena de La Polimerasa (PCR)Documento20 pagineReacción en Cadena de La Polimerasa (PCR)Jhon Kevin Bonilla LeónNessuna valutazione finora
- Manual VIHDocumento36 pagineManual VIHMemo TutNessuna valutazione finora
- Tema 1 Introduccion A La Inmunologia 2020-2021 x2Documento17 pagineTema 1 Introduccion A La Inmunologia 2020-2021 x2León Felipe Ureña100% (1)
- Biologia Euclides 01Documento14 pagineBiologia Euclides 01stiven guerrero paivaNessuna valutazione finora
- Mapa Conceptual Sistema InmuneDocumento2 pagineMapa Conceptual Sistema InmunedenisseNessuna valutazione finora
- Laringitis Aguda y CrónicaDocumento14 pagineLaringitis Aguda y CrónicaCarly Arratia Valdez50% (2)
- Enter o CoccusDocumento47 pagineEnter o Coccusbilly casasNessuna valutazione finora
- Promsa InformesDocumento2 paginePromsa InformesZerjmaster19Nessuna valutazione finora
- Clase #5 Genoma HumanoDocumento34 pagineClase #5 Genoma HumanoAsafh FernandezNessuna valutazione finora
- Tema 1Documento30 pagineTema 1Paula EscobarNessuna valutazione finora
- EnterobacteriasDocumento13 pagineEnterobacteriasAbigail VCNessuna valutazione finora
- FINAL DE BIOLOGÍA - 1RA MARZO 2022-MescladoDocumento67 pagineFINAL DE BIOLOGÍA - 1RA MARZO 2022-MescladoTercio SANTOSNessuna valutazione finora
- Lectura 3aDocumento16 pagineLectura 3aYerlin Huamán BautistaNessuna valutazione finora
- Guia7-Sistema-Inmune en Los Seres VivosDocumento18 pagineGuia7-Sistema-Inmune en Los Seres VivosMaria Elena SaraviaNessuna valutazione finora
- Glosario de Anatomia Patologica (4ta Semana) .Documento6 pagineGlosario de Anatomia Patologica (4ta Semana) .JUAN FRANCISCO GOMEZ CERINONessuna valutazione finora
- Generalidades de Los AntibióticosDocumento11 pagineGeneralidades de Los AntibióticosDiego SalinasNessuna valutazione finora
- Modulo 1 Asistente de Laboratorio y ExtraccionistaDocumento212 pagineModulo 1 Asistente de Laboratorio y Extraccionistaveradebora602Nessuna valutazione finora
- Fito 9Documento17 pagineFito 9Jose Alcantara VergaraNessuna valutazione finora
- MENINGITISDocumento49 pagineMENINGITISDiana Janeth García ZamoraNessuna valutazione finora
- ApicomplexaDocumento42 pagineApicomplexaPedro PalmaNessuna valutazione finora
- EmbDocumento3 pagineEmbana mariaNessuna valutazione finora
- Cuadro SinopticoDocumento1 paginaCuadro SinopticoPepe Mejia100% (2)
- Antibioticos y Quimioterapeuticos, Resistencia, Mecanismos de AcciónDocumento90 pagineAntibioticos y Quimioterapeuticos, Resistencia, Mecanismos de AcciónJosé Manuel100% (16)
- CuestionarioDocumento4 pagineCuestionarioRogelioNessuna valutazione finora
- Guías Prácticas de GenéticaDocumento27 pagineGuías Prácticas de GenéticaLuis SierraNessuna valutazione finora
- Apuntes Pruebas BioqimicasDocumento40 pagineApuntes Pruebas BioqimicasAbii De OsorioNessuna valutazione finora
- Evaluacion Final Periodo Iv Noveno 2015Documento2 pagineEvaluacion Final Periodo Iv Noveno 2015Lina Luz Perez MedranoNessuna valutazione finora