Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Fisica M PDF
Caricato da
yordan0 valutazioniIl 0% ha trovato utile questo documento (0 voti)
151 visualizzazioni2 pagineEste documento presenta varios problemas de cálculo de termodinámica que involucran transferencia de calor y cambios de estado. Los problemas implican calcular temperaturas finales, cantidades de calor transferido y masas de sustancias cuando se ponen en contacto bloques metálicos, hielo, agua y otros materiales a diferentes temperaturas iniciales dentro de calorímetros y otros recipientes.
Descrizione originale:
Titolo originale
fisica m.pdf
Copyright
© © All Rights Reserved
Formati disponibili
PDF, TXT o leggi online da Scribd
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoEste documento presenta varios problemas de cálculo de termodinámica que involucran transferencia de calor y cambios de estado. Los problemas implican calcular temperaturas finales, cantidades de calor transferido y masas de sustancias cuando se ponen en contacto bloques metálicos, hielo, agua y otros materiales a diferentes temperaturas iniciales dentro de calorímetros y otros recipientes.
Copyright:
© All Rights Reserved
Formati disponibili
Scarica in formato PDF, TXT o leggi online su Scribd
0 valutazioniIl 0% ha trovato utile questo documento (0 voti)
151 visualizzazioni2 pagineFisica M PDF
Caricato da
yordanEste documento presenta varios problemas de cálculo de termodinámica que involucran transferencia de calor y cambios de estado. Los problemas implican calcular temperaturas finales, cantidades de calor transferido y masas de sustancias cuando se ponen en contacto bloques metálicos, hielo, agua y otros materiales a diferentes temperaturas iniciales dentro de calorímetros y otros recipientes.
Copyright:
© All Rights Reserved
Formati disponibili
Scarica in formato PDF, TXT o leggi online su Scribd
Sei sulla pagina 1di 2
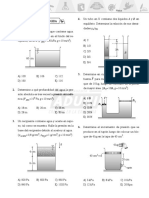
PRÁCTICA 1: TERMODINÁMICA PARTE II
1.- Un bloque de cobre de 75 g se saca de El calorímetro y el agua se encuentran
un horno y se echa en un vaso de cristal en equilibrio térmico a 10,0 °C. Se
de 300 g que contiene 200 g de agua. Se colocan dos bloques metálicos dentro del
observa que la temperatura del agua y el agua. Uno de ellos es una pieza de cobre
calorímetro se elevan desde 12 °C a 27 de 50,0 g a 80,0 °C. El otro bloque tiene
°C. ¿Cuál era la temperatura del horno si una masa de 0,0 g y se halla
el calor específico del cobre es igual a originalmente a una temperatura de 100
0,093 y el del vidrio 0,118? °C.
(R.: 533,24 °C). El sistema completo se estabiliza a una
2.- 20 g de hielo en el calorímetro de temperatura final de 20,0 °C. (a)
cobre de 10 g de masa se encuentran a Determine el calor específico de la
una temperatura de − 30 °C. ¿Cuánto muestra desconocida. (b) Adivine cuál es
vapor a 100 °C debe condensarse si el el material de la muestra desconocida,
hielo se transforma en agua y se calienta usando los datos reflejados en alguna
a 40 °C. tabla sobre calores específicos.
(R.: 4,6 g) (R.: a) 0,435 cal/g °C)
3.- Una muestra de 50,0 g de cobre se 6.- Un termómetro de 0,055 kg de masa y
halla a una temperatura de 25,0 °C. Si se cuyo calor específico es de 0,2 cal/g
añaden a la muestra 1200 J de energía marca 15 °C. Luego se sumerge
mediante transferencia de calor, ¿cuál completamente en 0,3 kg y alcanza la
será la temperatura final del cobre? (ccobre misma temperatura final que el agua. Si
= 38 J/kg °C) el termómetro marca 44,4 °C y es exacto,
(R.: 87,0 °C) ¿cuál era la temperatura del agua antes de
4.- Una herradura de hierro de 1,5 kg, que se sumergiera el termómetro?
que inicialmente se encuentra a una (R.: 45,5 °C)
temperatura de 60,0 °C, se introduce en 7.- Un calorímetro, de calor específico
un cubo que contiene 20,0 kg de agua a despreciable, contiene 200 g de agua y
20,0°C. ¿Cuál es la temperatura final? 500 g de hielo a una temperatura de 0 °C.
(Ignore el calor específico del contenedor se toma un bloque metálico de 0,3 kg de
y suponga que la cantidad de agua que se un horno a una temperatura de 220 °C y
evapora al introducir la herradura es se deja caer rápidamente dentro del
despreciable) calorímetro. Determine 1
(R.: 29,6 °C) (a) el calor específico del bloque
5.- Un calorímetro de aluminio, con una metálico,
masa de 100 g, contiene 250 g de agua.
Prof. Giovanni Salini C. | Dr. en Cs. Físicas| Física II (230016) | Departamento de Física |
Noviembre 2011
(b) ¿para qué masa del bloque, a la (c) ¿Qué sucederá si se añaden 200 g de
misma temperatura de 220 °C, se hielo fundente?
evaporará el 1% del agua? ccobre = 39 J/kg K; chielo = 4180 JkgK.
LV = 540 cal /g; LF = 80 cal/g. (R.: a) 190 g; b) 6 °C)
(R.: a) 0,6 cal/g °C; b) 1,58 kg)) 12.- Un bloque de cobre de 1,00 kg a 20
8.- Una bala de plomo de 3,0 g a 30,0 °C °C se deja caer en un gran tanque de
es disparada con una rapidez de 240 m/s, nitrógeno líquido a 77,3 K. ¿Cuántos
incrustándose en un gran bloque de hielo kilógramos de nitrógeno se habrán
a 0 °C. ¿Qué cantidad de hielo se funde? evaporado cuando el cobre alcance la
cplomo= 128 J/kg°C; LF=3,33×105 J/kg. temperatura de 77,3 K? ccobre = 0,0920
(R.: 0,294 g). cal/g °C; el calor latente de vaporización
9.- Dos cubos de hielo de 50 g se el nitrógeno es de 48,0 cal/g.
introducen en un vaso que contiene 200 13.- Un calorímetro de cobre de 50,0 g
g de agua. Si la temperatura inicial del contiene 250 g de agua a 20,0 °C.
agua era 25 °C, y si el hielo provenía ¿Cuánto vapor debe condensarse en el
directamente de un refrigerador que agua para que la temperatura final del
opera a − 15 °C, ¿cuál será la sistema alcance los 50,0 °C?
temperatura final de la bebida? Calor (R.: 12,9 g de vapor)
específico del hielo es de 0,5 cal/g °C y
el calor latente de fusión es 80 cal/g.
10.- En un vaso Dewar que contiene 300
g de un líquido a 25 °C se introducen
150 g de hielo a − 6 °C.
(a) Se fundirá todo el hielo suponiendo
que el vaso está bien aislado?
(b) Si no se funde totalmente, ¿qué masa
de hielo subsistirá una vez alcanzado el
equilibrio?
(c) ¿A qué temperatura debería estar
inicialmente el líquido para que se
fundiera justamente el hielo y todo el
sistema quedara a 0 °C.
(R.: b) 57 g de hielo; c) 40 °C)
11.- En un recinto térmicamente aislado
hay un litro de agua a 12 °C, En ella se
introducen 150 g de cobre a 200 °C.
(a) ¿Qué cantidad de hielo fundente
habrá que añadir para que, una vez 2
fundida, la temperatura final sea de 0°C?
(b) ¿Qué temperatura se alcanzará si se
añaden 100 g de hielo fundente?
Prof. Giovanni Salini C. | Dr. en Cs. Físicas| Física II (230016) | Departamento de Física |
Noviembre 2011
Potrebbero piacerti anche
- BarfDocumento34 pagineBarfmiguel33% (3)
- Autoescala de Ansiedad de ZungDocumento2 pagineAutoescala de Ansiedad de ZungALexandraNessuna valutazione finora
- Folleto Jaguar en MexicoDocumento18 pagineFolleto Jaguar en MexicoPedro Mentado100% (1)
- Esfuerzos AxilesDocumento29 pagineEsfuerzos AxilesIvanNessuna valutazione finora
- Elaboración de Un Tratamiento (Jabón) A Base de La Sábila (Aloe Vera) para La Disminución Del Acné.Documento28 pagineElaboración de Un Tratamiento (Jabón) A Base de La Sábila (Aloe Vera) para La Disminución Del Acné.Saby Chuan50% (4)
- CALORIMETRÍADocumento21 pagineCALORIMETRÍANoelia Pedrozo100% (1)
- Guia 2 Termo Fisica 2-2-2012Documento2 pagineGuia 2 Termo Fisica 2-2-2012Carlos RíosNessuna valutazione finora
- Bull Worker 2Documento26 pagineBull Worker 2jaglarti1997100% (2)
- Educacion SocioemocionalDocumento50 pagineEducacion SocioemocionalAra Zunún50% (2)
- Calor Nuevo PDFDocumento4 pagineCalor Nuevo PDFPatricio AcostaNessuna valutazione finora
- Maniqui Primer ParcialDocumento5 pagineManiqui Primer ParcialSol Alejandra Gomez Pinto100% (1)
- La Voz - 2014Documento108 pagineLa Voz - 2014Lorena Do Val100% (2)
- Fisica 13 Cambio de Fase (1) UnlockedDocumento6 pagineFisica 13 Cambio de Fase (1) UnlockedGerardo Manrique TelloNessuna valutazione finora
- 02 Dinamica Rotacional I V2 PDFDocumento2 pagine02 Dinamica Rotacional I V2 PDFDiego AlejandroNessuna valutazione finora
- Copia de TEMPERATURA Y DILATACIÓN1Documento3 pagineCopia de TEMPERATURA Y DILATACIÓN1Jorge Condori VilcaNessuna valutazione finora
- Boletin Problemas Campo Magn - Fisica 2 - 2015-16Documento6 pagineBoletin Problemas Campo Magn - Fisica 2 - 2015-16Ana LopezNessuna valutazione finora
- CURVILINEODocumento3 pagineCURVILINEOAntonella Gutiérrez HerreraNessuna valutazione finora
- Semana 8 - FísicaDocumento4 pagineSemana 8 - FísicaSintia IrigoinNessuna valutazione finora
- DILATACIONDocumento4 pagineDILATACIONEmely Castañeda SotoNessuna valutazione finora
- CalorimetríaDocumento5 pagineCalorimetríaDogezNessuna valutazione finora
- Leyes de Newton IIIDocumento4 pagineLeyes de Newton IIIArturo Rubén Lozano PérezNessuna valutazione finora
- EjerciciosDocumento2 pagineEjerciciosluis fernando lopez quispeNessuna valutazione finora
- Trabajo DinamicaDocumento15 pagineTrabajo DinamicacarlosNessuna valutazione finora
- Ejercicios Resueltos UD 1 ElectroestaticaDocumento15 pagineEjercicios Resueltos UD 1 Electroestaticaandoni_losada3501Nessuna valutazione finora
- Magnitud Del Campo MagnéticoDocumento9 pagineMagnitud Del Campo MagnéticoJoseKenwan0% (1)
- MRU Prim OpcDocumento7 pagineMRU Prim OpcalfredoNessuna valutazione finora
- Fisica Rudy Espinoza NimaDocumento3 pagineFisica Rudy Espinoza NimaNicolleSosaPerezNessuna valutazione finora
- Electromagnetism oDocumento15 pagineElectromagnetism oNilson Rincon GNessuna valutazione finora
- Problemas y Aplicaciones de La Primera Ley de La TermodinámicaDocumento37 pagineProblemas y Aplicaciones de La Primera Ley de La TermodinámicaalexanderNessuna valutazione finora
- Ejercicios T.5. Campo MagnéticoDocumento5 pagineEjercicios T.5. Campo Magnéticoiretchai100% (1)
- EJERCICIOS PROPUESTOS de CAPACITANCIA Corriente y Resistencia Campo MagneticoDocumento2 pagineEJERCICIOS PROPUESTOS de CAPACITANCIA Corriente y Resistencia Campo MagneticoAlvaro Christian Apaza LajoNessuna valutazione finora
- Ejercicios de Fisica Sobre La DilatacionDocumento6 pagineEjercicios de Fisica Sobre La DilatacionMarcos Oliverth Zúñiga ZapataNessuna valutazione finora
- Utf 8Documento10 pagineUtf 8Maria Xime Velasquez MontañoNessuna valutazione finora
- FisicaDocumento2 pagineFisicapichanaqui mendez palaciosNessuna valutazione finora
- Tarea # 4 Ejercicios Propuestos de Corriente y Resistencia 2022-1Documento2 pagineTarea # 4 Ejercicios Propuestos de Corriente y Resistencia 2022-1Alessandra LazoNessuna valutazione finora
- ClasicoDocumento4 pagineClasicoluis lopezNessuna valutazione finora
- Ejercicios de Magnetismo PDFDocumento2 pagineEjercicios de Magnetismo PDFskak26Nessuna valutazione finora
- Fisica 09 Ondas ViajerasDocumento6 pagineFisica 09 Ondas ViajerasRoque RodolfoNessuna valutazione finora
- Problema Ascensor 120918Documento1 paginaProblema Ascensor 120918Angel ZabalaNessuna valutazione finora
- CamposDocumento5 pagineCamposangelaNessuna valutazione finora
- t18 Electromagnetismo II Lbyron 2020-IIDocumento7 paginet18 Electromagnetismo II Lbyron 2020-IIEdinson FernandezNessuna valutazione finora
- F 09Documento3 pagineF 09Quimica TecnologiaNessuna valutazione finora
- Cant Mov 2022docDocumento8 pagineCant Mov 2022docBalo DueNessuna valutazione finora
- Teoria de Exponentes A1Documento1 paginaTeoria de Exponentes A1Neiser ChoquehuancaNessuna valutazione finora
- Guia de Ejercicios N 1Documento4 pagineGuia de Ejercicios N 1Carlos VildenNessuna valutazione finora
- Proelm 2Documento8 pagineProelm 2Teresa del RíoNessuna valutazione finora
- Tema 22 - Fenómenos TérmicosDocumento5 pagineTema 22 - Fenómenos TérmicosErick Keyser Abanto VillarrealNessuna valutazione finora
- Problemas Propuestos Ecuaciones 1Documento1 paginaProblemas Propuestos Ecuaciones 1Noelia Eva Castillo LlicaNessuna valutazione finora
- 2do Seminario Fisica Adm 2006-IIDocumento16 pagine2do Seminario Fisica Adm 2006-IIRobinson Riojas BalderaNessuna valutazione finora
- Primer Taller de Electro 2011Documento2 paginePrimer Taller de Electro 2011Jimmy Alexander CLNessuna valutazione finora
- Campo MagnéticoDocumento2 pagineCampo MagnéticoPaco1960Nessuna valutazione finora
- Semana4 1raLeyMaquinasDocumento1 paginaSemana4 1raLeyMaquinasOmarVargasNessuna valutazione finora
- Tema 02 - HidrodinámicaDocumento4 pagineTema 02 - HidrodinámicaCésar Loyola AsmatNessuna valutazione finora
- Algoritmia SensorialDocumento4 pagineAlgoritmia SensorialValentin Zavaleta MiguelNessuna valutazione finora
- 8-Sistemas de Partículas (NXPowerLite) TDocumento86 pagine8-Sistemas de Partículas (NXPowerLite) TFederico AngoletanoNessuna valutazione finora
- 10 DomiciliariaDocumento3 pagine10 DomiciliariaJULIO MOHAMED TUYA CALVONessuna valutazione finora
- Prob 9Documento7 pagineProb 9Zoroastrocain Hans ZoroastrocainNessuna valutazione finora
- Int. ElectromagnéticaDocumento6 pagineInt. ElectromagnéticaRoberto VazquezNessuna valutazione finora
- 11 - ELECTROSTATICA II - Sel5 PDFDocumento4 pagine11 - ELECTROSTATICA II - Sel5 PDFWALTER OLIVARI RAMIREZNessuna valutazione finora
- Distribución Energética de Huecos y ElectronesDocumento4 pagineDistribución Energética de Huecos y ElectronesFernando Frias CabrejosNessuna valutazione finora
- 56211Documento7 pagine56211Marco Parada DemiquelNessuna valutazione finora
- Curso Fisica Moderna - Virgilio Acosta LimaneDocumento520 pagineCurso Fisica Moderna - Virgilio Acosta LimanejapeleNessuna valutazione finora
- 30882f - UMSS - Problemas de Olimpiada OBF - OBAA Fase Departamental 1ra Ed PDFDocumento143 pagine30882f - UMSS - Problemas de Olimpiada OBF - OBAA Fase Departamental 1ra Ed PDFHugo FloresNessuna valutazione finora
- 20.1 Electrodinamica (CEPRU)Documento4 pagine20.1 Electrodinamica (CEPRU)Venus PerezNessuna valutazione finora
- Balota N°10 Electrostatica Repaso PDFDocumento4 pagineBalota N°10 Electrostatica Repaso PDFwallyNessuna valutazione finora
- Guia 2 Termo Fisica 2 - UBBDocumento2 pagineGuia 2 Termo Fisica 2 - UBBCarlos RíosNessuna valutazione finora
- Física 2: CalorimetríaDocumento3 pagineFísica 2: CalorimetríaMirely Juleysi Guevara BecerraNessuna valutazione finora
- Cambios de FaseDocumento4 pagineCambios de FaseNoelia BohórquezNessuna valutazione finora
- TrabajosDocumento2 pagineTrabajosyordanNessuna valutazione finora
- TrabajosDocumento2 pagineTrabajosyordanNessuna valutazione finora
- Ultima PD PDFDocumento1 paginaUltima PD PDFyordanNessuna valutazione finora
- 2019-B - Introducción A La Geometría DiferencialDocumento6 pagine2019-B - Introducción A La Geometría DiferencialyordanNessuna valutazione finora
- SILABO Funcional 2019-BDocumento8 pagineSILABO Funcional 2019-ByordanNessuna valutazione finora
- Preguntas Teoricas PDFDocumento1 paginaPreguntas Teoricas PDFyordanNessuna valutazione finora
- 1era PCDocumento1 pagina1era PCyordanNessuna valutazione finora
- Cuzcano Solucionario AlgebraDocumento10 pagineCuzcano Solucionario AlgebrayordanNessuna valutazione finora
- 5-1 Cadena Del Valor-DetalladaDocumento5 pagine5-1 Cadena Del Valor-DetalladayordanNessuna valutazione finora
- Catálogo Soluciones Eléctricas Integrales 2016 PDFDocumento12 pagineCatálogo Soluciones Eléctricas Integrales 2016 PDFyordanNessuna valutazione finora
- Calidad USMPDocumento3 pagineCalidad USMPyordanNessuna valutazione finora
- Alimentación de Caninos y Felinos 1Documento19 pagineAlimentación de Caninos y Felinos 1yeximarNessuna valutazione finora
- Ac - S13Documento12 pagineAc - S13Adriana Fuentes LaraNessuna valutazione finora
- Infografia Resolución 256 de 2016Documento8 pagineInfografia Resolución 256 de 2016jasbleidy deviaNessuna valutazione finora
- Samu-Sistema de Atención Movil de UrgenciaDocumento18 pagineSamu-Sistema de Atención Movil de UrgenciaKarol M.Nessuna valutazione finora
- Pract. 10 - QuímicaDocumento8 paginePract. 10 - QuímicaDesaprende con GonzalesNessuna valutazione finora
- Catéteres para ACTPDocumento75 pagineCatéteres para ACTPmariae2Nessuna valutazione finora
- Upadesamrta 1Documento11 pagineUpadesamrta 1mahakaladasNessuna valutazione finora
- Cuadernillo Preguntas de RepasoDocumento69 pagineCuadernillo Preguntas de RepasoAldo MerinoNessuna valutazione finora
- Balance HidricoDocumento25 pagineBalance HidricoEduardo Luisenrique Sanchez CarrionNessuna valutazione finora
- Variedades 610Documento8 pagineVariedades 610Mónica LozaNessuna valutazione finora
- Memoria Tecnica Acueducto El Limon y Barro Blanco ImpresionDocumento100 pagineMemoria Tecnica Acueducto El Limon y Barro Blanco ImpresionCarlos Hugo Montoya AriasNessuna valutazione finora
- Tipos de FiebreDocumento6 pagineTipos de FiebreJosver PretellNessuna valutazione finora
- Acta - Fabricación de FiltrosfffDocumento4 pagineActa - Fabricación de FiltrosfffPaty ChiluisaNessuna valutazione finora
- Tarea Juan Valencia Serie Electrodos de ReferenciaDocumento12 pagineTarea Juan Valencia Serie Electrodos de Referenciajuan valenciaNessuna valutazione finora
- Sesi 15Documento5 pagineSesi 15manson msmsNessuna valutazione finora
- Trabajo Final Mantemiento Basico Del MotorDocumento19 pagineTrabajo Final Mantemiento Basico Del MotorRonaldo Quinto MachacaNessuna valutazione finora
- Productos de ExportacionDocumento7 pagineProductos de ExportacionBreña Matias JØrgeNessuna valutazione finora
- F6.1 2 3 PAU FísicaModernaDocumento21 pagineF6.1 2 3 PAU FísicaModernaDaniel RodríguezNessuna valutazione finora
- F-C-27 Lista Chequeo Andamio CrucetaDocumento1 paginaF-C-27 Lista Chequeo Andamio CrucetafrankruedaboteroNessuna valutazione finora
- Informe Circuitos en ConexiónDocumento38 pagineInforme Circuitos en ConexiónWILSON ANDRES CASTILLO BENITESNessuna valutazione finora
- Jumbo 10A PGIRSDocumento2 pagineJumbo 10A PGIRSLivington GabrielNessuna valutazione finora
- Laboratorio 2 Fresadora StarkDocumento8 pagineLaboratorio 2 Fresadora Starkdacs33349Nessuna valutazione finora