Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Practica Calificada Trabajo Pourbaix 2017
Caricato da
Katherin Carhuas QuispeCopyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Practica Calificada Trabajo Pourbaix 2017
Caricato da
Katherin Carhuas QuispeCopyright:
Formati disponibili
Escuela Profesional de Ingeniería Metalúrgica.
- UNSA
Corrosión y Protección de Metales.- Practica calificada – 2017
APELLIDOS: FIRMA
NOMBRES:
PRACTICA CALIFICADA
CONSTRUCCIÓN DEL DIAGRAMA E - pH
Resumen de las ideas clave
En este artículo vamos a aprender qué es un diagrama de Pourbaix, cuáles son sus principales características,
cuál es su utilidad y cómo se interpretan los datos que contienen. Todo ello lo veremos a través de ejemplos
prácticos para facilitar el aprendizaje de los conceptos básicos descritos en el presente documento.
2 Objetivos
Una vez que el alumno se lea con detenimiento este documento, será capaz de:
Interpretar los datos representados en un diagrama de Pourbaix.
Predecir las zonas de inmunidad, corrosión y pasivación de un metal en un medio agresivo
determinado.
3 Introducción
¿Cómo podemos determinar las regiones de estabilidad termodinámica de las especies de un metal en un
medio dado?. Esto podemos hacerlo a través de los diagramas potencial-pH, conocidos como diagramas
de Pourbaix, debido a que fue el primero en sugerirlos en 1945, los cuales serán descritos en el presente
documento.
4 Desarrollo
4.1 Definición de diagrama de Pourbaix
Un diagrama de Pourbaix es una representación gráfica del potencial (ordenada) en función del pH
(abscisa) para un metal dado bajo condiciones termodinámicas standard (usualmente agua a 25 ºC). El
diagrama tiene en cuenta los equilibriosmquímicos y electroquímicos y define el dominio de estabilidad para
el electrólito (normalmente agua), el metal y los compuestos relacionados, por ejemplo, óxidos, hidróxidos e
hidruros. Tales diagramas puedes construirlos a partir de cálculos basados en la ecuación de Nernst y en las
constantes de equilibrio de distintos compuestos metálicos [1-4].
A modo de ejemplo en la Figura 1 puedes ver el diagrama de Pourbaix para un sistema metal-agua, como
es el caso del sistema níquel-agua a 25 ºC. En dicho diagrama puedes observar las regiones de estabilidad
termodinámica de las especies de níquel en agua: Ni, NiH 0,5, β-Ni(OH)2, NiOOH (fase-beta), NiO2
(fasegamma), Ni+2, NiOH+, − Ni(OH)3- y Ni(OH)4-2 . La presencia de agentes complejantes, como por ejemplo,
cloruros, bromuros, cianuros, amoniaco, carbonatos, etc., puede modificar apreciablemente los diagramas
de Pourbaix debido a la formación con el metal de complejos altamente estables en disolución o de sales
insolubles. Como consecuencia, en los diagramas aparecen nuevos dominios para las especies iónicas en
disolución que ocupan espacios más amplios que los correspondientes a los sistemas metal-agua. En la
Figura 2 puedes ver un ejemplo de un diagrama de Pourbaix para el sistema ternario níquel-bromuro-agua
a 25 ºC, correspondiente al níquel en una disolución acuosa de bromuro de litio (LiBr) de 850 g/l a 25 ºC. En
dicho diagrama puedes observar la región de estabilidad termodinámica de una nueva especie acuosa:
NiBr2.
Ing. D. Carcausto Z. 1 Ing. V. Bustinza R.
Escuela Profesional de Ingeniería Metalúrgica.- UNSA
Corrosión y Protección de Metales.- Practica calificada – 2017
4.2 Características de los diagramas de Pourbaix
Como puedes observar en las Figuras 1 y 2, hay tres tipos generales de líneas en los diagramas de Pourbaix,
cada una representa un equilibrio entre dos especies:
Líneas horizontales. Indican reacciones con dependencia solamente del potencial.
Líneas verticales. Indican reacciones con dependencia solamente del pH.
Ing. D. Carcausto Z. 2 Ing. V. Bustinza R.
Escuela Profesional de Ingeniería Metalúrgica.- UNSA
Corrosión y Protección de Metales.- Practica calificada – 2017
Líneas oblicuas. Indican reacciones con dependencia tanto del potencial como del pH.
También puedes observar que estos tres tipos de líneas aparecen representadas en el diagrama con dos
tipos de trazado: continuo y discontinuo fino. Si aparecen con trazado continuo indican un equilibrio bien
entre dos especies sólidas o bien entre una especie sólida y una especie soluble con distintos valores de
actividad (10–6, 10–4, 10–2 y 100). Si aparecen con trazado discontinuo fino indican un equilibrio entre
dos especies solubles.
Por último, verás que en los diagramas aparecen dos líneas discontinuas gruesas señaladas como “a” y “b”,
que representan el equilibrio de descomposición del agua con desprendimiento de oxígeno e hidrógeno,
respectivamente. La región entre las dos líneas representa una zona donde el agua es estable con respecto
al oxígeno y al hidrógeno. Por encima de la línea “a” (condiciones oxidantes), el agua se descompone por
desprenderse oxígeno en forma de gas. Por debajo de la línea “b” (condiciones reductoras), el agua se
descompone por desaparecer los protones en forma de hidrógeno gaseoso.
4.3 Usos de los diagramas de Pourbaix
Los diagramas de Pourbaix son útiles en el campo de la corrosión, además de en otros muchos campos,
tales como electrolisis industrial, recubrimiento, electroobtención y electrorefinado de metales, celdas
eléctricas primarias y secundarias, tratamiento de aguas e hidrometalurgia, etc. [2]. Los diagramas de
Pourbaix son particularmente útiles en el estudio del comportamiento frente a la corrosión de materiales
metálicos, ya que permiten predecir las zonas de inmunidad, corrosión y pasivación de un metal en un medio
agresivo determinado. Si el metal en su forma elemental es la fase termodinámicamente estable, esto
indicará condiciones de inmunidad. La corrosión ocurrirá si un catión soluble del metal es la fase
termodinámicamente estable. Si un anión complejo soluble del catión en medio alcalino es la fase
termodinámicamente estable, lo que ocurre en el caso de metales anfóteros, como por ejemplo, hierro,
aluminio, cinc, etc., esto indicará condiciones de corrosión alcalina. La pasivación ocurrirá si un compuesto
sólido del metal es la fase termodinámicamente estable, como por ejemplo, óxido, hidróxido o hidruros. Esta
es la razón por la cual habitualmente en los estudios de corrosión los diagramas de Pourbaix aparecen de
forma simplificada mostrando las regiones descritas y sin precisar cuales son las especies estables en cada
condición.
En la Figura 3 puedes ver un diagrama de Pourbaix simplificado para el sistema níquel-agua a 25 ºC, mientras
que en la Figura 4 puedes ver un diagrama de Pourbaix simplificado para el sistema níquel- romuro-agua a
25ºC, correspondiente al níquel en una disolución acuosa de LiBr de 850 g/l a 25 ºC. Dichos diagramas
normalmente los tienes que representar considerando una actividad de 10 para las especies de níquel
–6
solubles, la cual se considera como delimitación neta entre las regiones de corrosión, por una parte, y las
regiones de inmunidad y pasivación por otra. Las áreas de corrosión aparecen sombreadas para
diferenciarlas de las áreas de inmunidad y pasivación.
Ing. D. Carcausto Z. 3 Ing. V. Bustinza
R.
Escuela Profesional de Ingeniería Metalúrgica.- UNSA
Corrosión y Protección de Metales.- Practica calificada – 2017
4.4 Interpretación de los diagramas de Pourbaix
Una vez visto qué son, cuales son las principales características y cuál es la utilidad de los diagramas de
Pourbaix, ahora vamos a ver cómo se interpretan los datos representados en dichos diagramas. En primer
lugar, vamos a interpretar el diagrama de Pourbaix para el sistema níquel agua a 25 ºC (Figura 1). Dicho
diagrama muestra que el níquel es un metal relativamente noble, debido a que su zona de inmunidad tiene
un parte en común con la zona de estabilidad del agua. Esto significa que el níquel no podrá reducir al agua
en este área. Sin embargo, la resistencia a la corrosión del níquel depende fuertemente del pH y de la
Ing. D. Carcausto Z. 4 Ing. V. Bustinza
R.
Escuela Profesional de Ingeniería Metalúrgica.- UNSA
Corrosión y Protección de Metales.- Practica calificada – 2017
presencia de agentes de oxidación. En disoluciones ácidas y neutras, el níquel se corroe a través de la
predominancia del ion Ni+2. En disoluciones débiles y fuertemente alcalinas, el níquel se pasiva con formación
del compuesto sólido β-Ni(OH)2. Si aumentamos la actividad de Ni+2 de 10–6 a 100 esto nos lleva a una
disminución del valor de pH para la formación de β-Ni(OH)2 a partir de Ni+2. En disoluciones fuertemente
alcalinas, el níquel se corroe a través de la formación de los iones − Ni(OH)3 y −2 Ni(OH)4 . A potenciales muy
altos, Ni+2, β-Ni(OH)2, −Ni(OH)3 y −2 Ni(OH)4 se oxidan para formar las especies sólidas iOOH (fase-beta) y NiO2
(fase-gamma). A bajos potenciales, el níquel y el ion Ni+2 pueden reducirse para formar el compuesto sólido
NiH0,5.
Ahora vamos a interpretar el diagrama de Pourbaix para el sistema níquel-agua a 25 ºC considerando sólo
las zonas de estabilidad de las especies solubles (líneas discontinuas finas en la Figura 1). Para el sistema
níquel-agua las especies de níquel solubles son: Ni+2, NiOH+, − Ni(OH)3 y −2 Ni(OH)4 . En este caso las zonas
de
predominancia de las especies de níquel solubles dependen sólo del pH, debido a que el diagrama
contiene únicamente especies solubles con el estado de oxidación +2.
Ahora vamos a interpretar el diagrama de Pourbaix para el sistema níquel-bromuroagua a 25 ºC (Figura 2).
La comparación del diagrama de Pourbaix para el sistema simple níquel-agua a 25 ºC en la Figura 1 con el
diagrama de Pourbaix para el sistema níquel-bromuro-agua a 25 ºC(Figura 2) muestra que la formación de
la especie acuosa NiBr2 extiende el rango de solubilidad del níquel a valores de pH más altos y a potenciales
más bajos, especialmente en disoluciones ácidas, neutras y débilmente alcalinas, como resultado de la
desestabilización de la especie sólida β-Ni(OH)2 y la promoción de un comportamiento más activo del níquel.
Finalmente, vamos a interpretar los diagramas de Pourbaix simplificados para el níquel en agua a 25 ºC en
ausencia y en presencia de ion bromuro (Figuras 3 y 4). La comparación de los diagramas de Pourbaix
simplificados para el níquel en agua en ausencia de ion bromuro (Figura 3) y en presencia de ion bromuro
(Figura 4) muestra que el tamaño de las áreas de inmunidad, corrosión y pasivación cambia con la presencia
de ion bromuro. Así, el área de corrosión en disoluciones ácidas, neutras y débilmente alcalinas aumenta,
mientras que las zonas de inmunidad, corrosión alcalina y pasivación disminuyen en presencia de ion
bromuro.
5 Cierre
A lo largo de este documento hemos aprendido qué son, cuales son las principales características y cuál es
la utilidad de los diagramas de Pourbaix, además de cómo se interpretan los datos representados en dichos
diagramas.
6 Bibliografía
[1] Pourbaix, M.: “Lecciones de corrosión electroquímica, tercera edición”, Ed. Instituto Español de
Corrosión y Protección, 1987.
[2] “ASM Handbook, vol. 13: Corrosion, ninth edition.”, Ed. ASM International, 1996, pág. 24.
[3] Fontana, M.G.: “Corrosion Engineeering, third edition”, Ed. McGraw Hill, 1988, pág. 453.
[4] Otero Huerta, E.: “Corrosion y degradación de materiales”, Ed. Síntesis, 1997, pág. 36.
Ing. D. Carcausto Z. 5 Ing. V. Bustinza
R.
Escuela Profesional de Ingeniería Metalúrgica.- UNSA
Corrosión y Protección de Metales.- Practica calificada – 2017
A partir de los datos termodinámicos G (Energía libre de Gibbs), de los compuestos de cobre soluble y sólido, se desarrolla la metodología para obtener el diagrama
0
E - pH del cobre.
Elemento o Compuesto G [kJ]
0 Concentración o actividad
Cu
0 0.00 1.0 [M] siempre
Cu
50.032 1.0 [M]
Cu
2 64.812 1.0 [M]
CuO -129.791 1.0 [M] siempre
Cu 2 O -146.119 1.0 [M] siempre
CuO2
2 -183.801 1.0 [M]
H+ 0.00 Concentración variable
H2 (gas) 0.00 1.0 atmósfera
O2 (gas) 0.00 1.0 atmósfera
H2O -237.337 1.0 [M] siempre
Para el caso del cobre en agua, se muestra a continuación las siguientes reacciones posibles, agregando además la reacción del agua, para así poder marcar la zona
de estabilidad del agua.
1) Cu 2 / Cu 0
2) Cu / Cu
0
2 2
3) Cu / Cu 4) CuO / Cu
5) Cu 2 / Cu 2 O 6) CuO / CuO 2
2
2 2 0
7) CuO 2 / Cu 2 O 8) CuO 2 / Cu
9) Cu 2O / Cu 0 10) CuO / Cu 2 O
11) 2 H 2e H 2 12) 4 H O2 4 e 2 H 2 O
1. Primero se deben plantear las reacciones posibles entre los elementos y compuesto en agua, equilibrando las reacciones por balance de masa y balance de
carga.
A continuación calcularemos a partir de los valores de G de los elementos o compuestos, el valor de G Re accion para cada reacción, y a partir de este
0
2.
0
0
valor, se calcula E Re accion para cada reacción propuesta.
Cuando se tiene una reacción del tipo aA bB ne cC dD , (los electrones siempre se ponen en el lado izquierdo de la reacción), el cálculo
de G Re accion y E Re accion se obtiene de la siguiente forma:
0 0
G Re accion (c • G C d • G D ) (a • G A b • G B )
0 0 0 0 0
0
y a través de la siguiente relación, se calcula el valor de E Re accion , cuando en la reacción hay involucrados n electrones :
3. Aplicando este razonamiento para las 12 reacciones propuesta, se obtiene las energías libres de cada una de las reacciones:
4. Conocidas las energías libres de las reacciones se determina los E° de cada una de las reacciones.
Ing. D. Carcausto Z. 6 Ing. V. Bustinza
R.
Escuela Profesional de Ingeniería Metalúrgica.- UNSA
Corrosión y Protección de Metales.- Practica calificada – 2017
A continuación se presenta una tabla resumen con los valores obtenidos de pE y Ln K , según corresponda.
0
Reacción E
0
Ln K
1)
2)
3)
4)
5)
6)
7)
8)
9)
10)
11) 2 H 2e H 2
12) 4 H O2 4 e 2 H 2 O
5. Conocidos los E0 para cada reacción, se procede a desarrollar la función que relaciona al Eh con el pH, para los casos en que la reacción involucra al ion Hidrogeno
y electrones :
Se pueden diferenciar dos casos, uno cuando el ion hidrogeno está en el producto, y otro cuando el ion hidrogeno esta en los reactantes.
Cuando el ion H+ está en el producto, la reacción tipo que se desarrolla es la siguiente :
Re actantes ne Pr oducto hH
Cuando el ion H+ está en los reactantes, la reacción tipo que se desarrolla es la siguiente :
Re actantes hH Pr oducto
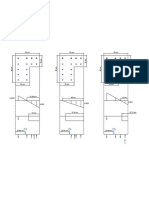
A continuación se muestra como queda el diagrama:
Ing. D. Carcausto Z. 7 Ing. V. Bustinza
R.
Escuela Profesional de Ingeniería Metalúrgica.- UNSA
Corrosión y Protección de Metales.- Practica calificada – 2017
Corrosión del cobre.-
Dadas sus propiedades, el cobre se aproxima a los metales nobles, especialmente por su excelente
resistencia a los agentes corrosivos naturales.
El cobre y la mayoría de sus aleaciones se caracterizan por su resistencia mecánica moderada,
unida a una elevada ductilidad, y esta circunstancia hace que sean especialmente adecuados para
tratamientos mecánicos en frío destinados a la fabricación de chapas, bandas y alambres.
Desde el descubrimiento de la electricidad y el consecuente desarrollo industrial de este sector, el
cobre adquiere su principal uso hasta nuestros días que es el conductor.
Asimismo se emplea en grifería (fontanería), arquitectura, en la industria en general y en transporte.
Dada su buena resistencia a la corrosión es empleado en obras artísticas (esculturas, monumentos,
etc.), con construcciones ornamentales y en los tejados de edificios, principalmente en el norte de
Europa.
La tuberías de cobre son utilizados en muchas instalaciones de sistemas de agua potable. Del total
de consumo de cobre en Europa y en USA en 1989, el tubo de cobre representó el 11% y 14%,
respectivamente. Esto supone aproximadamente 250.000 toneladas/año de tubos de cobre en cada
una de las regiones. Este alto grado de utilización se atribuye a numerosos factores, entre los que
destacan su durabilidad y resistencia a la corrosión.
Comercialmente puede obtenerse cobre de elevada pureza y en esta condición es el mejor
conductor de calor y electricidad conocido, a excepción de la plata. La presencia de impurezas, si
bien afecta especialmente a su conductividad y ductibilidad, hay que anotar, por otra parte, que
para otras aplicaciones no es preciso tan alto grado de pureza.
Para ello, suelen añadirse intencionadamente ciertos elementos, como el oxígeno, plata, selenio y
teluro, en pequeñas proporciones, que confieren propiedades particularmente adecuadas para
ciertas aplicaciones.
El cobre forma un gran número de aleaciones, entre las que destacan principalmente los latones
(Cu-Zn), los bronces (Cu-Sn), los cuproaluminios (Cu-Al), los cuproplomos (Cu-Pb), los
cuproníqueles (Cu-Ni), los cuproberilios (Cu-Be), cuprosilicios (Cu-Si), cupromanganesos (Cu-Mn)
y cuproantimonios (Cu-Sb).
Al igual que el resto del los metales, el cobre puede sufrir diferentes tipos de ataque corrosivo,
dependiendo del medio, del tipo de uso, etc. Estudio llevados a cabo por The American Society for
Testing and Materials (ASTM), donde se ha evaluado la velocidad de corrosión de probetas de
cobre expuestas a la atmósfera por más de 20 años, han demostrado que el cobre es un metal que
resiste muy bien el ataque corrosivo propio de atmósferas típicas de ambientes rurales, urbanas,
marinas, industriales y las diferentes combinaciones que establezcamos entre ellas. Se ha
determinado que en ambientes donde podamos tener NH3, el cobre sufre un ataque corrosivo
considerable. Teniendo en cuenta que este compuesto sólo puede estar en la atmósfera en zonas
industriales donde forme parte de la actividad de producción, el cobre permanecerá muy estable en
el resto de los medios.
Los materiales a base de cobre son muy estables en la atmósfera, debido, además de su carácter
semidoble, a la formación con el tiempo de delgadas capas protectoras (pátinas) sobre la superficie
metálica.
El color bruto rojo salmón cambia rápidamente a tonos marrones rojizos, los cuales se oscurecen
progresivamente para llegar a un color marrón oscuro después de algunos meses o años. Donde
primero se manifiesta es en las superficies inclinadas y horizontales, y tarda más en detectarse en
superficies verticales.
En atmósferas marinas o urbanas, la pátina puede comenzar a aparecer después de 5 ó 10 años
de exposición. En atmósferas rurales tarda bastante más (del orden de cien años), o puede llegar
a no aparecer si la atmósfera no está contaminada, y especialmente si la temperatura es baja. Los
climas áridos dificultan la patinación natural.
Ing. D. Carcausto Z. 8 Ing. V. Bustinza
R.
Escuela Profesional de Ingeniería Metalúrgica.- UNSA
Corrosión y Protección de Metales.- Practica calificada – 2017
El color marrón oscuro inicial se debe fundamentalmente al óxido de Cu (I). Los tonos verdosos
desarrollados después proceden de sales básicas de cobre, principalmente de sulfatos, cloruros,
nitratos y carbonatos, y en muy bajo porcentaje en compuestos de hierro y polvo de sílice.
La pátina formada en atmósferas urbanas o industriales contiene generalmente como sal básica
sulfato cúprico como principal componente. En atmósferas marinas predomina el cloruro cúprico.
Cuando la atmósfera es urbana y marina, la influencia urbana es mayor y el contenido predominante
es el de sulfatos. En ciertos ambientes rurales, es el sulfato cúprico el producto mayoritario, y en
otros es más frecuente la presencia de nitrato o carbonato cúprico [85-88, 89].
La composición de las distintas aleaciones de cobre afecta a la velocidad de corrosión de este
metal, pero estas diferencias afectan en menor medida que los factores medioambientales.
Velocidades típicas de corrosión del cobre y de la familia de materiales base cobre, una vez formada
la pátina protectora, pueden ser 1,5-2,5 μm/año en una atmósfera industrial y 0,7-1,5 μm/año en
una atmósfera marina (Acholes y Jacob, 1970).
Debido a la importancia de este metal se plantea la necesidad de estudiar el comportamiento de
dicho metal frente a la corrosión atmosférica para poder hacernos una idea del efecto que tendrán
los diversos factores medioambientales y los contaminantes sobre el mismo, y poder determinar la
magnitud del deterioro sufrido.
Hasta ahora he realizado una exposición de los factores decisivos para el estudio de la corrosión
atmosférica: factores medioambientales, humedad relativa, tiempo de exposición y los niveles de
los contaminantes (anhídrido sulfuroso e ion cloruro).
Para analizar la influencia de la humedad seria necesario disponer de datos referentes a atmósferas
puras en las que operara exclusivamente dicha variable.
La extrapolación a contaminación cero de la gráfica corrosión del cobre frente a contaminación por
SO2 en Madrid (Feliu y Morcillo, 1975) proporciona la cifra de 0,50 μm para las 2.120 h anuales
estimadas de humectación (0,24 μm por 1.000h).
Hay autores [90-93] que tienen en cuenta también la influencia de la temperatura en la corrosión
atmosférica. Así como la mayoría de los estudios encontrados son específicos para conducciones
de acero a altas temperaturas o instrumentación de acero sometida a alta temperatura, no existen
muchos datos sobre la utilización de esta variable en corrosión atmosférica. Esto puede ser debido,
entre otras causas, al efecto ambiguo que ejerce dicha variable.
De todos es sabido que al aumentar la Ta aumenta la velocidad de las reacciones electroquímicas
[94], pero al mismo tiempo se produce una evaporación de la capa de electrolito que recubre la
superficie, por lo que no pueden tener lugar procesos corrosivos. El resultado final de los
procesos corrosivos no sólo va a depender de la cinética de las reacciones electroquímicas, sino
que el tiempo que permanezca el metal mojado va a jugar un papel fundamental. Esta aparente
contradicción hace que esta variable sea muy ambigua.
En el caso específico de las islas, contamos con la ventaja de que no tenemos valores de T a
inferiores a O °C, y la Ta permanece casi invariable durante todo el año. No nos encontramos con
las bruscas variaciones de esta variable en un clima continental, donde podemos pasar de T as bajo
cero en invierno y cercanas a los 40 °C en verano.
No obstante, son pocas las ecuaciones empíricas encontradas en la bibliografía que incorporan
esta variable, reduciéndose a un número muy pequeño. Si recurrimos a la ecuación expuesta para
Ottawa, donde sí aparece esta variable, vemos que su influencia es muy poca, puesto que la
corrosión no se modifica aún realizando variaciones de diez o más grados [95].
El SO2 seco no ejerce ninguna influencia significativa en la corrosión del cobre, pero sí en presencia
de agua. La velocidad de corrosion del cobre aumenta al estar contaminada la atmósfera por
cantidades importantes de SO2. Lo mismo pasa con los latones y bronces.
Según Barton, es necesario alcanzar un nivel mínimo de SO 2 en la atmósfera para que este
contaminante influya significativamente en la velocidad de corrosión. Este nivel en el caso del cobre
parece situarse, igual que con el zinc, en los 0,62-0,68 mg·SO3/dm2 ·día. Una vez superado, la
velocidad de Corrosion aumenta considerablemente con el grado de contaminación.
Ing. D. Carcausto Z. 9 Ing. V. Bustinza
R.
Escuela Profesional de Ingeniería Metalúrgica.- UNSA
Corrosión y Protección de Metales.- Practica calificada – 2017
El mecanismo por el cual el SO2 ataca la superficie metálica no está del todo claro. Es probable
que se oxide a SO3 y reaccione con el agua para dar ácido sulfúrico. Es posible también que el
SO2 se disuelva en el agua con formación de ácido sulfuroso y sulfito metálico, que
posteriormente se oxida a sulfato.
No hay duda, por los datos que se poseen, que el ion cloruro es el contaminante que ejerce una
mayor influencia en la velocidad de corrosión del cobre, aunque se echan de menos estudios
sistemáticos sobre la acción concreta de este contaminante. Esto impide, en muchos casos, el
poder diferenciar en el aerosol marino, en qué porcentaje influye la presencia de cloruros y cual es
el correspondiente al aporte de humedad dado por ese aerosol.
Según Berukshtis y Clark (1966), el Cu y Al serían metales más sensibles a la presencia del ion
cloruro que el acero dulce. Estos autores encuentran que en una atmósfera marina la corrosion del
Cu se multiplica por 3,7 mientras que la del acero lo hace sólo por 1,2 respecto a la de una
atmósfera rural del interior.
Un trabajo de Sanyal y col. (1969), expone que niveles de contaminación del orden de 300-600
mgNaCl/m2·día provocan una importante exaltación de la corrosión del cobre puro. Los datos de
Ambler y Bain (1955), referidos a un latón con el 65% de Cu, desvelan que contenidos superiores
a unos 200 mg·NaCl/m2·día incrementan la velocidad media de corrosión una 4-10 veces respecto
a la de una atmósfera pura.
Según datos de la bibliografía existente referentes a la corrosión atmosférica del cobre en diferentes
lugares del mundo, se muestra que la velocidad de corrosión de este metal tiende a disminuir con
el tiempo, sobre todo en los primeros 5-10 años, debido seguramente a la patina protectora que se
forma con el paso de los años. Hasta el décimo año, poco más o menos, la velocidad de corrosión
se reduce hasta la mitad de su valor inicial, experimentando después ya muy pequeñas variaciones.
Ensayos realizados después de 20 años de exposición no revelan con claridad que la velocidad de
corrosión del cobre siga descendiendo de modo indefinido, lo que hace concluir a Uhlig (1963) que:
“dentro de errores experimentales de las determinaciones, la velocidad de corrosión para un período de 20
años es aproximadamente la misma que para uno de 10 años”.
Es de indudable interés disponer de datos referidos a períodos mayores de exposición. De los
estudios realizados para largos períodos, como los de Tracy (1951), examina la corrosión de las
planchas de cobre utilizadas en el tejado de una iglesia de Filadelfia después de 213 años de
exposición, o los de Leidheiser (1971), que estudia la degradación por corrosión de los tejados de
cobre de algunos edificios de Copenhague después de 200 años, o más, muestran unas
velocidades de corrosión que no difieren mucho de las obtenidas en estudios para 10-20 años de
exposición antes comentados.
Raramente se usa el cobre puro como material resistente a la corrosión en ambientes marinos. Sus aleaciones,
tales como las de cobre-níquel, bronces-aluminio y bronces-aluminio-níquel se usan de forma amplia en
aplicaciones marinas. De estudios previos efectuados con la finalidad de determinar el efecto que ejerce el ion
cloruro en la corrosión del cobre, se ha determinar que ejerce una fuerte influencia en el mecanismo corrosivo
del cobre.
Según Berukshtis y Klard (1966), el cobre y el aluminio serían metales más sensibles a la presencia del ion
cloruro que el acero dulce. Estos autores encuentran que, en una atmósfera marina, la corrosión del cobre se
multiplica por 3,7 veces y por 1,2 la del acero respecto a una atmósfera rural del interior.
Los primeros estudios electroquímicos llevados a cabo sobre el cobre fueron realizados por Bengough et al
[134, 135], los cuáles estudiaron la corrosión del cobre en agua de mar determinando que el principal producto
de corrosión formado es el cloruro de cobre, CuCl, formado por la reacción:
Ing. D. Carcausto Z. 10 Ing. V. Bustinza
R.
Escuela Profesional de Ingeniería Metalúrgica.- UNSA
Corrosión y Protección de Metales.- Practica calificada – 2017
Como mecanismo de reacción se propuso que este cloruro de cobre, que es bastante soluble en disoluciones
salinas neutras, reacciona para dar lugar al óxido de cobre (cuprita), el cuál es el principal constituyente de las
capas de productos de corrosión a mayor escala. La cuprita evoluciona a hidróxido de cobre, atacamita o
malaquita en presencia de agua de mar. Los mecanismos de reacción serían los siguientes:
A raíz de la ecuación anterior se observa que la estabilidad de la cuprita es inversamente dependiente de la
concentración de iones cloruro. Si analizamos el diagrama de Pourbaix para el cobre en agua de mar (figura
7.5), se observa que para condiciones normales y con disolución neutra, la forma más estable es la cuprita.
El efecto que ejercen los iones cloruro y sulfato en la corrosión del cobre ha sido poco estudiado desde el
punto de vista electroquímico en cuanto a su relación con la corrosión atmosférica.
En cuanto a la evolución del potencial de corrosión Ecorr en ensayo a circuito abierto se observa un
comportamiento muy estable del cobre, con un tiempo limite de estabilización del potencial de 1800 segundos.
De los resultados expuestos se puede observar que no existe una variación lineal del potencial de corrosión a
medida que aumentamos la concentración del agente agresivo, sea NaCl o Na2SO4. El mismo comportamiento
ha sido observado en las variables Rp e Icorr, donde el perfil obtenido no es uniforme. Si tenemos en cuenta
que todas las probetas han sido sometidas a un mismo periodo de inmersión inicial se descarta el hecho de que
estas oscilaciones puedan ser debidas a la formación de una capa de productos de corrosión más o menos
compacta.
Ing. D. Carcausto Z. 11 Ing. V. Bustinza
R.
Potrebbero piacerti anche
- 3er Exm RefinacionDocumento113 pagine3er Exm RefinacionKatherin Carhuas QuispeNessuna valutazione finora
- 2 Exm LixiviacionDocumento143 pagine2 Exm LixiviacionKatherin Carhuas QuispeNessuna valutazione finora
- AMALGAMACIONDocumento59 pagineAMALGAMACIONKatherin Carhuas QuispeNessuna valutazione finora
- GRAVIMETRIADocumento139 pagineGRAVIMETRIAKatherin Carhuas QuispeNessuna valutazione finora
- GTAWDocumento72 pagineGTAWKatherin Carhuas QuispeNessuna valutazione finora
- Mantenimiento PDFDocumento70 pagineMantenimiento PDFKatherin Carhuas QuispeNessuna valutazione finora
- GMAWDocumento47 pagineGMAWKatherin Carhuas QuispeNessuna valutazione finora
- ListadoPadron IEDocumento3 pagineListadoPadron IEKatherin Carhuas QuispeNessuna valutazione finora
- Shou GangDocumento16 pagineShou GangKatherin Carhuas QuispeNessuna valutazione finora
- FCAWDocumento17 pagineFCAWKatherin Carhuas QuispeNessuna valutazione finora
- Ficha de Aprendizaje 01 - PrimeroDocumento7 pagineFicha de Aprendizaje 01 - PrimeroKatherin Carhuas QuispeNessuna valutazione finora
- Ppt-Teoria 5° - EstudianteDocumento11 paginePpt-Teoria 5° - EstudianteKatherin Carhuas QuispeNessuna valutazione finora
- Doc3 Model 11111Documento1 paginaDoc3 Model 11111Katherin Carhuas QuispeNessuna valutazione finora
- FALLASDocumento1 paginaFALLASKatherin Carhuas QuispeNessuna valutazione finora
- Presentación Metalografia 1-2016Documento51 paginePresentación Metalografia 1-2016Vládimir Villalta BolomerNessuna valutazione finora
- DOP REAL de Una Planta de OllasDocumento1 paginaDOP REAL de Una Planta de OllasKatherin Carhuas QuispeNessuna valutazione finora
- Problemas de HidrometalurgiaDocumento12 pagineProblemas de HidrometalurgiaKatherin Carhuas QuispeNessuna valutazione finora
- Gestion de Relaves Mineros 120820170423 Phpapp02Documento57 pagineGestion de Relaves Mineros 120820170423 Phpapp02pierrepy0% (1)
- HidroDocumento3 pagineHidroKatherin Carhuas QuispeNessuna valutazione finora
- Diseno de Un Sistema de Propulsion Con Chorro de ADocumento182 pagineDiseno de Un Sistema de Propulsion Con Chorro de AMartín GuevaraNessuna valutazione finora
- Física 17.1Documento17 pagineFísica 17.1Gabriela Itzel Trejo Jiménez0% (1)
- Guia de Apendizaje 1Documento20 pagineGuia de Apendizaje 1cristian sanvovalNessuna valutazione finora
- Canal ParshallDocumento25 pagineCanal ParshalljuanNessuna valutazione finora
- Solicitud de Pertinencia AmbientalDocumento33 pagineSolicitud de Pertinencia AmbientalfgodoykNessuna valutazione finora
- AcrílicoDocumento7 pagineAcrílicoRodrigo MYNessuna valutazione finora
- “AMPLIACION Y MEJORAMIENTO DEL SISTEMA DE AGUA POTABLE, CREACION DEL SERVICIO DE ALCANTARILLADO, LETRINIFICACION E INSTALACION DE LA PLANTA DE TRATAMIENTO DE AGUAS RESIDUALES DE LAS COMUNIDADES DE UCHUY CRUZ, JAUCAYPATA, ACOS Y HUANCHOS, DISTRITO DE PAUCARBAMBA, PROVINCIA DE CHURCAMPA - HUANCAVELICA”Documento312 pagine“AMPLIACION Y MEJORAMIENTO DEL SISTEMA DE AGUA POTABLE, CREACION DEL SERVICIO DE ALCANTARILLADO, LETRINIFICACION E INSTALACION DE LA PLANTA DE TRATAMIENTO DE AGUAS RESIDUALES DE LAS COMUNIDADES DE UCHUY CRUZ, JAUCAYPATA, ACOS Y HUANCHOS, DISTRITO DE PAUCARBAMBA, PROVINCIA DE CHURCAMPA - HUANCAVELICA”PaúlAngelBellidoEspinozaNessuna valutazione finora
- TLL 02 Grupo02Documento35 pagineTLL 02 Grupo02Israel PanimbozaNessuna valutazione finora
- Hidro-Investigaciones 1Documento8 pagineHidro-Investigaciones 1Stephanie PolicarpioNessuna valutazione finora
- Informe de AlgintosDocumento7 pagineInforme de AlgintosDoris AbadNessuna valutazione finora
- Control de Líquidos Administrados y EliminadosDocumento14 pagineControl de Líquidos Administrados y EliminadosFeliphe De La Pernía VillarealNessuna valutazione finora
- Estudio de Impacto Ambiental Peña ColoradaDocumento108 pagineEstudio de Impacto Ambiental Peña ColoradaClorinda Astete ChuquichaicoNessuna valutazione finora
- Congreso Mexicano Del PetróleoDocumento21 pagineCongreso Mexicano Del PetróleoFrancisco de la CruzNessuna valutazione finora
- Adhesivos y Fragues para CerámicosDocumento6 pagineAdhesivos y Fragues para CerámicosJaime Jiménez LópezNessuna valutazione finora
- SISS (2021) - MaFi - Facturación SSRDocumento19 pagineSISS (2021) - MaFi - Facturación SSRvacomanoNessuna valutazione finora
- Experimento de Calorimetria Química PDFDocumento6 pagineExperimento de Calorimetria Química PDFtiana.vadell1858Nessuna valutazione finora
- Materiales de Reparación de Hormigón, Mortero Y CementoDocumento8 pagineMateriales de Reparación de Hormigón, Mortero Y CementoJulio OlayaNessuna valutazione finora
- 5 Impacto de Un ChorroDocumento8 pagine5 Impacto de Un ChorroLinda Milagros RamirezNessuna valutazione finora
- Tanques de Almacenamiento de HCBDocumento8 pagineTanques de Almacenamiento de HCBJean Pierre Jurado RNessuna valutazione finora
- Diaz S Duiii ExpoDocumento21 pagineDiaz S Duiii Expomainares67Nessuna valutazione finora
- Proyecto Abastos UniquindioDocumento52 pagineProyecto Abastos UniquindioLUIS FELIPE RESTREPO ROMERONessuna valutazione finora
- Estudio Integral Geográfico de La Cuenca Del Río OmasDocumento11 pagineEstudio Integral Geográfico de La Cuenca Del Río OmasSupoQuisocalaDuxNessuna valutazione finora
- Tesis Culto en Cerro XicoDocumento224 pagineTesis Culto en Cerro XicoDavBodri100% (2)
- Manual SubsoladorDocumento21 pagineManual SubsoladorDianaKatherineNessuna valutazione finora
- Informe de PeltonDocumento25 pagineInforme de PeltonJesus EslavaNessuna valutazione finora
- Alimentación para La Revolución - La Decadencia y Fin de La Proteína Animal - Salud Ambiente Ética - Juan Esteche Abr 2023Documento34 pagineAlimentación para La Revolución - La Decadencia y Fin de La Proteína Animal - Salud Ambiente Ética - Juan Esteche Abr 2023Daniela Esther DellasoppaNessuna valutazione finora
- Trabajo de Rodrigo 2020Documento155 pagineTrabajo de Rodrigo 2020Pelagio PerezNessuna valutazione finora
- C127 - Gs Agregado GruesoDocumento10 pagineC127 - Gs Agregado GruesoClash ClansNessuna valutazione finora
- Tarea 8. Trabajo IntegradorDocumento11 pagineTarea 8. Trabajo IntegradorReyna RuvalcabaNessuna valutazione finora