Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
GASESfiki
Caricato da
Royni Ramirez CcantoCopyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
GASESfiki
Caricato da
Royni Ramirez CcantoCopyright:
Formati disponibili
2013
GASES
JESUS ALBERTO ORTIZ QUISPE
E.A.P INGENIERIA METALURGICA
LABORATORIO DE FISICOQUIMICA
GASES
INDICE:
RESUMEN
INTRODUCCION
OBJETIVOS
FUNDAMENTO TEORICO
DATOS, CALCULOS Y RESULTADOS.
DISCUSION DE RESULTADOS
CONCLUSIONES
RECOMENDACIONES
BIBLIOGRAFIA
APENDICE
Informe del Laboratorio de Fisicoquímica E.A.P Ingeniería Metalúrgica
GASES
RESUMEN
En esta experiencia realizada en el laboratorio se verifico la ley de Boyle-Mariotte,
mediante mediciones de volúmenes y presiones, siempre a una temperatura
constante. Y tmb calcular la relación de capacidades calorificas.
Tambien se observo el comportamiento de algunos gases mediante en:
a) Compresión isotermica del aire: Este experimento nos permite
comprobar la ley de Boyle.
Esta experiencia hace uso de Mercurio (Hg) por su alta densidad atrapando el
aire en el tubo originando un volumen inicial, luego se adiciona mas
Mercurio(Hg) con el fin de tener una compresion en el volumen de aire,
Esta experiencia se trabajo con 5 datos de volumenes con presiones
diferentes, lo cual nos permite calcular una presión de 774.2 mm-Hg (Valor
experimental) en el que analizando con el resultado teorico tuvimos un error
de 0.014%(un error casi al minimo) en relación al valor teorico 770.312mm-
Hg.
Estos datos obtenidos deben aproximarse a los datos teoricos, para asi graficar
la curva experimental y comparar con la curva teorica, con un error minimo
posible.
b) Expansión adiabatica: Este experimento nos permite calcular la relación
de Cp/Cv.
El experimento se trabajo con 5 datos de presiones cada una con una
diferencia de altura diferente que permite calcular las relaciones de
capacidades calorificas Cp/Cv = 1,352(valor experimental), analizando el
resultado con el valor teorico tuvimos un error de 0,00%, en relación al valor
teorico de 1.40 (valor teorico).
Por ultimo en esta experiencia se cumplio con el objetivo de comprobar las
leyes de los gases, en este caso la ley de Boyle y las relaciones de
capacidades calorificas Cp/Cv, comprobando de forma aceptable, según los
resultados obtenidos.
Informe del Laboratorio de Fisicoquímica E.A.P Ingeniería Metalúrgica
GASES
INTRODUCCION
En esta experiencia en el laboratorio tiene por objetivo buscar la demostración
analiticamente de la compresión isotérmica del aire y la expansión adiabática,
mediante la utilización de diversos equipos, materiales y sustancias químicas
(mercurio), por medio del cual comprobaremos la ley de Boyle (compresión
isotérmica) y la relación de capacidades caloríficas (expansión adiabática),
utilizando el aire como compuesto gaseoso.
OBJETIVOS
Comprobar la ley de Boyle - Mariotte, midiendo volumenes de aire para
diferentes presiones.
Determinar la relación de capacidades calorificas que existe entre Cp y
Cv.
La función que tiene el Mercurio de atrapar el aire por su alta densidad
en un espacio cerrado, y asi medir la diferencia de alturas del Mercurio
en un tubo en U por su presión que produce.
Comprender el comportamiento de los gases.
Informe del Laboratorio de Fisicoquímica E.A.P Ingeniería Metalúrgica
GASES
FUNDAMENTO TEORICO
GAS:
Se denomina gas al estado de agregación de la materia
que no tiene forma ni volumen propio. Su principal
composición son moléculas no unidas, expandidas y con
poca fuerza de atracción, haciendo que no tengan volumen
y forma definida, provocando que este se expanda para
ocupar todo el volumen del recipiente que la contiene, con
respecto a los gases, las fuerzas gravitatorias y de
atracción entre partículas, resultan insignificantes.
ECUACION DE ESTADO:
Es la relación matematica entre las propiedades que fijan el estado
termodinamico de un sistema: masa (m), volumen (V), presion (P) y
temperatura (T).
LEY DE BOYLE:
La ley de Boyle establece que a temperatura constante, la presión de una
cantidad fija de gas es inversamente proporcional al volumen que ocupa.
Consideremos el siguiente proceso que se lleva a cabo a temperatura
constante (isotérmico):
Un cilindro contiene un gas que ocupa un volumen V1, se encuentra a
una presión P1 (representada por la pesa sobre el émbolo) y una
temperatura T1.
Al agregar dos pesas, la presión sobre el gas aumentará a P2 y éste se
comprimirá hasta un volumen V2, a una T2.
Como el proceso es isotérmico, T1 = T2
Este proceso se puede representar en un diagrama P - V, mediante una
curva que se denomina isoterma.
Si ahora retiramos dos pesas, el gas se expandirá hasta el estado inicial,
completando un ciclo.
Lo que Boyle descubrió es que si la cantidad de gas y la temperatura
permanecen constantes, el producto de la presión por el volumen es
constante.
Por lo que la expresión matemática de esta ley es:
Si la presión se expresa en atmósferas (atm) y el volumen en litros (l), la
constante k estará dada en (l·atm), que son unidades de energía y entonces, la
constante de Boyle representa el trabajo realizado por el gas al
expandirse o comprimirse.
Informe del Laboratorio de Fisicoquímica E.A.P Ingeniería Metalúrgica
GASES
LEY DE AVOGADRO:
Es aquella en el que las constantes son presión y temperatura, siendo el
Volumen directamente proporcional al Número de moles (n).
Matemáticamente, la fórmula es:
V1/n1=V2/n2
LEY DE CHARLES:
A una presión dada, el volumen ocupado
por un gas es directamente proporcional a
su temperatura.
Matemáticamente la expresión:
V1/T1 = V2/T2; P=cte
LEY DE GAY-LUSSAC:
La presión del gas, que se mantiene a
volumen constante, es directamente
proporcional a la temperatura:
P1/T1 = P2/T2; V=cte
Es por esto que para poder envasar gas,
como gas licuado, primero se ha de enfriar
el volumen de gas deseado, hasta una
temperatura característica de cada gas, a fin
de poder someterlo a la presión requerida
para licuarlo sin que se sobrecaliente, y,
eventualmente, explote.
Informe del Laboratorio de Fisicoquímica E.A.P Ingeniería Metalúrgica
GASES
LEY DE LOS GASES IDEALES:
Las tres leyes mencionadas pueden combinarse matemáticamente en la
llamada ley general de los gases. Su expresión matemática es:
Siendo P la presión, V el volumen, n el número de moles, R la constante
universal de los gases ideales y T la temperatura en Kelvin.
El valor de R = 0,082 atm·l·K−1·mol−1 si se trabaja con atmósferas y litros
De esta ley se deduce que un mol de gas ideal ocupa siempre un volumen
igual a 22,4 litros a 0 °C y 1 atmósfera. También se le llama la ecuación de
estado de los gases; ya que solo depende del estado actual en que se
encuentre el gas.
GASES FINALES:
Si se quiere afinar más o si se quiere medir el comportamiento de algún gas
que escapa al comportamiento ideal, habrá que recurrir a las ecuaciones de los
gases reales que son variadas y más complicadas cuanto más precisas.
Los gases reales no se expanden infinitamente, sino que llegaría un momento
en el que no ocuparían más volumen. Esto se debe a que entre sus
átomos/moléculas se establecen unas fuerzas bastante pequeñas, debido a los
cambios aleatorios de sus cargas electrostáticas, a las que se llama fuerzas de
Van der Waals.
Dentro de los gases orgánicos, el que tendrá un comportamiento más ideal
será el metano perdiendo idealidad a medida que se engrosa la cadena de
carbono. Así, el butano es de esperar que tenga un comportamiento ya
bastante alejado de la idealidad. Esto es porque cuanto más grande es la
partícula fundamental constituyente del gas, mayor es la probabilidad de
colisión e interacción entre ellas, factor que hace disminuir la idealidad. Algunos
de estos gases se pueden aproximar bastante bien mediante las ecuaciones
ideales, mientras que en otros casos hará falta recurrir a ecuaciones reales
muchas veces deducidas empíricamente a partir del ajuste de parámetros.
También se pierde la idealidad en condiciones extremas, altas presiones o
bajas temperaturas. Por otra parte, la concordancia con la idealidad puede
aumentar si trabajamos a bajas presiones o altas temperaturas. También por
su estabilidad química.
Informe del Laboratorio de Fisicoquímica E.A.P Ingeniería Metalúrgica
GASES
Comportamiento de los gases
Para el comportamiento térmico de partículas de la materia existen cuatro
cantidades medibles que son de gran interés: presión, volumen, temperatura y
masa de la muestra del material.
Cualquier gas se considera como un fluido, porque tiene las propiedades que le
permiten comportarse como tal.
Sus moléculas, en continuo movimiento, logran colisionar las paredes que los
contiene y casi todo el tiempo ejercen una presión permanente. Como el gas se
expande, la energía intermolecular (entre molécula y molécula) hace que un
gas, al ir añadiéndole energía calorífica, tienda a aumentar su volumen.
Un gas tiende a ser activo químicamente debido a que su superficie molecular
es también grande, es decir, entre cada partícula se realiza mayor contacto,
haciendo más fácil una o varias reacciones entre las sustancias.
Para entender mejor el comportamiento de un gas, siempre se realizan
estudios con respecto al gas ideal, aunque este en realidad nunca existe y las
propiedades de este son:
Un gas está constituido por moléculas de igual tamaño y masa, pero una
mezcla de gases diferentes.
Se le supone con un número pequeño de moléculas; así su densidad es baja y
su atracción molecular es nula.
El volumen que ocupa el gas es mínimo, en comparación con el volumen total
del recipiente.
Las moléculas de un gas contenidas en un recipiente, se encuentran en
constante movimiento, por lo que chocan, ya entre sí o contra las paredes del
recipiente que las contiene.
Para explicar el comportamiento de los gases, las nuevas teorías utilizan tanto
la estadística como la teoría cuántica, además de experimentar con gases de
diferentes propiedades o propiedades límite, como el UF6, que es el gas más
pesado conocido.
Un gas no tiene forma ni volumen fijo; se caracteriza por la casi nula cohesión y
la gran energía cinética de sus moléculas, las cuales se mueven.
CAPACIDAD CALORÍFICA
Hay dos tipos de capacidad calorífica, esto es según se calienta la sustancia a
presión constante o a volumen constante. Este ultimo da energía
proporcionada va incrementar la interna de la sustancia y a esa capacidad la
designamos por Cv.Por otra parte, al calentar una sustancia a presión
constante, la energía suministrada no solo incrementa la interna si no que hace
posible la expanción de la sustancia venciendo la acción que ejerce que ejerce
la presión atmosférica, por esta razón la designamos como Cp.
Informe del Laboratorio de Fisicoquímica E.A.P Ingeniería Metalúrgica
GASES
EXPANSIÓN ADIABÁTICA:
Es un proceso termodinámico en el cual un gas se hace pasar de una presión
mayor a otra inferior sin que tome o ceda calor al medio, realizando un trabajo
sobre su entorno y bajando su temperatura, la cual no debe confundirse con el
intercambio de calor que, por definición de proceso adiabático, es nulo.
Donde:
E Q W
E : Cambio de energía de sustancia, E = nCv (dT)
Q: calor
W: trabajo realizado por el sistema,
-W = P v
En el proceso adiabático E = W luego:
nCv t = -P v
nCv t = -nRT v /v Integrando
Cv ln T2/T1= -RLn V2/V1
Se observa que el cambio de energía se relaciona con el cambio de volumen
del sistema.
Informe del Laboratorio de Fisicoquímica E.A.P Ingeniería Metalúrgica
GASES
DATOS, CALCULOS Y RESULTADOS
PARTE EXPERIMENTAL:
EXPERIMENTO 1: COMPRENSION ISOTERMICA DEL AIRE:
Datos
Diámetro del tubo. 0,6cm.
Radio del tubo(R). 0,3cm.
Altura inicial (H). 44,8cm.
Temperatura Ambiente. 23 ºC.
Presión Atmosférica (Patm). 756 mm-Hg.
% de humedad relativa(Hr). 80%
.
VAIRE = xR2xH
Vol aire: x (0.3)2 x (44.8): 12.667cm3(Volumen inicial).
DETERMINACIÓN DE LAS ALTURAS DE NIVELES DE MERCURIO:
Pruebas ∆ Hi (Alturas de Hi (Alturas
niveles de para el aire)
mercurio)
1 0,70 44,10
2 1,30 43,50
3 1,80 43,00
4 2,40 42,40
5 2,90 41,90
Informe del Laboratorio de Fisicoquímica E.A.P Ingeniería Metalúrgica
GASES
Volumen de aire para las graduaciones del tubo de las nuevas alturas para el
mercurio:
Niveles de Hg (cm) Volúmenes de Aire (cm3)
∆H1 = 0,70 V1 = 44,10cm x x (0,3 cm)2 = 12,469
∆H2 = 1,30 V2 = 43,50cm x x (0,3 cm)2 = 12,299
∆H3 = 1,80 V3 = 43,00cm x x (0,3 cm)2 = 12,158
∆H4 = 2,40 V4 = 42,40cm x x (0,3 cm)2 = 11,988
∆H5 = 2,90 V5 = 41,90cm x x (0,3 cm)2 = 11,847
DETERMINANDO LA PRESION TOTAL:
Donde la presión total es:
PT = PAt + PH
PT : Presión Total.
PAt : Presión Atmosférica = 756 mm-Hg
PH : Presión debido las alturas.
PT = PAt + PH (mm-Hg)
PT1 = PAT + PH1 = 756 mm-Hg + (0.7 cm) (10 mmHg / cm) 763 mmHg
PT2 = PAT + PH2 = 756 mm-Hg + (1.3 cm) (10 mmHg / cm) 769 mmHg
PT3 = PAT + PH3 = 756 mm-Hg + (1.8 cm) (10 mmHg / cm) 774 mmHg
PT4 = PAT + PH4 = 756 mm-Hg + (2.4 cm) (10 mmHg / cm) 780 mmHg
PT5 = PAT + PH5 = 756 mm-Hg + (2.9 cm) (10 mmHg / cm) 785 mmHg
Promedio de Presión Total ( Pexperimental) 774.2 mmHg
Pexperimental = (PT1 + PT2 + PT3 + PT4 + PT5)/5 = 774.2 mmHg
Informe del Laboratorio de Fisicoquímica E.A.P Ingeniería Metalúrgica
GASES
DETERMINANDO LA CONSTANTE K, PV = K:
PT (mm-Hg) Volumen (cm3) K (mm-Hg x cm3)
763 12,469 K1 = 9513,847
769 12,299 K2 = 9457,931
774 12,158 K3 = 9410,292
780 11,988 K3 =9350,640
785 11,847 K3 =9299,895
K Promedio( Kprom) 9406,521 mm-Hg x cm3
Donde el Kprom es: (K1+K2+K3+K4+K5)/5 = 9406,521mm-Hg x cm3
VOLUMEN VS PRESION TOTALES
790
785
PT(mm-Hg)
780
775
770
765
760
11.8 11.9 12 12.1 12.2 12.3 12.4 12.5 12.6
VOLUMEN(cm3)
DETERMINANDO LAS PRESIONES TEORICAS CON EL “K”
PROMEDIO:
P = K/Vi (mm-Hg x cm3 / cm3) Presiones teóricas (mm-Hg)
PT1 = 9406,521/ 12,469 754,393
PT2 = 9406,521/ 12,299 764,819
PT3 = 9406,521/ 12,158 773,689
PT4 = 9406,521/ 11,988 784,661
PT5 = 9406,521/ 11,847 794,000
Presión Teórica promedio(Pteorico) 774,312
Pteorico = (PT1 + PT2 + PT3 + PT4 + PT5)/5 = 774,312 mm-Hg
Informe del Laboratorio de Fisicoquímica E.A.P Ingeniería Metalúrgica
GASES
GRAFICO DE PRESION TEORICA VS VOLUMEN:
P teorico VS VOLUMEN
800
P teorico(mm-Hg)
790
780
770
760
750
11.8 11.9 12 12.1 12.2 12.3 12.4 12.5 12.6
VOLUMEN (cm3)
GRAFICO P*V VS P Teoricas:
9550
9500
K(mm-Hg x cm3)
9450
9400
9350
9300
9250
750 760 770 780 790 800
Presion Teorica(mm-Hg)
Informe del Laboratorio de Fisicoquímica E.A.P Ingeniería Metalúrgica
GASES
EXPERIMENTO 2: EXPANSION ADIABATICA
Este experimento permite calcular la relación de capacidades caloríficas Cp/Cv:
De la ecuación para un proceso adiabático se deduce:
Cv Ln P2/P3 = -RLn P1/P3
Donde:
P1 = Presión inicial del sistema.
P2 = Presión inmediatamente después de la expansión.
P3 = Presión luego que el gas alcance nuevamente la temperatura inicial.
Se demuestra que:
CP/Cv = (P1 – P2)/ (P1-P3)
Según las presiones manométricas: P1 – P2 = h1.
Luego de la expansión: P 3 – P2 = h2
Entonces:
CP/Cv = h1 / (h1 – h2)
Datos:
Patm = 756 mm-Hg
∆𝐡𝟏 (cm) ∆𝐡𝟐 (cm)
𝟓. 𝟔 1.6
𝟒. 𝟑 1
𝟔. 𝟗 2
𝟔. 𝟒 0.9
𝟕. 𝟔 2.5
Informe del Laboratorio de Fisicoquímica E.A.P Ingeniería Metalúrgica
GASES
Siendo:
CP P1− P2
=
CV P1 − P3
P1 = presión inicial del sistema.
P2 = presión inmediatamente después de la expansión.
P3 = presión luego que el gas alcance nuevamente la temperatura inicial.
P1 − P3 = h2
CP h1
=
CV h1 − h2
DE ACUERDO CON LAS PRESIONES MANOMETRICAS: P1− P2 = h1
𝐡𝟏 (cm) 𝐡𝟐 (cm) 𝐡𝟏 − 𝐡𝟐 (cm) 𝐂𝐏 𝐡𝟏
=
𝐂𝐕 𝐡𝟏 − 𝐡𝟐
𝟓. 𝟔 1.6 4 1.40
𝟒. 𝟑 1 3.3 1.30
𝟔. 𝟗 2 4.9 1.41
𝟔. 𝟒 0.9 5.5 1.16
𝟕. 𝟔 2.5 5.1 1.49
C
ENTONCES CP (PROMEDIO):
V
CP (1,4 +1,3+ 1,4+ 1,49)
(prom) = = 1,4
CV 4
Obs: se elimina el dato Cp/Cv= 1,16 por variar mucho
en comparación de los demas datos obtenidos para
determinar un error minimo posible.
Informe del Laboratorio de Fisicoquímica E.A.P Ingeniería Metalúrgica
GASES
DETERMINANDO LOS % DE ERROR DEL EXPERIMENTO
a) Comprensión isotérmica del aire:
%E = Valor promedio – Valor práctico x 100
Valor promedio
%E = 774,312 mm-Hg – 774.2mm-Hg x 100 = 0.0014%
770.312mm-Hg
b) En la expansión Adiabática:
%E = Valor Teórico – Valor práctico x 100
Valor Teórico
%E = 1.40– 1.40 x 100 = 0,00%
1.40
Informe del Laboratorio de Fisicoquímica E.A.P Ingeniería Metalúrgica
GASES
DISCUSION DE RESULTADOS:
Para la primera parte en el que se trato el tema de Compresión
isotermica del aire se obtuvo una presión de 774, 2mm.-Hg (Presión
experimental) comprando con la presion de 774,312 mm-Hg(Presión
Teorica) llevando a un error de 0.014%, un error minimo en que se
trabajo tendiendo hacer los mas preciso posible al determinar los datos,
pero siempre tenemos los factores humanos que no nos permite hacer lo
mas exacto posible.
Para la segunda parte en el que se trato el tema de expansión
𝐂𝐏
adiabática se obtuvo un (𝐞𝐱𝐩𝐞𝐫𝐢𝐦𝐞𝐧𝐭𝐚𝐥) de 1,352 comparando con
𝐂𝐕
𝐂𝐏
la (𝒕𝒆𝒐𝒓𝒊𝒄𝒂) de 1,4 llevando a un error de 0,00%, se llego a este
𝐂𝐕
porcentaje por que se elimino unos de los Cp/Cv (experimental) ya q
variaba mucho en comparación con los demas datos obtenidos el cual
era el 1,16.
Informe del Laboratorio de Fisicoquímica E.A.P Ingeniería Metalúrgica
GASES
CONCLUSIONES:
Las leyes que rigen los gases se pudo demostrar en laboratorio
(teniendo un margen minimo de error) y teniendo en cuenta los
materiales necesarios para poder experimentar.
a) Compresion isotermica:
Se puede deducir de los graficos obtenidos que, efectivamente que a
temperatura constante la presión de un gas es inversamente
proporcional a su volumen de acuerdo con la ley de Boyle.
Los resultados experimentales en el laboratorio no suelen ser iguales a
los teorico debido a que siempre hay un margen de error debibo a la
exactitud y presición del que realiza el experimento y de los materiales.
b) Expansión adiabatica:
Si hay un dato que varia demasiado con repesto alos demas datos
determinados, este dato que varia demasiado se elimina, para evitar un
% de error avultado.
Los gases se expanden libremente hasta llenar el recipiente que los
contiene, debido a la colisición de atomos o moleculas direccionandose
aleatoriamente.
Informe del Laboratorio de Fisicoquímica E.A.P Ingeniería Metalúrgica
GASES
RECOMENDACIONES:
Se debe tener cuidado al trabajar en el laboratorio para poder eliminar
posibles errores en los resultados obtenidos.
Portar preferiblemente equipos de proteccion personal (EEP) para prevenir
cualquier accidente.
Trabajar con la guía y su previa lectura antes de empezar el laboratorio.
Cada vez que se termine de usar un determinado instrumento se debe lavar
y dejar en el lugar indicado.
Se debe tener en cuenta siempre las condiciones de operación en el
laboratorio.
a) Compresión isotermica:
Al momento de adicionar el Hg al tubo en U por primera vez, este debe
calibrarse, hasta que tengan las mismas alturas (en el brazo cerrado y en el
abierto).
Al momento de adicionar el Hg este debe adicionarse con sumo cuidado ya
que si esta en contacto con este,puede causar irritacion a la piel o
enrojecimiento
Al momento de anotar los datos obtenidos en el experimento, preferible ser
lo mas preciso posible para evitar el un porcentaje de error avultado, pero
siempre se tienen los factores q no nos permiten hacer los mas exacto
posible
a) Expansión adiabatica:
Para este expermiento se requiere de mucha concentración y
rapides al momento de anotar las diferencia de las alturas
.
Producir una expansión rapida destapado y tapando el capilar
conectado al tapon.
Informe del Laboratorio de Fisicoquímica E.A.P Ingeniería Metalúrgica
GASES
BIBLIOGRAFÍA:
LIBROS
BABOR-ÍBARZ - Química General - 8º Edición – Marión – Barcelona – 1979
Raymond chang – química general – 7 edición.
Guía de laboratorio de Fisicoquímica
GASTON PONS MUZZO (1987) “Físico Química”: Editorial Bruño.
PAGINAS WEB:
http://es.wikipedia.org/wiki/Ley_de_Boyle-Mariotte
http://www.alegsa.com.ar/Definicion/de/expansion_adiabatica.php
http://es.wikipedia.org/wiki/Difusi%C3%B3n_gaseosa
http://procesoisotermico.blogspot.com/2009/04/termodinamica.html
http://hyperphysics.phy-astr.gsu.edu/hbasees/kinetic/shegas.html
Informe del Laboratorio de Fisicoquímica E.A.P Ingeniería Metalúrgica
GASES
APENDICE:
Capacidad Calorifíca de los gases
Para los gases ideales, si se determina la capacidad calorífica molar para un
mismo gas a:
volumen constante se denomina,CV
presión constante se denomina, CP
La relación existente entre ellas está determinada por la expresión siguiente:
Donde:
R es la constante de los gases ideales expresada en unidades de energía: .
R = 0,082atm.L/mol.K
La capacidad calorífica de los gases ideales varía, si se trata de gases
monoatómicos, diatómicos y triatómicos.
En la tabla siguiente se muestran los valores de capacidad calorífica a
volumen constante ( CV ) y a presión constante ( CP ) para gases ideales
monoatómicos, diatómicos y triatómicos.
Gas Ejm Cv Cp
Monoatomico He, Ne, Ar, etc 3R/2 5R/2
Diatomico H2, Aire, etc 5R/2 7R/2
Triatomico NO2, SO2, etc 7R/2 9R/2
Informe del Laboratorio de Fisicoquímica E.A.P Ingeniería Metalúrgica
GASES
Demostración Teorica de la relación Cp/Cv del aire:
Sabiendo:
Donde: Cp = 7R/2 ( Como el aire es un gas diatomico)
Cp – R = Cv
7R/2 – R = Cv
Cv = 5R/2
Por lo tanto:
Cp/Cv = (7R/2) / (5R/2) = 1,4 ( Valor Teorico)
Informe del Laboratorio de Fisicoquímica E.A.P Ingeniería Metalúrgica
GASES
GASES EN LA METALURGIA:
Los gases tienen amplios usos en la industria metalúrgica y metalmecánica; se
emplean para acelerar o frenar procesos, calentar, enfriar, alterar y preservar
productos.
Los gases son elementos sin forma ni volumen propio. Sus moléculas no
unidas, expandidas y con poca fuerza de atracción les otorgan propiedades
especiales para la transformación y aleación de los metales, entre otras
numerosas aplicaciones. “Son usados como combustibles y comburentes en
procesos de calentamiento para fusión y corte de metales, hasta para formar
atmósferas protectoras inertes o activas en tratamientos térmicos de metales”
PROCESOS METALÚRGICOS CON GAS:
Combustión: En sentido estricto es una reacción química entre un cuerpo y el
oxígeno combinándose allí, una sustancia oxidante (comburente) y otra
reductora (combustible) con desprendimiento de calor y eventualmente de luz y
llama.
Refi nación: Los gases en la refi nación de metales no ferrosos ayudan a
prolongar la vida útil de los materiales, disminuyen el impacto ambiental de la
explotación minera y reducen las emisiones producidas por empresas
contaminantes.
Tratamientos térmicos: Para ciertos tratamientos térmicos tales como el
recocido limpio, recocido brillante, recocido sin descarburación, temple,
cementación gaseosa, carbonitruración, entre otros, se emplean diferentes
gases como el amoniaco e hidrocarburos gaseosos,los cuales se mezclan con
nitrógeno para evitar la oxidación de los metales.
Enfriamiento: Se emplea nitrógeno para el enfriamiento de los troqueles de
fundición.
Hidrometalurgia: En esta área, los gases son un insumo importante y
económico para el tratamiento de minerales en procesos como la
flotación y la lixiviación
SOLDADURA: La soldadura a gas fue unos de los primeros procesos de fusión
desarrollados por la industria, aplicándose a gran variedad de materiales y
aleaciones.
Informe del Laboratorio de Fisicoquímica E.A.P Ingeniería Metalúrgica
Potrebbero piacerti anche
- Seccon Iv M.ingDocumento35 pagineSeccon Iv M.inggeorginaNessuna valutazione finora
- Cremas deDocumento63 pagineCremas deLyzzi Llerena Meza100% (2)
- Aseguramiento de Calidad Planes de MuestreoDocumento38 pagineAseguramiento de Calidad Planes de MuestreoramsesmuseNessuna valutazione finora
- Aplicación de Los Metodos Numericos en La Ingenieria QuimicaDocumento36 pagineAplicación de Los Metodos Numericos en La Ingenieria QuimicaJulio Abraham Teran Lindo67% (3)
- Ing. Del Gas NaturalDocumento177 pagineIng. Del Gas NaturalAlejandro JaramilloNessuna valutazione finora
- Teoría Del Gas Real: La Relación Exacta Para Gases RealesDa EverandTeoría Del Gas Real: La Relación Exacta Para Gases RealesNessuna valutazione finora
- Ley General Del Estado GaseosoDocumento9 pagineLey General Del Estado GaseosoAleejandraa LhNessuna valutazione finora
- Gas IdealDocumento8 pagineGas IdealGustavo Armando López DíazNessuna valutazione finora
- Practica #1 Gases Reales e IdealesDocumento12 paginePractica #1 Gases Reales e IdealesAlbert Solis DiazNessuna valutazione finora
- Trabajo 3 SuelosDocumento1 paginaTrabajo 3 Suelosanthony33% (3)
- Informe FisicoquimicaDocumento87 pagineInforme FisicoquimicaxiasndkasxNessuna valutazione finora
- Masa Molar PDFDocumento13 pagineMasa Molar PDFMarlon AlarconNessuna valutazione finora
- Ejercicios Clase!Documento44 pagineEjercicios Clase!GUILLERMO50% (2)
- Gases Ideales y Procesos de Los GasesDocumento9 pagineGases Ideales y Procesos de Los GasesBeacker Huaquisto RaimeNessuna valutazione finora
- U5 QuimicaDocumento50 pagineU5 QuimicaMarlen Mares GálvezNessuna valutazione finora
- Alexis Cabreratareas7Documento10 pagineAlexis Cabreratareas7Alexis Cabrera67% (3)
- Ley de Los Gases FicoDocumento47 pagineLey de Los Gases Ficoelver regalado goicocheaNessuna valutazione finora
- Actividad 3-Interaccion Con Los Gases IdealesDocumento16 pagineActividad 3-Interaccion Con Los Gases IdealesWilson Beltran Carrion100% (1)
- Clase 9. Biología de Los EcosistemasDocumento17 pagineClase 9. Biología de Los EcosistemasCesar Britos AquinoNessuna valutazione finora
- CaratulaDocumento21 pagineCaratulaJose VilelaNessuna valutazione finora
- Laboratorio Fisico Quimica AmbientalDocumento32 pagineLaboratorio Fisico Quimica AmbientalmariaNessuna valutazione finora
- Informe de Lab Fisica 2 Ley de BoyleDocumento17 pagineInforme de Lab Fisica 2 Ley de BoyleDean Jimenez Hurtado100% (1)
- Informe de Laboratorio de Quimica: Ley de Avogadro y de BoyleDocumento7 pagineInforme de Laboratorio de Quimica: Ley de Avogadro y de BoyleDenysFuentes0% (1)
- Guia de Gases TerminadaDocumento31 pagineGuia de Gases Terminadakendyyanethbs100% (7)
- Informe Ley de BoyleDocumento13 pagineInforme Ley de BoyleGilvert J Vasquez Mendoza100% (1)
- Informe Fisico Quimica 2019-1Documento38 pagineInforme Fisico Quimica 2019-1Valdez LuisNessuna valutazione finora
- Quimi Unidad 4 - Primer Semestre en SSTDocumento32 pagineQuimi Unidad 4 - Primer Semestre en SSTNelson LopezNessuna valutazione finora
- Informe Fisico Quimica 2019 1Documento39 pagineInforme Fisico Quimica 2019 1RICARDO ANGEL BERRIO PEREZNessuna valutazione finora
- Investigacion GasesDocumento10 pagineInvestigacion GasesArlin Jose AristizabalNessuna valutazione finora
- 1 Ing. Del Gas Semana 1Documento102 pagine1 Ing. Del Gas Semana 1Ladiiziitha ThiinkerNessuna valutazione finora
- 5-Informe de Laboratorio - Ley de BoyleDocumento6 pagine5-Informe de Laboratorio - Ley de Boyleandrea delgadoNessuna valutazione finora
- P02Gas Real Con Comportamiento IdealDocumento22 pagineP02Gas Real Con Comportamiento IdealYaWenLuNessuna valutazione finora
- GasDocumento6 pagineGasPame LxuNessuna valutazione finora
- GASES Fiqui JulioDocumento20 pagineGASES Fiqui JulioRaku VNessuna valutazione finora
- GasesDocumento4 pagineGasesJesúsEnriqueGarciaNessuna valutazione finora
- Guia-de-GasesDocumento27 pagineGuia-de-GasesjimminNessuna valutazione finora
- GasesDocumento6 pagineGasesJose Chavez TobarNessuna valutazione finora
- Lab 2 QMC 1206Documento16 pagineLab 2 QMC 1206Andrea Flores MedranoNessuna valutazione finora
- Trabajo Escrito QuímicaDocumento11 pagineTrabajo Escrito QuímicaEl ThuanNessuna valutazione finora
- Lab 7Documento9 pagineLab 7Daniela DiazNessuna valutazione finora
- Ley de BoyleDocumento17 pagineLey de BoyleJuan Pablo Moran CaballeroNessuna valutazione finora
- Tarea 1 - Gases IdealesDocumento7 pagineTarea 1 - Gases IdealesNancy Olivia VentoleroNessuna valutazione finora
- Cap 7 Gases Ideales 19 Mayo 2013 PDFDocumento14 pagineCap 7 Gases Ideales 19 Mayo 2013 PDFKriiztal GodinezNessuna valutazione finora
- Cb. Leyes de Los GasesDocumento10 pagineCb. Leyes de Los Gasesesthefania navarreteNessuna valutazione finora
- Laboratorio Ley de BoyleDocumento5 pagineLaboratorio Ley de BoyleAlejandra Palma Solano100% (1)
- Año Del Fortalecimiento de La Soberanía NacionalDocumento10 pagineAño Del Fortalecimiento de La Soberanía NacionalAlejandro Isac Mugruza GrandezNessuna valutazione finora
- Informe 04 Grupo 4 Laboratorio de QuimicaDocumento15 pagineInforme 04 Grupo 4 Laboratorio de QuimicaGaudhiNessuna valutazione finora
- TERMODINAMICA Casi TerminadoDocumento13 pagineTERMODINAMICA Casi TerminadoEDER BAQUENessuna valutazione finora
- Ley de Los Gases 1.1Documento8 pagineLey de Los Gases 1.1Ryu AtílionNessuna valutazione finora
- Gases Química PDFDocumento8 pagineGases Química PDFMax ChazzNessuna valutazione finora
- Densidad y Peso MolecularDocumento14 pagineDensidad y Peso MolecularPamelaNessuna valutazione finora
- Practica #1 Ley de CharlesDocumento14 paginePractica #1 Ley de CharlesChristian Pinedo ReateguiNessuna valutazione finora
- Gases Ideales VirtuallDocumento9 pagineGases Ideales VirtuallMIGUEL ANGEL COILA APAZANessuna valutazione finora
- Informe 5Documento23 pagineInforme 5Eva Caballero0% (1)
- Laboratorio 1 - Leyes de Los GasesDocumento10 pagineLaboratorio 1 - Leyes de Los GasesRafael Gustavo Alfaro AlemanNessuna valutazione finora
- Informe 4Documento17 pagineInforme 4GaudhiNessuna valutazione finora
- Cuestionario Previo 9 (Ley de Boyle-Mariotte) - 1 - 280Documento8 pagineCuestionario Previo 9 (Ley de Boyle-Mariotte) - 1 - 280Alan Alberth OHNessuna valutazione finora
- Practica 2Documento8 paginePractica 2AyrtonNessuna valutazione finora
- Laboratorio Ley de BoyleDocumento3 pagineLaboratorio Ley de BoyleCaros GamerNessuna valutazione finora
- CONOCIMIENTOS PREVIOS. Flores Zaragoza D. Janet, MTZ García S. Paola, Morales Reséndiz K. EvelynDocumento7 pagineCONOCIMIENTOS PREVIOS. Flores Zaragoza D. Janet, MTZ García S. Paola, Morales Reséndiz K. EvelynKarina Evelyn Morales ReséndizNessuna valutazione finora
- 4 B-Trabajo 2 Colaborativo Parte 2 Est - Gas 3ro - ZulemaFiinalDocumento12 pagine4 B-Trabajo 2 Colaborativo Parte 2 Est - Gas 3ro - ZulemaFiinalStephany VillafañeNessuna valutazione finora
- Informe de Física AnghelyDocumento7 pagineInforme de Física AnghelyVicto Orlando Avila LorduyNessuna valutazione finora
- Laboratorio de Fisica 200Documento12 pagineLaboratorio de Fisica 200retroman2Nessuna valutazione finora
- Material Unidad 3Documento14 pagineMaterial Unidad 3cesar augusto garcia guerreroNessuna valutazione finora
- Trazabilidad FeDocumento6 pagineTrazabilidad FeRoyni Ramirez CcantoNessuna valutazione finora
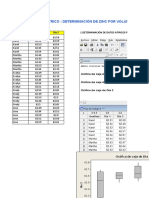
- Comparacion de Medias-Varianzas Iguales SOLDocumento29 pagineComparacion de Medias-Varianzas Iguales SOLRoyni Ramirez CcantoNessuna valutazione finora
- Trazabilidad AgDocumento4 pagineTrazabilidad AgRoyni Ramirez CcantoNessuna valutazione finora
- Reporte 75-Polimetalicos CompletoDocumento4 pagineReporte 75-Polimetalicos CompletoRoyni Ramirez CcantoNessuna valutazione finora
- Trazabilidad PBDocumento6 pagineTrazabilidad PBRoyni Ramirez CcantoNessuna valutazione finora
- Tabla de Graficos de ControlDocumento1 paginaTabla de Graficos de ControlRoyni Ramirez CcantoNessuna valutazione finora
- Diagrama de Pareto-Ejemplo1Documento3 pagineDiagrama de Pareto-Ejemplo1Yasha GomezNessuna valutazione finora
- Aleaciones Bronce PDFDocumento1 paginaAleaciones Bronce PDFHV B JGNessuna valutazione finora
- Adsorcion Por Carbon ActivadoDocumento8 pagineAdsorcion Por Carbon ActivadoRoyni Ramirez CcantoNessuna valutazione finora
- Hoja de ReporteDocumento2 pagineHoja de ReporteRoyni Ramirez CcantoNessuna valutazione finora
- Control Diario de Temperatura de ColadaDocumento3 pagineControl Diario de Temperatura de ColadaRoyni Ramirez CcantoNessuna valutazione finora
- Marco Teorico de TesisDocumento16 pagineMarco Teorico de TesisRoyni Ramirez CcantoNessuna valutazione finora
- VulcanoDocumento5 pagineVulcanoRoyni Ramirez CcantoNessuna valutazione finora
- Catalogo Vulcano 2017Documento19 pagineCatalogo Vulcano 2017Royni Ramirez CcantoNessuna valutazione finora
- Reg-LQK.3.1.1 Tratamiento Planta ComihuasaDocumento63 pagineReg-LQK.3.1.1 Tratamiento Planta ComihuasaRoyni Ramirez CcantoNessuna valutazione finora
- MyGA - Terminos Mas UsadosDocumento13 pagineMyGA - Terminos Mas UsadosRoyni Ramirez CcantoNessuna valutazione finora
- Trabajo #01Documento4 pagineTrabajo #01Royni Ramirez CcantoNessuna valutazione finora
- HacDocumento2 pagineHacRoyni Ramirez CcantoNessuna valutazione finora
- FundMoldeo 7Documento18 pagineFundMoldeo 7Royni Ramirez CcantoNessuna valutazione finora
- Optimizacion y Simulación de Procesos Metalurgicos - SilaboDocumento2 pagineOptimizacion y Simulación de Procesos Metalurgicos - SilaboRoyni Ramirez CcantoNessuna valutazione finora
- Población BacterialDocumento16 paginePoblación BacterialRoyni Ramirez CcantoNessuna valutazione finora
- Población BacterialDocumento3 paginePoblación BacterialRoyni Ramirez CcantoNessuna valutazione finora
- Sílabo Metalurgia y Gestión Del Medio Ambiente I Sem 2018 M CabreraDocumento8 pagineSílabo Metalurgia y Gestión Del Medio Ambiente I Sem 2018 M CabreraRoyni Ramirez CcantoNessuna valutazione finora
- Reg-LQK.3.1.9 Leyes y Densidad Aparente de CubicacionDocumento5 pagineReg-LQK.3.1.9 Leyes y Densidad Aparente de CubicacionRoyni Ramirez CcantoNessuna valutazione finora
- Tesis en Ingenieria Metalurgica: Ing. Eusebio Dionicio Padilla Edionisiop@unmsm - Edu.peDocumento32 pagineTesis en Ingenieria Metalurgica: Ing. Eusebio Dionicio Padilla Edionisiop@unmsm - Edu.peRoyni Ramirez CcantoNessuna valutazione finora
- Solucionario 22 Jun05Documento4 pagineSolucionario 22 Jun05Royni Ramirez CcantoNessuna valutazione finora
- VulcanoDocumento5 pagineVulcanoRoyni Ramirez CcantoNessuna valutazione finora
- Rola TesisDocumento8 pagineRola TesisRoyni Ramirez CcantoNessuna valutazione finora
- Solucionario 22 Jun05Documento6 pagineSolucionario 22 Jun05Daniel Castillo AnchivilcaNessuna valutazione finora
- Paper Efecto CoronaDocumento5 paginePaper Efecto CoronaPresupuesto 2020Nessuna valutazione finora
- Catalogo MitanetDocumento70 pagineCatalogo MitanetGustavo Buendia MatamorosNessuna valutazione finora
- Hidrograma de La TormentaDocumento9 pagineHidrograma de La TormentaAntuane FloresNessuna valutazione finora
- Estudio TetraselmisDocumento83 pagineEstudio TetraselmisFranciscoNessuna valutazione finora
- Unidad 5 Lógica SecuencialDocumento14 pagineUnidad 5 Lógica SecuencialIsaac aquinoNessuna valutazione finora
- 2 - Capítulo II - F2Documento15 pagine2 - Capítulo II - F2Arnold Jhony Jara EstebanNessuna valutazione finora
- Boletin - Problemas - 3Documento10 pagineBoletin - Problemas - 3Pablo MadrugaNessuna valutazione finora
- Matriz de ConsistenciaDocumento1 paginaMatriz de ConsistenciadavidNessuna valutazione finora
- VISCOSIDADDocumento6 pagineVISCOSIDADLuceroNessuna valutazione finora
- Tema 7Documento28 pagineTema 7MariaNessuna valutazione finora
- Semejanza de TurbomáquinasDocumento18 pagineSemejanza de TurbomáquinasRogerNessuna valutazione finora
- Unidad 3 La Gestion de Stock. Prevision de Las NecesidadesDocumento10 pagineUnidad 3 La Gestion de Stock. Prevision de Las Necesidadesestudios spainNessuna valutazione finora
- Balance de EnlaceDocumento8 pagineBalance de EnlacejoseNessuna valutazione finora
- Interpretación de Datos ClimáticosDocumento35 pagineInterpretación de Datos ClimáticosGeografía LiveNessuna valutazione finora
- Analisis HidrometricoDocumento12 pagineAnalisis Hidrometricorodney montoya aizacayoNessuna valutazione finora
- Formación RosablancaDocumento2 pagineFormación RosablancaAndrea Juliana MuñozNessuna valutazione finora
- Operacionalización de Variables: Odontología Activa Revista Científica January 2019Documento7 pagineOperacionalización de Variables: Odontología Activa Revista Científica January 2019Jorge SanchezNessuna valutazione finora
- Sotfware SimuladoresDocumento16 pagineSotfware SimuladoresDaliannis MelendezNessuna valutazione finora
- Programacion LinealDocumento19 pagineProgramacion LinealAMYNNXXXXNessuna valutazione finora
- Act. Práctica # 2Documento2 pagineAct. Práctica # 2Sara Isabel Robleto ValdiviaNessuna valutazione finora
- Afica de Puntos PDFDocumento3 pagineAfica de Puntos PDFgerly diazNessuna valutazione finora
- Plano Sin Ortofoto Desarrollos Turisticos AztecaDocumento1 paginaPlano Sin Ortofoto Desarrollos Turisticos AztecaCarlos HernandezNessuna valutazione finora
- Guia de Trabajo 4, El Regulador FV PDFDocumento7 pagineGuia de Trabajo 4, El Regulador FV PDFFinca Integral Recreativa EducacionalNessuna valutazione finora