Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Síntesis de 1-fenil-2,5-dimetilpirrol mediante reacción de Paal-Knorr
Caricato da
vanessavargas114100%(1)Il 100% ha trovato utile questo documento (1 voto)
5K visualizzazioni3 paginehetero
Titolo originale
Informe 2 Sintesis de 1-Fenil-2,5-Dimetilpirrrol (Autoguardado)
Copyright
© © All Rights Reserved
Formati disponibili
DOCX, PDF, TXT o leggi online da Scribd
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentohetero
Copyright:
© All Rights Reserved
Formati disponibili
Scarica in formato DOCX, PDF, TXT o leggi online su Scribd
100%(1)Il 100% ha trovato utile questo documento (1 voto)
5K visualizzazioni3 pagineSíntesis de 1-fenil-2,5-dimetilpirrol mediante reacción de Paal-Knorr
Caricato da
vanessavargas114hetero
Copyright:
© All Rights Reserved
Formati disponibili
Scarica in formato DOCX, PDF, TXT o leggi online su Scribd
Sei sulla pagina 1di 3
Tetrahedron Letters
journal homepage: www.elsevier.com
Obtencin del 1-fenil-2,5-dimetilpirrol
Ingrid Vanessa Vargas Horta
UDCA, Bogot DC, ivarga@udca.edu.co, Colombia
ARTICLE INFO ABSTRACT
Synthesis of Faal Knorr was carried out to obtain 1-phenyl-2,5-dimethylpyrrole
from a condensation between acetonylacetone and aniline using HCl as catalyst.
Keywords: 0.4339 g of white crystals were obtained in about 15% yield, their melting point
Pirroles between 49-50 C very close to the theoretical data. The product obtained was
1,4-dicarbonyl characterized by infrared analysis showing C-N stretch strips characteristic of
Condensation tertiary amines at 1380 cm -1, benzene C-H stretches at 3099 cm -1, and
Amines resonances of both the benzene and pyrrole cycles 1598-1519 and 1494-1402
Dehydration cm-1 respectively.
1. Introduccin Existen otras maneras de sintetizar sistemas pirrolicos, por
ejemplo usando furano con amoniaco en presencia de un
El pirrol es una molcula de un gran alto inters biolgico, catalizador cido. La sntesis de pirroles de Hantzsch es un
encontrados en la clorofila de las plantas y en algunos mtodo para la obtencin de pirroles sustituidos usando B-
alcaloides como la nicotina y la cocana, Se ha estudiado en cetosteres con alfa-haloacetonas en presencia de amoniaco
gran medida los anillos pirrolicos debido a que este descrita por primera vez por el qumico Arthur Rudolf
compuesto presenta un heterotomo, el Nitrgeno, lo que le Hantzsch. (Venkataraman Amarnath, 1991)
da la posibilidad de comportarse como un compuesto bsico
o un compuesto acido, es decir, un compuesto anftero.
El pirrol es una sal importante en la industria farmacutica,
un ejemplo es el N-metilpirrol es un precursor del cido N-
Para la formacin de anillos pirrolicos se obtienen metilpirrolcarboxlico, el cual se usa como precursor para la
prcticamente mediante cicloadiciones y fabricacin de algunos medicamentos, adems se usa
ciclocondensaciones por lo general se usa la sntesis de Paal- tambin en la industria alimentaria como el 2-acetil-pirrol
Knorr, que parte de un compuesto dicarbonlico enolizable que da sabor a nuez y avellanas (Qumica de Heterociclos.,
que se trata con el derivado de una amina; el compuesto s.f ).
dicarbonlico sufre una condensacin con la amina primaria
para obtener el pirrol. (Knorr, 2010) 2. Experimental
Para la formacin del 1-fenil-2,5-dimetilpirrol, se llevo a
cabo mezclando en un baln redondo de 50 mL, 2 mL de
H3C
N
CH3 acetonilacetona, 1.6 mL de anilina, 15 mL de Etanol al 96%
H3C CH3 + H2N aprox. y 2 gotas de HCl concentrado, se someti a reflujo
O O
hexane-2,5-dione aniline por una hora, la mezcla se verti en un Erlenmeyer que
contena 50mL de agua destilada y 3 mL de HCl conc, se
2,5-dimethyl-1-phenyl-1H-pyrrole Mezcl y se adicion unas gotas de NaOH conc, para
Figura 1. Reaccin de Paal-Knorr. Sntesis de 1-fenil-2,5-difenilpirrol neutralizar la mezcla, posteriormente se llev a Frio para
acelerar la formacin de cristales, luego se realizaron lavados
con agua destilada para eliminar trazas de solvente. El catalizador promoviendo la protonacin de la molcula del
producto se recristaliz usando Etanol: agua en una compuesto dicarbonlico y con ello a deshidratacin. Durante
proporcin de 4:1, posterior su filtracin a presin reducida los 10 minutos del reflujo, se pudo observar, un cambio de
y finalmente se someti a un secado en estufa 40C para que color de la solucin a amarillenta lo que indica que la
el producto quedara libre de agua y poder tomar el punto de reaccin se llev a cabo. Despus del reflujo, se le agrego
fusin. agua destilada acidulada a la solucin con HCl para
neutralizar un posible exceso de anilina, formndose una
pequeas gotas aceitosas en la solucin.
3. Resultados y discusin
3.1 Obtencin del 1-fenil-2,5-dimetilpirrol Para la formacin del precipitado se llevaron a cabo dos
ensayos el primero adicionando NaCl, esto con el fin de
Tabla 1. Resultados experimental Vs Datos tericos deshidratar y que se concentre la solucin, lo que permite
mayor precipitacin o si no se disuelve completamente toda
Experimental Terico la sal, los granos que quedan por disolver, puede acutuar
Punto de Fusin 49-50C 51-52C como micronucleos de crsitalizacin para iniciar la
Cantidad 0.4339 g 2.907 g cristalizacin.
obtenida
El segundo ensayo se adicion hidrxido de sodio para
neutralizar el pH de la solucin y con est se evidenci una
rpidamente la turbidez esperada, asi que una vez adicionado
el Hidrxido se llev a nevera donde se form el precipitado,
lo que indica la formacin de cristales de pirrol, ya filtrado el
O O
CH3 H3C
precipitado, se realiz una recristalizacin con etanol-agua
H3C + H2N
H3C
H
N
+
para purificar el producto, obteniendo un punto de fusin
O H
O
-
experimental de 49-50C, muy cercano al terico, por lo que
se puede deducir que si se logr obtener el pirrol; se obtuvo
H
HO
CH3 HO
CH3 0.4339 g de cristales de color blanco caractersticos del pirrol,
H3C
O
N
+
H sin embargo el rendimiento de la reaccin result muy baja
N N
OH H H
(14.92%), esto probablemente a la corta cantidad de tiempo
CH3 -
O
CH3
HO
CH3 en que se dej la reaccin en el reflujo que hiciera que no
reaccionara por completo los reactivos o falta de tiempo en
CH3
el enfriamiento. Otra posible causa se debe a la incorrecta
manipulacin del material durante la recristalizacin o
N + 2 H2O
prdida en el filtrado al vacio.
CH3
.
Tambin se realiz lectura en IR dando como resultado las
siguientes bandas ms importantes en el espectro
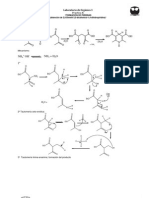
Figura 2, Mecanismo de reaccin del 1-fenil-2,5-dimetilpirrol. Tomado de
http://depa.fquim.unam.mx/amyd/archivero/TEMA2UNIDAD2_27081.pdf
Bandas (cm-1) Descripcin
3099 Estiramiento -CH (Benceno)
2927 Dimetilos (-CH3)
La sntesis de Paal Knorr se lleva a cabo usando dicarbolinos
1598 Resonancia pirrol
junto con aminas sustituidas en medio acido, el mecanismo
de reaccin que se muestra en la figura 2, inicia con un ataque 1519 Resonancia pirrol
nucleoflico del nitrgeno de la amina a uno de los carbonilos 1494 Resonancia benceno
de la acetonilacetona deslocalizando la carga en el oxgeno, 1402 Resonancia benceno
posteriormente por una trasferencia de protones se estabilizan 1380 Estiramiento C-N en aminas terciarias
las cargas tanto del nitrgeno que tenia carga positiva y del
oxgeno que tenia carga negativa, luego se emite un segundo Segn la literatura el anillo pirrolico sale en una banda en
ataque nucleoflico al segundo carbonilo de manera 3490 cm-1, banda que no aparece en el espectro IR sin
intermolecular seguido de una deshidratacin formando el embargo se evidencian estiramiento de las aminas terciarias
pirrol. (Qumica del pirrol, furano y tiofeno, s.f) cerca a 1380 cm-1
Para llevar a cabo la obtencin del 1-fenil-2,5-dimetilpirrol, 4. Conclusiones
en esta prctica se realiz mediante la condensacin de un
compuesto 1,4-dicarbonlico (2 mL de 2,5 hexanodiona) y Se logr obtener el producto deseado 1-fenil-2,5-
anilina (1.6 mL), por el mtodo de reflujo, utilizando como dimetilpirrol mediante una condensacin por medio de la
disolvente 2mL de etanol y 2 gotas de HCl concentrado, sntesis de Paal Knorr usando como catalizador HCl, esto
aplicando calor, donde el medio cido funciona como basndonos en el punto de fusin experimental que fue de 49-
50C dando un resultado muy crcanos al dato terico.
Para la formacin de los cristales se debe tener presente que
la solucin debe estar en un pH neutro, de lo contario no se
formara ningn precipitado.
Para obtener mayor producto de cristales, se debe dejar por
lo menos ms tiempo en el proceso de reflujo y as mismo en
el enfriamiento de esta manera los reactivos reaccionen
completamente.
La temperatura tambin es un factor importante ya que al
momento de recristalizar al tener altas temperaturas podemos
fundir el compuesto completamente sin dejar producto final
Bibliografa
Knorr, R. d. (09 de Octubre de 2010). Qumica orgnica III.
Recuperado el 01 de Abril de 2017, de
https://tenshinoakuma.wordpress.com/2008/10/09/
reacciones-paal-knorr/
Qumica de Heterociclos. (s.f ). Ampliacin de qumica
orgnica avanzada. Obtenido de Capitulo 2.
Heterocilos de 5 miembros :
https://riuma.uma.es/xmlui/bitstream/handle/1063
0/7274/Tema_2.Heterociclos_aromaticos_cinco_
miembros.pdf?sequence=1
Qumica del pirrol, furano y tiofeno. (s.f). Recuperado el 02
de Abril de 2017, de Unidad 2, Heteroiclos de 5
miembros:
http://depa.fquim.unam.mx/amyd/archivero/TEM
A2UNIDAD2_27081.pdf
Venkataraman Amarnath, D. C. (29 de April de 1991).
Intermediates in the Paal-Knorr Synthesis of
Pyrroles. J. Org, Chem, 56, 6924-6931.
Potrebbero piacerti anche
- Organica 3 Práctica 2. Síntesis de Pirroles. Obtención Del 1-Fenil-2,5 DimetilpirrolDocumento2 pagineOrganica 3 Práctica 2. Síntesis de Pirroles. Obtención Del 1-Fenil-2,5 DimetilpirrolUziel AG0% (1)
- Dihidropiridina CartelDocumento1 paginaDihidropiridina CartelRoy InquisdorNessuna valutazione finora
- Practica No.6 Formación de PiridinasDocumento11 paginePractica No.6 Formación de PiridinasFran Castrejon PilgrimNessuna valutazione finora
- IndolesDocumento9 pagineIndolesMagda Cervantes83% (12)
- Informe 5 Preparacion de 2-FenilindolDocumento11 pagineInforme 5 Preparacion de 2-FenilindolDani SantoyoNessuna valutazione finora
- Reporte 04 QODocumento2 pagineReporte 04 QOloloNessuna valutazione finora
- PRACTICA 7 Sintesis 2-FenilindolDocumento14 paginePRACTICA 7 Sintesis 2-FenilindolMateo Valencia78% (9)
- PIRROLES AntecedentessDocumento2 paginePIRROLES Antecedentessarelii2550% (4)
- Reporte DHPDocumento4 pagineReporte DHPEfraínNessuna valutazione finora
- 3,5 Dicarbetoxi 2,6 Dimetil 4 Fenil 1,4 DihidropiridinaDocumento17 pagine3,5 Dicarbetoxi 2,6 Dimetil 4 Fenil 1,4 DihidropiridinaIngrid Daniela0% (1)
- FurionaDocumento4 pagineFurionaetnaverdNessuna valutazione finora
- Práctica 5 Síntesis de 3-Fenil-5-Isoxazolona. (3-Fenilisoxazol-5 (4H) - ONA) .Documento3 paginePráctica 5 Síntesis de 3-Fenil-5-Isoxazolona. (3-Fenilisoxazol-5 (4H) - ONA) .Uziel AGNessuna valutazione finora
- Síntesis de FuroínaDocumento4 pagineSíntesis de FuroínaRichard DomNessuna valutazione finora
- Práctica 10 - Síntesis de 3-Metil-1-Fenil-1,2-Dihidropirazol-5-OnaDocumento7 paginePráctica 10 - Síntesis de 3-Metil-1-Fenil-1,2-Dihidropirazol-5-OnaPau FlurscheimNessuna valutazione finora
- Síntesis de PirrolesDocumento4 pagineSíntesis de PirrolesVale Pika FresaNessuna valutazione finora
- Reporte 9Documento2 pagineReporte 9Melanie MartinezNessuna valutazione finora
- Previo de Orgánica III Práctica 4Documento3 paginePrevio de Orgánica III Práctica 4ChirinoNessuna valutazione finora
- Obtencion de PirrolesDocumento6 pagineObtencion de PirrolesLeslie Valdes100% (1)
- Formación de PiridinasDocumento8 pagineFormación de Piridinas.:("*"BLacK BuLLeT"*"):.100% (6)
- Obtención de 1,4 Dihidropiridina 1Documento21 pagineObtención de 1,4 Dihidropiridina 1AxelWarnerNessuna valutazione finora
- Obtención 1-fenil-2,5-dimetilpirrol reacción Paal-KnorrDocumento4 pagineObtención 1-fenil-2,5-dimetilpirrol reacción Paal-KnorrmiroslavalaropaNessuna valutazione finora
- "FORMACIÓN DE PIRIDINAS (Obtención de 2,6-Dimetil-3,5-Dicarbetoxi-1,4-DihidropiridinaDocumento5 pagine"FORMACIÓN DE PIRIDINAS (Obtención de 2,6-Dimetil-3,5-Dicarbetoxi-1,4-DihidropiridinaIsabella Van Buuren50% (2)
- Practica 3Documento3 paginePractica 3Francisco Lozano Gómez100% (1)
- Práctica 9. Obtencion de La 2,3-DifenilquinoxalinaDocumento4 paginePráctica 9. Obtencion de La 2,3-DifenilquinoxalinaAndrés Arganis100% (5)
- Proyecto - Síntesis de 2,3-DifenilquinoxalinaDocumento5 pagineProyecto - Síntesis de 2,3-DifenilquinoxalinaJosé Silva Fragoso80% (5)
- Practica 1 Sintesis de Isoxazoles Obtencion de 3,5-DimetilisoxazolDocumento12 paginePractica 1 Sintesis de Isoxazoles Obtencion de 3,5-DimetilisoxazolAtaRii CuellarNessuna valutazione finora
- Practica 8Documento4 paginePractica 8fcbarcelona-08hotmail.comNessuna valutazione finora
- Síntesis de 3 Fenil 5 Isoxazolona.Documento1 paginaSíntesis de 3 Fenil 5 Isoxazolona.Jess Marquéz Sarana100% (1)
- Sintesis 3,5-DIETOXICARBONIL,-2,6-DIMETIL-4-FENILDIHIDROPIRIDINADocumento6 pagineSintesis 3,5-DIETOXICARBONIL,-2,6-DIMETIL-4-FENILDIHIDROPIRIDINARocioNessuna valutazione finora
- FORMACIÓN DE CUMARINAS: OBTENCIÓN DE 7-HIDROXI-4-METILCUMARINA (β-METILUMBELIFERONA) .Documento2 pagineFORMACIÓN DE CUMARINAS: OBTENCIÓN DE 7-HIDROXI-4-METILCUMARINA (β-METILUMBELIFERONA) .Montserrat Rafael Colín100% (1)
- Obtencion de 1,4 DihidropiridinasDocumento13 pagineObtencion de 1,4 DihidropiridinasErik Contreras Luis100% (1)
- Síntesis de 7-Hidroxi-4,4-MetilcumarinaDocumento3 pagineSíntesis de 7-Hidroxi-4,4-MetilcumarinaJuan Antonio de la RosaNessuna valutazione finora
- Reporte 7 Sintesis de HantzschDocumento7 pagineReporte 7 Sintesis de Hantzschangelreyes7gpapirrinNessuna valutazione finora
- Formación de PirazolonasDocumento4 pagineFormación de PirazolonasAdrian PINessuna valutazione finora
- Práctica 7 SÍNTESIS DE PIRIMIDINASDocumento2 paginePráctica 7 SÍNTESIS DE PIRIMIDINASVanya MenesesNessuna valutazione finora
- 2 FenilindolDocumento20 pagine2 FenilindolAna Soffia Gomez AriasNessuna valutazione finora
- Evaluación de Farmacológica de Los Sistemas Colinérgicos y Adrenérgicos en Aorta y Tráquea de RataDocumento5 pagineEvaluación de Farmacológica de Los Sistemas Colinérgicos y Adrenérgicos en Aorta y Tráquea de RataNicholas's BarretoNessuna valutazione finora
- Práctica 8 - QO3Documento2 paginePráctica 8 - QO3Marianiux Wolff Nurmi50% (2)
- Informe No 1Documento5 pagineInforme No 1LV HeribertoNessuna valutazione finora
- Condensación de Pechmann para cumarinasDocumento3 pagineCondensación de Pechmann para cumarinasAlberto Antonio Alvarez AlvaradoNessuna valutazione finora
- Práctica 10Documento3 paginePráctica 10Pauzh Pérez100% (2)
- Síntesis de 3,5-dimetilisoxazolDocumento4 pagineSíntesis de 3,5-dimetilisoxazolGuillermo CasillasNessuna valutazione finora
- Sintesis de N-ButiraldehidoDocumento9 pagineSintesis de N-ButiraldehidoGustavo Javier Pérez ContrerasNessuna valutazione finora
- Práctica 12. "Síntesis 5,5-Difenilhidantoina"Documento5 paginePráctica 12. "Síntesis 5,5-Difenilhidantoina"Xanat CortésNessuna valutazione finora
- Práctica No. 1 Síntesis de Furanos. Obtención Del Furfural.Documento3 paginePráctica No. 1 Síntesis de Furanos. Obtención Del Furfural.Uziel AGNessuna valutazione finora
- 5,5 DifenilhidantoínaDocumento2 pagine5,5 DifenilhidantoínaMónica MedinaNessuna valutazione finora
- Sintesis de N-ButiraldehidoDocumento11 pagineSintesis de N-ButiraldehidoBrian Jeef Blancas SotoNessuna valutazione finora
- 3 Nitrobenzoato de MetiloDocumento5 pagine3 Nitrobenzoato de MetiloAdlaremse BlueNessuna valutazione finora
- Práctica 1,1Documento14 paginePráctica 1,1Ivonee PerezNessuna valutazione finora
- Ápendice 1. Practica 1Documento7 pagineÁpendice 1. Practica 1Akai Tsuki0% (1)
- Cuestionario DibenzalacetonaDocumento3 pagineCuestionario DibenzalacetonaRaúl Flores100% (1)
- Informe Pseudo Sanger - NinhidrinaDocumento2 pagineInforme Pseudo Sanger - NinhidrinaDaniel OlmosNessuna valutazione finora
- Practica Furfural FinalDocumento5 paginePractica Furfural Finalfcbarcelona-08hotmail.comNessuna valutazione finora
- Obtención de 1-fenil-2,5-dimetilpirrol mediante reacción de Paal-KnorrDocumento4 pagineObtención de 1-fenil-2,5-dimetilpirrol mediante reacción de Paal-KnorrJesus RaroNessuna valutazione finora
- Previo Práctica 4 - 1-Fenil-2,5-DimetilpirrolDocumento54 paginePrevio Práctica 4 - 1-Fenil-2,5-DimetilpirrolJonathan JacomeNessuna valutazione finora
- Pract 6Documento13 paginePract 6Manuela RamirezNessuna valutazione finora
- Síntesis de 1-Fenil-2,5-dimetilpirrol mediante reacción de Paal-KnorrDocumento3 pagineSíntesis de 1-Fenil-2,5-dimetilpirrol mediante reacción de Paal-KnorrMatias Cajallena VeraNessuna valutazione finora
- Informe 2-FenilindolDocumento9 pagineInforme 2-FenilindolCristhian RomeroNessuna valutazione finora
- Síntesis de Pirrol PROYECTODocumento10 pagineSíntesis de Pirrol PROYECTOdavid canoNessuna valutazione finora
- Informe de Laboratorio 4 - Quimica Organica IDocumento6 pagineInforme de Laboratorio 4 - Quimica Organica I0211720020 ANDREA CAMILA GIRALDO OSPINO ESTUDIANTE ACTIVONessuna valutazione finora
- Estudio de Caminos de Reacción: A + B C + DDocumento10 pagineEstudio de Caminos de Reacción: A + B C + Dvanessavargas114Nessuna valutazione finora
- Obtencion de Pirroles PDFDocumento6 pagineObtencion de Pirroles PDFvanessavargas114Nessuna valutazione finora
- Alcaloides del tropano: compuestos nitrogenados bicíclicos en plantasDocumento4 pagineAlcaloides del tropano: compuestos nitrogenados bicíclicos en plantasvanessavargas114Nessuna valutazione finora
- Articulo de Computacional-Energia Rotacional ButanoDocumento4 pagineArticulo de Computacional-Energia Rotacional Butanovanessavargas114Nessuna valutazione finora
- Analisis de Aminoacidos Por Tlc-Informe 1Documento3 pagineAnalisis de Aminoacidos Por Tlc-Informe 1vanessavargas114Nessuna valutazione finora
- Informe Titulacion de Un AminoacidoDocumento3 pagineInforme Titulacion de Un Aminoacidovanessavargas114Nessuna valutazione finora
- BIOLOGIADocumento5 pagineBIOLOGIAEdiie Lopez RiosNessuna valutazione finora
- Staphylococcus SPPDocumento29 pagineStaphylococcus SPPSamuel VilchezNessuna valutazione finora
- Prueba 2 Glucidos y Lipidos Biologia 1 MedioDocumento3 paginePrueba 2 Glucidos y Lipidos Biologia 1 MedioMarisol SaavedraNessuna valutazione finora
- Taller A-CDocumento3 pagineTaller A-CJohnFedericoMartinezMuñozNessuna valutazione finora
- Cómo hacer jabón líquido a partir de aceite de cocina usadoDocumento17 pagineCómo hacer jabón líquido a partir de aceite de cocina usadovillegas2kkNessuna valutazione finora
- Trabajo Práctico FISICADocumento7 pagineTrabajo Práctico FISICAEsterGabar0% (1)
- Parcial AminasDocumento12 pagineParcial AminasJohaAlvarez0% (1)
- Composición-Quimica-De-La-Materia-Viva - Parte I - Parte Ii 2021Documento118 pagineComposición-Quimica-De-La-Materia-Viva - Parte I - Parte Ii 2021Katherine Katiuzka Escobar Carhuaz0% (1)
- Biomoléculas Orgánicas-IIDocumento21 pagineBiomoléculas Orgánicas-IIMikie AngieNessuna valutazione finora
- Alcohol EsDocumento8 pagineAlcohol EsLiz KapaNessuna valutazione finora
- L-217 Revest. para La Protecc. Ext. de TuberiasDocumento8 pagineL-217 Revest. para La Protecc. Ext. de TuberiasRomner Cordova100% (1)
- Unidad III. TransferenciaDocumento5 pagineUnidad III. TransferenciaJhonatan BentancurtNessuna valutazione finora
- Proteasa de Pepino de Mar PDFDocumento145 pagineProteasa de Pepino de Mar PDFMagaly BenaventeNessuna valutazione finora
- Marco Teorico TerminadoDocumento79 pagineMarco Teorico TerminadoAnonymous Twf6Ej7CVNessuna valutazione finora
- Universidad Peruana Los Andes Facultad de Ingeniería Escuela Profesional de Ingeniería CivilDocumento238 pagineUniversidad Peruana Los Andes Facultad de Ingeniería Escuela Profesional de Ingeniería CivilKATIA HUIZA PEREZNessuna valutazione finora
- RS Plantas IndicadorasDocumento4 pagineRS Plantas IndicadorasSaraNessuna valutazione finora
- Investigación de GlicerolDocumento12 pagineInvestigación de GlicerolJuan MiguelNessuna valutazione finora
- BioquímicaDocumento4 pagineBioquímicaMadeleine Mori FreyreNessuna valutazione finora
- AmonolisisDocumento25 pagineAmonolisismilagros abadNessuna valutazione finora
- Aldehidos y CetonasDocumento14 pagineAldehidos y CetonasElena Muñoz MancillaNessuna valutazione finora
- Fertilizante en EucaliptoDocumento6 pagineFertilizante en EucaliptoCRISTANCHO TORRES AURA CAMILANessuna valutazione finora
- Lab Q.Inorgánica-01Documento16 pagineLab Q.Inorgánica-01Fernando MoragaNessuna valutazione finora
- Bioquimica Microbiana Tercer ParcialDocumento13 pagineBioquimica Microbiana Tercer ParcialLizbeth RamirezNessuna valutazione finora
- Solucionario Ht-Éteres..... 7 PDFDocumento3 pagineSolucionario Ht-Éteres..... 7 PDFJoaquín A. MuñozNessuna valutazione finora
- Lipidos industria fabricaciónDocumento4 pagineLipidos industria fabricaciónGeiner Mauricio Ricardo VidarteNessuna valutazione finora
- Universidad Mayor de San Andres Facultad de Agronomía Carrera de Ingenieria AgronómicaDocumento90 pagineUniversidad Mayor de San Andres Facultad de Agronomía Carrera de Ingenieria AgronómicaIbar QDNessuna valutazione finora
- Hoja 3.rectificacion Simplificado 11 12Documento2 pagineHoja 3.rectificacion Simplificado 11 12Laura Sánchez CuestaNessuna valutazione finora
- Valentina BiordDocumento2 pagineValentina BiordJennifer J ColmenaresNessuna valutazione finora
- Impulsamos La Industria: Catálogo 2022Documento31 pagineImpulsamos La Industria: Catálogo 2022Abraham VegaNessuna valutazione finora
- Ficha Tecnica GMX P 2020Documento1 paginaFicha Tecnica GMX P 2020Raúl MoralesNessuna valutazione finora