Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Solventes Proticos y Aproticos
Caricato da
Sebastián Posada0 valutazioniIl 0% ha trovato utile questo documento (0 voti)
74 visualizzazioni2 pagineQuimica orgánica, solventes proticos y apróticos para mecanismos de reacción por sustitucion nucleofílica
Titolo originale
228589874 Solventes Proticos y Aproticos Docx
Copyright
© © All Rights Reserved
Formati disponibili
PDF, TXT o leggi online da Scribd
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoQuimica orgánica, solventes proticos y apróticos para mecanismos de reacción por sustitucion nucleofílica
Copyright:
© All Rights Reserved
Formati disponibili
Scarica in formato PDF, TXT o leggi online su Scribd
0 valutazioniIl 0% ha trovato utile questo documento (0 voti)
74 visualizzazioni2 pagineSolventes Proticos y Aproticos
Caricato da
Sebastián PosadaQuimica orgánica, solventes proticos y apróticos para mecanismos de reacción por sustitucion nucleofílica
Copyright:
© All Rights Reserved
Formati disponibili
Scarica in formato PDF, TXT o leggi online su Scribd
Sei sulla pagina 1di 2
Dentro de los solventes polares, se encuentran:
1) los que son prticos
2) los que son aprticos.
Un solvente polar prtico, es aquel que es capaz de estabilizar las cargas al
formar puentes de hidrgeno con ellas. Por otro lado, uno aprtico y polar, es
aquel que es capaz de formar una capa fuerte de solvatacin solo alrededor de un
catin, sin formar puente de hidrgeno.
El solvente prtico es capaz de solvatar cationes y aniones puesto que ambos
polos de su dipolo estn fcilmente disponibles. En el ejemplo de ms abajo, que
corresponde a una molcula de alcohol, el protn que es la parte positiva del
dipolo del solvente, es muy pequeo y produce muy poco impedimento estrico al
oxgeno que es la parte negativa del dipolo.
los dos polos del dipolo
estn fcilmente disponibles
disponible
R
RR O
C O
H
R dificilmente disponible
por impedimento estrico
PRTICO APRTICO
En el caso de un solvente aprtico (el ejemplo corresponde a una molcula
de acetona), el oxgeno que es el polo negativo del dipolo, esta disponible para
solvatar una carga positiva. Sin embargo el polo positivo del solvente, que es el
carbono en este caso, queda oculto e impedido por el oxgeno y por los grupos
alquilo voluminosos. El polo positivo del solvente entonces no ser capaz de
acercarse al in negativo y solvatarlo. Por esta razn, los solventes polares
aprticos son capaces de solvatar slo las cargas positivas o cationes.
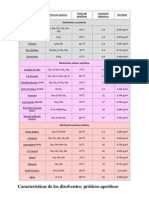
En la siguiente lista de solventes comunes, se cubre un rango de
polaridades y se los cataloga como de tipo prtico o aprticos:
Solvente Frmula Cte. Dielctrica Tipo polar
Agua H2O 78,5 Prtico
cido Frmico HCOOH 59,0 Prtico
Dimetilsulfoxido CH3SOCH3 49,0 Aprtico
Dimetilformamida HCON(CH3)2 36,7 Aprtico
Acetonitrilo CH3CN 36,2 Aprtico
Metanol CH3OH 32,6 Prtico
Hexametilfosforamida ((CH3)2N)3PO 30,0 Aprtico
Etanol CH3CH2OH 24,0 Prtico
Acetona CH3COCH3 20,7 Aprtico
cido Actico CH3COOH 6,0 Prtico
Potrebbero piacerti anche
- Analisis Retrosintetico y Sintesis Organica - Resolucion de Ejemplos Practicos 2010 PDFDocumento653 pagineAnalisis Retrosintetico y Sintesis Organica - Resolucion de Ejemplos Practicos 2010 PDFTamara Michelle Naula100% (2)
- Extracción y Recristalización de Un FármacoDocumento6 pagineExtracción y Recristalización de Un FármacoLeidy Viviana Burbano Ortega100% (11)
- Metabolitos Secundarios de La EspinacaDocumento2 pagineMetabolitos Secundarios de La EspinacaANA MARIA DIAZ BONILLANessuna valutazione finora
- Ley de Lambert - BeerDocumento57 pagineLey de Lambert - BeerChincoyaFNessuna valutazione finora
- Practica #3 Determinación Del Peso Molecular Por Crioscopia.Documento6 paginePractica #3 Determinación Del Peso Molecular Por Crioscopia.Alondra Monserrat Castrejón Anguiano0% (1)
- Reporte 5 OrgánicaDocumento4 pagineReporte 5 OrgánicaIsabel ZuñigaNessuna valutazione finora
- Práctica No.6Documento6 paginePráctica No.6Mariel MirandaNessuna valutazione finora
- Reporte de CloretonaDocumento5 pagineReporte de CloretonaFernanda GómezNessuna valutazione finora
- Practica 1. Efecto Del Tamaño de Partícula y de Temperatura Sobre La Velocidad de La ReacciónDocumento5 paginePractica 1. Efecto Del Tamaño de Partícula y de Temperatura Sobre La Velocidad de La ReacciónPau Flurscheim100% (1)
- Mecanismo de Reacción para Obtener AspirinaDocumento1 paginaMecanismo de Reacción para Obtener AspirinaEnrique Gómez Rincón75% (4)
- Solucionario Quimica Organica Bruice 5dDocumento433 pagineSolucionario Quimica Organica Bruice 5dLauroGarcía93% (59)
- Practica #4 Determinación Del Peso Molecular Por El Método Rast.Documento5 paginePractica #4 Determinación Del Peso Molecular Por El Método Rast.Alondra Monserrat Castrejón Anguiano100% (1)
- Práctica No. 8 - Extracción y Cristalización de Ácido AcetilsalicílicoDocumento7 paginePráctica No. 8 - Extracción y Cristalización de Ácido AcetilsalicílicoJael Morales UrrutiaNessuna valutazione finora
- Expo Heterociclos 4 MiembrosDocumento17 pagineExpo Heterociclos 4 Miembroskampanita_say23100% (1)
- Cuestionarios Química Orgánica.Documento42 pagineCuestionarios Química Orgánica.Banks100% (2)
- Epoxidación SharplessDocumento14 pagineEpoxidación SharplessHezrra Perez KauffmanNessuna valutazione finora
- Epoxido de MenadionaDocumento6 pagineEpoxido de MenadionaUriel DíazNessuna valutazione finora
- Problemas RESUELTOS PrecipitacionDocumento37 pagineProblemas RESUELTOS PrecipitacionSuzy KuticuteNessuna valutazione finora
- Resumen Cálculo. Luz ContinuaDocumento17 pagineResumen Cálculo. Luz ContinuaAnonymous lD22XeNessuna valutazione finora
- Práctica de Destilacion de Una Mezcla AzeotropicaDocumento9 paginePráctica de Destilacion de Una Mezcla AzeotropicaYessica ChávezNessuna valutazione finora
- Síntesis de Fenacetina 15.Documento8 pagineSíntesis de Fenacetina 15.D. ARMANDO R. TAPIA100% (1)
- Cloruro de TerbutiloDocumento6 pagineCloruro de Terbutiloyocepunkrocker100% (1)
- DisolventeDocumento4 pagineDisolventejuliob412Nessuna valutazione finora
- Acidez de Hidrógenos AlfaDocumento2 pagineAcidez de Hidrógenos AlfaBeymar ContrerasNessuna valutazione finora
- 03 Lab Serie EspectroquimicaDocumento5 pagine03 Lab Serie EspectroquimicaDesmond MacLeod CareyNessuna valutazione finora
- Practica 5. Gravimetria de CA en Oxalato de Calcio MonohidratadoDocumento4 paginePractica 5. Gravimetria de CA en Oxalato de Calcio MonohidratadoJoha SkyNessuna valutazione finora
- Obtención del éter β-naftil metílico (nerolina)Documento11 pagineObtención del éter β-naftil metílico (nerolina)MyriamNessuna valutazione finora
- Obtención de Acetaldehído Con H2so4Documento16 pagineObtención de Acetaldehído Con H2so4militarml50% (4)
- Estructura Quimica de Las Ftalainas y Sus Miembros Mas ImportantesDocumento2 pagineEstructura Quimica de Las Ftalainas y Sus Miembros Mas ImportantesbrenchhhNessuna valutazione finora
- GUÍA No. 06 OBTENCIÓN DEL DIOXALATO CUPRATO DE POTASIODocumento6 pagineGUÍA No. 06 OBTENCIÓN DEL DIOXALATO CUPRATO DE POTASIOYamilex FrancisNessuna valutazione finora
- Pruebas de InsaturacionDocumento19 paginePruebas de InsaturacionSteves FloresNessuna valutazione finora
- Cetenas de Quimicca OrganicaDocumento6 pagineCetenas de Quimicca OrganicaWilber Lopez AvilaNessuna valutazione finora
- Halogenuros de Alquilo. PropiedadesDocumento10 pagineHalogenuros de Alquilo. PropiedadesAndrea PachecoNessuna valutazione finora
- DiagramaDocumento2 pagineDiagramaAlan SalinasNessuna valutazione finora
- Práctica4. Síntesis de BenciloDocumento8 paginePráctica4. Síntesis de BenciloSamantha Calvillo100% (1)
- Haluros de Arilo RealDocumento10 pagineHaluros de Arilo RealAnDreNessuna valutazione finora
- Reducción de Aldehídos y CetonasDocumento19 pagineReducción de Aldehídos y CetonasSilvia Rivera Sivila80% (10)
- Práctica 1. Isomería Cis - TransDocumento8 paginePráctica 1. Isomería Cis - TransAndres Ordoñez100% (2)
- Mecanismos SN1, SN2, E1 y E2Documento36 pagineMecanismos SN1, SN2, E1 y E2FannyLuna88% (17)
- Palmer Capitulo VDocumento10 paginePalmer Capitulo VCesar Fernando Sarrin CepedaNessuna valutazione finora
- Guia de Quimica Organica-Intermediarios de ReaccionDocumento7 pagineGuia de Quimica Organica-Intermediarios de ReaccionJose Hernandz0% (2)
- Acido Picrico ObtencionDocumento4 pagineAcido Picrico ObtencionCatalino de la MNessuna valutazione finora
- Mecanismo de Reacción para La AcetanilidaDocumento4 pagineMecanismo de Reacción para La AcetanilidaBrayanm Quispe Molina0% (2)
- Cloruro de TerbutiloDocumento6 pagineCloruro de TerbutiloFrank HurtadoNessuna valutazione finora
- ACIDO BENZOICO POLARIDAD. - Tiene Un Anillo Bencénico No Polar Que Conforma La MayorDocumento5 pagineACIDO BENZOICO POLARIDAD. - Tiene Un Anillo Bencénico No Polar Que Conforma La MayorEvelyn Quispe TorrezNessuna valutazione finora
- Cristalizacion Con Carbon Activado y en Par de DisolventesDocumento7 pagineCristalizacion Con Carbon Activado y en Par de Disolventes.:("*"BLacK BuLLeT"*"):.69% (16)
- Fotometría de Llama..Documento12 pagineFotometría de Llama..Fabian Andres Otárola Otárola100% (1)
- Sintesis 1-Clorobutano Reaccion - SN2Documento8 pagineSintesis 1-Clorobutano Reaccion - SN2Oscar G. Marambio100% (1)
- Práctica 10 Síntesis de BenciloDocumento5 paginePráctica 10 Síntesis de BenciloValezNessuna valutazione finora
- Desplazamiento de ComplejosDocumento2 pagineDesplazamiento de ComplejosMÌthon Guayan100% (2)
- Beta MetoxinaftalenoDocumento11 pagineBeta MetoxinaftalenoAreli CastilloNessuna valutazione finora
- Obtencion Del Acido AcetilsalicilicoDocumento9 pagineObtencion Del Acido Acetilsalicilicofernando77% (13)
- Métodos de Síntesis de Haluros de AlquiloDocumento4 pagineMétodos de Síntesis de Haluros de AlquiloArilu2010Nessuna valutazione finora
- 11 Aldehidos y CetonasDocumento15 pagine11 Aldehidos y Cetonasedson0% (1)
- Examen Parcial de Quimica 2 Fia-Uni (Masguito)Documento9 pagineExamen Parcial de Quimica 2 Fia-Uni (Masguito)Ricardo ChuraNessuna valutazione finora
- Parcial SolucionDocumento4 pagineParcial Soluciondarkwolf1003Nessuna valutazione finora
- Aldehidos y CetonasDocumento39 pagineAldehidos y CetonasKEVIN SMITH SURICHAQUI PARHUAYNessuna valutazione finora
- Identificación Aldehídos, Cetonas y Ácidos CarboxílicosDocumento32 pagineIdentificación Aldehídos, Cetonas y Ácidos CarboxílicosAndres SantiagoNessuna valutazione finora
- Laboratorio Quimica OrganicaDocumento43 pagineLaboratorio Quimica OrganicaRyo Poma100% (1)
- Acidez en Moléculas OrganicasDocumento109 pagineAcidez en Moléculas OrganicasAlicia SanchezNessuna valutazione finora
- Acidez 3 y Mec. BuenoDocumento138 pagineAcidez 3 y Mec. BuenoasdafadNessuna valutazione finora
- Practica #1Documento16 paginePractica #1Myriam TorresNessuna valutazione finora
- Qué Es Un Auto HíbridoDocumento15 pagineQué Es Un Auto HíbridoOscar SotoNessuna valutazione finora
- Refractometria Final 1.0Documento22 pagineRefractometria Final 1.0Kevin VizcarraNessuna valutazione finora
- Reservorios III - SuperposicionDocumento16 pagineReservorios III - SuperposicionIvAn TiToNessuna valutazione finora
- DESHIDRATACION de Aceite Gas y DesaladoDocumento30 pagineDESHIDRATACION de Aceite Gas y DesaladoJC AR100% (1)
- Quinua y La Cerveza PDFDocumento12 pagineQuinua y La Cerveza PDFabel_csulcaNessuna valutazione finora
- Propiedades Mecánicas de Perfiles METASADocumento20 paginePropiedades Mecánicas de Perfiles METASAcliford_montalvanNessuna valutazione finora
- Caracteisticas de Las CarnesDocumento8 pagineCaracteisticas de Las CarnesMarco AntonioNessuna valutazione finora
- AnexoIII HallazgosFinalOctDocumento37 pagineAnexoIII HallazgosFinalOctCarlos Alfredo Lopez VegaNessuna valutazione finora
- NFPA 1971 2013 (Cambio en Prendas) PDFDocumento2 pagineNFPA 1971 2013 (Cambio en Prendas) PDFjailton Rodriguez ArceNessuna valutazione finora
- Testigo Del ChorroDocumento4 pagineTestigo Del ChorroazorazurNessuna valutazione finora
- SCIU-164 - TAREA - U008 - Wilfredo CajoDocumento6 pagineSCIU-164 - TAREA - U008 - Wilfredo CajoWilfredo CajoNessuna valutazione finora
- Practica 1Documento21 paginePractica 1Jennifer Marlene MartinezNessuna valutazione finora
- Clase de Fenoles Version 2017Documento35 pagineClase de Fenoles Version 2017Ricardo MogollonNessuna valutazione finora
- Informe de Quimica Numero 8Documento7 pagineInforme de Quimica Numero 8geraldinehelen0% (1)
- BMyE Con RXDocumento7 pagineBMyE Con RXFelix AlorNessuna valutazione finora
- Trabajo de Perido Fisica Decimo 2019Documento2 pagineTrabajo de Perido Fisica Decimo 2019Daniel GómezNessuna valutazione finora
- Agar Hierro y LisinaDocumento1 paginaAgar Hierro y LisinaAlfredo Benjamin Fuentes OrtizNessuna valutazione finora
- Tema GeneralDocumento47 pagineTema GeneralTitoxd CastroNessuna valutazione finora
- Arcata, Informe Pruebas de Sedimentacion Mineral MacarenaRelaves, 06-12-12 - Final-Usuario - PDFDocumento12 pagineArcata, Informe Pruebas de Sedimentacion Mineral MacarenaRelaves, 06-12-12 - Final-Usuario - PDFMary Elyzabeth Loayza MedinaNessuna valutazione finora
- Evidencia 2Documento3 pagineEvidencia 2vivianaNessuna valutazione finora
- Plan de Estudios Por Areas Curriculares 2005 Ingeniería Forestal UnsaacDocumento5 paginePlan de Estudios Por Areas Curriculares 2005 Ingeniería Forestal UnsaacCésar Pillco MercadoNessuna valutazione finora
- Construccion de Las Celdas CritalinasDocumento11 pagineConstruccion de Las Celdas CritalinasrichradNessuna valutazione finora
- De La Alquimia Al Método CientificoDocumento26 pagineDe La Alquimia Al Método CientificoCRISTIAN100% (2)
- Práctica #1 Viscosimetros CapilaresDocumento7 paginePráctica #1 Viscosimetros CapilaresRicardo LongoriaNessuna valutazione finora
- TFC - Gonzalo Gutiérrez SomavillaDocumento35 pagineTFC - Gonzalo Gutiérrez SomavillaGonzalo Gutiérrez SomavillaNessuna valutazione finora
- Articulo de RevisionDocumento21 pagineArticulo de RevisionNayelli FloresNessuna valutazione finora
- Informe de Curvas de CalibraciónDocumento11 pagineInforme de Curvas de CalibraciónSara RodríguezNessuna valutazione finora