Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Qui Mica
Caricato da
joyedy0 valutazioniIl 0% ha trovato utile questo documento (0 voti)
7 visualizzazioni3 pagineQuímica apuntes
Titolo originale
QuiMica
Copyright
© © All Rights Reserved
Formati disponibili
DOCX, PDF, TXT o leggi online da Scribd
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoQuímica apuntes
Copyright:
© All Rights Reserved
Formati disponibili
Scarica in formato DOCX, PDF, TXT o leggi online su Scribd
0 valutazioniIl 0% ha trovato utile questo documento (0 voti)
7 visualizzazioni3 pagineQui Mica
Caricato da
joyedyQuímica apuntes
Copyright:
© All Rights Reserved
Formati disponibili
Scarica in formato DOCX, PDF, TXT o leggi online su Scribd
Sei sulla pagina 1di 3
Propiedades Fsicas:
La presencia del grupo carbonilo convierte a los aldehdos y cetonas en
compuestos polares. Los compuestos de hasta cuatro tomos de carbono,
forman puente de hidrgeno con el agua, lo cual los hace completamente
solubles en agua. Igualmente son solubles en solventes orgnicos.
Punto de Ebullicin: los puntos de ebullicin de los aldehdos y cetonas son
mayores que el de los alcanos del mismo peso molecular, pero menores que el
de los alcoholes y cidos carboxlicos comparables. Esto se debe a la formacin
de dipolos y a la ausencia de formacin de puentes de hidrgeno
intramoleculares en stos compuestos.
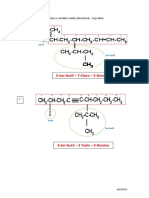
No es de sorprender que los aldehdos y las cetonas se asemejen en la
mayora de sus propiedades como consecuencia de poseer el grupo
carbonilo. Sin embargo, en los aldehdos el grupo carbonilo est unido a
un tomo de hidrgeno, mientras que en las cetonas se une a dos
grupos orgnicos. Esta diferencia estructural afecta a sus propiedades
de dos formas fundamentales:
- Los aldehdos se oxidan con facilidad mientras que las cetonas lo
hacen con dificultad
- Los aldehdos suelen ser ms reactivos que las cetonas en adiciones
nucleoflicas, que es la reaccin ms caracterstica de este tipo de
compuestos
Punto de Ebullicin
Al ser el grupo carbonilo un grupo muy polar determina el que los aldehdos y
cetonas tengan puntos de ebullicin ms altos que los hidrocarburos del mismo
peso molecular.
Sin embargo, los aldehdos y las cetonas no pueden formar enlaces de
hidrgeno entre s, por lo cual sus puntos de ebullicin son menores que los de
los correspondientes alcoholes.
Si la diferencia de electronegatividad es diferente a cero entonces es POLAR,
caso contrario es APOLAR.
Por su Geometra Molecular, si es Lineal o tetradrico entonces es APOLAR, si
es Asimtrico (angular) entonces es POLAR.
Mayor intensidad del Enlace Dipolo-Dipolo, mayor punto de ebullicin.
Puente de Hidrogeno, tipo de enlace dipolo-dipolo, se produce entre molculas
polares, con la caracterstica que esas molculas polares tienen que contener
un Hidrogeno unido a elementos de alta electronegatividad (F, O, N). Enlace
dipolo muy fuerte.
Intensidad:
E.P.H. > D-D > F.L.
cido Carboxlico: Los cidos carboxlicos presentan puntos de ebullicin
elevados debido a la presencia de doble puente de hidrgeno. Los cidos
carboxlicos hierven a temperaturas an ms altas que los alcoholes. Estos
puntos de ebullicin tan elevados se deben a que un par de molculas del
cido carboxlico se mantienen unidas no por un puente de hidrgeno sino por
dos
Alcoholes: El grupo OH es muy polar y, lo que es ms importante, es capaz de
establecer puentes de hidrgeno: con sus molculas compaeras o con otras
molculas neutras.
Los aldehdos y las cetonas no pueden formar enlaces de hidrgeno entre s,
posen enlaces dipolo, por lo cual sus puntos de ebullicin son menores que los
de los correspondientes alcoholes.
Potrebbero piacerti anche
- Caso Practico - Los Tipos de Interés y El Valor Temporal de Dinero - Caso Práctico PDFDocumento5 pagineCaso Practico - Los Tipos de Interés y El Valor Temporal de Dinero - Caso Práctico PDFMolly Mckinnon100% (7)
- Aportes de Los Cientificos A La Quimica OrganicaDocumento4 pagineAportes de Los Cientificos A La Quimica OrganicaLuis Vargas33% (9)
- Exposicion de CetonasDocumento4 pagineExposicion de CetonasJose CondeNessuna valutazione finora
- Examen QuímicaDocumento3 pagineExamen Químicajoyedy100% (1)
- Ayuda OralDocumento7 pagineAyuda OraljoyedyNessuna valutazione finora
- Soldadura Con Oxigeno y Gas CombustibleDocumento2 pagineSoldadura Con Oxigeno y Gas CombustiblejoyedyNessuna valutazione finora
- Lista SongDocumento46 pagineLista SongjoyedyNessuna valutazione finora
- Despido InjustificadoDocumento2 pagineDespido InjustificadojoyedyNessuna valutazione finora
- 3 A - Autoevaluación - Semana 3Documento2 pagine3 A - Autoevaluación - Semana 3joyedyNessuna valutazione finora
- Quimica Preg 5Documento2 pagineQuimica Preg 5joyedyNessuna valutazione finora
- Vigas InfoDocumento15 pagineVigas InfojoyedyNessuna valutazione finora
- Ejercicios de Enlace QuimicoDocumento18 pagineEjercicios de Enlace Quimicoafrunp5186Nessuna valutazione finora
- Practica 4 QuimicaDocumento9 paginePractica 4 QuimicaAlejandra Rubio García100% (1)
- Investigar Los Subniveles de Energía Por Capa SDocumento4 pagineInvestigar Los Subniveles de Energía Por Capa SJaciel RicoyNessuna valutazione finora
- Reaccion de DesidratacionDocumento9 pagineReaccion de DesidratacionFernanda MartinezNessuna valutazione finora
- 1-Compuestos Organicos e Inorganicos I ParteDocumento17 pagine1-Compuestos Organicos e Inorganicos I ParteSócrates Becerra MurilloNessuna valutazione finora
- Taller Elementos y Compuestos QuimicosDocumento22 pagineTaller Elementos y Compuestos QuimicosMaria Tere BoMaNessuna valutazione finora
- CICLOHEXENODocumento3 pagineCICLOHEXENOVladimir GarciaNessuna valutazione finora
- Labo-N10 - Colorantes ÁcidosDocumento15 pagineLabo-N10 - Colorantes ÁcidosJOSE AYALANessuna valutazione finora
- Comportamiento de Grupos Funcionales, Practica 1Documento18 pagineComportamiento de Grupos Funcionales, Practica 1Christian Ventura Fuentes0% (2)
- Solucion - Ejercicios Isomeria y ReactividadDocumento18 pagineSolucion - Ejercicios Isomeria y ReactividadLara Si FraNessuna valutazione finora
- Compuestos Carbonílicos: Aldehídos y CetonasDocumento44 pagineCompuestos Carbonílicos: Aldehídos y CetonasEzequiel HernándezNessuna valutazione finora
- Características de Los Grupos FuncionalesDocumento6 pagineCaracterísticas de Los Grupos FuncionalesLeonel Goudett PuesmeNessuna valutazione finora
- Clase 7 Quim - Inorganica Cualitativa Espinoza ElisabetDocumento86 pagineClase 7 Quim - Inorganica Cualitativa Espinoza ElisabetJhosephFlorRiveraNessuna valutazione finora
- Halogenuros de AlquinoDocumento22 pagineHalogenuros de AlquinoBlanca Alejandra EscobarNessuna valutazione finora
- Capitulo 11 Fuerzas Intermoleculares Liquidos y SolidosDocumento12 pagineCapitulo 11 Fuerzas Intermoleculares Liquidos y SolidostaipantaiNessuna valutazione finora
- Examen Ebau Canarias Junio 2017 ResueltoDocumento8 pagineExamen Ebau Canarias Junio 2017 ResueltoAshok Bhoiwani CabreraNessuna valutazione finora
- Credito Publico GeneralidadesDocumento31 pagineCredito Publico GeneralidadesVerushka LeivaNessuna valutazione finora
- Identificacion de Carbohidratos ReductoresDocumento5 pagineIdentificacion de Carbohidratos ReductoresDavid Colorado VegaNessuna valutazione finora
- Guia para Planificacion Quimica OrganicaDocumento8 pagineGuia para Planificacion Quimica OrganicaRicardo SierraNessuna valutazione finora
- Glosario de GenéticaDocumento45 pagineGlosario de GenéticaYery MercadoNessuna valutazione finora
- Estructura de LewisDocumento23 pagineEstructura de LewisCGOROZCONessuna valutazione finora
- InfografiaDocumento1 paginaInfografiaPaulaAndrea50% (4)
- Las AminasDocumento5 pagineLas AminasIncaluqueSortijaYhonCarlosNessuna valutazione finora
- QUIMICA ORGANICA (Segundo Informe) - UNASAMDocumento11 pagineQUIMICA ORGANICA (Segundo Informe) - UNASAMJhomel Menen Cueva Fernandez100% (1)
- Compuestos OrganimetálicosDocumento27 pagineCompuestos OrganimetálicosAndres Gonzalo Restrepo GuerreroNessuna valutazione finora
- 2 Enlazamiento AtomicoDocumento14 pagine2 Enlazamiento AtomicoPeter_SkwNessuna valutazione finora