Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Resumen Los Gases
Caricato da
ppeinado00Copyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Resumen Los Gases
Caricato da
ppeinado00Copyright:
Formati disponibili
TEMA 2: GASES. PROPIEDADES. LEYES. TEORIA CINETICO-MOLECULAR.
0.- ESTADOS DE AGREGACIN DE LA MATERIA
Existen 3 estados de agregacin de la materia: slidos, lquidos o gases.
Muchas sustancias, bajo las condiciones apropiadas, pueden existir en los tres estados.
Sublimacin
Fusin
Vaporizacin
Slido
Lquido
Solidificacin
Gaseoso
Condensacin
Sublimacin regresiva
Evaporacin: Afecta slo a la superficie libre del lquido y tiene lugar a cualquier T.
Vaporizacin
Ebullicin: Afecta a todo el lquido y tiene lugar a una cierta T, que depende de la presin exterior.
Caractersticas de los tres estados:
Gases:
- Carecen de forma definida y no poseen un volumen propio.
- Son expansibles y compresibles.
Lquidos: - Carecen de forma definida, pero poseen su propio volumen definido.
- Son poco o nada compresibles y expansibles.
Slidos: - Tienen forma propia y volumen definido.
- No son compresibles ni expansibles, a no ser que se ejerza sobre ellos fuerzas de gran
intensidad.
Los gases y los lquidos pueden adaptarse a la forma del recipiente que los contienen, as como escapar por
un orificio que se practique en el recipiente, por lo que reciben el nombre de fluidos.
Normalmente, un lquido tiene una densidad mucho mayor (700 a 1.700 veces) que un gas, mientras que un
slido tiene una densidad ligeramente mayor que un lquido.
TEORA CINTICO-MOLECULAR
La teora cintico-molecular o teora cintica, fue desarrollada inicialmente para los gases.
- Los gases estn formados por partculas (tomos o molculas) muy pequeas separadas unas de otras
que se mueven constantemente chocando entre si y con las paredes del recipiente de forma elstica,
es decir el choque cambia su direccin pero no su velocidad.
- Los gases ocupan el volumen de todo el recipiente que los contiene.
- Los gases ejercen presin sobre las paredes del recipiente que los
contiene. Esta presin se debe a los choques de las partculas del gas con
las paredes.
- Cuanto mas rpido se mueven las partculas del gas, mayor es la
temperatura.
- Las fuerzas atractivas de cohesin entre las molculas, o fuerzas
intermoleculares, son muy dbiles o nulas.
Este modelo tambin es aplicable a slidos y lquidos.
Con la teora cintico-molecular se pueden explicar las caractersticas de cada estado:
Slidos: Sus partculas se encuentran en contacto y no pueden desplazarse, por eso tienen una forma y volumen
propios, no son compresibles ni expansibles, son relativamente duros y rgidos y su densidad es alta.
Lquidos: Sus las partculas se encuentran muy prximas y pueden desplazarse unas sobre otras, as tienen volumen
propio pero se adaptan a la forma del recipiente que las contiene y su densidad es algo menor que la de los slidos.
Gases: Como las fuerzas de atraccin son muy dbiles, las partculas estn muy separadas unas de otras y se mueven en
todas las direcciones y al no haber nada que retenga las partculas prximas entre s, los gases se expanden hasta llenar
el recipiente, y por existir grandes distancias entre ellas, son fcilmente compresibles y su densidad es mucho menor
que la de los slidos y lquidos.
1.- LEYES DE LOS GASES
Cualquier muestra dada de un gas puede describirse en funcin de cuatro propiedades fundamentales:
masa; se mide en kg (SI) y gramos.
volumen; se mide en m3 (SI), en L o en mL. 1m3=103 L
3
presin; se mide en Pa, pascal (SI), en atmsferas o en mm de mercurio. 1 atm=1,013 10 Pa=760 mm de
Hg.
temperatura; se mide en K (SI), o en C. T(K) = T(C) + 273 K.
1.1. Ley de Boyle-Mariotte: Presion y Volumen
Para una determinada masa de gas el volumen es inversamente
proporcional a la presin ejercida, si la temperatura se mantiene constante:
V = constante 1 / P
con T y m constantes
Se puede enunciar tambin de la siguiente forma:
"Cuando un gas experimenta transformaciones a temperatura constante,
el producto del volumen del gas por la presin que ejerce permanece
constante"
PV = constante (T y m constantes)
Esta relacin se conoce como Ley de Boyle-Mariotte.
Otra forma ms conveniente de escribir esta ley para comparar la misma muestra de gas, a temperatura
constante, bajo diferentes condiciones de presin y volumen, es:
P1V1 = P2V2 = P3 V3
; (T y m constantes)
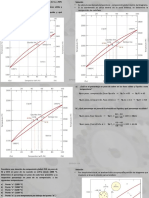
1.2. Ley de Charles: Temperatura y Volumen
Un gas al calentarse se expande de forma uniforme; as, por cada grado de aumento de la temperatura, el
aumento de volumen del gas es de 1/273 veces su volumen a 0 C. Por tanto, tal y como muestra la figura (a), el
volumen de un gas es una funcin lineal de su temperatura Celsius (la grfica V- t es una recta).
Figura a
Figura b
(K)
En la prctica, todos los gases se condensan para dar lquidos y slidos a temperaturas superiores a los -273 C
(cero absoluto) por lo que, de hecho, ningn gas puede ser enfriado hasta que se anule su volumen.
La escala absoluta o Kelvin de temperaturas fue sugerida por primera vez por Lord Kelvin. Y se relaciona
con la Celsius mediante las expresiones:
T (K) = T (C) + 273
T (C) = T (K) - 273
Ley de Charles:
"Cuando un gas experimenta transformaciones a presin constante, el cociente entre el volumen que
ocupa y su temperatura absoluta permanece constante."
V / T = constante ; (P y m constantes)
V1 V2
=
T1 T2
(P y m constantes)
Para que las comparaciones resulten ms sencillas, lo que se suele hacer es referir el volumen de una muestra
dada de un gas a 0 C (273,15 K) y 1 atm; estas condiciones son conocidas como condiciones normales (lo
que se suele abreviar como c.n.).
2
1.3. 2 Ley de Gay-Lussac: Presion y Temperatura
En sus experimentos Gay-Lussac encontr que la presin del gas, mantenido a volumen constante,
aumentaba uniformemente al calentarse. Si la temperatura se expresa en C se obtiene una funcin lineal
como muestra la figura a, mientras que si se expresa en K, se observa que la presin es directamente
proporcional a la temperatura absoluta (figura b).
(K)
Figura a
Figura b
Ley de Gay-Lussac:
"Cuando un gas experimenta transformaciones a volumen constante, el cociente entre la presin que
ejerce y su temperatura absoluta permanece constante."
P1 P2
=
T1 T2
(V y m constantes)
1.4. Ecuacin General de los Gases Ideales
Combinando las leyes anteriores se obtiene la ecuacin conocida como ecuacin general de los gases
ideales:
P1V1 P2V2
=
T1
T2
Se dice que son gases ideales los gases que cumplen las leyes de Boyle-Mariotte, Gay-Lussac y Charles.
2. ECUACIN DE ESTADO DE LOS GASES IDEALES
De la ecuacin general de los gases ideales se deduce que, para cualquier gas ideal en cualquier estado:
PV
= cte
T
Si introducimos 1 mol de un gas ideal cualquiera en un recipiente, la constante, es R denominada constante
de los gases. Si la presin se expresa en atmsferas, el volumen en litros y la temperatura en K, el valor de R
es de 0,082 atml/molK, mientras que en el S.I. el valor de R = 8,3 J / mol .K
Para una cantidad determinada de gas, la ley de los gases ideales puede expresarse tambin en funcin de las
condiciones iniciales y las finales:
PV
o bien
PV = nRT
= nR
T
La ecuacin de los gases ideales, se cumple estrictamente para los llamados gases ideales: gases hipotticos
en los que el tamao de las molculas es absolutamente despreciable frente a la distancia existente entre las
molculas (volumen nulo) y en el que adems no existieran fuerzas intermoleculares. Sin embargo, el
comportamiento de los gases reales difiere ligeramente del ideal a causa del tamao de las molculas y
tambin porque existen fuerzas intermoleculares. No obstante, para todos los clculos que se efectan
normalmente, puede suponerse que los gases reales se comportan como se fueran ideales.
Volumen molar (22,4 L): volumen que ocupa 1 mol de un gas a 1 atm de presin y 0 C de temperatura
2.1 Aplicaciones De La Ley De Estado De Los Gases Ideales
a) Clculo de la masa molecular de un gas
De acuerdo con la ley general de los gases:
PV=nRT
y como el nmero de moles, n, es igual a: n = m / M (masa de un mol), resulta:
m
m . R .T
P .V =
. R . T , si despejamos la
Mm =
masa molar, M, tenemos:
P .V
Mm
Conociendo el valor de la masa de un mol (masa molar) se puede deducir fcilmente el valor de su masa
molecular (mismo valor numrico pero expresado en u).
b) Clculo de la densidad de un gas
De la ecuacin general de los gases: P . V =
m
.R .T ,
Mm
teniendo en cuenta que la densidad es: d = m / V,
resulta:
es decir: P . M m =
m
.R .T
V
P . Mm = d . R . T
por lo que podremos determinar la densidad de un gas a partir de:
d=
P . Mm
R .T
3. LEY DE DALTON DE LAS PRESIONES PARCIALES
En una mezcla de gases en la que no se produce ninguna reaccin entre ellos, cada uno de los gases se
distribuye uniformemente a travs del recipiente y cada molcula se mueve independientemente de las
dems, es decir, del mismo modo que lo hara en ausencia de molculas de los otros gases. Por lo tanto, la
presin ejercida por cualquier gas de una mezcla es la misma que ejercera si el gas llenara por s solo el
recipiente. Esta presin es denominada presin parcial del gas.
En consecuencia: "La presin total ejercida por una mezcla gaseosa es igual a la suma de las
presiones parciales de los gases componentes de la mezcla".
P total = P1 + P2 + P3 + ...
Como la presin parcial de un gas es proporcional al nmero de moles de dicho gas ( y por tanto al
nmero de molculas) presentes en la mezcla: Pi = k . ni , sabiendo el valor de la presin total se puede
calcular la presin parcial de cada gas, si se conoce su composicin volumtrica o molecular.
Ejemplo: en la atmsfera el 78% de las molculas son de N2, el 21% son de O2 y el 1% de Ar. Si la
presin total es de 1,00 atm, el nitrgeno ejerce una presin parcial de 0,78 atm, el oxgeno 0,21 atm y el
argn 0,01 atm.
En general, para un gas, i, de la mezcla:
Pi = X i PT
n
, siendo X i ( fraccin molar ) = i
nT
La ecuacin de los gases ideales se le puede aplicar a la mezcla y a todos y cada uno de los gases de la mezcla.
As, por ejemplo, para el gas 2 se cumplir P2V = n2RT, siendo V el volumen total de la mezcla gaseosa.
En general, para el gas i, se cumplir PiV = niRT.
Para toda la mezcla: PT V = nT RT.
Si en una mezcla de gases se produce una reaccin entre sus componentes, para determinar la presin total
hay que tener en cuenta la estequiometra de la reaccin.
4.- INTERPRETACIN DE LAS LEYES DE LOS GASES POR LA TEORA CINTICA
El hecho de que haya grandes distancias entre las molculas de los gases y que las fuerzas
intermoleculares sean muy dbiles, despreciables, hace que las molculas sean independientes unas de otras,
por lo que las propiedades de los gases son independientes de la naturaleza de los mismos, es decir, todos los
gases se comportan del mismo modo. Por el contrario, en un slido o en un lquido, las propiedades
dependen de la intensidad de las fuerzas intermoleculares, as como del tamao y forma de las molculas.
a) Ley de Boyle-Mariotte ( P.V = cte , para m y T ctes):
Supongamos que tenemos una cierta masa de gas encerrada en
un recipiente cuya cubierta superior est provista de un mbolo
mvil. Al reducir el volumen a la mitad manteniendo constante la
temperatura, y por tanto las molculas movindose a la misma
velocidad, el nmero de colisiones por unidad de superficie que se
producirn contra las paredes del recipiente ser el doble, ya que
el espacio se ha reducido a la mitad. En consecuencia la presin
alcanzar un valor doble de la original.
b) Ley de Charles y Gay-Lussac ( V = cte . T , para m y P ctes):
Si tenemos una cierta masa de gas encerrada en
un recipiente provisto de un mbolo mvil a una
cierta temperatura, las molculas chocarn contra las
paredes del recipiente y el mbolo ejerciendo una
cierta presin que equilibra a la presin atmosfrica
exterior. Al calentar el gas, las partculas se mueven
ms deprisa, producindose un mayor nmero de
choques contra el mbolo, y por tanto, un aumento
de la presin interior que superar a la presin
atmosfrica exterior, lo que hace que el mbolo se
desplace con el consiguiente aumento de volumen..
Este aumento de volumen reduce el nmero de
colisiones contra el mbolo y por tanto se reduce la
presin interior. De esta forma, el desplazamiento
del mbolo tiene lugar hasta que la presin interior
vuelve a equilibrarse con la presin exterior. As
pues, a presin constante, el volumen aumenta
conforme lo hace la temperatura.
c) 2 Ley de Gay-Lussac ( P = cte . T , para m y V ctes)
Supongamos un recipiente de volumen constante que contiene una
cierta masa de gas. Al aumentar la temperatura aumenta la velocidad
de las molculas, producindose un mayor nmero de choques contra
las paredes del recipiente, lo que origina un aumento de la presin.
Cero absoluto de temperaturas (lmite inferior de temperaturas)
Al enfriar un gas la velocidad y la energa cintica media de sus molculas disminuye, por lo que debe
alcanzarse una temperatura a la cual la energa cintica y la velocidad se anulen. Lgicamente, no pueden
disminuirse ms all de este lmite, y sta debe ser la temperatura ms baja que puede alcanzarse ( cero
absoluto = 0 K ).
Potrebbero piacerti anche
- Resumen Reacciones Orgánica 2º BachillerDocumento4 pagineResumen Reacciones Orgánica 2º BachillerSaraGFNessuna valutazione finora
- Apuntes Filosofia 1º Oxford 2022Documento20 pagineApuntes Filosofia 1º Oxford 2022PatriciaNessuna valutazione finora
- Ejercicios Disoluciones 3º EsoDocumento2 pagineEjercicios Disoluciones 3º EsoMª Esperanza Rodrigo MaseroNessuna valutazione finora
- Unidad 1 3º Eso AlgaidaDocumento40 pagineUnidad 1 3º Eso AlgaidaAna Del MontecarmeloNessuna valutazione finora
- Repaso Tema 2Documento2 pagineRepaso Tema 2Sonsoles EncinarNessuna valutazione finora
- 03 Guia Didactica Enlace QuimicoDocumento34 pagine03 Guia Didactica Enlace QuimicoGerardo Carballido100% (1)
- Tema de DisolucionesDocumento7 pagineTema de DisolucionesMESA DOMÍNGUEZ ANANessuna valutazione finora
- Leyes de NewtonDocumento6 pagineLeyes de NewtonRodrigo Ignacio Bravo MuñozNessuna valutazione finora
- U07 SolucionarioDocumento25 pagineU07 SolucionarioSheyla Alamillo Calvillo100% (2)
- Tema 1 - El Trabajo Científico. Medidas de MagnitudesDocumento13 pagineTema 1 - El Trabajo Científico. Medidas de MagnitudesramoncinNessuna valutazione finora
- 2oBachCCSS EBAU Asturias 2021-Ordinaria Resuelto OficialDocumento9 pagine2oBachCCSS EBAU Asturias 2021-Ordinaria Resuelto OficialAntonioGonzalezNessuna valutazione finora
- 3ºeso-Aparatos Del CuerpoDocumento6 pagine3ºeso-Aparatos Del Cuerpocapi8081Nessuna valutazione finora
- Examen 4 Eso EnlaceDocumento2 pagineExamen 4 Eso EnlaceSara Maria Bello SalcedoNessuna valutazione finora
- Examen Numeros Reales SolucionadoDocumento2 pagineExamen Numeros Reales SolucionadocaadoiNessuna valutazione finora
- Problemas Disoluciones (Basicos)Documento1 paginaProblemas Disoluciones (Basicos)scoabueloNessuna valutazione finora
- Fuerzas en Fluidos. Física y Química de 4º de ESODocumento13 pagineFuerzas en Fluidos. Física y Química de 4º de ESOfrodríguez_30Nessuna valutazione finora
- Cálculo Concentraciones - t3 - fq3Documento3 pagineCálculo Concentraciones - t3 - fq3ramoncin100% (1)
- ComposiciondelamateriaDocumento5 pagineComposiciondelamateriaRemediosNessuna valutazione finora
- 28 Ejercicios Resueltos de Energhia Calo PDFDocumento27 pagine28 Ejercicios Resueltos de Energhia Calo PDFjuanchiNessuna valutazione finora
- Esquema RenacimientoDocumento3 pagineEsquema Renacimientoesquemacaste100% (1)
- Apuntes Presiones y Fuerzas Hidrostatica 4 ESO 2012Documento6 pagineApuntes Presiones y Fuerzas Hidrostatica 4 ESO 2012douglas3018362Nessuna valutazione finora
- Mat3esoacad Generador U12Documento17 pagineMat3esoacad Generador U12afnNessuna valutazione finora
- Actividades de Repaso de Física y QuímicaDocumento15 pagineActividades de Repaso de Física y QuímicaCarmen María López MartínezNessuna valutazione finora
- Enlace QuimicoDocumento8 pagineEnlace QuimicoCristhian Alexander Rafael BaylònNessuna valutazione finora
- Recopilacion Examenes fq1bchDocumento8 pagineRecopilacion Examenes fq1bchCarlos XabierNessuna valutazione finora
- 4º Eso Soluciones Actividades Tema 2Documento12 pagine4º Eso Soluciones Actividades Tema 2Paqui RodríguezNessuna valutazione finora
- Ejercicios de Formulación Orgánica 4º de Eso FormulaDocumento23 pagineEjercicios de Formulación Orgánica 4º de Eso FormulaSALMA SAKIOU0% (1)
- Química 3º Eso Pmar AnayaDocumento16 pagineQuímica 3º Eso Pmar AnayadanieldeagredagonzalezNessuna valutazione finora
- Tema 3 FQ 2c2ba EsoDocumento2 pagineTema 3 FQ 2c2ba EsoChristelledejour0% (1)
- EXAMEN DE LENGUA 3eso 2º 3 15junioDocumento1 paginaEXAMEN DE LENGUA 3eso 2º 3 15junioFernando Lamas Ferreiro100% (1)
- Examen de Función de Nutrición y Reproducción. 3º ESODocumento9 pagineExamen de Función de Nutrición y Reproducción. 3º ESOmetayosaNessuna valutazione finora
- Preguntas de SelectividadDocumento16 paginePreguntas de SelectividadjmgyuyuNessuna valutazione finora
- Fuerzas 4 EsoDocumento25 pagineFuerzas 4 EsolauramznNessuna valutazione finora
- Examen t3 Disoluciones 3 Eso CompletoDocumento1 paginaExamen t3 Disoluciones 3 Eso CompletoRo RamosNessuna valutazione finora
- Disoluciones 2 EsoDocumento1 paginaDisoluciones 2 EsoMarta YudegoNessuna valutazione finora
- Citología SelectividadDocumento8 pagineCitología Selectividadauladenaturales100% (1)
- 1º Perífrasis Verbales T y Act 3º EsoDocumento2 pagine1º Perífrasis Verbales T y Act 3º EsotxustoNessuna valutazione finora
- Tema 2 Dinamica 4 Eso Fisica y QuimicaDocumento15 pagineTema 2 Dinamica 4 Eso Fisica y QuimicafernandoNessuna valutazione finora
- Resumen UD 3 Elementos y Compuestos 3 ESO SantillanaDocumento4 pagineResumen UD 3 Elementos y Compuestos 3 ESO SantillanablueknowNessuna valutazione finora
- Semejanza y TrigonometriaDocumento7 pagineSemejanza y TrigonometriaCristyNessuna valutazione finora
- Refuerzo Fyq 2Documento84 pagineRefuerzo Fyq 2Jonathan Jurado BenitezNessuna valutazione finora
- 1617 - Comentario de Texto - Cohesión y CoherenciaDocumento6 pagine1617 - Comentario de Texto - Cohesión y CoherenciaSusana BonillaNessuna valutazione finora
- Fisica y Química, 4 ESO Santillana PDF Humedad TeoríaDocumento1 paginaFisica y Química, 4 ESO Santillana PDF Humedad TeoríaMaria Paulina Cuervo RamirezNessuna valutazione finora
- Tema 4-Biologia-4º EsoDocumento7 pagineTema 4-Biologia-4º EsoSergio Canales MuñozNessuna valutazione finora
- Resumen de Literatura 2 EsoDocumento4 pagineResumen de Literatura 2 EsoBelMar JJNessuna valutazione finora
- Tema 1 - El Trabajo CientíficoDocumento4 pagineTema 1 - El Trabajo CientíficoJuan Antonio Cabrera MartínezNessuna valutazione finora
- Soluciones Actividades 3 Eso Tema 3Documento10 pagineSoluciones Actividades 3 Eso Tema 3Lucre Fernández100% (1)
- Formulario Distribución Normal y BinomialDocumento1 paginaFormulario Distribución Normal y BinomialEstíbaliz Pérez SanabriaNessuna valutazione finora
- Tema2 Ejercicios Resueltos Dinamica Estudio de Las Fuerzas 4 EsoDocumento69 pagineTema2 Ejercicios Resueltos Dinamica Estudio de Las Fuerzas 4 Esoisabel moral ramaNessuna valutazione finora
- Ejercicios Concentraciones ResueltosDocumento6 pagineEjercicios Concentraciones ResueltosCarolina SalcedoNessuna valutazione finora
- Manual Formulación Inorgánica (3º ESO) PDFDocumento23 pagineManual Formulación Inorgánica (3º ESO) PDFMonica DenisaNessuna valutazione finora
- 02-Ejercicios de MovimientosDocumento3 pagine02-Ejercicios de MovimientosFernando Morián CaballeroNessuna valutazione finora
- Actividades de Fisica y Quimica 3 EsoDocumento19 pagineActividades de Fisica y Quimica 3 EsoMARIANANessuna valutazione finora
- TEMA 9. Dinámica. Fuerzas y Sus EfectosDocumento10 pagineTEMA 9. Dinámica. Fuerzas y Sus EfectosbeatrizNessuna valutazione finora
- GasesDocumento4 pagineGasesJesúsEnriqueGarciaNessuna valutazione finora
- Gases Química PDFDocumento8 pagineGases Química PDFMax ChazzNessuna valutazione finora
- Semana 13 - GasesDocumento26 pagineSemana 13 - GasesNadia AlfaroNessuna valutazione finora
- 02 - GasesDocumento6 pagine02 - GasesAnita Elizabeth Layza MendiolaNessuna valutazione finora
- Informe Quimica 5Documento17 pagineInforme Quimica 5Valeria DuharteNessuna valutazione finora
- Representación de FuncionesDocumento2 pagineRepresentación de Funcionesppeinado00Nessuna valutazione finora
- Ejercicios - Magnitudes y UnidadesDocumento3 pagineEjercicios - Magnitudes y Unidadesppeinado00Nessuna valutazione finora
- Ejercicios de Inecuaciones PDFDocumento1 paginaEjercicios de Inecuaciones PDFWagner Mas PecheNessuna valutazione finora
- Ejercicios de Inecuaciones PDFDocumento1 paginaEjercicios de Inecuaciones PDFWagner Mas PecheNessuna valutazione finora
- Calculadora EstadísticaDocumento3 pagineCalculadora Estadísticappeinado00Nessuna valutazione finora
- Ex - Ecuaciones y SistemasDocumento2 pagineEx - Ecuaciones y Sistemasppeinado00Nessuna valutazione finora
- Examen PolinomiosDocumento1 paginaExamen Polinomiosppeinado00Nessuna valutazione finora
- Ejercicios Derivadas PDFDocumento17 pagineEjercicios Derivadas PDFppeinado00Nessuna valutazione finora
- Los Cinco ReinosDocumento1 paginaLos Cinco Reinosppeinado00Nessuna valutazione finora
- Fijador MaquillajeDocumento2 pagineFijador Maquillajeppeinado00Nessuna valutazione finora
- Inecuaciones Con Valor AbsolutoDocumento1 paginaInecuaciones Con Valor Absolutoppeinado00Nessuna valutazione finora
- Inecuaciones Con Valor AbsolutoDocumento1 paginaInecuaciones Con Valor Absolutoppeinado00Nessuna valutazione finora
- Formulacion InorganicaDocumento18 pagineFormulacion Inorganicappeinado00Nessuna valutazione finora
- Resumen La MateriaDocumento6 pagineResumen La Materiappeinado00Nessuna valutazione finora
- Formulario CombinatoriaDocumento1 paginaFormulario CombinatoriaLuis ManuelNessuna valutazione finora
- Criterios de DivisibilidadDocumento3 pagineCriterios de Divisibilidadppeinado00Nessuna valutazione finora
- Calculadora EstadísticaDocumento4 pagineCalculadora Estadísticappeinado00Nessuna valutazione finora
- Resolucion Triangulos RectangulosDocumento4 pagineResolucion Triangulos Rectangulosppeinado00Nessuna valutazione finora
- Inferencia EstadísticaDocumento4 pagineInferencia Estadísticappeinado00Nessuna valutazione finora
- Los Cinco ReinosDocumento1 paginaLos Cinco Reinosppeinado00Nessuna valutazione finora
- Símbolos MatemáticosDocumento1 paginaSímbolos Matemáticosppeinado00Nessuna valutazione finora
- Calculadora EstadísticaDocumento4 pagineCalculadora Estadísticappeinado00Nessuna valutazione finora
- Criterios de DivisibilidadDocumento3 pagineCriterios de Divisibilidadppeinado00Nessuna valutazione finora
- Fisica Universitaria - CAP 28Documento2 pagineFisica Universitaria - CAP 28ppeinado00Nessuna valutazione finora
- Ejercicios CondensadoresDocumento4 pagineEjercicios Condensadoresppeinado00Nessuna valutazione finora
- Raices CuadradasDocumento7 pagineRaices Cuadradasppeinado00Nessuna valutazione finora
- Pag WebDocumento3 paginePag Webppeinado00Nessuna valutazione finora
- Componentes Intrinsecas de La AceleracionDocumento3 pagineComponentes Intrinsecas de La Aceleracionppeinado00Nessuna valutazione finora
- Ejercicios MASDocumento4 pagineEjercicios MASppeinado000% (1)
- Sistema TermodinamicoDocumento50 pagineSistema Termodinamicoflor torresNessuna valutazione finora
- CuestionarioDocumento165 pagineCuestionarioAlvarez Angeles LeonardoNessuna valutazione finora
- Ecuaciones de EstadoDocumento4 pagineEcuaciones de Estadoda1031soNessuna valutazione finora
- Tema 8 PresentacionDocumento32 pagineTema 8 PresentacionFlavio MontezaNessuna valutazione finora
- República Bolivariana de Venezuela EnsayoDocumento7 pagineRepública Bolivariana de Venezuela Ensayoronny alvillarNessuna valutazione finora
- Invtg11 Efecto Joule ThompsonDocumento9 pagineInvtg11 Efecto Joule ThompsonanakarenNessuna valutazione finora
- Quimica Cuantica de Solidos Unidad 5Documento67 pagineQuimica Cuantica de Solidos Unidad 5Cristhian Felipe Suarez MoreaNessuna valutazione finora
- 7 Equilibrio QuimicoDocumento43 pagine7 Equilibrio QuimicojustinaNessuna valutazione finora
- Configuraciones ElectrónicasDocumento6 pagineConfiguraciones ElectrónicasJazmina PintoNessuna valutazione finora
- Aplicaciones de La Energia InternaDocumento5 pagineAplicaciones de La Energia InternaDarwin Huillca DiazNessuna valutazione finora
- Ecuacion Butler Volmer DetallesDocumento3 pagineEcuacion Butler Volmer DetallesLibros ArgónNessuna valutazione finora
- Informe N°05 de Fisica IiDocumento16 pagineInforme N°05 de Fisica IiJemito :vNessuna valutazione finora
- Ciencias de La Tierra. Transferencia de Energia en La Atmosfera Terrestre. Andres Espinoza.5to Año ADocumento4 pagineCiencias de La Tierra. Transferencia de Energia en La Atmosfera Terrestre. Andres Espinoza.5to Año AJesus RinconNessuna valutazione finora
- Reacciones QuímicasDocumento6 pagineReacciones QuímicasEstefany Rosales SolanoNessuna valutazione finora
- Ingeniería Termodinámica: Sistemas de RefrigeraciónDocumento26 pagineIngeniería Termodinámica: Sistemas de RefrigeraciónJoss CazarNessuna valutazione finora
- Tipos de Reactores Químicos Con Sus CaracterísticasDocumento6 pagineTipos de Reactores Químicos Con Sus CaracterísticasTroyAllen100% (1)
- Cuestionario DESTILACIONDocumento5 pagineCuestionario DESTILACIONJuan Jose ClavijoNessuna valutazione finora
- Funciones Del Agua en La Preparación de AlimentosDocumento16 pagineFunciones Del Agua en La Preparación de AlimentosJhoncitoToniCorazonNessuna valutazione finora
- Gravimetria de VolatilizaciónDocumento12 pagineGravimetria de VolatilizaciónJonathan Vertel100% (1)
- Guia 1Documento14 pagineGuia 1pejeNessuna valutazione finora
- Curso Basico de Simulacion de Procesos Con Aspen Hysys PDFDocumento144 pagineCurso Basico de Simulacion de Procesos Con Aspen Hysys PDFLonny Logann Rojas SolisNessuna valutazione finora
- Ventilacion de Minas-Trabajo N°2Documento27 pagineVentilacion de Minas-Trabajo N°2BRYAN ALDAHIR GONZALES EDONESNessuna valutazione finora
- Resultado2 Conductividad EtanolDocumento13 pagineResultado2 Conductividad EtanolLiliana RodríguezNessuna valutazione finora
- Ejercicios de Fisicoquímica AndreaDocumento2 pagineEjercicios de Fisicoquímica AndreaAndrea NievesNessuna valutazione finora
- Practica 1Documento4 paginePractica 1Eduardo TrejoNessuna valutazione finora
- Diagramas Import-Com Global, S.ADocumento6 pagineDiagramas Import-Com Global, S.ADioskar VegaNessuna valutazione finora
- 5-Cef SB - Oxidos AcidosDocumento3 pagine5-Cef SB - Oxidos AcidosFranco VillarrealNessuna valutazione finora
- Prob. Resueltos - Diagramas de Fase - Aleaciones Binarias IsomórficasDocumento11 pagineProb. Resueltos - Diagramas de Fase - Aleaciones Binarias IsomórficasJoseph CujilemaNessuna valutazione finora
- CW19Documento23 pagineCW19Jess TellezNessuna valutazione finora
- Estudio de La Cinética de Las Capas BoruradasDocumento226 pagineEstudio de La Cinética de Las Capas BoruradasMarcela Barraza CádizNessuna valutazione finora