Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Determinación Del Porcentaje de Carbonato de Calcio Por Retrotitulación PDF
Caricato da
DanyiCardenasTitolo originale
Copyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Determinación Del Porcentaje de Carbonato de Calcio Por Retrotitulación PDF
Caricato da
DanyiCardenasCopyright:
Formati disponibili
LABORATORIO
DE
QUMICA
ANALTICA
Prctica
6.
Determinacin
del
porcentaje
de
carbonato
de
calcio
por
retrotitulacin
I.
Introduccin terica
SOLUBILIDAD
EN
AGUA,
los
carbonatos
son
insolubles
en
su
mayora,
excepto
los
del
primer
grupo
de
la
Tabla
Peridica
y
los
de
amonio;
por
lo
que
para
su
determinacin
se
emplea
un
mtodo
indirecto.
El
Carbonato
de
Calcio
(CaCO3)
se
disuelve
en
HCl
de
concentracin
conocida,
agregando
un
exceso
de
este
ltimo.
El
exceso
de
HCl
se
titula
con
una
base
fuerte
(NaOH),
tambin
de
concentracin
conocida.
La
reaccin
que
se
lleva
a
cabo
es:
CaCO3
+
2HCl
CaCl2
+
H2O
+
CO2
Se
reconoce
porque
produce
efervescencia
al
desprender
CO2
El
exceso
de
HCl
se
titula
con:
NaOH
HCl
+
NaOH
Na+
+
Cl-
+
H2O
A
este
tipo
de
titulacin
se
le
conoce
como:
titulacin
por
retroceso.
SELECCIN
DEL
INDICADOR,
en
esta
reaccin
el
punto
de
equivalencia
tiene
un
pH
=
7,
por
lo
que
el
indicador
adecuado
sera
el
azul
de
bromotimol
(cuyo
rango
de
6.0
a
7.6);
sin
embargo
se
usa
el
anaranjado
de
metilo
(3.2
a
4.4)
debido
al
rango
de
vire,
ya
que
de
esta
manera
se
evitan
errores
al
pasarse
de
volumen
durante
la
titulacin,
puesto
que
el
azul
de
bromotimol
reacciona
con
el
CO2
del
medio
cambiando
continuamente
el
pH
de
la
solucin
y
aparentando
no
llegar
nunca
al
punto
final
(el
color
cambia
constantemente
de
azul,
punto
final,
a
amarillo
y
viceversa).
Para
esta
determinacin
se
hace
necesario
manejar
bien
los
siguientes
conceptos:
GRAVIMETRA:
Es
la
parte
del
anlisis
cuantitativo
que
se
basa
en
la
determinacn
de
un
elemento
o
compuesto
por
la
formacin
de
un
producto
insoluble,
estable
y
fcil
de
pesar,
en
el
cual
intervenga
el
elemento
o
compuesto
a
analizar.
Todos
los
clculos
del
anlisis
gravimtrico
estn
basados
en
las
leyes
de
la
estequiometra.
LEYES
DE
LA
ESTEQUIOMETRA:
La
estequiometra
es
la
parte
de
la
Qumica
que
se
relaciona
con
las
proporciones
en
que
se
combinan
los
elementos
o
compuestos
en
las
reacciones.
Generalmente
se
expresan
los
resultados
en
trminos
de
porcentaje,
%:
!!
% = !100
!
Px<
W
Px
=
Peso
del
elemento
o
compuesto
de
inters
W
=
Peso
total
de
la
muestra
II. Objetivos
Al finalizar la prctica el alumno ser capaz de:
1. Aplicar experimentalmente la teora de la neutralizacin .
2. Identificar una titulacin y una retrotitulacin
III. Material y reactivos
1. 1 frasco Problema
2. 1 bureta de 50 mL
3. 1 matraces erlenmeyer de 250 mL
4. 1 Vaso de precipitados de 250 mL
5. 1 probeta de 50 mL (opcional)
6. 1 frasco lavador con agua destilada
7. 1 esptula pequea
8. 1 matraz aforado de 250 mL
9. Carbonato de calcio
10. Anaranjado de metilo
11. HCl 0.1 N
IV. Tcnica
general
PARA
DETERMINAR
EL
PORCENTAJE
DE
CARBONATO
DE
CALCIO
REQUISITO
Dejar
previamente
un
frasco
problema
perfectamente
limpio,
seco
y
rotulado
con
nombre
y
grupo,
para
poder
colocar
en
l
la
muestra
individual
de
carbonato
de
calcio
y
as
poder
desarrollar
la
presente
prctica.
El
alumno
que
no
deje
su
material,
automticamente
no
tendr
derecho
a
prctica,
SIN
EXCEPCIN.
Muestra:
carbonato
de
calcio
Indicador:
anaranjado
de
metilo
1. Se
entrega
a
cada
alumno
su
muestra
de
carbonato
de
calcio
insoluble
en
agua
y
contaminado
con
otras
sustancias,
en
diferentes
proporciones.
2. Lavar
adecuadamente
el
material
de
vidrio.
3. Numerar
tres
matraces
erlenmeyer.
4. Pesar
en
balanza
digital,
aprximadamente
0.5
g
de
muestra.
5. Vaciar
la
muestra
a
un
matraz
erlenmeyer
enjuagando
el
papel
encerado
con
agua
destilada.
6. Repetir
el
paso
4
y
5
dos
veces
ms.
7. Diluir
la
muestra,
hasta
que
se
haya
disuelto
totalmente,
agregando
con
la
bureta
50
mL
de
HCl
0.1
N.
8. Si
no
se
logra
la
total
dilucin
,
entonces
agregar
25
mL
ms.
9. Ajustar el volumen del matraz a 100 mL con agua destilada.
10. Agregar a cada matraz de 2 a 3 gotas de anaranjado de metilo, quedando la
solucin de color rojo.
11. Enjuagar la bureta con NaOH , 0.1N.
12. Llenar la bureta con NaOH 0.1N.
13. Poner un fondo blanco para colocar el matraz a titular.
14. Titular la solucin hasta obtener coloracin canela o desparezca la tonalidad
roja.
15. Leer en la bureta el volumen de NaOH utilizado y reportar. Efectuar la
operacin por triplicado.
NOTA: Tanto el NaOH como el HCl tienen una normalidad terica de 0.1 N; sin
embargo, para los clculos de la prctica deber considerarse el valor real,
reportado a travs de los propios estudiantes obtenido de un anlisis
estadstico previo y registrado en cada uno de los garrafones preparados en la
prctica # 2.
V. Cuestionario
1.
2.
3.
4.
Cmo sabes cuando una sustancia est disuelta?
Qu diferencia existe entre ajustar volumen y aforar?
Si te pasas de volumen al aforar qu debes hacer?
Por qu se considera que la determinacin del carbonato de calcio se
efecta por retroceso?
5. Por qu es necesario conocer el pH en el punto de equivalencia?
6. Cmo eliminas las burbujas de aire en la bureta?
7. Por qu enjuagas la bureta previamente con la solucin con la que despus
la vas a llenar para titular?
8. Cul es el indicador adecuado en el caso de la determinacin del
carbonato de calcio?
9. Por qu en la determinacin del CaCO3 usas el HCl y cul es la razn por la
que debes medirlo en la bureta?
10. Qu diferencia existe entre Ka y Kb?
11. A mayor Ka o Kb es mayor o menor la disociacin y por qu?
12. Qu es retrotitulacion?
Lic. Evert Mendoza Colina Msc.
Potrebbero piacerti anche
- Reactividad de carbonilos y aromáticosDocumento68 pagineReactividad de carbonilos y aromáticosEren GarciaNessuna valutazione finora
- PRÁCTICA 5 Sintesis de Complejos de CobaltoDocumento8 paginePRÁCTICA 5 Sintesis de Complejos de CobaltoMARIAM ANTHUANET PLAZO GELDRESNessuna valutazione finora
- Práctica 5 Volumetría de PrecipitaciónDocumento6 paginePráctica 5 Volumetría de PrecipitaciónAnahí FigueroaNessuna valutazione finora
- Práctica 6 - Titulación Por Retroseso, Factores de DiluciónDocumento5 paginePráctica 6 - Titulación Por Retroseso, Factores de Diluciónalbina vargasNessuna valutazione finora
- Aldehidos y Cetonas, Condensacion AldolicaDocumento9 pagineAldehidos y Cetonas, Condensacion AldolicaLiliana BuenoNessuna valutazione finora
- Determinación Del Contenido Carbonato de Calcio en Tabletas ComercialesDocumento14 pagineDeterminación Del Contenido Carbonato de Calcio en Tabletas ComercialesBender RodríguezNessuna valutazione finora
- Síntesis de aspirinaDocumento4 pagineSíntesis de aspirinaRubén Gonzalo UsnayoNessuna valutazione finora
- Determinar pureza carbonato sodioDocumento11 pagineDeterminar pureza carbonato sodioeduardoNessuna valutazione finora
- Determinación de Hierro LLDocumento2 pagineDeterminación de Hierro LLesli0% (1)
- 04 Tema4Documento17 pagine04 Tema4Rakel Martinez AlonsoNessuna valutazione finora
- Nomenclatura de AlcoholesDocumento9 pagineNomenclatura de AlcoholesCristian Edwin Machaca RamosNessuna valutazione finora
- Determinación de cobre con EDTADocumento4 pagineDeterminación de cobre con EDTADaniela IbarraNessuna valutazione finora
- Ejercicios de Espectroscopia de Uv VisDocumento2 pagineEjercicios de Espectroscopia de Uv VisJosé Iván Cardoso Salvador0% (1)
- Organometalica 1Documento19 pagineOrganometalica 1Kade CadeNessuna valutazione finora
- Ácido BenzoicoDocumento8 pagineÁcido BenzoicoMoises EstradaNessuna valutazione finora
- Práctica 7 Reaccion de CannizaroDocumento5 paginePráctica 7 Reaccion de CannizaroAnonymous PkNprTYjsQNessuna valutazione finora
- Aplicación Analítica de La IodimetríaDocumento4 pagineAplicación Analítica de La IodimetríaEvelyn Paguay Carrillo100% (1)
- SaponificaciónDocumento3 pagineSaponificacióndaniel de graciaNessuna valutazione finora
- Alcohol BencilicoDocumento3 pagineAlcohol BencilicoStoneNessuna valutazione finora
- 1,2 DihidropiridinaDocumento6 pagine1,2 DihidropiridinaDaniela IbarraNessuna valutazione finora
- Guia Glicinato de CobreDocumento2 pagineGuia Glicinato de CobreFreider CaicedoNessuna valutazione finora
- Preparacion de Un Coloide - Propiedades Clásicas.Documento7 paginePreparacion de Un Coloide - Propiedades Clásicas.omariluapNessuna valutazione finora
- INFORME Acido FormicoDocumento4 pagineINFORME Acido FormicoKamila MartinNessuna valutazione finora
- Materiales PDFDocumento20 pagineMateriales PDFSara NarváezNessuna valutazione finora
- Caracterización Complejos de CobreDocumento7 pagineCaracterización Complejos de CobrePili SarNessuna valutazione finora
- Fotorreducción de BenzofenonaDocumento9 pagineFotorreducción de BenzofenonaJuan Diego TrujilloNessuna valutazione finora
- Gravime. I.agr.20.Corregido ProblemaDocumento28 pagineGravime. I.agr.20.Corregido ProblemaDANIEL CHAVEZ MICHANessuna valutazione finora
- Práctica No 7, 8, 9,10Documento15 paginePráctica No 7, 8, 9,10Luis CVNessuna valutazione finora
- Info de La Sal de MohrDocumento4 pagineInfo de La Sal de MohrAlexandra LunaNessuna valutazione finora
- Practica 4 Complejos - de - CuDocumento6 paginePractica 4 Complejos - de - CuJoan GarcíaNessuna valutazione finora
- INFORME PRACTICA 3 CALOR DE DISOLUCION Y DE NEUTRALIZACION-comprimidoDocumento13 pagineINFORME PRACTICA 3 CALOR DE DISOLUCION Y DE NEUTRALIZACION-comprimidoDimar MontejoNessuna valutazione finora
- Identificacion de Muestra Problema Por Medio de Espectroscopia IrDocumento6 pagineIdentificacion de Muestra Problema Por Medio de Espectroscopia IrAbel de Jesús RiveraNessuna valutazione finora
- Practica 3 QO.Documento14 paginePractica 3 QO.mikke pereaNessuna valutazione finora
- Practica de LipidosDocumento5 paginePractica de LipidosEsther SoledadNessuna valutazione finora
- Espectrometría infrarroja: análisis químicoDocumento4 pagineEspectrometría infrarroja: análisis químicomary kely chambi choqueNessuna valutazione finora
- Determinación de CA en Piedra CalizaDocumento9 pagineDeterminación de CA en Piedra CalizaFransNicolasRomoGuerraNessuna valutazione finora
- Guia PL No 3. Determinación de AluminioDocumento4 pagineGuia PL No 3. Determinación de Aluminiofer100% (1)
- Quimica Analitica Practica 03Documento8 pagineQuimica Analitica Practica 03Meléndez Meléndez John CharlesNessuna valutazione finora
- Informe de Química Orgánica Ensayos Preliminares y Análisis ElementalDocumento6 pagineInforme de Química Orgánica Ensayos Preliminares y Análisis ElementalSebastian Carrillo RojasNessuna valutazione finora
- Informe Valoracion ConductimetricaDocumento4 pagineInforme Valoracion ConductimetricaAlex GonzálezNessuna valutazione finora
- Pruebas Generales de AlcoholesDocumento8 paginePruebas Generales de Alcoholesdario villamizarNessuna valutazione finora
- Espectro IR ParacetamolDocumento5 pagineEspectro IR ParacetamolAmairani Garcia MancillaNessuna valutazione finora
- Practica 11 OrganicaDocumento8 paginePractica 11 OrganicaChe Zambrano BadilloNessuna valutazione finora
- Centrum 11Documento3 pagineCentrum 11Roberto Andres Delgado MillanNessuna valutazione finora
- Practica 6Documento5 paginePractica 6miguelNessuna valutazione finora
- Informe #7 Valoraciones Por Formación de ComplejosDocumento5 pagineInforme #7 Valoraciones Por Formación de ComplejosLinaRodriguez0126Nessuna valutazione finora
- Practica de Determinacion de Vainillina.Documento6 paginePractica de Determinacion de Vainillina.JESUS ANTONIO VAZQUEZ ACOSTA0% (1)
- AnaliticaDocumento1 paginaAnaliticaSayuriNessuna valutazione finora
- Bioquimica Informe USCDocumento4 pagineBioquimica Informe USCDaniela Materon LunaNessuna valutazione finora
- Determinacion Gravimetrica de S Como SulfatoDocumento7 pagineDeterminacion Gravimetrica de S Como SulfatoBrayanZurdo100% (1)
- Presentacion Validacion MeloxicamDocumento95 paginePresentacion Validacion MeloxicamANGIE CAROLINA CAMBEROS RODRIGUEZNessuna valutazione finora
- Cuestionario Lab 7Documento3 pagineCuestionario Lab 7Elvis Cocho100% (1)
- Informe de VaporDocumento4 pagineInforme de Vaporsebastian canasNessuna valutazione finora
- ALCALIMETRIADocumento42 pagineALCALIMETRIASTEFHANY PAOLA MENDOZA HERNANDEZNessuna valutazione finora
- Previo - Polimerización de AldehídosDocumento8 paginePrevio - Polimerización de AldehídosKarla García100% (1)
- Calculo de La Concentración Del HCLDocumento4 pagineCalculo de La Concentración Del HCLMaycol AyalaNessuna valutazione finora
- Practica #4 Sintesis Del YodoformoDocumento3 paginePractica #4 Sintesis Del YodoformoGabriel ArturoNessuna valutazione finora
- Lab 2. Soluciones AmortiguadorasDocumento4 pagineLab 2. Soluciones AmortiguadorasRoger RamosNessuna valutazione finora
- Qan U1 A6 JeacDocumento8 pagineQan U1 A6 Jeacisrael_cassio_1Nessuna valutazione finora
- MARCO TEORICO Determinacion AlcalinidadDocumento14 pagineMARCO TEORICO Determinacion AlcalinidadRenzo DiazNessuna valutazione finora
- El Valor de La VidaDocumento10 pagineEl Valor de La VidaDanyiCardenasNessuna valutazione finora
- El Amor Empieza en Ti MismoDocumento8 pagineEl Amor Empieza en Ti MismoDanyiCardenasNessuna valutazione finora
- Guias 15 SeptiembreDocumento2 pagineGuias 15 SeptiembreDanyiCardenasNessuna valutazione finora
- Laboratorio de FisicaDocumento1 paginaLaboratorio de FisicaDanyiCardenasNessuna valutazione finora
- Guias de Laboratorio 1°Documento1 paginaGuias de Laboratorio 1°DanyiCardenasNessuna valutazione finora
- Nomenclatura InorganicaDocumento3 pagineNomenclatura InorganicaDanyiCardenasNessuna valutazione finora
- El HorlaDocumento33 pagineEl HorlaDanyiCardenasNessuna valutazione finora
- Descubre Tu VocaciónDocumento4 pagineDescubre Tu VocaciónDanyiCardenasNessuna valutazione finora
- Calendario Principiantes - GYM VIRTUALDocumento6 pagineCalendario Principiantes - GYM VIRTUALDanyiCardenasNessuna valutazione finora
- CN Grado05 03Documento60 pagineCN Grado05 03IgnacioF.FernandezPabaNessuna valutazione finora
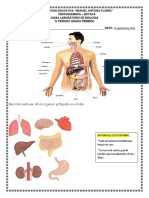
- Laboratorio de Biologia 3er PeriodoDocumento1 paginaLaboratorio de Biologia 3er PeriodoDanyiCardenasNessuna valutazione finora
- 8 y 9 SeptiembreDocumento2 pagine8 y 9 SeptiembreDanyiCardenasNessuna valutazione finora
- Crónica PeriodísticaDocumento4 pagineCrónica PeriodísticaDanyiCardenasNessuna valutazione finora
- 1° Luz SonidoDocumento62 pagine1° Luz SonidoDanyiCardenasNessuna valutazione finora
- Programacion Día Del Estudiante 2020Documento1 paginaProgramacion Día Del Estudiante 2020DanyiCardenasNessuna valutazione finora
- BIOLOGIADocumento2 pagineBIOLOGIADanyiCardenasNessuna valutazione finora
- Tejidos LauraDocumento1 paginaTejidos LauraDanyiCardenasNessuna valutazione finora
- ENTREGASDocumento1 paginaENTREGASDanyiCardenasNessuna valutazione finora
- Taller Reproduccion 2do PeriodoDocumento1 paginaTaller Reproduccion 2do PeriodoDanyiCardenasNessuna valutazione finora
- Taller Reproduccion 2do Periodo...Documento2 pagineTaller Reproduccion 2do Periodo...DanyiCardenasNessuna valutazione finora
- Aprendizajes Tercer Periodo Ciencias Naturales 5Documento1 paginaAprendizajes Tercer Periodo Ciencias Naturales 5DanyiCardenasNessuna valutazione finora
- Taller Cuarto Periodo CircuitosDocumento2 pagineTaller Cuarto Periodo CircuitosDanyiCardenasNessuna valutazione finora
- Joseph John Thomson, pionero del modelo atómicoDocumento20 pagineJoseph John Thomson, pionero del modelo atómicoDanyiCardenasNessuna valutazione finora
- La MateriaDocumento3 pagineLa MateriaDanyiCardenasNessuna valutazione finora
- Examen 5 GradoDocumento2 pagineExamen 5 GradoDanyiCardenasNessuna valutazione finora
- Ley de CharlesDocumento2 pagineLey de CharlesDanyiCardenasNessuna valutazione finora
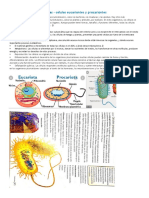
- CELULADocumento2 pagineCELULADanyiCardenasNessuna valutazione finora
- TextosExpositivosCaracterísticasEstructuraDocumento8 pagineTextosExpositivosCaracterísticasEstructuraDanyiCardenas100% (1)
- Evaluacion Sociales 2° 2 AprendizajeDocumento1 paginaEvaluacion Sociales 2° 2 AprendizajeDanyiCardenasNessuna valutazione finora
- Ley de Boyle y MariotteDocumento3 pagineLey de Boyle y MariotteDanyiCardenasNessuna valutazione finora
- Plan de Marketing Dulce VidaDocumento22 paginePlan de Marketing Dulce VidaHumberto Pacheco PanezNessuna valutazione finora
- Zonas EspecialesDocumento8 pagineZonas EspecialesJason PeredaNessuna valutazione finora
- Carta de Contestacion Sunat - GamboaDocumento2 pagineCarta de Contestacion Sunat - GamboaRafael Ruiz AsipaliNessuna valutazione finora
- Segmentación psicográfica y penetración de mercado para expansión de heladeríaDocumento5 pagineSegmentación psicográfica y penetración de mercado para expansión de heladeríaOmar parra100% (1)
- Servicio al cliente y marketingDocumento10 pagineServicio al cliente y marketing´angie vargas jerezNessuna valutazione finora
- Estado de Origen y Aplicacion de FondosDocumento26 pagineEstado de Origen y Aplicacion de Fondosabel aramis machado rodriguezNessuna valutazione finora
- El PerfumeDocumento219 pagineEl PerfumeNelson Eduardo Zuñiga Roco100% (1)
- Como Organizar Los Documentos y La Carpeta CADIVIDocumento12 pagineComo Organizar Los Documentos y La Carpeta CADIVIMaria Jose DelgadoNessuna valutazione finora
- Administracion de Operaciones Chase 2009 WordDocumento44 pagineAdministracion de Operaciones Chase 2009 WordLuci CastroNessuna valutazione finora
- (3042) +agosto+13+al+19+de+agosto+2011 +publicado+agosto+25+de+2011Documento1.277 pagine(3042) +agosto+13+al+19+de+agosto+2011 +publicado+agosto+25+de+2011Adolfo SoriaNessuna valutazione finora
- Libro Azul OnlineDocumento92 pagineLibro Azul OnlineEsau Rmz50% (4)
- Simulador Paso 3Documento24 pagineSimulador Paso 3Diego suarezNessuna valutazione finora
- Medida Cautelar Fuera de Proceso - LaboralDocumento5 pagineMedida Cautelar Fuera de Proceso - LaboralLelis Pilco GómezNessuna valutazione finora
- Analisis de Criticidad.-1Documento6 pagineAnalisis de Criticidad.-1Mj Mh100% (1)
- Eco Avanzada ProgramaDocumento3 pagineEco Avanzada ProgramawaitNessuna valutazione finora
- Control concurrencia bases datos relacionalesDocumento5 pagineControl concurrencia bases datos relacionalesbloodyroardNessuna valutazione finora
- AC-FT-007-Control de Dimensional - 03Documento1 paginaAC-FT-007-Control de Dimensional - 03Cesar Astorayme MarochoNessuna valutazione finora
- Resumen del libro El sistema de producción de ToyotaDocumento3 pagineResumen del libro El sistema de producción de ToyotaArnaldo Diaz50% (2)
- Introducción PriyectoDocumento3 pagineIntroducción PriyectoPatricia Felix MarroquinNessuna valutazione finora
- Las 4C del marketing: enfocarse en el clienteDocumento12 pagineLas 4C del marketing: enfocarse en el clienteJhair Jesus Donayre PacherresNessuna valutazione finora
- Promoción y comunicaciónDocumento13 paginePromoción y comunicaciónMary NebNessuna valutazione finora
- Descuento SimpleDocumento10 pagineDescuento SimpleZimplemente Rennizito AyalaNessuna valutazione finora
- Estrategia y Proyectos CEMENTO PACASMAYODocumento13 pagineEstrategia y Proyectos CEMENTO PACASMAYOJessica NievesNessuna valutazione finora
- Resumen Del Capitulo 3 Finazas y NegociosDocumento3 pagineResumen Del Capitulo 3 Finazas y Negocioskarlha coronado calderonNessuna valutazione finora
- The Fashion ChannelDocumento18 pagineThe Fashion ChannelEspañol Extranjeros0% (1)
- 04 AlquinosDocumento13 pagine04 AlquinosAbel ÇarrilloNessuna valutazione finora
- CIFDocumento28 pagineCIFjuan carlosNessuna valutazione finora
- Castro Meza Santiago E.E F.F 2Documento44 pagineCastro Meza Santiago E.E F.F 2Zantiago CM100% (3)
- Tarea OpampDocumento4 pagineTarea OpampferolonoNessuna valutazione finora
- Capacitacion Gestion CalidadDocumento40 pagineCapacitacion Gestion CalidadCAROLINANessuna valutazione finora
- Cómo hacer que te pasen cosas buenas: Entiende tu cerebro, gestiona tus emociones, mejora tu vidaDa EverandCómo hacer que te pasen cosas buenas: Entiende tu cerebro, gestiona tus emociones, mejora tu vidaValutazione: 5 su 5 stelle5/5 (1866)
- Batidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoDa EverandBatidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoValutazione: 5 su 5 stelle5/5 (2)
- ¿Por qué mis padres no me aman?: Empezando a sanarDa Everand¿Por qué mis padres no me aman?: Empezando a sanarValutazione: 4.5 su 5 stelle4.5/5 (33)
- Disciplina con amor para adolescentes (Discipline With Love for Adolescents): Guía para llevarte bien con tu adolescente (A Guide for Getting Along Well With Your Adolescent)Da EverandDisciplina con amor para adolescentes (Discipline With Love for Adolescents): Guía para llevarte bien con tu adolescente (A Guide for Getting Along Well With Your Adolescent)Valutazione: 5 su 5 stelle5/5 (10)
- La revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaDa EverandLa revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaValutazione: 5 su 5 stelle5/5 (200)
- Resetea tu mente. Descubre de lo que eres capazDa EverandResetea tu mente. Descubre de lo que eres capazValutazione: 5 su 5 stelle5/5 (196)
- El poder del optimismo: Herramientas para vivir de forma más positivaDa EverandEl poder del optimismo: Herramientas para vivir de forma más positivaValutazione: 4.5 su 5 stelle4.5/5 (15)
- Terapia cognitivo-conductual (TCC) y terapia dialéctico-conductual (TDC): Cómo la TCC, la TDC y la ACT pueden ayudarle a superar la ansiedad, la depresión, y los TOCSDa EverandTerapia cognitivo-conductual (TCC) y terapia dialéctico-conductual (TDC): Cómo la TCC, la TDC y la ACT pueden ayudarle a superar la ansiedad, la depresión, y los TOCSValutazione: 5 su 5 stelle5/5 (1)
- Tu cerebro emocional: Saca partido de lo que sientes y transforma tu vidaDa EverandTu cerebro emocional: Saca partido de lo que sientes y transforma tu vidaValutazione: 5 su 5 stelle5/5 (2)
- Psiconeuroinmunología para la práctica clínicaDa EverandPsiconeuroinmunología para la práctica clínicaValutazione: 5 su 5 stelle5/5 (4)
- No desperdicies tus emociones: Cómo lo que sientes te acerca a Dios y le da gloriaDa EverandNo desperdicies tus emociones: Cómo lo que sientes te acerca a Dios y le da gloriaValutazione: 4.5 su 5 stelle4.5/5 (11)
- Influencia. La psicología de la persuasiónDa EverandInfluencia. La psicología de la persuasiónValutazione: 4.5 su 5 stelle4.5/5 (14)
- Resumen de El Sutil Arte de que te Importe un Carajo, de Mark MansonDa EverandResumen de El Sutil Arte de que te Importe un Carajo, de Mark MansonValutazione: 4.5 su 5 stelle4.5/5 (15)
- Pensamiento Crítico: Utiliza modelos mentales para desarrollar tomas de decisiones efectivas y habilidades de resolución de problemas. Supera los obstáculos cognitivos y las falacias en los sistemas para pensar con claridad en tu vida cotidiana.Da EverandPensamiento Crítico: Utiliza modelos mentales para desarrollar tomas de decisiones efectivas y habilidades de resolución de problemas. Supera los obstáculos cognitivos y las falacias en los sistemas para pensar con claridad en tu vida cotidiana.Valutazione: 4.5 su 5 stelle4.5/5 (33)
- Maneja tus emociones: Curso intensivo de mindfulness y regulación emocionalDa EverandManeja tus emociones: Curso intensivo de mindfulness y regulación emocionalValutazione: 4.5 su 5 stelle4.5/5 (140)
- Disciplina Mental: Técnicas infalibles para lograr todo lo que te propones y eliminar la pereza y la procrastinación de tu vida para siempreDa EverandDisciplina Mental: Técnicas infalibles para lograr todo lo que te propones y eliminar la pereza y la procrastinación de tu vida para siempreValutazione: 5 su 5 stelle5/5 (3)
- Te odio - no me abandones: Comprender el trastorno límite de personalidadDa EverandTe odio - no me abandones: Comprender el trastorno límite de personalidadValutazione: 5 su 5 stelle5/5 (3)
- La conciencia en el cerebro: Descifrando el enigma de cómo el cerebro elabora nuestros pensamientosDa EverandLa conciencia en el cerebro: Descifrando el enigma de cómo el cerebro elabora nuestros pensamientosValutazione: 2.5 su 5 stelle2.5/5 (3)
- Cómo terminar lo que empiezas: El arte de perseverar, pasar a la acción, ejecutar los planes y tener disciplinaDa EverandCómo terminar lo que empiezas: El arte de perseverar, pasar a la acción, ejecutar los planes y tener disciplinaValutazione: 4.5 su 5 stelle4.5/5 (6)
- Reprogramando tu cerebro: Técnicas simples para vencer el miedo, la ansiedad y el pánico, mejora tu vida diaria aprovechando las bondades de la neuroplasticidadDa EverandReprogramando tu cerebro: Técnicas simples para vencer el miedo, la ansiedad y el pánico, mejora tu vida diaria aprovechando las bondades de la neuroplasticidadValutazione: 5 su 5 stelle5/5 (3)
- Interpretación del ECG: Una Guía Práctica e Intuitiva para Aprender a Leer el ECG y Diagnosticar y Tratar ArritmiasDa EverandInterpretación del ECG: Una Guía Práctica e Intuitiva para Aprender a Leer el ECG y Diagnosticar y Tratar ArritmiasNessuna valutazione finora
- Guía para superar los pensamientos atemorizantes, obsesivos o inquietantes: Libérate de los pensamientos negativos con la terapia cognitivo conductual (CBT)Da EverandGuía para superar los pensamientos atemorizantes, obsesivos o inquietantes: Libérate de los pensamientos negativos con la terapia cognitivo conductual (CBT)Valutazione: 4 su 5 stelle4/5 (24)
- Nunca fuimos modernos: Ensayos de antropología simétricaDa EverandNunca fuimos modernos: Ensayos de antropología simétricaNessuna valutazione finora
- Teoría polivagal práctica y terapiaDa EverandTeoría polivagal práctica y terapiaValutazione: 5 su 5 stelle5/5 (4)