Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Prueba de Diagnostico Fisica Quimica
Caricato da
QuimicaAndinoCopyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Prueba de Diagnostico Fisica Quimica
Caricato da
QuimicaAndinoCopyright:
Formati disponibili
GESTION PEDAGOGICA CURRICULAR
UNIDAD EDUCATIVA ANDINO
NOMBRE DEL ESTUDIANTE:
GRADO/CURSO:
FECHA:
SEGUNDO DE BACHILLERATO
PRUEBA DE DIANSTICO
REA:
ASIGNATURA:
DOCENTE:
PUNTAJE TOTAL
EVALUACIN:
MATEMTICA
FSICA-QUMICA
JUAN MORA
DE
LA
CALIFICACI
N
10
El cero absoluto equivale a: (0.25 puntos)
A. 0 kelvin.
B. 273 Kelvin.
C. 20 Celsius.
D. -273 Kelvin.
La presin se mide en: (0.25 puntos)
A. Kelvin
B. Atmsferas
C. mililitros
D. Coulombios
Cuando hablamos de CONDICIONES NORMALES podemos decir que: (0.25 puntos)
A. Cualquier cantidad de un gas ocupa un volumen de
A B C
22.4 litros.
B. La presin es de 1 atmsfera y la temperatura 0 Kelvin
C. La presin es de 1 Torr y la temperatura es de 273
Celsius
D. La presin es de 1 atmsfera y la temperatura de 0
Celsius
Podemos definir a una solucin qumica como: (0.25 puntos)
A. La combinacin de dos sustancias que reaccionan
qumicamente entre s.
B. La mezcla homognea entre 2 sustancias.
C. La mezcla heterognea entre 2 sustancias.
D. La obtencin de una sustancia cida
De los siguientes factores indique cul de ellos influye en la solubilidad de una sustancia: (0.25
puntos)
a) Temperatura
b) Humedad
c) Cantidad de luz
d) Cantidad de soluto
A. a y b
B. b y c
A B C D
C. c y d
D. b y d
La molaridad indica: (0.25 puntos) Escriba la ecuacin en el espacio en blanco
A. El nmero de moles de solvente que existe en un litro
A
de solucin
Versin: 01/05/2013
UEAR2-67
Pgina 1 de 4
GESTION PEDAGOGICA CURRICULAR
B. El nmero de moles de soluto que existe en un Kg de
solvente.
C. El nmero de moles de soluto que existe en un litro de
solucin
D. El nmero de equivalentes qumicos que existe en un
litro de solucin
La siguiente ecuacin se puede emplear para calcular: (0.25 puntos)
A.
B.
C.
D.
Molaridad.
%m/m.
Normalidad
%m/V
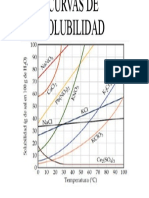
De acuerdo al siguiente grfico qu sustancia es ms soluble a 80C: (0.25 puntos)
A.
B.
C.
D.
Bromuro de sodio.
Bromuro de potasio
Nitrato de sodio
Sulfato de Cerio
Existen sustancias que, cuando se encuentran en solucin permiten el paso de corriente elctrica.
Dichas sustancias se conocen como: (0.25 puntos)
A. Electrolitos.
B. Electrones
A B C D
C. Amortiguadoras
D. Aislantes
Segn Arrhenius un cido es una sustancia: (0.25 puntos)
A.
B.
C.
D.
Capaz de liberar iones hidrgeno
Capaz de liberar iones OH
Que no tiene la capacidad de liberar iones
Producto de la reaccin entre un xido bsico y agua
Las sales halgenas se pueden formar cuando reacciona: (0.25 puntos)
A.
B.
C.
D.
xido bsico + agua
Hidrgeno + metal
cido hidrcido + hidrxido
cido oxocido + hidrxido
Versin: 01/05/2013
UEAR2-67
Pgina 2 de 4
GESTION PEDAGOGICA CURRICULAR
Las sales oxisales se pueden formar cuando reacciona: (0.25 puntos)
A.
B.
C.
D.
xido bsico + agua
Hidrgeno + metal
cido hidrcido + hidrxido
cido oxocido + hidrxido
A. Oxidacin
A B C
B. Igualacin
C. Balanceo
D. Reduccin
RESUELVA LOS SIGUIENTES EJERCICIOS: (REALICE EL PROCEDIMIENTO EN EL
ESPACIO EN BLANCO
Identifique cul de los siguientes compuestos es un hidrxido o base: (0.25 puntos)
A.
B.
C.
D.
CuO
NaOH
HCl
H2SO4
Identifique cul de los siguientes compuestos es un cido oxocido (0.25 puntos)
A.
B.
C.
D.
CaO
HNO3
KOH
HF
Identifique cul de los siguientes compuestos es una sal halgena (0.25 puntos)
A.
B.
C.
D.
KBr
CaNO3
KOH
KMnO4
Identifique cul de los siguientes compuestos es una sal oxisal (0.25 puntos)
A.
B.
C.
D.
H2S
AgNO3
BaCl2
HClO3
En la siguiente ecuacin, qu proceso experimenta el nitrgeno:
HNO3 + HI -----> NO + I2 + H2O
Cul ser la molaridad y la normalidad de una solucin de H 2SO4 cuyo volumen es de 400 ml si se
conoce que la densidad de dicha solucin es de 1,3 g/ml y tiene una concentracin de 10%m/m:
A
Versin: 01/05/2013
UEAR2-67
Pgina 3 de 4
GESTION PEDAGOGICA CURRICULAR
A)
B)
C)
D)
M
M
M
M
=
=
=
=
1.3
1.5
2.4
3.4
N
N
N
N
=
=
=
=
2.6
1.5
1.2
6.8
COMPLETE LAS SIGUIENTES ECUACIONES Y ESCRIBA EL NOMBRE DE LA SAL
RESULTANTE
Ca(OH)2 + HCl
____________ + ________________
______________________
Au(OH)3 + H2Se
____________ + ________________
______________________
COMPLETE LAS SIGUIENTES ECUACIONES Y ESCRIBA EL NOMBRE DE LA SAL
RESULTANTE
Cu(OH)2 + H2SO4
____________ + ________________
______________________
Cr(OH)3 + H4Sb2O5
____________ + ________________
______________________
Complete la siguiente ecuacin qumica empleando el mtodo de igualacin de oxido-reduccin
___H2SO4 + ___Cu
Versin: 01/05/2013
UEAR2-67
___CuSO4 + ___SO2 + ___H2O
Pgina 4 de 4
Potrebbero piacerti anche
- Cuestionario Primer Quimestre #1 Química 2doDocumento11 pagineCuestionario Primer Quimestre #1 Química 2doMauro MuñozNessuna valutazione finora
- TAREA#1Documento3 pagineTAREA#1Roberth Intriago CedeñoNessuna valutazione finora
- Practica QuímicaDocumento15 paginePractica Químicaheidi monestelNessuna valutazione finora
- Plan Anual Tercero Bgu 1Documento23 paginePlan Anual Tercero Bgu 1Carlos Oswaldo García Paredes100% (1)
- Taller de DisolucionesDocumento3 pagineTaller de DisolucionesAndrea GomezNessuna valutazione finora
- Preguntas para Reflexionar y ResponderDocumento6 paginePreguntas para Reflexionar y Responderalberto diazNessuna valutazione finora
- Actividades para El Examen RemedialDocumento10 pagineActividades para El Examen RemedialAnonymous B24Yz6gANessuna valutazione finora
- EXAMEN 3ros Quimica 2019 - 2020Documento4 pagineEXAMEN 3ros Quimica 2019 - 2020Jorge AuquillaNessuna valutazione finora
- Diagnostico de Fisica InicioDocumento3 pagineDiagnostico de Fisica InicioEder ChingaNessuna valutazione finora
- Planificación Por Unidad de Aprendizaje 1Documento2 paginePlanificación Por Unidad de Aprendizaje 1Marcelo MonjeNessuna valutazione finora
- PLANIFICACIÓN SEMANAL 2do BGUDocumento3 paginePLANIFICACIÓN SEMANAL 2do BGUXimena AgilaNessuna valutazione finora
- Guia N 1 Taller Acidos Bases y SalesDocumento3 pagineGuia N 1 Taller Acidos Bases y SalesMaria Catalina Arcos RátivaNessuna valutazione finora
- Actividad 3ero de Bachillerato QuimicaDocumento3 pagineActividad 3ero de Bachillerato Quimicamanuel villafuerteNessuna valutazione finora
- 5 Concentracion FisicasDocumento1 pagina5 Concentracion FisicasCamilo SanabriaNessuna valutazione finora
- Planeacion Didactica Ciencias Bloque 4 Secuencia 20Documento2 paginePlaneacion Didactica Ciencias Bloque 4 Secuencia 20bernardo rubioNessuna valutazione finora
- Taller BiomoleculasDocumento7 pagineTaller BiomoleculasMarta FuentesNessuna valutazione finora
- Evaluaciones Ciencias Naturales II QuimestreDocumento17 pagineEvaluaciones Ciencias Naturales II QuimestreAlex ORDOÑEZNessuna valutazione finora
- Química Básica Numeros Cuanticos PDFDocumento69 pagineQuímica Básica Numeros Cuanticos PDFJOHANNessuna valutazione finora
- Proyecto N 4 Quimica - 1ro de BachilleratoDocumento10 pagineProyecto N 4 Quimica - 1ro de BachilleratoOdalis TobarNessuna valutazione finora
- Expansion Fondo OceánicoDocumento2 pagineExpansion Fondo Oceánicomersanfer100% (2)
- EVALUACIÓN DIAGNÓSTICO CBTis 3Documento5 pagineEVALUACIÓN DIAGNÓSTICO CBTis 3Eder ZarateNessuna valutazione finora
- Mper - 101839 - Plan de Nivelación - Química - Grado 10°Documento4 pagineMper - 101839 - Plan de Nivelación - Química - Grado 10°Alex G'a100% (1)
- Banco de Preguntas QuimicaDocumento32 pagineBanco de Preguntas Quimicajhandry quiñonezNessuna valutazione finora
- Prueba de NomenclaturaDocumento2 paginePrueba de NomenclaturaRoqueNessuna valutazione finora
- Taller N°2 - Concepto de Mol y Número de AvogadroDocumento6 pagineTaller N°2 - Concepto de Mol y Número de AvogadroMiriam ArriagadaNessuna valutazione finora
- Practica Anhidridos 2012Documento4 paginePractica Anhidridos 2012Reynaldo Pizarro0% (1)
- Prueba de Diagnostico Noveno 2022)Documento3 paginePrueba de Diagnostico Noveno 2022)Sonia ArguelloNessuna valutazione finora
- Examen de Grado Tercero Bgu BiologíaDocumento8 pagineExamen de Grado Tercero Bgu BiologíaCristian PomaNessuna valutazione finora
- Guia QuimicaDocumento20 pagineGuia Quimicali_t23Nessuna valutazione finora
- Ejercicio de Preparación de Examen .Quim Organica Parte A Sin Respuestas PDFDocumento7 pagineEjercicio de Preparación de Examen .Quim Organica Parte A Sin Respuestas PDFMarisol Gonsalez GarzonNessuna valutazione finora
- CUESTIONARIO - Quimica Inorganica - 1er Año de Bachillerato - Tercer Parcial - IntensivoDocumento3 pagineCUESTIONARIO - Quimica Inorganica - 1er Año de Bachillerato - Tercer Parcial - IntensivoGermán Suárez100% (1)
- Programa Instruccional Ciencias IntegradasDocumento7 paginePrograma Instruccional Ciencias IntegradasFaviolaNessuna valutazione finora
- Cuestionario de QuímicaDocumento11 pagineCuestionario de QuímicaWilsom RomeroNessuna valutazione finora
- Examen Acumulativo Química 1 Periodo PDFDocumento3 pagineExamen Acumulativo Química 1 Periodo PDFAna BorjaNessuna valutazione finora
- Guia de Trabajo Independiente Ciclo de KrebsDocumento2 pagineGuia de Trabajo Independiente Ciclo de KrebsDiego Carlos Perez VanstrahlenNessuna valutazione finora
- Quimica Enlace Quc3admicoDocumento2 pagineQuimica Enlace Quc3admicoAlejandro AlejandroNessuna valutazione finora
- Taller Acidos CarboxilicosDocumento1 paginaTaller Acidos CarboxilicosQuimica SherwoodNessuna valutazione finora
- Actividades Sobre Los Organos de Los SentidosDocumento3 pagineActividades Sobre Los Organos de Los SentidosKleber DccNessuna valutazione finora
- 1.taller Nro 10 DE CIENCIAS NATURALESDocumento6 pagine1.taller Nro 10 DE CIENCIAS NATURALESjenniferNessuna valutazione finora
- Igualacion Ion ElectronDocumento6 pagineIgualacion Ion Electronsissy vargas merloNessuna valutazione finora
- Plan de Clases Tabla PeriodicaDocumento5 paginePlan de Clases Tabla Periodicaximena rodriguez cadenaNessuna valutazione finora
- 1ro BGU QUIMICA EVALUACION DIAGNOSTICADocumento3 pagine1ro BGU QUIMICA EVALUACION DIAGNOSTICADalila DelgadoNessuna valutazione finora
- Plan Clase Quimica 2Documento12 paginePlan Clase Quimica 2Lizzy HeartlyNessuna valutazione finora
- Plan Unidad Biologia 1Documento12 paginePlan Unidad Biologia 1Yolanda CarrilloNessuna valutazione finora
- Guia de Aprendizaje 1. Soluciones QuimicasDocumento6 pagineGuia de Aprendizaje 1. Soluciones QuimicasPEUBEPE JAJAJANessuna valutazione finora
- GUÍA 2 Química 2do BGUDocumento14 pagineGUÍA 2 Química 2do BGUbyit s5100% (1)
- Evaluacion de Fisica Electromagnetismo e ImanDocumento1 paginaEvaluacion de Fisica Electromagnetismo e ImanPalmar Con sentido de PertenenciaNessuna valutazione finora
- GUIA DE APRENDIZAJE N°9 CIENCIAS NATURALES Word PDFDocumento2 pagineGUIA DE APRENDIZAJE N°9 CIENCIAS NATURALES Word PDFCristina Ripoll0% (1)
- Pca OctavosDocumento7 paginePca OctavosPaco RoblesNessuna valutazione finora
- Examen-1° QUIMESTRE - 3°BGU-QUIMICADocumento3 pagineExamen-1° QUIMESTRE - 3°BGU-QUIMICAsisa tenelema100% (1)
- Quincena 7Documento29 pagineQuincena 7william BarreraNessuna valutazione finora
- Imprimir Sopa de Letras - Hibridación Del Carbono (11º Secundaria - Quimica - Hibridación - Hibridacion Del Carbono - Tetraédrica)Documento2 pagineImprimir Sopa de Letras - Hibridación Del Carbono (11º Secundaria - Quimica - Hibridación - Hibridacion Del Carbono - Tetraédrica)Gerardo GonzalezNessuna valutazione finora
- EJERCICIOS PROPUESTOS Compuestos Carbonilicos 2016-IIDocumento2 pagineEJERCICIOS PROPUESTOS Compuestos Carbonilicos 2016-IIAfir MinayaNessuna valutazione finora
- ExamenDocumento7 pagineExamenCarlos LopezNessuna valutazione finora
- Planificación Sem 4 Quimica 3 BguDocumento5 paginePlanificación Sem 4 Quimica 3 BguroynaNessuna valutazione finora
- Taller Reacciones Quimicas OrganicasDocumento1 paginaTaller Reacciones Quimicas OrganicasMaicol MedinaNessuna valutazione finora
- Bgu - Pca - 3 BiologíaDocumento14 pagineBgu - Pca - 3 BiologíaEvangelista Armando Peña100% (1)
- Quimica 2 Bgu Pca-Pud 6u PlusDocumento47 pagineQuimica 2 Bgu Pca-Pud 6u PlusShirley ChangNessuna valutazione finora
- 7 Ejercicios Acido Bases PDFDocumento8 pagine7 Ejercicios Acido Bases PDFDAYSI ECHEVERRIANessuna valutazione finora
- UntitledDocumento2 pagineUntitledQuimicaAndinoNessuna valutazione finora
- Guía ÓxidosDocumento2 pagineGuía ÓxidosQuimicaAndinoNessuna valutazione finora
- Ejercicio de Evaluación QUÍMICA 1er Quimestre 3 BGUDocumento2 pagineEjercicio de Evaluación QUÍMICA 1er Quimestre 3 BGUQuimicaAndinoNessuna valutazione finora
- Ejercicios Estequimetria Evaluación 3Documento1 paginaEjercicios Estequimetria Evaluación 3QuimicaAndinoNessuna valutazione finora
- Evaluacion Sumartiva Fisica Parcial 2Documento2 pagineEvaluacion Sumartiva Fisica Parcial 2QuimicaAndinoNessuna valutazione finora
- Guía HIDRUROS, HIDRÁCIDOS E HIDRÓXIDOSDocumento3 pagineGuía HIDRUROS, HIDRÁCIDOS E HIDRÓXIDOSQuimicaAndinoNessuna valutazione finora
- Hidrocarburos RevisiónDocumento1 paginaHidrocarburos RevisiónQuimicaAndinoNessuna valutazione finora
- HNO + Cu - Cu (NO) + No + H O: C. Estequiométricos Masa Molar No. de Moles Masa (Gramos) 60 70 20Documento1 paginaHNO + Cu - Cu (NO) + No + H O: C. Estequiométricos Masa Molar No. de Moles Masa (Gramos) 60 70 20QuimicaAndinoNessuna valutazione finora
- Evaluacion RedoxDocumento4 pagineEvaluacion RedoxQuimicaAndinoNessuna valutazione finora
- Ejercicios Estequimetria Evaluación 1Documento1 paginaEjercicios Estequimetria Evaluación 1QuimicaAndinoNessuna valutazione finora
- Formato Laboratorio Orgánica 5Documento2 pagineFormato Laboratorio Orgánica 5QuimicaAndinoNessuna valutazione finora
- Ejercicios de Aplicación Densidad 2Documento2 pagineEjercicios de Aplicación Densidad 2QuimicaAndinoNessuna valutazione finora
- Cds + Hno - CD (NO) + S + No + H O: C. Estequiometricos Masa Molar No. de Moles 0.35 Masa (Gramos)Documento1 paginaCds + Hno - CD (NO) + S + No + H O: C. Estequiometricos Masa Molar No. de Moles 0.35 Masa (Gramos)QuimicaAndinoNessuna valutazione finora
- Evaluacion Unidad 3 Quimica 1 BguDocumento2 pagineEvaluacion Unidad 3 Quimica 1 BguQuimicaAndinoNessuna valutazione finora
- Curvas de SolubilidadDocumento1 paginaCurvas de SolubilidadQuimicaAndinoNessuna valutazione finora
- Refuerzo Supletorio Semana 2Documento2 pagineRefuerzo Supletorio Semana 2QuimicaAndinoNessuna valutazione finora
- Equilibrio Químico Ejercicio 1Documento1 paginaEquilibrio Químico Ejercicio 1QuimicaAndinoNessuna valutazione finora
- Leyes de Gases 2Documento2 pagineLeyes de Gases 2QuimicaAndinoNessuna valutazione finora
- Primero Bachillerato PcaDocumento10 paginePrimero Bachillerato PcaQuimicaAndinoNessuna valutazione finora
- Organizador ProyectoDocumento1 paginaOrganizador ProyectoQuimicaAndinoNessuna valutazione finora
- Taller Individual Aparato Digestivo (Anatomia y Fisiologia)Documento3 pagineTaller Individual Aparato Digestivo (Anatomia y Fisiologia)QuimicaAndino100% (3)
- FISICA2Documento2 pagineFISICA2QuimicaAndino50% (2)
- Trabajo Examen Remedial Primero BachDocumento1 paginaTrabajo Examen Remedial Primero BachQuimicaAndinoNessuna valutazione finora
- Taller Individual Aparato Urinario (Anatomia y Fisiologia)Documento2 pagineTaller Individual Aparato Urinario (Anatomia y Fisiologia)QuimicaAndinoNessuna valutazione finora
- Segundo Bachillerato Pca FisicaDocumento12 pagineSegundo Bachillerato Pca FisicaQuimicaAndinoNessuna valutazione finora
- Preguntas Semiabiertas TomaÌ S de AquinoDocumento2 paginePreguntas Semiabiertas TomaÌ S de AquinoSonia Nieto ConesaNessuna valutazione finora
- Bobina de TeslaDocumento7 pagineBobina de TeslaEdgar LemaNessuna valutazione finora
- Epistemologia de La Bibliotecología5 - 230817 - 211112Documento10 pagineEpistemologia de La Bibliotecología5 - 230817 - 211112Denise SanabriaNessuna valutazione finora
- Curso H2 Verde - Dia 1 - Producción de H2Documento59 pagineCurso H2 Verde - Dia 1 - Producción de H2Francisco Ignacio Soto VergaraNessuna valutazione finora
- Aplicación de Lenguajes de Programacion y PlanosDocumento12 pagineAplicación de Lenguajes de Programacion y PlanosGonzalo SepulvedaNessuna valutazione finora
- Barrantes ObjetivosDocumento7 pagineBarrantes ObjetivosCarla EscobarNessuna valutazione finora
- Problemas de TermodinamicaDocumento5 pagineProblemas de TermodinamicayisiNessuna valutazione finora
- Cap 5 - Valor PresenteDocumento12 pagineCap 5 - Valor PresenteLaura Alejandra GutierrezNessuna valutazione finora
- Guía de TP-Energia-Prof. Carlos Cruz - 2023Documento2 pagineGuía de TP-Energia-Prof. Carlos Cruz - 2023Tupac 2006Nessuna valutazione finora
- La Formación de Rocas y Suelos en ColombiaDocumento14 pagineLa Formación de Rocas y Suelos en ColombiaThe FlowercatNessuna valutazione finora
- 844ER 742242 RevC ES PDFDocumento22 pagine844ER 742242 RevC ES PDFManuel Pezoa LacomaNessuna valutazione finora
- Filtro Hodrick & PrescottDocumento36 pagineFiltro Hodrick & PrescottPablo CosarNessuna valutazione finora
- Física de Semiconductores UNAMDocumento4 pagineFísica de Semiconductores UNAMFranyer Guillen100% (1)
- Volumen II-5 GeofisícaDocumento46 pagineVolumen II-5 GeofisícaMayane ArelyNessuna valutazione finora
- Unidad I. Pre CalculoDocumento10 pagineUnidad I. Pre CalculomarioinsturainrNessuna valutazione finora
- Marco Teórico de Gestión Por ProcesosDocumento13 pagineMarco Teórico de Gestión Por Procesosmauryca2003Nessuna valutazione finora
- La Importancia Del Análisis Descriptivo en Los Proyectos de InvestigaciónDocumento8 pagineLa Importancia Del Análisis Descriptivo en Los Proyectos de InvestigaciónalextcNessuna valutazione finora
- Metodos de Solucion de ProblemasDocumento9 pagineMetodos de Solucion de ProblemasAdan ZuñigaNessuna valutazione finora
- METODOLOGIADocumento59 pagineMETODOLOGIAAprendiz Elyon YirehNessuna valutazione finora
- UDocumento2 pagineURandyNessuna valutazione finora
- Ciclos RankineDocumento6 pagineCiclos RankineJaazania DiazNessuna valutazione finora
- Arquitectura de SoftwareDocumento11 pagineArquitectura de SoftwareFalex McNessuna valutazione finora
- Tarea 5 de EstadisticaDocumento7 pagineTarea 5 de Estadisticarosanna jaquezNessuna valutazione finora
- Soluciones Reales e IdealesDocumento3 pagineSoluciones Reales e IdealesLiss Encalada50% (2)
- Practica 1 PLCDocumento12 paginePractica 1 PLCErian Alexander Vega PiñonNessuna valutazione finora
- Esterilizacion de CristaleriaDocumento3 pagineEsterilizacion de CristaleriaYesse MaldonadoNessuna valutazione finora
- Derivadas Parciales 2012 4 PDFDocumento35 pagineDerivadas Parciales 2012 4 PDFcxhxb777Nessuna valutazione finora
- TP2 - EnunciadoDocumento3 pagineTP2 - EnunciadoSistemasutnNessuna valutazione finora
- Trabajo Prensa Hidraulica 2Documento5 pagineTrabajo Prensa Hidraulica 2Alex Patricio Avendaño VargasNessuna valutazione finora
- 2º Guia Ejercicio MatematicaDocumento210 pagine2º Guia Ejercicio Matematicaerova44771093% (14)