Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Primera Convocatoria 12-13
Caricato da
José María MedianeroCopyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Primera Convocatoria 12-13
Caricato da
José María MedianeroCopyright:
Formati disponibili
Escuela Superior de Ingeniera de Sevilla
Dpto. Ingeniera Qumica y Ambiental
Qumica General. Grados Ingeniera Tecnologas Industriales y Qumica
Examen de Junio. Curso 2012-13
Apellidos_______________________________________________________________ Nombre________________________________________________
Cul de las siguientes configuraciones electrnicas es la del W:
[Kr] 6s2 5d4
[Xe] 6s2 5d4
[Kr] 5s2 4d4 3f14
X [Xe] 6s2 5d4 4f14
Escriba (suponiendo que se cumplen las tendencias generales de variacin de las propiedades peridicas) el smbolo del elemento:
Del cuarto periodo
Con mayor primer potencial de ionizacin
Con menor radio covalente-metlico
Kr
Del grupo 14
Con menor electronegatividad
Con mayor afinidad electrnica
Con mayor primer potencial de ionizacin
C
Pb
Con mayor radio covalente-metlico
Con menor primer potencial de ionizacin
[Kr] 4d10
Pb
C
Con mayor electronegatividad
Escriba (referidas al gas noble anterior) las configuraciones electrnicas del Iodo (I)
Como elemento neutro
Con configuracin de par inerte
[Kr] 5s2 4d10 5p5
Con config. de pseudo gas noble
Kr
Br
Con config. de gas noble
Indique el estado de oxidacin del elemento en negrita en los compuestos que se indican:
NO +2
K2MnO4 +6
H2O2 -1
Cr3(PO4)2
MnO2 +4
[Kr] 5s2 4d10
[Kr] 5s2 4d10 5p6 = [Xe]
+2
CaHAsO3
+3
Para llevar a cabo la reaccin 3 A + B 2 C
se introducen en un recipiente 60 moles de A y 30 moles de B. El reactivo limitante es A y el otro reactivo se encuentra en un exceso del 50 %
Si el rendimiento es del 60 % la cantidad de C formada es 24 moles, y los grados de conversin logrados son: de A 60 %; de B 40 %
El aire estequiomtrico para quemar un cierto combustible son 8 moles de aire/mol de combustible.
Si se opera con un 25% de exceso de aire calcule los moles introducidos por mol de combustible:
de O2 2,1
de N2
7,9
Conocidos los calores de formacin de H(g) (218 kJ/mol), Cl(g) (121 kJ/mol) y HCl(g) (-92 kJ/mol), determine:
Calor de reaccin de: H2(g) + Cl2(g) 2HCl(g)
Calor de formacin de H2(g) 0 kJ/mol
Energa de enlace H-Cl
Energa de enlace Cl-Cl 242 kJ/mol
-184 kJ/mol
431 kJ/mol
Para el agua Hvap = 44 kJ/mol. La diferencia entre los poderes calorficos superior e inferior, ambos en kJ/mol, del butano vale
544 = 220 kJ/mol
El cp de X(g) (PM:50 g/mol) vale 40 J/(molK). El calor necesario para calentar un kg de X(g) de 25 a 75C es 1000/50 moles 40/1000 kJ/(molK) 50 K = 40 kJ
Un recipiente (V=cte) contiene, a una cierta temperatura y a 20 atm, una mezcla de dos gases A y B en la que la fraccin molar del primero es 0,4. Calcule:
La presin parcial de A
0,420 = 8 atm
La presin en el recipiente tras extraer todo el A
Si se introduce un nmero de moles igual al que hay del gas A de un tercer gas C, calcule:
La presin parcial de A
8 atm
La presin en el recipiente
20 8 = 12 atm
20 + 8 = 28 atm
EH2 / EN2 1 (E slo depende de T)
Calcule la relacin entre la energa cintica de un mol de H2(g) (PM = 2) y un mol de N2(g) (PM = 28), ambos a 40C
Calcule la relacin entre las densidades (g/L), a las mismas p y T, de SO2(g) (PM: 64) y O2(g) (PM: 32)
=2
Seale los estados en los que se puede encontrar una sustancia: - A una presin mayor a la del punto triple
- A un presin menor que la del punto triple
X Slido
X Lquido
X Gaseoso
X Slido
Lquido
X Gaseoso
1 atm (por definicin)
Valor de la presin de vapor del agua a su temperatura de ebullicin normal
Una solucin ideal, a 300K, formada por 2 moles de A (pA= 1,2 atm) y 2 moles de B (pB= 0,8 atm) tiene una presin de vapor
0,51,2 + 0,50,8 = 1 atm
La fraccin molar de A en el vapor en equilibrio con dicha solucin vale: 0,6 y su presin parcial
0,51,2 = 0,6 atm
Las constantes molales ebulloscpica y crioscpica del agua valen 0,52 y 1,86 Kkg/mol, respectivamente.
Calcule para una solucin acuosa con 0,25 moles de AlCl3 (sal muy soluble) por litro de agua: m = 1
Temperatura de fusin 0 -1,86 = -1,86C Temp. de ebullicin:
El agua de un ro est en equilibrio con el aire, a p= 1 atm. Calcule, a 25C, la [O2] disuelta en el agua.
La constante de Henry para el sistema H2O-O2 vale, a 25C, 0,024 atmL de agua/mg O2
= 0, 21 atm
100+0,52 = 100,52C
[O2] = 0,221/0,024 = 8,75 mg/L
Las constantes de Henry (atm) de los sistemas agua-gas, a 25C, para los gases indicados son O2: 42590, H2: 70990, CO2: 1630
El orden de solubilidad de estos gases en agua es:
El orden del punto de ebullicin de las sustancias no polares He(l), O2(l), CCl4(l) y C20H42(l) es
Para que existan interacciones por puente de hidrgeno es necesario que en la molcula haya enlaces
CO2 > O2 > H2
C20H42(l) > CCl4(l) > O2(l) > He(l)
N-H, OH o FH
Escuela Superior de Ingeniera de Sevilla
Dpto. Ingeniera Qumica y Ambiental
Qumica General. Grados Ingeniera Tecnologas Industriales y Qumica
Examen de Junio. Curso 2012-13
Apellidos_______________________________________________________________ Nombre________________________________________________
4
El proceso 2SO2(g)+O2(g) 2SO3(g) tiene Hr = -197,8 kJ/mol y Sr= -188 J/(molK)
Calcule el valor de las constantes de equilibrio, a 298 K: K = ___7,1x1024__ y el de Kp __7,1x1024 atm-1___ y el de Kc__1,74x1026 L/mol___
Aumenta
Su constante de equilibrio, disminuye al aumentar la temperatura y
no cambia
Aumenta
disminuye al aumentar la presin
no cambia
(Tache lo que no proceda)
Si en un recipiente, a 298 K y 3 atm, hay el mismo nmero de moles de SO2, y SO3, Calcule el valor de:
Presin parcial de SO2_____1 atm_____ Cociente de reaccin, Q _1_
Gr _-141,78 kJ/mol____
Gr ____-141,78 kJ/mol __
Se dice que esta reaccin es espontnea (K>1) en el rango de temperaturas: ________0 - 1052 K_____________________
Sea la reaccin 2 A(g) B(g). Un recipiente de 1 m3, a 500K y 100 atm, est en equilibrio cuando contiene un nmero de moles de B que es 9 veces el de A.
Calcule el valor de la constante de equilibrio _____0,9_______
Si se ha partido de A puro, el grado de conversin alcanzado es___0,947___
Si se introduce un inerte, de modo que se duplica el nmero de moles totales en el recipiente, y se espera a que se alcance el equilibrio
Grado de conversin en el equilibrio____0,947_______
Presin en el recipiente_______200 atm___________
Los potenciales normales de reduccin de los pares Cu(s)/Cu2+ y Zn(s)/Zn2+ son 0,34 V y -0,76 V, respectivamente. Si se forma una pila con ambos pares, con
[Cu2+] = [Zn2+] = 1M, indique:
Notacin de la pila__Zn(s)/Zn2+
(ac) 1M // Cu2+ (ac) 2M/Cu(s)___________________
Especie que se oxida____Zn (s)_____Especie que se reduce___ Cu2+ (ac) _____
Potencial inicial de la pila_______1,1 V_____________
Potencial de la pila en el equilibrio_______0 V__________
Si el reactivo limitante es el Zn(s) del que hay 0,5 moles, la capacidad de la pila es
______26,8 _________ Ah
Un compuesto poco soluble MX2(s) [ MX2(s) 2X (ac) + M2+(ac) ] tiene una solubilidad en agua pura de 0,001 mol/L. Calcule
Kps ____4x10-9________________
Solubilidad en una solucin acuosa con [X] = 0,01 M__________4x10-5__________
Concentraciones en solucin cuando a 1 L de agua se le aaden 0,01 moles de MX2(s):
[X] ___0,002______________ [M2+] ______0,001_________
Concentraciones en solucin cuando a 1 L de agua se le aaden 0,0001 moles de MX2(s): [X] ___0,0002_________ [M2+] ___0,0001____________
Se conocen los valores de los productos de solubilidad de los siguientes compuestos: Ag3AsO4: 1,010-22, BiAsO4: 4,410-10 y Cd3(AsO4)2, 2,210-33
Determine los potenciales aceptores de los pares:
Ag3AsO4/Ag+___22_________
Ag3AsO4/AsO43____7,33_______
Una solucin acuosa contiene Ag+, Bi3+ y Cd2+, todos en concentracin 1M. Calcule el pAsO43lim (-log[AsO43]lim) que indica el lmite de existencia de
Ag3AsO4(s)___22_____________
BiAsO4(s)_____9,36____________
Cuando se va aadiendo AsO43 el orden de precipitacin es 1_
Cd3(AsO4)2(s) ____16,33________________
Ag3AsO4(s) __ 2 __ Cd3(AsO4)2(s) _ y 3___ BiAsO4(s) ___________
Cuando, en la solucin en equilibrio, la [AsO43]= 10-18 mol/L
La solucin est saturada en ___ Ag3AsO4(s)____ , _________________, ________________
y las concentraciones de cationes en solucin son [Ag+] ___0,046 ______
[Bi3+ ] ____1______ y [Cd2+] ___1_____
Escuela Superior de Ingeniera de Sevilla
Dpto. Ingeniera Qumica y Ambiental
Qumica General. Grados Ingeniera Tecnologas Industriales y Qumica
Examen de Junio. Curso 2012-13
Apellidos_______________________________________________________________ Nombre________________________________________________
Se queman, con aire, 1311 kg/h de un combustible con la siguiente composicin en peso: C: 77 % N: 2,8% H: 4,9% S: 1,8% Inertes: 13,5.
En los gases de combustin hay CO2, H2O y SO2, N2 y O2.
Las escorias (slidas) producidas contienen todos los inertes y carbono no quemado, siendo su composicin en peso: Inertes: 92%, C no quemado: 8%.
La temperatura de los gases de salida es 388C, y la presin parcial de oxgeno a la salida es de 0,02 atmsferas (supngase presin total constante de 1 atmsfera
en todo el proceso). Calcule
13859,6 kg/h
a) Caudal de aire estequiomtrico (kg/h)
1,5%
b) Porcentaje de carbono no quemado
c) Exceso de aire a la entrada (% sobre el estequiomtrico)
d) Caudal de gases de salida (m3/h)
11,3%
29937,2 m3/h
e) Concentracin de SO2 en los gases de salida (mg/m3)
1576,5 mg/m3
Pesos atmicos O=16; N=14; C=12; S=32; H=1.
6
La reaccin S(s) + R(g) 2T(g)
tiene Sr=0,040 kJ/molK (suponer que no vara con la T).y una constante de equilibrio, a 25C, K=1.
a) Calcule el valor de la constante de equilibrio a 288C
9,54
b) Calcule la presin total y el volumen que ha de tener un recipiente para que 7 moles de S, 3 moles de R y 8 moles de T estn en equilibrio a 25C.
0,51 atm
521,3 L
c) En un recipiente de 13 litros se introducen, a 25C, 7 moles de S, 3 moles de R y 8 moles de T y se deja que evolucionen hasta el equilibrio.
Calcule la presin total en el equilibrio.
14,85 atm
d) Una vez alcanzado el equilibrio en el apartado anterior, se retiran los slidos, se introducen 1,1 litros de agua y se agita hasta alcanzar el equilibrio gas-liquido.
Calcule la presin total en el equilibrio.
Datos:
Suponga que prcticamente todo el agua est en estado lquido. Densidad del agua = 990 kg/m3;
15,4 atm
Valores de las constantes de Henry: HT/H2O = 440 atmmol agua/mol R; HR/H2O = .
e) Calcule el tiempo necesario para que una sustancia A que se descompone segn la reaccin elemental: 2A B + C,
se reduzca a 1/10 y 1/40 de su concentracin inicial de 0,42 mol/L, sabiendo que necesita 183 s para pasar a de 0,42 a 0,21 mol/L.
1657 s
7137s
f) Identifique el orden de reaccin y calcule la constante de velocidad (indique unidades) de la reaccin 2A B, en funcin de los siguientes datos
t(segundos)
[A] (mol/L)
0
0,1
5
0,082
10
0,067
15
0,055
20
0,045
Orden 1
k
0,02 s-1
g) Por qu factor se multiplica la velocidad de reaccin de la sntesis de IH (g) , a 520K, cuando, aadiendo un catalizador, su energa de activacin se reduce de
170 a 70 kJ/mol
vc/vsc=1,111010
Escuela Superior de Ingeniera de Sevilla
Dpto. Ingeniera Qumica y Ambiental
Qumica General. Grados Ingeniera Tecnologas Industriales y Qumica
Examen de Junio. Curso 2012-13
Apellidos_______________________________________________________________ Nombre________________________________________________
I. Un recipiente de 5L, lleno inicialmente de aire a 20C y a la presin atmosfrica, se cierra y a continuacin se introducen en l 3L de agua, dejando que el aire
se sature de humedad. A continuacin se introduce CO2(g) hasta que la presin en el recipiente alcanza el valor de 5 atm, cuntos moles de CO2 se han introducido
en el sistema?
naire = PV/RT = 15/(0,082293) = 0,208 moles
0,206 moles
Al introducir 3 L de agua el volumen ocupado por el aire se reduce a 2 L: paire = 15/2 = 2,5 atm
Presin del vapor de agua: 18/760 =0,024 atm
Se introduce CO2 hasta que la presin es 5 atm: P = 5 = paire + pH2O + pCO2, i pCO2 = 2,48 atm
nCO2 = pCO2, i V/RT= 2,482/(0,082293) = 0,206 moles
Posteriormente se agita bien el recipiente, hasta que se alcanza el equilibrio.
Cul ser la presin parcial del CO2 en ese momento?
1,04 atm
De los 0,208 moles de CO2, z quedan en forma de gas y 0,208-z se disuelven
p = Hx :
z0,082293/2 = 1428,57 (0,208-z) / (3000/18) z = 0,0867 moles
pCO2, eq = 0,08670,082293/2 = 1,04 atm
3,56 atm
Cunto valdr la presin total?
P = paire+ pH2O + pCO2, eq = 2,5 +0,024 + 1,04 = 3,56 atm
II. A partir de los datos de las Tablas termoqumicas, determine la presin de vapor del n-hexano (en atm) a 25C
Hf, kJ/mol
S, J/(molK)
0,2 atm
n-C6H14(l) n-C6H14(g)
-198,6
-167,1
Hvap = 31,5 kJ/mol
295,9
388,4
Svap = 92,5 J/(molK)
Gr(298) = 31,5 29892,510-3 = -RTlnK = -8,31410-3298ln(pC6H14) pC6H14 = 0,2 atm
340,6 K
y calcule adems, la temperatura de ebullicin normal del n-hexano ( K).
ln(p2/p1) = - Hvap/R (1/T2 1/T1)
ln(0,2/1) = 31500/8,314(1/298 1/Teb) Teb = 340,6 K
III. Sabiendo que la presin de vapor, a 25C, del tolueno vale 30 mm de Hg y la del benceno 100 mm de Hg, determine para una mezcla lquida equimolecular de
benceno y tolueno con comportamiento ideal, la presin correspondiente a la primera de burbuja de vapor (en mm de Hg)
xT= xB= 0,5
pT = xTpT = 0,530 = 15 mm Hg
pB = xB pB = 0,5100 = 50 mm Hg
65 mm Hg
23,1% Tolueno y 76,9% Benceno
y la composicin (% v/v) de dicha burbuja
yT = pT/p = 15/65 = 0,231
pagua (20C) = 18 mmHg
p = pT + pB =
HCO2 en agua (20C) = 1428,57 molatm/atm
Escuela Superior de Ingeniera de Sevilla
Dpto. Ingeniera Qumica y Ambiental
Qumica General. Grados Ingeniera Tecnologas Industriales y Qumica
Examen de Junio. Curso 2012-13
Apellidos_______________________________________________________________ Nombre________________________________________________
3
I. Una disolucin 0,1 M de una sal sdica de un cido desconocido, NaX, tiene un pH de 8,5. Calcule la constante Ka de dicho cido.
[H+]
10-8,5
(10-14
1/0,1)1/2
K=
10-4
10-4
II.Se quiere preparar 1L de una disolucin tampn de pH = 8,5, mezclando una disolucin de NaY 0,1 M con una disolucin 0,1 M del cido, HY. Determine qu
volmenes de cada disolucin inicial (HY y NaY) hay que tomar. El par HY/Y tiene un potencial aceptor de 8
xL
(1-x) L
Solucin deHY
241
mL
Solucin de NaY
760
mL
Y 0,1 M
HY 0,1 M
[H+] = 10-8,5 = 10-8 (1-x)/x
x = 0,76 L
EN CADA UNO DE LOS APARTADOS I y II REPRESENTE EL DIAGRAMA DE INTERVALOS DE PREDOMINIO CORRESPONDIENTE
III. Se aaden 0,3 moles de Zn(s) a 1 L de una disolucin de MnO4- 0,1M. Represente el diagrama de intervalos de predominio, indique las especies predominantes
cuando se alcance el equilibrio, y calcule el potencial (V) de la disolucin y las concentraciones de TODAS las especies.
E (Zn2+/Zn(s) = -0,763V,
E (MnO4-/ Mn2+) = 1,51 V
E -0,78V
Zn (s)
0,3 mol
MnO4- 1 L 0,1 M 0,1 mol
PA = -12,93
PA = 25,59
Semirreacciones
MnO4- + 8 H+ + 5 electrones Mn2+ + 4 H2O
Zn (s) Zn2+ (ac) + 2 electrones
Reaccin global
5 Zn (s) + 2 MnO4- 2 Mn2+ + 5 Zn2+ (ac)
i 0,3
0,1
r 0,25
0,1
0,1
0,25
f 0,05
0
0,1
0,25
Zn(s) = 0,05
[Zn2+] = 0,25
[MnO4] = 10-62
[Mn2+] = 0,1
[e] = (10-(-12,932) 1/0,25)1/2 = 1013,23
pe = -13,23
E = -0,78 V
10-25,595 = [MnO4- ][e]5/[Mn2+]
[MnO4- ] = 10-62 M
Escuela Superior de Ingeniera de Sevilla
Dpto. Ingeniera Qumica y Ambiental
Qumica General. Grados Ingeniera Tecnologas Industriales y Qumica
Examen de Junio. Curso 2012-13
Apellidos_______________________________________________________________ Nombre________________________________________________
Formular
1) cido nitroso
HNO2
PbI4
2) Yoduro plumbico
3) Bisulfato sdico
NaHSO4
4) Anhdrido perclrico
Ca(OH)2
5) Hidrxido clcico
6) Bromito de litio
Cl2O7
LiBrO2
7) Perxido de plata
Ag2O2
8) Permanganato de potasio
KMnO4
Nombrar
16)
CaO
xido de calcio
17)
H2CO3
cido carbnico
18)
MgSiO3
Silicato de magnesio
19)
(NH4)2SO4.
Sulfato amnico
20)
CrBr3
Bromuro crmico
21)
Br2O
Anhidrido hipobromoso
22)
AlH3
Hidruro de aluminio
23)
Cd(OH)2
Hidrxido de cadmio
24)
AgMnO4
Permanganato potsico
25)
NH3
Amoniaco
26)
CH3-CH2-COOH
cido propanoico
27)
CHC-CCH
Butadiino
28)
CH3CN
Etanonitrilo
Benceno
29)
30)
-OH
Fenol
9) cido fosfrico
H3PO4
10) In mercrico
Hg2+
11) Propanona
12) Formaldehdo
CH3COCH3
HCHO
13) Benzoato de metilo
C6H5COOCH3
14) Dimetileter.
CH3OCH3
15) Metilamina
CH3NH2
Potrebbero piacerti anche
- CatálogoDocumento48 pagineCatálogoJosé María MedianeroNessuna valutazione finora
- Elementos de SujeciónDocumento15 pagineElementos de SujeciónJosé María MedianeroNessuna valutazione finora
- Prontuario Perfiles Arcelor MittalDocumento34 pagineProntuario Perfiles Arcelor MittalJosé María MedianeroNessuna valutazione finora
- Cuotas Colegio IngenierosDocumento1 paginaCuotas Colegio IngenierosJosé María MedianeroNessuna valutazione finora
- V LvulasDocumento8 pagineV LvulasJosé María MedianeroNessuna valutazione finora
- Elementos de MontajeDocumento7 pagineElementos de MontajeJosé María MedianeroNessuna valutazione finora
- Dieta de 1Documento2 pagineDieta de 1Samy FlorezNessuna valutazione finora
- Parte Amistoso de Accidente - ES PDFDocumento2 pagineParte Amistoso de Accidente - ES PDFLuis Fernandez RodriguezNessuna valutazione finora
- Memoria FracturaDocumento20 pagineMemoria FracturaJosé María MedianeroNessuna valutazione finora
- Presentación FatigaDocumento13 paginePresentación FatigaJosé María MedianeroNessuna valutazione finora
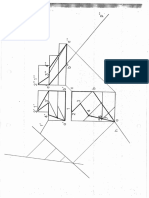
- Construcciones y Cortes II Soluci NDocumento1 paginaConstrucciones y Cortes II Soluci NJosé María MedianeroNessuna valutazione finora
- Memoria FatigaDocumento22 pagineMemoria FatigaJosé María MedianeroNessuna valutazione finora
- Memoria Práctica Funciones de PesoDocumento11 pagineMemoria Práctica Funciones de PesoJosé María MedianeroNessuna valutazione finora
- Mantenimiento Basado en FiabilidadDocumento4 pagineMantenimiento Basado en FiabilidadJosé María MedianeroNessuna valutazione finora
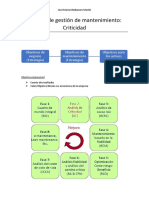
- CriticidadDocumento6 pagineCriticidadJosé María MedianeroNessuna valutazione finora
- Resumen Tema 10Documento3 pagineResumen Tema 10José María MedianeroNessuna valutazione finora
- Resumen Tema 6 y 7Documento10 pagineResumen Tema 6 y 7José María MedianeroNessuna valutazione finora
- Resumen Tema 8Documento4 pagineResumen Tema 8José María MedianeroNessuna valutazione finora
- Mantenimiento Productivo TotalDocumento5 pagineMantenimiento Productivo TotalJosé María MedianeroNessuna valutazione finora
- Documentación PDFDocumento3 pagineDocumentación PDFJosé María MedianeroNessuna valutazione finora
- Terminología Del MantenimientoDocumento6 pagineTerminología Del MantenimientoJosé María MedianeroNessuna valutazione finora
- Documentación Del MantenimientoDocumento4 pagineDocumentación Del MantenimientoJosé María MedianeroNessuna valutazione finora
- Gestion de La CalidadDocumento3 pagineGestion de La CalidadJosé María MedianeroNessuna valutazione finora
- AuditoríasDocumento4 pagineAuditoríasJosé María MedianeroNessuna valutazione finora
- Resumen ISO 9001Documento5 pagineResumen ISO 9001José María MedianeroNessuna valutazione finora
- NormalizaciónDocumento4 pagineNormalizaciónJosé María MedianeroNessuna valutazione finora
- SMP Grupo 17Documento25 pagineSMP Grupo 17José María MedianeroNessuna valutazione finora
- Análisis Piping B31.1 y DerivadasDocumento8 pagineAnálisis Piping B31.1 y DerivadasJosé María MedianeroNessuna valutazione finora
- Mecanica CuanticaDocumento16 pagineMecanica Cuanticafisikuni100% (2)
- Curvas de CompresiónDocumento5 pagineCurvas de CompresiónJosé Ávila BNessuna valutazione finora
- Tipos de Operaciones en La Industria IIDocumento53 pagineTipos de Operaciones en La Industria IIdavinik910Nessuna valutazione finora
- NEUTRALIZACIONDocumento12 pagineNEUTRALIZACIONAndyPaoNessuna valutazione finora
- Manual Pit 500 Intercambios TermicosDocumento149 pagineManual Pit 500 Intercambios TermicosBreidy Florez ariza100% (1)
- Informe Poisson Lab. CalidadDocumento12 pagineInforme Poisson Lab. CalidadDaniel Carvajal Tinoco100% (2)
- H° 1 PDFDocumento82 pagineH° 1 PDFGermán Nicolás Luna MoretaNessuna valutazione finora
- SEDIMENTACIONfDocumento16 pagineSEDIMENTACIONfEstiben GDNessuna valutazione finora
- Qué Hay Dentro de Las Bolsas de Gel RefrigeranteDocumento7 pagineQué Hay Dentro de Las Bolsas de Gel RefrigeranteQF Fredii Anthony GutyNessuna valutazione finora
- REACCIONES DE OXIDACIÓN Síntesis Del N-ButiraldehídoDocumento3 pagineREACCIONES DE OXIDACIÓN Síntesis Del N-ButiraldehídoPlutarco Chuquihuanga CórdovaNessuna valutazione finora
- M Esther Carrasco 1 PDFDocumento14 pagineM Esther Carrasco 1 PDFverito21041993Nessuna valutazione finora
- Guia de Homotecias 3ro CDocumento5 pagineGuia de Homotecias 3ro CestelaNessuna valutazione finora
- Ensayo La Quimica Es Importante en La Ing IndustrialDocumento1 paginaEnsayo La Quimica Es Importante en La Ing IndustrialKarol Balaguera100% (2)
- Hypack MaxDocumento38 pagineHypack MaxcarlosmrpNessuna valutazione finora
- Controlador IEADocumento20 pagineControlador IEAHernan GiorgettiNessuna valutazione finora
- Manual de TelequinesisDocumento8 pagineManual de TelequinesisEleazzar Álvarez86% (7)
- Historia de La Caída LibreDocumento5 pagineHistoria de La Caída LibreMaria Teresa Santacruz80% (5)
- Fusión NuclearDocumento11 pagineFusión NuclearCamiloVenturaNessuna valutazione finora
- G8 Integrales TriplesDocumento6 pagineG8 Integrales TriplesRaysha Ross Enciso RaveloNessuna valutazione finora
- Problem As 34Documento7 pagineProblem As 34edwraulNessuna valutazione finora
- Manual - JVC Gz-mg130Documento121 pagineManual - JVC Gz-mg130tecnico402Nessuna valutazione finora
- CATALOGO DE OeM LG938 ESP REV1-2009Documento130 pagineCATALOGO DE OeM LG938 ESP REV1-2009Gustavo100% (1)
- Tarea 6Documento11 pagineTarea 6ManuelNessuna valutazione finora
- Preparacion y Valoracion de Soluciones de Acidimetria-AlcalimetriaDocumento3 paginePreparacion y Valoracion de Soluciones de Acidimetria-AlcalimetriaHarold La Fuente PalominoNessuna valutazione finora
- Arcillas ExpansivasDocumento4 pagineArcillas ExpansivasRaúl Zeas CárdenasNessuna valutazione finora
- Problemas Resueltos Termodinamica PDFDocumento29 pagineProblemas Resueltos Termodinamica PDFKalethJNessuna valutazione finora
- Jorge Castillo Control3Documento9 pagineJorge Castillo Control3jorge100% (1)
- Monografía - WatercadDocumento32 pagineMonografía - WatercadInga De La Cruz Yussara100% (2)
- Energia y TrabajoDocumento5 pagineEnergia y TrabajoAlexis Gil SuárezNessuna valutazione finora
- Mecatrónica Sistemas de Control Electrónico en Ingeniería Mecánica y Eléctrica 2da Edición W.Bolton PDFDocumento539 pagineMecatrónica Sistemas de Control Electrónico en Ingeniería Mecánica y Eléctrica 2da Edición W.Bolton PDFRhosdailys RamirezNessuna valutazione finora