Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Informe Conductimetria-Daniel Arias 174681 PDF
Caricato da
Daniel AriasDescrizione originale:
Titolo originale
Copyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Informe Conductimetria-Daniel Arias 174681 PDF
Caricato da
Daniel AriasCopyright:
Formati disponibili
UNIVERSIDAD NACIONAL DE COLOMBIA
FACULTAD DE CIENCIAS
LABORATORIO DE ANALISIS QUMICO INSTRUMENTAL
a
Cra 30 N45-30 Ciudad Universitaria, Universidad Nacional de Colombia, Bogot, Colombia, Laboratorio de anlisis qumico
instrumental, mdulo de electroqumica Grupo 2. E-mail :deariasr@unal.edu.co
1
DETERMI NACI ON DE SULFATOS EN UNA
SOLUCI ON DE SULFATO DE SODI O
MEDI ANTE UNA TI TULACI ON
CONDUCTI METRI CA
Daniel Esteban Arias Ramirez
a
.
1. RESUMEN.
Se prepar una solucin de sulfato de sodio, la cual se us como titulante por efectos de
practicidad en el desarrollo del anlisis, luego se prepararon soluciones 0,05 M de Cloruro de
bario y de Nitrato de bario, se calibro el electrodo preparando una solucin 8,4X10
-3
M, la cual
posee una conductancia de 1000 uS, se realiz el procedimiento por duplicado por cada uno de
las soluciones de bario.
2. MARCO TEORICO
1,2
Conductimetra
Es la capacidad de una solucin para
transporta la corriente elctrica. En las
soluciones acuosas los transportadores son
los cationes y aniones, por lo cual es ms
lgico pensar en trminos de resistencia. La
resistencia se relacin con la conductancia
S, por una relacin inversa simple:
S=1/R (1)
Aspectos que afectan las medidas de
conductancia
1. Naturaleza de los electrodos: La
transferencia de carga se afecta con
el material de los electrodos.
2. rea superficial de los electrodos:
A mayor rea menor polarizacin,
ya que hay mayor transferencia de
carga.
3. Forma de los electrodos: Tiene un
efecto directo sobre el campo
elctrico que se forma entre los
electrodos el cual es el causante del
potencial medido.
4. Posicin relativa de los electrodos:
A mayor distancia entre los
electrodos, menor conductividad.
5. Tipo de sustancia
6. Concentracin
7. Temperatura: A mayor temperatura
mayor movilidad del ion.
8. La carga del ion
Fenmenos y ecuaciones
1. Conductancia S:
S= k A/d (2)
k= Conductividad; A=rea del electrodo;
d=Distancia entre los electrodos
k es la suma de las contribuciones de todas
las especies inicas en la solucin, en la que
cada contribucin de cada ion depende de
su concentracin de la magnitud de su carga
y su movilidad.
2. Movilidad del ion U
i
: Velocidad
lmite del ion en un campo elctrico
de fuerza unitaria
UNIVERSIDAD NACIONAL DE COLOMBIA
FACULTAD DE CIENCIAS
LABORATORIO DE ANALISIS QUMICO INSTRUMENTAL
a
Cra 30 N45-30 Ciudad Universitaria, Universidad Nacional de Colombia, Bogot, Colombia, Laboratorio de anlisis qumico
instrumental, mdulo de electroqumica Grupo 2. E-mail :deariasr@unal.edu.co
2
V= velocidad del ion;
= Fuerza del campo
elctrico; Z
i
= carga del ion, e carga
elemental, = Viscosidad, r = radio del ion.
3. Relacin entre conductividad y
movilidad
|
(4)
F= Constante de Faraday; C
i
=
Concentracin del iesimo ion.
4. Conductividad equivalente
(5)
C
eq
= Concentracin equivalente del ion,
C
eq
=C|
|.
La conductividad molar de un electrolito
debera ser independiente de la
concentracin si k fuera directamente
proporcional a la concentracin del
electrolito. Pero la conductividad molar
depende de la concentracin. La no
proporcionalidad entre el nmero de iones
en una disolucin y la concentracin del
electrolito.
Ley de Kohlraush
Los electrolitos fuertes estn virtualmente
ionizados por completo, por lo cual la
concentracin de iones en disolucin es
proporcional a la concentracin del
electrolito.
(6)
Ley de migracin independiente de los
iones
Se demostr que
se puede expresar
como una suma de las contribuciones de los
iones individuales.
(7)
= Conductividad molar de los iones
= Numero de cationes y aniones
3. PROCEDIMIENTO
Preparacin de soluciones
Preparar soluciones de Na
2
SO
4
,
BaCl
2
, Ba(NO
3
)
2
0,05M
Solucin de NaCl 8,3X10
-3
M
Procedimiento de titulacin
Calibrar el Conductimetra con la
solucin de cloruro de sodio,
teniendo en cuenta que esta
solucin tendr una conductancia
de 1000 uS.
Montar el Na
2
SO
4
en la bureta
Tomar 5 ml de la alcuota
respectiva y agregar 30 ml de agua
des ionizada.
Agregar volmenes 0,5 ml y
registrar la conductancia.
Lavar y limpiar el electrodo y el
reactor muy bien despus de cada
procedimiento de titulacin.
Realizar el procedimiento por
duplicado.
UNIVERSIDAD NACIONAL DE COLOMBIA
FACULTAD DE CIENCIAS
LABORATORIO DE ANALISIS QUMICO INSTRUMENTAL
a
Cra 30 N45-30 Ciudad Universitaria, Universidad Nacional de Colombia, Bogot, Colombia, Laboratorio de anlisis qumico
instrumental, mdulo de electroqumica Grupo 2. E-mail :deariasr@unal.edu.co
3
4. RESULTADOS Y DISCUSIN.
Se realizaron las medidas por duplicados usando la solucin de sulfatos como titulante
Analito Volumen de equivalencia (ml) Concentracin (M)
Promedio
(ml)
Ba(NO
3
)
2
4,769 0,0524
0,0524
4,772 0,0524
BaCl
2
4,349 0,0575
0,0575
4,344 0,0576
Tabla 1. Volmenes de equivalencia y concentraciones para las especies tituladas.
Donde se calcularon los valores respectivos de concentracin de sulfato para cada especie.
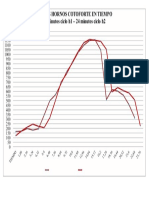
Figura 1. Conductimetrias de cada especie en funcin del volumen del sulfato de bario
agregado.
Figura 2. Curvas de titulacin conductimtrica terica para cada especie.
Se tiene la conductancia entre muchos
factores, depender principalmente de la
concentracin de iones en solucin, en un
primer momento los iones en solucin para
el caso del BaCl
2
, sern el cloruro y el
bario, los cuales sern los responsables de
la conductancia en la solucin a medida que
se agrega sulfato de sodio, se tiene da la
reaccin: Ba
2+
+ SO
4
-2
= BaSO
4
donde se
tiene un k de 3,94x10
4
por lo cual puede
considerarse que la reaccin esta
desplazada a la derecha, entonces en este
momento la conductancia estar dada por
los iones cloruro, los cuales disminuyen sus
conductancia por efectos de dilucin ya que
se est agregando ms volumen, la
contribucin del sodio ser muy baja ya que
este estar en concentracin muy bajas y
teniendo en cuenta que la conductividad de
este ion es la ms baja contribuir al
aumento de la conductancia muy poco, por
ltimo el bario libre en solucin disminuir
su concentracin por efectos de reaccin
con el sulfato y por efectos de dilucin, este
ion es el que posee la conductividad ms
alta entonces su presencia o ausencia ser
determinante en la suma total de
conductancia. No habr contribucin por
parte del sulfato ya que este al entrar en
contacto con el bario producir el
precipitado insoluble y nunca estar libre en
solucin. Por lo tanto la conductancia total
disminuir.
ION Conductividad (SL/mmol)
Ba 12,72
NO3 7,15
Na 5,01
SO4 16
Cl 7,64
Tabla 2. Conductividad de las especies en
el sistema
En el punto de equivalencia se tiene que ya
no existe ms bario libre en solucin,
entonces habr un exceso de sulfato de
sodio, el cual se disocia produciendo iones
sodio y bario, luego por una mol de sulfato
de sodio, se liberan 2 moles de sodio, por lo
cual la contribucin a la conductancia de
este ion ser importante aunque su
conductividad sea la ms baja, la especie
que posee la conductividad ms alta es el
sulfato que en este punto podr estar libre
en la solucin debido a la ausencia de bario
por la tanto su contribucin a la
conductancia ser definitiva, por esta razn
despus del punto de equivalencia la
conductancia empezara a subir.
Respecto a la curva terica de
conductividad (figura 2), se calcul
teniendo en cuenta la ley de migracin
independiente de los iones y teniendo en
cuenta que todas las sales son electrolitos
fuertes, lo cual es muy factible ya que si se
tienen en cuenta las reglas empricas de
solubilidad se tiene que todos los nitratos
son solubles, todos los cloruros son
solubles excepto los de plata, plomo, cobre
y mercurio y todos los sulfatos son solubles
excepto los de calcio, bario, estroncio,
plomo, plata. Se observa que la
conductancia para ambas especies es mayor
en las curvas de titulacin terica que en la
curvas de titulacin experimentales, lo cual
puede ser debido a que los factores que
afectan las medidas en la conductividad
como: la temperatura, los valores de
conductividad tomados para realizar la
curva son a 25C, esta variable no se tuvo
en cuenta en la toma de los datos, esta
variable afecta la energa cintica de los
iones en solucin, lo cual a su vez afecta su
movilidad, procesos de transferencia de
masa, no son tenidos en cuenta en la curva
de titulacin terica. Como es de esperar la
curva de titulacin terica del BaCl
2
est
por encima de la curva del Ba(NO
3
)
2
el
nico ion que cambia es el anin, la carga y
la cantidad de moles de anin libre es la
misma, donde la carga tambin es la misma,
por lo cual el factor de diferencia ser la
conductividad es ligeramente mayor en el
cloruro que para el nitrato.
La conductimetra como tcnica de anlisis
cuantitativo, posee muchas dificultades, ya
que en una muestra real la cantidad y
variedad de iones en solucin es muy alta,
entonces la medida no se deber al analito
de inters sino a la suma de la contribucin
de todos los iones de la muestra, por otro
lado la ley de Kohlraush solo se cumple
para electrolitos fuertes, lo cual no siempre
puede obtenerse en una muestra real.
UNIVERSIDAD NACIONAL DE COLOMBIA
FACULTAD DE CIENCIAS
LABORATORIO DE ANALISIS QUMICO INSTRUMENTAL
a
Cra 30 N45-30 Ciudad Universitaria, Universidad Nacional de Colombia, Bogot, Colombia, Laboratorio de anlisis qumico
instrumental, mdulo de electroqumica Grupo 2. E-mail :deariasr@unal.edu.co
5
5. CONCLUSIONES
Las concentraciones de sulfatos
fueron de 0,0524 M, 0,0575 M
adicionando el sulfato y usando
BaNO
3
y BaCl
2
respectivamente.
La conductimetra es una tcnica
que posee muy pocas aplicaciones
desde el punto de vista del anlisis
cuantitativo.
El punto de equivalencia es
pronunciado y por la tanto el
clculo del volumen de
equivalencia es muy acertado.
6. BIBLIOGRAFIA
(1) Notas de clase anlisis qumico instrumental
Texto Guia Conductimetria
(2) P.W. Atkins, J. De
Paula, Fisicoquimica, 8th Edition, O.U.P.,
2006. Pag 739
Potrebbero piacerti anche
- Santander territorio dinámico, complejo y diverso: una perspectiva desde la geografía física y sus interacciones ecosistémicasDa EverandSantander territorio dinámico, complejo y diverso: una perspectiva desde la geografía física y sus interacciones ecosistémicasNessuna valutazione finora
- Lab 3 ConductividadDocumento22 pagineLab 3 ConductividadJose VillalbaNessuna valutazione finora
- Determinación Del Grado de Disociación, Del Coeficiente de Actividad Iónica Medio y de Las Constantes Del Equilibrio de Disociación (Ka y KC) de Un Ácido Débil Por Medidas de ConductividadDocumento12 pagineDeterminación Del Grado de Disociación, Del Coeficiente de Actividad Iónica Medio y de Las Constantes Del Equilibrio de Disociación (Ka y KC) de Un Ácido Débil Por Medidas de ConductividadCarolinaQuimbayaNessuna valutazione finora
- Informe ConductividadDocumento16 pagineInforme ConductividadGiancarlo Gloria MarcatincoNessuna valutazione finora
- Labo 4 CineticaDocumento5 pagineLabo 4 CineticaRoger LopezNessuna valutazione finora
- Determinacion de AlcalinidadDocumento4 pagineDeterminacion de Alcalinidadjose jilNessuna valutazione finora
- Problemas A Resolver PDFDocumento41 pagineProblemas A Resolver PDFAda ArenasNessuna valutazione finora
- Propiedades Coligativas de Las Soluciones. Lab 4Documento6 paginePropiedades Coligativas de Las Soluciones. Lab 4ronaldoNessuna valutazione finora
- Propiedades termodinámicas de sustancias puras y ecuaciones de estadoDocumento1 paginaPropiedades termodinámicas de sustancias puras y ecuaciones de estadoastroboyatlas0% (1)
- Sintesis Del AlumbreDocumento10 pagineSintesis Del AlumbreJésica HerreraNessuna valutazione finora
- Cloruros FinalDocumento11 pagineCloruros FinalFabiola Del Pilar CuroNessuna valutazione finora
- Labo de Fico 2 Valoraciones ConductometricasDocumento15 pagineLabo de Fico 2 Valoraciones ConductometricasJoseNessuna valutazione finora
- Numero de TransporteDocumento9 pagineNumero de TransporteAndrEs ZuñiGaNessuna valutazione finora
- Celdas Galvánicas y Su TermodinámicaDocumento8 pagineCeldas Galvánicas y Su TermodinámicaMiguel Jiménez FloresNessuna valutazione finora
- Pila Daniell: Teoría, construcción y medición de f.e.mDocumento4 paginePila Daniell: Teoría, construcción y medición de f.e.mAngelMLNessuna valutazione finora
- TP N° 2 - Valoración Conductimétrica de Un Ácido FuerteDocumento7 pagineTP N° 2 - Valoración Conductimétrica de Un Ácido FuerteJuanNessuna valutazione finora
- Síntesis de anaranjado de metiloDocumento16 pagineSíntesis de anaranjado de metiloDelany BrendaNessuna valutazione finora
- Laboratorio de Fisicoquimica II - Equilibrio de DistribucionDocumento10 pagineLaboratorio de Fisicoquimica II - Equilibrio de DistribucionLuis Jesus Carbajal LozanoNessuna valutazione finora
- Labo de QMC-104 (Cinetica Quimica)Documento20 pagineLabo de QMC-104 (Cinetica Quimica)Luvinca Daniela Plata AlconNessuna valutazione finora
- PEC2 Química Analítica Instrumental 2021 2022Documento3 paginePEC2 Química Analítica Instrumental 2021 2022Alicia SánchezNessuna valutazione finora
- Practica 3. Ondas Mecánicas en Medios Elásticos.Documento24 paginePractica 3. Ondas Mecánicas en Medios Elásticos.Cassandra GonzálezNessuna valutazione finora
- Galio - Indio - TalioDocumento11 pagineGalio - Indio - TalioNico AgueroNessuna valutazione finora
- Conductividad de Soluciones ElectróliticasDocumento12 pagineConductividad de Soluciones ElectróliticasVictor Mauricio Ugarte MamaniNessuna valutazione finora
- Viscosidad Practica N1 of PDFDocumento16 pagineViscosidad Practica N1 of PDFKevin Rojas CalizayaNessuna valutazione finora
- 008 Práctica 8 PotenciometríaDocumento3 pagine008 Práctica 8 PotenciometríaSteward FloresNessuna valutazione finora
- Comportamiento del capacitor planoDocumento10 pagineComportamiento del capacitor planoDaniel GiraldoNessuna valutazione finora
- Guia de Operación de Procesos Industriales - ITSADocumento35 pagineGuia de Operación de Procesos Industriales - ITSAEDITORIAL_ITSANessuna valutazione finora
- YodimetriaDocumento5 pagineYodimetriaMax RomànNessuna valutazione finora
- Comportamiento de sistemas gaseososDocumento10 pagineComportamiento de sistemas gaseososDavid Fernandez0% (1)
- Informe 13N ConductividadDocumento17 pagineInforme 13N ConductividadNICK MARALLANONessuna valutazione finora
- Colisiones Con Una Pared y Efusió1Documento7 pagineColisiones Con Una Pared y Efusió1Greis JazminNessuna valutazione finora
- Análisis de Nitratos, Método de La BrucinaDocumento5 pagineAnálisis de Nitratos, Método de La BrucinaAida Jimenez100% (1)
- CUESTIONARIODocumento14 pagineCUESTIONARIOPaty Nunez MelendezNessuna valutazione finora
- Separación de Una Solución de Violeta de CristalDocumento7 pagineSeparación de Una Solución de Violeta de CristalAlbita GarciaNessuna valutazione finora
- Análisis Químico CualitativoDocumento80 pagineAnálisis Químico CualitativoGuadalupe CallisayaNessuna valutazione finora
- ELECTROQUÍMICADocumento6 pagineELECTROQUÍMICADennis Lara VasquezNessuna valutazione finora
- 6 Informe..Documento8 pagine6 Informe..Luis ContrerasNessuna valutazione finora
- Produccion de Carbonato de CalcioDocumento5 pagineProduccion de Carbonato de CalcioCamilo TorresNessuna valutazione finora
- Membrana Celular y Potencial de Acción en Tejidos ExcitablesDocumento6 pagineMembrana Celular y Potencial de Acción en Tejidos ExcitablesLexer GarcíaNessuna valutazione finora
- Protocolo 3 Cinetica QuimicaDocumento11 pagineProtocolo 3 Cinetica QuimicaChristian ZamoraNessuna valutazione finora
- Solubilidad Informe 3Documento32 pagineSolubilidad Informe 3Gabriel Monzòn Luna100% (1)
- Estructura Cristalina3bDocumento19 pagineEstructura Cristalina3bsebastian coboNessuna valutazione finora
- Determinación de las constantes de distribución y disociación del ácido acético mediante extracciones líquido-líquido a diferentes pHDocumento4 pagineDeterminación de las constantes de distribución y disociación del ácido acético mediante extracciones líquido-líquido a diferentes pHDarla SanchezNessuna valutazione finora
- Ácidos carboxílicos y derivadosDocumento22 pagineÁcidos carboxílicos y derivadosedsonNessuna valutazione finora
- Cuestionario ComplexometriaDocumento1 paginaCuestionario ComplexometriaJhenny RosarioNessuna valutazione finora
- Manual Met Cuanti P1 y P2Documento36 pagineManual Met Cuanti P1 y P2Esteban RicoNessuna valutazione finora
- Termodinamica ENUNCIADOSDocumento4 pagineTermodinamica ENUNCIADOSMåiirå SDj K. ZYtNessuna valutazione finora
- 2 SolubilidadDocumento5 pagine2 SolubilidadWISELANessuna valutazione finora
- E2208004 6 Taller Smog FotoquimicoDocumento8 pagineE2208004 6 Taller Smog FotoquimicoRaul GranadosNessuna valutazione finora
- Taller CromatografíaDocumento10 pagineTaller CromatografíaAna CarolinaNessuna valutazione finora
- Lab. Equilibrio Químico..Documento8 pagineLab. Equilibrio Químico..Shadia Peña RojasNessuna valutazione finora
- Informe #6 - Argentometría - G4Documento25 pagineInforme #6 - Argentometría - G4STEFHANY PAOLA MENDOZA HERNANDEZNessuna valutazione finora
- Modelamiento y Simulacion de Lechos FijosDocumento4 pagineModelamiento y Simulacion de Lechos FijosJulian Solo JulainNessuna valutazione finora
- QUIMICA AMBIENTAL PROBLEMAS DE ESTEQUIOMETRIADocumento2 pagineQUIMICA AMBIENTAL PROBLEMAS DE ESTEQUIOMETRIAJJ YajureNessuna valutazione finora
- Determinación calor reacción Zn-CuSO4Documento5 pagineDeterminación calor reacción Zn-CuSO4Jem DHNessuna valutazione finora
- CHARLES ListoDocumento38 pagineCHARLES ListoGianpierre Rojas AgapitoNessuna valutazione finora
- Reporte 3 de Fico 4Documento9 pagineReporte 3 de Fico 4Octavio Coronel MolinaNessuna valutazione finora
- Conduct IV I DadDocumento19 pagineConduct IV I DadunackremaNessuna valutazione finora
- Determinación de Sulfatos por ConductometriaDocumento6 pagineDeterminación de Sulfatos por ConductometriaMiguel castro ariNessuna valutazione finora
- Celdas Electroquimicas PDFDocumento4 pagineCeldas Electroquimicas PDFHector Ivan Cordoba BuenoNessuna valutazione finora
- Tema 11 Carbohidratos Ejercicios: Jose Luis Garrido LaraDocumento17 pagineTema 11 Carbohidratos Ejercicios: Jose Luis Garrido LaraDaniel AriasNessuna valutazione finora
- Tema 12 Aminoácidos, Péptidos Y Proteínas: Jose Luis Garrido LaraDocumento45 pagineTema 12 Aminoácidos, Péptidos Y Proteínas: Jose Luis Garrido LaraDaniel AriasNessuna valutazione finora
- Perfil Nacional Consumo Frutas y Verduras Colombia 2013Documento264 paginePerfil Nacional Consumo Frutas y Verduras Colombia 2013Daniel AriasNessuna valutazione finora
- Dtser 245Documento86 pagineDtser 245Nely PerezNessuna valutazione finora
- Tema 4 Enoles y Enonas. Aldehidos y Cetonas Alfa, Beta InsaturadosDocumento44 pagineTema 4 Enoles y Enonas. Aldehidos y Cetonas Alfa, Beta InsaturadosDaniel AriasNessuna valutazione finora
- Diagnóstico de Carne Bovina ESPECÍFICODocumento8 pagineDiagnóstico de Carne Bovina ESPECÍFICONancy Sofia Padilla GuerreroNessuna valutazione finora
- Tema 9 Compuestos DifuncionalesDocumento38 pagineTema 9 Compuestos DifuncionalesDaniel AriasNessuna valutazione finora
- Tema 11 Carbohidratos: Jose Luis Garrido LaraDocumento45 pagineTema 11 Carbohidratos: Jose Luis Garrido LaraDaniel AriasNessuna valutazione finora
- Tema 12 Aminoácidos Ejercicios: Jose Luis Garrido LaraDocumento15 pagineTema 12 Aminoácidos Ejercicios: Jose Luis Garrido LaraDaniel AriasNessuna valutazione finora
- Tema 10 Compuestos Aromaticos Policiclicos y HeterociclicosDocumento43 pagineTema 10 Compuestos Aromaticos Policiclicos y HeterociclicosDaniel AriasNessuna valutazione finora
- Boyaca Cifras 2019-ComprimidoDocumento213 pagineBoyaca Cifras 2019-ComprimidoDaniel AriasNessuna valutazione finora
- Educación y Desarrollo en Un Municipio Rural: El Caso de Pauna en BoyacáDocumento194 pagineEducación y Desarrollo en Un Municipio Rural: El Caso de Pauna en BoyacáSebastian RamirezNessuna valutazione finora
- Prueba Admision Segundo Semestre 2011 UNAL Discapacitados Auditiva UNB PDFDocumento33 paginePrueba Admision Segundo Semestre 2011 UNAL Discapacitados Auditiva UNB PDFAlexis Gil SuárezNessuna valutazione finora
- NTC 1325 productos cárnicos procesadosDocumento22 pagineNTC 1325 productos cárnicos procesadosDiego ChaparroNessuna valutazione finora
- 2 2011prim Cinet Apuntes2 MecanismosDocumento0 pagine2 2011prim Cinet Apuntes2 MecanismosIván BravoNessuna valutazione finora
- SonoquimiciaDocumento9 pagineSonoquimiciaDaniel AriasNessuna valutazione finora
- CV-educación-experiencia-idiomasDocumento2 pagineCV-educación-experiencia-idiomasYeudiel CruzNessuna valutazione finora
- Receta EmpanadasDocumento2 pagineReceta EmpanadasDaniel AriasNessuna valutazione finora
- Brochure TECSOL 2015Documento10 pagineBrochure TECSOL 2015Daniel AriasNessuna valutazione finora
- Curvas HornosDocumento1 paginaCurvas HornosDaniel AriasNessuna valutazione finora
- Aumento EbulliscopicoDocumento9 pagineAumento EbulliscopicoDaniel AriasNessuna valutazione finora
- Descenso Crioscopico de Un Sistema Agua AlaninaDocumento15 pagineDescenso Crioscopico de Un Sistema Agua AlaninaDaniel AriasNessuna valutazione finora
- Ecuación Del Calor en Una Placa BidimensionalDocumento4 pagineEcuación Del Calor en Una Placa BidimensionalDaniel AriasNessuna valutazione finora
- DifusiónDocumento7 pagineDifusiónDaniel AriasNessuna valutazione finora
- INFORME Estrutura Del AguaDocumento10 pagineINFORME Estrutura Del AguaDaniel AriasNessuna valutazione finora
- Primer Entrega Trabajo de Modelamiento Celdas SolaresDocumento11 paginePrimer Entrega Trabajo de Modelamiento Celdas SolaresDaniel AriasNessuna valutazione finora
- Trabajo Final ProgramacionDocumento16 pagineTrabajo Final ProgramacionDaniel AriasNessuna valutazione finora
- Trabajo Sobre AnalogiasDocumento2 pagineTrabajo Sobre AnalogiasDaniel AriasNessuna valutazione finora
- Examenes Ingenieria NavalDocumento23 pagineExamenes Ingenieria NavalKristina MuñizNessuna valutazione finora
- Evaluacion Practica QUIMICA (Laboratorio Quimica)Documento15 pagineEvaluacion Practica QUIMICA (Laboratorio Quimica)Juan Aldemar PerezrinconNessuna valutazione finora
- Marcha Analitica A Cambio de Packs 1 3Documento16 pagineMarcha Analitica A Cambio de Packs 1 3Ralf42RDPPLENessuna valutazione finora
- PDF Sintesis de Dibenzalacetona Anderson F Angulo Karen D Rios Resumen - CompressDocumento1 paginaPDF Sintesis de Dibenzalacetona Anderson F Angulo Karen D Rios Resumen - CompressStefany BarqueroNessuna valutazione finora
- 14.EM-Q (18) Unlocked PDFDocumento44 pagine14.EM-Q (18) Unlocked PDFGuillermo Martinez AguirreNessuna valutazione finora
- Informe 05-1Documento12 pagineInforme 05-1Jesus Manuel CruzNessuna valutazione finora
- Informe Final Patologías Del ConcretoDocumento70 pagineInforme Final Patologías Del ConcretoIsai CespedesNessuna valutazione finora
- Silabo Química Acuática-2021IDocumento6 pagineSilabo Química Acuática-2021IHenry JuarezNessuna valutazione finora
- Tesis Doctorado 2015 - Olga ÁnguloDocumento87 pagineTesis Doctorado 2015 - Olga ÁnguloAndre FerNessuna valutazione finora
- Cristalización - Sublimación - Quimica Organica I. 8Documento7 pagineCristalización - Sublimación - Quimica Organica I. 8MAYRA DENISSE SIÑANI CRUZNessuna valutazione finora
- Detalles ExperimentalesDocumento6 pagineDetalles ExperimentalesnubrolitoNessuna valutazione finora
- Sustancias IrritantesDocumento3 pagineSustancias IrritantesSofiaMarinHenao100% (2)
- Practica 3 Tecnología Farmacéutica LDocumento7 paginePractica 3 Tecnología Farmacéutica LSofía Alvarez HernandezNessuna valutazione finora
- Cinetica y EquilibrioDocumento23 pagineCinetica y EquilibrioNieves Del Barrio Masegosa100% (1)
- Procesos Selexol y Girbotol 1Documento10 pagineProcesos Selexol y Girbotol 1Andrea GarciaNessuna valutazione finora
- Volumetría NeutralizaciónDocumento3 pagineVolumetría NeutralizaciónManuel TelloNessuna valutazione finora
- Ecofrec TF49 MSDS Hoja de SoldaduraDocumento5 pagineEcofrec TF49 MSDS Hoja de SoldaduraIng Martha Patricia Ramirez GarciaNessuna valutazione finora
- Cristalización: Fundamentos y diseño de cristalizadoresDocumento36 pagineCristalización: Fundamentos y diseño de cristalizadoresAlfredo Martinez Peralta100% (1)
- ContenidoDocumento13 pagineContenidoAlexisNessuna valutazione finora
- Alcaloides, Generalidades y CaracteristicasDocumento3 pagineAlcaloides, Generalidades y CaracteristicasJuan Pardo0% (1)
- Sintesis de ColorantesDocumento2 pagineSintesis de Colorantesvvveeee100% (1)
- Química Analítica-Solubilidad ElectrolitosDocumento4 pagineQuímica Analítica-Solubilidad ElectrolitosCatalina AlanizNessuna valutazione finora
- Pratica 3, Cuantificacion de Proteinas en Suero SanguineoDocumento10 paginePratica 3, Cuantificacion de Proteinas en Suero SanguineoXiomi EscobarNessuna valutazione finora
- Eflorescencias en El HormigónDocumento5 pagineEflorescencias en El HormigónNaara GonzalezNessuna valutazione finora
- InformeDocumento12 pagineInformeyaritza quirozNessuna valutazione finora
- Contaminacion Ambiental Por Mercurio en La Mineria Artesanal en La Provincia de NazcaDocumento47 pagineContaminacion Ambiental Por Mercurio en La Mineria Artesanal en La Provincia de NazcaDely Huamani100% (1)
- IsotretinoinaDocumento7 pagineIsotretinoinaelias2222Nessuna valutazione finora
- Acido CitricoDocumento6 pagineAcido CitricoJessicaNessuna valutazione finora
- Grasa Champion MSDS - En.esDocumento9 pagineGrasa Champion MSDS - En.esWilliams VázquezNessuna valutazione finora
- Equilibrio - Quimico-Poster PDFDocumento2 pagineEquilibrio - Quimico-Poster PDFVictoria Vizcaíno GarcíaNessuna valutazione finora