Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Bioelectric I Dad
Caricato da
Alex Av Carrera0 valutazioniIl 0% ha trovato utile questo documento (0 voti)
15 visualizzazioni11 pagineTitolo originale
Bioelectric i Dad
Copyright
© © All Rights Reserved
Formati disponibili
DOCX, PDF, TXT o leggi online da Scribd
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
© All Rights Reserved
Formati disponibili
Scarica in formato DOCX, PDF, TXT o leggi online su Scribd
0 valutazioniIl 0% ha trovato utile questo documento (0 voti)
15 visualizzazioni11 pagineBioelectric I Dad
Caricato da
Alex Av CarreraCopyright:
© All Rights Reserved
Formati disponibili
Scarica in formato DOCX, PDF, TXT o leggi online su Scribd
Sei sulla pagina 1di 11
UNIVERSIDAD TECNOLGICA EQUINOCCIAL
Facultad de las Ciencias de la Salud Eugenio Espejo
Escuela de Odontologa
Bioloelectricidad
Preparada por
Alex Carrera
Quito, Ecuador
2014
BIOLOELECTRICIDAD
La bioelectricidad se estudia desde dos puntos de vista:
a) Como la fuente de energa elctrica en el interior de las clulas
b) Como la corriente electroltica (o corriente inica) debido a los campos elctricos en el
exterior de la clula.
Los lquidos intra y extracelular no tienen la misma composicin, sus concentraciones son
distintas, tal como se indica en la siguiente tabla.
Las clulas son las fuentes fundamentales de los potenciales bioelctricos, entendindose
como tales a las diferencias de potencial existentes entre el interior y exterior de la clula.
1. BOMBA SODIO-POTASIO
La bomba sodio-potasio es una protena de membrana fundamental en la fisiologa de las
clulas que se encuentra en todas nuestras membranas celulares. Su funcin es el transporte
de los iones inorgnicos ms importantes en biologa (el sodio y el potasio) entre el medio
extracelular y el citoplasma, proceso fundamental en todo el reino animal.
Descubrimiento
Esta protena la caracteriz el dans Jens Skou por casualidad en los aos 50, y por ello recibi
el premio Nobel en 1997. Desde entonces la investigacin ha determinado muchos de los
aspectos tanto de la estructura y funcionamiento de la protena, como de su funcin en la
fisiologa, de tremenda importancia en medicina.
Funcionamiento y estructura
Estructura proteica
La bomba sodio potasio ATP(adenin-tri-fosfatido) es una proteina transmembrana que acta
como un transportador de intercambio antiporte (transferencia simultnea de dos diferentes
direcciones) que hidroliza ATP. Es una ATPasa de transporte tipo P, es decir, sufre
fosforilaciones reversibles durante el proceso de transporte. Est formada por dos
subunidades, alfa y beta, que forman un tetrmero integrado en la membrana. La subunidad
alfa est compuesta por ocho segmentos transmembrana y en ella se encuentra el centro de
unin del ATP que se localiza en el lado citoslico de la membrana. Tambin posee dos centros
de unin bilaterales al extracelulares y tres centros de unin al intracelulares que se
encuentran accesibles para los iones en funcin de si la protena est fosforilada. La subunidad
beta contiene una sola regin helicoidal transmembrana y no parece ser esencial para el
transporte ni para la actividad.
Funcionamiento
El funcionamiento de la bomba electrognica de Na+/ K+(sodio-potasio) , se debe a un cambio
de conformacin en la protena que se produce cuando es fosforilada por el ATP. Como el
resultado de la catlisis es el movimiento transmembrana de cationes, y se consume energa
en forma de ATP, su funcin se denomina transporte activo. La demanda energtica es
cubierta por la molcula de ATP, que al ser hidrolizada, separa un grupo fosfato, generando
ADP y liberando la energa necesaria para la actividad enzimtica. En las mitocondrias, el ADP
es fosforilado durante el proceso de respiracin generndose un reservorio continuo de ATP
para los procesos celulares que requieren energa. En este caso, la energa liberada induce un
cambio en la conformacin de la protena una vez unidos los tres cationes de sodio a sus
lugares de unin intracelular, lo que conlleva su expulsin al exterior de la clula. Esto hace
posible la unin de dos iones de potasio en la cara extracelular que provoca la desfosforilacin
de la ATP, y la posterior traslocacin para recuperar su estado inicial liberando los dos iones de
potasio en el medio intracelular.
Los procesos que tienen lugar en el transporte son:
1. Unin de tres Na+ a sus sitios activos.
2. Fosforilacin de la cara citoplasmtica de la bomba que induce a un cambio de
conformacin en la protena. Esta fosforilacin se produce por la transferencia del grupo
terminal del ATP a un residuo de cido asprtico de la protena.
3. El cambio de conformacin hace que el Na+ sea liberado al exterior.
4. Una vez liberado el Na+, se unen dos molculas de K+ a sus respectivos sitios de unin de la
cara extracelular de las protenas.
5. La protena se desfosforila producindose un cambio conformacional de sta, lo que
produce una transferencia de los iones de K+ al citosol.
Funciones
La bomba de sodio-potasio es crucial e imprescindible para que exista la vida animal ya que
tiene las funciones expuestas a continuacin. Por ello se encuentra en todas las membranas
celulares de los animales, en mayor medida en clulas excitables como las clulas nerviosas y
clulas musculares donde la bomba puede llegar a acaparar los dos tercios del total de la
energa en forma de ATP de la clula.
Mantenimiento de la osmolaridad y del volumen celular
La bomba de Na+/K+ juega un papel muy importante en el mantenimiento del volumen
celular. Entre el interior y el exterior de la clula existen diferentes niveles de concentracin.
Como quiera que la bomba extrae de la clula ms molculas de las que introduce tiende a
igualar las concentraciones y, consecuentemente, la presin osmtica.
Sin la existencia de la bomba, dado que los solutos orgnicos intracelulares, a pesar de
contribuir en s mismos poco a la presin osmtica total, tienen una gran cantidad de solutos
inorgnicos asociados, la concentracin intracelular de estos (que generalmente son iones) es
mayor que la extracelular. Por ello, se producira un proceso osmtico, consistente en el paso
de agua a travs de la membrana plasmtica hacia el interior de la clula, que aumentara de
volumen y diluira sus componentes. Las consecuencias seran catastrficas ya que la clula
podra llegar a reventar (proceso conocido como lisis).
Transporte de nutrientes
El gradiente producido por el Na+ impulsa el transporte acoplado (activo secundario) de la
mayora de nutrientes al interior de la clula. Lo que quiere decir que el fuerte gradiente que
impulsa al sodio a entrar en la clula (vase ms adelante) es aprovechado por protenas
especiales de membrana para "arrastrar" otros solutos de inters utilizando la energa que se
libera cuando el sodio se introduce en la clula.
Potencial elctrico de membrana
Esta bomba es una protena electrognica ya que bombea tres iones cargados positivamente
hacia el exterior de la clula e introduce dos iones positivos en el interior celular. Esto supone
el establecimiento de una corriente elctrica neta a travs de la membrana, lo que contribuye
a generar un potencial elctrico entre el interior y el exterior de la clula ya que el exterior de
la clula est cargado positivamente con respecto al interior de la clula. Este efecto
electrognico directo en la clula es mnimo ya que slo contribuye a un 10% del total del
potencial elctrico de la membrana celular. No obstante, casi todo el resto del potencial deriva
indirectamente de la accin de la bomba de sodio y potasio, y se debe en su mayor parte al
potencial de reposo para el potasio. Mantenimiento de los gradientes de sodio y potasio
Impulsos nerviosos
La concentracin intracelular de sodio es 5-15 mM mientras que la extracelular es mucho
mayor (145 mM). Sin embargo, las concentraciones intra y extracelulares de potasio son 140
mM y 5 mM respectivamente. Esto nos indica que hay un fuerte gradiente electroqumico que
impulsa a las dos sustancias a moverse: el sodio hacia dentro y el potasio hacia fuera de la
clula. Como la membrana es impermeable a estos solutos, controlando la entrada y salida de
estas sustancias (principalmente), la clula genera cambios de concentracin de iones a ambos
lados de la membrana, y como los iones tienen carga elctrica, tambin se modifica el
potencial a su travs. Combinando estos dos factores, las clulas de un organismo son capaces
de transmitirse seales elctricas (vase: potencial de accin) y comunicarse entre ellas, paso
fundamental para la evolucin del reino animal.
La bomba de Na+/K+ contribuye a equilibrar el potencial de membrana y mantener el
potencial de reposo (es decir, las concentraciones constantes a ambos lados) cuando el
impulso nervioso ya se ha transmitido. Este impulso nervioso hace que los canales de Na+ se
abran generando un desequilibrio en la membrana y despolarizndola. Cuando el impulso ha
pasado los canales de Na+ se cierran y se abren los de K+. Para que el potencial de membrana
vuelva a su estado normal la bomba de Na+/K+ empieza a funcionar haciendo que la
membrana del axn vuelva a su estado de reposo (sacando el sodio que entr y metiendo el
potasio que sali).
Transduccin de seales
Recientemente se ha descubierto que, independientemente de su funcin de transporte
inico, la bomba tiene una funcin como receptor de seales. As, se ha descrito en miocitos
de rata en cultivo una modificacin en el ritmo de crecimiento tanto celular como mittico
cuando se aaden al medio anlogos de ouabana que actan sobre la protena.
Este cambio no se debe a la modificacin de las concentraciones inicas sino a protenas, seal
que acta en la cascada de las MAP quinasas.
2. POTENCIAL DE REPOSO
Es la diferencia de potencial existente entre el interior y el exterior de una clula en reposo.
Este potencial se debe a la desigual distribucin de iones entre el lquido intracelular y
extracelular. El potencial de membrana se detecta introduciendo un microelectrodo que
atraviesa la membrana celular y aplicando otro en la superficie, siendo negativo el interior
respecto al exterior (ver figura). Por convenio el potencial V0 del fluido extracelular se toma
igual a cero y el de lquido intracelular, de un axn por ejemplo, es Vi = -90mV.
3. POTENCIAL DE NERNST
El potencial de Nernst est definido como el nivel de potencial de difusin a travs de una
membrana que se opone directamente a la difusin neta de un ion en particular a travs de la
misma. Dicho potencial est en el interior de la membrana y se asume que el lquido
extracelular se mantiene a un potencial elctrico de cero voltios si la temperatura corporal es
la adecuada (aproximadamente 37 C).
Es el potencial de equilibrio de un in para el cual no hay flujo neto de dicho in a travs de la
membrana celular. Este potencial se calcula con la frmula:
Donde KB = 1.38x10-23J/K es la constante de Boltzmann, T la temperatura absoluta, q la carga
del in, Ce y Ci las concentraciones en el exterior e interior de la clula.
4. POTENCIAL DE ACCIN.
Es la alteracin del potencial de reposo de una clula por accin de un estmulo superior al
umbral, dando lugar a la sucesin de la despolarizacin y repolarizacin de la membrana
celular (ver figura) y se explican de la siguiente manera:
a) Durante el estado de reposo no circula ninguna corriente a travs de la membrana. Al actuar
es estmulo, superior al umbral, la permeabilidad del sodio aumenta transitoriamente; una
corriente de iones de Na+ penetra en el interior de la clula cambiando la carga de la
membrana (despolarizacin y fase ascendente del potencial de accin). Poco despus se
presenta una subida de la permeabilidad del K+; la corriente externa de K+ que de este modo
se produce ocasiona el regreso del potencial de membrana al de reposo (repolarizacin y fase
de descendente del potencial de accin).
b) El regreso del potencial al valor de reposo depende de dos mecanismos: por un lado, la
nueva disminucin que se presenta durante la larga despolarizacin, de la permeabilidad del
Na+ y en segundo lugar, el aumento desencadenado en forma retardada por la
despolarizacin, de la permeabilidad del potasio; ambos mecanismos producen un
restablecimiento de la relacin Pk = PNa y con ellos un reingreso al valor de reposo.
ELEMENTOS ELCTRICOS DE LA CLULA NERVIOSA
La informacin que se transmite en el cuerpo humano se hace mediante pulsos elctricos en
las fibras nerviosas denominadas axones. Los axones tienen dimetros comprendidos entre 1 y
20 m y pueden ser bastantes largos. La vaina de mielina que rodea a algunos axones reduce
la capacidad elctrica. Cada vaina de mielina, formada por clulas de Schwann, tiene
aproximadamente 1mm de longitud, pero la distancia entre vainas de mielina sucesivas es 1
m. En estos espacios celulares, denominados nodos de Ranvier, el axn est en contacto
directo con el lquido extracelular (o instersticial). Precisamente, en estos nodos se lleva a cabo
la amplificacin de los pulsos nerviosos en un nervio revestido de mielina.
RESISTENCIA ELECTRICA DEL AXON
Suponiendo que el axn consiste de una membrana cilndrica que tiene un lquido conductor
(el axoplasma), la corriente puede viajar a lo largo del axn en este fluido y tambin puede
escapar a travs de la membrana (figura a).
La resistencia R de una longitud L determinada de axn al paso del corriente axn es:
Donde a es la resistividad del axoplasma y A el rea de su seccin transversal.
La resistencia de la unidad de rea de la membrana a la corriente de prdida iperd se denota
por Rm (figura b) y la resistencia de prdida para una superficie de rea.
La distancia L = para la cual las resistencias R y R son iguales se llama parmetro espacial y se
calcula con la frmula
Este parmetro indica que distancia recorre una corriente antes que la mayor parte de ella se
pierde a travs de la membrana.
CAPACIDAD ELECTRICA DE UN AXN.
La membrana celular es muy fina por lo cual una pequea seccin parece casi plana y a ambos
lados de ella se acumulan cargas elctricas de signo opuesto (figura c)
La carga por unidad de superficie divida por la diferencia de potencial resultante es la
capacidad elctrica por unidad de rea:
Un trozo de axn de longitud L y radio r tiene un rea A = 2rL y su capacidad es:
Las resistencias Rm, capacidades Cm y resistividades del axn con y sin mielina se muestran en
la siguiente tabla.
CIRCUITO ELECTRICO DEL AXN, El circuito anlogo del axn puede desarrollarse dividindolo
en muchos segmentos cortos. El fluido extracelular tiene una resistencia elctrica muy
pequea y puede considerarse como un conductor perfecto. Cada segmento de axn presenta
una resistencia R debido al fluido intracelular (o axoplasma) al paso de la corriente iaxn a lo
largo de su longitud. La membrana tiene una resistencia R a una corriente de prdida iperd
ms una capacidad C.
Una serie de varios segmentos de axn es entonces anloga a la compleja red de resistencias y
condensadores mostrados en la siguiente figura. La fem del circuito representa el estmulo
aplicado.
RESPUESTA DEL AXN A ESTIMULOS DEBILES.
Cuando un estmulo inferior al umbral acta sobre un axn sin mielina, se produce un pulso
que recorre el axn y se atena despus de pocos milmetros. En el lugar del estmulo, x=0, el
potencial Vi cambia lentamente de 90mV a 60mV; para otros valores de x los potenciales
cambian ms lentamente alcanzando un potencial final entre estos extremos.
Si la diferencia entre el potencial de reposo y el potencial final en x = 0 es Vd, entonces l a
diferencia a una distancia x es:
donde es el parmetro espacial y x la distancia entre el estmulo y el punto en consideracin.
Por el contrario, cuando un estmulo superior al umbral acta sobre un axn se produce un
pulso que recorre la longitud del axn sin atenuacin.
IMPULSO NERVIOSO
El impulso nervioso es un potencial de accin que se propaga a lo largo del axn de una clula
nerviosa. En la siguiente figura se representa la conduccin del impulso en las fibras nerviosas
mielnicas y amielnicas. En el punto estimulado, las membranas se despolarizan al hacerse
ms permeables al Na+. Cuando el potencial de membrana se acerca al potencial de equilibrio
del Na+, aparece una diferencia de potencial entre esa regin particular y una regin vecina,
inactiva, dela membrana, donde el potencial es prximo al potencial de equilibrio de K+.
A consecuencia de la diferencia de potencial entre esas dos regiones pasa una corriente local
entre la regin activa y la inactiva, por el lquido intracelular, hasta descargar la membrana. La
corriente regresa nuevamente a la regin activa por el lquido extracelular, a travs de la
membrana. Esta corriente local reduce la carga de la membrana en la regin activa.
La velocidad de propagacin del impulso en una fibra mielnica es:
Donde X es la distancia entre dos nodos sucesivos y el tiempo necesario para reducir la carga
de la membrana y aumentar por encima del umbral el potencial en el segundo nodo:
Aqu, X=10-3m, r el radio del axn y los valores de a y Cm se dan en la tabla A.
BIBLIOGRAFIA
B. Alberts y col. Biologa Molecular de la Clula, 3 ed., Editorial Omega, 1998, pp. 34-39, 78,
94.
A Lehninger. Principios de Bioqumica. 3 ed., Editorial Omega, 2001, pp. 67-69, 80, 84.
Bioelectricidad Universidad Nacional de Santa
Potrebbero piacerti anche
- Acceso CameralDocumento20 pagineAcceso CameralAlex Av CarreraNessuna valutazione finora
- Oral and Maxillofacial Infections 4th Ed - TopazianDocumento568 pagineOral and Maxillofacial Infections 4th Ed - TopazianHari Kumar67% (15)
- Guia CACES Componentes y Ejemplos de Preguntas OdontologíaDocumento14 pagineGuia CACES Componentes y Ejemplos de Preguntas OdontologíaAlex Av CarreraNessuna valutazione finora
- DROGASDocumento20 pagineDROGASAlex Av CarreraNessuna valutazione finora
- Geren CIADocumento17 pagineGeren CIAAlex Av CarreraNessuna valutazione finora
- Tarjeta AlexDocumento12 pagineTarjeta AlexAlex Av CarreraNessuna valutazione finora
- Proporciones Divinas PDFDocumento8 pagineProporciones Divinas PDFAlex Av CarreraNessuna valutazione finora
- Séptima A 8va SemanaDocumento9 pagineSéptima A 8va SemanaAlex Av CarreraNessuna valutazione finora
- OsteoporosisDocumento2 pagineOsteoporosisAlex Av CarreraNessuna valutazione finora
- Selección Del Sitio para El Implante MandibularDocumento12 pagineSelección Del Sitio para El Implante MandibularAlex Av CarreraNessuna valutazione finora
- AlginatoDocumento36 pagineAlginatoAlex Av CarreraNessuna valutazione finora
- Cirugia Maxilofacial Pediatrica - LeviDocumento77 pagineCirugia Maxilofacial Pediatrica - LeviLex Puma IdmeNessuna valutazione finora
- Naturales 9 EGBDocumento224 pagineNaturales 9 EGBLuis RoblesNessuna valutazione finora
- Proporciones Divinas PDFDocumento8 pagineProporciones Divinas PDFAlex Av CarreraNessuna valutazione finora
- Clasificacion de AngleDocumento13 pagineClasificacion de AngleDemond Jose100% (4)
- LECTURA #1 Srta MirusDocumento47 pagineLECTURA #1 Srta MirusAlex Av CarreraNessuna valutazione finora
- Biologia1-Evaluacion Por Competencia A DocentesDocumento22 pagineBiologia1-Evaluacion Por Competencia A DocentesMarisol Teheran CastroNessuna valutazione finora
- Evaluacion Cierre Apical HidroxidoDocumento7 pagineEvaluacion Cierre Apical HidroxidoJavier MendozaNessuna valutazione finora
- Veronica MacrolidosDocumento15 pagineVeronica MacrolidosAlex Av CarreraNessuna valutazione finora
- Historia de Implantologia PDFDocumento42 pagineHistoria de Implantologia PDFHans Arosti0% (1)
- LaserDocumento12 pagineLaserAlex Av Carrera100% (1)
- OCLUSIONDocumento17 pagineOCLUSIONDiana Quinto100% (1)
- Cirugia Maxilofacial Pediatrica - LeviDocumento77 pagineCirugia Maxilofacial Pediatrica - LeviLex Puma IdmeNessuna valutazione finora
- CoronasDocumento7 pagineCoronasAlex Av CarreraNessuna valutazione finora
- AngleDocumento5 pagineAngleAlex Av CarreraNessuna valutazione finora
- HuesosDocumento41 pagineHuesosIsabel CarmonaNessuna valutazione finora
- Hibridación Del CarbonoDocumento6 pagineHibridación Del CarbonoAlex Av CarreraNessuna valutazione finora
- Edgar Preguntas Simulacro 2Documento4 pagineEdgar Preguntas Simulacro 2Profe OnlineNessuna valutazione finora
- Traducción en Eucariotas y Procariotas - Grupo 5Documento5 pagineTraducción en Eucariotas y Procariotas - Grupo 5Dario FrancoNessuna valutazione finora
- Clase 1. Introducción A La MicrobiologíaDocumento17 pagineClase 1. Introducción A La MicrobiologíaVivineyneyRickyNessuna valutazione finora
- Manual de Procedimientos para El Laboratorio Clinico Veterinario en El Centro de Recepcion y RehabilitacionDocumento30 pagineManual de Procedimientos para El Laboratorio Clinico Veterinario en El Centro de Recepcion y RehabilitacionJorge ParejaquispeNessuna valutazione finora
- Informe Tpn° 2 FISIo FinalDocumento6 pagineInforme Tpn° 2 FISIo FinalAyelen Gonzalez NuñezNessuna valutazione finora
- Memorias 22° Congreso Internacional de Actualización ApícolaDocumento128 pagineMemorias 22° Congreso Internacional de Actualización ApícolaTanya Petirrojo del FuturoNessuna valutazione finora
- Tesis Nivel de Conocimiento Del Vih Sida Finalizada 2 ModificadaDocumento105 pagineTesis Nivel de Conocimiento Del Vih Sida Finalizada 2 ModificadaMaritzel RochaNessuna valutazione finora
- Mapa y Cuadro de Parásitos - DrawioDocumento1 paginaMapa y Cuadro de Parásitos - DrawioBeker solisNessuna valutazione finora
- Actividad IntegradoraDocumento9 pagineActividad IntegradoraMarijose May CazolaNessuna valutazione finora
- Historia Del Coeficiente de CorrelacionDocumento3 pagineHistoria Del Coeficiente de CorrelacionFer GonzalesNessuna valutazione finora
- Las Celulas P. y E.Documento4 pagineLas Celulas P. y E.Leo Almontes LeonNessuna valutazione finora
- Ordoñez Rodriguez TamaraDocumento29 pagineOrdoñez Rodriguez TamaraAlbertoMonNessuna valutazione finora
- Fitorremediacion de Suelos Contaminados Por Plomo PDFDocumento68 pagineFitorremediacion de Suelos Contaminados Por Plomo PDFMiller Melquisede Montalvan ParedesNessuna valutazione finora
- ProteobacteriaDocumento3 pagineProteobacteriaAlondra Lizbeth Gutierrez TorresNessuna valutazione finora
- Institución Educativa Maria Jesus Mejia Guía de Aprendizaje Grado: Sexto Primer Periodo Codigo:Na Página: 1 de 1Documento6 pagineInstitución Educativa Maria Jesus Mejia Guía de Aprendizaje Grado: Sexto Primer Periodo Codigo:Na Página: 1 de 1JOSEGAMERNessuna valutazione finora
- ERITROCITOSDocumento31 pagineERITROCITOSAnge M. H. Dávila100% (1)
- Los AlimentosDocumento4 pagineLos AlimentosJairo Nel BeltranNessuna valutazione finora
- Articulo de Revisión - ProtozoosDocumento8 pagineArticulo de Revisión - ProtozoosVanessa GilNessuna valutazione finora
- RecuperacionDocumento3 pagineRecuperacionABRIL ILES SAMUEL ALEJANDRONessuna valutazione finora
- Patogenos e Indicadores Microbiologicos de Calidad de AguaDocumento3 paginePatogenos e Indicadores Microbiologicos de Calidad de AguaWendy RiverssNessuna valutazione finora
- Patrones Centrales de MovimientoDocumento9 paginePatrones Centrales de MovimientoDominique SalinasNessuna valutazione finora
- Actividad de Larvicidas de Estractos VegetalesDocumento8 pagineActividad de Larvicidas de Estractos VegetalesSolache DanielNessuna valutazione finora
- Microbiologia Del HuevoDocumento13 pagineMicrobiologia Del HuevoCristian Oleas AyalaNessuna valutazione finora
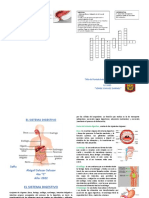
- Sistema Digestivo DIPTICODocumento3 pagineSistema Digestivo DIPTICOYenny Salazar RojasNessuna valutazione finora
- Guia #1Documento6 pagineGuia #1Martha sofia Rivera rodriguezNessuna valutazione finora
- La Otra Cara de La MonedaDocumento55 pagineLa Otra Cara de La Monedaenrique2001-1Nessuna valutazione finora
- Baynes - EnvejecimientoDocumento11 pagineBaynes - EnvejecimientoYónatan Martines ArrolloNessuna valutazione finora
- Mac y MatrizDocumento20 pagineMac y MatrizMarce De La CruzNessuna valutazione finora
- Consideraciones para Arboles SemillerosDocumento26 pagineConsideraciones para Arboles SemillerosFranco GilardenghiNessuna valutazione finora
- Sistema Digestivo IIDocumento87 pagineSistema Digestivo IIJUAN JOS� GARZON CARVAJALNessuna valutazione finora