Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Importante Preparo de Soluções PDF
Caricato da
Elaine Viana0 valutazioniIl 0% ha trovato utile questo documento (0 voti)
89 visualizzazioni41 pagine1) O documento apresenta experimentos de análise química quantitativa utilizando técnicas de volumetria como neutralização, precipitação e oxirredução.
2) São descritos procedimentos para preparação de soluções padrão e realização de experimentos como determinação de acidez em vinagre, teor de ácido cítrico em frutas e percentagem de cloro em alvejante.
3) As técnicas volumetricas permitem quantificar substâncias através de titulações utilizando reações de neutralização,
Descrizione originale:
Titolo originale
importante preparo de soluções.pdf
Copyright
© © All Rights Reserved
Formati disponibili
PDF, TXT o leggi online da Scribd
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documento1) O documento apresenta experimentos de análise química quantitativa utilizando técnicas de volumetria como neutralização, precipitação e oxirredução.
2) São descritos procedimentos para preparação de soluções padrão e realização de experimentos como determinação de acidez em vinagre, teor de ácido cítrico em frutas e percentagem de cloro em alvejante.
3) As técnicas volumetricas permitem quantificar substâncias através de titulações utilizando reações de neutralização,
Copyright:
© All Rights Reserved
Formati disponibili
Scarica in formato PDF, TXT o leggi online su Scribd
0 valutazioniIl 0% ha trovato utile questo documento (0 voti)
89 visualizzazioni41 pagineImportante Preparo de Soluções PDF
Caricato da
Elaine Viana1) O documento apresenta experimentos de análise química quantitativa utilizando técnicas de volumetria como neutralização, precipitação e oxirredução.
2) São descritos procedimentos para preparação de soluções padrão e realização de experimentos como determinação de acidez em vinagre, teor de ácido cítrico em frutas e percentagem de cloro em alvejante.
3) As técnicas volumetricas permitem quantificar substâncias através de titulações utilizando reações de neutralização,
Copyright:
© All Rights Reserved
Formati disponibili
Scarica in formato PDF, TXT o leggi online su Scribd
Sei sulla pagina 1di 41
Av. Dr.
Jos Loureiro da Silva, 655
Gravata RS
Curso Tcnico em Qumica
Componente Curricular: Anlise Qumica
Terceira Edio - 2010
Mdulo II
Apostila de Experimentos
Nome:______________________________________
Turma: ___________
Segunda Edio
Produo e digitao: Prof Marcelo Antunes Gauto
Coordenao e aprovao: Prof Gilber Ricardo Rosa
Terceira Edio:
Atualizao: Prof Cristina Lorenski Ferreira
Proibida a reproduo total ou parcial desta obra sem autorizao prvia do autor.
Gravata, agosto de 2010
Sumrio:
Introduo Qumica Analtica Quantitativa....................................................................................... 03
Laboratrio Qumico............................................................................................................................... 03
Tcnicas de Volumetria.......................................................................................................................... 04
Medidas de Massa........................................................................................................................... 04
Medidas de Volume.......................................................................................................................... 05
Aparelhos Volumtricos................................................................................................................... 06
Preparo e Padronizao de Solues................................................................................................... 11
Substncias padres primrios........................................................................................................ 11
Solues padres............................................................................................................................. 11
Volumetria de Neutralizao.................................................................................................................. 12
Preparo de soluo de Na
2
CO
3
........................................................................................................ 12
Preparo de soluo padro de HCl 0,1M......................................................................................... 12
Preparo de soluo padro de NaOH 0,1M..................................................................................... 13
Experimento 1 - Determinao do teor e cido actico no Vinagre.......................................... 15
Experimento 2 - Determinao da acidez total em Vinhos......................................................... 16
Experimento 3 - Determinao do teor de cido ctricos em Frutos......................................... 17
Experimento 4 Retrotitulao.................................................................................................... 18
Volumetria de Precipitao.................................................................................................................... 20
Preparo de soluo padro de AgNO
3
0,05M.................................................................................. 20
Experimento 5 - Determinao de cloreto em Soro fisiolgico................................................. 22
Volumetria de oxi-reduo..................................................................................................................... 23
Iodometria e Iodimetria ......................................................................................... .................... 23
Preparo de soluo padro de Na
2
S
2
O
3
0,1M............................................................................. 26
Preparo de soluo padro de Iodo 0,03M.................................................................................. 27
Experimento 6 - Anlise de comprimidos de Vitamina C....................................................... 29
Experimento 7 - Determinao da porcentagem de Cloro em Alvejante.............................. 30
Permanganometria......................................................................................................................... 31
Preparo de soluo padro de KMnO
4
0,02M............................................................................. 31
Experimento 8 - Determinao do teor de H
2
O
2
em gua oxigenada.................................... 33
Experimento 9 - Determinao de Ferro em lmina de barbear............................................ 34
Volumetria de Complexao.................................................................................................................. 35
Preparo de soluo de EDTA 0,02M............................................................................................ 35
Experimento 10 - Determinao da dureza em gua.............................................................. 37
Experimento 11 - Determinao de Clcio em Leite............................................................... 38
Bibliografia.............................................................................................................................................. 39
Apndice 1 Limpeza de materiais volumtricos............................................................................... 40
Apndice 2 Calibrao de equipamentos volumtricos................................................................... 40
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
3
So pequenas pores da
amostra de laboratrio
utilizadas para anlises.
Geralmente as anlises so
realizadas em rplicas,
melhorando a confiabilidade
dos resultados.
INTRODUO QUMICA ANALTICA QUANTITATIVA
A Qumica Analtica Quantitativa indica a quantidade de cada substncia presente em uma amostra.
Anlise Quantitativa Tpica:
1. Escolha do mtodo analtico:
Quantidade de amostra disponvel
Sensibilidade e exatido requeridas
Composio qumica da amostra
Nmero de amostras para anlise
Recursos disponveis
2. Obteno da Amostra
Amostragem: processo de seleo de uma quantidade de material cuja composio represente
exatamente o todo do material que est sendo analisado.
LABORATRIO QUMICO
Apesar do grande desenvolvimento terico da Qumica, ela continua a ser uma cincia
eminentemente experimental; da a importncia das aulas prticas de Qumica. A experincia treina o
aluno no uso de mtodos, tcnicas e instrumentos de laboratrio e permite a aplicao dos conceitos
tericos aprendidos.
O laboratrio Qumico o lugar privilegiado para a realizao de experimentos, possuindo
instalaes de gua, luz e gs de fcil acesso em todas as bancadas. Possui ainda local especial para
manipulao das substncias txicas (a capela), que dispe de sistema prprio de exausto de gases.
O laboratrio um local onde h um grande nmero de equipamentos e reagentes que possuem os
mais variados nveis de toxidez. Este um local bastante vulnervel a acidentes, desde que no se
trabalhe com as devidas precaues. Abaixo, apresentamos alguns cuidados que devem ser
observados, para a realizao das prticas, de modo a minimizar os riscos de acidentes.
Antes, durante e aps o experimento
No se entra num laboratrio sem um objetivo especfico, portanto necessria uma
preparao prvia ao laboratrio: O que vou fazer? Com que objetivo? Quais os princpios qumicos
envolvidos nesta atividade?
Durante a realizao dos experimentos so necessrias anotaes dos fenmenos
observados, das massas e dos volumes utilizados, do tempo decorrido, das condies iniciais e finais
do sistema, portanto um caderno deve ser usado especialmente para o laboratrio. Este caderno de
Alquota
Total do material do qual so retiradas
amostras
Lote
Amostra bruta representativa
Amostragem
Amostra de laboratrio
Preparo da amostra:
Etapas necessrias para
converter a amostra
bruta em uma forma
apropriada para anlise
qumica.
Alquota
Alquota
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
4
laboratrio possibilitar uma descrio precisa das atividades de laboratrio. No confie em sua
memria, tudo deve ser anotado.
Aps o experimento vem o trabalho de compilao das etapas anteriores atravs de um
relatrio. O relatrio um modo de comunicao escrita de cunho cientfico sobre o trabalho
laboratorial realizado.
Pr-laboratrio
1. Estude os conceitos tericos envolvidos, leia com ateno o roteiro da prtica e tire todas as
dvidas.
2. Obtenha as propriedades qumicas, fsicas e toxicolgicas dos reagentes a serem utilizados.
Essas instrues so encontradas no rtulo do reagente.
Aula prtica
1. O laboratrio um local de trabalho srio; portanto, evite brincadeiras que dispersem sua
ateno e de seus colegas.
2. O cuidado e aplicao de medidas de segurana responsabilidade de cada indivduo; cada
um deve precaver-se contra perigos devido a seu prprio trabalho e ao dos outros. Consulte o
professor sempre que tiver dvidas ou ocorrer algo inesperado ou anormal.
3. Faa apenas a experincia prevista; qualquer atividade extra no deve ser realizada sem a
prvia consulta ao professor.
4. No cheire, toque ou prove qualquer reagente. Lembre-se que a contaminao ocorre por
inalao e/ou ingesto e/ou absoro pela pele. No fume, coma ou beba no laboratrio.
5. Nunca deixe o bico de Bunsen aceso quando no estiver usando. No use substncias
inflamveis prximo a chama.
6. Trabalhe com cuidado com substncias txicas e corrosivas, como cidos, lcalis e solventes.
Todo material txico e/ou que exale vapor deve ser usado na capela.
7. Leia com ateno o rtulo do frasco de reagente antes de us-lo para certificar-se que o
frasco certo. Todo frasco contendo reagentes, amostras e solues deve ser devidamente
etiquetado (identificao do material e do responsvel e data).
8. No contamine os reagentes, voltando o reagente no utilizado ao frasco original ou usando
esptulas e pipetas sujas ou molhadas.
9. Experimentos em andamento devem apresentar anotaes indicando o procedimento em
caso de acidente. No utilize material de vidro quebrado, rachado ou com defeito,
principalmente para aquecimento ou em sistemas com vcuo.
10. Enxugue e lave qualquer local onde cair reagente. Nunca jogue papis, fsforo ou qualquer
slido na pia.
Ps-laboratrio
1. Lave todo o material logo aps o trmino da experincia, pois conhecendo a natureza do
resduo pode-se usar o processo adequado de limpeza.
2. Guarde todo o equipamento e vidraria. Guarde todos os frascos de reagentes, no os deixe
nas bancadas ou capelas. Desligue todos os aparelhos e lmpadas e feche as torneiras de
gs.
TCNICAS DE VOLUMETRIA
necessrio que qualquer pessoa que trabalhe em laboratrios de qumica analtica saiba
distinguir e usar convenientemente cada equipamento volumtrico, de modo a reduzir ao mnimo o
erro nas anlises.
Medidas de Massa: Balana analtica
- Centralize o material a ser pesado no prato da balana;
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
5
- Nunca colocar reagentes diretamente no prato da balana; pes-os em recipientes adequados
(pesa-filtro, bquer pequeno, vidro de relgio, barquinha de pesagem, papel apropriado para a
pesagem);
- No toque diretamente com as mos o material a ser pesado (utilize uma pina ou uma tira de
papel).
- A massa de muitos slidos varia com a umidade. Uma anlise tpica envolve a secagem da amostra
para que os resultados no sejam influenciados pela umidade do ambiente.
Secagem at massa constante: Uma amostra levada massa constante por meio de um ciclo de
aquecimento em temperaturas adequadas, resfriamento e pesagem. Este ciclo obtido at que se
obtenha massas sucessivas com concordncia de 0,2 a 0,3mg. A secagem realizada em estufa,
com temperatura adequada. Aps, a amostra mantida em dessecador.
Dessecador: uma cmara fechada que contm um agente de secagem chamado
dessecante (ex.: slica gel, sulfato de clcio, pentxido de fsforo, perclorato de magnsio anidro,
etc.). A tampa tratada com graxa para fazer um fechamento hermtico. O dessecante colocado
abaixo do disco de porcelana perfurado na parte de baixo do dessecador.
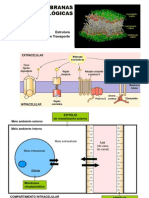
Medidas de Volume
Em um laboratrio so basicamente dois os tipos de frascos volumtricos disponveis, a saber:
aqueles calibrados para conter um certo volume, o qual se transferido no o ser totalmente (exibem
a sigla TC, to contain, gravada no vidro) e aqueles calibrados para transferir um determinado volume
(exibem a sigla TD, to deliver, gravada no vidro, dentro de certos limites de preciso).
Em trabalhos de laboratrio, as medidas de volume aproximadas so efetuadas, na quase
totalidade dos casos, com provetas graduadas; as de modo muito grosseiro, com bqueres com
escala e as medidas volumtricas, chamadas precisas, com aparelhos volumtricos (Figuras 1 e 2).
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
6
Aparelhos Volumtricos
A prtica de anlise volumtrica requer a medida de volumes lquidos com elevada preciso.
Para efetuar tais medidas so empregados vrios tipos de aparelhos, que podem ser classificados em
duas categorias:
a) Aparelhos calibrados para dar escoamento a determinados volumes (TD).
b) Aparelhos calibrados para conter um volume lquido (TC).
Na classe a esto contidas as pipetas e as buretas e, na classe b, esto includos os bales
volumtricos.
A medida de volumes lquidos com qualquer um dos referidos aparelhos est sujeita a uma srie
de erros devido s seguintes causas:
a) Ao da tenso superficial sobre as superfcies lquidas;
b) Dilataes e contraes provocadas pelas variaes de temperatura;
c) Imperfeita calibrao dos aparelhos volumtricos;
d) Erros de paralaxe.
A leitura de volume de lquidos claros deve ser feita pela parte inferior do menisco e a de
lquidos escuros pela parte superior, como mostra a Figura 3. Na leitura de volumes, o olho precisa
estar no nvel da superfcie do liquido, para se evitar o erro devido paralaxe, uma condio que faz
que o volume parea menor que seu valor verdadeiro, se o menisco for visto de cima, e maior, se o
menisco for visto de baixo.
Figura 3 Posio correta do menisco
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
7
1. Bales volumtricos: Os bales volumtricos so bales de fundo chato e gargalo comprido,
calibrados para conter determinados volumes lquidos (Figura 4).
Os bales volumtricos so providos de rolhas esmerilhadas
de vidro ou de polietileno. O trao de referncia marcando o
volume pelo qual o balo volumtrico foi calibrado gravado
sobre a meia-altura do gargalo (bulbo). A distncia entre o trao
de referncia e a boca do gargalo deve ser relativamente grande
para permitir a fcil agitao do lquido (a soluo deve ser bem
homogeneizada), depois de ser completado o volume at a
marca. O trao de referncia gravado sob a forma de uma linha
circular, tal que, por ocasio da observao, o plano tangente
superfcie inferior do menisco tem que coincidir com o plano do
crculo de referncia. Os bales volumtricos so construdos
para conter volumes diversos; os mais usados so os de 50, 100,
200, 500, 1000, 2000 mL.
Os bales volumtricos so especialmente usados na
preparao de solues de concentrao conhecida.
Para se preparar uma soluo em um balo volumtrico, transfere-se* ao mesmo, o soluto ou a
soluo a ser diluda. Adiciona-se, a seguir, solvente at cerca de 3/4 da capacidade total do balo.
Misturam-se os componentes e deixa-se em repouso at atingir a temperatura ambiente, tendo-se o
cuidado de no segurar o balo pelo bulbo. Adiciona-se solvente at acertar o menisco, isto , at o
nvel do lquido coincidir com a marca no gargalo. As ltimas pores do solvente devem ser
adicionadas com um conta-gotas, lentamente, e no devem ficar gotas presas no gargalo. O
ajustamento do menisco ao trao de referncia dever ser feito com a maior preciso possvel. Fecha-
se bem o balo e vira-se o mesmo de cabea para baixo, vrias vezes, agitando-o, para
homogeneizar o seu contedo. Antes de ser usado, o balo volumtrico deve ser bem lavado com
detergente e bem enxaguado. Raramente eles precisam ser secos. Se for necessria a secagem, esta
deve ser feita com o balo emborcado de cabea para baixo. A colocao de um tubo de vidro ligado
a uma trompa de vcuo dentro do balo pode ser feita para acelerar o processo de secagem.
*Transferncia quantitativa de lquido para um balo volumtrico. Quando estamos
preparando uma soluo padro, toda e qualquer perda de soluto acarretar em erros na anlise. Por
isso, devemos ter o mximo de cuidado para no ocorrer perdas de massa nos processos de
transferncias de um frasco para outro. Caso seja necessrio, insira um funil no balo volumtrico.
Use um basto de vidro para direcionar o fluxo do lquido do bquer para o funil. Retire a ltima gota
de lquido do bquer com a ajuda do basto de vidro. Enxge tanto o basto como o interior do
bquer com o solvente e transfira a "gua de enxge" para o balo volumtrico. Repita este processo
de enxge pelo menos duas vezes mais.
2. Pipetas: Existem duas espcies de pipetas:
a) Pipetas volumtricas ou de transferncia, construdas para dar escoamento, a um determinado
volume (Fig. 5B).
As pipetas volumtricas so constitudas por um tubo de vidro com um bulbo na parte central. O trao
de referncia gravado na parte do tubo acima do bulbo. A extremidade inferior afilada e o orifcio
deve ser ajustado de modo que o escoamento no se processe rpido demais, o que faria com que
pequenas diferenas de tempo de escoamento ocasionassem erros apreciveis. As pipetas
volumtricas so construdas com as capacidades de 1, 2, 5, 10, 20, 50, 100 e 200 mL, sendo de uso
mais freqente as de 10, 25 e 50 mL.
b) Pipetas graduadas ou cilndricas que servem para escoar volumes variveis de lquidos (Fig. 5A).
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
8
As pipetas graduadas consistem de um tubo de vidro estreito, geralmente graduado em 0,1mL. So
usadas para medir pequenos volumes lquidos. Encontram pouca aplicao sempre que se quer medir
volumes lquidos com elevada preciso. Tm a vantagem de se poderem medir volumes variveis.
Para se encher uma pipeta, coloca-se a ponta da mesma no lquido e
faz-se a suco com a pra de suco (NO usar a boca para
pipetagem em laboratrios). Deve-se ter o cuidado em manter a ponta
da mesma sempre abaixo do nvel da soluo do lquido. Caso
contrrio, ao se fazer a suco, o lquido alcana a pra de suco. A
suco deve ser feita at o lquido ultrapassar o trao de referncia.
Feito isto, tapa-se a pipeta com o dedo indicador (ligeiramente mido) -
caso no se esteja usando a pra de suco - e deixa-se escoar o
lquido lentamente at o trao de referncia (zero). O ajustamento deve
ser feito de maneira a evitar erros de paralaxe.
Os lquidos que desprendem vapores txicos e os lquidos corrosivos
devem sempre ser introduzidos na pipeta, atravs de pras de suco.
Para escoar os lquidos, deve-se colocar a pipeta na posio vertical,
com a ponta encostada na parede do recipiente que vai receber o
lquido; caso esteja usando a boca na pipetagem (tcnica
desaconselhvel), levanta-se o dedo indicador at que o lquido escoe
totalmente. Esperam-se 15 ou 20 segundos e retira-se a gota aderida a
ponta da pipeta, encostando-a a parede do recipiente (Figura 6).
i) Pipetas com escoamento total: contm duas faixas na parte superior, indicando que as mesmas
so calibradas para - assoprando-se at a ultima gota - liberar sua capacidade total.
ii) Pipetas com esgotamento parcial: contm na parte superior uma faixa estreita que as diferencia
das pipetas de escoamento total. No precisa ser assoprada (vide figura 6- letra D).
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
9
3- Buretas
As buretas servem para dar escoamento a volumes variveis de lquidos. So constitudas de
tubos de vidro uniformemente calibrados, graduados em 1mL e 0,1 mL. So providas de dispositivos,
torneiras de vidro ou polietileno entre o tubo graduado e sua ponta afilada, que permitem o fcil
controle de escoamento
As buretas podem ser dispostas em suportes universais contendo mufas (Figura 7).
As buretas de uso mais constantes so as de 50 mL, graduadas em dcimos de mL; tambm
so muito usadas as de 25 mL.
Nos trabalhos de escala semimicro, so freqentemente usadas as buretas de 5 e 10 mL,
graduadas em 0,01 ou 0,02mL.
Para o uso com solues que possam sofrer o efeito da luz, so recomendadas buretas de
vidro castanho.
As torneiras das buretas, quando forem de vidro, devem ser levemente lubrificadas para que
possam ser manipuladas com mais facilidade. Serve para este fim uma mistura de partes
iguais de vaselina e cera de abelhas; misturas especiais so encontradas no comrcio.
RECOMENDAES PARA USO DA BURETA
a) A bureta limpa e vazia deve ser
fixada em um suporte na posio
vertical.
b) Antes de se usar um reagente
lquido, deve-se agitar o frasco
que o contm, pois no raro
haver na parte superior do
mesmo, gotas de gua
condensada.
c) A bureta deve ser lavada, pelo
menos uma vez, com uma
poro de 5 mL do reagente em
questo, o qual dever ser
adicionado por meio de um funil,
em buretas que no possuam
gargalo especial; cada poro
deixada escoar completamente
antes da adio da seguinte.
d) Enche-se ento a bureta at um
pouco acima do zero da escala e
remove-se o funil.
e) Abre-se a torneira para encher a
ponta ou expulsar todo o ar e,
deixa-se escoar o lquido, at
que a parte inferior do menisco
coincida exatamente com a diviso zero (Figura 7). Quando se calibra a bureta (acerto do
zero) deve-se tomar o cuidado de eliminar todas as bolhas de ar que possam existir.
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
10
f) Coloca-se o frasco que vai receber o lquido sob a bureta e deixa-se o lquido
escoar, gota a gota, geralmente a uma velocidade no superior a 10 mL por minuto.
Controla-se a torneira da bureta com a mo esquerda (Figura 8). Aps o
escoamento da quantidade necessria de lquido, espera-se de 10 a 20 segundos e
l-se o volume retirado.
Notas:
1. Se ainda no estiver habituado com uma titulao, aconselhvel preparar uma amostra extra.
Nenhum cuidado tomado neste caso, j que sua funo a de determinar somente o valor
aproximado do ponto final da titulao. Este procedimento de sacrificar uma amostra freqentemente
resulta em ganho no tempo total de anlise.
2. Adies menores do que uma gota podem ser feitas permitindo que um pequeno volume de
titulante forme-se na ponta da bureta (na forma de uma gota suspensa) e ento encosta-se a ponta na
parede interna do erlen. Esta gota ento combinada com o resto do lquido, como descreve a nota 3.
Este procedimento chamado de tcnica da meia-gota.
3. Ao invs de ser enxaguado perto do ponto final da titulao, o erlen pode ser inclinado e rodado de
forma que o lquido capture qualquer gota que fique aderida nas paredes internas do erlen.
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
11
PREPARO E PADRONIZAO DE SOLUES
Em anlise volumtrica, a concentrao ou massa da amostra determinada a partir do
volume da soluo titulante de concentrao conhecida. Qualquer erro na concentrao da soluo
titulante levar a um erro na anlise.
O processo da adio da soluo padro at que a reao esteja completa chamado de
TITULAO. O reagente de concentrao exatamente conhecida chamado de titulante e a
substncia a ser determinada chamada titulada. Sabendo-se qual a quantidade da soluo padro
necessria para reagir totalmente com a amostra e a reao qumica envolvida calcula-se a
concentrao da substncia analisada.
O ponto exato onde a reao completa-se chamado de ponto de equivalncia ou ponto
final terico.
Na prtica, o trmino da titulao percebido por alguma modificao fsica provocada pela
prpria soluo ou pela adio de um reagente auxiliar, conhecido como indicador. O ponto em que
isto ocorre o ponto final da titulao. Esse o ponto experimental no qual sinalizado o final da
titulao (final da reao entre o titulante ou titulado).
A determinao da concentrao do titulante deve ser realizada, preferencialmente, atravs
do mesmo mtodo que ser aplicado na anlise, neste caso a titulao de neutralizao, mas ela
aplica-se s outras volumetrias, gravimetria e mtodos instrumentais.
Em qualquer reao estequiomtrica, o nmero de equivalentes dos reagentes devem ser
iguais. Partindo-se desse princpio, temos:
A + B C, onde A a amostra e B o titulante
neq
A
= neq
B
m
A
/Eq
A
= N
B
. V
B
ou N
A
. V
A
= N
B
. V
B
,
dependendo se foi realizada a medida de massa da amostra ou volume de uma soluo desta.
A soluo padro a ser usada em uma anlise volumtrica deve ser cuidadosamente
preparada, pois, caso contrrio, a determinao resultar em erros. A preparao dessas solues
requer direta ou indiretamente, o uso de um reagente quimicamente puro e com composio
perfeitamente definida. Os reagentes com essas caractersticas so chamados de padres
primrios.
Substncias padres primrios
Uma substncia padro primrio deve satisfazer os seguintes requisitos:
1. Deve ser de fcil obteno, purificao, secagem (preferivelmente a 110-120C), preservao
no estado de pureza (este requisito no geralmente satisfeito pelas substncias hidratadas,
porque difcil de remover completamente a umidade superficial sem que haja uma
decomposio parcial).
2. A substncia deve ser inaltervel ao ar durante a pesagem; esta condio implica que no
seja higroscpico, nem oxidvel ao ar, nem afetada pelo dixido de carbono. O padro dever
manter a sua composio imutvel durante o armazenamento.
3. A determinao de impurezas deve ser possvel e no deve, em geral, exceder a 0,01- 0,02%.
4. A substncia dever ser prontamente solvel sob as condies em que utilizada.
5. A reao com o soluo dever ser estequiomtrica e praticamente instantnea. O Erro de
titulao dever ser desprezvel, ou de fcil determinao.
6. Exemplos: Na
2
CO
3
, KHC
8
H
4
O
4
, NaCl, K
2
Cr
2
O
7
, KIO
3
, KBrO
3
, Na
2
C
2
O
4
.
Solues Padres
Mtodo direto: so as solues preparadas a partir da dissoluo, em balo volumtrico, de
quantidade exata de padro primrio.
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
12
Mtodo Indireto (padronizao): prepara-se uma soluo com concentrao aproximada desejada e,
depois, determina-se a concentrao exata pela determinao de sua capacidade de reao contra
um padro primrio.
VOLUMETRIA DE NEUTRALIZAO
1. Preparo de uma soluo padro do tipo direto de Na
2
CO
3
0,05mol/L
Introduo: o carbonato de sdio um padro primrio muito utilizado para padronizao de solues
cidas. O seu peso molecular de 106g/mol. O referido carbonato para fins analticos contm
umidade, devendo ser dessecado por meio de aquecimento com o cuidado para que no haja
rompimento de suas ligaes e produo de gs carbnico:
Na
2
CO
3
+ aquecimento a 300 Na
2
O + CO
2
Procedimento
Pesar, com mxima exatido, 5,3000g de carbonato de sdio anidro PA, previamente
dessecado a 200C, durante 1 hora. Transferir para um bquer e dissolver bem com gua deionizada
e, em seguida, transferir para um balo de 1 litro, evitando qualquer perda, com inmeras guas de
lavagens.
2. Preparo de uma soluo padro do tipo indireto de HCl 0.1mol/L
Determinar o volume necessrio de HCl concentrado (d = 1,15g/cm
3
e T= 30%) para preparar
250mL de soluo 0,1M de HCl. Despejar lentamente o volume de HCl calculado sobre um pouco de
gua deionizada em um balo volumtrico de 250mL de capacidade. Completar o volume at a marca
com gua deionizada. Homogeneizar a soluo conforme tcnica adequada citada anteriormente, ou
em caso de dvida solicite ajuda do professor. Transferir a soluo quantitativamente para o frasco
reagente** para posterior padronizao.
**Transferncia quantitativa para frasco reagente: abrimos aqui um parnteses para fornecer
algumas informaes a respeito das transferncias de solues prontas para frascos reagentes, j
que iremos muitas vezes, durante este curso, realizar tal procedimento.
Os frascos utilizados para acondicionar as solues preparadas so geralmente frascos de
vidro na cor mbar providos ou no de batoque (uma proteo plstica colocada antes da tampa nos
frascos, para uma melhor vedao). O frasco deve ser previamente lavado com detergente e
enxaguado com gua da torneira. Aps, lava-se com pelo menos trs pores de gua deionizada o
interior do frasco.
- Transferindo uma soluo padro: se a soluo do balo volumtrico que temos que
transferir for uma soluo padro, devemos contaminar o interior do frasco reagente com,
no mnimo, trs pores da soluo. Normalmente, gasta-se para tal, um volume de
soluo correspondente ao que est no gargalo do balo.
- Transferindo uma soluo a ser padronizada: se no balo houver uma soluo que iremos
padronizar posteriormente, podemos transferir o contedo do balo com o frasco reagente
umidecido com gua deionizada, sem que acarrete erros futuros, j que iremos padronizar
esta soluo.
Ao final, devemos rotular o frasco reagente, indicando o nome da soluo preparada, sua
concentrao exata (soluo padro) ou aproximada (soluo a ser padronizada), o nome do
preparador e a data em que foi produzida.
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
13
2.1. Padronizao da soluo de HCl utilizando soluo padro Na
2
CO
3
0,05M
Com Pipeta volumtrica, pipetar 10mL de Na
2
CO
3
0,05M, exatamente medidos, e transferir
para um frasco de erlenmeyer e acrescentar uma gota de alaranjado de metila. O alaranjado de metila
(conhecido tambm como metilorange) em meio alcalino fica com cor amarela e em meio cido fica
com cor avermelhada. Colocar na bureta o HCl 0,1M a ser padronizado, tendo o cuidado de lavar a
bureta com pores de 5mL de HCl e no deixar bolhas de ar no bico da bureta. Gotejar o cido no
erlenmeyer sob constante agitao. O HCl em contato com o carbonato vai nos dar a seguinte reao:
2HCl + Na
2
CO
3
2NaCl + H
2
CO
3
Gotejar HCl at que a colorao comece a desviar da inicial, o ponto de equivalncia ainda
no foi alcanado. A presena de H
2
CO
3
(cido carbnico) na reao antecipa o ponto final, ento
deve-se ferver a soluo durante dois minutos com a finalidade de romper o cido carbnico em H
2
O
e CO
2
.
H
2
CO
3
H
2
O + CO
2
Esfriar a soluo em gua corrente e continuar a titulao at que a colorao comece a
desviar para um alaranjado mais escuro. Anotar o volume de HCl gasto e repetir o procedimento por
mais duas vezes, no mnimo. Calcular a molaridade do HCl por intermdio da equao da diluio
usando a mdia aritmtica dos valores mais prximos.
2.2. Padronizao da soluo de HCl utilizando Tetraborato de Sdio
Pese, por diferena, em balana analtica cerca de 0,7 a 0,8g de tetraborato de sdio, brax
(Na
2
B
4
O
7
.10H
2
O; MM = 381,37g/mol) para dentro de um erlenmeyer de 250mL. Dissolva com
aproximadamente 50mL de gua destilada e adicione trs gotas do indicador misto (verde de
bromocresol + vermelho de metila). Titule com a soluo de HCl a padronizar at a soluo tornar-se
incolor. Repita o procedimento por mais duas vezes e calcule a molaridade da soluo de HCl.
3. Preparo de uma soluo padro do tipo indireto de NaOH 0,1mol/L
Determine a massa de NaOH necessria para preparar 250mL de soluo 0,1M. Despeje o
contedo de NaOH pesado para um erlenmeyer contendo pequena quantidade de gua deionizada e,
ento, dissolva bem com o auxlio do basto de vidro. Transferir quantitativamente a soluo para
dentro de um balo de 250mL e completar marca com gua deionizada. Homogeneizar conforme
tcnica descrita pelo professor. Aps, transferir a soluo para um frasco previamente limpo e rotular.
3.1. Padronizao da soluo de NaOH utilizando soluo padro HCl 0,1 mol/L
Com pipeta volumtrica, pipetar 10mL de soluo padro de HCl 0,1M preparada
anteriormente e transferir para um erlenmeyer limpo e acrescentar 3 gotas de fenolftalena. A
fenolftalena em meio cido fica incolor, enquanto em meio alcalino adquire colorao rsea (solicite
explicao do professor para entender melhor). Titular o contedo do erlenmeyer, colocando o NaOH
na bureta. O ponto final evidenciado pelo aparecimento de uma leve cor rsea persistente por mais
de 30 segundos. Caso seja obtida uma colorao muito forte, despreze a amostra. Anotar o volume
de NaOH gasto e calcular a molaridade da soluo atravs da equao fundamental da anlise
volumtrica (M
1
V
1
= M
2
V
2
).
3.2. Padronizao da soluo de NaOH utilizando Biftalato de Potssio
Pese, por diferena, em balana analtica cerca de 0,7 a 0,9g de Biftalato de Potssio (KHC
8
H
4
O
4
; MM
= 204,23 g/mol), previamente dessecado a 110 120C, para dentro de um erlenmeyer de 250mL.
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
14
Dissolva com aproximadamente 50mL de gua destilada (de preferncia recm fervida e resfriada).
Adicione duas gotas de fenolftalena e titule com a soluo de NaOH a padronizar at o aparecimento
de colorao rsea permanente por 30 segundos. Repita o procedimento por mais duas vezes e
calcule a molaridade da soluo de NaOH.
Questes
1. O que soluo padro? Por que nem todas as solues so padres?
2. O que padronizao? Quando ela necessria?
3. O que padro primrio? Quais os requisitos para que uma substncia seja um padro
primrio? Por que preciso sec-lo antes de sua utilizao?
4. Por que NaOH e HCl no so padres primrios?
5. O que transferncia quantitativa?
6. Quais dos equipamentos utilizados nestas prticas devem estar necessariamente secos:
esptula, recipiente de pesagem, balo volumtrico, basto de vidro, funil, pipeta, erlenmeyer
e bureta.
7. Quais so as fontes de erros no preparo e padronizao de solues?
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
15
Experimento 1:
Determinao do teor de cido actico no vinagre
O cido actico e um cido fraco, Ka de 1,8 x 10
-5
, apresenta-se como um lquido incolor, com
odor caracterstico de vinagre. totalmente solvel em gua, lcool etlico e na maioria dos solventes
orgnicos, amplamente usado em qumica industrial na forma de cido actico glacial 99,8% (m/m)
densidade 1,053 g/mL ou em solues de diferentes concentraes. Na indstria alimentcia
consumido como vinagre, que uma soluo diluda de cido actico glacial
(3,5 a 8% m/v).
Procedimento:
- Colocar com auxlio de uma pipeta volumtrica, 10 mL de vinagre em balo volumtrico de
100,0 mL e diluir at a marca com gua deionizada;
- Retirar uma alquota de 10,0 mL com uma pipeta calibrada e transferir para um
erlenmeyer de 125 mL;
- Adicionar aproximadamente 20 mL de gua destilada no erlenmeyer;
- Adicionar 3 a 5 gotas do indicador fenolftalena;
- Titular esta mistura com uma soluo padro de NaOH 0,1 mol/L contida numa bureta,
com agitao at a aparecimento de um leve rseo persistente na soluo do erlenmeyer;
- Anote o volume gasto na titulao;
- Repetir o procedimento para outra alquota de vinagre e calcular o teor mdio de acido
actico no vinagre;
- Repita o mesmo procedimento para outras alquotas de vinagre.
Questes:
1. Escreva as equaes correspondentes s reaes observadas.
2.
Calcular a molaridade do cido actico utilizando M
1
V
1
=M
2
V
2
3. Calcule a concentrao, em g/L do cido actico no vinagre.
4. Qual o teor de cido actico no vinagre analisado?
5. possvel usar o alaranjado de metila como indicador nesta titulao de vinagre? Elabore
uma explicao.
6. Suponha que uma soluo de cido clordrico consome a mesma quantidade de uma soluo
padro de NaOH por unidade de volume que um vinagre comercial. Ignorando o aspecto da
diferena no gosto, porque seria inaceitvel o uso de cido clordrico no preparo de um molho
de salada.
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
16
Experimento 2:
Determinao da acidez total de vinhos
Sabe-se que a acidez dos vinhos se deve a presena de cidos como o tartrico, mlico e
ctrico, entre os mais importantes. Estes cidos garantem a conservao do vinho bem como outras
caractersticas de suma importncia. O grau de acidez est tambm relacionado com a acidez total
titulvel, o pH, a quantidade de cidos dissociados e no dissociados, e a quantidade relativa de cada
um dos cidos presentes. Dentro dos padres comerciais, a acidez do sumo fica no intervalo de 0,6 a
0,9% (expresso como a quantidade de cido tartrico por 100mL de sumo ou vinho). Os vinhos doces
tm acidez no intervalo de 0,4 a 0,65%. Na fabricao do vinho importante saber a acidez titulvel
do mosto para poder determinar a quantidade correta de dixido de enxofre que ser adicionada e
tambm decidir se ou no necessria uma correo da acidez.
Esta determinao est sujeita interferncia do CO
2
dissolvido. Este erro pode ser
minimizado diluindo o vinho com gua quente, prximo da fervura, e depois deixando esfriar at a
temperatura ambiente antes de titular. Geralmente esse erro pequeno.
Procedimento:
Transferir 25mL de um vinho branco seco para um erlenmeyer de 250mL. Adicionar 100mL de
gua deionizada e 5 gotas de soluo alcolica de fenolftalena a 1%. Titular com uma soluo padro
de NaOH 0,1M. O ponto final indicado pela permanncia de uma leve cor rsea por mais de 30
segundos.
Repetir o procedimento acima para o vinho tinto, com o cuidado de que o ponto final
evidenciado pelo aparecimento de uma cor cinza-esverdeada.
A acidez titulvel do vinho normalmente expressa em cido tartrico %(m/v); massa molar
do C
2
H
4
O
2
(COOH)
2
= 150,09g/mol. Lembrar que o cido tartrico tem dois hidrognios titulveis at a
viragem da fenolftalena.
cido tartrico (g/100mL) = (V
b
) . (M
NaOH
) . (150,09) . (100)
(1000) . 2 . (V
am
)
onde:
V
b
o volume, em mL, da soluo de NaOH usada na titulao
M
NaOH
a concentrao da soluo de NaOH, em mol/L.
V
am
o volume, em mL, da amostra titulada
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
17
Experimento 3:
Determinao do teor de cido ctrico no suco dos frutos ctricos
Procedimento:
Espremer os frutos ctricos de maneira a obter seu suco para anlise. De posse do suco,
retirar uma alquota de 2mL e transferir para um erlenmeyer de 125mL. Adicionar 5mL de gua
deionizada e 2 gotas de fenolftalena. Titular com NaOH 0,1mol/L preparado anteriormente at o
aparecimento de uma leve colorao rsea persistente.
Fruto Volume de NaOH gasto Teor de cido ctrico
Reao que ocorre no processo:
Clculos:
1) Quantidade de cido ctrico
1mL de NaOH 0.007g c. Ctrico
XmL Yg de c. Ctrico
2) Teor de cido ctrico presente na amostra
2mL suco Yg de c. Ctrico
100mL suco Zg c. Ctrico
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
18
Experimento 4:
Determinao do teor de hidrxido de magnsio no leite de magnsia
RETROTITULAO
Uma titulao consiste na determinao da quantidade de uma espcie qumica (substncia
ou on) em soluo, medindo-se a quantidade de um reagente (de concentrao conhecida)
necessria para reagir completamente com a espcie qumica. Entretanto, algumas vezes, a espcie
qumica em soluo ou a reao utilizada tem caractersticas que no recomendam a titulao direta
desse modo. o que ocorre com o hidrxido de magnsio, que, por ser pouco solvel, faz com que
a determinao do ponto de equivalncia seja difcil. Para evitar este problema, o procedimento
adotado fazer com que a reao de neutralizao do hidrxido de magnsio ocorra totalmente
atravs de uma quantidade excessiva (perfeitamente conhecida) de soluo cida padro. Em
seguida, o excesso de cido (que no reagiu com o hidrxido de magnsio) titulado com uma
soluo bsica padro. Esse procedimento de determinao da quantidade em excesso conhecido
como RETROTITULAO.
A seguir, est descrito sucintamente o princpio do mtodo:
1. amostra adicionado excesso (V
a
) de soluo padro de cido (M
a
), ocorrendo a seguinte
reao:
Mg(OH)
2
+ 2HCl MgCl
2
+ 2H
2
O + HCl
exc
2. O excesso de cido titulado com soluo padro de NaOH:
HCl
exc
+ NaOH NaCl + H
2
O
3. Clculos:
a) Calcular o nmero de mol de NaOH que reagiu com o HCl: n NaOH = M NaOH . VNaOH
b) Calcular o nmero total de mols de HCl: n HCl TOTAL = M HCl . V HCl
c) Calcular o nmero de mols de HCl que reagiu com Mg(OH)
2
:nHCl (Mg(OH)2) =nHCl TOTAL nHCl (NaOH)
d) Calcular o nmero de mols do Mg(OH)
2
: 2 mol HCl ------------1 mol Mg(OH)
2
nHCl (Mg(OH)2)---------- x
e) Calcular a massa de Mg(OH)
2
: m Mg(OH)2
= x . 58g/mol
f)Calcular a porcentagem de Mg(OH)
2
presente na amostra: m Mg(OH)2 . 100 / m amostra
Procedimento:
- Agitar vigorosamente o frasco de leite de magnsia.
- Pesar imediatamente, com o auxlio de um conta gotas, no mais que 1,0g da amostra em
um erlenmeyer.
- Adicionar, com uma pipeta volumtrica de 25mL, exatamente 50mL de soluo padro de
HCl 0,1 mol/L, em duas etapas, e agitar o erlen at dissolver completamente
- Adicionar 3 gotas de fenolftalena ou vermelho de metila e titular com soluo padro de
NaOH 0,1 mol/L.
- Repetir o procedimento pelo menos mais uma vez.
- Calcular a porcentagem de hidrxido de magnsio no leite de magnsia
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
19
Questes:
1. Qual a diferena entre amostra homogneas e heterogneas? D um exemplo de cada uma.
2. Por que necessrio realizar a abertura da amostra por dissoluo com cido em lugar de
realizar a titulao diretamente na amostra?
3. O que titulao direta? E retrotitulao ou titulao de retorno?
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
20
A soluo que
sobrar na bureta
deve ser
acondicionada
em frasco para
resduos de
prata.
ppt branco
soluo amarela ppt vermelho
VOLUMETRIA DE PRECIPITAO
A volumetria de precipitao envolve a reao na qual forma-se um produto de baixa
solubilidade. Sua principal aplicao est na determinao de haletos e alguns ons metlicos. A
curva de titulao e a determinao do ponto final so grandemente afetadas pela diluio das
solues e solubilidade do produto.
A reao deve processar-se praticamente de forma quantitativa no ponto de equivalncia,
completar-se em tempo relativamente curto e oferecer condies para uma sinalizao do ponto final.
O titulante mais empregado a soluo padro de AgNO
3
(Argentimetria: anlise volumtrica
que utiliza AgNO
3
como reagente). O ponto final pode ser determinado de trs formas diferente:
Formao de um slido colorido (ex: mtodo de Mohr).
Formao de um complexo solvel (ex: mtodo de Volhard).
Mudana de cor associada com a adsoro de um indicador sobre a superfcie de um slido (ex:
mtodo de Fajans).
1. A determinao de cloreto, pelo Mtodo de Mohr um processo de precipitao fracionada:
primeiro precipita o analito (AgCl precipitado branco), no ponto final precipita o indicador (AgCrO
4
precipitado vermelho) a partir do qual, detecta-se o final da titulao. As reaes envolvidas so as
seguintes.
Ag
+
+ Cl
-
AgCl
(s)
Kps = 1,82 . 10
-10
2 Ag
+
+ CrO
4
2-
Ag
2
CrO
4
(s) Kps = 1,7 . 10
-12
Como a solubilidade do AgCl menor do que a do Ag
2
CrO
4
, o cloreto precipita primeiro.
Para que o ponto final seja visualizado preciso adicionar-se um excesso de titulante, tornando
necessria realizao de um branco (V
b
) que deve ser descontado do resultado da titulao da
amostra (V
a
).
A porcentagem de cloreto pode ser assim determinada:
V
Ag+
= V
a
- V
b
volume gasto na titulao do Cl
-
neq
Cl-
= neq
Ag+
n Cl
-
= n Ag
+
m
Cl
-
/MM
Cl
-
= M Ag
+
. V
Ag
+
% = (m
Cl
-
. 100)/ V
amostra
2. O Mtodo de Volhard um procedimento indireto para determinao de ons que precipitam com
a prata. O excesso de prata determinado por meio de titulao, com uma soluo padro de
tiocianato de potssio ou de amnio usando-se ons ferro(III) como indicador.
3. Mtodo de Fajans Indicadores de Adsoro: so compostos orgnicos que tendem a adsorver
(por interaes eletrostticas) sobre a superfcie do precipitado formado durante a titulao,
provocando uma alterao na colorao do precipitado). Ex: fluorescena utilizada na titulao de
cloreto com Nitrato de prata.
Preparao e padronizao ( via Mtodo de Mohr) de uma soluo de AgNO
3
0,05mol/l
Preparao: Pesar, com mxima exatido, 2,1234g de AgNO
3
P.A., previamente dessecado a 105C,
por 1 hora, dissolver em gua deionizada e avolumar em balo de 250mL. Transferir a soluo para
frasco mbar para evitar o contato com a luz (reduo da prata).
O resduo dever ser filtrado em um
funil disponvel em local indicado
pelo professor.
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
21
Padronizao:
Medir 5mL de soluo padro de cloreto de sdio 0,1000M e colocar em erlenmeyer.
Adicionar 10mL de gua deionizada, 1mL de cromato de potssio 5% como indicador e titular com a
soluo de nitrato de prata a ser padronizada mediante bureta, sob constante agitao, at colorao
vermelho-tijolo. A titulao s deve prosseguir at este ponto, onde verificamos uma leve, mas ntida,
mudana de colorao que deve permanecer aps vigorosa agitao.
Prova em branco:
o volume de gua deionizada igual ao volume final da soluo antes titulada, adicionam-se
1mL de cromato de potssio e 0,5g de carbonato de clcio e titula-se com nitrato de prata at que a
colorao seja igual da soluo resultante da titulao com cloreto de sdio.
A correo pela prova em branco, que no ser maior do que 0,03 a 0,10mL de nitrato de
prata que se subtrai do volume utilizado na titulao do cloreto de sdio. Repete-se a titulao com
outras duas pores de NaCl padro. As titulaes devem concordar em 0,1mL.
Questes:
1. Quais os requisitos para que uma reao possa ser empregada em volumetria de precipitao?
2. Escreva as reaes envolvidas no procedimento para determinao de haletos que precipitam
com a prata usando o mtodo de Mohr.
3. Por que se utiliza uma titulao em branco na titulao pelo mtodo de Mohr?
4. Defina: precipitao, solubilidade, produto de solubilidade.
5. Uma soluo contendo 0,205 g de NaCl e KCl gastou cerca de 30 mL de uma soluo de AgNO
3
0,10 mol/L para completa precipitao do on cloreto. Calcule o teor de cada sal na mistura.
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
22
A soluo que
sobrar na bureta
deve ser
acondicionada
em frasco para
resduos de
prata.
Experimento 5:
Determinao de Cloreto em Soro fisiolgico
Medir, em pipeta volumtrica, 10 mL de uma soluo de soro fisiolgico (0,9%) e transferir
para um erlenmeyer de 125mL. Adicionar 10 mL de gua e 1 mL de indicador cromato de potssio
5%. Titular com soluo padro de AgN0
3
a 0,05mol/L at mudana de cor de amarelo para vermelho-
tijolo. Repetir a anlise de soro por mais duas vezes. No esquecer de efetuar uma prova em branco
para subtrair do volume gasto na titulao do soro.
Clculo:
mg/L CI
-
= (A-B) x M x 35453
10
Onde:
A =mL gastos de Nitrato de Prata para a amostra.
B =mL gastos de Nitrato de Prata para a prova em branco.
M =Molaridade do Nitrato de Prata.
1) Calcular a porcentagem de NaCl e Cl
-
no soro e comparar com os dados da embalagem.
O resduo dever ser filtrado em um
funil disponvel em local indicado
pelo professor.
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
23
VOLUMETRIA DE OXI-REDUO:
Um processo no qual h transporte de eltrons chama-se de OXI-REDUO; a substncia
que fornece eltrons oxidada enquanto a substncia receptora reduzida. Em outras palavras um
agente oxidante combina com os eltrons e reduzido, ao passo que o agente redutor fornece os
eltrons, sendo oxidado.
A oxidao e reduo devem evidentemente ter lugar simultaneamente, pois numa reao
deste tipo o agente oxidante sempre reduzido e o agente redutor sempre oxidado no mesmo grau,
formando um sistema de oxi-reduo.
A volumetria de oxi-reduo trata da titulao de um agente oxidante com uma soluo de
um redutor e vice-versa. Este tipo de determinao compreende um grande nmero das anlises
volumtricas, devido ao grande nmero de substncias susceptveis de sofrer oxidao e reduo.
Para fins didticos pode-se dividir a volumetria de oxi-reduo em:
a) IODOMETRIA: em que a soluo padro uma soluo de tiossulfato de sdio, Na
2
S
2
O
3
. Aplica-
se para determinaes de cromo, cobre, gua oxigenada, hipocloritos e outros.
b) PERMANGANOMETRIA: em que a soluo padro usada permanganato de potssio, KMnO
4
.
Aplica-se para determinaes de ferro, mangans, clcio, gua oxigenada, e outros elementos.
c) DICROMATOMETRIA: em que a soluo padro dicromato de potssio, K
2
Cr
2
O
7
. Aplica-se
principalmente em anlise de ligas de minrio de ferro.
Como o dicromato de potssio gera resduo de alta toxidez ao meio ambiente, necessitando de
um tratamento especfico, vamos realizar experimentos apenas dos dois primeiros mtodos.
1. MTODOS ENVOLVENDO O IODO, I
2
: IODOMETRIA E IODIMETRIA
As aplicaes do iodo como reagente redox so bastante extensas, principalmente, porque:
(1) o potencial padro de reduo do par I
2
/I
-
intermedirio, e alm disso, pode agir como um agente
oxidante na forma de I
2,
ou como agente redutor na forma de I
3
-
;
(2) o
0
/
2
I I
E praticamente independente da acidez do meio at pH<8.
O par redox iodo/iodeto pode ser caracterizado pela semi- reao,
I
2
+ 2 2I
-
0
/
2
I I
E = 0,535V
indicando que o iodo um oxidante moderado e o iodeto um redutor relativamente fraco. O iodo
quantitativamente reduzido a iodeto em meio neutro, por redutores moderadamente fortes, como
Sn(II), H
2
SO
3
, SO
2
, H
2
S e o iodeto quantitativamente oxidado a iodo por oxidantes moderados ou
fortes, como H
2
O
2
, IO
3
-
, IO
4
-
, Cr
2
O
7
2-
, MnO
4
-
e CIO
-
.
H dois modos analticos na aplicao na qumica do iodo em titulaes de oxi-reduo:
1. IODIMETRIA (mtodo iodimtrico) : o constitunte em anlise redutor titulado diretamente com
soluo padro de iodo (para produzir iodeto) em meio levemente cidos ou levemente bsicos.
2. IODOMETRIA (mtodo iodomtrico): o constituinde em anlise oxidante adicionado ao I
-
(que
utilizado como redutor) em excesso para produzir iodo. O iodo liberado na reao associada ento
titulado, em meio neutro ou levemente cido, com soluo padro de tiossulafto de sdio (redutor).
Em resumo, a Iodimetria a titulao com o I
3
-
. A Iodometria a titulao do I
3
-
.
Os dois mtodos esto baseados:
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
24
(a) no fato de que o iodo na presena de iodeto produz o on triiodeto:
I
2(s)
+ I
-
I
3
-
K = 7,1.10
2
(b) no par redox tiiodeto/iodeto,
I
3
-
+ 2e
-
3I
-
E
0
I3
-
/I
-
= 0,536V
Pelo fato do potencial de reduo ser relativamente baixo, poucas substncias so oxidadas
pelo iodo, da a existncia de poucos mtodos iodimtricos. Por outro lado, muitas espcies so
capazes de oxidar o iodeto a iodo, resultando numa ampla variedade de mtodos indiretos ou
iodomtricos, onde a espcie de interesse quantitativamente reduzida em excesso de soluo de
iodeto liberando o eqivalente em iodo, e esse dosado por titulao com uma soluo padro de um
redutor. O mtodo iodomtrico mais vantajoso porque o iodo gerado in situ evitando perdas por
volatilizao, pois o iodo facilmente sublimvel.
Utilizao do Tiossulfato de Sdio
O tiossulfato de sdio o redutor mais empregado como titulante no iodo gerado nas
metodologias iodomtricas. Normalmente as solues so preparadas a partir do sal pentahidratado,
Na
2
S
2
O
3
.5H
2
O (MM = 248,18g/mol), e devem ser posteriormente padronizadas, pois este sal no se
enquadra como um padro primrio. Normalmente as solues devem ser preparadas com gua
destilada previamente fervida para eliminar o CO
2
dissolvido e tambm prevenir a decomposio do
tiossulfato por bactrias. de praxe adicionar algumas gotas de clorofrmio que funciona como um
eficiente preservativo. Alm disso, cerca de no mximo 0,1g/L de Na
2
CO
3
adicionada para garantir
uma leve alcalinidade na soluo, pois on S
2
O
3
2-
se decompe em meio cido, catalisado pela ao
da luz, liberando enxofre coloidal e conferindo uma turbidez na soluo. Por outro lado, hidrxidos de
metais alcalinos, Na
2
CO
3
> 0,1 g L
-1
e brax, no devem ser adicionados, pois tendem a acelerar a
decomposio sob ao do oxignio atmosfrico: S
2
O
3
2-
+ 2O
2
+ H
2
O 2SO
4
2-
+ 2H
+
. Assim, a
soluo deve ser armazenada em frasco escuro (mbar) logo aps a preparao.
O on tiossulfato (S
2
O
3
-2
) um agente redutor moderadamente forte. Na presena de iodo, o
on tiossulfato quantitativamente oxidado para formar o on tetrationato (S
4
O
6
-2
), de acordo com a
seguinte semi-reao:
2S
2
O
3
-2
) S
4
O
6
-2
+ 2e
-
O procedimento empregado na determinao de agentes oxidantes envolve a adio de um
excesso de iodeto de potssio a uma soluo levemente cida do analito. A reduo do analito produz
uma quantidade estequiometricamente equivalente de iodo. Ento o Iodo liberado titulado com uma
soluo padro de Na
2
S
2
O
3
. Um exemplo desse procedimento a determinao de hipoclorito de
sdio em alvejantes. As reaes so:
OCl
-
+ 2I
-
+ 2H
+
Cl
-
+ I
2
+ H
2
O
I
2
+ S
2
O
3
-2
2I
-
+ S
4
O
6
-2
Nessa prtica feita a dosagem de cloro-ativo numa amostra de alvejante a base de
hipoclorito de sdio ou clcio, a famosa gua sanitria, de uso domstico e em lavanderias. No
tratamento de gua de piscina, utiliza-se o hipoclorito de clcio, Ca(OCl)
2
misturado com cloreto de
clcio bsico, CaCl
2
.Ca(OH)
2
.2H
2
O.
O constituinte ativo responsvel pelo efeito alvejante e algicida, o on hipoclorito, o qual
instvel em meio cido. Por exemplo, sob ao de cido clordrico, ocorre a liberao de cloro:
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
25
OCl
-
+ 2H
+
+ Cl
-
Cl
2
+ H
2
O
O cloro-ativo de uma soluo alvejante a quantidade de cloro que pode ser liberado sob
ao de cido diludo, sendo expresso em %(m/v). No caso de amostras slidas, em %(m/m).
Portanto, por anlise qumica do contedo de hipoclorito, calcula-se por estequiometria a
concentrao em termos da porcentagem de cloro-ativo da amostra, e vice-versa. Esta forma de
expressar o teor de hipoclorito j se tornou corriqueira e est normatizada como padro de qualidade
de alvejantes a base de hipoclorito.
Utilizao da Goma de Amido
Em reaes redox envolvendo o Iodo como agente oxidante ou o iodeto como redutor, a goma
de amido utilizada como indicador sensvel, pois forma um complexo com o Iodo de colorao azul
intensa, e mesmo numa concentrao de 10
-5
mol L
-1
, o iodo pode ser detectado. Na presena de um
excesso de agente oxidante, a razo das concentraes de iodo e iodeto elevada fornecendo uma
cor azul para a soluo. Com o excesso de redutor, por outro lado, o on iodeto predomina e a cor
azul se faz ausente. A goma de amido no um indicador redox porque especfica presena de I
2
e no a uma modificao do potencial redox.
A frao ativa da goma de amido a amilose, um polmero do acar D glicose. O
polmero existe como uma hlice em espiral qual pequenas molculas podem se ajustar. Na
presena da goma de amido e de Iodeto, as molculas de Iodo formam cadeias de I
6
que ocupam o
centro da hlice da amilose. A cor azul escura da goma de amido-iodo surge da absoro visvel pela
ligao da cadeia de I
6
dentro da hlice.
O denominado amido solvel encontrado comercialmente e se dispersa facilmente em gua.
Uma vez que o amido susceptvel ao ataque por microorganismos, recomendvel preparar a
soluo no dia da anlise. Normalmente prepara-se soluo de amido solvel a 0,5 1,0%(m/v) e
adiciona-se cido brico como preservativo, para prolongar o tempo de vida til.
Importante:
Em Iodimetria (titulao com o I
3
-
), a goma de amido pode ser adicionada no incio da titulao. A
primeira gota de excesso de I
3
-
aps o ponto de equivalncia causa a mudana da cor da soluo para
azul escuro.
Em Iodometria (a titulao do I
3
-
), o on triiodeto est presente em toda a reao at o ponto de
equivalncia. A goma de amido no deve ser adicionada reao at que esteja imediatamente antes
do ponto de equivalncia onde a concentrao do iodo baixa. De outro modo, algum iodo tende a
permanecer ligado s partculas de goma de amido aps o ponto de equivalncia ser alcanado.
Ex.
O amido se decompe irreversivelmente em solues contendo concentraes elevadas de iodo.
Portanto, na titulao de solues de iodo com ons tiossulfato, como na determinao indireta de
oxidantes, a adio do indicador adiada (at que a maior parte do Iodo tenha sido reduzida) at que
a cor da soluo mude de vermelho-marrom para amarelo; nesse ponto, a titulao est quase
completa. O indicador pode ser adicionado ao sistema desde o incio quando solues de tiossulfato
esto sendo tituladas diretamente com o iodo.
Questes:
1. Para que os aspectos e procedimentos experimentais sejam bem assimilados, importante
compreender o significado dos termos seguintes. Descreva: Reao de oxi-reduo,
Estequiometria e Titulao redox.
2. Qual a diferena entre iodimetria e iodometria? Em qual tcnica, iodimetria ou iodometria, o
indicador goma de amido no adicionado at um pouco antes do ponto de equivalncia? Por
que?
3. Pesquise um pouco sobre o complexo amido-iodo.
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
26
Preparao da soluo padro 0,1M de Tiossulfato de sdio:
Procedimento:
Utiliza-se o sal penta hidratado para a produo da soluo de tiossulfato de sdio
(Na
2
S
2
O
3
.5H
2
O). Dissolvem-se 24,9g de tiossulfato hidratado e puro e 0,2g de Carbonato de sdio
anidro (Na
2
CO
3
utilizado para evitar precipitao do enxofre) em 1 litro de gua previamente fervida
(o CO
2
dissolvido torna a soluo cida e promove o desproporcionamento de S
2
O
3
-2
:
S
2
O
3
-2
+ H
+
HSO
3
-
+ S
(s)
Finalmente, deixa-se decantar por 24h e padroniza-se.
1. Padronizao com Iodato de Potssio(KIO
3
)
O Iodato de Potssio um excelente padro primrio para solues de tiossulfato. Nessa aplicao,
quantidades conhecidas do reagente de grau padro primrio so dissolvidas em gua contendo um
excesso de iodeto de potssio. Quando essa mistura acidificada com um cido forte, a reao
IO
3
-
+ 5I
-
+ 6H
+
3I
2
+ 2H
2
O
ocorre instantaneamente. Ento, o Iodo liberado titulado com a soluo de tiossulfato. A
estequiometra da reao : 1 mol de IO
3
-
= 3 mol de I
2
= 6 mol de S
2
O
3
-
.
Procedimento:
Pese, com exatido, de 0,12 a 0,17g de Iodato de Potssio (KIO
3
), previamente dessecado
(aquecimento em estufa a 150C 180C durante 1h) para dentro de um erlenmeyer de 250mL e
dissolva com 25mL de gua destilada. Adicione 2g de KI e agite at que a dissoluo seja completa.
Adicione 10mL de HCl 1M e titule, imediatamente, com a soluo de tiossulfato de sdio at que a
colorao da soluo torne-se amarela fraca. Ento, adicione 2mL de soluo de amido 0,5% e
prossiga a titulao at o desaparecimento da colorao azul. Repita o processo mais duas vezes.
Calcule a molaridade da soluo de tiossulfato de sdio.
2. Padronizao utilizando soluo padro de KMnO
4
0,02M
Adicionam-se 100mL de gua em 25mL de soluo padro de KMnO
4
0,02M e mistura-se
com soluo de iodeto de potssio (2g de KI dissolvidos completamente em 30mL de gua e 100mL
de H
2
SO
4
a 20%).
Goteja-se a soluo de Na
2
S
2
O
3
a ser padronizada na soluo de KMnO
4
padro at que a
colorao da soluo torne-se amarela fraca. Ento, adiciona-se 1mL da soluo de amido 1% e
titula-se at desaparecer a cor azul.
2KMnO
4
+ 3H
2
SO
4
+ 10KI K
2
SO
4
+ 2MnSO
4
+ 5I
2
+ 8H
2
O
Esta operao devera ser feita em local escuro e em temperatura de soluo menor do que 30C.
[Na
2
S
2
O
3
] = (VKMnO
4
) . (MKMnO
4
) . 5 . 2
2 . (VNa
2
S
2
O
3
)
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
27
Preparao de soluo 0,03M de Iodo
O iodo no muito solvel em gua (0,001mol/L). Para se obter solues de concentraes
analticas teis do elemento, o Iodo comumente dissolvido em solues moderadamente
concentradas de Iodeto de Potssio. Nesse meio, o Iodo razoavelmente solvel, em conseqncia
da reao
I
2(s)
+ I
-
I
3
-
K = 7,1.10
2
O iodo se dissolve lentamente em solues de KI, particularmente se a concentrao de
iodeto for baixa. Para garantir a completa dissoluo, o iodo sempre dissolvido em um pequeno
volume de uma soluo concentrada de KI. As solues preparadas pela dissoluo de Iodo em uma
soluo de KI so apropriadamente chamadas de solues de triiodeto.
As solues de Iodo no tm estabilidade por inmeras razes, uma delas a volatilidade do
soluto. As perdas de Iodo a partir de um frasco aberto ocorrem em um perodo relativamente curto,
mesmo na presena de um excesso de ons iodeto. Alm disso, o Iodo ataca a maioria de materiais
orgnicos vagarosamente. Conseqentemente, as rolhas ou tampas de borracha nunca so
empregadas para fechar os frascos de reagente.
Procedimento:
Pesam-se aproximadamente 1,9g de iodo puro em um vidro de relgio e transfere-se para um
bquer de 250mL contendo 5g de iodeto de potssio dissolvido em 25mL de gua. Agita-se
cuidadosamente para dissolver todo o iodo. Se necessrio, pode-se colocar mais um pouco de gua.
Transfere-se todo o contedo do bquer para um balo volumtrico de 250mL, completa-se at a
marca com gua deionizada e homogeneza-se. Aps, transfere-se todo o contedo do balo para
frasco mbar de 500mL.
Padronizao:
A padronizao pode ser feita titulando-se 10mL de soluo padro de Tiossulfato de sdio
0,1mol/L contra a soluo 0,03mol/L de iodo. Os 10mL de tiossulfato so transferidos com o auxlio de
uma pipeta volumtrica para um erlenmeyer de 125mL. Adiciona-se 1mL de soluo de amido 1% ao
erlenmeyer como indicador e titula-se at o aparecimento da cor azul.
I
2
+ 2Na
2
S
2
O
3
2NaI + Na
2
S
4
O
6
[I
2
] = (MNa
2
S
2
O
3
) . (VNa
2
S
2
O
3
)
2 . (VI
2
)
IODIMETRIA: Anlise de Comprimidos de Vitamina C
A vitamina C (C
6
H
8
O
6
) ou cido ascrbico (com massa molar igual a 176,13g/mol) analisada
normalmente atravs da reao com um agente oxidante, a qual deve ser realizada o mais
rapidamente possvel, visto que o cido facilmente oxidado pelo prprio oxignio do ar, formando
cido dehidroascrbico.
A semi-reao de oxidao do cido ascrbico a seguinte:
A sobra da bureta dever ser
acondicionada em local apropriado,
indicado pelo professor.
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
28
cido
ascrbico
cido
dehidroascrbico
Complexo
Amido- Iodo
azul intenso
O iodo por ser um oxidante de poder moderado oxida o cido ascrbico somente at o cido
dehidroascrbico. A reao bsica envolvida na reao :
Lembrar que a vitamina C rapidamente oxidada pelo prprio oxignio dissolvido na soluo.
Assim, as amostras devem ser analisadas o mais rpido possvel depois de dissolvidas.
O frasco de titulao deve ser fechado com papel alumnio durante a titulao para evitar a
absoro de oxignio adicional do ar. A pequena oxidao causada pelo oxignio j dissolvido na
soluo no significante, mas a gitao contnua em um erlenmeyer aberto pode absorver uma
quantidade suficiente de oxignio para causar um erro significativo na determinao.
Existem vrios agentes oxidantes que podem ser empregados na determinao de vitamina
C, sendo que um dos mais simples o iodo.
O mtodo iodimtrico, como j vimos, baseia-se na converso de iodo molecular em on
iodeto, de acordo com a semi-reao:
I
2(aq.)
+ 2e
-
2I
-
(aq.)
Na prtica que ser desenvolvida, ser preparada uma soluo de vitamina C que ser
titulada com uma soluo padro de iodo. A vitamina C provoca a reduo do iodo a iodeto que em
soluo aquosa incolor. O iodo reduzido no pode reagir com a molcula de amido, mas quando
ocorre o consumo total das molculas de cido ascrbico (vitamina C), as molculas de iodo em
presena de iodeto reagem com as macromolculas de amido formando complexos de adsoro com
os ons triiodeto conferindo a mistura de reao uma colorao azul intensa.
I
-
+ I
2
+ Amido Amido I
3
-
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
29
Experimento 6:
Anlise de Comprimidos de Vitamina C
Procedimento:
Prepara-se e padroniza-se um soluo de iodo 0,03mol/L. Usa-se como amostra de
comprimido de vitamina C (Vitasay, Cetiva, Cebion, Cenevit,...) de maneira a se obter uma amostra
com aproximadamente 0,8g. Pesa-se ento a amostra, evitando contato manual, por diferena se
possvel e tranfere-se para um balo volumtrico de 100mL previamente lavado. Desde que a soluo
de iodo 0,03M titulante esteja pronta, ento dissolva o comprimido no balo, adicionando
aproximadamente 50mL de gua, fechando o frasco e agitando at que o material se dissolva. Pode
haver uma pequena quantidade de aglutinante que no ir dissolver, mas isso no causar erros.
A seguir, completa-se o volume do balo at a marca, com gua deionizada. Coloca-se a
soluo de iodo 0,03mol/L na bureta.
Pipetam-se exatamente 10mL de soluo de vitamina C e transfere-se para um erlenmeyer de
125mL. Adicionam-se 5mL de soluo de indicador de amido. Cobre-se a boca do erlenmeyer com
papel alumnio ou cartolina, tendo uma pequena abertura para inserir a ponta da bureta e titula-se
rapidamente at o aparecimento da cor azul. Faz-se em triplicata pelo menos, mas no se transfere a
amostra seguinte para o erlenmeyer at que a anterior tenha sido titulada.
Calcula-se a porcentagem de cido ascrbico na amostra e tambm a quantidade (mg) de
vitamina C em cada comprimido:
%cido ascrbico = (
V
I
2
) . (
M
I
2
) . 176,13 . 10 x 100
1000 . (m
comprimido
)
Onde:
V
I
2
o volume de soluo de iodo gasto, em mL.
M
I
2
a concentrao molar da soluo de iodo.
m
comprimido
a massa de comprimido da amostra.
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
30
Cloro
ativo
Experimento 7:
Determinao da percentagem de Cloro ativo em alvejante
Procedimento:
Pipete 25 mL da amostra para dentro de um balo volumtrico de 250mL e dilua com gua
deionizada at a marca e homogenize.
Pipete trs alquotas de 50mL da soluo para dentro de frascos erlenmeyer de 250mL.
Adicione (somente no momento da titulao e na ordem) 2g de KI, 15mL de H
2
SO
4
2M e titule com
soluo padro de Na
2
S
2
O
3
0,1M at chegar a uma colorao amarela plida. Adicione 5mL de
soluo de amido 0,2% e continue a titulao at o desaparecimento da cor azul. Determine a
porcentagem de Cloro ativo (MM = 70,92g/mol) no alvejante.
Reaes:
OCl
-
+ 2I
-
+ 2H
+
Cl
-
+ I
2
+ H
2
O (excesso de KI)
I
2
+ 2S
2
O
3
-2
2I
-
+ S
4
O
6
-2
O constituinte ativo o hipoclorito que responsvel pela ao alvejante (OCl
-
/ CI
-
)
OCl
-
+ CI
-
+ 2H
+
Cl
2
+ H
2
O
Questes:
1. Qual o mtodo da Iodometria empregado nesta tcnica?
2. Por que a adio de amido somente deve ser feita pouco antes do ponto final?
3. O que determina o desaparecimento da cor azul no ponto final?
4. Quais as causas de erro( devido ao Iodo) na Iodometria?
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
31
violeta incolor
ppt marrom
verde
2. PERMANGANOMETRIA
utiizada uma soluo padro de permanganato de potssio. O KMnO
4
um forte agente
oxidante como uma cor violeta intensa. Existem 3 trs reaes possveis do MnO
4
-
, conforme o pH:
1. Em pH fortemente cido: MnO
4
-
+ 8H
+
+ 5e
-
Mn
2+
+ 4H
2
O
2. Em pH neutro ou levemente alcalino: MnO
4
-
+ 4H
+
+ 3e- MnO
2(s)
+ 2H
2
O
3. Em pH fortemente alcalino: MnO
4
-
+ e
-
MnO
4
-2
Trabalharemos em meio fortemente cido, em que o KMnO
4
serve como seu prprio indicador.
As solues aquosas de Permanganato de Potssio no so totalmente estveis em virtude da
oxidao da gua:
4MnO
4
-
+ 2H
2
O 4MnO
2(s)
+ 3O
2(g)
+ 4OH
-
As solues de permanganato, quando adequadamente preparadas, so razoavelmente estveis,
porque a reao de decomposio lenta.
Preparao e Padronizao de uma soluo 0,02M de KMnO
4
O Permanganato de Potssio no um padro primrio, pos traos de MnO
2
esto,
invariavelmente, presentes. Alm disso, a gua destilada geralmente contm impurezas orgnicas
suficientes para para reduzir algum MnO
4
-
recm dissolvido a MnO
2
Cuidados: a gua deionizada contm traos de substncias redutoras, que reagem com o
KMnO
4
para formar dixido de mangans hidratado. necessrio eliminar essas substncias
oxidveis para preparar uma soluo estvel de permanganato porque o dixido de mangans
finamente dividido provoca a autodecomposio do permanganato. Essa eliminao se consegue
fervendo a soluo, por 1 hora, para acelerar a reao entre o MnO
4
-
e as impurezas orgnicas.
Finalmente esfria-se a mistura e filtra-se em um funil de vidro sinterizado limpo para remover o MnO
2
precipitado. O papel de filtro no pode ser utilizado (matria orgnica!).
Preparao:
Dissolver cerca de 0,8g de permanganato de potssio PA, em 150mL de gua deionizada e
aquecer fervura, mantendo a temperatura entre 60 e 70C, durante 60 minutos. Deixa-se a soluo
resfriar por 2 ou 3 dias temperatura ambiente. Filtrar com funil de vidro sinterizado. Transferir o
filtrado para um balo de 250mL e completar at a marca com gua deionizada. Homogeneizar e
transferir o contedo para um frasco mbar de 500mL, protegendo a soluo contra evaporao,
poeira, vapores redutores e conserv-lo em local escuro aps o uso.
Padronizao:
Pesar, com preciso de 0,1mg, de 0,1200 a 0,1500g de oxalato de sdio puro e previamente
dessecado entre 105 e 110C. Colocar dentro de um erlenmeyer de 250mL e dissolver em 50mL de
gua deionizada. Adicionar 30mL de cido sulfrico 1M e aquecer de 80 a 90C. Titular com KMnO
4
0,02M, gota-a-gota, agitando constantemente, at aparecimento da cor rsea persistente por 30
segundos.
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
32
A temperatura da soluo no deve ser inferior a 60C no ponto final.
Reao: 5H
2
C
2
O
4
+ 2MnO
4
-
+ 6H
+
10CO
2
+ 2Mn
2+
+ 8H
2
O
Clculo do fator de correo:
F = m
0,0067 . (VKMnO
4
)
Onde:
m a massa de oxalato de sdio de que se partiu para a titulao;
VKMnO
4
o volume consumido de permanganato.
A sobra da bureta dever ser
acondicionada em local apropriado,
indicado pelo professor.
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
33
violeta incolor
Experimento 8
Determinao do teor de H
2
O
2
em amostra de gua oxigenada
Introduo: o perxido de hidrognio possui propriedades oxidantes e redutoras, dependendo
do potencial de oxidao das substncias com que reage. O potencial de oxidao de uma espcie
qumica mede sua tendncia a se oxidar, isto , o seu poder redutor.
Procedimento:
Pipetar 10mL de amostra de gua oxigenada e transferir para balo volumtrico de 100mL.
Completar o volume do balo com gua deionizada at a marca. Desta soluo, pipetar uma alquota
de 10mL (com a pipeta limpa) para um erlenmeyer de 250mL e adicionar 80mL de gua deionizada e
10mL de cido sulfrico 3mol/L. Titular com o padro de KMnO
4
0,02M at leve rseo permanente.
Expressar o resultado em porcentagem de H
2
O
2
(m/v).
Reao: 2MnO
4
-
+ 5H
2
O
2
+ 6H
+
2Mn
2+
+ 5O
2
+ 8H
2
O
Clculo:
%H
2
O
2
= V . [KMnO
4
] . 2,5 . 100 . 34,02
Onde:
V o volume, em litros, de KMnO
4
padro gasto;
[KMnO
4
] a concentrao molar da soluo padro;
2,5 o resultado da razo entre H
2
O
2
e KMnO
4
, segundo estequiometria;
100 o resultado das diluies da amostra (10mL amostra e 10mL alquota).
Questes:
a) Qual a concentrao de H
2
O
2
em volumes? (Dado: 2H
2
O
2
2H
2
O + O
2
)
b) Quais so as melhores condies de estabilidade para o H
2
O
2
?
c) Explique: por que no h necessidade do uso de um indicador neste experimento?
A sobra da bureta dever ser
acondicionada em local apropriado,
indicado pelo professor.
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
34
Experimento 9:
Determinao de ferro em lmina de barbear
Procedimento:
Pesar lmina de barbear com preciso de 0,1mg. Anotar a massa e dissolver a lmina com
20mL de H
2
SO
4
3mol/L em bquer de 50mL, com o auxlio de aquecimento em uma chapa. Durante a
dissoluo da lmina, o bquer dever estar tapado com um vidro de relgio para evitar que haja
perda de vapores.
Deixar esfriar a soluo formada e filtrar direto para dentro de um balo de 100mL. Efetuar
vrias lavagens com gua deionizada, respeitando o volume do balo e, em seguida, homogeneizar.
Retirar uma alquota de 10mL da soluo, transferir para erlenmeyer de 125mL e adicionar 30mL de
gua deionizada. Titular com KMnO
4
0,1 padro at leve rseo persistente. Repetir o processo por
mais duas vezes no mnimo.
Obs.: a pipeta volumtrica dever ser ambientada bem como a bureta com as respectivas solues.
Reao: 5Fe
2+
+ MnO
4
-
+ 8H
+
Mn
2+
+ 5Fe
3+
+ 4H
2
O
Massa inicial da lmina (g)
Concentrao molar KMnO
4
Volume de KMnO
4
gasto 1
Volume de KMnO
4
gasto 2
Volume de KMnO
4
gasto 3
Volume mdio:
Clculos:
Considerando n como nmero de mol, temos:
V
KMnO4
. [KMnO
4
] = n KMnO
4
para 10mL de soluo
n KMnO
4
5n Fe
2+
n Fe
2+
. 10 = n
total
Fe
2+
1mol Fe 55,8g
n mol Fe
2+
Xg
massa da lmina 100%
Xg Y%
Y = % Fe na lmina
Resultados:
N de mol de KMnO
4
N de mol de Fe
2+
Massa de ferro na soluo
% ferro na lmina
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
35
VOLUMETRIA DE COMPLEXAO
A titulometria com formao de complexos ou complexometria baseia-se em reaes que
envolvem um on metlico e um agente ligante com formao de um complexo suficientemente
estvel.
Apesar de existir um grande nmero de compostos usados na complexometria, os complexos
formados com o cido etilenodiaminotetractico (EDTA), so os mais comuns. Vrios ons
metlicos reagem estequiometricamente com o EDTA. Este um cido tetracarboxlico, possuindo
quatro hidrognios ionizveis, sendo simplificadamente representado por H
4
Y. A reao com on
metlico pode ser genericamente representa por:
M
+q
+ Y
4-
MY
(q-4)
O EDTA na forma de cido ou sal dissdico pode ser obtido em alto grau de pureza, podendo
ser usado como padro primrio, porm, se necessrio pode ser padronizado contra soluo padro
de Zinco ou com Carbonato de Clcio.
A soluo aquosa de EDTA apresenta as espcies H
4
Y, H
3
Y
-
, H
2
Y
2-
, HY
3-
e Y
4-
, sendo que a
forma predominante depende do pH. O EDTA um cido fraco para o qual pK
1
= 2,0; pK
2
= 2,7; pK
3
=
6,2; pK
4
= 10,3.. Estes valores demonstram claramente que os dois primeiros prtons so mais
facilmente ionizveis do que os outros dois restantes. Este reagente possui uma grande versatilidade
que provm da sua potncia como agente complexante e da disponibilidade de numerosos
indicadores on-metal, cada um efetivo em um intervalo limitado de pH.
A espcie complexante Y
4-
,
,
portanto necessrio um ajuste de pH, a fim de obter uma
constante de formao condicional (K) favorvel para o on metlico em questo.
K= K
abs
.
4
onde
4
a frao da espcie Y
4-
em dado pH, e K
abs
a constante de formao absoluta do
complexo formado por EDTA e o on metlico.
Preparao da soluo de EDTA 0,02mol/L
Introduo:
O EDTA forma um complexo com quase todos os ons metlicos com carga positiva maior do
que uma unidade, e mesmo metais alcalinos, como sdio e ltio. Os complexos so formados
estequiometricamente e em quase todos os casos quase que instantaneamente. interessante
considerar a estabilidade dos complexos com o pH do meio, j que o EDTA pode complexar o on H
+
.
Os complexos com metais bivalentes so estveis em meio amoniacal, mas tendem a ionizar em meio
cido. O EDTA pode ser obtido na forma do cido propriamente dito ou na forma de sal dissdico
dihidratado. As duas formas possuem alta massa molar, mas o sal dissdico tem a vantagem de ser
mais facilmente solvel em gua. Algumas aplicaes importantes do EDTA so as determinaes de
dureza de gua, de clcio em leite e magnsio em calcrio.
Procedimento:
Pesar 1,8612g (at 0,1mg) de sal dissdico (designado por Na
2
H
14
N
2
O
8
.2H
2
O), seco a 70-
80c por duas horas numa estufa. As duas molculas de gua de hidratao permanecem intactas
nestas condies de secagem.
Transfere-se quantitativamente a amostra pesada para um balo volumtrico de 250mL.
Adiciona-se cerca de 200mL de gua deionizada, agita-se at dissolver totalmente o sal e depois dilui-
se at a marca. Esta soluo deve preferencialmente ser armazenada em frasco plstico e pode,
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
36
nestas condies ser considerada um padro primrio. A partir da massa pesada, calcula-se a
concentrao exata da soluo de EDTA em mol/L.
Massa molar do EDTA: 372,24g
Preparao e padronizao da soluo de EDTA 0,01mol/L
Preparao:
Pese aproximadamente 1,9g de Na
2
H
14
N
2
O
8
.2H
2
O (MM = 372,24g/mol) para dentro de um copo de
bquer e dilua a 500mL com gua deionizada. Transfira a soluo para um frasco de plstico.
Padronizao:
Pese com exatido entre 0,1 0,15g de CaCO
3
, previamente seco, adiciona-se 1mL de HCl 1:1 para
a solubilizao do sal. Transfere-se esta soluo para um balo volumtrico de 100mL e avoluma-se.
Pipete trs alquotas de 25mL da soluo de CaCO
3
(do balo) para dentro de frascos erlenmeyer de
250mL. Adicionar, na seqncia, aproximadamente 25 mL de gua deionizada, 5mL de soluo
tampo pH = 10 (NH
4
OH/ NH
4
Cl) e 3 gotas de indicador Negro de Eriocromo T (NET) no momento da
titulao. Titule cada alquota com uma soluo de EDTA (recm preparada) at o aparecimento de
colorao azul ntida pura (no violeta). Calcule a molaridade da soluo de EDTA preparada.
Preparao do tampo pH = 10 (NH
3
/NH
4
Cl)
Dissolver 65g de NH
4
Cl em gua, adicionar 570mL de uma soluo de NH
3
concentrado e diluir para 1
litro. Este tampo melhor armazenado em frasco de polietileno para evitar a passagem de ons
metlicos do vidro para a soluo tampo.
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
37
Experimento 10:
Determinao da dureza em uma amostra de gua
O ndice de dureza da gua um dado muito importante usada para avaliar a sua qualidade.
Denomina-se dureza total a soma das durezas individuais atribudas presena de ons clcio e
magnsio. A composio qumica da gua e, portanto, a sua dureza, depende em grande parte do
solo da qual procede. Assim, guas brandas so encontradas em solos baslticos, arenferos e
granticos, enquanto que guas que procedem de solos calcrios apresentam freqentemente
durezas elevadas.
Numerosos processos industriais, tais como fbricas de cervejas, conservas, de papel e
celulose, e muitas outras, requerem gua branda. Para o caso de lavanderias as gua duras
ocasionam elevado consumo de sabo (em conseqncia da formao de sabes insolveis de clcio
e magnsio) e resultam em danos para tecidos. Tambm importante considerar que as guas duras
formam crostas em caldeiras de vapor, ocasionando com isso elevadas perdas de calor e podendo
provocar exploses, devido ao aumento da presso interna. Mediante controle peridico com
titulaes com o EDTA possvel garantir segurana para estas instalaes. A Portaria 1.469/00 do
Ministrio da Sade estipula em 500mg/L de CaCO
3
o limite mximo permitido para dureza total.
Principio do mtodo: O processo consiste na titulao da dureza com uma soluo padro de cido
etilenodiaminotetractico (EDTA), que forma ons complexos muito estveis com o clcio e magnsio
ou outros ons responsveis pela dureza. Ao adicionar o Negro de Eriocromo T a uma amostra que
tenha dureza, formar-se- um on complexo fraco de cor violeta. Durante a titulao, todos os ons
que do dureza so complexados pelo EDTA, rompendo-se a ligao com o Negro de Eriocromo T, em
funo do EDTA formar um comlexo mais estvel com os ons causadores da dureza. Este mecanismo
libera aos poucos o Negro de Eriocromo e, no fim da reao, verifica-se a troca da cor para o azul. O
meio fortemente tamponado, pois em pHs mais baixos o EDTA protonado em vez de complexar
com o clcio e o magnsio.
Procedimento: Transferir uma alquota de 50mL de amostra para um erlenmeyer de 250mL, adicionar
1mL de soluo tampo pH 10 e, a seguir, 5gotas do indicador Negro de Eriocromo T. O tampo deve
ser adicionado antes do indicador de modo que pequenas quantidades de ferro presentes na amostra
precipitem na forma de hidrxido de ferro, impedindo sua reao com o indicador. Titula-se a alquota
com EDTA 0,02mol/L at a mudana de cor de vermelho-vinho para azul puro.
A reao, e consequentemente a mudana de cor, lenta prximo do ponto final, e por esta
razo o titulante deve ser adicionado gota a gota e com vigorosa agitao.
Calcular a dureza da gua e dar o resultado na forma de CaCO
3
, para cada alquota
analisada, sendo a massa molar do CaCO
3
igual a 100,09g/mol.
Clculo: mg/L CaCO
3
= [EDTA] . V
EDTA
(mL) . 100,09
0,05
Questes:
1. Observe a tabela:
De acordo com a
tabela, responda qual
seria a classificao da
gua analisada durante
o experimento?
2. De que maneira podemos remover a dureza existente nas guas duras?
Classificao da gua conforme sua dureza, em mg/L CaCO
3
0 75mg/L Mole (soft)
75 150mg/L Moderada
150 300mg/L Dura (hard)
Acima de 350mg/L Muito dura
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
38
Experimento 11:
Determinao de Clcio no Leite
Procedimento:
Transferir, volumetricamente, para um erlenmeyer de 250mL, 10mL de leite e acrescentar
50mL de gua deionizada. Adicionar 5mL de soluo tampo (NH
4
Cl/NH
4
OH) a soluo dentro do
erlenmeyer. Adicionar alguns cristais de KCN (capela!) para mascarar alguns ons que podem
bloquear o indicador (Zn
+2
, Cu
+2
, F
+3
). Em seguida, adicionar 20 gotas de soluo de magnsio. Por
ltimo, acrescentar algumas gotas de indicador NET e proceder a titulao com uma soluo padro
de EDTA 0,01M. Repetir o mesmo procedimento com mais duas alquotas de leite.
Expressar o valor de clcio encontrado no leite ( em mg de Ca/100mL). Compare o valor
encontrado com o valor nutricional descrito pelo fabricante.
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
39
Bibliografia:
1. SOLOMONS, T.W G., Qumica orgnica. Rio de Janeiro: LTC, 1983. V. 2.
2. AMARAL, L. Qumica orgnica. So Paulo: Editora Moderna Ltda,1981.
3. ALLINGER, N. L.; CAVA, M. P.; JONGH, D. C. et al. Qumica orgnica. 2. ed, Rio de Janeiro,
Guanabara Dois, 1978.
4. HART, A.; SHUETZ, R. D. Qumica orgnica. Rio de Janeiro, Editora Campus LTDA, 1983.
5. MORITA, T.; ASSUMPO, R. M. V. Manual de solues, reagentes & solventes. 2. ed, So
Paulo: Edgard Blcher LTDA.,1972.
6. BACCAN, N.; ANDRADE, J. C. de; GODINHO, O . E. S.; BARONE, J. S., Qumica analtica
quantitativa elementar. So Paulo: Editora Edgard Blcher Ltda, 1979.
7. HARRIS, DANIEL C. Anlise Qumica Quantitativa, 5. ed, L.T.C. Editora, Rio de Janeiro, 2001.
8. SKOOG, D. A.; WEST, D. M. ;HOLLER, F. J.; CROUCH, S. R. Fundamentos de Qumica
Analtica, 8. ed, CENGAGE Learning
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
40
Apndice 1:
Limpeza de materiais volumtricos
Todos os equipamentos volumtricos utilizados em uma anlise quantitativa devem estar
perfeitamente limpos antes do uso, pois a presena de substncias gordurosas nas paredes internas
pode induzir erros no resultado final da anlise.
Verifica-se o estado de limpeza de um aparelho volumtrico enchendo-o com gua e
observando-se seu escoamento. Se gotculas ou uma pelcula no uniforme de gua, aderentes s
paredes internas do equipamento, forem detectadas, ento torna-se necessrio limp-lo.
Solues de limpeza
Se construdos com vidro, estes aparelhos no so atacados por cidos (exceto cido
fluordrico) ou solues diludas de detergente, a no ser aps um contato muito prolongado ou se o
solvente for evaporado.
Utiliza-se geralmente como solues de limpeza soluo detergente a 1-2%, soluo
sulfocrmica ou soluo de etanolato de sdio ou potssio.
Em muitos casos, dependendo do estado em que se encontra o material volumtrico,
suficiente o uso da soluo de detergente (s vezes ligeiramente aquecida). A alternativa seguinte o
emprego (cuidadoso) da soluo sulfocrmica (dicromato de sdio ou potssio dissolvido em cido
sulfrico). De um modo geral, o tempo de contato desta soluo com o vidro no precisa ser longo,
mas deve-se observar a cor da sulfocrmica antes do seu uso, pois se for verde sinal que sua
eficincia ser muito pequena (presena de ons Cr
3+
) e por isso no deve ser utilizada.
O etanolato de sdio ou potssio deve ser usado somente em casos extremos porque ataca
rapidamente o equipamento volumtrico. O tempo de contato do etanolato no deve ultrapassar 60
segundos. Se esta soluo de limpeza for usada deve-se, depois de enxaguar algumas vezes o
equipamento volumtrico, usar uma soluo de HCl diluda para neutralizar qualquer trao de
substncia alcalina e, em seguida, lav-lo novamente com gua. Deve-se evitar ao mximo o uso
repetitivo de alcoolato na limpeza do material volumtrico.
O material volumtrico dado limpo ao se verificar que a gua destilada escorre
uniformemente pelas suas paredes internas.
Apndice 2:
O efeito da temperatura nas medidas de volume.
O volume ocupado por uma dada massa de lquido varia com a temperatura, assim como
varia tambm o recipiente no qual est colocado o lquido, durante a medida. Entretanto, a maioria
dos equipamentos de medida de volume so feitos de vidro, o qual felizmente tem pequeno
coeficiente de expanso. Consequentemente, as variaes no volume em funo da temperatura de
um recipiente de vidro no precisam ser consideradas em trabalhos comuns em qumica analtica.
O coeficiente de expanso para solues aquosas diludas (aproximadamente 0,025% /
o
C) tal que
uma variao de 5
o
C tem efeito considervel na confiabilidade da medida volumtrica.
As medidas volumtricas devem tomar como referncia alguma temperatura padro; este
ponto de referncia geralmente 20
o
C. A temperatura ambiente da maioria dos laboratrios fica
suficientemente perto de 20
o
C de modo que no h necessidade de se efetuar correes das medidas
de volume. No entanto, o coeficiente de expanso para lquidos orgnicos podem requerer correes
para diferenas de temperatura de 1
o
C ou at menos.
Anlise Qumica
PARA SUA SEGURANA, INDISPENSVEL O USO DE EPIS DURANTE AS AULAS PRTICAS.
41
Calibrao de Equipamentos Volumtricos
A vidraria volumtrica calibrada medindo-se a massa de um lquido que pode preencher o
equipamento volumtrico (geralmente gua destilada). O lquido usado deve ter densidade conhecida
na temperatura ambiente. Ao realizar uma calibrao, deve-se fazer correo devido diferena de
densidade da gua e das dos pesos padres.
Conduta geral nos procedimentos de calibrao.
Toda a vidraria volumtrica deve estar rigorosamente limpa antes da calibrao ( o teste do
filme homogneo de gua deve ser feito). Buretas e pipetas no precisam estar secas, mas os bales
volumtricos devem ser drenados e secos a temperatura ambiente. A gua usada para a calibrao
deve estar em equilbrio trmico com o ambiente. Esta condio melhor estabelecida se um frasco
grande com a gua a ser usada for mantido no ambiente com antecedncia, anotando sua
temperatura a intervalos freqentes, e aguardando at que no haja mais variaes de temperatura.
Frascos comuns de pesagem ou mesmo pequenos erlens podem ser usados como receptores
para o lquido de calibrao.
Calibrao de uma pipeta volumtrica.
Determine primeiramente a massa do recipiente vazio, at a casa dos miligramas. Transfira
uma poro de gua (equilibrada com a temperatura ambiente) para o frasco receptor (erlen) com a
pipeta e pese novamente com preciso em miligramas. Calcule a massa de gua por diferena entre
estas duas massas obtidas. Calcule o volume dispensado da pipeta, usando as tabelas fixadas nos
balces do laboratrio para correes. Repita a calibrao vrias vezes. Calcule o volume mdio.
Calibrao de uma bureta.
Preencha a bureta com a gua equilibrada termicamente com o ambiente e certifique-se de
que no h bolhas de ar na ponta da bureta. Espere 1 minuto para a drenagem do lquido dentro da
bureta. Ento, diminua o nvel do lquido at trazer o menisco marca de 0,00 mL. Toque a ponta da
bureta na parede de um bquer para remover qualquer possvel gota aderida. Espere 5 minutos e
reverifique o volume. Se a torneira estiver firme, no deve haver nenhuma variao perceptvel.
Durante este intervalo, pese (com preciso de miligrama) um erlen de 125 mL.
Transfira devagar ( a cerca de 10 mL / min) aproximadamente 10 mL de gua ao frasco. Toque a
ponta da bureta na parede do erlen. Espere 1 minuto, anote o volume aparente que foi dispensado da
bureta e preencha-a com gua. Pese o erlen novamente. A diferena entre esta massa e a inicial d a
massa de gua dispensada. Use as tabelas fixadas nos balces do laboratrio para converter esta
massa em volume real. Subtraia o volume aparente do volume real. Esta diferena a correo que
deve ser aplicada ao volume aparente para se obter o volume real. Repita esta calibrao at
alcanar uma concordncia de 0,02 mL.
Comece novamente da marca do zero, repita esta calibrao, mas agora dispensando cerca
de 20 mL para o erlen. Repita este procedimento a intervalos de 10 mL at o volume total da bureta.
Prepare um grfico da correo a ser aplicada como funo de volume dispensado pela bureta. A
correo associada com qualquer intervalo de volume pode ser determinada atravs deste grfico.
Calibrao de um balo volumtrico.
Pese o balo seco e limpo at a preciso de miligrama. Ento preencha-o at sua marca de
calibrao com gua equilibrada termicamente com o ambiente e repese-o. Calcule o volume do balo
com a ajuda das tabelas de correo novamente. (O ideal no ter contato manual direto com o balo
durante as pesagens para que a gordura das mos no interfira).
Potrebbero piacerti anche
- Exercícios de Equilíbrio Químico - Profº Agamenon RobertoDocumento46 pagineExercícios de Equilíbrio Químico - Profº Agamenon Robertocb_penatrujillo92% (26)
- Apostila 2 Semestre 2006Documento51 pagineApostila 2 Semestre 2006fear4523Nessuna valutazione finora
- Qumica Analtica Qualitativa - Novos Roteiros 2013 - F Inal 3 2Documento77 pagineQumica Analtica Qualitativa - Novos Roteiros 2013 - F Inal 3 2Marcilio CarlosNessuna valutazione finora
- Ciencias Dos Materiais Lista de Exercicios - CompressDocumento25 pagineCiencias Dos Materiais Lista de Exercicios - CompressMarcos OliveiraNessuna valutazione finora
- Química Analítica ExperimentalDocumento41 pagineQuímica Analítica ExperimentalBetuchoNessuna valutazione finora
- Apostila de Quimica Analitica Experimental Da UfpeDocumento44 pagineApostila de Quimica Analitica Experimental Da Ufpeantonioasp100% (1)
- Aulas práticas de Química GeralDocumento28 pagineAulas práticas de Química GeralDianaFurtadoNessuna valutazione finora
- Roteiro Analitica I IFCE - VERSÃO COMPLETADocumento82 pagineRoteiro Analitica I IFCE - VERSÃO COMPLETAAriana BritoNessuna valutazione finora
- Apostila Laboratório Quimica Tecnológica CelularDocumento64 pagineApostila Laboratório Quimica Tecnológica Celularleonardoalmeidasantana27Nessuna valutazione finora
- Apostila Quim Experimental 1 - UFPEDocumento48 pagineApostila Quim Experimental 1 - UFPEmikey12345452863879Nessuna valutazione finora
- Apostila Química Experimental 1Documento59 pagineApostila Química Experimental 1Grazi LeiteNessuna valutazione finora
- Laboratório de Química: Segurança ExperimentalDocumento44 pagineLaboratório de Química: Segurança ExperimentalIzaias AiresNessuna valutazione finora
- Síntese de compostos orgânicos: reações e aplicaçõesDocumento38 pagineSíntese de compostos orgânicos: reações e aplicaçõesNathália AmaralNessuna valutazione finora
- Análise Química UFCEDocumento72 pagineAnálise Química UFCEEmanoel SantosNessuna valutazione finora
- Manual de Labotório Analítica Exp IIDocumento31 pagineManual de Labotório Analítica Exp IIdocadias2Nessuna valutazione finora
- Apostila de Química Analítica Quantitativa - FinalDocumento51 pagineApostila de Química Analítica Quantitativa - FinalCarlos Augusto LimaNessuna valutazione finora
- Apostila Seg Lab Materiais Manual de Elaboração de RelatóriosDocumento37 pagineApostila Seg Lab Materiais Manual de Elaboração de RelatóriosMichael BarrosNessuna valutazione finora
- Apostila de Química Analitica V (LABORATÓRIO) 2o sem 2022 - 23_11_22 V1-2Documento50 pagineApostila de Química Analitica V (LABORATÓRIO) 2o sem 2022 - 23_11_22 V1-2Ciência GeralNessuna valutazione finora
- Apostila de Prática Quanti - Aluno BiotecnologiaDocumento79 pagineApostila de Prática Quanti - Aluno BiotecnologiaI don't know who I amNessuna valutazione finora
- Apostila QG - Experimental - 2019 - Word - Alcy FavachoDocumento34 pagineApostila QG - Experimental - 2019 - Word - Alcy FavachoRenato FreitasNessuna valutazione finora
- Apostila de Quimica Analítica QuantitativaDocumento51 pagineApostila de Quimica Analítica Quantitativajordania8803100% (1)
- QAE-Apostila de Química ExperimentalDocumento71 pagineQAE-Apostila de Química Experimentallindojamir02Nessuna valutazione finora
- Roteiro de QuimicaDocumento23 pagineRoteiro de QuimicaFabrício QuadrosNessuna valutazione finora
- Apostila QA QuantitativaDocumento57 pagineApostila QA QuantitativarodrigomarconNessuna valutazione finora
- Roteiro de aulas práticas- MED 2024Documento37 pagineRoteiro de aulas práticas- MED 20248wr8r8jbsyNessuna valutazione finora
- Laboratorio I QuimicaDocumento97 pagineLaboratorio I QuimicaRafael Gabriel100% (1)
- Segurança no laboratório de química: diretrizes essenciaisDocumento146 pagineSegurança no laboratório de química: diretrizes essenciaisPietra MatosNessuna valutazione finora
- Laboratório de Quimica AnaliticaDocumento71 pagineLaboratório de Quimica AnaliticaElviradeMelloNessuna valutazione finora
- AQQT Apostila PDFDocumento58 pagineAQQT Apostila PDFMarcos ViniciusNessuna valutazione finora
- Roteiros de Aulas Práticas de BioquímicaDocumento46 pagineRoteiros de Aulas Práticas de Bioquímicawalmeidamiranda7988Nessuna valutazione finora
- Química Inorgânica Experimental I - Lic. Quim.Documento50 pagineQuímica Inorgânica Experimental I - Lic. Quim.Lourençop TufasNessuna valutazione finora
- Afericao de Materiais VolumetricosDocumento17 pagineAfericao de Materiais VolumetricosZacarias JoãoNessuna valutazione finora
- Roteiros_Laboratorio_Quim_TecnologicaDocumento64 pagineRoteiros_Laboratorio_Quim_TecnologicaLiliane ResendeNessuna valutazione finora
- Práticas Química AmbientalDocumento75 paginePráticas Química AmbientalLetícia BragaNessuna valutazione finora
- Análise Química LaboratorialDocumento39 pagineAnálise Química LaboratorialIzabela AraujoNessuna valutazione finora
- Termodinâmica Equilíbrio QuímicoDocumento24 pagineTermodinâmica Equilíbrio QuímicoAnna MoraisNessuna valutazione finora
- Azdoc - Tips Relatorio de QaeDocumento48 pagineAzdoc - Tips Relatorio de QaeLarissa TaynaNessuna valutazione finora
- Relatório Laboratório Química GeralDocumento16 pagineRelatório Laboratório Química GeralGames ViciusNessuna valutazione finora
- Apostila - Aulas Práticas de Ciência Dos MateriaisDocumento34 pagineApostila - Aulas Práticas de Ciência Dos MateriaisKarine SNessuna valutazione finora
- Apostila de Saneamento AmbientalDocumento58 pagineApostila de Saneamento AmbientalJoao Paulo Reis BarrosNessuna valutazione finora
- BromatologiaDocumento174 pagineBromatologiaFabio OliveiraNessuna valutazione finora
- Atendente de Laboratório: Funções e Coleta de AmostrasDocumento22 pagineAtendente de Laboratório: Funções e Coleta de AmostrasIzadoraNessuna valutazione finora
- Apostila de Química Geral ExperimentalDocumento30 pagineApostila de Química Geral ExperimentalGrupo LokarNessuna valutazione finora
- Experiment Os de Qui Mica GeralDocumento165 pagineExperiment Os de Qui Mica GeralFernando Honorato NascimentoNessuna valutazione finora
- CombinePDF 1679756062750iDocumento255 pagineCombinePDF 1679756062750iGabriel SoaresNessuna valutazione finora
- Experimentos de Química GeralDocumento333 pagineExperimentos de Química GeralGabriel SoaresNessuna valutazione finora
- Preparação Da Amostra para CromatografiaDocumento250 paginePreparação Da Amostra para CromatografiaLeidiana Elias XavierNessuna valutazione finora
- Apostila Química Experimental I - 2023-2Documento59 pagineApostila Química Experimental I - 2023-2adsonmenezes.rutoNessuna valutazione finora
- Apostila de Práticas - QOExp - 2Documento61 pagineApostila de Práticas - QOExp - 2t4qnjfx4yqNessuna valutazione finora
- Apostila QUI02023 - Profa. JessieDocumento81 pagineApostila QUI02023 - Profa. JessieAna BeatrizNessuna valutazione finora
- Auxiliar de Lab Livro DigitalDocumento92 pagineAuxiliar de Lab Livro DigitalTaina LealNessuna valutazione finora
- Apostila QUI02023 - 2020 1Documento85 pagineApostila QUI02023 - 2020 1smmendoncaNessuna valutazione finora
- Relatório G10Documento33 pagineRelatório G10Cris OliveiraNessuna valutazione finora
- Bases Químicas da BiologiaDocumento56 pagineBases Químicas da BiologiaAllana CerqueiraNessuna valutazione finora
- Filmes FinosDa EverandFilmes FinosNessuna valutazione finora
- Modelagem Numérica e Computacional com Similitude e Elementos Finitos: Desenvolvimento de Equação Preditiva para o Cálculo da Força de Retenção em Freios de EstampagemDa EverandModelagem Numérica e Computacional com Similitude e Elementos Finitos: Desenvolvimento de Equação Preditiva para o Cálculo da Força de Retenção em Freios de EstampagemNessuna valutazione finora
- Livro Nanotecnologia Em Processos IndustriaisDa EverandLivro Nanotecnologia Em Processos IndustriaisNessuna valutazione finora
- 1 Lista EsteqDocumento1 pagina1 Lista EsteqElaine VianaNessuna valutazione finora
- Erros e Tratamentos de Dados AnalíticosDocumento41 pagineErros e Tratamentos de Dados AnalíticosElaine VianaNessuna valutazione finora
- Deslocamento de Equilíbrio Químico: Concentração e PressãoDocumento26 pagineDeslocamento de Equilíbrio Químico: Concentração e PressãoElaine VianaNessuna valutazione finora
- Questões QuimicaDocumento23 pagineQuestões QuimicaWalisson SoaresNessuna valutazione finora
- Cap.9 - Quando o Bebê ChoraDocumento8 pagineCap.9 - Quando o Bebê ChoraElaine VianaNessuna valutazione finora
- EquilibrioDocumento18 pagineEquilibrioBruna RibeiroNessuna valutazione finora
- Serviço Público Federal avalia aprendizagem de QuímicaDocumento2 pagineServiço Público Federal avalia aprendizagem de QuímicaElaine VianaNessuna valutazione finora
- EquilibrioDocumento18 pagineEquilibrioBruna RibeiroNessuna valutazione finora
- Constante de equilíbrio Kc para reação de formação de HCNDocumento22 pagineConstante de equilíbrio Kc para reação de formação de HCNDeborah LGNessuna valutazione finora
- Questões QuimicaDocumento23 pagineQuestões QuimicaWalisson SoaresNessuna valutazione finora
- Eq QuímicoDocumento23 pagineEq QuímicoElaine VianaNessuna valutazione finora
- Resumo Cinetica Quimica PDFDocumento11 pagineResumo Cinetica Quimica PDFKelen FonsecaNessuna valutazione finora
- Soluções Químicas AvançadasDocumento110 pagineSoluções Químicas AvançadasElaine Viana0% (1)
- A2 Diagramas de FasesDocumento43 pagineA2 Diagramas de Fasesgsoares_10Nessuna valutazione finora
- SL Equilibrio QuimicoDocumento30 pagineSL Equilibrio QuimicoHoir HieroNessuna valutazione finora
- ProteínasDocumento15 pagineProteínasElaine VianaNessuna valutazione finora
- Soluções Químicas AvançadasDocumento110 pagineSoluções Químicas AvançadasElaine Viana0% (1)
- Água PH e TampõesDocumento11 pagineÁgua PH e TampõesElaine VianaNessuna valutazione finora
- LipídeosDocumento28 pagineLipídeosElaine VianaNessuna valutazione finora
- BioeletrogeneseDocumento76 pagineBioeletrogeneseElaine VianaNessuna valutazione finora
- Aula Prática Sistema TampãoDocumento2 pagineAula Prática Sistema TampãoElaine Viana100% (1)
- Lab4 PDFDocumento2 pagineLab4 PDFElaine VianaNessuna valutazione finora
- 2014.1.plano de Ensino - Laboratório de Química GeralDocumento6 pagine2014.1.plano de Ensino - Laboratório de Química GeralElaine VianaNessuna valutazione finora
- Epi - LaboratórioDocumento34 pagineEpi - LaboratórioElaine VianaNessuna valutazione finora
- Óleos e Gorduras IAL Cap16Documento37 pagineÓleos e Gorduras IAL Cap16Elaine VianaNessuna valutazione finora
- Apostila 2007Documento34 pagineApostila 2007ifiwereceloNessuna valutazione finora
- Banner 2001Documento1 paginaBanner 2001Elaine VianaNessuna valutazione finora
- ApostilatqDocumento27 pagineApostilatqPedro MirandaNessuna valutazione finora
- Produto 1Documento6 pagineProduto 1Maria Tereza PenaNessuna valutazione finora
- Est Dirigido Cineticaqui-1Documento6 pagineEst Dirigido Cineticaqui-1Zoé AraújoNessuna valutazione finora
- Termoquímica IntroduçãoDocumento28 pagineTermoquímica IntroduçãoleaorsNessuna valutazione finora
- Ficha de Ciências Naturais - 5. Ano: Cabeçalho Do AgrupamentoDocumento3 pagineFicha de Ciências Naturais - 5. Ano: Cabeçalho Do AgrupamentoDegrau Do Sucesso100% (1)
- Lista de Exercício 2 - 2023 ELETROQUIMICA APLICADADocumento1 paginaLista de Exercício 2 - 2023 ELETROQUIMICA APLICADAMarina Gontijo Souza MacedoNessuna valutazione finora
- Estudo Hidrocarbonetos AromáticosDocumento40 pagineEstudo Hidrocarbonetos AromáticosAzevedoCarlos Mateus100% (1)
- C.q.médio LRDocumento6 pagineC.q.médio LRAmanda RezendeNessuna valutazione finora
- Elementos do bloco s reatividadeDocumento13 pagineElementos do bloco s reatividadeGeovane SouzaNessuna valutazione finora
- UntitledDocumento2 pagineUntitledJuliaNessuna valutazione finora
- Prova de Conhecimentos Adquiridos No Curso Tecnologias Hidráulicas Aplicadas A WTGsDocumento3 pagineProva de Conhecimentos Adquiridos No Curso Tecnologias Hidráulicas Aplicadas A WTGsrildo1966Nessuna valutazione finora
- 2018-Caderno de Questões - Prova IDocumento12 pagine2018-Caderno de Questões - Prova ISidineia NascimentoNessuna valutazione finora
- An 4601Documento1 paginaAn 4601Edmilson Santos BatistaNessuna valutazione finora
- Planejamento Anual 9ºA e 9ºBDocumento5 paginePlanejamento Anual 9ºA e 9ºBMariana BertheNessuna valutazione finora
- Quadro Modelo IBUTGDocumento2 pagineQuadro Modelo IBUTGapi-3704990100% (3)
- Manual de terminologia e conceitos de manutenção eletromecânicaDocumento32 pagineManual de terminologia e conceitos de manutenção eletromecânicaAnderson GuimarãesNessuna valutazione finora
- FISPQ Catalisador PU IndustrialDocumento11 pagineFISPQ Catalisador PU IndustrialJorge Henrique Lima JuniorNessuna valutazione finora
- EPIs para soldadoresDocumento13 pagineEPIs para soldadoresDouglas De Souza BarretoNessuna valutazione finora
- Resolução de exercícios de condução e convecção através de paredes planas, cilíndricas e esféricasDocumento12 pagineResolução de exercícios de condução e convecção através de paredes planas, cilíndricas e esféricasfabio_ma0% (1)
- Propriedades das superligas de níquel para aplicações aeroespaciaisDocumento35 paginePropriedades das superligas de níquel para aplicações aeroespaciaisJ. GirotoNessuna valutazione finora
- Tutorial ACD LABDocumento40 pagineTutorial ACD LABDanilo BatistaNessuna valutazione finora
- Relatório 5 - Índice de IodoDocumento5 pagineRelatório 5 - Índice de IodoMilena SantosNessuna valutazione finora
- 17834-Texto Do Artigo-70154-1-10-20140624Documento16 pagine17834-Texto Do Artigo-70154-1-10-20140624lu canal do amorNessuna valutazione finora
- Atividade Tratamentos Térmicos - A3Documento4 pagineAtividade Tratamentos Térmicos - A3Matheus YrionNessuna valutazione finora
- Funções Inorgânica2Documento26 pagineFunções Inorgânica2Jaime ChogaNessuna valutazione finora
- Eric - AterramentoDocumento72 pagineEric - AterramentoMário SérgioNessuna valutazione finora
- Atividade Semana 1 - Não Pontuada - Revisão Da TentativaDocumento3 pagineAtividade Semana 1 - Não Pontuada - Revisão Da TentativaAline AmbéNessuna valutazione finora
- Manual de Segurança para LaboratórioDocumento10 pagineManual de Segurança para LaboratórioNayra Maciel100% (1)
- Estradas e TransportesDocumento32 pagineEstradas e TransportesAlan MoraisNessuna valutazione finora
- Análise de riscos para instalação de linhaDocumento11 pagineAnálise de riscos para instalação de linhaMauricio MagalhaesNessuna valutazione finora