Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Generalidades de Inmunología.
Caricato da
Sam ReyesTitolo originale
Copyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Generalidades de Inmunología.
Caricato da
Sam ReyesCopyright:
Formati disponibili
1.
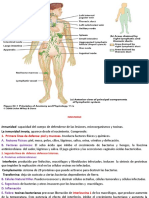
2 VISIN GENERAL DEL SISTEMA INMUNITARIO El sistema inmunitario consta de varias "lneas de defensa" principales: Inmunidad innata (= natural o inespecfica): es una lnea de defensa que permite controlar a mayor parte de los agentes patgenos. Inmunidad adquirida (= adaptativa o especfica): suministra una respuesta especfica frente a cada agente infeccioso. Posee memoria inmunolgica especfica, que tiende a evitar que el agente infeccioso provoque enfermedad en una segunda infeccin. Pero incluso antes de que acte la inmunidad inespecfica, el organismo posee una serie de barreras naturales que lo protegen de la infeccin de los agentes patgenos, as como una proteccin biolgica por medio de la microflora (microbiota) natural que posee. Comenzaremos nuestro estudio de la inmunidad precisamente por estas primeras lneas defensivas. 1.2.1 Barreras anatmicas y fsicas 1.2.1.1 Barreras anatmicas (superficies corporales): la piel y membranas mucosas La parte externa de la epidermis est compuesta de varias capas de clulas muertas, recubiertas de la protena queratina, resistente al agua. Dicha capa se renueva cada 15-30 das. La dermis subyacente contiene tejido conectivo con vasos sanguneos, glndulas sebceas y sudorparas, y folculos pilosos. La piel es una autntica barrera infranqueable para la mayor parte de los microorganismos. El papel de barrera de la piel se pone de manifiesto por contraste, por ejemplo al comprobar lo fcilmente que se producen infecciones a partir de quemaduras. Pero como contrapartida, en un organismo sano, las heridas se cierran rpidamente por cogulos. Algunos patgenos pueden obviar la barrera de la piel debido a que son inoculados por artrpodos vectores (caros, mosquitos, chinches, etc.). Por otro lado, existen zonas de la superficie del cuerpo no recubiertas por piel: ojos intestino tracto respiratorio tracto urinario En estas zonas hay fluidos (y en su caso tapizado ciliar) que colaboran a la eliminacin de microorganismos Algunos microorganismos han desarrollado estructuras para invadir el cuerpo del hospedador a partir de las mucosas. Por ejemplo, el virus de la gripe posee una molcula que le capacita para unirse firmemente a las clulas de la membrana mucosa y as escapar al efecto de las clulas ciliadas. Muchas bacterias patgenas logran adherirse a las mucosas a travs de sus fimbrias, que se unen con ciertas glucoprotenas o glucolpidos de los epitelios de tejidos determinados. 1.2.1.2 Funcin del pH Por ejemplo, en el estmago, el pH bajo (alrededor de pH 2) impide que lo atraviese la mayora de microorganismos, excepto algunos patgenos (p. ej., Salmonella, Vibrio cholerae, etc.). pH ligeramente cido de la piel y de la vagina. 1.2.1.3 Funcin de la temperatura Muchas especies no son susceptibles a ciertos microorganismos sencillamente porque su temperatura corporal inhibe el crecimiento de stos. As, los pollos presentan inmunidad innata al ntrax debido a que su temperatura es demasiado alta para que el patgeno pueda crecer. 1.2.1.4 Sustancias antimicrobianas del organismo La lisozima aparece en muchas secreciones (nasofaringe, lgrimas, sudor, sangre, pulmones, tracto genitourinario...). beta-lisina, producida por las plaquetas. Espermina en el semen.
1.2.1.5 Secuestro de hierro, que hace que el Fe libre en el organismo sea muy escaso (del orden de 10 -8M). En las clulas, el Fe est "secuestrado" formando complejos con molculas como hemoglobina, mioglobina, citocromos, ferritina, etc. En la sangre, el Fe est unido a la transferrina. Sin embargo, algunos patgenos han evolucionado mecanismos para obtener Fe a partir de algunas de estas protenas: se trata de un tipo de molculas llamadas siderforos, que pueden captar Fe a partir de la transferrina. Como ejemplo, la enterobactina de miembros de la familia Enterobactericeas. 1.2.2 Proteccin de la microbiota normal La microbiota normal del organismo evita la colonizacin del hospedador por microorganismos exgenos. Esa es la razn por la que una limpieza exagerada de la piel y de la vagina puede ser causa de infecciones por microbios exgenos. Recurdese el papel de proteccin que confiere la bacteriaLactobacillus acidophilus en el hbitat de la vagina. Por otro lado, un abuso de antibiticos suministrados por va oral puede llegar a alterar el equilibrio ecolgico de la microflora intestinal. En la piel existen dos tipos principales de "hbitat": la superficie de la piel propiamente dicha es un medio relativamente "hostil", ya que es seca y muy salada, de modo que normalmente slo la pueden colonizar algunas bacterias bien adaptadas: Micrococcus, Staphylococcus epidermidis, S. aureus. Las glndulas: sudorparas y sebceas. En estas ltimas, durante la adolescencia se desarrolla el tpico acn (espinillas), producido por el ataque dePropionibacterium acnes. La boca posee una poblacin heterognea de bacterias, donde son importantes los representantes orales del gnero Streptococcus: S. salivaris (en la lengua), S. mitis (en los carrillos) y S. mutans (en los dientes). Este ltimo es uno de los principales responsables de la placa dental y de la caries. El intestino grueso posee una abundantsima flora microbiana, con una concentracin del orden de 1010 bacterias/ml. Funciona como si fuera un quimiostato.
1.2.3 1.2.3.1
Sistema inmunitario (propiamente dicho) Sistema de inmunidad innata, natural o inespecfica
Elementos del sistema de inmunidad natural. Si el microorganismo o partcula extraos logran atravesar la piel y los epitelios, se pone en marcha el sistema de inmunidad natural (inespecfica o innata), en el que participan los siguientes elementos: Clulas: Fagocitos (o sea, leucocitos del sistema retculo-endotelial, que se originan en la medula sea):en la sangre: los PMN neutrfilos (de vida corta) y los monocitos; en los tejidos: los macrfagos, que se diferencian a partir de los monocitos. Todos ellos fagocitan y destruyen los agentes infecciosos que logran atravesar las superficies epiteliales. Clulas asesinas naturales (clulas NK): son leucocitos que se activan por interferones inducidos en respuesta a virus. Reconocen y lisan clulas "enfermas", infectadas por virus o malignizadas (cancerosas). Factores solubles: Protenas de fase aguda: aumentan su concentracin rpidamente unas 100 veces ante una infeccin Una de ellas (la protena C-reactiva) se une a la protena C de la superficie del neumococo, favoreciendo que ste sea recubierto por el sistema de protenas del complemento (al que aludiremos enseguida), lo cual a su vez facilita la fagocitosis por los fagocitos. Sistema del complemento: se trata de un conjunto de unas 20 protenas del suero que interaccionan entre s y con otros componentes de los sistemas inmunes innato y adquirido. En el sistema de inmunidad innata el sistema se activa por la llamada ruta alternativa. He aqu un resumen de sus efectos:
El complemento se activa por ruta alternativa al contacto con la superficie del microorganismo. El hecho de que el complemento quede activado tiene una serie de consecuencias: lisis directa del microorganismo quimiotaxis sobre fagocitos recubrimiento del microorganismo con una de las protenas del complemento (la C3b), lo que facilita la fagocitosis (a este fenmeno se le llama opsonizacin) la activacin del complemento controla tambin la reaccin de inflamacin aguda. Funcionamiento del sistema de inmunidad natural Endocitosis La endocitosis es la ingestin de material soluble (macromolculas) del fluido extracelular por medio de invaginacin de pequeas vesculas endocticas. La endocitosis puede ocurrir de dos maneras distintas: A) Pinocitosis La internalizacin de las macromolculas ocurre por invaginacin inespecfica de la membrana plasmtica. Debido a esa inespecificidad, la cuanta de la internalizacin depende de la concentracin de las macromolculas. B) Endocitosis mediada por receptor Las macromolculas son selectivamente internalizadas debido a su unin a un receptor especfico de la membrana. En cualquiera de estos dos casos, tras la internalizacin, las vesculas endocticas se fusionan entre s y despus con los endosomas. En el caso de endocitosis, el contenido cido de los endosomas hace que se disocie la macromolcula de su receptor. El endosoma se fusiona con el lisosoma primario, para dar el lisosoma secundario. Los lisosomas primarios derivan del aparato de Golgi y transportan grandes cantidades de enzimas hidrolticos (proteasas, nucleasas, lipasas, etc.). Dentro de los lisosomas secundarios, las macromolculas ingeridas son digeridas hasta productos hidrolizados (pptidos, aminocidos, nucletidos y azcres), que finalmente son eliminados de la clula. Fagocitosis La fagocitosis es la unin del microorganismo (o, en general, un agente particulado, insoluble) a la superficie de una clula fagoctica especializada (PMN, macrfago), por algn mecanismo inespecfico, de tipo primitivo (ameboide): emisin de pseudpodos y englobamiento, para crear un fagosoma (10-20 veces mayor que el endosoma) al que se unen lisosomas; a partir de aqu el proceso es similar al descrito anteriormente. La fusin de los grnulos de los fagocitos origina la destruccin del microbio en unos pocos minutos. La expansin de la membrana en la fagocitosis (emisin de pseudpodos) requiere la participacin de los microfilamentos, cosa que no ocurre en la pinocitosis-endocitosis. La destruccin del microorganismo en los lisosomas secundarios de los fagocitos se produce por dos tipos de mecanismos: Mecanismos dependientes de oxgeno: Se activa una ruta metablica (hexosa monofosfato) que consume grandes cantidades de oxgeno, lo que a su vez produce grandes cantidades de radicales txicos antimicrobianos (como el O2-, H2O2, OH-, O21), que a su vez pueden reaccionar para dar otras sustancias txicas, como hipocloritos y cloruros. Estas sustancias provocan una intensa halogenacin que afecta a muchas bacterias y virus. Mecanismos dependientes de xido ntrico (NO). Mecanismos independientes de oxgeno: Liberacin de enzimas hidrolticos: lisozima, protenas catinicas, proteasas, etc., que ejecutan un efecto bactericida o bacteriosttico.
Pero como hemos dicho, el paso inicial de la fagocitosis implica que el fagocito debe ser capaz de unirse al microorganismo y activar la membrana para poder englobarlo. Para ello, cuenta con una ayuda evolutiva que se ha "aadido" al sistema primitivo ameboide, y que aumenta su eficacia: el sistema de activacin del complemento por la va alternativa. Activacin del complemento por la ruta alternativa: Como ya dijimos, el complemento es un conjunto de 20 protenas del plasma, que interactan entre s y con otros elementos de los sistemas inmunitarios innato y adquirido, para mediar una serie de importantes respuestas inmunolgicas. El complemento se activa por dos rutas diferentes: la ruta clsica, (que corresponde al sistema de inmunidad especfica, y que depende de interacciones antgeno-anticuerpo), y la ruta alternativa (perteneciente al sistema natural). Ambas rutas consisten en un sistema de activacin enzimtica en cascada, que sigue la lgica de que el producto de una reaccin es a su vez una enzima para la siguiente reaccin, producindose una respuesta rpida y amplificada del estmulo inicial. En la ruta alternativa podemos distinguir dos grandes fases: la iniciacin por el componente C3 y el ensamblaje del complejo de ataque a la membrana (CAM). a) Iniciacin de la ruta alternativa por el componente C3. La accin concertada del polisacrido microbiano y de la properdina del hospedador estabiliza a la C3convertasa, que de esta forma comienza a producir grandes cantidades de C3b que se fijan a la superficie del microorganismo; a su vez, el C3b fijado provoca la produccin y fijacin de mayores cantidades de convertasa (C3bBb). b) Ensamblaje sobre la membrana del microorganismo del complejo de ataque a la membrana (CAM), por la "va post-C3": Ahora comienzan a juntarse, junto al C3b, y en orden secuencial, una serie de otros componentes del sistema complemento, que finalmente constituyen el llamado complejo de ataque a la membrana (CAM), que representa un canal totalmente permeable a iones y agua. Como lo que acabamos de describir ocurre en toda la superficie del microorganismo, el resultado son innumerables complejos CAM ensamblados en la membrana citoplsmica, por los que entran grandes cantidades de agua con iones Na +, que pueden provocar la lisis del microorganismo. En este proceso se liberan algunos componentes solubles del complemento, de los cuales los ms importantes son el C3a y el C5a. Funciones biolgicas del complemento activado por la ruta alternativa: a) Como acabamos de ver, una primera secuela (aunque no siempre ocurre en todos los microorganismos) es la lisis celular por el CAM. El recubrimiento del microorganismo por numerosas unidades de C3b es un ejemplo de opsonizacin: facilita la unin de los fagocitos al agente extrao, para su inmediata fagocitosis. Papel de los pequeos pptidos solubles C3a y C5a: b) estimulan la tasa respiratoria de los PMN neutrfilos, lo que supone una activacin de sus mecanismos destructivos dependientes de oxgeno (citados ms arriba). estos pptidos son anafilotoxinas, es decir, estimulan la desgranulacin de los mastocitos y de los PMN basfilos , lo cual supone la liberacin de una variedad de sustancias i. ii. iii. histamina: provoca vasodilatacin y aumento de la permeabilidad de los capilares sanguneos. heparina: efecto anticoagulante. factores quimiotcticos que atraen a PMN neutrfilos y eosinfilos.
Todo ello, como se puede ver, va encaminado a congregar hacia el foco de infeccin a las clulas fagocticas, parte de las cuales se activan para mecanismos defensivos. Pero adems, estas anafilotoxinas inducen el que los mastocitos sinteticen prostaglandinas (PG) y leucotrienos (LT), cuyos papeles fisiolgicos son:
intervenir en el mecanismo fisiolgico del dolor favorecer an ms la quimiotaxis de los PMN favorecer ms la vasodilatacin. Reaccin de inflamacin aguda: La inflamacin es una reaccin ante la entrada de un microorganismo a un tejido, con sntomas de dolor (debido a PG y LT), enrojecimiento, hinchazn y sensacin de calor, con un edema debido a la acumulacin de lquido rico en leucocitos. Esta reaccin deriva de algunos de los componentes citados en el anterior epgrafe: Los pptidos C3a y C5a, junto con los factores quimitcticos segregados por los mastocitos atraen hacia el tejido afectado a los PMN que estn circulando por la sangre, que atraviesan los capilares ayudados por el efecto de vasodilatacin de la histamina. Al llegar al foco del microorganismo invasor, las clulas atradas despliegan todo su arsenal: los PMN neutrfilos reconocen (por medio de unos receptores especficos) a los microorganismos "opsonizados" (recubiertos) por C3b, los fagocitan, y en el fagolisosoma formado descargan su "artillera qumica", entre ella los mecanismos dependientes de oxgeno, que han sido activados por C3a y C5a. La vasodilatacin y el incremento en la permeabilidad capilar facilitan la entrada al tejido daado de las enzimas del sistema de coagulacin sangunea: se activa una cascada enzimtica que conduce a la acumulacin de cadenas insolubles de fibrina, que constituyen el cogulo sanguneo. Una vez ocurrida la respuesta de inflamacin aguda, y eliminado el microorganismo por los fagocitos, tiene lugar la reparacin del tejido daado y la regeneracin con tejido nuevo. La reparacin comienza con el crecimiento de vasos capilares en el entramado de fibrina del cogulo sanguneo. Conforme el cogulo se disuelve, va siendo sustituido por fibroblastos nuevos. La cicatriz es el resultado de la acumulacin de nuevos capilares y de fibroblastos. Otros mecanismos de inmunidad inespecfica: A) Mecanismos humorales: Protenas de fase aguda. Estas protenas incrementan su concentracin espectacularmente cuando se produce una infeccin. Una de las m<s importantes es la protena C-reactiva (CRP), que se produce en el hgado ante dao en tejidos. Se une al llamado polisacrido C de la pared celular de una amplia variedad de bacterias y de hongos. Esta unin activa a su vez al complemento, lo que facilita su eliminacin, bien sea por lisis dependiente del complemento (por el complejo de ataque a la membrana, CAM), bien sea por potenciacin de la fagocitosis mediada por el complemento. Interferones (consultar lo estudiado en Virologa). Los interferones modulan, adems la funcin de las clulas NK. B) Mecanismos celulares: dependen de clulas que destruyen "desde fuera" (no por fagocitosis): clulas NK (asesinas naturales): son linfocitos grandes, distintos de los B y T que veremos ms adelante, y que a diferencia de estos poseen grnulos citoplsmicos. Su papel es reconocer clulas tumorales o infectadas con virus, se unen a ellas y liberan al espacio que queda entre ambas el contenido de sus grnulos. una perforina, protena que se ensambla en la superficie de la clula enferma y origina un canal parecido al de CAM, provocando la lisis. factores citotxicos, que matan a la clula enferma PMN eosinfilos: especializados en atacar grandes parsitos, incluyendo helmintos.
1.2.3.2
El sistema de inmunidad adaptativa o especfica
Algunos microorganismos no desencadenan activacin del complemento por la ruta alternativa, y no pueden ser lisados porque no llegan a quedar opsonizados por la protena C3b. Incluso existen microbios que escapan al control de los fagocitos. Para poder enfrentarse con estos "invasores", la evolucin ha desarrollado en los vertebrados, y principalmente en los mamferos, una barrera defensiva adicional, an ms sofisticada, consistente en un tipo de molculas que funcionan como "adaptadores flexibles", que por un lado se unen a los fagocitos, y por el otro se unen al microorganismo, no importa de qu tipo se trate. Este tipo de adaptadores son los anticuerpos. En cada tipo de anticuerpos existen 3 regiones: una que reconoce especficamente a cada invasor dos con funciones biolgicas: unin al complemento, activndolo por la ruta clsica; unin a fagocitos. En la inmunidad especfica se dan dos tipos de respuesta: inmunidad especfica humoral inmunidad especfica celular. A continuacin se expone un breve resumen de ambas respuestas, que nos servir para "abrir boca" de cara al estudio con ms detalle que emprenderemos ms tarde. Los anticuerpos son los mediadores de la inmunidad especfica humoral. La unin entre el antgeno (Ag) y el anticuerpo especfico (Ac) provoca: la activacin del complemento por la ruta clsica, que puede conducir, al igual que en la ruta alternativa, a la lisis del microorganismo invasor; opsonizacin (recubrimiento) de los fagocitos con complejos Ag-Ac, lo cual facilita la fagocitosis; neutralizacin directa de ciertas toxinas y virus por la simple unin Ag-Ac. Obsrvese que los dos primeros efectos son formas que tiene el sistema especfico de "aprovechar" elementos del sistema de inmunidad innata, mediante los cuales determinados elementos de este sistema inespecfico son "encarrilados" mediante los anticuerpos (que son especficos) hacia el foco de la infeccin de un determinado microorganismo, para su eliminacin. Los Ac estn producidos por las clulas plasmticas, diferenciadas a partir de los linfocitos B . Los Ag son las molculas del microorganismo o partcula extaa que evocan y reaccionan con los Ac. Son los Ag los que seleccionan el Ac especfico que les har frente. Sin embargo, cada tipo de Ac est preformado antes de entrar en contacto por primera vez con el Ag. Cada linfocito B que se diferencia en la mdula sea est programado genticamente para sintetizar un solo tipo de Ac , a la espera de contactar con el Ag especfico. Tras su primer contacto con el Ag especfico, cada linfocito B se multiplica y diferencia hasta dar un clon de clulas plasmticas, que fabrican y excretan grandes cantidades del Ac especfico para el que estaba programado el linfocito original. A este fenmeno se le conoce con el nombre de seleccin y expansin clonal. En cada individuo existen cientos de miles, o millones de tipos de linfocitos B, cada uno preparado para originar un clon productor del correspondiente Ac. La respuesta de formacin de Ac provocada tras el primer contacto de cada Ag con el linfocito B se llama respuesta primaria. Este primer contacto confiere al individuo una memoria inmunolgica, de forma que el cuerpo se encuentra preparado para afrontar la eventualidad de una segunda infeccin por el mismo agente. En la respuesta secundaria la formacin de Ac es ms rpida y ms intensa. Ello se debe a que a partir del linfocito primario que tuvo el primer contacto, aparte del clon de clulas plasmticas (responsable de la respuesta primaria), se gener en paralelo otro clon de clulas B de memoria: cuando el Ag entre por
segunda vez, hay en el cuerpo m<s clulas preparadas que las que encontr en la primera ocasin. Adems, estos linfocitos cebados de memorianecesitan menos divisiones celulares antes de poder diferenciarse a su vez en clulas plasmticas productoras de Ac. La memoria inmunolgica es especfica para cada antgeno. Su base es que cada anticuerpo reconoce un solo antgeno (an ms: como veremos, reconocen porciones concretas de cada antgeno, denominadas epitopos). Cmo puede el organismo reconocer tan especficamente molculas "extraas", a las que ataca, y discriminarlas respecto de sus propias molculas, a las que respeta? En 1960 Burnett y Fenner propusieron un hiptesis que se demostrara b<sicamente correcta aos ms tarde: El cuerpo desarrolla ontogenticamente un sistema para distinguir lo propio y evitar reaccionar contra l. Cuando el sistema linfoide se est desarrollando (desde la fase fetal a la perinatal) van llegando a l componentes circulantes de las molculas de las distintas partes del cuerpo; as, el sistema inmune "aprende" a reconocer a estos componentes, y se provoca una incapacidad permanente para reaccionar contra ellos (se "suprimen" o inactivan los clones de linfocitos que reconocen "lo propio"). La inmunidad celular es la otra rama de la inmunidad especfica La inmunidad humoral, por s misma, sera de poca utilidad frente a patgenos intracelulares, bien sea los estrictos (virus) o facultativos (como losMycobacterium o muchos protozoos, como las Leishmania). Para ello ha evolucionado un sistema de inmunidad celular, que est mediatizado por linfocitos T, parecidos citolgicamente a los B, pero que se diferencian en el timo. Los linfocitos T reconocen al Ag extrao siempre que est situado sobre la superficie de clulas del propio organismo hospedador. Pero no pueden reconocer al Ag por s solo, sino que ste ha de estar en combinacin con una molcula marcadora de la superficie celular, que le "dice" al linfocito que est en contacto con una clula "enferma". El receptor de los linfocitos T (TCR) es diferente a los Ac, aunque ambos comparten algunos rasgos estructurales. Las molculas marcadoras de superficie pertenecen al llamado sistema principal de histocompatibilidad (MHC, de "Major Histocompatibility Complex"). Los linfocitos T, al igual que los B, se seleccionan y se activan combinndose con el antgeno (aunque necesitan junto a l molculas MHC), lo que provoca su expansin clonal. Funcionalmente, existen dos tipos de linfocitos T: linfocitos T citototxicos o matadores (TC); linfocitos T colaboradores o coadyuvantes ("helper") (TH); Los linfocitos T citotxicos son los principales efectores de la inmunidad especfica celular: destruyen clulas del propio organismo infectadas por virus. En el cuerpo existe multitud de clones distintos de T C, cada uno de los cuales posee en su superficie receptores distintos de los Ac, aunque con porciones parecidas a las de los Ac. Cada clon de TC est programado para fabricar un solo tipo de receptor, y reconoce la combinacin de un determinado Ag junto con una molcula MHC de clase I, situados sobre la superficie de la clula diana enferma. De esta forma, el TC entra en estrecho contacto con la clula diana, tras de lo cual le da el llamado "beso de la muerte", consistente en la secrecin de sustancias citotxicas, que la matan. Tambin secreta interfern gamma (IFN-(), que tiende a reducir la diseminacin del virus en caso de que ste no induzca bien el IFN-" o el IFN-8. Los linfocitos T colaboradores no tienen actividad matadora, sino que ocupan un papel central en el sistema inmune, activando a otras clulas: macrfagos, linfocitos TC y B. Se unen a una combinacin de {Ag + MHC de clase II} presente en la superficie de macrfagos que tengan en su interior algn parsito que ha logrado sobrevivir intracelularmente. (En estos casos, el macrfago, aunque no ha logrado vencer por s mismo al parsito, ha logrado al menos procesar y enviar a la superficie antgenos del invasor). Al unirse al macrfago de esta manera, se induce en el TH la produccin de IFN-
gamma y de linfocinas, que activan las funciones del macrfago , provocando la muerte intracelular del parsito. De nuevo nos encontramos con otro ejemplo de conexin entre el sistema de inmunidad natural y el adquirido. (El sistema de inmunidad adquirida, que es muy especfico, y que supone un logro evolutivo "reciente" -apareci en los vertebrados- aprovecha lo que ya saba hacer el ms primitivo sistema de inmunidad natural, mejorndolo y confirindole especificidad de modo indirecto; esto es un buen ejemplo de que la evolucin no suele desechar logros antiguos, sino que los reutiliza y modifica para integrarlos en sistemas cada vez ms complejos y perfectos). Los linfocitos TH juegan un papel importante en la activacin y expansin clonal de los linfocitos B para producir anticuerpos, y de los linfocitos T citotxicos. Como se ve, la inmunidad innata y la adquirida no se dan independientes una de la otra, sino que interactan estrechamente entre s en toda respuesta inmune. Como ha quedado indicado, los macrfagos y otras clulas del sistema innato de inmunidad intervienen en la activacin de la respuesta inmune especfica (adquirida); por otro lado, varios factores solubles del sistema de inmunidad adquirida (citoquinas, componentes del complemento) potencian la actividad de las clulas fagocticas del sistema innato. Resumiendo, podemos expresar as las principales caractersticas de las respuestas inmunes especficas: Especificidad hacia antgenos distintos. De hecho, como veremos oportunamente la especificidad es hacia porciones concretas del antgeno o partcula extraa, denominados epitopos o determinantes antignicos. Dicha especificidad es anterior al contacto con el antgeno, y se produce durante las primeras fases de vida del individuo, en las que se originan clones diferentes de linfocitos T y B, cada uno con un tipo de receptor capacitado para enfrentarse ulteriormente a epitopos concretos. Diversidad: el repertorio de linfocitos en cada individuo es gigantesco (se calcula que en humanos es al menos de mil millones), y se deriva de variaciones en los sitios de unin para el antgeno en los correspondientes receptores de clulas T y B. El origen de dichas variantes reside en un complejo conjunto de mecanismos genticos. Memoria inmunolgica, de modo que el organismo guarda recuerdo de cada agente o partcula extraa tras su primer contacto con l. En los ulteriores encuentros del sistema inmune con cada antgeno se producir una respuesta secundaria ms rpida, ms intensa y en el caso de los anticuerpos, cualitativamente superior a la respuesta primaria. La memoria inmunolgica se aprovecha para las tcnicas de vacunacin activa, que tan importantes son en la profilaxis de enfermedades infecciosas. Autolimitacin, de modo que la respuesta va decayendo con el tiempo, conforme se va eliminando el agente extrao, debido a unos sistemas de retrorregulacin que devuelven el sistema inmune a su nivel basal, preparndolo para nuevas respuestas. Existen varias patologas por hipersensibilidad, en las que se produce una reaccin excesiva del sistema inmune, que puede ser lesiva para el hospedador. Discriminacin entre lo propio y lo ajeno: durante las primeras fases ontogenticas del individuo el sistema inmune especfico "aprende" a reconocer lo propio, de modo que se induce un estado de autotolerancia (incapacidad de atacar a los componentes del propio individuo). Esto supone que lostrasplantes de tejidos procedentes de donadores genticamente distintos sean rechazados. Los fallos en este sistema de discriminacin entre lo propio y lo ajeno puede desembocar en enfermedades por autoinmunidad (ataque a componentes propios). En los prximos captulos veremos: la base celular del sistema inmune los desencadenantes de la respuesta: antgenos Anticuerpos y reacciones antgeno-anticuerpo Base gentica de la diversidad de los anticuerpos Otras molculas del sistema inmune que interactan con los antgenos, as como el procesamiento de stos Origen y seleccin de clulas T y sus papeles Visin global de la respuesta inmune (humoral y celular), incluyendo el contexto anatmico donde se producen Las citoquinas como factores solubles de la inmunidad adquirida Respuestas inmunes mediatizadas por inmunoglobulina IgE
Regulacin de la respuesta inmunitaria y origen de la tolerancia Cmo se imbrica el sistema complemento en las respuestas inmunes A partir de este ltimo punto entramos en aspectos ms "aplicados" de la inmunologa: trataremos las estrategias del sistema inmune frente a agentes externos concretos (virus, bacterias, protozoos, etc.), o hacia clulas cancerosas, as como diversas patologas derivadas de alteraciones del sistema inmune (hipersensibilidad, autoinmunidad, inmunodeficiencias), sin olvidar los mtodos que la tcnica nos suministra para manipular el sistema inmune (vacunas, injertos).
Copyright 1999 Enrique Iez Pareja. Prohibida la reproduccin con fines comerciales.
Potrebbero piacerti anche
- Sistemas Amplificadores de Respuesta InmuneDocumento20 pagineSistemas Amplificadores de Respuesta InmuneXiomara GarciaNessuna valutazione finora
- InmunologíaDocumento14 pagineInmunologíaMiriam Sánchez De LucasNessuna valutazione finora
- 14inmunologia PDFDocumento40 pagine14inmunologia PDFJessica MartínezNessuna valutazione finora
- 4 Biología Electivo Guía Inmunidad PDFDocumento13 pagine4 Biología Electivo Guía Inmunidad PDFcamilo_jeraldo_1Nessuna valutazione finora
- Caracteristicas Generales Del Sistema InmunologicoDocumento5 pagineCaracteristicas Generales Del Sistema InmunologicoWilfer Hilaquita Condori0% (2)
- 1-El Sistema Imunológico y La Inmunidad InnataDocumento24 pagine1-El Sistema Imunológico y La Inmunidad InnataYolandaNessuna valutazione finora
- Fisiología de Los Sistemas Linfático e InmunitarioDocumento17 pagineFisiología de Los Sistemas Linfático e InmunitarioYaRe isaNessuna valutazione finora
- 1era. CLASE PDFDocumento39 pagine1era. CLASE PDFEliangel lacleNessuna valutazione finora
- Mecanismos de Defensa Del Huésped Frente A La InfecciónDocumento2 pagineMecanismos de Defensa Del Huésped Frente A La InfeccióngsaNessuna valutazione finora
- INMUNOLOGIADocumento29 pagineINMUNOLOGIAmonica.vega.baNessuna valutazione finora
- INMUNOLOGIADocumento26 pagineINMUNOLOGIAMaria Cruz LavadoNessuna valutazione finora
- Atención de Enfermería A Pacientes Con Enfermedades InfecciosasDocumento28 pagineAtención de Enfermería A Pacientes Con Enfermedades InfecciosasAgny MoraNessuna valutazione finora
- Nuevo Documento de Microsoft WordDocumento6 pagineNuevo Documento de Microsoft WordNadia JacquelineNessuna valutazione finora
- Fisio Tema 30Documento8 pagineFisio Tema 30lucisNessuna valutazione finora
- 2702-LIBRO N°3 - SALUD HUMANA-BIOLOGÍA MENCIÓN-2016-web PDFDocumento64 pagine2702-LIBRO N°3 - SALUD HUMANA-BIOLOGÍA MENCIÓN-2016-web PDFMACARENA CASTILLO MUNOZNessuna valutazione finora
- InmunidadDocumento12 pagineInmunidadLulu PerezNessuna valutazione finora
- Informe Inmunidad FinalDocumento13 pagineInforme Inmunidad Finalfrancklinmp.2022Nessuna valutazione finora
- Bloque 5 InmunologiaDocumento16 pagineBloque 5 InmunologiaPepa ValdesNessuna valutazione finora
- InmunologiaDocumento16 pagineInmunologiaJose Frco100% (1)
- Biología B5Documento13 pagineBiología B5Daniela SolanaNessuna valutazione finora
- GUIA SISTEMA INMUNE Doris Sanchez Grado Octavo NuevoDocumento4 pagineGUIA SISTEMA INMUNE Doris Sanchez Grado Octavo Nuevojuan camilo100% (1)
- Punto 4 S.IDocumento7 paginePunto 4 S.Iandreas.bb1902Nessuna valutazione finora
- Sistema InmunitarioDocumento30 pagineSistema InmunitarioSandiely CarmonaNessuna valutazione finora
- Modo de Entrada de Los MicroorganismosDocumento11 pagineModo de Entrada de Los MicroorganismosBetsy Viviani Vargas BautistaNessuna valutazione finora
- Tema 3 FISIOPATOLOGÍA-higieneDocumento7 pagineTema 3 FISIOPATOLOGÍA-higieneevaNessuna valutazione finora
- U.T. 3. Reconocimiento de Los Trastornos Del Sistema InmunitarioDocumento19 pagineU.T. 3. Reconocimiento de Los Trastornos Del Sistema InmunitarioAdriel Rodriguez AgudoNessuna valutazione finora
- Unidad 9 Sistema Inmunológico Abril 2020-4Documento15 pagineUnidad 9 Sistema Inmunológico Abril 2020-4Tania FloresNessuna valutazione finora
- Inmunidad Innata Y Adquirida: Integrantes: Alejandra Riadi Samur Nicole Viveros GunckelDocumento15 pagineInmunidad Innata Y Adquirida: Integrantes: Alejandra Riadi Samur Nicole Viveros GunckelLandon ConnorNessuna valutazione finora
- InmunologiaDocumento17 pagineInmunologiaLara MayoralNessuna valutazione finora
- Inmuno 202209161606033fwqv2525wDocumento10 pagineInmuno 202209161606033fwqv2525wMarianella PonceNessuna valutazione finora
- Mecanismos de DefensaDocumento6 pagineMecanismos de DefensaJose GuevaraNessuna valutazione finora
- Exposicion Sistema InmunologicoDocumento3 pagineExposicion Sistema InmunologicoJhuly Jovana Haro PérezNessuna valutazione finora
- Inmunologia Unidad1Documento24 pagineInmunologia Unidad1Genesis Anahi Santamaria RamosNessuna valutazione finora
- Eje 1 Sistema Inmune Mecanismos InespecificosDocumento7 pagineEje 1 Sistema Inmune Mecanismos InespecificosMary Tamara JimenezNessuna valutazione finora
- Inmunidad Microbiana (Mariela-Unellez)Documento8 pagineInmunidad Microbiana (Mariela-Unellez)Jesus Rodríguez50% (2)
- Resumen de InmunidadDocumento10 pagineResumen de InmunidadLisbeth Crespo CuencaNessuna valutazione finora
- Discusion 2Documento8 pagineDiscusion 2Milver EscalanteNessuna valutazione finora
- Actividad N 5 y N 6 - SISTEMA INMUNITARIODocumento6 pagineActividad N 5 y N 6 - SISTEMA INMUNITARIOMariana PaolaNessuna valutazione finora
- Guia de Comprension Lectora para Activida N8Documento6 pagineGuia de Comprension Lectora para Activida N8Lorena Guerra QuezadaNessuna valutazione finora
- Sistema InmunitarioDocumento31 pagineSistema Inmunitariooscarsan2013Nessuna valutazione finora
- Reconocimiento de Los Trastornos Del Sistema InmunitarioDocumento16 pagineReconocimiento de Los Trastornos Del Sistema InmunitarioNoa GoyanesNessuna valutazione finora
- Clase 5, 09 - 04Documento13 pagineClase 5, 09 - 04Isabella MoralesNessuna valutazione finora
- InmunidadDocumento9 pagineInmunidadNargarothFukkNessuna valutazione finora
- Biología 2º Bach Anexo - InmunologíaDocumento10 pagineBiología 2º Bach Anexo - InmunologíagenusxyzNessuna valutazione finora
- InmudidadDocumento34 pagineInmudidadFabrizzio RomeroNessuna valutazione finora
- Mecanismo de Defensa Natural de Nuestro OrganismoDocumento10 pagineMecanismo de Defensa Natural de Nuestro OrganismoPriscillaLoretoToledoRamosNessuna valutazione finora
- Taller Células Del Sistema Inmune Humano Como Modelo de Estudio de La Célula EucariotaDocumento9 pagineTaller Células Del Sistema Inmune Humano Como Modelo de Estudio de La Célula EucariotaLuis Eduardo Perez LopezNessuna valutazione finora
- Apuntes de Anatomia Del S. Respiratorio y DigestivoDocumento14 pagineApuntes de Anatomia Del S. Respiratorio y DigestivoPau GallardoNessuna valutazione finora
- El Sistema InmunitarioDocumento109 pagineEl Sistema InmunitarioMikel OrosaNessuna valutazione finora
- El Proceso InfecciosoDocumento14 pagineEl Proceso InfecciosoSilviaJaelVillcaRamirezNessuna valutazione finora
- Tortora Inmunidad InnataDocumento11 pagineTortora Inmunidad InnatafranciscaNessuna valutazione finora
- Barreras BiológicasDocumento3 pagineBarreras Biológicascgonzalezjara50% (2)
- INMUNOLOGÍADocumento10 pagineINMUNOLOGÍAmzspqbzx7dNessuna valutazione finora
- Glóbulos Blancos o LeucocitosDocumento4 pagineGlóbulos Blancos o LeucocitosFrancisco Walde HuamanNessuna valutazione finora
- Respuesta Inmmune MicrobiologiaDocumento7 pagineRespuesta Inmmune MicrobiologiaAndrea Gissel Mart�nez BocanegraNessuna valutazione finora
- HISTOLOGÍA DEL SISTEMA INMUNE - ExpoDocumento26 pagineHISTOLOGÍA DEL SISTEMA INMUNE - Expociudadazul2011Nessuna valutazione finora
- INMUNOLOGDocumento27 pagineINMUNOLOGortiz1081Nessuna valutazione finora
- Clase 2 Inmunologia Celular y MolecularDocumento44 pagineClase 2 Inmunologia Celular y Molecular05-TL-HU-KARINA SUSAN CARLOS PEREZNessuna valutazione finora
- Tabla Células Sanguineas PDFDocumento3 pagineTabla Células Sanguineas PDFSam ReyesNessuna valutazione finora
- Factores de CoagulaciónDocumento22 pagineFactores de CoagulaciónSam ReyesNessuna valutazione finora
- Reglas de BaldwinDocumento7 pagineReglas de BaldwinSam ReyesNessuna valutazione finora
- MHCDocumento11 pagineMHCSam ReyesNessuna valutazione finora
- Leishmania MexicanaDocumento32 pagineLeishmania MexicanaSam ReyesNessuna valutazione finora
- Historia de La FarmaciaDocumento176 pagineHistoria de La FarmaciaSam ReyesNessuna valutazione finora
- Neumonia en Adultos - UptodateDocumento40 pagineNeumonia en Adultos - UptodateJmv VegaNessuna valutazione finora
- INMUNOLOGÍADocumento73 pagineINMUNOLOGÍAIVANNA VALENTINA ANGULO ECHEGARAYNessuna valutazione finora
- Anemia Hemolitica Inducida Por DrogasDocumento8 pagineAnemia Hemolitica Inducida Por DrogasMaría José Mattamala InostrozaNessuna valutazione finora
- Sistema Linfático TripticoDocumento2 pagineSistema Linfático TripticoMaria Elena Sanchez Guevara100% (1)
- Inmunologia Basica y Clil oDocumento220 pagineInmunologia Basica y Clil oCarlos Cabrera100% (3)
- Órganos Linfáticos - InmunidadDocumento8 pagineÓrganos Linfáticos - InmunidadDanilo CavassimNessuna valutazione finora
- Bacterias y VirusDocumento6 pagineBacterias y VirusNicolás Polito MuñozNessuna valutazione finora
- Modulo 5Documento14 pagineModulo 5Bamboo SeniorNessuna valutazione finora
- Toxicologia Industrial PDFDocumento37 pagineToxicologia Industrial PDFjaniroMANessuna valutazione finora
- Trabajo de Investigación Formativa Grupo 8Documento52 pagineTrabajo de Investigación Formativa Grupo 8JOSHUA DANIEL ARAPA BUDIELNessuna valutazione finora
- Inmunógenos y Antígenos: Características, Procesamiento, PresentaciónDocumento6 pagineInmunógenos y Antígenos: Características, Procesamiento, PresentaciónroseNessuna valutazione finora
- Chavez Vasquez Nancy1Documento2 pagineChavez Vasquez Nancy1Las Orquideas CixNessuna valutazione finora
- Manual Anemia Infecciosa EquinaDocumento30 pagineManual Anemia Infecciosa Equinaapuntesdelcev100% (2)
- Diapo Micro PDFDocumento438 pagineDiapo Micro PDFMarta GonsalvesNessuna valutazione finora
- Pci CCNN 2019Documento9 paginePci CCNN 2019Teonila DotaNessuna valutazione finora
- Nevos Vasculares PDFDocumento12 pagineNevos Vasculares PDFFABIOLA NOEMI MAMANI PAREDEZNessuna valutazione finora
- Respuesta Inmunológica Frente A HongosDocumento2 pagineRespuesta Inmunológica Frente A HongosAlondra VegaNessuna valutazione finora
- Resuemen de VirologiaDocumento79 pagineResuemen de VirologiaCésar AlcaláNessuna valutazione finora
- Leucocitos FPTDocumento74 pagineLeucocitos FPTMariana RomeroNessuna valutazione finora
- Leucocitos - 08Documento39 pagineLeucocitos - 08Cecilia Rodríguez CámaraNessuna valutazione finora
- Mecanismos Lesivos BacterianosDocumento19 pagineMecanismos Lesivos BacterianoscarmenNessuna valutazione finora
- 2018-08-09 Saber Vivir ArgentinaDocumento56 pagine2018-08-09 Saber Vivir ArgentinaAnonymous RSHGV3O7sNessuna valutazione finora
- Experiencia 1 DPCCDocumento7 pagineExperiencia 1 DPCCLesly Marili Morante AncajimaNessuna valutazione finora
- Aujeszky 2Documento40 pagineAujeszky 2M.C. Jose Ramon Hernandez SalgadoNessuna valutazione finora
- Causalidad Tarea 2 Laboratoria EpidemiologiaDocumento7 pagineCausalidad Tarea 2 Laboratoria EpidemiologiaRafaela Ernestina EncarnaciónNessuna valutazione finora
- Fisiopatología de Los Leucocitos. TXDocumento7 pagineFisiopatología de Los Leucocitos. TXIngrith CáceresNessuna valutazione finora
- Fisiopatología de Las AlergiasDocumento12 pagineFisiopatología de Las AlergiasMontse Lopez ChavezNessuna valutazione finora
- Celulas SanguineasDocumento4 pagineCelulas SanguineasAngie CruzNessuna valutazione finora
- Qué Es El CONAPDISDocumento4 pagineQué Es El CONAPDISDoctora JuridicoNessuna valutazione finora
- Periodo de Lactancia-CerdosDocumento24 paginePeriodo de Lactancia-CerdosAnonymous LANCVGRE8Nessuna valutazione finora