Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Practicas Evaporadores
Caricato da
Ricardo Rivas GonzálezCopyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Practicas Evaporadores
Caricato da
Ricardo Rivas GonzálezCopyright:
Formati disponibili
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
t
Laboratorio de operaciones de separacin I
Alumno:
Torres Ortiz Eduardo
Grupo: 6im3
Reporte de prcticas
Profra. Hortensia Dvalos
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
PRACTICA No. 1
EVAPORADOR DE SIMPLE EFECTO DEL TIPO DE CIRCULACIN FORZADA CON
RECIRCULACIN.
Objetivos:
Que el alumno al trmino de las sesiones correspondientes al estudio de este equipo sea capaz de:
Explicar el funcionamiento del Evaporador de Simple Efecto de Circulacin Forzada.
Operar el equipo realizando cambios en las variables que puedan ser controladas a voluntad del operador.
Analizar los efectos de los cambios de las variables y como lograr un aumento en la capacidad de
produccin.
Introduccin terica:
EVAPORACION
Evaporacin es una operacin de la Ingeniera Qumica, que consiste en separar parcialmente el solvente de un la
solucin formada por un soluto no voltil, calentando la solucin hasta su temperatura de ebullicin.
Su objetivo es concentrar soluciones, evaporando parte del solvente: generalmente lo que se evapora es vapor de
agua saturada, el cual al condensarse en una superficie metlica, transmite su calor latente a travs de la pared
metlica que separa el vapor de calentamiento de la solucin que se esta concentrando.
EQUIPOS UTILIZADOS EN EVAPORACION
Los evaporadores son cambiadores de calor, en los cuales el medio de calentamiento es el vapor de agua saturado
que transmite su calor latente al condensador a la presin de saturacin con la que entra al evaporador. La
solucin que se va a concentrar recibe el calor, aumentando su temperatura hasta que se inicie la evolucin y se
produce la evaporacin. El vapor producido debe eliminarse continuamente para mantener una presin interior
constante. El liquido que se concentra debe eliminarse tambin con1inuamente para obtener una solucin a la
concentracin deseada.
EVAPORADORES DE CIRCULACIN FORZADA.
Entre los diseos mas importantes estn los siguientes:
+ Tubos largos verticales, solucin dentro de tubos.
+ Tubos largos horizontales, solucin dentro de tubos
+ Tubos cortos horizontales, solucin fuera de tubos.
+ Tubos largos Inclinados, solucin fuera de tubos.
En estos tipos de evaporadores la ebullicin de la solucin no se efecta dentro de los tubos; esta temperatura se
calcula a la presin del espacio de vapor ya la concentracin final de la solucin. La solucin se recircula por
medio de una bomba centrfuga de gran capacidad, haciendo pasar por el interior de los tubos a alta velocidad
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
saliendo al espacio de vapor en don de se mantiene una baja presin y ah es donde se produce la evaporacin
instantnea, La solucin diluida se introduce en el tubo de recirculacin des pues de la bomba centrfuga y el
producto solucin concentrada se obtiene del tubo de recirculacin antes de la bomba centrfuga.
La circulacin forzada imparte una gran velocidad de la solucin por el interior de los tubos por o que necesita
una cierta energa potencial, la cual se convierte a energa cintica, al cambiar la velocidad de la solucin a la
salida de los tubos; y por efecto del calentamiento de la solucin al pasar por los tubos y por la perdida de presin
al salir de los tubos, la solucin hierve instantneamente, transformando su calor sensible a calor latente que
adquiere el agua evaporada que se produce en el espacio vapor del evaporador .
Para que la evaporacin contine producindose con rapidez hay que eliminar el vapor tan rpido como se forma.
Por este motivo, un lquido se evapora con la mxima rapidez cuando se crea una corriente de aire sobre su
superficie o cuando se extrae el vapor con una bomba de vaco.
1.- TABLA DE DATOS DE CONDICIONES DE OPERACIN:
Presin manomtrica del vapor (Kg/Cm
2
)
0.7
2
cm
Kgf
Temperatura de alimentacin (C) 25 C
Vaco en el condensador (mmHg.) 350 mmHg
2.- TABLA DE DATOS EXPERIMENTALES:
Dimetro
del tanque
(m)
Temperaturas (C) Tiempo de
operacin
(min)
Diferencias de
altura de nivel
(cm)
M
A
(Kg./h)
Solucin diluida
0.596 25 15 13.5
M
p
(Kg./h)
Solucin
concentrada 0.346 67 15 23.5
E (Kg./h)
Solvente
evaporado
0.346
E
67
Ec
48
15 17.2
M
v
(Kg./h)
Vapor de agua de
caldera
0.402
Mv
110
Mvc
44
15 17.1
M
H2O
(Kg./h)
Agua de
condensacin
0.56
t
entrada
25
t
salida
36
0.5 8.6
M
R
(Kg./h)
Masa de
recirculacin
t
entrada de la cal andri a
65
t
salida de la
calandria
71
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
3.- SECUENCIA DE CLCULOS:
BALANCE DE MATERIALES.
Masa de la solucin diluida
u
A A
2
A
h D 785 . 0 A
=
A
M
m cm h
A
135 . 0 5 . 13 = = A
A
a 25 C=
( )
3 3
3 3
3
5 . 996
1
100
1000
1
9965 . 0
m
Kg
m
cm
g
kG
cm
g
=
|
|
.
|
\
|
|
|
.
|
\
|
( ) ( )
|
.
|
\
|
=
|
.
|
\
|
=
h
kg m
Kg
m
M
A
1
min 60
min
5 . 2
min 15
0.042m 302 . 997 596 . 0 785 . 0
3
2
=150
hr
kg
Masa de la solucin concentrada
u
) h ( ) ( Dp 785 . 0
P P
2
A
=
P
M
m cm 235 . 0 5 . 23 h
p
= = A
( )
3 3
3 3
3
P
8 . 978
1
100
1000
1
9788 . 0 67
m
Kg
m
cm
g
Kg
cm
g
C a =
|
|
.
|
\
|
|
|
.
|
\
|
=
hr
kg
h
kg
m
Kg
M
P
466 . 86
1
min 60
min
4411 . 1
min 15
(.235m) ) 68 . 978 ( (0.346m) 785 . 0
3
2
=
|
.
|
\
|
= =
Masa del evaporado
( ) ( ) ( )
u
E E E
E
h D
M
A
=
2
785 . 0
m cm h
E
172 . 0 2 . 17 = = A
3
8 . 978 67
m
Kg
C a
E
=
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
( ) ( ) ( )
h
Kg
h
Kg
m
m
Kg
M
E
3 . 63
1
min 60
min
055 . 1
min 15
172 . 8 . 978 346 . 0 785 . 0
3
2
=
|
.
|
\
|
=
|
.
|
\
|
=
Del balance de metera general.
Mc Mp M Mv M
E A
+ + = + (1)
Balance de vapor
Mc Mv = (2)
Sustituyendo 2 en 1 y despejando M
A
Mp M M
E A
+ =
Mp M M
A E
+ =
h
Kg
h
Kg
h
Kg
M
E
543 . 63 466 . 86 150 = =
Balance de calor
McHc MpHp H M MvHv H M
E E A A
+ + = +
McHc v Mv MvHv + =
McHc MvHv v Mv =
A A E E
H M MpHp H M MvHv + + =
A A
t Cp H A =
tp Cp Hp A =
CpEPE t a H H
ev E E
+ =
( )
Kg
Kcal
C
C Kg
Kcal
H
A
25 0 25
1 = =
( )
Kg
Kcal
C
C Kg
Kcal
Hp 67 0 67
1 = =
Kg
Kcal
Kg
Kcal
C a H
E
1 . 626 ) 0 ( 5 . 0 1 . 626 67 = + =
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Calor absorbido
A A E E A
H M MpHp H M Q + =
h
Kcal
Kg
Kcal
h
Kg
Kg
Kcal
Kg
Kcal
Kg
Kcal
h
Kg
Q
A
352 . 41675 25 150 67 466 . 86 1 . 626 3 . 63 =
|
|
.
|
\
|
|
|
.
|
\
|
|
|
.
|
\
|
+
|
|
.
|
\
|
=
Calor suministrado
V V S
M Q =
kg
kcal
C a
h
kg kg
m
m
Kg
m
M
m
Kg
C a v
h D
M
V
V
V V V
V
6 . 532 110
86
min
433 . 1
min 15
) 171 . ( ) 4 . 990 ( ) 4026 . 0 ( 785 . 0
990 44
785 . 0
3
2
3
2
=
= =
|
|
|
|
.
|
\
|
=
=
|
|
.
|
\
| A
=
u
hr
kcal
kg
kcal
h
kg
Q
S
6 . 45803 ) 6 . 532 )( 86 ( = =
Calor perdido
A S P
Q Q Q =
hr
kcal
hr
kcal
hr
kcal
Q
P
25 . 4128 352 . 41675 6 . 45803 = =
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Calculo de U
C t t t
C t t t
C
C
C
C C
t
t
t t
T
C hm
kcal
C m
h
Kcal
T A
Q
U
T A U Q
n Sol s VS
n Sol e VS
A
A
= = = A
= = = A
=
=
A
A
A A
= A
=
A
=
A =
45 65 110
39 71 110
9284 . 41
39
45
ln
39 45
ln
019 . 1038
) 928 . 41 )( 9575 . 0 (
41675
' 2
' 1
2
1
2 1
2 2
( )( )( )
tubos tubos de Nmero nt
m cm D
m L
m m nt L D A
4
03 . 0 3
55 . 2
9575 . 0 4 55 . 2 03 . 0 ) (
2 2
= =
= =
=
= = = t t
Factor de economia.
utilizado vapor Kg
evaporado de Kg
M
E
V
.
.
= = c
utilizado vapor Kg
evaporado de Kg
h
kg
h
Kg
.
.
7664 . 0
596 . 82
3 . 63
= = c
Capacidad evaporativa.
( )( )( )( )
2
.
2 2
.
9613 . 0 4 55 . 2 03 . 0
.
.
84 . 65
9613 . 0
3 . 63
m nt L D A
m h
evaporado de Kg
m
h
Kg
A
E
C
calor de transf
calor de transf
E
= = =
= = =
t t
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Capacidad de transferencia de vapor.
T U
A
Q
C
calor de transf
A
Q
A = =
.
2 2
1176 . 43353
9613 . 0
352 . 41675
hm
kcal
m
h
Kcal
C
Q
= =
Eficiencia trmica.
100 x
Q
Q
t
S
A
= q
Calculo de la velocidad a la entrada de los tubos de la calandria Ve
t Cp
Q
M
t Cp M Q
A
R
R A
A
=
A =
( )
h
Kg
C
C Kg
Kcal
h
Kcal
M
R
892 . 6945
65 71 *
1
352 . 41675
=
=
( )
( )
s
m
s
h
h
m
m
Kg
m
h
Kg
A
M
Ve
p flujo
R
69 . 0
. 3600
1
3189 . 2509
459 . 979 002826 . 0
892 . 6945
3
2
=
|
.
|
\
|
=
|
.
|
\
|
= =
3
459 . 979 68
m
Kg
C a =
( ) ( ) ( ) ( )
2
2 2
002826 . 0 4 03 . 0 785 . 0 785 . 0 m nt D A
flejo
= = =
91 100
6 . 45803
352 . 41675
= = x
hr
kcal
h
Kcal
t q
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Velocidad a la salida de los tubos de la calandria.
+ Como se trata de el mismo liquido y no hay cambio de fase la velocidad va a ser la misma a la entrada y a
la salida, por lo tanto:
s
m
Vs 69 . 0 =
Tiempo de residencia.
s
m Vs Ve
Vmedia 69 . 0
2
69 . 0 69 . 0
2
=
=
+
=
s
s
m
m
Vmedia
Ltubos
t
residencia
68 . 3
69 . 0
54 . 2
= = =
4.- Condensador.
Calculo suministrado por el solvente
kg
kcal
T evaporado del latente Calor
Donde
kg
kcal
h
Kg
Q
E Q
C Evaporado E
C
E C
1 . 559 @
:
h
kcal
03 . 35391 ) 1 . 559 )( 3 . 63 (
. 66
= =
= =
=
=
Calor transferido al agua.
.
1
h
kcal
8 . 27871 C 25) - (36
Kg
Kcal
1 8 . 533 2
) (
2
2
2 2 2
2
Kg
Kcal
Cp
h
Kg
Q
T T Cp M Q
O H
A
O H Entrada Salida O H O H A
O H
O H
=
=
|
|
.
|
\
|
|
.
|
\
|
=
=
h
Kg
h
kg
m
m
Kg
m
M
m
Kg
h D
M
O H
O H O H O H
O H
8 . 2533
1
min 60
min
23 . 42
min 5 . 0
) 086 . 0 )( 9 . 996 ( ) 56 . 0 ( 785 . 0
9 . 996
785 . 0
3
2
3
2
2
2 2 2
2
=
|
.
|
\
|
= =
=
A
=
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Calor perdido.
h
Kcal
Qc Q Qs
A
77 . 93832 03 . 35391 1239223 = = =
Eficiencia trmica.
78
03 . 35391
8 . 27871
= = =
h
Kcal
h
Kcal
Qc
Q
t
A
q
Fuerza impulsora a la transferencia de calor.
C t 51 25 76 = = A
Coeficiente global de transferencia de calor.
2
2 2
9226 . 1 9613 . 0 2 . 2
902 . 1317
) 51 )( 9226 . 1 (
8 . 129223
m calandria la de A x A
C hm
kcal
C m
h
Kcal
U
T A
Q
U
tc
tc
A
= = =
= =
A
=
La velocidad de agua de condensacin
tubos nt
m cm D
E A
nt D A
s
m
s
h
h
m
m E
h
Kg
v
A
M
v
flujo
flujo
O H
O H flujo
O H
O H
2
03 . 0 3
3 413 . 1 2 03 . 0 785 . 0
785 . 0
4981 . 0
3600
1
2059 . 1793
1000 3 413 . 1
8 . 2533
2
2
2
2
2
2
=
= =
= =
=
=
|
.
|
\
|
=
=
=
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
5.-Tabla de resultados.
Kg/hr Q
A
Kcal/h
Q
S
Kcal/h
Qp
kcal/h
U
Kcal/hm
2C
C
E
(kg/hm
2
) C
Q
(kcal(hm
2
)
M
A
150
41675.4 45803.6 4128.25 1038.019 0.7664 65.84 43353.12
M
P
86.466
E 63.3
Ve(m/s) Vs(m/s)
91% 0.69 0.69
Condensador
M
H2O
kg/hr
Q
C
Kcal/kg
Q
H20
Kcal/kg
Qs
Kcal/h
t U V
H20
(m/s)
2533.8 35391.03 27871.8 9383.2 78% 1317.902 0.4981
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
CONCLUCIONES:
Ya que este tipo de evaporadores cuanta con una recirculacin se va a generar una presin hidrosttica
dentro de los tubos, lo cual va generar que la ebullicin sea dentro del separador y no dentro de los tubos
como en el caso de los evaporadores de circulacin natural; este proceso que se lleva a cabo dentro del
separador se llama flasheo, lo cual se genera por una diferencia de presiones generada al mantener el
separador un poco mas arriba que la calandria, este flasheo tambin es generado gracias a que la
recirculacin esta viene con una temperatura mayor del separador calentando a la solucin fresca.
La presin hidrosttica es generada por la columna hidrosttica que se forma al recircular la solucin y
se junta con la solucin de alimentacin fresca, posterior mente es alimentada a la calandria para as
repetir el proceso de flasheo y de recirculacin.
Este tipo de equipos es ms utilizado cuando se quiere concentrar soluciones alcalinas como el NaOH, el
inconveniente es que al utilizar este tipo de sustancias se puede generar con mayor facilidad
incrustaciones en los tubos y disminuir su capacidad de transferencia de calor, en nuestro caso el equipo
lo acababan de limpiar, por lo cual, al realizar la prctica nos genero una eficiencia muy elevada del
99%, pero claro que este no es el nico factor por lo cual la eficiencia es alta, tambin influyo el manejo
del equipo y el tipo de solucin con el que trabajamos.
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
PRACTICA No. 2
EVAPORADOR DE SIMPLE EFECTO DE CIRCULACIN NATURAL DEL TIPO DE PELCULA
ASCENDENTE-DESCENDENTE.
Objetivos:
Qu el alumno al trmino de las sesiones correspondientes al estudio de este equipo experimental sea capaz
de:
+ Explicar el funcionamiento del evaporador de Simple Efecto con Circulacin Natural del tipo de Pelcula
Ascendente-Descendente.
+ Operar el equipo realizando cambios en las variables que pueden ser controladas a voluntad del operador.
+ Analizar los efectos de los cambios de las variables y como lograr un aumento en la capacidad de
produccin.
Introduccin terica:
EVAPORADOR DE PELICULA DESCENDENTE
Estos tipos de evaporadores son los ms difundidos en la industria alimenticia, por las ventajas
operacionales y econmicas que los mismos poseen. Estas ventajas se pueden resumir de la siguiente
forma:
Alta eficiencia, economa y rendimiento.
Alta flexibilidad operativa.
Altos coeficientes de transferencias trmicos.
Capacidad de trabajar con productos termosensibles o que puedan sufrir deterioro parcial o total de sus
propiedades.
Limpieza rpida y sencilla (CIP)
En estos evaporadores la alimentacin es introducida por la parte superior del equipo, la cual ha sido
normalmente precalentada a la temperatura de ebullicin del primer efecto, mediante intercambiadores
de calor adecuados al producto
Se produce una distribucin homognea del producto dentro de los tubos en la parte superior del
evaporador, generando una pelcula descendente de iguales caractersticas en la totalidad de los tubos.
Este punto es de suma importancia, ya que una insuficiente mojabi lidad de los tubos trae aparejado
posibles sitios en donde el proceso no se desarrolla correctamente, lo cual lleva a bajos rendimientos de
evaporacin, ensuciamiento prematuro de los tubos, o eventualmente al taponamiento de los mismos.
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Dentro de los tubos se produce la evaporacin parcial, y el producto que esta siendo concentrado,
permanece en ntimo contacto con el vapor que se genera. Los dos fluidos, tanto el producto como su
vapor, tienen igual sentido de flujo, por lo que la salida de ambos es por la parte inferior de los tubos.
En la parte inferior del evaporador se produce la separacin de estas dos fases. El concentrado es tomado
por bombas y el vapor se enva al condensador (simple efecto), mientras que los sistemas mltiefecto
utilizan como medio calefactor, el vapor generado en el efecto anterior, y por lo tanto el vapor generado
en el ltimo cuerpo es el que se enva al condensador.
EVAPORADOR DE PELICULA ASCENDENTE
Un evaporador de pelcula ascendente consta de una calandria de tubos dentro de una carcasa, la
bancada de tubos es ms larga que en el resto de evaporadores (10-15m). El producto utilizado debe ser
de baja viscosidad debido a que el movimiento ascendente es natural. Los tubos se calientan con el
vapor existente en el exterior de tal forma que el lquido asciende por el interior de los tubos, debido al
arrastre que ejerce el vapor formado. El movimiento de dichos vapores genera una pelcula que se
mueve rpidamente hacia arriba.
En estos tipos de evaporadores la alimentacin se produce por la parte inferior del equipo y la misma
asciende por los tubos.
El principio terico que tienen estos evaporadores se asimila al 'efecto si fn', ya que cuando la
alimentacin se pone en contacto con los tubos calientes, comienza a producirse la evaporacin, en
donde el vapor se va generando paulatinamente hasta que el mismo, empieza a ejercer presin hacia los
tubos, determinando de esta manera, una pelcula ascendente. Esta presin, tambin genera una
turbulencia en el producto que est siendo concentrado, lo que permite mejor la transferencia trmica, y
por ende, la evaporacin.
En estos evaporadores existe alta diferencia de temperaturas entre la pared y el lquido en ebullicin.
Cabe mencionar que la altura de los mismos es limitada, ya que la capacidad del vapor en arrastrar la
pelcula formada hacia la parte superior del equipo no es suficiente y determina la altura mxima posible
para el diseo.
Son evaporadores en los cuales se puede re circular el producto concentrado, donde el mismo es enviado
nuevamente al interior del equipo, y de esta forma, asegurar un correcto caudal de alimentacin.
EVAPORADOR DE CIRCULACION NATURAL
En un evaporador de circulacin natural se distribuyen una serie de tubos cortos verticales (calandria de
tubos) dentro de una carcasa por donde circula el vapor. Cuando se calienta el producto, la propia
evaporacin de este hace que vaya subiendo por el interior de los tubos (evaporacin sbita que arrastra
el lquido), mientras que por el exterior de los mismos condensa el vapor calefactor.
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
El producto concentrado junto con el vapor generado pasa a una cmara de vaco, donde el vapor se
destina al condensador (si tiene valor aadido) o se libera, y el producto concentrado puede volver a
introducirse como alimentacin si se requiere mayor concentracin, o extraerlo del equipo como
producto final.
1.- TABLA DE DATOS DE CONDICIONES DE OPERACIN:
Presin manomtrica del vapor (Kg/Cm
2
)
0.8
2
cm
Kgf
Temperatura de alimentacin (C) 64 C
Vaco en el condensador (mmHg.) 360 mmHg
2.- TABLA DE DATOS EXPERIMENTALES:
Dimetro
del tanque
(m)
Temperaturas (C) Tiempo de
operacin
(min)
Diferencias de
altura de nivel
(cm)
M
A
(Kg./h)
Solucin diluida 0.596 64 15 17.5
M
p
(Kg./h)
Solucin
concentrada 0.346 68 15 27.1
E (Kg./h)
Solvente
evaporado
0.346
E
68
Ec
58
15 24
M
v
(Kg./h)
Vapor de agua de
caldera
0.402
Mv
110
Mvc
54
15 19.7
M
H2O
(Kg./h)
Agua de
condensacin
0.56
t
entrada
24
t
salida
40
0.5 10.5
3.- SECUENCIA DE CALCULOS.
BALANCE DE MATERIALES.
Masa de la solucin diluida
u
A A
2
A
h D 785 . 0 A
=
A
M
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
m cm h
A
175 . 0 5 . 17 = = A
A
a 64 C=
( )
3 3
3 3
3
6 . 980
1
100
1000
1
9806 . 0
m
Kg
m
cm
g
kG
cm
g
=
|
|
.
|
\
|
|
|
.
|
\
|
( ) ( )
|
.
|
\
|
=
|
.
|
\
|
=
h
kg m
Kg
m
M
A
1
min 60
min
19 . 3
min 15
0.175m 6 . 980 596 . 0 785 . 0
3
2
=191.4
hr
kg
Masa de la solucin concentrada
u
) h ( ) ( Dp 785 . 0
P P
2
A
=
P
M
m cm 271 . 0 1 . 27 h
p
= = A
( )
3 3
3 3
3
P
978
1
100
1000
1
978 . 0 67
m
Kg
m
cm
g
Kg
cm
g
C a =
|
|
.
|
\
|
|
|
.
|
\
|
=
hr
kg
h
kg
m
Kg
M
P
6 . 99
1
min 60
min
66 . 1
min 15
(.271m) ) 978 ( (0.346m) 785 . 0
3
2
=
|
.
|
\
|
= =
Masa del evaporado
( ) ( ) ( )
u
E E E
E
h D
M
A
=
2
785 . 0
m cm h
E
24 . 0 24 = = A
3
978 68
m
Kg
C a
E
=
( ) ( ) ( )
h
Kg
h
Kg
m
m
Kg
M
E
23 . 88
1
min 60
min
47 . 1
min 15
24 . 978 346 . 0 785 . 0
3
2
=
|
.
|
\
|
=
|
.
|
\
|
=
Del balance de metera general.
Mc Mp M Mv M
E A
+ + = + (1)
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Balance de vapor
Mc Mv = (2)
Sustituyendo 2 en 1 y despejando M
A
Mp M M
E A
+ =
Mp M M
A E
+ =
h
Kg
h
Kg
h
Kg
M
E
8 . 91 6 . 99 286 . 191 = =
Balance de calor
McHc MpHp H M MvHv H M
E E A A
+ + = +
McHc v Mv MvHv + =
McHc MvHv v Mv =
A A E E
H M MpHp H M MvHv + + =
A A
t Cp H A =
tp Cp Hp A =
CpEPE t a H H
ev E E
+ =
( )
Kg
Kcal
C
C Kg
Kcal
H
A
64 0 64
1 = =
( )
Kg
Kcal
C
C Kg
Kcal
Hp 68 0 68
1 = =
Kg
Kcal
Kg
Kcal
C a H
E
1 . 626 ) 0 ( 5 . 0 1 . 626 67 = + =
Calor absorbido
A A E E A
H M MpHp H M Q + =
h
Kcal
Kg
Kcal
h
Kg
Kg
Kcal
Kg
Kcal
Kg
Kcal
h
Kg
Q
A
2 . 51999 64 4 . 191 68 6 . 99 1 . 626 8 . 91 =
|
|
.
|
\
|
|
|
.
|
\
|
|
|
.
|
\
|
+
|
|
.
|
\
|
=
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Calor suministrado
V V S
M Q =
kg
kcal
C a
h
kg kg
m
m
Kg
m
M
m
Kg
C a v
h D
M
V
V
V V V
V
6 . 532 110
58 . 98
min
643 . 1
min 15
) 197 . ( ) 4 . 985 ( ) 4026 . 0 ( 785 . 0
4 . 985 54
785 . 0
3
2
3
2
=
= =
|
|
|
|
.
|
\
|
=
=
|
|
.
|
\
| A
=
u
hr
kcal
kg
kcal
h
kg
Q
S
7 . 52503 ) 6 . 532 )( 58 . 98 ( = =
Calor perdido
A S P
Q Q Q =
hr
kcal
hr
kcal
hr
kcal
Q
P
2 . 504 2 . 51999 7 . 52503 = =
Fuerza impulsora a la transferencia de calor.
m
t t t A = A = A
2 1
C t 42 68 110
1
= = A
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Coeficiente global de transferencia de calor.
( )( )( )
55 . 2
9575 . 4 55 . 2 03 . 0
91 . 1287
) 42 )( 9575 . 1 (
2 . 51999
2
2 2
=
= = =
= =
A
=
L
m DLNt A
C hm
kcal
C m
h
Kcal
U
T A
Q
U
tc
tc
A
t t
4
03 . 0 3
=
= =
Nt
cm D
Factor de economia.
utilizado vapor Kg
evaporado de Kg
M
E
V
.
.
= = c
utilizado vapor Kg
evaporado de Kg
h
kg
h
Kg
.
.
93122 . 0
58 . 98
8 . 91
= = c
Capacidad evaporativa.
( )( )( )( )
2
.
2 2
.
9575 . 0 4 55 . 2 03 . 0
.
.
875 . 95
9575 . 0
8 . 91
m nt L D A
m h
evaporado de Kg
m
h
Kg
A
E
C
calor de transf
calor de transf
E
= = =
= = =
t t
Capacidad de transferencia de vapor.
T U
A
Q
C
calor de transf
A
Q
A = =
.
2 2
7 . 54307
9575 . 0
2 . 51999
hm
kcal
m
h
Kcal
C
Q
= =
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Eficiencia trmica.
100 x
Q
Q
t
S
A
= q
Calculo de la velocidad a la entrada de los tubos de la calandria Ve
p flujo
A
A
M
Ve
=
3
978 68
m
Kg
C a =
( ) ( ) ( ) ( )
2
2 2
001413 . 0 2 03 . 0 785 . 0 785 . 0 m nt D A
flejo
= = =
( )
( )
s
m
s
h
h
m
m
Kg
m
h
Kg
A
M
Ve
p flujo
A
03847 . 0
. 3600
1
504 . 138
978 001413 . 0
4 . 191
3
2
=
|
.
|
\
|
=
|
.
|
\
|
= =
Velocidad del solvente evaporado.
flujo
E E
A
VespEaT M
Vs =
Kg
m
C Ea Ve
3
504 . 5 68 =
( )( ) ( )
2 2
001413 . 0 2 03 . 0 785 . 0 m m A
flujo
= =
s
m
s
h
h
m
m
Kg
m
h
Kg
Vs 4664 . 95
. 3600
1
343679
001413 . 0
504 . 5 23 . 88
2
3
=
|
.
|
\
|
=
|
|
.
|
\
|
|
.
|
\
|
=
03 . 99 100
7 . 52503
2 . 51999
= = x
hr
kcal
h
Kcal
t q
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Tiempo de residencia de la solucin dentro de los tubos.
s
m Vs Ve
Vmed 7592 . 47
2
48 . 95 03847 . 0
2
=
+
=
+
=
( )
. 1064 . 0
7592 . 47
54 . 2 2 *
s
s
m
m
Vmed
T L
t
r
= = =
CONDENSADOR.
Calculo suministrado por el solvente
kg
kcal
T evaporado del latente Calor
Donde
kg
kcal
h
Kg
Q
E Q
C Evaporado E
C
E C
5 . 558 @
:
h
kcal
5 . 49276 ) 5 . 558 )( 23 . 88 (
. 66
= =
= =
=
=
Calor transferido al agua.
.
1
h
kcal
84 . 49619 C 24) - (40
Kg
Kcal
1 24 . 3101
) (
2
2
2 2 2
2
Kg
Kcal
Cp
h
Kg
Q
T T Cp M Q
O H
A
O H Entrada Salida O H O H A
O H
O H
=
=
|
|
.
|
\
|
|
.
|
\
|
=
=
h
Kg
h
kg
m
m
Kg
m
M
m
Kg
C a
h D
M
O H
O H O H O H
O H
214 . 3101
1
min 60
min
6869 . 51
min 5 . 0
) 105 . 0 )( 2 . 992 ( ) 56 . 0 ( 785 . 0
2 . 992 40
785 . 0
3
2
3
2
2
2 2 2
2
=
|
.
|
\
|
= =
=
A
=
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Calor perdido.
h
Kcal
Qc Q Qs
A
34 . 343 5 . 49276 84 . 49619 = = =
Eficiencia trmica.
% 3 . 99 100 *
84 . 49619
5 . 49276
= = =
h
Kcal
h
Kcal
Qc
Q
t
A
q
Fuerza impulsora a la transferencia de calor.
2
2 1
t t
t
A + A
= A
36
2
44 28
=
+
= At
Coeficiente global de transferencia de calor.
2
2 2
922 . 1 9613 . 0 2 . 2
387 . 403
) 36 )( 922 . 1 (
84 . 49619
m calandria la de A x A
C hm
kcal
C m
h
Kcal
U
T A
Q
U
tc
tc
A
= = =
= =
A
=
La velocidad de agua de condensacin
tubos nt
m cm D
E A
nt D A
s
m
s
h
h
m
m E
h
Kg
v
A
M
v
flujo
flujo
O H
O H flujo
O H
O H
2
03 . 0 3
3 413 . 1 2 03 . 0 785 . 0
785 . 0
6096 . 0
3600
1
773 . 2194
1000 3 413 . 1
214 . 3101
2
2
2
2
2
2
=
= =
= =
=
=
|
.
|
\
|
=
=
=
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
5.- Tabla de resultados.
Kg/hr Q
A
Kcal/h
Q
S
Kcal/h Qp kcal/h U
Kcal/hm
2C
C
E
(kg/hm
2
) C
Q
(kcal(hm
2
)
M
A
191.4
51999.2 52503.7 504.2 1287.91 0.9312 95.875 54307.7
M
P
99.6
E 88.23
Ve(m/s) Vs(m/s)
99% 0.03847 95.4664
Condensador.
M
H2O
kg/hr
Q
C
Kcal/kg
Q
H20
Kcal/kg Qs Kcal/h t U V
H20
(m/s)
3101.21 49276.5 49619.84 343.34
99%
403.387 0.6096
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
CONCLUCIONES:
Como se puede observar en la secuencia de clculos y en la tabla de datos experimentales este equipo
tiene muy buena eficiencia trmica ya que obtuvimos un valor de 99% con lo cual corroboramos la
informacin de la bibliografa, la cual nos dice que este tipos de evaporadores es muy utilizado para
sustancias orgnicas como son los jugos de frutas o de verduras.
En estos evaporadores la velocidad en los tubos es muy corta lo cual es muy importante ya que solo se
evapora el solvente contenido en los jugos de frutas o verduras y no se afectan las propiedades de este,
en pocas palabras las vitaminas y minerales de los jugos no son afectados.
Como la sustancia es calentada previamente la ebullicin de la solucin se lleva a cabo dentro de los
tubos gracias a que el vapor suministra su calor latente aumentando la temperatura de la solucin
haciendo la ebullicin sea ms rpida. Ya que este tipo de sustancias no puede recircularse para tener
una mayor obtencin de producto es necesario cambiar los parmetros en la capacidad de evaporacin
tales como la temperatura, el vaco o el vapor de calentamiento.
Concluyendo, este tipo de equipos es muy til para el proceso de jugos en los cuales se necesita
concentrar sin cambiar ninguna de sus propiedades ya que para el hombre es muy importante aprovechar
todas las vitaminas y minerales, por lo cual la ebullicin de la solucin se lleva a cabo dentro de los
tubos evitando que exista presin hidrosttica afectando otros parmetros del equipo.
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
PRACTICA 3
EVAPORADOR DE TRIPLE EFECTO DEL TIPO CIRCULACIN NATURAL
El Principio de Efecto Mltiple consta de una reutilizacin de calor latente para evaporaciones
sucesivas y es una de las grandes ayudas para la economa de vapor. Su aplicacin est
limitada, pero merece un estudio detallado porque, aunque es posible utilizarlo, el anlisis de
su trabajo da tales ejemplos perfectos de tcnica de vapor correcta e incorrecta. Una vez que
los fundamentales de la tcnica estn dominados, hay docenas de caminos en los cuales se
pueden aplicar todos estos tipos de direcciones y que dan economas sencillas, amplias y
permanecientes. Cuando el vapor se utiliza para evaporar agua a partir del producto, el calor
original en el vapor se separa en dos.
1) Calor latente de vaporizacin (o condensacin) que existe por la evaporacin del agua a
partir del producto, mientras que se condensa el vapor original.
2) Calor de agua o apreciable que se retiene en la condensacin que se forma cuando el
vapor original se condensa. Las proporciones de estas divisiones dependen de la presin en
la cual el vapor original abandona su calor latente. El calor en la condensacin en cualquier
presin particular es mejor que el calor en condensacin en presin inferior. Sin embargo, si la
presin en la condensacin se reduce, el calor excesivo provoca la generacin de vapor como
Flash o Auto evaporacin. El vapor tal como flash est tan til como cualquier otro vapor en
la misma presin.
DESCRIPCIN
El Evaporador de Efecto Doble consta de una estructura robusta y paneles de construccin
entera de acero instalado con un rea de trabajo para el estudiante interconectndose con el
panel de atrs y con patas ajustables.
El banco de vapor incluye dos buques evaporadores con tubera de nter conexin y vlvulas
para permitir una evaporacin de efecto nico o doble. La lnea de alimentacin de vapor
incluye una vlvula de reduccin de vapor y una vlvula de alivio de seguridad. El vapor
utilizado se mide por una baja refrigeracin de la condensacin e utilizando vasos de
coleccin. Mdulos de medicin de presin de tipo Bourdon se suministran para indicaciones
de presiones y termopares y estn utilizados para medir la temperatura, que puede
seleccionarse individualmente para demostrarse en un termmetro anlogo.
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
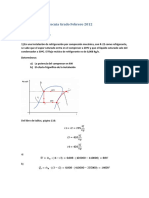
Evaporador de mltiples efectos.
Un esquema de un evaporador de tres efectos se muestra en la figura.
El vapor que se retira del primer efecto est relacionado con el flujo de vapor vivo y economa
del primer efecto as:
Anlogamente, el vapor procedente de la evaporacin en el segundo efecto est relacionado
con el vapor del primer efecto:
Este razonamiento puede extenderse para mltiples efectos:
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
La ecuacin anterior puede usarse para calcular las razones vapor evaporado-vapor vivo Vs el
nmero de efectos para valores dados de E, condiciones de presin y temperatura (Chen y
Hernndez, 1997).
La entalpa DH
i
que gana al hervir el agua en un efecto dado no es exactamente igual al calor
latente de evaporacin. En la alimentacin hacia delante (en paralelo) la solucin que viene de
un efecto anterior estar por encima de su punto de ebullicin por la reduccin de presin.
Tambin cuenta el que el vapor que produce cada efecto est sobrecalentado por el
fenmeno de elevacin de punto de ebullicin (EPE). En un balance de energa estos factores
usualmente se desprecian.
La diferencia de temperatura disponible en un evaporador de mltiple efecto es la diferencia
entre la temperatura del vapor vivo de caldera que ingresa al equipo y la temperatura de los
vapores generados en el ltimo efecto. Los clculos de evaporadores de este tipo se hacen
por tanteo y error; se asume un DT disponible para cada efecto. Haciendo los balances de
materia y energa por efecto se compara la transferencia de calor necesaria para lograr la
velocidad de evaporacin deseada por etapa.
1.- TABLA DE DATOS DE CONDICIONES DE OPERACIN:
Presin manomtrica del vapor (Kg/Cm
2
)
1
2
cm
Kgf
Temperatura de alimentacin (C) 25 C
Vaco en el condensador (mph.) 350 mmHg
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
2.- TABLA DE DATOS EXPERIMENTALES:
Dimetro del
tanque (m)
Temperaturas (C) Tiempo de
operacin
Diferencias de
altura de nivel
(cm)
M
A
(Kg./h)
Solucin diluida
0.596 76 10 11.4
M
p
(Kg./h)
Solucin
concentrada
0.346 90 10 18.1
E
1
(Kg./h)
Solvente
evaporado
0.346
E
1
90
Ec
1
90
10 6.5
E
2
(Kg./h)
Solvente
evaporado
0.346
E
2
82
Ec
2
82
10 4
E
3
(Kg./h)
Solvente
evaporado
0.346
E
3
72
Ec
3
72
10 7.5
M
v
(Kg./h)
Vapor de agua de
caldera
0.402
Mv
108
Mvc
36
10 7.7
M
H2O
(Kg./h)
Agua de
condensacin
0.56
t
entrada
25
t
salida
32
1 16.7
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
3.- SECUENCIA DE CALCULOS.
1. Balance global de materiales de todo el sistema
u
P
2
P
h D 785 . 0 A
=
P
P
M
m cm h 181 . 1 . 18 = = A
3
52 . 976 72
cm
Kg
C a
p
=
( ) ( ) ( )
h
kg
h
kg m
Kg
m
M
P
72 . 99
1
min 60
min
662 . 1
min 10
0.181m 52 . 976 346 . 0 785 . 0
3
2
=
|
.
|
\
|
=
|
.
|
\
|
=
u
) h ( ) ( (0.346) 785 . 0
E E
2
1
A
=
E
M
m cm h 065 . 0 5 . 6 = = A
3
2 . 965 90
m
Kg
C a
E
=
h
Kg
h
kg
m
Kg
M
E
34 . 35
1
min 60
min
589 . 0
10
(0.065m) ) 2 . 965 ( (0.346m) 785 . 0
3
2
1
=
|
.
|
\
|
= =
u
) h ( ) ( (0.346) 785 . 0
E E
2
2
A
=
E
M
m cm h 04 . 0 4 = = A
3
48 . 970 82
m
Kg
C a
E
=
h
Kg
h
kg
m
Kg
M
E
9 . 21
1
min 60
min
365 . 0
min 10
(0.04m) ) 48 . 970 ( (0.346m) 785 . 0
3
2
2
=
|
.
|
\
|
= =
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
u
) h ( ) ( (0.346) 785 . 0
E E
2
3
A
=
E
M
m cm h 75 . 0 5 . 7 = = A
3
52 . 976 72
m
Kg
C a
E
=
h
Kg
h
kg
m
Kg
M
E
316 . 41
1
min 60
min
6886 . 0
min 10
(0.075m) ) 52 . 976 ( (0.346m) 785 . 0
3
2
3
=
|
.
|
\
|
= =
hr
Kg
M
M
E E E M M
A
A
P A
269 . 198
316 . 41 9 . 21 34 . 35 72 . 99
3 2 1
=
+ + + =
= + + + =
2.- BALANCE DE MATERIALES PARA CADA EFECTO
EFECTO 1
hr
Kg
M
hr
Kg
M
hr
Kg
M
M M M
P
E
A
E A P
929 . 162 34 . 35 269 . 198
34 . 35
269 . 198
1
1
1 1
= =
=
=
=
EFECTO 2
hr
Kg
M
hr
Kg
M
hr
Kg
M M
M M M
P
E
A P
E A P
029 . 141 9 . 21 929 . 162
9 . 21
929 . 162
2
2
2 1
2 2 2
= =
=
= =
=
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
EFECTO 3
hr
Kg
M
hr
Kg
M
hr
Kg
M M
M M M
P
E
A P
E P P
713 . 99 316 . 41 029 . 141
316 . 41
029 . 141
3
3
3 2
3 2 3
= =
=
= =
=
3.-BALANCE DE CALOR PARA CADA EFECTO.
EFECTO 1
Calor suministrado:
m cm h 077 . 0 7 . 7 = = A
3
56 . 993 36
m
Kg
C
E
=
h
Kg
h
kg
m
m
Kg
m
M
h D
M
V
V V V
V
26 . 58
1
min 60
min
971 .
min 10
) 077 . ( ) 56 . 993 ( ) 402 . 0 ( 785 . 0
785 . 0
3
2
2
=
|
.
|
\
|
= =
|
|
.
|
\
| A
=
u
Kg
Kcal
C T E
V
9 . 533
108 @
=
=
hr
Kcal
kg
Kcal
hr
Kg
Q
M Q
S
V V S
014 . 31105 9 . 533 ( * ) 26 . 58 (
1
1
= =
=
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Calor absorbido
A A E P P A
H M H E H M Q + =
1 1 1 1 1
( )
( )
Kg
Kcal
Kg
Kcal
CpEPE H H
Kg
Kcal
C
C Kg
Kcal
T Co H
Kg
Kcal
C
C Kg
Kcal
Tp Cp H
C E E
A C A
C P
2 . 635 0 5 . 0 2 . 635
76 0 76
1
90 ) 0 90 (
1
90 @
76 @ 1
90 @ 1
= + = + =
= = A =
= = A =
h
Kcal
Q
h
Kcal
Q Q Q
h
Kcal
Q
Kg
Kcal
h
Kg
Kg
Kcal
h
Kg
Kg
Kcal
h
Kg
Q
NA
A S NA
A
A
879 . 9061
135 . 22043 014 . 31105
135 . 22043
) 76 )( 269 . 198 ( ) 2 . 635 )( 34 . 35 ( ) 90 )( 929 . 162 (
1
1 1 1
1
1
=
= =
=
+ =
EFECTO 2
Calor suministrado
Kg
Kcal
C E
2 . 545
90 @ 1
=
hr
Kcal
kg
Kcal
hr
Kg
Q
M Q
S
E E S
368 . 19267 ) 2 . 545 ( * ) 34 . 35 (
2
1 1 2
= =
=
Calor absorbido
1 1 2 2 2 2 2 P P E P P A
H M H E H M Q + =
Kg
Kcal
H
Kg
Kcal
H
Kg
Kcal
H
C P
C E
C P
90
1 . 632
82
90 @ 1
90 @ 2
82 @ 2
=
=
=
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
h
Kcal
Q
h
Kcal
Q Q Q
h
Kcal
Q
Kg
Kcal
h
Kg
Kg
Kcal
h
Kg
Kg
Kcal
h
Kg
Q
NA
A S NA
A
A
61 . 8523
785 . 10743 368 . 19267
758 . 10743
) 90 )( 929 . 162 ( ) 1 . 632 )( 9 . 21 ( ) 82 )( 024 . 141
2
2 2 2
2
2
=
= =
=
+ =
EFECTO 3
Calor suministrado
Kg
Kcal
C E
1 . 550
82 @ 2
=
hr
Kcal
kg
Kcal
hr
Kg
Q
M Q
S
E E S
19 . 12047 ) 1 . 550 )( 9 . 21 (
3
2 2 3
= =
=
2 2 3 3 3 3 3 P P E P P A
H M H E H M Q + =
Kg
Kcal
H
Kg
Kcal
H
Kg
Kcal
H
C P
C E
C P
82
1 . 628
72
82 @ 2
72 @ 3
72 @ 3
=
=
=
h
Kcal
Q
h
Kcal
Q Q Q
h
Kcal
Q
Kg
Kcal
h
Kg
Kg
Kcal
h
Kg
Kg
Kcal
h
Kg
Q
NA
A S NA
A
A
348 . 9518
538 . 21565 19 . 12047
538 . 21565
) 82 )( 029 . 141 ( ) 1 . 628 )( 316 . 41 ( ) 72 )( 713 . 99 (
3
3 3 3
3
3
=
= =
=
+ =
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Calor total
h
Kcal
Q
Q Q Q Q
hr
Kcal
Q
Q Q Q Q
h
Kcal
Q
Q Q Q Q
TOTAL NA
NA NA NA TOTAL NA
TOTAL S
S S S TOTAL S
TOTAL A
A A A TOTAL A
141 . 8067
348 . 9518 61 . 8523 879 . 9061
572 . 62419
19 . 12047 014 . 31105 368 . 19267
435 . 54352
758 . 10743 538 . 21565 139 . 22043
3 2 1
3 2 1
3 2 1
=
+ = + + =
=
+ + = + + =
=
+ + = + + =
Calculo de la eficiencia trmica
% 87 100
572 . 62419
435 . 54352
100
% 179 100
19 . 12047
538 . 21565
100
% 76 . 55 100
368 . 19267
758 . 10743
100
% 8 . 70 100
014 . 31105
134 . 22043
100
3
3
3
2
2
2
1
1
1
= = =
= = =
= = =
= = =
ST
AT
T
S
A
S
A
S
A
Q
Q
Q
Q
Q
Q
Q
Q
q
q
q
q
Fuerza impulsora
C T
C t t T
C t t T
C t t T
T T T T
T
P E
P E
P VS
T
= A
= = = A
= = = A
= = = A
A + A + A = A
36
10 72 82
8 82 90
18 90 108
3 2 3
2 1 2
1 1
3 2 1
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Clculo de u para cada efecto y total del proceso
( )( )( )( )
tubos tubos de Nmero nt
m cm D
m L
m nt L D A
4
03 . 0 3
54 . 2
9575 . 0 4 54 . 2 03 . 0
2
= =
= =
=
= = = t t
C hm
kcal
C m
h
Kcal
T A
Q
U
C T
A
=
A
=
= A
2 2
1
1
1
1
975 . 1278
) 18 )( 9575 . 0 (
135 . 22043
18
C hm
kcal
C m
h
Kcal
T A
Q
U
C T
A
=
A
=
= A
2 2
2
2
2
2
577 . 1402
) 8 )( 9575 . 0 (
783 . 10743
8
C hm
kcal
C m
h
Kcal
T A
Q
U
C T
A
=
A
=
= A
2 2
3
3
3
3
275 . 2252
) 10 )( 9575 . 0 (
538 . 21565
10
C hm
kcal
U
U
U U U
U
T
T
T
=
+ +
==
+ +
=
2
3 2 1
771 . 515
275 . 2252
1
877 . 1402
1
975 . 1278
1
1
1 1 1
1
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Clculo el factor de economa.
utilizado vapor Kg
evaporado de Kg
M
E
V
.
.
1
1
= = c
utilizado vapor Kg
evaporado de Kg
h
kg
h
Kg
.
.
6066 . 0
26 . 58
34 . 35
1
= = c
utilizado vapor Kg
evaporado de Kg
E
E
.
.
2
1
2
= = c
utilizado vapor Kg
evaporado de Kg
h
kg
h
Kg
.
.
6196 . 0
34 . 35
9 . 21
2
= = c
utilizado vapor Kg
evaporado de Kg
E
E
.
.
3
2
3
= = c
utilizado vapor Kg
evaporado de Kg
h
kg
h
Kg
.
.
886 . 1
9 . 21
316 . 41
3
= = c
utilizado vapor Kg
evaporado de Kg
M
E
T
V
T
.
.
= = c
utilizado vapor Kg
evaporado de Kg
h
kg
h
Kg
T
.
.
6919 . 1
26 . 58
556 . 98
= = c
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Clculo de la capacidad de evaporacin.
2
.
2 2
.
1
1
9575 . 0
.
.
91 . 36
9575 . 0
34 . 35
m nt L D A
m hr
evaporado de Kg
m
h
Kg
A
E
C
calor de transf
calor de transf
E
= =
= = =
t
2 2
.
2
2
.
.
872 . 22
9575 . 0
9 . 21
m hr
evaporado de Kg
m
h
Kg
A
E
C
calor de transf
E
= = =
2 2
.
3
3
.
.
1498 . 43
9575 . 0
316 . 41
m hr
evaporado de Kg
m
h
Kg
A
E
C
calor de transf
E
= = =
2 2
.
.
.
31 . 34
) 9575 . 0 ( * 3
556 . 98
m hr
evaporado de Kg
m
h
Kg
A
E
C
calor de transf
T
ET
= = =
Clculo de la capacidad de transferencia de calor.
T U
A
Q
C
calor de transf
A
Q
A = =
.
1
1
2 2
1
399 . 23004
9575 . 0
712 . 22026
hm
kcal
m
h
Kcal
C
Q
= =
2 2
2
435 . 11230
9575 . 0
142 . 10753
hm
kcal
m
h
Kcal
C
Q
= =
2 2
3
509 . 22536
9575 . 0
708 . 21578
hm
kcal
m
h
Kcal
C
Q
= =
2 2
225 . 18934
) 9575 . 0 ( * 3
562 . 54388
hm
kcal
m
h
Kcal
C
QT
= =
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Clculo de la velocidad de la solucin a la entrada
( )( ) ( )
s
m
seg
h
h
m
m
Kg
m
h
Kg
v
tubos tubos de Nmero nt
m nt D A
m
kg
A
M
v
E
flujo
C
P flujo
A
E
02 . 0
3600
1
156 . 72
) 2 . 965 )( 00283 . 0 (
096 . 197
. 4
00283 . 4 03 . 0 785 . 0 785 . 0
2 . 965
3
2
1
2 2 2
3
90 @
1
=
|
|
.
|
\
|
= =
= =
= = =
=
=
( )( ) ( )
s
m
seg
h
h
m
m
Kg
m
h
Kg
v
tubos tubos de Nmero nt
m nt D A
m
kg
A
M
v
E
flujo
C
P flujo
P
E
01636 . 0
3600
1
913 . 58
) 48 . 970 )( 00283 . 0 (
756 . 161
. 4
00283 . 0 4 03 . 0 785 . 0 785 . 0
48 . 970
3
2
2
2 2 2
3
82 @
2
2
=
|
|
.
|
\
|
= =
= =
= = =
=
=
( )( ) ( )
s
m
seg
h
h
m
m
Kg
m
h
Kg
v
tubos tubos de Nmero nt
m nt D A
m
kg
A
M
v
E
flujo
C
P flujo
P
E
014 . 0
3600
1
607 . 50
) 52 . 976 )( 00283 . 0 (
856 . 139
. 4
00283 . 0 4 03 . 0 785 . 0 785 . 0
52 . 976
3
2
3
2 2 2
3
72 @
3
3
=
|
|
.
|
\
|
= =
= =
= = =
=
=
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Clculo de la velocidad de la solucin a la salida
2 2 2
3
76 .
2
3
1
.
. 1
1
00283 . 0 ) 4 ( ) 03 . 0 )( 785 . 0 ( 785 . 0
361 . 2 @
1898 . 8
3600
1
3 . 29483
00283 . 0
) 361 . 2 )( 34 . 35 (
@
m m nt D A
kg
m
T a edo evaporadol solvente del especifico Volumen T E V
s
m
seg
h
h
m
m
kg
m
h
Kg
v
A
T E V M
v
flujo
C E E esp
S
flujo
E esp E
S
= =
= =
=
|
|
.
|
\
|
= =
=
=
2 2 2
3
82 .
2
3
2
.
. 2
2
00283 . 0 ) 4 ( ) 03 . 0 )( 785 . 0 ( 785 . 0
175 . 3 @
8249 . 6
3600
1
78 . 24569
0028 . 0
) 175 . 3 )( 9 . 21 (
@
m m nt D A
kg
m
T a edo evaporadol solvente del especifico Volumen T E V
s
m
seg
h
h
m
m
kg
m
h
Kg
v
A
T E V M
v
flujo
C E E esp
S
flujo
E esp E
S
= =
= =
=
|
|
.
|
\
|
= =
=
=
2 2 2
3
72 .
2
3
3
.
. 3
3
00283 . 0 ) 4 ( ) 03 . 0 )( 785 . 0 ( 785 . 0
677 . 4 @
8249 . 6
3600
1
894 . 68280
00283 . 0
) 677 . 4 )( 316 . 41 (
@
m m nt D A
kg
m
T a edo evaporadol solvente del especifico Volumen T E V
s
m
seg
h
h
m
m
kg
m
h
Kg
v
A
T E V M
v
flujo
C E E esp
S
flujo
E esp E
S
= =
= =
=
|
|
.
|
\
|
= =
=
=
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Tiempo de residencia
2
1
Vs Ve
V
media
+
=
media
R
V
t l
t
.
=
s
m
s
m
s
m
V
media
1049 . 4
2
189 . 8 02 . 0
1
=
+
=
s
m
s
m
s
m
V
media
42063 . 3
2
8249 . 6 01636 . 0
1
=
+
=
s
m
s
m
s
m
V
media
49 . 9
2
966 . 18 014 . 0
1
=
+
=
seg
seg
m
m
t
R
6187 . 0
1049 . 4
54 . 2
1
= =
seg
seg
m
m
t
R
742 . 0
42063 . 3
54 . 2
2
= =
seg
seg
m
m
t
R
2676 . 0
49 . 9
54 . 2
3
= =
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
CONDENSADOR
Clculo del consumo de agua.
3
25
3
2
2
045 . 997
90 . 2458
01667 . 0
) 167 . 0 )( 045 . 997 ( ) 56 . 0 ( 785 . 0
785 . 0
2
2
2 2 2
2
m
Kg
hr
kg
hr
m
m
Kg
m
M
h D
M
C a O H
O H
O H O H O H
O H
=
= =
A
=
Clculo del calor suministrado al condensador por el solvente evaporado.
h
Kg
E
kg
kcal
T evaporado del latente Calor
kg
kcal
h
Kg
Q
E Q
C Evaporado E
C
E C
29 . 41 evaporado de masa Gasto
1 . 556 @
h
kcal
369 . 22961 ) 1 . 556 )( 29 . 41 (
. 72
3 3
= =
= =
= =
=
=
Clculo del calor aceptado por el agua de condensacin
Kg
Kcal
Cp
hr
kcal
h
Kg
Q
T T Cp M Q
O H
A
O H Entrada Salida O H O H A
O H
O H
1
3 . 17212 C 25) - (32
Kg
Kcal
1 90 . 2458
) (
2
2
2 2 2
2
=
= =
=
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Calor no aprovechado
h
kcal
069 . 5749 3 . 17212 369 . 22961 = =
=
hr
kcal
h
Kcal
Q
Q Q Q
NA
A C NA
Calculo de la eficiencia trmica del condensador
100 =
C
A
Q
Q
q
% 9 . 74 100
369 . 22961
3 . 17212
= = q
Calculo de la fuerza impulsora de la transferencia de calor
C t t t
C t t t
n Sol e VS
n Sol s VS
= = = A
= = = A
40 32 72
47 25 72
' 2
' 1
C t
t t t
T
T
= A
+ = A + A = A
5 . 43
2 ) 40 47 ( 2
2 1
Clculo del coeficiente global de transferencia de calor.
C 43.5 40)/2 r.(47 condensado el en ra temperatu de Diferencia
915 . 1 9575 . 0 2 . 2
62 . 206
) 5 . 43 )( 915 . 1 (
3 . 17212
2
2 2
= + = A
= = =
= =
A
=
T
m calandria la de A x A
C hm
kcal
C m
h
Kcal
U
T A
Q
U
tc
tc
A
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Clculo de la velocidad de circulacin del agua en los tubos del condensador.
( )( ) ( )
tubos nt
m cm D
m A
nt D A
seg
m
m
Kg
m
h
Kg
v
A
M
v
flujo
flujo
O H
O H flujo
O H
O H
2
03 . 0 3
10 * 413 . 1 2 03 . 0 785 . 0
785 . 0
48 . 0
)
.
045 . 997 )( 10 * 413 . 1 (
90 . 2458
2 3 2
2
3
2 3
2
2
2
2
=
= =
= =
=
= =
=
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
TABLA DE RESULTADOS
EVAPORADOR
Ma(Kg/h)
Mp
(Kg/h)
Qa
(Kcal/h)
Qs
(Kcal/h)
QNA
(Kcal/h)
%
T
(C)
EFECTO
1
198.269 162.929 22043.135 31105.014 9061.879 70.8 18
EFECTO
2
169.929 141.029 10743.758 19267.368 8523.61 55.76 8
EFECTO
3
141.029 99.713 21565.538 12047.19 -9518.348 179 10
TOTAL 509.227 403.671 54352.435 62419.572 8067.141 87 36
U
(Kcal/hm2C)
CE
(Kg/hm2)
CQ
(Kcal/hm2)
(s)
EFECTO
1
1278.975 0.6066 36.91 23004.399 0.6187
EFECTO
2
1402.577 0.6196 22.872 11230.435 0.742
EFECTO
3
2252.275 1.886 43.1498 22536.509 0.2676
TOTAL 515.771 1.6919 34.31 18934.225
CONDENSADOR
Qs
(Kcal/h)
QAH2O
(Kcal/h)
QNA
(Kcal/h)
MH2O
(Kg/h)
T
(C)
U
(Kcal/hm2C
)
V
(m/s)
CONDENSADO
R
22961.36 17212.3
5749.06
9
2458.90
74.9
%
43.5 206.62 0.48
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
CONCLUCIONES:
Como se puede observar en los clculos y en las tablas de resultados la eficiencia trmica de este equipo
es la ms baja con respecto a la de los dems equipos, pero esto se compensa ya que este tipo de equipos
es mas econmico, la razn principal es que hay un gran ahorro en la utilizacin de vapor de
calentamiento; este equipo esta instalado en serie por lo cual sabemos que en el primer efecto se
alimenta vapor de calentamiento enviado desde la caldera, el evaporado del primer efecto es enviado al
segundo para ser utilizado como medio de calentamiento, el evaporado del segundo efecto es enviado al
tercer efecto para calentar la solucin concentrada.
Cada condensado de los evaporados es recolectado en tanques individuales para poder realizar los
clculos con mayor facilidad y para poder realizar los balances de materia y energa de cada equipo as
como del condensador. Cabe mencionar que el principio de este equipo es el mismo que el del equipo de
circulacin natural, lo nico que los diferencia es que hay ms calandrias y hay un aprovechamiento de
vapor.
Concluyendo podemos decir que este equipo es muy utilizado en la industria por la cantidad de recursos
financieros que se pueden ahorrar por el aprovechamiento de vapor de cada efecto, aunque exista una
eficiencia trmica menor ms no baja es un equipo eficiente ya que nuestros clculos nos arrojaron un
valor de 87% lo cual nos indica que tiene una buena transferencia de calor.
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
TABLA COMPARATIVA DE TODOS LOS EQUIPOS.
ECF ECN EME
M
A
150 187.83 198.33
M
E
63.3 88.23 98.61
M
P
86.46 99.6 99.72
Q
A
41675.35 49845.87 54503.6
Q
S
45803.6 50602.87 62416.44
t 91 98.5 87.42
U 1038.019 1287.96
U
1
=1280.84, U
2
=1411.99
U
3
=2252.56, U
T
=517.291
T 41.92 42
T
1
=18, T
2
=8, T
3
=10
Ve 0.69 0.038
V
1
= 0.02, V
2
=0.0144, V
3
=0.01
Vs 0.69 95.48
V
1
=8.18, V
2
=6.32, V
3
=18.96
R
3.68 0.1064
1
=0.61,
2
= 0.74,
3
=0.26
Ct 65.84 92.14 34.29
C
Q
43353.11 52055.08 18977.1
0.7664 0.9798 1.69
CON
DEN
SA
DOR
W 2533.8 3101.214 2461.26
E 63.3 88.23 41.32
QA 27871.8 48762.63 1729.15
QS 35948 49731.84 23435.06
t 78 98.05 73.78
U 1317.902 721.37 223.74
Como se observa en esta tabla el equipo mas eficiente es el de circulacin natural ya cuanta con
una eficiencia de 98.5, esta tabla fue construida con los valores de todos los compaeros por lo cual
algunos de ellos no concuerdan con los resultados presentes en los clculos de las practicas de este
trabajo.
En conclusin, no se puede decir que equipo va a ser el mas eficiente en cada proceso ya que cada
equipo esta diseado para trabajar con sustancias diferentes, pero en este caso trabajamos como
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
solucin concentrada con agua se puede decir que el ms eficiente es el evaporador de circulacin
natural.
PRACTICA 4
CRISTALIZACIN
La operacin de cristalizacin es aquella por media de la cual se separa un componente de una solucin
liquida transfirindolo a la fase slida en forma de cristales que precipitan. Es una operacin necesaria
para todo producto qumico que se presenta comercialmente en forma de polvos o cristales, ya sea el
azcar o sacarosa, la sal comn o cloruro de sodio.
En la cadena de operaciones unitarias de los procesos de fabricacin se ubica despus de la evaporacin
y antes de la operacin de secado de los cristales y envasado.
Toda sal o compuesto qumico disuelto en algn solvente en fase liquida puede ser precipitada por
cristalizacin bajo ciertas condiciones de concentracin y temperatura que el ingeniero qumico debe
establecer dependiendo de las caractersticas y propiedades de la solucin, principalmente la solubilidad
o concentracin de saturacin, la viscosidad de la solucin, etc.
Para poder ser transferido a la fase slida, es decir, cristalizar, un soluto cualquiera debe eliminar su
calor latente o entalpa de fusin, por lo que el estado cristalino adems de ser el ms puro, es el de
menor nivel energtico de los tres estados fsicos de la materia, en el que las molculas permanecen
inmviles unas respecto a otras, formando estructuras en el espacio, con la misma geometra, sin
importar la dimensin del cristal.
TIPO DE CRISTALES
Un cristal puede ser definido como un slido compuesto de tomos arreglados en orden, en un modelo
de tipo repetitivo. La distancia interatmica en un cristal de cualquier material defini do es constante y es
una caracterstica del material. Debido a que el patrn o arreglo de los tomos es repetido en todas
direcciones, existen restricciones definidas en el tipo de simetra que el cristal posee.
La forma geomtrica de los cristales es una de las caractersticas de cada sal pura o compuesto qumico,
por lo que la ciencia que estudia los cristales en general, la cristalografa, los ha clasificado en siete
sistemas universales de cristalizacin:
Sistema Cbico
Las sustancias que cristalizan bajo este sistema forman cristales de forma cbica, los cuales se pueden
definir como cuerpos en el espacio que manifiestan tres ejes en ngulo recto, con segmentos, ltices,
aristas de igual magnitud, que forman seis caras o lados del cubo. A es ta familia pertenecen los
cristales de oro, plata, diamante, cloruro de sodio, etc.
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Sistema Tetragonal
Estos cristales forman cuerpos con tres ejes en el espacio en ngulo recto, con dos de sus segmentos de
igual magnitud, hexaedros con cuatro caras iguales, representados por los cristales de oxido de estao.
Sistema Ortorrmbico
Presentan tres ejes en ngulo recto pero ninguno de sus lados o segmentos son iguales, formando
hexaedros con tres pares de caras iguales pero diferentes entre par y par, representados por los cristales
de azufre, nitrato de potasio, sulfato de bario, etc.
Sistema Monoclnico
Presentan tres ejes en el espacio, pero slo dos en ngulo recto, con ningn segmento igual, como es el
caso del brax y de la sacarosa.
Sistema Triclnico
Presentan tres ejes en el espacio, ninguno en ngulo recto, con ningn segmento igual, formando
cristales ahusados como agujas, como es el caso de la cafena.
Sistema Hexagonal
Presentan cuatro ejes en el espacio, tres de los cuales son coplanares en ngulo de 60, formando un
hexgono bencnico y el cuarto en ngulo recto, como son los cristales de zinc, cuarzo, magnesio,
cadmio, etc.
Sistema Rombodrico
Presentan tres ejes de similar ngulo entre si, pero ninguno es recto, y segmentos iguales, como son los
cristales de arsnico, bismuto y carbonato de calcio y mrmol.
IMPORTANCIA DE LA CRISTALIZACIN EN LA INDUSTRIA
En muchos casos, el producto que sale para la venta de una planta, tiene que estar bajo la forma de
cristales. Los cristales se han producido mediante diversos mtodos de cristalizacin que van desde los
ms sencillos que consisten en dejar reposar recipientes que se llenan originalmente con soluciones
calientes y concentradas, hasta procesos continuos rigurosamente controlados y otros con muchos pasos
o etapas diseados para proporcionar un producto que tenga uniformidad en la forma, tamao de la
partcula, contenido de humedad y pureza.
La cristalizacin es importante como proceso industrial por los diferentes materiales que son y pueden
ser comercializados en forma de cristales. Su empleo tan difundido se debe probablemente a la gran
pureza y la forma atractiva del producto qumico slido, que se puede obtener a partir de soluciones
relativamente impuras en un solo paso de procesamiento. En trminos de los requerimientos de energa,
la cristalizacin requiere mucho menos para la separacin que lo que requiere la destilacin y otros
mtodos de purificacin utilizados comnmente. Adems se puede realizar a temperaturas relativamente
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
bajas y a una escala que vara desde unos cuantos gramos hasta miles de toneladas diarias. La
cristalizacin se puede realizar a partir de un vapor, una fusin o una solucin. La mayor parte de las
aplicaciones industriales de la operacin incluyen la cristalizacin a partir de soluciones. Sin embargo, la
solidificacin cristalina de los metales es bsicamente un proceso de cristalizacin y se ha desarrollado
gran cantidad de teora en relacin con la cristalizacin de los metales.
La cristalizacin consiste en la formacin de partculas slidas en el seno de una fase homognea.
Las partculas se pueden formar en una fase gaseosa como en el caso de la nieve, mediante solidificacin
a partir de un lquido como en la congelacin de agua para formar hielo o en la manufactura de
monocristales, o bien por cristalizacin de soluciones lquidas.
Se puede decir que la cristalizacin es un arte, dando a entender que la realidad tcnica es sobrepasada
en ocasiones por todos los factores empricos que estn involucrados en la operacin.
Estos sistemas geomtricos son constantes para los cristales del mismo compuesto qumico,
independientemente de su tamao. Los cristales son la forma ms pura de la materia, si bien sucede que
precipitan simultneamente cristales de varias sustancias formando soluciones slidas de varios colores
como son los minerales como el mrmol veteado, el jade, onix, turquesas, etc., en los cuales cada color
es de cristales de una sal diferente. Sin embargo cuando cristaliza solamente un solo compuesto
qumico, los cristales son 100% puros.
Adems de su forma geomtrica, los cristales son caracterizados por su densidad, su ndice de
refraccin, color y dureza.
MTODOS DE CRISTALIZACIN
Enfriamiento de una disolucin de concentracin baja
Si se prepara una disolucin concentrada a alta temperatura y se enfra, se forma una disolucin
sobresaturada, que es aquella que tiene, momentneamente, ms soluto disuelto que el admisible por la
disolucin a esa temperatura en condiciones de equilibrio. Posteriormente, se puede conseguir que la
disolucin cristalice mediante un enfriamiento controlado. Esencialmente cristaliza el compuesto
principal, y las aguas madre se enriquecen con las impurezas presentes en la mezcla inicial al no
alcanzar su lmite de solubilidad.
Cambio de disolvente
Preparando una disolucin concentrada de una sustancia en un buen disolvente y aadiendo un
disolvente peor que es miscible con el primero, el principal del slido disuelto empieza a precipitar, y las
aguas madres se enriquecen relativamente en las impurezas. Por ejemplo, puede separarse cido
benzoico de una disolucin de ste en acetona agregando agua.
Evaporacin del disolvente
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
De manera anloga, evaporando el disolvente de una disolucin se puede conseguir que empiecen a
cristalizar los slidos que estaban disueltos cuando se alcanzan los lmites de sus solubilidades. Este
mtodo ha sido utilizado durante milenios en la fabricacin de sal a partir de salmuera o agua marina.
Sublimacin
En algunos compuestos la presin de vapor de un slido puede llegar a ser lo bastante elevada como
para evaporar cantidades notables de este compuesto sin alcanzar su punto de fusin (sublimacin). Los
vapores formados condensan en zonas ms fras ofrecidas por ejemplo en forma de un "dedo fro",
pasando habitualmente directamente del estado gaseoso al slido, (sublimacin regresiva) separndose,
de esta manera, de las posibles impurezas. Siguiendo este procedimiento se pueden obtener slidos
puros de sustancias que subliman con facilidad como la cafena, el azufre elemental, el cido saliclico,
el yodo, etc.
Enfriamiento selectivo de un slido fundido
Para purificar un slido cristalino ste puede fundirse. Del lquido obtenido cristaliza, en primer lugar, el
slido puro, enriquecindose, la fase lquida, de las impurezas presentes en el slido original. Por
ejemplo, este es el mtodo que se utiliza en la obtencin de silicio ultrapuro para la fabricacin de
sustratos u obleas en la industria de los semiconductores. Al material slido (silicio sin purificar que se
obtiene previamente en un horno elctrico de induccin) se le da forma cilndrica. Luego se lleva a cabo
una fusin por zonas sobre el cilindro. Se comienza fundiendo una franja o seccin del cilindro por un
extremo y se desplaza dicha zona a lo largo de este hasta llegar al otro extremo. Como las impurezas son
solubles en el fundido se van separando del slido y arrastrndose hacia el otro extremo. Este proceso de
fusin zonal puede hacerse varias veces para asegurarse que el grado de pureza sea el deseado.
Finalmente se corta el extremo en el que se han acumulado las impurezas y se separa del resto. La
ventaja de este proceso es que controlando adecuadamente la temperatura y la velocidad a la que la
franja de fundido se desplaza por la pieza cilndrica, se puede obtener un material que es un monocristal
de silicio que presenta las caras de la red cristalina orientadas en la manera deseada.
Crecimiento cristalino
Para obtener cristales grandes de productos poco solubles se han desarrollado otras tcnicas. Por
ejemplo, se puede hacer difundir dos compuestos de partida en una matriz gelatinosa. As el compuesto
se forma lentamente dando lugar a cristales mayores. Sin embargo, por lo general, cuanto ms lento es el
proceso de cristalizacin tanto mejor suele ser el resultado con respecto a la limpieza de los productos de
partida y tanto mayor suelen ser los cristales formados.
La forma y el tamao de los cristales pueden ser influenciados a aparte por condicionantes como el
disolvente o la concentracin de los compuestos, aadiendo trazas de otros componentes como protenas
(esta es la manera con que los moluscos, las diatomeas, los corales, etc consiguen depositar sus
conchas o esqueletos de calcita o cuarzo en la forma deseada.)
La teora ms aceptada para este fenmeno es que el crecimiento cristalino se realiza formando capas
monomoleculares alrededor de germen de cristalizacin o de un cristalito inicial. Nuevas molculas se
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
adhieren preferentemente en la cara donde su adhesin libera ms energa. Las diferencias energticas
suelen ser pequeas y pueden ser modificadas por la presencia de dichas impurezas o cambiando las
condiciones de cristalizacin.
En multitud de aplicaciones se puede necesitar la obtencin de cristales con una determinada forma y/o
tamao como: la determinacin de la estructura qumica mediante difraccin de rayos X, la
nanotecnologa, la obtencin de pelculas especialmente sensibles constituidas por cristales de sales de
plata planos orientados perpendicularmente a la luz de incidencia, la preparacin de los principios
activos de los frmacos, etc
EQUIPOS DE CRISTALIUZACIN
Cristalizadores de tanque.
La cristalizacin en tanques (un mtodo antiguo que todava se usa en casos especiales) consiste en
enfriar soluciones saturadas en tanques abiertos. Despus de cierto tiempo, se drena el licor madre y se
extraen los cristales. En este mtodo es difcil controlar la nucleacin y el tamao de los cristales.
Adems, los cristales contienen cantidades considerables del licor madre y, por otra parte, los costos de
mano de obra son elevados. En algunos casos, el tanque, se enfra por medio de serpentines o chaquetas
y se usa un agitador para lograr una mejor velocidad de transferencia de calor; sin embargo, puede haber
acumulacin de cristales en las superficies de estos dispositivos. Este tipo de equipo tiene aplicaciones
limitadas y algunas veces se usa para la manufactura de productos qumicos de alto valor y derivados
farmacuticos.
Cristalizadores con raspadores de superficie.
Un tipo de cristalizador con raspadores de superficie consiste en una artesa abierta de 0.6 m de ancho
con fondo semicircular y chaqueta de enfriamiento en el exterior. La rotacin a baja velocidad de un
agitador en espiral mantiene los cristales en suspensin. Las aspas pasan cerca de las paredes y rompen
los depsitos que se forman en la superficie de enfriamiento. Por lo general, el producto tiene una
distribucin de tamaos de cristal bastante amplia.
Evaporador-cristalizador con circulacin de lquido.
La sobresaturacin se produce por evaporacin. El lquido circulante se extrae por la bomba de tomillo
hacia el interior del tubo del calentador por condensacin de vapor de agua. El lquido caliente fluye
despus hacia el espacio del vapor donde se produce una vaporizacin repentina que causa
sobresaturacin. El vapor de salida se condensa, el lquido sobresaturado fluye hacia el tubo de bajada y
despus asciende a travs del lecho de cristales fluidizados y agitados, que de esta manera crecen. El
lquido saturado de salida vuelve al calentador como corriente de recirculacin, donde se une a la
alimentacin de entrada. Los cristales grandes se sedimentan y el producto se extrae como suspensin de
cristales y licor madre. Este modelo se llama tambin cristalizador de Oslo.
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
Cristalizador al vaco con circulacin de magma.
En el cristalizador al vaco con circulacin de magma o suspensin de cristales la circula por fuera del
cuerpo principal del aparato por medio de un tubo de circulacin o bomba en espiral. El magma fluye a
travs de un calentador, donde su temperatura se eleva de 2 a 6 K. Entonces, el licor calentado se
mezcla con la suspensin del cuerpo principal y se produce una ebullicin en la superficie del lquido,
misma que causa sobresaturacin en el lquido arremolinado cerca de la superficie, provocando
depsitos en los cristales suspendidos de esta zona, que salen por la tubera de circulacin, mientras los
vapores salen por la parte superior. El vaco se produce con un eyector de chorro de vapor.
NITRATO DE POTASIO
El compuesto qumico nitrato de potasio salitre o nitrato potsico es un nitrato cuya frmula es KNO
3
.
Actualmente, la mayora del nitrato de potasio viene de los vastos depsitos de nitrato de sodio en los
desiertos Chilenos. El nitrato de sodio es purificado y posteriormente se le hace reaccionar en una
solucin con cloruro de potasio (KCl), en la cual el nitrato de potasio, menos soluble, cristaliza.
Aplicaciones
Una de las aplicaciones ms tiles del nitrato de potasio es la produccin de cido ntrico, aadiendo
cido sulfrico concentrado a una solucin acuosa de nitrato de potasio, resultando cido ntrico y
sulfato de potasio, que son separados mediante destilacin fraccionada.
Tambin se usa como fertilizante, en propelentes de cohetes y en varios artefactos pirotcnicos como
bombas de humo, en las cuales una mezcla con azcar produce una nube de humo de un volumen 600
veces superior al suyo.
En conservacin de alimentos, el nitrato de potasio es un ingrediente poco comn de la carne salada.
Como conservante es conocido como E252.
Tambin es un componente principal en compuestos usados para descomponer con ms rapidez restos
orgnicos, como los tocones de los rboles, porque acelera el proceso de descomposicin.
La creencia popular dice que el nitrato de potasio es un afrodisaco, pero en realidad no tiene esa clase
de efectos en los humanos.
Finalmente, el nitrato de potasio es el agente oxidante(aporte de oxgeno), componente indispensable de
la plvora. Aunque el nitrato de potasio se usa para producir plvora, por s mismo no es combustible ni
inflamable.
Es bastante utilizado tambin para el tratamiento de la hipersensibilidad que afecta a la pulpa dentaria.
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
DESARROLLO EXPERIMENTAL
Vamos a obtener cristales de KNO
3
mediante el enfriamiento de una solucin concentrada
Para el experimento se toman 85 g de KNO
3
en 100 g vamos a la curva de solubilidad y observamos en
el aje de las Y que se tiene a esta temperatura de 50C debemos de pesar 85g KNO
3
/100g H
2
O.
Sabiendo cuanto se va a pesar y a que temperatura se va a llevar a cabo el experimento, se procede a
pesar en una balanza analtica 85 g de KNO
3
,
en un matraz erlenmeyer se pesan 100 g de H
2
O se mezcla
la sal y el agua, tomndose la temperatura y se somete a calentamiento; la siguiente tabla muestra los
tiempos y temperaturas tomados mientras se realizaba el experimento.
Tiempo (min) Temperatura (C)
1 16
5 24
10 40
13 50
14 68
El tiempo es muy variado ya que al estar calentando fuimos aumentando la temperatura para que la
disolucin se llevara a cabo con ms facilidad y mucho mas rpido; en el minuto 13 se alcanzo la
temperatura necesaria para disolver los 85 gm de la sal pero aun no se disolva totalmente.
El minuto 14 la temperatura fue de 68C, en este punto de calentamiento se disolvi todo el soluto, se
suspendi el calentamiento e inmediatamente se comenzaron a formar los cristales, ya que el
procedimiento que utilizamos fue de enfriamiento natural los cristales que se formaron fueron los del
sistema cristalino ortorrmbico.
Estos cristales fueron de mayor tamao comparndolos con los del sistema de enfriamiento forzado ya
que estos cristales eran ms pequeos o ms finos,
Una semana despus de su reposo se tomo una vez ms la temperatura de la solucin la cual nos dio de
24C que era la temperatura ambiente, se decanto la solucin para tener solo los cristales y se elimino el
agua.
INSTITUTO POLITCNICO NACIONAL
ESCUELA SUPERIOR DE INGENIERA QUMICA
E INDUSTRIAS EXTRACTIVAS
OPERACIONES DE SEPARACIN I
REPORTE DE PRCTICAS
De dejo secar por completo para poder pesar y estar seguros de que no hay agua en la sal.
. 27 . 58 gm Wc =
% 5 . 68 100 *
85
27 . 58
= =
mg
gm
q
Conclusiones:
En esta prctica obtuvimos cristales de nitrato de potasio, la cual consisti en observar una curva de
solubilidad y realizar la disolucin, este procedimiento es muy importante para las operaciones de
separacin ya que es el proceso que le sigue a la evaporacin.
Esto se da gracias a la diferencia de solubilidades que tiene nuestra sal a diferentes temperaturas una vez
que es calentada la solucin saturada se comienza a disolver en nuestro solvente que debe de tener
ciertas caractersticas, que son: No debe de reaccionar con la sal y tambin debe de ser voltil para que
se pueda eliminar fcilmente de nuestros cristales.
La eficiencia obtenida es un poco baja ya que al momento de eliminar el solvente no utilizamos papel
filtro y en el agua eliminada aun exista bastante sal disuelta, la cual fue eliminada junto con el agua.
Con el peso obtenido de los cristales observamos en la grafica de solubilidad que le corresponde una
temperatura de 30C ya que obtuvimos 58.27mg de cristales.
Este tipo de procedimientos junto con la evaporacin son de gran importancia ya que dentro de la
industria qumica nos es de gran ayuda para purificar y separar productos, pero no solo en la qumica
nos sirve, tambin es utilizado en la industria alimenticia y muchas otras ms.
Potrebbero piacerti anche
- Problemas resueltos de Hidráulica de CanalesDa EverandProblemas resueltos de Hidráulica de CanalesValutazione: 4.5 su 5 stelle4.5/5 (7)
- Práctica 2 DesorciónDocumento11 paginePráctica 2 DesorciónMiguel Angel Garcia100% (4)
- Tratamiento de Aguas Residuales Curtiembres - ADocumento41 pagineTratamiento de Aguas Residuales Curtiembres - ADiegoEcheverríaMontesdeoca100% (8)
- Eficiencia energética en las instalaciones de calefacción y acs en los edificios. ENAC0108Da EverandEficiencia energética en las instalaciones de calefacción y acs en los edificios. ENAC0108Nessuna valutazione finora
- Destilacion DiferencialDocumento10 pagineDestilacion DiferencialEdgar RamírezNessuna valutazione finora
- Reporte Practica 3 Arrastre Con VaporDocumento12 pagineReporte Practica 3 Arrastre Con VaporLuis Daniel Gil PachecoNessuna valutazione finora
- BIOSEPARACIONES PRACTICA 7-Saldaña Alejos IbrahimDocumento11 pagineBIOSEPARACIONES PRACTICA 7-Saldaña Alejos Ibrahimibrahim saldañaNessuna valutazione finora
- PRACTICA - 3 - Evaporador de Simple Efecto de Circulación Natural Del Tipo de Película Ascendente-DescendenteDocumento35 paginePRACTICA - 3 - Evaporador de Simple Efecto de Circulación Natural Del Tipo de Película Ascendente-DescendenteCarlos JimenezNessuna valutazione finora
- Evaporadores Circulacion ForzadaDocumento14 pagineEvaporadores Circulacion ForzadaAngel Chavira100% (1)
- 00058382Documento7 pagine00058382Chaca Ibarra SánchezNessuna valutazione finora
- Destilación Reflujo TotalDocumento14 pagineDestilación Reflujo TotalBrian Guzman RamirezNessuna valutazione finora
- Resumen Ackoff-Russell-L-El-Arte-de-Resolver-Problemas PDFDocumento6 pagineResumen Ackoff-Russell-L-El-Arte-de-Resolver-Problemas PDFRicardo Rivas González0% (2)
- Informe Torre Empaque Azar Lem5Documento35 pagineInforme Torre Empaque Azar Lem5anaivonne1912agNessuna valutazione finora
- Informe Organica II Sintesis de CiclohexenoDocumento14 pagineInforme Organica II Sintesis de CiclohexenoOlivia López CarrielNessuna valutazione finora
- Torre de EnfriamientoDocumento16 pagineTorre de EnfriamientoGerardo F. MartinezNessuna valutazione finora
- Fase3 Grupo 80Documento11 pagineFase3 Grupo 80Andrea Avila0% (1)
- SUSAN RAMIREZ Las Haciendas Azucareras Del Valle de Lambayeque1670-1800pdf PDFDocumento24 pagineSUSAN RAMIREZ Las Haciendas Azucareras Del Valle de Lambayeque1670-1800pdf PDFGuillermo GonzalesNessuna valutazione finora
- Practica 1 Evapordor Simple Efecto Circulacion NaturalDocumento13 paginePractica 1 Evapordor Simple Efecto Circulacion Naturalnapoimperio23Nessuna valutazione finora
- Práctica 2 IpsDocumento14 paginePráctica 2 IpsJose Manuel Millan RamirezNessuna valutazione finora
- Practica EvaporacionDocumento7 paginePractica EvaporacionCristopher VazquezNessuna valutazione finora
- Practica 6 - Proceso PolitropicoDocumento13 paginePractica 6 - Proceso PolitropicoVanessa EstradaNessuna valutazione finora
- Practicas EvaporadoresDocumento57 paginePracticas EvaporadoreseclipseazulNessuna valutazione finora
- Eje 3 Procesos Industriales 3Documento20 pagineEje 3 Procesos Industriales 3Jairo Alberto Gómez llanesNessuna valutazione finora
- Practica N°1 ProcesosDocumento15 paginePractica N°1 ProcesosNormitaValdezNessuna valutazione finora
- Práctica 1.Documento12 paginePráctica 1.Yarely EspinozaNessuna valutazione finora
- Tarea 7 Termodinámica Capitulo 5 Libro Raúl Monsalvo VázquezDocumento19 pagineTarea 7 Termodinámica Capitulo 5 Libro Raúl Monsalvo VázquezMercury's VlogsNessuna valutazione finora
- Practica 7 - Maquina FrigorificaDocumento8 paginePractica 7 - Maquina FrigorificaVanessa EstradaNessuna valutazione finora
- Informe III Calor 2Documento13 pagineInforme III Calor 2Andres Josadac Ortiz RodriguezNessuna valutazione finora
- Trabajo Práctico de Resolución de ProblemasDocumento24 pagineTrabajo Práctico de Resolución de ProblemasJoao MurilloNessuna valutazione finora
- Practica 3 ForzadoDocumento18 paginePractica 3 ForzadoHeidy QuintanaNessuna valutazione finora
- Act IntegradoraDocumento14 pagineAct IntegradoraRefugio Rodriguez Miguel AngelNessuna valutazione finora
- Informe de EvaporacionDocumento16 pagineInforme de EvaporacionFlor MatiasNessuna valutazione finora
- Practica 1 Evaporadores Circulacion NaturalDocumento9 paginePractica 1 Evaporadores Circulacion NaturalGabo MedinaNessuna valutazione finora
- Ap 14Documento6 pagineAp 14Kirigaya KazutoNessuna valutazione finora
- Practica Ips Simple EfectoDocumento14 paginePractica Ips Simple EfectoJavier BarraganNessuna valutazione finora
- Integrador 3 - Aucapiña - TuapanteDocumento7 pagineIntegrador 3 - Aucapiña - TuapanteBryan Sebastian AlvarezNessuna valutazione finora
- Informe de Laboratorio 2 Mec. Fluidos PDFDocumento14 pagineInforme de Laboratorio 2 Mec. Fluidos PDFHarold BarcasnegrasNessuna valutazione finora
- Guía Laboratorio N°4 - Evaporadores - IQA-222 - 2020-2Documento9 pagineGuía Laboratorio N°4 - Evaporadores - IQA-222 - 2020-2juan pinto holiNessuna valutazione finora
- Triple EfectoDocumento15 pagineTriple EfectoDiego ValenciaNessuna valutazione finora
- P2 - Reflujo TotalDocumento33 pagineP2 - Reflujo TotalJesus MendezNessuna valutazione finora
- Termodinamica Trabajo Colaborativo 1Documento6 pagineTermodinamica Trabajo Colaborativo 1Oscar Julian VillanuevaNessuna valutazione finora
- 1IM-131 (B) - Lab2 - JA HG AI NPDocumento8 pagine1IM-131 (B) - Lab2 - JA HG AI NPJosimar AvilaNessuna valutazione finora
- Practica #5Documento5 paginePractica #5Miguel Angel Sejas VillarroelNessuna valutazione finora
- ZamoranoDocumento17 pagineZamoranoulisesNessuna valutazione finora
- Sistema de Reactores CSTR en Serie (Final)Documento15 pagineSistema de Reactores CSTR en Serie (Final)andreapc_026146100% (1)
- Reporte 5 Lem 3 Flujo CruzadoDocumento13 pagineReporte 5 Lem 3 Flujo CruzadoAdanJimenez100% (1)
- Laboratorio de Reactor Batch RX IIDocumento18 pagineLaboratorio de Reactor Batch RX IIEileen CornelioNessuna valutazione finora
- Práctica 1 - Difusion MolecularDocumento16 paginePráctica 1 - Difusion MolecularJemmy Villalobos100% (1)
- Camisa Serpentín Transferencia de CalorcDocumento16 pagineCamisa Serpentín Transferencia de CalorcEnrique Porron100% (1)
- TERMODINÁMICA Sistemas AbiertosDocumento4 pagineTERMODINÁMICA Sistemas AbiertosNisolaksNessuna valutazione finora
- Transferencia de Calor. Ejercicios de Aplicación. MartínezDocumento13 pagineTransferencia de Calor. Ejercicios de Aplicación. Martínezluisulloaim0% (1)
- Tarea Del Primer Departamental de Operaciones de Separacion 2Documento18 pagineTarea Del Primer Departamental de Operaciones de Separacion 2csantiago_259422Nessuna valutazione finora
- Laboratorio de ReaccionesDocumento33 pagineLaboratorio de ReaccionesMARLONNessuna valutazione finora
- Practica 4 - Elemento Final de Control - Reyes NicanorDocumento10 paginePractica 4 - Elemento Final de Control - Reyes NicanorNicole Reyes NicanorNessuna valutazione finora
- Bombas Centrifugas PracticasDocumento9 pagineBombas Centrifugas Practicascoolkid23Nessuna valutazione finora
- Laboratorio 5 Ecuación Integral de Conservación de Masa y de Momentum LinealDocumento11 pagineLaboratorio 5 Ecuación Integral de Conservación de Masa y de Momentum LinealDarwing Salvador Chuquizuta AguilarNessuna valutazione finora
- Práctica 24. Intercambiador de Tubos ConcéntricosDocumento12 paginePráctica 24. Intercambiador de Tubos ConcéntricosIris JoyceNessuna valutazione finora
- Laboratorio de Quimica GeneralDocumento8 pagineLaboratorio de Quimica GeneralGiovani Periche PachecoNessuna valutazione finora
- 2012feb 1semanaDocumento8 pagine2012feb 1semanaLeyda AtenciaNessuna valutazione finora
- Extraccion Liquido Liquido FinDocumento15 pagineExtraccion Liquido Liquido FinLuis Henry Camacho Romero100% (1)
- Entropia y Eficiencia Maquina StirlingDocumento5 pagineEntropia y Eficiencia Maquina Stirlinggualberto_pillco100% (1)
- Leyes de FaradayDocumento16 pagineLeyes de FaradayRicardo Rivas GonzálezNessuna valutazione finora
- Calculos Calentador SolarDocumento8 pagineCalculos Calentador SolarsalgoraNessuna valutazione finora
- MonocromadorDocumento3 pagineMonocromadorRicardo Rivas GonzálezNessuna valutazione finora
- Manual Ing - BravoDocumento49 pagineManual Ing - BravoRicardo Rivas GonzálezNessuna valutazione finora
- Conduccion de Calor en Regimen TransitorioDocumento13 pagineConduccion de Calor en Regimen Transitorioerrevilo67% (3)
- Mapa UnderworldDocumento1 paginaMapa UnderworldRicardo Rivas González100% (1)
- Desarrollo de Hojas de Cálculo Excel Con Macros para La Resolución de Problemas de DestilaciónDocumento48 pagineDesarrollo de Hojas de Cálculo Excel Con Macros para La Resolución de Problemas de DestilaciónRicardo Rivas GonzálezNessuna valutazione finora
- 7 Ecosistema de AmericaDocumento6 pagine7 Ecosistema de AmericaSergle Sánchezz LópezzNessuna valutazione finora
- Química - 1 - TareaDocumento3 pagineQuímica - 1 - Tareaalfredo zavaletaNessuna valutazione finora
- Acta de Supervision 02Documento2 pagineActa de Supervision 02SERVICIOS PUBLICOSNessuna valutazione finora
- Manual de Buenas Practicas de Manufactura en RestaurantesDocumento18 pagineManual de Buenas Practicas de Manufactura en RestaurantesEliana Arcos ParqueNessuna valutazione finora
- Galileo Controloladpr PDFDocumento8 pagineGalileo Controloladpr PDFGernando Perez CaluoNessuna valutazione finora
- Fernández, A. (2014) .Documento192 pagineFernández, A. (2014) .mdb1805Nessuna valutazione finora
- Taller Reconocer Las Características y Componentes de La Evaluación de Impactos AmbientalesDocumento3 pagineTaller Reconocer Las Características y Componentes de La Evaluación de Impactos AmbientalesVictor Alejandro MontoyaNessuna valutazione finora
- GlicolDocumento59 pagineGlicolLuis Aban100% (4)
- Hidroneumatico Tanque 60LTS Elbi BonnettDocumento2 pagineHidroneumatico Tanque 60LTS Elbi Bonnettchristian carranzaNessuna valutazione finora
- Tesis Tavizon Alvarado Eva PatriciaDocumento67 pagineTesis Tavizon Alvarado Eva PatriciacjpardomaNessuna valutazione finora
- Ciencia y Comunidad en La Conservación de Los Humedales Tomo I 2aDocumento126 pagineCiencia y Comunidad en La Conservación de Los Humedales Tomo I 2aFlor AylenNessuna valutazione finora
- Hoja de Datos de SeguridadDocumento13 pagineHoja de Datos de SeguridadIvi HoylosNessuna valutazione finora
- Todos Sobre Las RocasDocumento20 pagineTodos Sobre Las RocasLuis SunceriNessuna valutazione finora
- Marco TeoricoDocumento10 pagineMarco TeoricoMarcos Smart GadgetsNessuna valutazione finora
- Resinas Compuestas, Generalidades y PropiedadesDocumento4 pagineResinas Compuestas, Generalidades y PropiedadesMauricio GómezNessuna valutazione finora
- NMX B 030 1984Documento19 pagineNMX B 030 1984Maximino SánchezNessuna valutazione finora
- Perfil de Saneamiento Intergral de HuacrapuquioDocumento153 paginePerfil de Saneamiento Intergral de HuacrapuquioRoyer Jorge Orellana Porras100% (1)
- Ejecucion Del MantenimientoDocumento5 pagineEjecucion Del MantenimientoDiego Alejandro Cobos Caballero100% (1)
- Principales Presas Del Peru y El MundoDocumento11 paginePrincipales Presas Del Peru y El MundoJarol Carrion SalvatierraNessuna valutazione finora
- Bocatomas Dep - Ancash - Sanchez Sandoval - Mendoza MedinaDocumento16 pagineBocatomas Dep - Ancash - Sanchez Sandoval - Mendoza MedinaHebert Sanchez SandovalNessuna valutazione finora
- Laboratorio 6 Consolidaci-UnidemnsionalDocumento23 pagineLaboratorio 6 Consolidaci-UnidemnsionalCristian David Mora BermudezNessuna valutazione finora
- IMPAC7000 FibratadoDocumento2 pagineIMPAC7000 FibratadoAMMON MIBSAM MORA JIMENEZNessuna valutazione finora
- Diamante de SeguridadDocumento11 pagineDiamante de SeguridadDanNessuna valutazione finora
- 1.4 Tipos de CuencasDocumento4 pagine1.4 Tipos de CuencasWilliam PadillaNessuna valutazione finora
- POLIPROPILENODocumento36 paginePOLIPROPILENOAlex Levano VelasquezNessuna valutazione finora
- Inv E-127 Determinación de Los Factores de Contracción de Los SuelosDocumento25 pagineInv E-127 Determinación de Los Factores de Contracción de Los SuelosDiego VargasNessuna valutazione finora
- Quimiica InformeDocumento13 pagineQuimiica InformeIsaac OrtegaNessuna valutazione finora
- 1..1. Metodos de ExtraccionDocumento2 pagine1..1. Metodos de ExtraccionCarmen Rosa FloresNessuna valutazione finora