Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Inserto Anti-Hbs 60453002s
Caricato da
hgbioTitolo originale
Copyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Inserto Anti-Hbs 60453002s
Caricato da
hgbioCopyright:
Formati disponibili
S
Anti-HBs
La Bandeja de Desarrollo tiene 6 filas (A-F) de 12 pocillos. Cada fila contiene una solucin reactiva lista para ser usada en cada etapa del ensayo. La prueba es realizada en etapas, pasando el Peine de una fila a otra, con un perodo de incubacin en cada etapa. Para comenzar la prueba, las muestras de suero o plasma son agregadas al diluyente en los pocillos de la fila A de la Bandeja de Desarrollo. Luego se inserta el Peine en los pocillos de la fila A. Los anticuerpos anti-HBs, en caso de estar presentes en las muestras, se unirn con el HBsAg en los puntos inferiores del diente del Peine (Figura 1). Los componentes no unidos son lavados en la fila B. En la fila C, los anticuerpos anti-HBs capturados en los puntos inferiores del diente reaccionarn con el HBsAg biotinilado. En la fila D el complejo antgeno biotinilado/anticuerpo en los puntos inferiores del diente, y la albmina de suero bovino biotinilada de los puntos superiores (Control Interno) reaccionarn con estreptavidina conjugada con fosfatasa alcalina (FA). En la fila E, los componentes no ligados son eliminados mediante un lavado. En la fila F, la fosfatasa alcalina unida reaccionar con un sustrato cromognico. Los resultados pueden verse como puntos azul grisceos en la superficie del diente del Peine.
Formacin del complejo HBsAg-anticuerpo; 120 min/37C
anti-HBs
Cdigo: 60453002
Formato: 3 x 12 pruebas
B B
Para diagnstico in vitro nicamente
Unin del HBsAg biotinilado; 30 min/37C
Uso Previsto
HBsAg biotinilado
FA B SA B SA FA
El kit ImmunoComb II Anti-HBs es una prueba semicuantitativa rpida para la deteccin de anticuerpos contra el antgeno de superficie de la Hepatitis B en suero o plasma humano.
Unin de la estreptavidina-FA; 20 min/37C
Introduccin
El vrus de la hepatitis B (HBV) pertenece a una nueva familia de vrus de ADN llamados Hepadnaviridae. Se caracteriza por un marcado hepatotropismo y un singular medio de replicacin a travs de un mecanismo de transcripcin inversa. El virin completo, o partcula Dane, consiste de una molcula de ADN circular protegida por un antgeno nucleocspide/nuclear (HBcAg) y rodeada por un envoltorio de lipoprotena conocido como antgeno de superficie (HBsAg). El HBsAg tambin se encuentra en la sangre en forma de partculas incompletas esfricas o filamentosas no infecciosas. Un componente menor del nucleocspide HBV, el antgeno HBe (HBeAg), tambin puede detectarse en la sangre durante la fase replicativa del virus. El vrus de la hepatitis B es un vrus ubicuo de distribucin global. Las principales rutas de trasmisin viral son horizontales, a travs de la contaminacin sexual y parenteral, y vertical, a travs de la trasmisin prenatal de la madre infectada al feto. Las consecuencias clnicas de la infeccin de HBV varan entre las totalmente inaparentes (70% de los casos) a la hepatitis ictrica aguda. La mayora de los pacientes se recuperan completamente seis meses despus del comienzo de la enfermedad. Una pequea proporcin de la poblacin infectada (<1.5%) puede desarrollar hepatitis fulminante, a menudo con consecuencias fatales. En una proporcin sustancial (hasta 10%) de los pacientes adultos, el HBV puede persistir, progresando eventualmente hasta la hepatitis crnica con desarrollo final de cirrosis y hpatocarcinoma. Los portadores crnicos de hepatitis B (200 millones en todo el mundo) constituyen la principal reserva del virus y contribuyen a la diseminacin de la enfermedad. Los anticuerpos contra HBsAg (anti-HBs) son los principales anticuerpos neutralizadores de HBV, que usualmente persisten durante toda la vida y protegen contra la reinfeccin. El nivel de anti-HBs, por lo tanto, sirve como un indicador para evaluar la recuperacin de la infeccin de HBV, o el xito de la vacunacin utilizando partculas de HBsAg. Concentraciones de anticuerpos de 10 IU/L indican inmunidad al HBV.
B SA
estreptavidina (SA) - FA
FA
Reaccin enzimtica de color; 10 min/37C
sustrato cromognico
Figura 1. Principio de la Prueba
El kit incluye un Control Positivo (anti-HBs) y un Control Negativo, que deben incluirse cada vez que se realiza la prueba. Al trmino de sta, el diente utilizado con el Control Positivo debe mostrar dos puntos de color azul grisceo. El diente usado con el Control Negativo debe mostrar el punto superior y un punto inferior muy tnue o la ausencia del mismo. El punto superior tambin deber aparecer en todos los dems dientes para confirmar que el kit funciona apropiadamente y que la prueba fue realizada correctamente.
Contenido del Kit
Peines
El kit contiene 3 Peines de plstico. Cada Peine tiene 12 dientes, uno para cada prueba (Figura 2). Cada diente es sensibilizado en dos areas reactivas: punto superior albmina de suero bovino biotinilada (Control Interno) punto inferior HBsAg recombinante
ImmunoComb II
53 53 53 53 53 53 53 53 53 53 53 53
Control Interno HBsAg recombinante
Figura 2. Peine
Los Peines son suministrados en empaques de aluminio que contienen una bolsa desecante.
Principio de la Prueba
La prueba ImmunoComb II Anti-HBs es un inmunoensayo enzimtico de fase slida (EIA), basado en un principio de reconocimiento doble. La fase slida es un Peine con 12 proyecciones ("dientes"). Cada diente est sensibilizado en dos reas reactivas: punto superior albmina de suero bovino biotinilada (Control Interno) punto inferior HBsAg recombinante
Bandejas de Desarrollo
El kit contiene 3 Bandejas de Desarrollo, cubiertas con papel de aluminio. Cada Bandeja de Desarrollo (Figura 3) contiene todos los reactivos necesarios para la prueba. La Bandeja de Desarrollo consiste de 6 filas (A-F) de 12 pocillos cada una.
60453002/S12/OR
Los contenidos de cada fila son los siguientes: Fila A diluyente de la muestra Fila B solucin de lavado Fila C HBsAg biotinilado Fila D estreptavidina conjugada con fosfatasa alcalina Fila E solucin de lavado Fila F solucin de sustrato cromognico que contiene 5-bromo4-cloro-3-indolil fosfato (BCIP) y nitro azul tetrazolio (NBT)
Figura 3. Bandeja de Desarrollo
Control Positivo 1 frasco (tapa roja) de 1,5 mL, de plasma humano inactivado con calor, diludo a un nivel crtico de 10 IU/mL para anti-HBs. Control Negativo 1 frasco (tapa verde) de 1,5 mL de plasma humano diludo, inactivado con calor y negativo a anti-HBs. Perforador para perforar el papel de aluminio que cubre los pocillos de la Bandeja de Desarrollo. CombScale para leer los resultados de la prueba.
Preparacion de la Bandeja de Desarrollo 1. Incube la Bandeja de Desarrollo en una incubadora a 37C por 45 minutos. 2. Cubra la mesa de trabajo con papel absorbente, a ser desechado como desecho biocontaminante al concluir la prueba. 3. Mezcle los reactivos sacudiendo la Bandeja de Desarrollo. Nota: No retire la cubierta de aluminio de la Bandeja de Desarrollo; rmpala usando la punta desechable de la pipeta o el perforador, slo cuando las instrucciones de la prueba as lo indiquen. Preparacin del Peine Precaucin: para asegurar el funcionamiento apropiado de la prueba, no toque los dientes del Peine. 1. Abra el empaque de aluminio por el borde perforado. Retire el Peine. 2. Es posible utilizar todo el Peine y la Bandeja de Desarrollo o solamente una parte. Para utilizar parte del Peine: a. Determine cuantos dientes va a necesitar para analizar las muestras y los controles. Se necesita un diente para cada prueba. Cada diente tiene impreso el nmero de cdigo del kit, "53", para permitir la identificacin de los dientes sueltos. b. Doble y rompa verticalmente el Peine, o crtelo con tijeras (ver Figura 4) para separar el nmero requerido para las pruebas (Nro. de pruebas mas 2 controles). c. Vuelva a meter la porcin no utilizada del Peine en el empaque de aluminio (con la bolsa desecante). Cierre bien el envoltorio (con un clip, por ejemplo) a fin de mantenerlo seco. Almacene el Peine en la caja original del kit a temperaturas de 2 a 8C para su uso posterior.
ImmunoComb II
53 53 53 53 53 53 53 53 53 53 53 53
Seguridad y Precauciones
Todos los materiales de origen humano usados en la preparacin del kit pasaron pruebas que demostraron que no son reactivos a HBsAg, as como a anticuerpos de HIV o el virus de la hepatitis C. Ya que ningn mtodo de prueba puede garantizar por completo la ausencia de contaminacin viral, todas las soluciones de referencia y todas las muestras humanas deben ser manejadas como si fueran potencialmente infecciosas. Use guantes quirrgicos y ropas de laboratorio. Siga los procedimientos de laboratorio aceptados para el trabajo con suero o plasma humano. No use la pipeta aspirando con la boca. Deseche todas las muestras, Peines* usados, Bandejas de Desarrollo y otros materiales usados con el kit como desechos biocontaminantes. No mezcle reactivos de lotes diferentes. No use este kit luego de la fecha de caducidad. El kit es enviado a 2-8 C. Durante el transporte el kit puede ser conservado a menos de 30 C durante cortos perodos de tiempo que no excedan de 48 horas. Los controles internos indican que el kit no ha sido daado durante el transporte. Conservar el kit en su caja original a 2-8 C. No congelar el kit. Despus de abrir el kit inicialmente, los componentes deben ser conservados a 2-8 C. El funcionamiento del kit despus de su apertura inicial, es estable hasta la fecha de caducidad del mismo si se conserva a 2-8 C. Despus del uso inicial, el peine y la bandeja de reactivos no pueden ser utilizados ms de tres veces.
Figura 4. Fraccionamiento del Peine
Nota: Realice las incubaciones a 37C. Las etapas de lavado deben llevarse a cabo a temperatura ambiente (2226C). Reaccin Antgeno-Anticuerpo (Fila A de la Bandeja de Desarrollo) 1. Pipetee 100 l de muestra. Perfore la cubierta de papel aluminio en un pocillo de la fila A de la Bandeja de Desarrollo con la punta de la pipeta o el perforador y vierta la muestra en el fondo del pocillo. Mezcle vaciando y rellenando repetidamente la solucin con la pipeta. Deseche la punta de la pipeta. 2. Repita el paso 1 para las dems muestras. Use un nuevo pocillo en la fila A y cambie la punta de la pipeta para cada muestra o control. 3. a. Inserte el Peine (con el lado impreso hacia Ud.) en los pocillos de la Fila A conteniendo las muestras y controles. Mezcle: retire e inserte el Peine en los pocillos varias veces. b. Deje el Peine en la Fila A e incube por 120 minutos a 37C. Programe el cronmetro. Hacia el final de los 120 minutos, perfore el papel de aluminio de la Fila B usando el perforador. No abra ms pocillos de los necesarios. c. Al cumplirse los 120 minutos, saque el Peinte de la Fila A. Absorba el lquido adherido a las puntas de los dientes apoyndolos sobre un papel absorbente limpio. No toque la superficie frontal del diente. Primer Lavado (Fila B) 4. Inserte el Peine en los pocillos de la fila B. Agite: inserte y retire vigorosamente el Peine en los pocillos por al menos 10 segundos para que quede bien lavado. Repita el lavado varias veces agitando en el trascurso de 2 minutos; mientras tanto, perfore el papel aluminio de la fila C. Despus de 2 minutos, retire el Peine y absorba el lquido adherido como en el paso 3c. Unin del HBsAg Biotinilado (Fila C) 5. Inserte el Peine en los pocillos de la fila C. Mezcle igual que en el paso 3a. Incube la Bandeja de Desarrollo con el Peine por 30 minutos (use el cronmetro) a 37C. Perfore el papel aluminio de la fila D. Despus de 30 minutos, retire el Peine y absorba el lquido adherido. Unin de la Estreptavidina /Fosfatasa alcalina (Fila D) 6. Inserte el Peine en los pocillos de la fila D. Mezcle. Incube la Bandeja de Desarrollo con el Peine por 20 minutos (use el cronmetro) a 37C. Perfore el papel aluminio de la fila E. Despus de 20 minutos, retire el Peine y absorba el lquido adherido.
Instrucciones de la Prueba
Conservacin y estabilidad del kit
Manejo de las Muestras
Es posible usar suero o plasma en la prueba. Las muestras pueden ser almacenadas por 7 das a temperaturas de 2 a 8C antes de la prueba. Para almacenar las muestras por ms de 7 das, conglelas a -20C o a temperaturas ms bajas. Despus de descongelar las muestras de suero, centrifguelas. Use el sobrenadante para la prueba. Evite congelar y descongelar repetidamente. Los anticoagulantes como heparina, EDTA y citrato sdico no han mostrado tener efecto sobre los resultados del test.
Procedimiento de la Prueba
Equipo Necesario
Pipetas de precisin ajustables con puntas desechables con capacidad de 100 l. Tijeras Cronmetro de laboratorio o reloj.
Preparacin para la Prueba
Ponga todos los reactivos y las muestras a temperatura ambiente y realice la prueba a temperatura 37C.
* A menos que sea archivado para consulta posterior
60453002/S12/OR
Segundo Lavado (Fila E) 7. Inserte el Peine en los pocillos de la fila E. Agite repetidamente durante 2 minutos, como en el paso 4. Mientras tanto, perfore el papel aluminio de la fila F. Despus de 2 minutos, retire el Peine y absorba el lquido adherido. Reaccin de Color (Fila F) 8. Inserte el Peine en los pocillos de la fila F. Mezcle. Incube la Bandeja de Desarrollo con el Peine por exactamente 10 minutos (use el cronmetro) a 37C. Despus de 10 minutos, retire el Peine. Detencin de la Reaccin (Fila E) 9. Inserte de nuevo el Peine en la fila E. Despus de un minuto, retire el Peine y djelo secar al aire.
Orgenics CombScale
ANTI-HBs IU/L 5 10 C+ 25 50 100
Almacenamiento de Partes No Usadas del Kit
Bandeja de Desarrollo Si no us todos los pocillos de la Bandeja de Desarrollo, puede almacenarla para ser usada posteriormente: Selle los pocillos usados con cinta adhesiva ancha a fin de que nada se derrame fuera de los pocillos, incluso en caso de que la Bandeja de Desarrollo sea volcada. Otros Materiales del Kit Vuelva a colocar la(s) Bandejas(s) de Desarrollo, Peine(s), perforador, controles e instrucciones en la caja original del kit y almacene a temperaturas de 2C a 8C.
Figura 7. CombScale
Documentacin de los Resultados Debido a que el color que aparece en los Peines es estable, es posible archivar los Peines para consulta posterior.
Limitaciones
Como ocurre con otras pruebas ideadas para ser usadas en diagnsticos in vitro, los resultados de esta prueba deben ser evaluados en relacin con todos los sntomas, historial clnico y otras pruebas de laboratorio del paciente. La sensibilidad y especificidad del kit ImmunoComb II Anti-HBs fueron evaluadas en un panel de 170 muestras de suero, en comparacin con dos ensayos de referencia EIA. Los resultados combinados son resumidos en la Tabla 2. Tabla 2. Resultados de la Prueba Ensayo de Referencia Positivo Negativo ImmunoComb II Anti-HBs Positivo 50 2 Negativo 0 118
Resultados de la Prueba
Validacin
Caractersticas del Ensayo*
Para confirmar el funcionamiento correcto de la prueba y demostrar la validez de los resultados, deben cumplirse las siguientes tres condiciones (ver Figura 5): 1. El Control Positivo debe producir dos puntos en el diente del Peine. 2. El Control Negativo debe producir un punto superior (Control Interno). El punto inferior no aparece o aparece muy tnuemente, sin afectar la interpretacin de los resultados. 3. Cada muestra analizada debe producir un punto superior (Control Interno). Si cualquiera de las tres condiciones no se cumple, los resultados de la prueba no son vlidos y las muestras y controles deben ser reexaminados.
Se calcularon las caractersticas del ensayo, encontrndose los siguientes reultados: Sensibilidad 100 % Especificidad 98.3 %
Control Positivo
Control Negativo
Resultados Invlidos
Repetibilidad
Cada uno de 6 sueros fue evaluado 12 veces en un solo peine, y los resultados fueron cuantificados en lectura de absorbancia. El CV de la medida de los valores no excedi el 10 %.
Figura 5. Validacin de la Prueba
Lectura e Interpretacin de los Resultados
Lectura Cualitativa Compare la intensidad del punto inferior de cada diente de la muestra con la del punto inferior al diente del Control Positivo (Figura 6) Un punto con una intensidad mayor que o igual a la del Control Positivo indica la presencia de anti-HBs a un ttulo de 10 IU/L. Un punto con una intensidad menor que la del Control Positivo es considerado como un resultado negativo.
Reproducibilidad
Seis sueros fueron evaluados por duplicado en 10 kits separados, y los resultados fueron cuantificados en lectura de absorbancia. El coeficiente de variacin (% C.V.) de los resultados no excedi el 10%.
Reaccin cruzada
Reaccin cruzada con muestras positivas para agentes tales como el virus de la hepatitis A, el virus de la hepatitis C, citomegalovirus y toxoplasma no fueron significativas.
Resultado Negativo Control Muestra Positivo Anti-HBs a titulo de = 10 IU/L
Interferencia
No se observ interferencia en muestras hemolisadas (hemoglobina hasta 10 mg/ml), lipmicas (Colesterol hasta 281.6 mg/dL; Triglicridos hasta 381.0 mg/dL) y bilirubina alta (hasta 20 mg/dl).
Figura 6. Resultados de la Prueba
Interpretacin Semicuantitativa por Lectura Visual El nivel de anti-HBs en cada muestra puede ser evaluado comparando la intensidad del color del punto inferior en cada diente, con la escala de color del CombScale suministrado con el kit. Esto se hace como sigue (Figura 7): Calibracin del CombScale
1.
2.
Calibre el CombScale. Coloque el punto inferior en el diente del Control Positivo bajo la intensidad de color ms similar en la escala de colores. Ajuste la regla hasta que aparezca la lectura "10; C+" en la ventanilla sobre la intensidad de color seleccionada. Lea los resultados sin cambiar la posicin calibrada de la regla. Compare la intensidad de color de cada punto inferior con la intensidad ms similar en la escala de colores. Registre el valor indicado en la ventanilla sobre esa intensidad como el ttulo aproximado de anti-HBs para la muestra correspondiente.
Follet EAC. 1988. Diagnosis of hepatitis B infection. In: Hugh Y, McMillan A, eds. Immunological diagnosis of sexually transmitted diseases. Marcel Dekker, New York. pp. 433-450. Herrera JL. 1994. Serological diagnosis of viral hepatitis. S Med J 87:677-684. Hollinger FB. 1991. Hepatitis B virus. In: Viral Hepatitis. (Hollinger FB, Purcel RH, Robinson WS, Gerin JL, Ticehurst J, eds.) Raven Press, New York. pp 73-138. Kiyasu PK, Caldwell SH. 1993. Diagnosis and treatment of the major hepatotropic viruses. Am J Med Sci 306:248-261. Krugman S, Overby LR, Mushawar IK, Ling C-M, Frsner GG, Deinhart F. 1979. Viral hepatitis, type B: studies on natural history and prevention re-examined. N Engl J Med 300:101-106.
* Datos detallados disponibles
Bibliografa
60453002/S12/OR
Ogra PL, Beutner KR. 1981. Hepatitis viruses. In: Milgrom F, Abeyounis CJ, Kano K, eds. Principles of immunological diagnosis in medicine. Lea & Febiger, Philadelphia. pp 247-259. Robinson WS. 1991. Hepadnaviridae and their replication. In: Viral Hepatitis. (Hollinger FB, Purcell, RH, Robinson WS, Gerin JL, Ticehurst J, eds.) Raven Press, New York.pp 39-71. Swenson PD. 1991. Hepatitis viruses. In: Balows A, Hausler WJ, Herrmann KL, Isenberg HD, Shadomy HJ, eds. Manual of Clinical Microbiology, Fifth edition. American Society for Microbiology, Washington, DC. pp 959-983. Fabricante: Representante Autorizado en EU: Orgenics France S.A. 19, rue Lambrechts 92400 Courbevoie, France Tel: +33-1 41 99 92 90 Fax: +33-1 41 99 92 95 Version: 60453002/S12/OR (04/2007)
Orgenics Ltd., part of the Inverness Medical Innovations Group. P.O.B 360 Yavne 70650, Israel Tel: ++ 972 8 942 92 01 Fax: ++ 972 8 943 87 58
Leyenda de los smbolos
CARD PLATE CONTROL CONTROL +
ImmunoComb tarjeta Bandejas de Desarrollo Control positivo Control negativo Perforador Consulte las instrucciones de uso Atencin,ver instrucciones de uso
PERFORATOR
IVD
Producto sanitario para diagnstico in vitro Limite de temperatura
Contenido suficiente para n ensayos Fabricante Representante autorizado en la Comunidad Europea
REF COMBSCALE LOT
Nmero de catlogo CombScale
Cdigo de lote Fecha de caducidad Nmero de serie
60453002/S12/OR
Resumen de los Principales Procedimientos de la Prueba
Preincubacin de la Bandeja de Desarrollo: 45 minutos a 37C
Tomar muestras y controles
Agregar las muestras y controles a la Fila A. Mezclar
Sacar el Peine del empaque
Insertar el Peine y mezclar en la Fila A. Incubar a 37C
Perforacin de la Fila B
Absorber el lquido adherido a los dientes
Insertar el Peine y Agitar en la Fila B. Incubar
Luego de mezclar/agitar e incubar en las Filas C, D y E
10
Reaccin de color en la Fila F
Resultados
Resumen del Procedimiento de la Prueba
Las instrucciones abreviadas abajo son para los usuarios experimentados en el uso del kit ImmunoComb II Anti-HBs. (Para instrucciones detalladas, favor referirse al texto completo) 1. Incube la Bandeja de Desarrollo en un incubador a 37C por 45 minutos. 2. Vierta 100 l de cada muestra y control en los pocillos de la Fila A de la Bandeja de Desarrollo y mezcle. 3. Inserte el Peine en la Fila A y contine como se describe en la Tabla 1. Tabla 1. Resumen del Procedimiento de la Prueba Paso Reaccin Antgeno-Anticuerpo Lavado Unin de HBsAg biotinilado Unin de estreptavidina/ fosfatasa alcalina Lavado Reaccin de color Detencin de la reaccin Fila A B C D E F E Proceda como sigue Mezcle;incube 2 horas a 37C; absorba. Agite; incube 2 minutos; absorba. Mezcle; incube 30 minutos a 37C; absorba. Mezcle; incube 20 minutos a 37C; absorba. Agite; incube 2 minutos; absorba. Mezcle; incube 10 minutos a 37C. Incube 1 minuto; seque al aire.
2
Manera de romper el Peine
60453002/S12/OR
Potrebbero piacerti anche
- Manejo de CepasDocumento3 pagineManejo de CepaslabhomeopaticoNessuna valutazione finora
- Aparato Digestivo 40789 17450Documento19 pagineAparato Digestivo 40789 17450Dany Villarroel MuñozNessuna valutazione finora
- Práctica 5 Uso y Manejo de BalanzasDocumento3 paginePráctica 5 Uso y Manejo de BalanzasDaniel GómezNessuna valutazione finora
- Manual de Prácticas Módulo IiiDocumento93 pagineManual de Prácticas Módulo IiiKaren LopezNessuna valutazione finora
- Anticuerpos Antigliadina AgaDocumento1 paginaAnticuerpos Antigliadina AgaJosechu Gómez Gil0% (1)
- Validacion MicrobiologicaDocumento8 pagineValidacion Microbiologicaa. tarqui m.Nessuna valutazione finora
- Tp-Inserto Lote 620BDocumento2 pagineTp-Inserto Lote 620BFreddy QuizhpiNessuna valutazione finora
- Norma de Aceites y Grasas PDFDocumento10 pagineNorma de Aceites y Grasas PDFjosue alvarez vargasNessuna valutazione finora
- Manual Maldi Biotyper 3.1 Ver. 2Documento26 pagineManual Maldi Biotyper 3.1 Ver. 2Elias ENessuna valutazione finora
- Manual PAI Tomo 1Documento114 pagineManual PAI Tomo 1Edu Vega67% (3)
- Discapacidad AuditivaDocumento18 pagineDiscapacidad AuditivaPatnay GarcicaNessuna valutazione finora
- Anti HBC EsDocumento8 pagineAnti HBC EsDaniel A. Chirinos100% (1)
- Manual POE Malaria Honduras 2006Documento97 pagineManual POE Malaria Honduras 2006cesiahdezNessuna valutazione finora
- Mga 0251. Densidad Relativa: Factor de Coleo T - 'Documento2 pagineMga 0251. Densidad Relativa: Factor de Coleo T - 'Mariana SaldivarNessuna valutazione finora
- Farcotec PDFDocumento42 pagineFarcotec PDFAna Laura Briones torresNessuna valutazione finora
- Guia Analisis Biologicos 2020 PDFDocumento133 pagineGuia Analisis Biologicos 2020 PDFSHIRLEY HUANCAHUIRE MAMANINessuna valutazione finora
- Identificación de Carbapenemasas Por Test de Hodge TritonDocumento24 pagineIdentificación de Carbapenemasas Por Test de Hodge TritonDannie Troncoso0% (1)
- Intercambiabilidad Terapéutica Entre Alopurinol Genérico y El Medicamento Innovador Zyloric™ 100, Lima-2017Documento75 pagineIntercambiabilidad Terapéutica Entre Alopurinol Genérico y El Medicamento Innovador Zyloric™ 100, Lima-2017Daniel González ScarpulliNessuna valutazione finora
- Estudio in Vitro de Los Extractos de Marañón (Anacardium Occidentales) Con Acción Hipoglicémica para Su Uso Como Alimento Nutracéuticos 6 de Abril TerminadoDocumento39 pagineEstudio in Vitro de Los Extractos de Marañón (Anacardium Occidentales) Con Acción Hipoglicémica para Su Uso Como Alimento Nutracéuticos 6 de Abril TerminadoLucia NovoaNessuna valutazione finora
- Seminario Laboratorio de Farmacognosia1.0Documento44 pagineSeminario Laboratorio de Farmacognosia1.0Raul GamboaNessuna valutazione finora
- Control de Calidad de Los Medios de CultivosDocumento37 pagineControl de Calidad de Los Medios de CultivosDELFIS SUAREZ PADILLANessuna valutazione finora
- Guia Bioquimica Clinica - Practica 1 - 7Documento26 pagineGuia Bioquimica Clinica - Practica 1 - 7Edgar SoteloNessuna valutazione finora
- Métodos InternacionalesDocumento4 pagineMétodos InternacionalesDiana AimeeNessuna valutazione finora
- 6 - Manual de Garantía de Calidad Laboratorio ClínicoDocumento53 pagine6 - Manual de Garantía de Calidad Laboratorio ClínicoMARIA ALEJANDRA OTALORA SANABRIANessuna valutazione finora
- ValidaciónDocumento19 pagineValidaciónCbrera JoseNessuna valutazione finora
- IBG 10 - Equipo #4Documento9 pagineIBG 10 - Equipo #4Rigoberto Huamani TincoNessuna valutazione finora
- USP - Guia Lab Analisis Granulometrico.2.1.1Documento7 pagineUSP - Guia Lab Analisis Granulometrico.2.1.1Jorge SorianoNessuna valutazione finora
- Antologia para Laboratorio de InmunologiaDocumento15 pagineAntologia para Laboratorio de InmunologiaJosé Ángel RoblesNessuna valutazione finora
- Guia para Laboratorio de HLGDocumento6 pagineGuia para Laboratorio de HLGDaniel PargaNessuna valutazione finora
- Control-calidad-interno-y-tecnicas-procedimientos-Hematologia-XN SYSMEXDocumento21 pagineControl-calidad-interno-y-tecnicas-procedimientos-Hematologia-XN SYSMEXlindaNessuna valutazione finora
- P-LG-13 Procedimiento Higiena y Limpieza Personal V1Documento3 pagineP-LG-13 Procedimiento Higiena y Limpieza Personal V1dgaitanruedaNessuna valutazione finora
- CL DT J32933 ES ADocumento10 pagineCL DT J32933 ES AMary Romero CastroNessuna valutazione finora
- RPR CarbonDocumento2 pagineRPR CarbonEmily0% (1)
- Ficha Técnica Hematologia2Documento6 pagineFicha Técnica Hematologia2Omar UbarnesNessuna valutazione finora
- Inserto (2012) LIATEST D-DI PLUSDocumento1 paginaInserto (2012) LIATEST D-DI PLUSManuel Perez Gomez100% (2)
- 85 Prueba de Endotocxinas BacterianasDocumento5 pagine85 Prueba de Endotocxinas BacterianasNicolás VargasNessuna valutazione finora
- Interfaz de Laboratorio - PXLab - V4Documento9 pagineInterfaz de Laboratorio - PXLab - V4Gerri ValdezNessuna valutazione finora
- Procedimiento de Analisis de MuestrasDocumento10 pagineProcedimiento de Analisis de MuestrasVanni CaamalNessuna valutazione finora
- Producción de Antibióticos Por BacteriasDocumento5 pagineProducción de Antibióticos Por BacteriasRichard Crespo PérezNessuna valutazione finora
- Norma Oficial MexicanaDocumento41 pagineNorma Oficial MexicanaSilvia GarciaNessuna valutazione finora
- Ejemplo de TesisDocumento41 pagineEjemplo de TesisRoimaMujicaNessuna valutazione finora
- Grupo KES Boletin 13Documento52 pagineGrupo KES Boletin 13sazunaxNessuna valutazione finora
- 12754c Adenosin Deaminasa AdaDocumento1 pagina12754c Adenosin Deaminasa AdajorgeNessuna valutazione finora
- Manual de Prácticas de Laboratorio de Hematología-Páginas-45-64,66-73Documento28 pagineManual de Prácticas de Laboratorio de Hematología-Páginas-45-64,66-73Celeste IcóNessuna valutazione finora
- MGA-MD1241-procedimientos de Muestreo y Tablas de Inspeccion Por AtributosDocumento23 pagineMGA-MD1241-procedimientos de Muestreo y Tablas de Inspeccion Por AtributosAlejandra LopezNessuna valutazione finora
- Cuestionario MGA 0381Documento16 pagineCuestionario MGA 0381Andres PelayoNessuna valutazione finora
- Entrenamiento Detallado Basico Usuario AU400eDocumento61 pagineEntrenamiento Detallado Basico Usuario AU400eGuillermo LopezNessuna valutazione finora
- TCM en Los Estudios de Estabilidad y Almacenamiento de Los MedicamentosDocumento7 pagineTCM en Los Estudios de Estabilidad y Almacenamiento de Los MedicamentosKatya OsunaNessuna valutazione finora
- Especificaciones de Calidad de Los Productos TerminadosDocumento10 pagineEspecificaciones de Calidad de Los Productos TerminadosROSA LUZNessuna valutazione finora
- INSERT PotasioDocumento1 paginaINSERT PotasioJairo DpNessuna valutazione finora
- 267 - mdt01 Manual de Limpieza y Desinfeccion v2 PDFDocumento27 pagine267 - mdt01 Manual de Limpieza y Desinfeccion v2 PDFAlicia Vera AnteloNessuna valutazione finora
- GM1012 HERPES SIMPLEX 1 ELISA IgG IgM - ES - 03.14Documento4 pagineGM1012 HERPES SIMPLEX 1 ELISA IgG IgM - ES - 03.14Carlos EnriquezNessuna valutazione finora
- Mga007 CotDocumento2 pagineMga007 Cotvioleta xNessuna valutazione finora
- Rotavirus SpinreactDocumento1 paginaRotavirus SpinreactEric Silva ContrerasNessuna valutazione finora
- Diseño Experimental 1Documento7 pagineDiseño Experimental 1Iris VazquezNessuna valutazione finora
- BD VacutainerDocumento3 pagineBD VacutainerMarco LandaNessuna valutazione finora
- Guia EquipamientoDocumento38 pagineGuia EquipamientoGreciaGodinez100% (1)
- Guia Del InvimaDocumento19 pagineGuia Del InvimaCALIDADNessuna valutazione finora
- LDHDocumento3 pagineLDHLeandro GarnicaNessuna valutazione finora
- ImmunoComb II HIV TrispotDocumento6 pagineImmunoComb II HIV TrispotOnigiri No KokoroNessuna valutazione finora
- Rubella IgGDocumento5 pagineRubella IgGSyncler_16Nessuna valutazione finora
- 3000-1102 Spa COREDocumento7 pagine3000-1102 Spa CORERosmeri MelaniNessuna valutazione finora
- Codificacion Cie 10Documento44 pagineCodificacion Cie 10TANIANessuna valutazione finora
- OdontologíaDocumento5 pagineOdontologíaroberto cepedaNessuna valutazione finora
- Taller de Nivelacion SegundoperiodoDocumento4 pagineTaller de Nivelacion SegundoperiodoXìíņä VâŕğåşNessuna valutazione finora
- GeneticaDocumento23 pagineGeneticaMinita TovarNessuna valutazione finora
- OBLIGACIÓN DE INFORMAR DE LOS RIESGOS LABORALES (D.S. #40, TÍTULO VI) - Coemco - Corporación Educacional Masónica de ConcepciónDocumento15 pagineOBLIGACIÓN DE INFORMAR DE LOS RIESGOS LABORALES (D.S. #40, TÍTULO VI) - Coemco - Corporación Educacional Masónica de ConcepciónCristian BenavidesNessuna valutazione finora
- Herencia de Los Grupos SanguineosDocumento2 pagineHerencia de Los Grupos SanguineosJose RiosNessuna valutazione finora
- Planificacion 6° N° 1Documento6 paginePlanificacion 6° N° 1krelito82Nessuna valutazione finora
- Melanoma Nasomaxilar 2016Documento6 pagineMelanoma Nasomaxilar 2016Sergio PerezNessuna valutazione finora
- Sondas y DrenajesDocumento18 pagineSondas y DrenajesGiovanna Josè Garrido VitelliNessuna valutazione finora
- Reporte de OuchternolyDocumento14 pagineReporte de OuchternolyQFB Dano ReyesNessuna valutazione finora
- El CuttingDocumento4 pagineEl CuttingErickHuaringa100% (1)
- ARTRÓPODOSDocumento14 pagineARTRÓPODOSJesus Alberto Bacilio EscobedoNessuna valutazione finora
- AMC - Registro Al XXVI Verano de La Investigación Científica - (Julián Adrián - Mellado)Documento11 pagineAMC - Registro Al XXVI Verano de La Investigación Científica - (Julián Adrián - Mellado)julian adrianNessuna valutazione finora
- Patologia de Torax y AbdomenDocumento9 paginePatologia de Torax y AbdomenSoledad ColqueNessuna valutazione finora
- Monitoreo de Poblaciones y Condición de Salud de Aves Marinas y Lobos Marinos en Islas Del Norte Del Golfo de California, MéxicoDocumento15 pagineMonitoreo de Poblaciones y Condición de Salud de Aves Marinas y Lobos Marinos en Islas Del Norte Del Golfo de California, MéxicoTiffany RengifoNessuna valutazione finora
- Convulsiones PediátricasDocumento48 pagineConvulsiones PediátricasMilagros Jeniffer Orrego CarbajalNessuna valutazione finora
- Mijas Semanal #982 Del 11 Al 17 de Febrero de 2022Documento40 pagineMijas Semanal #982 Del 11 Al 17 de Febrero de 2022mijassemanalNessuna valutazione finora
- Funcion de Los LinfocitosDocumento5 pagineFuncion de Los LinfocitosgendiNessuna valutazione finora
- Prendas de Protección HospitalariaDocumento9 paginePrendas de Protección HospitalariaKely MonterosNessuna valutazione finora
- E SodioDocumento32 pagineE SodioSocarmaluNessuna valutazione finora
- Guía Sistema CirculatorioDocumento3 pagineGuía Sistema CirculatorioLoreto Paredes UaracNessuna valutazione finora
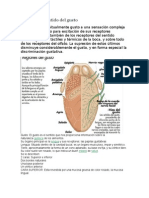
- Órgano Del Sentido Del GustoDocumento21 pagineÓrgano Del Sentido Del GustoKissisbell Suarez ArroyoNessuna valutazione finora
- PozoleDocumento2 paginePozoleNathalye De Lacruz MendozaNessuna valutazione finora
- 4 Mecanica RespiratoriaDocumento16 pagine4 Mecanica Respiratoriajira1987Nessuna valutazione finora
- F52.4 Eyaculación PrecozDocumento2 pagineF52.4 Eyaculación PrecozJoel WladimirNessuna valutazione finora
- Curso Primer RespondienteDocumento139 pagineCurso Primer RespondienteJooss Arano MurilloNessuna valutazione finora
- Guía de Parásitos InternosDocumento118 pagineGuía de Parásitos InternosJuan DavidNessuna valutazione finora