Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Categorías Riesgo Teratogénico
Caricato da
Carlos Daniel Aguilar PérezTitolo originale
Copyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Categorías Riesgo Teratogénico
Caricato da
Carlos Daniel Aguilar PérezCopyright:
Formati disponibili
Categoras de Medicamentos de acuerdo al Riesgo Teratognico
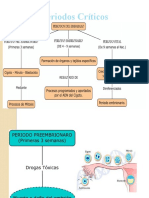
La etiqueta de algunos medicamentos de prescripcin contiene informacin acerca del nivel de riesgo para el feto y el grado de precaucin necesaria en su uso. La FDA ha establecido 5 categoras (A, B, C, D y X) para indicar el potencial teratognico de una sustancia. Este formato fue anunciado originalmente en el Boletn Farmacolgico de la FDA de septiembre de 1979. Debido a las revisiones de la rotulacin, son muchos los productos que hoy utilizan el formato estadounidense. En 1989, el ADEC (Comit Australiano de Evaluacin Farmacolgica) adopt un sistema similar de clasificacin, aunque algo expandido. Alemania estableci su propio sistema de clasificacin. A continuacin se presentan las definiciones estadounidense y australiana de las categoras de riesgo en el embarazo (Anon, 1997; Anon, 1982; Briggs et al, 1998; ADEC, 1996).
Categora de Riesgo Teratognico (FDA)
CATEGORA A: estudios controlados realizados en mujeres no han demostrado riesgo para el feto durante el primer trimestre (y no existe evidencia de riesgo durante trimestres posteriores) y la posibilidad de teratognesis parece remota. CATEGORA B: los estudios realizados en animales no han mostrado riesgo teratognico para el feto pero no existen estudios controlados en mujeres embarazadas o cuando los estudios realizados en animales han mostrado un efecto adverso (diferente que un decremento en la fertilidad) que no se ha confirmado en estudios controlados de mujeres embarazadas durante el primer trimestre (y no existe evidencia de riesgo en trimestres posteriores). CATEGORA C: los estudios realizados en animales, han mostrado efectos adversos en el feto (teratognicos, embriocidas u otros) y no existen estudios controlados en mujeres o no existen estudios disponibles ni en mujeres ni en animales. Slo deben administrarse si el beneficio potencial justifica el riesgo para el feto. CATEGORA D: existe una clara evidencia de teratogenicidad, pero el beneficio de su uso puede ser aceptable a pesar del riesgo (por ejemplo, si el frmaco es necesario en una situacin lmite o para una enfermedad grave en la que frmacos ms seguros son inefectivos o no pueden usarse). CATEGORA X: estudios en animales o humanos han demostrado anomalas fetales o hay evidencia de riesgo teratognico basado en la experiencia humana, o ambos, y el riesgo de uso en la mujer embarazada claramente supera un posible beneficio. Contraindicados en mujeres que estan o pueden quedarse embarazadas. Definiciones Australianas de las Categoras de Riesgo en el Embarazo (ADEC) A - Los medicamentos que han sido utilizados en un buen nmero de mujeres gestantes y mujeres en edad reproductiva, sin haber observado incremento alguno en la frecuencia de malformaciones u otros efectos nocivos directos o indirectos sobre el feto. B1 - Los medicamentos que han sido utilizados solamente por un nmero limitado de mujeres gestantes y mujeres en edad reproductiva, sin haber observado incremento alguno en la frecuencia de malformaciones u otros efectos nocivos directos o indirectos sobre el feto humano. Los estudios en animales* no presentan evidencia de incidencia incrementada de dao fetal. B2 - Los medicamentos que han sido utilizados solamente por un nmero limitado de mujeres gestantes y mujeres en edad reproductiva, sin haber observado incremento alguno en la frecuencia de malformaciones u otros efectos nocivos directos o indirectos sobre el feto humano. Los estudios en animales* son inadecuados o inexistentes, pero los datos disponibles no indican evidencia de incidencia incrementada de dao fetal. B3 - Los medicamentos que han sido utilizados solamente por un nmero limitado de mujeres gestantes y mujeres en edad reproductiva, sin haber observado incremento alguno en la frecuencia de malformaciones u otros efectos nocivos directos o indirectos sobre el feto humano. Los estudios en animales* indican evidencia de incidencia incrementada de dao fetal cuya significancia es considerada incierta en humanos. C - Los medicamentos que, debido a sus efectos farmacolgicos, han causado o son sospechosos de causar efectos nocivos sobre el feto humano o el neonato, sin ocasionar malformaciones. Estos efectos pueden ser reversibles. Para una informacin ms detallada deben consultarse los textos acompaantes. D - Los medicamentos que han causado, los sospechosos de haber causado o los que probablemente pueden causar un incremento en la incidencia de malformaciones o dao irreversible en el feto humano. Estas sustancias tambin pueden tener efectos farmacolgicos adversos. Para una informacin ms detallada deben consultarse los textos acompaantes. X - Los medicamentos que tienen un riesgo tan elevado de causar lesin permanente al feto que no deben utilizarse en la mujer embarazada o con posibilidad de embarazo. * Los estudios en animales presentados como soporte para la aprobacin de nuevos medicamentos deben estar en
concordancia con la Gua Australiana sobre Registro de Medicamentos, Volumen 1: Productos Farmacuticos de Prescripcin y Otros Especificados, segunda edicin. Nota: En los medicamentos de las categoras B1, B2 y B3 no existen estudios en humanos o son inadecuados, y por lo tanto la subclasificacin se basa en los datos disponibles obtenidos de animales. La asignacin de una categora B no implica mayor seguridad que la categora C. Los medicamentos dentro de la categora D no estn absolutamente contraindicados en el embarazo (por ejemplo los anticonvulsivos). Adems, en algunos casos, la categora “D” ha sido asignada sobre la base de “sospecha”. abcPediatra Powered by Mambo Generated: 5 July, 2011, 17:08
Potrebbero piacerti anche
- Formato para Mordedura PerroDocumento9 pagineFormato para Mordedura PerroEdwin Llan Ibm CorpNessuna valutazione finora
- La dieta de la fertilidad y el embarazo: La alimentación (para ellas y para ellos) antes, durante y después de tu embarazoDa EverandLa dieta de la fertilidad y el embarazo: La alimentación (para ellas y para ellos) antes, durante y después de tu embarazoNessuna valutazione finora
- Nuevos usos para viejos medicamentosDa EverandNuevos usos para viejos medicamentosNessuna valutazione finora
- Oftalmologia VeterinariaDocumento21 pagineOftalmologia VeterinariaGev Danny Carrasco EspinozaNessuna valutazione finora
- Medicamentos y EmbarazoDocumento2 pagineMedicamentos y EmbarazoKelly Sahonero HinojosaNessuna valutazione finora
- Farmaco 2Documento2 pagineFarmaco 2Lozano Ramos Hiromi GuadalupeNessuna valutazione finora
- Uso de Medicamentos en El Embarazo MDocumento2 pagineUso de Medicamentos en El Embarazo MMilena Bautista AguilarNessuna valutazione finora
- FDA Clasificación de fármacos embarazo 5 categorías riesgoDocumento2 pagineFDA Clasificación de fármacos embarazo 5 categorías riesgoMaria FuentesNessuna valutazione finora
- La Clasificación de La FDA Es Una HDocumento2 pagineLa Clasificación de La FDA Es Una HxdemorfeoxNessuna valutazione finora
- Categorías Farmacológicas en Embarazo Según La FDADocumento1 paginaCategorías Farmacológicas en Embarazo Según La FDACarlos ParraNessuna valutazione finora
- Tabla de Categorías Farmacológicas en Embarazo Según La FDADocumento1 paginaTabla de Categorías Farmacológicas en Embarazo Según La FDATania Fiorella Becerra Flores100% (1)
- Apéndice 3 - Clasificación de Los Fármacos Por Su Riesgo Al Feto (FDA)Documento1 paginaApéndice 3 - Clasificación de Los Fármacos Por Su Riesgo Al Feto (FDA)valeryfran11Nessuna valutazione finora
- Categorías de Riesgo TeratogénicoDocumento2 pagineCategorías de Riesgo TeratogénicoMery AlcantaraNessuna valutazione finora
- Clasificación de Los Fármacos Por Su Riesgo Al FetoDocumento2 pagineClasificación de Los Fármacos Por Su Riesgo Al Fetoelias moralesNessuna valutazione finora
- Farmacos Durante El EmbarazoDocumento3 pagineFarmacos Durante El EmbarazoPau GarnicaNessuna valutazione finora
- Libro-Enfermedades-Alergicas FBBVA Anexo 38 1Documento1 paginaLibro-Enfermedades-Alergicas FBBVA Anexo 38 1jdlopez8-esNessuna valutazione finora
- MarielaDocumento5 pagineMarielaDanitza Mariela Reaño ChungaNessuna valutazione finora
- Med EmbarazoDocumento13 pagineMed EmbarazoLINA MARCELA GONZALEZ TORONessuna valutazione finora
- Tema 4 - Anexo - Seguridad de Los Fármacos en El EmbarazoDocumento1 paginaTema 4 - Anexo - Seguridad de Los Fármacos en El EmbarazoCris SpNessuna valutazione finora
- Farmacos y EmbarzoDocumento6 pagineFarmacos y EmbarzoBeatriz LunaNessuna valutazione finora
- Los Medicamentos en El Embarazo PresentarDocumento22 pagineLos Medicamentos en El Embarazo PresentarKristian Ch50% (2)
- Teratologia HumanaDocumento15 pagineTeratologia HumanaEliixiita GuerreroNessuna valutazione finora
- Qué Es La FDADocumento5 pagineQué Es La FDAKevin LeonelNessuna valutazione finora
- Sesiones Tarea Maria Guadalupe MoraDocumento10 pagineSesiones Tarea Maria Guadalupe MoraMarya SalazarNessuna valutazione finora
- Terapeutica Obstetrica y Clasificacion de MedicamentoDocumento18 pagineTerapeutica Obstetrica y Clasificacion de MedicamentoAvi Erika Ruiz CastilloNessuna valutazione finora
- Medicamentos y EmbarazoDocumento32 pagineMedicamentos y Embarazopavilion2100% (2)
- FDADocumento2 pagineFDAStalin BenavidesNessuna valutazione finora
- FDA: regulador de alimentos y medicamentos en EEUUDocumento5 pagineFDA: regulador de alimentos y medicamentos en EEUUQuispe Quispe IvonneNessuna valutazione finora
- Guia de Uso de Medicamentos en Embarazo y Lantacia - CIME-UMAZADocumento3 pagineGuia de Uso de Medicamentos en Embarazo y Lantacia - CIME-UMAZAJuan Edward LeonNessuna valutazione finora
- Farmacos y EmbarazoDocumento5 pagineFarmacos y EmbarazoMónica Rojas OlavarríaNessuna valutazione finora
- Farmacología ObstétricaDocumento37 pagineFarmacología Obstétricacynthia HernandezNessuna valutazione finora
- Farmacologia TeratogenesisDocumento8 pagineFarmacologia TeratogenesisCRISTIAN ENRIQUE REVOLLAR PANAIFONessuna valutazione finora
- Efect. Adv. de Las DrogasDocumento14 pagineEfect. Adv. de Las DrogasLita Mejía BecerraNessuna valutazione finora
- Medicamentos en GestantesDocumento13 pagineMedicamentos en GestantesMarcelo Carrasco ValderramaNessuna valutazione finora
- Boletín N°22 2023 FCV Medicamentos en el Embarazo Part. IDocumento7 pagineBoletín N°22 2023 FCV Medicamentos en el Embarazo Part. ITannia OssandonNessuna valutazione finora
- Medicamentos y Categorias en EmbarazadasDocumento46 pagineMedicamentos y Categorias en EmbarazadasAbraham Rivas MiguelNessuna valutazione finora
- Gua Farmacolgica para La Mujer Embarazada en El Rea de UrgenciasDocumento17 pagineGua Farmacolgica para La Mujer Embarazada en El Rea de UrgenciasLaura TabordaNessuna valutazione finora
- Medicamentos y embarazo: clasificación de riesgos según la FDADocumento13 pagineMedicamentos y embarazo: clasificación de riesgos según la FDAalguacil.f2644Nessuna valutazione finora
- Fármacos en El Embarazo y Lactancia - MedwaveDocumento1 paginaFármacos en El Embarazo y Lactancia - MedwaveJenifer Morales NúñezNessuna valutazione finora
- Protocolo de Atencion A La Mujer GetanteDocumento42 pagineProtocolo de Atencion A La Mujer GetanteGustavo PeñaNessuna valutazione finora
- Clasificación FDA medicamentos anti-VIH embarazoDocumento1 paginaClasificación FDA medicamentos anti-VIH embarazoManuel SaldanaNessuna valutazione finora
- Desventajas y Desventajas Del Uso de FármacosDocumento6 pagineDesventajas y Desventajas Del Uso de FármacosjeiselllaNessuna valutazione finora
- Medicamentos en El Embarazo ClasificacionDocumento15 pagineMedicamentos en El Embarazo ClasificacionJairo Fernando Acero CordobaNessuna valutazione finora
- Tratamiento Farmacologico Enfermedades GI Durante Embarazo PDFDocumento13 pagineTratamiento Farmacologico Enfermedades GI Durante Embarazo PDFEvelyn Maribel Vargas PavezNessuna valutazione finora
- Capitulo Iii Medicamentos Teratogenicos, ClasificacionDocumento26 pagineCapitulo Iii Medicamentos Teratogenicos, ClasificacionKarla PachecoNessuna valutazione finora
- Tema 14 Farmacos en El EmbarazoDocumento21 pagineTema 14 Farmacos en El EmbarazoKemberling Fernandez PeñaNessuna valutazione finora
- Atención Prenatal - Fármacos .MonitoreoDocumento29 pagineAtención Prenatal - Fármacos .Monitoreopatricio burgos cedeñoNessuna valutazione finora
- Antipsicóticos en El EmbarazoDocumento7 pagineAntipsicóticos en El EmbarazoJota Orellana CuellarNessuna valutazione finora
- Tarea 1 - Qué Es El FDA (07 - 06 - 22)Documento2 pagineTarea 1 - Qué Es El FDA (07 - 06 - 22)meilyn broncanoNessuna valutazione finora
- Variaciones individuales a los fármacos: causas genéticas y ambientalesDocumento3 pagineVariaciones individuales a los fármacos: causas genéticas y ambientalesJunior Leonardo Cuevas De Los SantosNessuna valutazione finora
- Manejo Odontológico de Paciente EmbarazadaDocumento42 pagineManejo Odontológico de Paciente EmbarazadaCristian Rosas85% (13)
- Monografia FARMACOLOGIA GESTACIONAL 1 PresentarDocumento30 pagineMonografia FARMACOLOGIA GESTACIONAL 1 Presentarleslie maribel mamani mamaniNessuna valutazione finora
- Farmacologia - Foro de DebateDocumento3 pagineFarmacologia - Foro de DebateEDUARDO SEBASTIAN CUMPA ALVAREZNessuna valutazione finora
- e6BV5P 12revision02Documento15 paginee6BV5P 12revision02andres martinezNessuna valutazione finora
- Fármacos Clasificación Embarazo y LactanciaDocumento4 pagineFármacos Clasificación Embarazo y LactanciaJoha AlcocerNessuna valutazione finora
- Natural potency - ¿Qué hacer si su »mejor parte« está en huelga?: Remedios naturales que aumentan la potencia para aumentar la virilidad desde la capacidad para tener una erección hasta la constanciaDa EverandNatural potency - ¿Qué hacer si su »mejor parte« está en huelga?: Remedios naturales que aumentan la potencia para aumentar la virilidad desde la capacidad para tener una erección hasta la constanciaValutazione: 1 su 5 stelle1/5 (1)
- Un Ingrediente Natural Que Causa Cáncer - Basado En Las Enseñanzas De Frank Suarez: Los Secretos Ocultos De La CarrageninaDa EverandUn Ingrediente Natural Que Causa Cáncer - Basado En Las Enseñanzas De Frank Suarez: Los Secretos Ocultos De La CarrageninaNessuna valutazione finora
- Nutrición y cancer: Guía para la prevención y tratamiento del cancer (2ª edición)Da EverandNutrición y cancer: Guía para la prevención y tratamiento del cancer (2ª edición)Valutazione: 3.5 su 5 stelle3.5/5 (3)
- Vademécum Pediátrico BreveDocumento3 pagineVademécum Pediátrico BreveCarlos Daniel Aguilar PérezNessuna valutazione finora
- Procedimientos Tecnicos en Urgencias PDFDocumento986 pagineProcedimientos Tecnicos en Urgencias PDFAngela ßecerril ÐelgadoNessuna valutazione finora
- INSTITUTO MEXICANO DEL SEGURO SOCIAL Guía de Rotación para El Médico Interno de Pregrado en Medicina InternaDocumento6 pagineINSTITUTO MEXICANO DEL SEGURO SOCIAL Guía de Rotación para El Médico Interno de Pregrado en Medicina InternaCarlos Daniel Aguilar PérezNessuna valutazione finora
- Voluntarios PalaciegosDocumento3 pagineVoluntarios PalaciegosCarlos Daniel Aguilar PérezNessuna valutazione finora
- El Suicidio de Un Médico Que No Encontró Cura para El Amor Reportaje Erik Dimas El Universal 6 06 16Documento9 pagineEl Suicidio de Un Médico Que No Encontró Cura para El Amor Reportaje Erik Dimas El Universal 6 06 16Carlos Daniel Aguilar PérezNessuna valutazione finora
- Cor PulmonaleDocumento17 pagineCor PulmonaleCarlos Daniel Aguilar PérezNessuna valutazione finora
- Osteoporosis SG HebdDocumento44 pagineOsteoporosis SG HebdCarlos Daniel Aguilar PérezNessuna valutazione finora
- Anamnesis OftalmologicaDocumento3 pagineAnamnesis OftalmologicaCarlos Daniel Aguilar Pérez0% (1)
- Colágena matriz extracelularDocumento33 pagineColágena matriz extracelularCarlos Daniel Aguilar Pérez100% (1)
- Factores de Coagulación y Sustancias RelacionadasDocumento1 paginaFactores de Coagulación y Sustancias RelacionadasJaime Dionicio Calderón0% (1)
- Insuficiencia Cardiaca: Clasificación, Factores de Riesgo y DiagnósticoDocumento16 pagineInsuficiencia Cardiaca: Clasificación, Factores de Riesgo y DiagnósticoGuillermo Castro ContardoNessuna valutazione finora
- Cuarto de Moldes y AccesoriosDocumento41 pagineCuarto de Moldes y AccesoriosCarolay ParedesNessuna valutazione finora
- Consentimiento Informado IMPLANTE SUBDERMICO - INSERCIÓN - RETIRODocumento2 pagineConsentimiento Informado IMPLANTE SUBDERMICO - INSERCIÓN - RETIROMilena AfricanoNessuna valutazione finora
- Prevención de Accidentes Objetos CortopunzantesDocumento2 paginePrevención de Accidentes Objetos CortopunzantesJose GuzmanNessuna valutazione finora
- Apreciación Critica Del AlumnoDocumento1 paginaApreciación Critica Del AlumnoMichaelAragonLuqueNessuna valutazione finora
- TCA BorradorDocumento7 pagineTCA BorradorFrank TommoNessuna valutazione finora
- Embolia Pulmonar ResumenDocumento5 pagineEmbolia Pulmonar ResumenFlor GarroNessuna valutazione finora
- FarmacologiaDocumento21 pagineFarmacologiaEVELYN ROSERONessuna valutazione finora
- EcografiaDocumento2 pagineEcografiaKarerina 007Nessuna valutazione finora
- Obesity Imunity 2016Documento10 pagineObesity Imunity 2016Sandra Carolina Hernández BuenoNessuna valutazione finora
- La AtenciónDocumento9 pagineLa AtenciónAngie Abigail zevallos samameNessuna valutazione finora
- ExposantiretDocumento69 pagineExposantiretRoberto Páramo AlmeidaNessuna valutazione finora
- Neoplasia Ii Anaplasia y Diferenciacion 3Documento24 pagineNeoplasia Ii Anaplasia y Diferenciacion 3Ruth FernandezNessuna valutazione finora
- VENDAJEDocumento22 pagineVENDAJEanais gacituaNessuna valutazione finora
- 0000000050cnt 01 Manual UcetiDocumento146 pagine0000000050cnt 01 Manual Ucetivalentina gonzalezNessuna valutazione finora
- Escala de Autoevaluación para La Depresión de Zung PDFDocumento16 pagineEscala de Autoevaluación para La Depresión de Zung PDFMerope CripsisNessuna valutazione finora
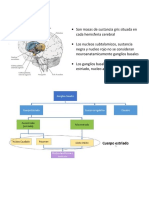
- Ganglios BasalesDocumento46 pagineGanglios BasalesAndres DangondNessuna valutazione finora
- Semiologia PsiquiatricaDocumento4 pagineSemiologia PsiquiatricaJhoan NicolasNessuna valutazione finora
- 3°formato Farmacoterapia AmbulatorioDocumento48 pagine3°formato Farmacoterapia Ambulatorioelvis vidal berrocal hinostrozaNessuna valutazione finora
- MR 353 Es PDFDocumento11 pagineMR 353 Es PDFJORFRAYANVA83Nessuna valutazione finora
- Diagnostico de AutismoDocumento25 pagineDiagnostico de AutismoJose Paulino San Ros50% (2)
- Trabajo N°1 Yanet Alcantara FernandezDocumento6 pagineTrabajo N°1 Yanet Alcantara FernandezYANET ALCANTARANessuna valutazione finora
- Caso Clinico Asma - PPPDocumento20 pagineCaso Clinico Asma - PPPAnonymous 70mZuYhFNessuna valutazione finora
- Casos Clinicos Clasicos Enarm 2018Documento554 pagineCasos Clinicos Clasicos Enarm 2018liliana millanNessuna valutazione finora
- Fármacos Que Afectana Al Sistema Nervioso CentralDocumento30 pagineFármacos Que Afectana Al Sistema Nervioso CentralJose RamosNessuna valutazione finora
- Tema 2. Iaas - Lavado de Manos-EsterilizacionDocumento30 pagineTema 2. Iaas - Lavado de Manos-Esterilizacionpamela lazcano100% (1)
- Bgacomuneros 4282635 Taccraneosimple 13887531Documento2 pagineBgacomuneros 4282635 Taccraneosimple 13887531Alexa EstradaNessuna valutazione finora