Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Cloruro de Sodio
Caricato da
ivanjcm85Descrizione originale:
Copyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Cloruro de Sodio
Caricato da
ivanjcm85Copyright:
Formati disponibili
Cloruro de sodio
Cloruro de sodio
Cloruro de sodio
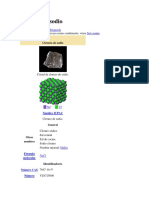
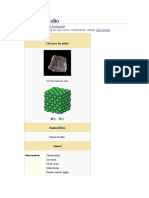
Cristal de cloruro de sodio.
__ Na+__ ClNombre (IUPAC) sistemtico Cloruro de sodio General Otros nombres Cloruro sdico Sal comn Sal de cocina Sodio cloruro NaCl Identificadores Nmero CAS Nmero RTECS 7647-14-5 [1]
Frmula molecular
VZ4725000 Propiedades fsicas
Estado de agregacin Apariencia Densidad Masa molar Punto de fusin Punto de ebullicin Estructura cristalina
Slido Incoloro; aunque parece blanco si son cristales finos o pulverizados. 2165 kg/m3; 2,165 g/cm3 58,4 g/mol 1074K (801C) 1738K (1465C) f.c.c. Propiedades qumicas
Solubilidad en agua Producto de solubilidad
35,9 g por 100 mL de agua 37,79 mol2 Termoqumica
fH0gas
-181,42 kJ/mol
Cloruro de sodio
2
-385,92 kJ/mol -411,12 kJ/mol 229,79 Jmol-1K Riesgos
fH0lquido fH0slido S0gas, 1 bar
Ingestin Inhalacin Piel Ojos
Peligroso en grandes cantidades; su uso a largo plazo en cantidades normales puede traer problemas en los riones. Puede producir irritacin en altas cantidades. Puede producir resequedad. Puede producir irritacin y molestia. Compuestos relacionados
Compuestos relacionados Cloruro de potasio Valores en el SI y en condiciones estndar (25 C y 1 atm), salvo que se indique lo contrario.
El cloruro de sodio, ms conocido como sal de mesa, o en su forma mineral halita, es un compuesto qumico con la frmula NaCl. El cloruro de sodio es una de las sales responsable de la salinidad del ocano y del fluido extracelular de muchos organismos. Tambin es el mayor componente de la sal comestible, es comnmente usada como condimento y conservante de comida. En la antigedad, el cloruro de sodio era muy apetecido como un bien transable y como condimento, y se remuneraba en la poca preclsica romana a los soldados que construan la Va Salaria que empezaba en las canteras de Ostia hasta Roma con un generoso salarium argentum. Tambin era el salario de un esclavo ya que se entregaba una pequea bolsa con sal; por lo que la palabra asalariado tiene un significado etimolgicamente peyorativo.[2]
Propiedades qumicas
El cloruro de sodio es un compuesto inico formado por un catin sodio (Na+) y un anin cloruro (Cl-), y, como tal, puede reaccionar para tener cualquiera de estos dos iones. Como cualquier otro cloruro inico soluble, precipita cloruros insolubles cuando es agregado a una solucin de una sal metlica apropiada como nitrato de plata: NaCl(ac) + AgNO3(ac) AgCl(s) + NaNO3(ac). Otro mtodo para separar ambos componentes es mediante la electrlisis. Si se aplica electrlisis con un elevado potencial a una salmuera alcalina, el producto andico es gas cloro (Cl2) y el catdico es hidrxido de sodio (NaOH) e hidrgeno (H2). 2 NaCl (electrlisis) = 2 NaOH + Cl2 (gas)+ H2(gas) El cloruro de sodio como la mayora de las sales inicas confiere propiedades coligativas a sus disoluciones, es decir es capaz de variar la presin de vapor de la disolucin, elevar el punto de ebullicin y descender el punto de congelacin segn su concentracin molar. El cloruro de sodio qumicamente puro no es higroscpico, el que la sal ordinaria se humedezca se debe a las impurezas de cloruro de magnesio, sustancia que si absorbe la humedad atmosfrica.
Cloruro de sodio
Produccin
El cloruro de sodio es producido en masa por la evaporacin de agua de mar o salmuera de otros recursos, como lagos salados y minando la roca de sal, llamada halita. En 2008, la produccin mundial de sal estuvo estimada en 210 millones de toneladas mtricas, y los principales pases productores eran Estados Unidos (40,3 millones de toneladas), China (32,9), Alemania (17,7), India (14,5) y Canad (12,3).[3]
Regulacin fisiolgica
El in Na+ es causante de la regulacin osmtica celular regulando el potencial de membrana expulsando el in K +, facilita en gran manera el impulso nervioso y es aportado al organismo en gran medida como sal de mesa.
Antisptico local y preservante de alimentos
La sal gracias a su elevado poder osmtico es capaz de deshidratar a un amplio espectro de virus y bacterias en estado no-esporulado, por lo que se usa como un doloroso antisptico para desinfectar heridas. Muy pocos microorganismos como los halfilos y organismos superiores como los crustceo braquipodos conocidos como las Artemias pueden resistirse al poder osmtico de la sal. Entre los microorganismos resistentes a la salinidad esta el caso de la bacteria , B. marismortui encontrada en el Mar muerto. La salazn de las carnes de conserva es una forma de preservar estas de la accin bacteriana retrasando la descomposicin proteica.
Supresor de nieve
El cloruro de sodio en salmuera al 24% es usado en los centros invernales como supresor de nieve, al disolverse la sal baja el punto de congelacin y genera energa de entalpa (H= -385,820 KJ/mol) al disolverse.
Plantas
El sodio es un nutriente no esencial para las plantas, por lo que se necesita en muy bajas dosis. Es por ello que a dosis superiores a la necesaria, la sal es txica. Ciertos grupos de plantas como las plantas C4 o la CAM necesitan dosis mayores de este elemento y otras llamadas halfitas son ms tolerantes al exceso de sal.
Referencias
[1] Nmero CAS (http:/ / nlm. nih. gov/ cgi/ mesh/ 2006/ MB_cgi?rn=1& term=7647-14-5) [2] Salario (http:/ / etimologias. dechile. net/ ?salario) [3] Susan R. Feldman. Sodium chloride. Kirk-Othmer Encyclopedia of Chemical Technology. John Wiley & Sons, Inc. Published online 2005.
Enlaces externos
Wikimedia Commons alberga contenido multimedia sobre Cloruro de sodio. Commons La salinidad en el suelo (http://www.edafologia.net/conta/tema12/efectos.htm) Importancia de la sal en la nutricin del ganado (http://web.archive.org/web/http://www.saltinstitute.org/ publications/stm/stm-7.html)
Fuentes y contribuyentes del artculo
Fuentes y contribuyentes del artculo
Cloruro de sodio Fuente: http://es.wikipedia.org/w/index.php?oldid=73366636 Contribuyentes: 3coma14, Aadrover, Abin, Acratta, Airunp, Akhram, Alhen, Alvaro qc, Angel GN, Antonio Peinado, Archaeodontosaurus, ArwinJ, Baen, Balderai, Beto29, BetoCG, Bigsus, Cansado, Cipin, Cmx, Dark Bane, Dbzmusic007, Diegusjaimes, Dodo, Edslov, El Moska, Eloy, Emiduronte, Erudito234, F.martinez.pastor, FAR, Filipo, Florencio, Foundling, Gengiskanhg, Gerard00p2, Gtz, Hahmo, Halfdrag, Hari Seldon, Helmy oved, Interwiki, Jarisleif, Jheridan, Jkbw, Jorge c2010, Joseaperez, Josemiotto, Laureano55, Maldoror, Mampato, Manbemel, Matdrodes, Mercenario97, Miguel A. Ortiz Arjona, Moriel, Muro de Aguas, N0thingness, Nonick, Orgullomoore, PaulaGG, Petronas, Petruss, Pitxulin1, Pixeltoo, Plux, Qwertyytrewqqwerty, Rascamonos, Rastrojo, Retama, Rizobio, Rosarinagazo, Smccr, SuperBraulio13, Tamorlan, Tano4595, Technopat, Template namespace initialisation script, Tirithel, Tomas Samuel, Triku, Tycho, UA31, UAwiki, Untrozo, Wesisnay, Xexito, Zofwar, 209 ediciones annimas
Fuentes de imagen, Licencias y contribuyentes
Archivo:Selpologne.jpg Fuente: http://es.wikipedia.org/w/index.php?title=Archivo:Selpologne.jpg Licencia: Creative Commons Attribution-Sharealike 3.0,2.5,2.0,1.0 Contribuyentes: Didier Descouens Archivo:Sodium-chloride-3D-ionic.png Fuente: http://es.wikipedia.org/w/index.php?title=Archivo:Sodium-chloride-3D-ionic.png Licencia: Public Domain Contribuyentes: Benjah-bmm27 Archivo:Commons-logo.svg Fuente: http://es.wikipedia.org/w/index.php?title=Archivo:Commons-logo.svg Licencia: logo Contribuyentes: SVG version was created by User:Grunt and cleaned up by 3247, based on the earlier PNG version, created by Reidab.
Licencia
Creative Commons Attribution-Share Alike 3.0 //creativecommons.org/licenses/by-sa/3.0/
Potrebbero piacerti anche
- Tema de TesisDocumento18 pagineTema de TesisJose Carlos Huamani QuicañoNessuna valutazione finora
- Cloruro de SodioDocumento10 pagineCloruro de SodiobetshabeNessuna valutazione finora
- Cloruro de SodioDocumento7 pagineCloruro de SodioJuan Carlos MosqueraNessuna valutazione finora
- Sal y SalmueraDocumento8 pagineSal y SalmueraJhoel Mamani PinedoNessuna valutazione finora
- Cloruro de SodioDocumento10 pagineCloruro de SodioJohn Rafael Carrillo DolugarNessuna valutazione finora
- HALITADocumento7 pagineHALITAwalterNessuna valutazione finora
- Cloruro de SodioDocumento2 pagineCloruro de SodioJezziNessuna valutazione finora
- Cloro OF - XD - Docx 11Documento36 pagineCloro OF - XD - Docx 11Fernando José Amézquita CalderónNessuna valutazione finora
- AguaDocumento7 pagineAguaMarlis RodriguezNessuna valutazione finora
- ACTIVIDADESDocumento9 pagineACTIVIDADESjes14Nessuna valutazione finora
- Beneficios y Afectaciones Del Cloruro de Sodio en Los Seres VivosDocumento13 pagineBeneficios y Afectaciones Del Cloruro de Sodio en Los Seres VivosAndrea ZVNessuna valutazione finora
- Cloruro de Sodio UzielDocumento8 pagineCloruro de Sodio UzielUziel Cosme OjedaNessuna valutazione finora
- Acido Clorhídrico: ObjetivoDocumento9 pagineAcido Clorhídrico: ObjetivoLuis Ignacio AstroñaNessuna valutazione finora
- Cloruro de SodioDocumento27 pagineCloruro de SodioluzNessuna valutazione finora
- Diagrama de La SalDocumento35 pagineDiagrama de La SalManuel Rios75% (4)
- Industria Del Cloro-AlcaliDocumento50 pagineIndustria Del Cloro-AlcaliJorge BautistaNessuna valutazione finora
- Cloruro de Sodio (NaCl)Documento15 pagineCloruro de Sodio (NaCl)KAROLINA FLORES DUARTENessuna valutazione finora
- Cloruro de SodioDocumento12 pagineCloruro de Sodiovict1992Nessuna valutazione finora
- Proceso de Producción de NaclDocumento4 pagineProceso de Producción de NaclIrvinJosueVillasecaCastilloNessuna valutazione finora
- Cloruro de SodioDocumento4 pagineCloruro de SodioHector MolinaNessuna valutazione finora
- MoleculaDocumento16 pagineMoleculaAlexsoulNessuna valutazione finora
- Wa0031Documento26 pagineWa0031Christofer Felix Pacherres MendozaNessuna valutazione finora
- Industria de La SalDocumento7 pagineIndustria de La SalAnderson Rodriguez Torres100% (1)
- Nitrato de PlataDocumento4 pagineNitrato de PlataYndira RamirezNessuna valutazione finora
- Cloruro de SodioDocumento1 paginaCloruro de SodioSharon Alexandra Bolaños SilvaNessuna valutazione finora
- Caracteristicas de SalesDocumento6 pagineCaracteristicas de SalesChristian Daga QuispeNessuna valutazione finora
- 1V14N1-ramirez-san Jose-SodioDocumento11 pagine1V14N1-ramirez-san Jose-SodiovilmaNessuna valutazione finora
- Sal ComúnDocumento24 pagineSal ComúnCompuDell MazateNessuna valutazione finora
- Ácido SulfúricoDocumento14 pagineÁcido SulfúricoDavid GarciaNessuna valutazione finora
- 10 Guia Química Veintena 71Documento10 pagine10 Guia Química Veintena 71Pepito LopezNessuna valutazione finora
- Cloruro Sódico y Su FormaciónDocumento5 pagineCloruro Sódico y Su FormaciónJimmy Victorino CezpedezNessuna valutazione finora
- PDF Document 3Documento3 paginePDF Document 3bo bNessuna valutazione finora
- Informe de QuimicaDocumento14 pagineInforme de QuimicaMaritza Paico ruizNessuna valutazione finora
- Unidad3.2.rangel Ramírez María MatildeDocumento9 pagineUnidad3.2.rangel Ramírez María Matildealda.camposrNessuna valutazione finora
- Hal UrosDocumento21 pagineHal UrosAnonymous 0EWrsfxsNessuna valutazione finora
- Cloruro de SodioDocumento23 pagineCloruro de SodioJose GarciaNessuna valutazione finora
- Sal ComunDocumento1 paginaSal ComunMisael OcheitaNessuna valutazione finora
- Ud1.3 Productos Químicos en JoyeríaDocumento40 pagineUd1.3 Productos Químicos en JoyeríajmpbNessuna valutazione finora
- Quimica de 5to Año de BachilleratoDocumento20 pagineQuimica de 5to Año de BachilleratoMarisol GuzmanNessuna valutazione finora
- Las Sales y Sus Aplicaciones en La VidaDocumento5 pagineLas Sales y Sus Aplicaciones en La VidaAgustin Gonzalez RumualdoNessuna valutazione finora
- CapacitacionDocumento15 pagineCapacitacionNataly Montoya GutierrezNessuna valutazione finora
- Lectura Del Cloruro de SodioDocumento1 paginaLectura Del Cloruro de Sodiojean carlos canales brunoNessuna valutazione finora
- NACL ProcesdsdsamienDocumento23 pagineNACL ProcesdsdsamienDaniel MontanaresNessuna valutazione finora
- Cristalizacion Del CobreDocumento10 pagineCristalizacion Del CobreJhon AcevedoNessuna valutazione finora
- Origen Del NaclDocumento8 pagineOrigen Del NaclAlejandro RomeroNessuna valutazione finora
- ClorosodaDocumento16 pagineClorosodawinderNessuna valutazione finora
- BUSTAMANTE, SALVADOR Sal de MesaDocumento35 pagineBUSTAMANTE, SALVADOR Sal de MesaPercy Reyes RegaladoNessuna valutazione finora
- Nacl ProyectoDocumento16 pagineNacl ProyectoPaul Carly Duche ChaguayNessuna valutazione finora
- SodioDocumento9 pagineSodioEnriqueCondoFNessuna valutazione finora
- Introducción A La MineríaDocumento18 pagineIntroducción A La MineríaconitalarrainNessuna valutazione finora
- Estudio de Mercado HCLDocumento4 pagineEstudio de Mercado HCLMatias ANessuna valutazione finora
- Sulfato de SodioDocumento8 pagineSulfato de SodioCAICAY OTOYA LUIS EDUARDONessuna valutazione finora
- Tarea de ElectroDocumento7 pagineTarea de ElectroGuadalupe CallisayaNessuna valutazione finora
- Sulfato de Cobre WIKIPEDIADocumento8 pagineSulfato de Cobre WIKIPEDIAEDWIN MOLLINEDO VELIZNessuna valutazione finora
- Familia IA - 011 SodioDocumento5 pagineFamilia IA - 011 SodioTiffani Estrella EstrellaNessuna valutazione finora
- HalitaDocumento5 pagineHalitaCLAUDIO DAIMER SONCCO CHAÑINessuna valutazione finora
- SEMANA13Documento11 pagineSEMANA13Danner Jair Sanchez SaavedraNessuna valutazione finora
- Yeso, Sales y AnhidritaDocumento20 pagineYeso, Sales y AnhidritaEadwine Ed100% (1)
- Bono (Finanzas)Documento3 pagineBono (Finanzas)ivanjcm85Nessuna valutazione finora
- Estadística AplicadaDocumento1 paginaEstadística Aplicadaivanjcm85Nessuna valutazione finora
- Kiwi (Fruta)Documento3 pagineKiwi (Fruta)ivanjcm85Nessuna valutazione finora
- El Código Da VinciDocumento8 pagineEl Código Da Vinciivanjcm85Nessuna valutazione finora
- Allium CepaDocumento5 pagineAllium Cepaivanjcm85Nessuna valutazione finora
- AzúcarDocumento8 pagineAzúcarivanjcm85Nessuna valutazione finora
- Limbo (Videojuego)Documento10 pagineLimbo (Videojuego)ivanjcm85Nessuna valutazione finora
- Manual DewaltDocumento68 pagineManual DewaltFreddy RodriguezNessuna valutazione finora
- Huracán Alberto (1982)Documento4 pagineHuracán Alberto (1982)ivanjcm85Nessuna valutazione finora
- Memoria de Solo LecturaDocumento3 pagineMemoria de Solo Lecturaivanjcm85Nessuna valutazione finora
- Ingreso y Salida de Aditivos e Insumos en General 2024Documento600 pagineIngreso y Salida de Aditivos e Insumos en General 2024Geraldine DayanaNessuna valutazione finora
- Compuestos Del Hidrógeno SolucionesDocumento2 pagineCompuestos Del Hidrógeno SolucionesJavier Iglesias100% (1)
- Ayudantía SN1 - SN2 PAUTADocumento28 pagineAyudantía SN1 - SN2 PAUTAPía RedlichNessuna valutazione finora
- Cuestiones Bloque III.1 - Soluciones - ResumenDocumento4 pagineCuestiones Bloque III.1 - Soluciones - ResumenDavid TorresNessuna valutazione finora
- Informe 6 Acido ClorhidricoDocumento8 pagineInforme 6 Acido ClorhidricoMaria Esther Contreras Serrano0% (1)
- NullDocumento8 pagineNullLNessuna valutazione finora
- Piridoxina PDFDocumento3 paginePiridoxina PDFJeniffer Garcia DazaNessuna valutazione finora
- HidrácidosDocumento2 pagineHidrácidosTANIA LIZBETH SANCHEZ MORGADO 102Nessuna valutazione finora
- Taller Clasificación de ReaccionesDocumento3 pagineTaller Clasificación de Reaccionesmarilu viafara l.Nessuna valutazione finora
- Practica Sales Hidracidas MixtasDocumento1 paginaPractica Sales Hidracidas MixtasClaudia ValenciaNessuna valutazione finora
- Practica n1Documento3 paginePractica n1Yeselin ZuritaNessuna valutazione finora
- Agar MarinoDocumento5 pagineAgar MarinoEstefania MendezNessuna valutazione finora
- Fletes 2014Documento18 pagineFletes 2014Jose ParraNessuna valutazione finora
- Clase 8 de Abril - Ejercicios de Rendimiento y PurezaDocumento3 pagineClase 8 de Abril - Ejercicios de Rendimiento y PurezaJuan Andrés Vélez100% (1)
- Formulación Sales BinariasDocumento4 pagineFormulación Sales BinariasAdsebuma Estupiñán LeónNessuna valutazione finora
- Refinacion Del Oro Con Agua Regia ConvDocumento5 pagineRefinacion Del Oro Con Agua Regia Convarnaldo_ibarrolaNessuna valutazione finora
- Hidrocarburos AromaticosDocumento9 pagineHidrocarburos AromaticosIPPNessuna valutazione finora
- Hoja de Trab 1-2 Quimica PDFDocumento5 pagineHoja de Trab 1-2 Quimica PDFJose AbellaNessuna valutazione finora
- HALOGENADOSDocumento2 pagineHALOGENADOSMax Guerrero AlarconNessuna valutazione finora
- Hidrácidos EjerciciosDocumento3 pagineHidrácidos EjerciciosMaria CriadoNessuna valutazione finora
- Tabla de Iones PositivosDocumento2 pagineTabla de Iones PositivosMontan Zamuel100% (4)
- MDZ0000355 - CoF en SalmuerasDocumento2 pagineMDZ0000355 - CoF en SalmuerasNatalia SorianoNessuna valutazione finora
- Taller #2 Determinacion de Cloruros Por PotenciometriaDocumento4 pagineTaller #2 Determinacion de Cloruros Por PotenciometriaEMERSONNessuna valutazione finora
- Diagrama en Bloque de Tratamiento de Agua para VerDocumento1 paginaDiagrama en Bloque de Tratamiento de Agua para VerDaia Fontana0% (1)
- Anexo - ChangDocumento6 pagineAnexo - ChangNhorita RiveraNessuna valutazione finora
- Reaccionario-Derivados de Ácidos CarboxílicosDocumento2 pagineReaccionario-Derivados de Ácidos CarboxílicosRicardo Alfonso Trujillo SantillanaNessuna valutazione finora
- Radical Halogénico 22Documento6 pagineRadical Halogénico 22Carla RomeroNessuna valutazione finora
- DETERMINACIÓN DE HALUROS EN UNA MEZCLA CON AgNO3Documento7 pagineDETERMINACIÓN DE HALUROS EN UNA MEZCLA CON AgNO3Fabián Eduardo CamayoNessuna valutazione finora
- Tabla Constantes KpsDocumento3 pagineTabla Constantes KpsAle González SánchezNessuna valutazione finora
- Cloruros de AcidoDocumento5 pagineCloruros de AcidoabdielNessuna valutazione finora