Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
Potencial de Acción Cardíaco
Caricato da
Marcos Miguel Huaco RomeroTitolo originale
Copyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
Potencial de Acción Cardíaco
Caricato da
Marcos Miguel Huaco RomeroCopyright:
Formati disponibili
Potencial de accin cardaco
El potencial de accin cardaco es un potencial de accin especializado que tiene lugar en el corazn, que presenta propiedades nicas necesarias para el funcionamiento del sistema de conduccin elctrica del corazn.1 El potencial de accin (PA) cardaco difiere de forma significativa en diferentes porciones del corazn. Esta diferenciacin de PA genera diferentes caractersticas elctricas de las distintas zonas del corazn. Por ejemplo, el tejido conductivo especializado del corazn tiene la capacidad de despolarizarse sin ninguna influencia externa. Esta propiedad se conoce como el automatismo del msculo cardaco. La actividad elctrica de los tejidos especializados de conduccin no son aparentes en el electrocardiograma de superficie (ECG o EKG - de la palabra alemana). Esto se debe a la pequea masa de estos tejidos en comparacin al miocardio.
ndice
[ocultar]
1 Vista general 2 Principales canales inicos y corrientes cardacas 3 El potencial de reposo de la membrana celular 4 Fases del potencial de accin cardaco
o o o o o
4.1 Fase 0 4.2 Fase 1 4.3 Fase 2 4.4 Fase 3 4.5 Fase 4
5 Automatismo cardaco
o o o
5.1 Localizacin de las clulas marcapasos 5.2 Canales inicos marcapasos 5.3 Variaciones del automatismo
6 Referencias 7 Vase tambin 8 Enlaces externos
Vista general[editar editar cdigo]
Concentraciones ionicas intra- y extracelulares (mmol/L) Elemento Ion Extracelular Intracelular Ratio Sodio Na+ 135 - 145 10 14:1
El msculo cardaco tiene algunas similitudes con el msculo esqueltico, as como importantes
Potasio Cloruro
K+ Cl
-
3.5 - 5.0 95 - 110
155 20 - 30 10-4
1:30 4:1 2x 104:1
propiedades nicas. Como losmiocitos esquelticos Calcio (y los axones para esta propiedad), un miocito cardaco dado tiene un potencial de
Ca2+ 2
Aunque el contenido intracelular de Ca2+ es alrededor de 2 mM, en su mayora est unido a molculas o secuestrado en orgnulos intracelulares (mitocondrias y retculo sarcoplsmico).
membrana negativo cuando est en reposo. Una diferencia importante es la duracin de los PA:
En un nervio tpico, la duracin de un PA es de alrededor de 1 milisegundo (ms). En clulas musculares esquelticas, la duracin es aproximadamente 2-5 ms. Sin embargo, la duracin del PA ventricular es de 200 a 400 ms.
Estas diferencias se basan en variaciones en la conductancia inica de cada tipo celular, que son las responsables de los cambios en el potencial de membrana. Comparando el msculo esqueltico y el cardaco, una diferencia importante es la manera en la que ambos aumentan la concentracin mioplsmica de Ca2+ para inducir la contraccin:
Cuando el msculo esqueltico es estimulado por axones motores somticos, un flujo de Na+ hacia el interior de la clula rpidamente despolariza el miocito esqueltico y desencadena la liberacin de calcio desde el retculo sarcoplsmico.
En miocitos cardacos, sin embargo, la liberacin de Ca2+ desde el retculo sarcoplsmico es inducido por el flujo de Ca2+ hacia el interior celular a travs de canales de calcio voltajedependientes en el sarcolema. Este fenmeno se denomina liberacin de calcio inducida por calcio e incrementa la concentracin mioplsmica de Ca2+ libre, lo que produce la contraccin muscular.
En ambos tipos de msculo, despus de un periodo muerto (el periodo refractario absoluto), los canales de potasio se reabren y el flujo resultante de K+ hacia el exterior celular produce larepolarizacin hasta el estado de reposo. Los canales de calcio voltaje-dependientes en el sarcolema cardaco normalmente se activan debido a un flujo de sodio hacia el interior celular durante la fase "0" del potencial de accin (ver ms adelante). Debe observarse que hay importantes diferencias fisiolgicas entre las clulas nodales y las clulas ventriculares; las diferencias especficas en los canales inicos y los mecanismos de polarizacin generan propiedades nicas de las clulas del nodo sinusal, sobre todo las despolarizaciones espontneas (automatismo del msculo cardaco), necesarias para la actividad demarcapasos del nodo sinusal.
Principales canales inicos y corrientes cardacas[editar editar
cdigo]
Los canales inicos son selectivos para diferentes aniones y cationes. Por ejemplo, algunos canales inicos son selectivos para iones sodio, potasio, calcio y cloro. Es ms, un ion particular puede tener
diferentes canales responsables de su movimiento a travs de la membrana, como ocurre con el potasio. Existen dos tipos de canales inicos:
dependientes de voltaje, que se abren o cierran en respuesta a cambios en el potencial de membrana; la mayor parte de los canales inicos que participan en el PA cardaco son de este tipo;
canales operados por receptores, que se abren o cierran en respuesta a seales qumicas que se detectan por receptores en la membrana celular (el sarcolema). Por ejemplo, la acetilcolina(el neurotransmisor liberado por el nervio vago del sistema parasimptico) se une a receptores del sarcolema y produce la apertura de un tipo especial de canales para el potasio ( IK, ACh).1
Corrientes principales durante el potencial de accin ventricular
Corriente Apertura dep. Voltaje Voltaje y receptor Voltaje Voltaje CaV1.2 CACNA1C Protena NaV1.5 SCN5A Gen Fase 0 de los miocitos Fase / funcin
Rpida Na+: INa
Lenta Na+ (funny): If
Fase 4 de la corriente marcapasos en las clulas del nodo s nodo AV
Tipo L (lenta): ICa(L)
Entrada lenta, de larga duracin; fase 2 miocitos y fases 4clulas del nodo sinusal y nodo AV Corriente transitoria; contribuye a la fase 4 de la corriente marcapasos en las clulas del nodo sinusal y nodo AV
Tipo T (transitoria): ICa(T)
Inward rectifying: IK1 Voltaje
Kir2.1/2.2/2.3
Mantiene el potencial negativo en la fase 4; se cierra con la KCNJ2/KCNJ12/KCNJ4 despolarizacin; su descenso contribuye a las corrientes marcapasos KCND2/KCND3 KCNQ1 KCNH2 Contribuye a la fase 1 en los miocitos 2,3 Repolarizacin: fase 3 El ATP lo inhibe; se abre cuando el ATP disminuye Activado por acetilcolina; acoplado a una protena G
Transient outward: Ito1
Voltaje Voltaje Voltaje Receptor Receptor Voltaje Voltaje Voltaje
KV4.2/4.3 KV7.1 KV11.1 (hERG)
Delayed rectifier slow: IKs
Delayed rectifier rapid: IKr
Sensible a ATP: IK,
ATP
Activado por acetilcolina: IK, ACh
INaCa
intercambiador 3Na+1Ca2+ 3Na+-2K+-ATPase transportador de Ca2+ - ATPasa
NCX1 (SLC8A1) ATP1A ATP1B
homeostasis inica homeostasis inica homeostasis inica
INa,K
IpCa
Los canales inicos pueden estar en conformacin abierta, cerrada o inactiva. Los iones slo pueden pasar a travs de los canales cuando estn en conformacin abierta. En los canales dependientes de voltaje, el paso de una conformacin a otra est regulado por el potencial de membrana. El caso mejor estudiado es el de los canales rpidos de sodio. Cuando la membrana est en reposo (-90 mV), estos canales estn cerrados, impidiendo la entrada de sodio al interior celular. Cuando la membrana se despolariza (+20 mV), el canal pasa a la conformacin abierta, y el sodio entra. Durante la fase de repolarizacin , el canal est en estado inactivo, que tampoco permite la entrada de sodio. Cuando el potencial vuelve a alcanzar el estado de reposo, el canal recupera la conformacin cerrada original. Cuando estn en situacin de hipoxia, los miocitos se despolarizan hasta un nivel de reposo menos negativo (a -55 mV), en el que los canales de sodio estn en un estado inactivo, lo que altera los PA de los miocitos, ya que las corrientes rpidas de sodio se encuentran bloqueadas. Otros canales inicos tambin presentan conformaciones abiertas y cerradas, pero los detalles a nivel molecular no se conocen bien an.1 Los canales de calcio Existen dos tipos de canales de calcio voltaje-dependientes, y ambos juegan un papel crtico en la fisiologa del msculo cardaco. Estos canales responden de forma diferente a los cambios de voltaje a travs de la membrana:
Los canales de calcio tipo L ('L' por "larga" duracin) responden a potenciales ms altos, se abren ms despacio y permanecen abiertos ms tiempo que los de tipo T. Debido a sus propiedades, los canales tipo L son importantes para mantener un PA en los miocitos. Los canales tipo L son las dianas de un tipo de drogas denominadas dihidropiridinas, que bloquean las corrientes producidas por estos canales.
Los canales de calcio tipo T ('T' por "transitorios") son importantes en la iniciacin de los PA. Por su rpida cintica, los canales de calcio tipo T se encuentran comnmente en clulas que tienen un comportamiento elctrico rtmico:
neuronas implicadas en actividades rtmicas como caminar o respirar; clulas marcapasos del corazn (en el nodo sinusal y el nodo AV), que controlan los latidos cardacos.
El potencial de reposo de la membrana celular[editar editar cdigo]
El potencial de reposo de la membrana est generado por la diferencia en concentraciones inicas y conductancias a travs de la membrana celular durante la fase 4 del potencial de accin. El potencial de reposo normal en el miocardio ventricular vara entre -85 a -95 mV. Este potencial est determinado por la permeabilidad selectiva de la membrana celular a varios iones. La membrana es permeable sobre todo al K+ y relativamente impermeable al resto de los iones. El potencial de membrana est por ello dominado por el potencial de equilibrio del K+, siguiendo el gradiente de K+ a
travs de la membrana celular. El potencial de Nernst para el K+ a 37 C puede calcularse utilizando la ecuacin de Nernst:1
El mantenimiento de este gradiente inico se debe a la accin de diferentes bombas inicas y mecanismos de intercambio, que incluyen la ATPasa Na+-K+, el intercambiador Na+-Ca2+ y el canal de K+ denominado inward rectifier (rectificador de entrada) IK1. En el interior celular, el K+ es el catin principal, y el fosfato y las bases conjugadas de los cidos orgnicos son los aniones dominantes. En exterior celular, predominan el Na+ y el Cl-.
Fases del potencial de accin cardaco[editar editar cdigo]
El potencial de accin cardaco tiene cinco fases.
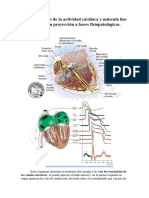
Corrientes relativas de iones en relacin con las fases en el ECG.
El modelo estndar para comprender el potencial de accin cardaco es el PA delmiocito ventricular y las clulas de Purkinje. El PA tiene 5 fases, numeradas del 0 al 4. La fase 4 es el potencial de reposo de la membrana, y describe el PA cuando la clula no est estimulada. Cuando la clula es estimulada elctricamente (normalmente por una corriente elctrica procedente de una clula adyacente), empieza una secuencia de acciones, que incluyen la entrada y salida de mltiples cationes y aniones, que conjuntamente producen el potencial de accin celular, propagando la estimulacin elctrica a las clulas adyacentes. De esta manera, la estimulacin elctrica pasa de una clula a todas las clulas que la rodean, alcanzando a todas las clulas del corazn.
Fase 0[editar editar cdigo]
La fase 0 es la fase de despolarizacin rpida. La pendiente de la fase 0 representa la tasa mxima de despolarizacin de la clula y se conoce como dV/dt max. La despolarizacin rpida se debe a la apertura de los canales rpidos de Na+ , lo que genera un rpido incremento de la conductancia de la membrana para el Na+ (gNa+) y por ello una rpida entrada de iones Na+ (INa) hacia el interior celular. Al mismo tiempo, la gK+ disminuye. Estos dos cambios en la conductancia modifican el potencial de membrana, alejndose del potencial de equilibrio del potasio (-96 mV, como vimos antes) y acercndose al potencial de equilibrio del sodio (+52 mV). La habilidad de la clula de abrir los canales rpidos de Na+ durante la fase 0 est en relacin con el potencial de membrana en el momento de la excitacin. Si el potencial de membrana est en su lnea basal (alrededor de -85 mV), todos los canales rpidos de Na+ estn cerrados, y la excitacin los abrir todos, causando una gran entrada de iones Na+. Sin embargo, si el potencial de membrana es menos negativo (lo que ocurre durante la hipoxia), algunos de los
canales rpidos de Na+estarn en un estado inactivo, insensibles a la apertura, causando una respuesta menor a la excitacin de la membrana celular, y una V max menor. Por esta razn, si el potencial de reposo de la membrana deviene demasiado positivo, la clula puede ser no excitable, y la conduccin a travs del corazn puede retrasarse, incrementando el riesgo de arritmias.
Fase 1[editar editar cdigo]
La fase 1 del PA tiene lugar con la inactivacin de los canales rpidos de sodio. La corriente transitoria hacia el exterior que causa la pequea repolarizacin ("notch") del PA es debida al movimiento de los iones K+ y Cl-, dirigidos por las corrientes transient outward Ito1 y Ito2, respectivamente. La corriente Ito1 contribuye particularmente a la depresin de algunos PA de los cardiomiocitos ventriculares. Se ha sugerido que el movimiento de iones Cl- a travs de la membrana durante la fase 1 es el resultado del cambio en el potencial de membrana, debido a la salida de los iones K +, y no es un factor que contribuya a la despolarizacin inicial ("notch").
Fase 2[editar editar cdigo]
La fase "plateau" del PA cardaco se mantiene por un equilibrio entre el movimiento hacia el interior del Ca2+ (ICa) a travs de los canales inicos para el calcio de tipo L (que se abren cuando el potencial de membrana alcanza -40mV) y el movimiento hacia el exterior del K+ a travs de los canales lentos de potasio slow delayed rectifier, IKs. La corriente debida al intercambiador sodio-calcio (INa,Ca) y la corriente generada por la bomba Na-K (INa,K) tambin juegan papeles menores durante la fase 2.
Fase 3[editar editar cdigo]
Durante la fase 3 (la fase de "repolarizacin rpida") del PA, los canales voltaje-dependientes para el calcio de tipo L se cierran, mientras que los canales lentos de potasio slow delayed rectifier(IKs) permanecen abiertos. Esto asegura una corriente hacia fuera, que corresponde al cambio negativo en el potencial de membrana, que permite que ms tipos de canales para el K+ se abran. Estos son principalmente los canales rpidos para el K + rapid delayed rectifier (IKr) y los canales de K+ inwardly rectifying (IK1). Esta corriente neta positiva hacia fuera (igual a la prdida de cargas positivas por la clula) causa la repolarizacin celular. Los canales de K+ delayed rectifier se cierran cuando el potencial de membrana recupera un valor de -80 a -85 mV, mientras que IK1permanece funcionando a travs de la fase 4, contribuyendo a mantener el potencial de membrana de reposo.
Fase 4[editar editar cdigo]
La fase 4 es el potencial de reposo de la membrana. La clula permanece en este periodo hasta que es activada por un estmulo elctrico, que proviene normalmente una clula adyacente. Esta fase del PA es asociada con la distole de la cmara del corazn.
Al potencial de reposo de la membrana, la conductancia para el potasio (gK+) es alta en relacin a las conductancias para el sodio (gNa+) y el calcio (gCa2+). En esta fase, la gK+ se mantiene a travs de los canales para el K+ de tipo inward rectifying (IK1). Cuando el potencial de membrana pasa de -90 mV a -70 mV (debido, por ejemplo, al estmulo de una clula adyacente) se inicia la fase siguiente. Durante las fases 0, 1, 2 y parte de la 3, la clula es refractaria a la iniciacin de un nuevo PA: es incapaz de despolarizarse. Este es el denominado periodo refractario efectivo. Durante este periodo, la clula no puede iniciar un nuevo PA porque los canales estn inactivos. Este es un mecanismo de proteccin, que limita la frecuencia de los potenciales de accin que puede generar el corazn. Esto permite al corazn tener el tiempo necesario para llenarse y expulsar la sangre. El largo periodo refractario tambin evita que el corazn realice contracciones sostenidas, de tipo tetnico, como ocurre en el msculo esqueltico. Al final del periodo refractario efectivo, hay un periodo refractario relativo, en el cual es necesaria una despolarizacin por encima del umbral para desencadenar un PA. En este caso, como no todos los canales para el sodio estn en conformacin de reposo, los PA generados durante el periodo refractario relativo tienen una pendiente menor y una amplitud menor. Cuando todos los canales para el sodio estn en conformacin de reposo, la clula deviene completamente activable, y puede generar un PA normal.
Automatismo cardaco[editar editar cdigo]
En el miocardio, el automatismo es la capacidad de los msculos cardacos de despolarizarse espontneamente, es decir, sin estimulacin elctrica externa a partir del sistema nervioso. Estadespolarizacin espontnea se debe a que las membranas plasmticas de las clulas cardacas tienen una permeabilidad reducida para el K+, pero permiten el transporte pasivo de iones calcio, lo que permite que se genere una carga neta. El automatismo se demuestra sobre todo en el nodo sinusal, el denominado "marcapasos del corazn". Anormalidades en el automatismo generan cambios en el ritmo cardaco.
Localizacin de las clulas marcapasos[editar editar cdigo]
Las clulas que pueden realizar una despolarizacin espontnea ms rpidamente son las clulas del marcapasos primario del corazn, localizado en el nodo sinusal, que definen el ritmo cardaco. La actividad elctrica que se origina en el nodo sinusal se propaga al resto del corazn. La conduccin ms rpida de la actividad elctrica se produce a travs del sistema de conduccin elctrica del corazn. En el corazn existen otras clulas con capacidad marcapasos, en el nodo atrioventricular (AV) y en el sistema de conduccin ventricular, pero sus tasas de latido son menores que la tasa del nodo sinusal, por lo que su actividad marcapasos est normalmente suprimida. Si el nodo sinusal se inactiva, o sus potenciales de accin disminuyen por debajo de la tasa de los
marcapasos secundarios, la supresin de stos se elimina, lo que permite que los marcapasos secundarios se conviertan en el marcapasos del corazn. Cuando sto ocurre, se dice que aparece un marcapasos "ectpico".
Canales inicos marcapasos[editar editar cdigo]
El mecanismo de automatismo del corazn implica los canales denominados canales marcapasos de la familia HCN, activados por hiperpolarizacin, dependientes de nucletidos cclicos: el AMP cclico (AMPc) se une directamente a estos canales y aumenta la probabilidad de que se abran (vase Funny current).2 Estos canales poco selectivos para cationes conducen ms corriente a medida que el potencial de membrana se hace ms negativo, o hiperpolarizado. Conducen tanto iones potasio como sodio. La actividad de estos canales en el nodo sinusal causa que el potencial de membrana se haga lentamente ms positivo (despolarizado), hasta que, en un momento dado, los canales para el calcio se activan y se inicia un PA. La dependencia de AMPc de los canales If es una propiedad fisiolgica particularmente importante, ya que la activacin del sistema simptico aumenta los niveles de AMPc, produciendo la activacin de los canales If a voltajes ms positivos. Este mecanismo produce un incremento de la corriente a voltajes diastlicos, y por tanto una aceleracin del ritmo cardaco. La activacin del sistema parasimptico (que reduce los niveles de AMPc) disminuye los latidos cardacos por la accin opuesta, es decir, modificando la activacin de los canales If a potenciales ms negativos (hiperpolarizados). Debido a su importancia en la generacin de la actividad marcapasos del corazn y en la modificacin de la frecuencia espontnea, los canales f son dianas naturales de drogas dirigidas a controlar farmacolgicamente el ritmo cardaco. Algunos agentes, denominados "agentes reductores de la frecuencia cardaca" actan inhibiendo especficamente los canales f.3 Ivabradine es el inhibidor de los canales f ms especfico y selectivo, y el nico comercializado para el tratamiento farmacolgico de la angina de pecho estable crnica con un ritmo sinusal normal e intolerancia a los -bloqueadores.
Variaciones del automatismo[editar editar cdigo]
La actividad intrnseca de las clulas del marcapasos del corazn es la despolarizacin espontnea a un ritmo regular, generando el latido normal del corazn, que puede variar entre 100 a 110 despolarizaciones por minuto. El latido cardaco, sin embargo, puede variar entre 60 y 200 latidos por minuto. Estas variaciones se deben sobre todo a la accin del sistema nervioso autnomo sobre el nodo sinusal:
En condiciones de reposo, domina la influencia del sistema parasimptico, a travs del nervio vago, generando lo que se denomina tono vagal: el ritmo del nodo sinusal se reduce, mantenindolo alrededor de 70 latidos por minuto (cronotropa negativa).
El sistema autnomo aumenta el ritmo cardaco disminuyendo el tono vagal y simultneamente aumentando la accin del sistema simptico sobre el nodo sinusal. Este efecto se denominacronotropa positiva. El efecto del sistema simptico se realiza a travs de la accin del AMPc: el neurotransmisor de los nervios simpticos (noradrenalina) se une a los receptores -adrenrgicos en la membrana celular, lo cual activa una cascada de sealizacin que produce un aumento en los niveles de AMPc. Esto produce un aumento de la apertura de los canales de calcio tipo L y de los canales f, lo cual genera un aumento de la tasa de despolarizacin, y por tanto un aumento del ritmo cardaco (taquicardia).
El sistema parasimptico libera el neurotransmisor acetilcolina, que se une a sus receptores y produce una disminucin del AMPc y por tanto el efecto contrario (bradicardia). Existen otros mecanismos no neuronales que pueden modificar la actividad marcapasos:
las catecolaminas circulantes (adrenalina y noradrenalina) producen un aumento de la frecuencia cardaca, por un mecanismo similar al descrito para el sistema simptico;
el hipertiroidismo produce taquicardia, ya que aumenta el metabolismo celular, aumentan los niveles de ATP y eso induce un aumento de la actividad de la bomba sodio-potasio, lo que produce una mayor rapidez en la corriente del sodio (y viceversa para el hipotiroidismo);
la hiperpotasemia causa taquicardia, ya que al aumentar la concentracin exterior de potasio, disminuye la conductancia al potasio y aumenta la tasa de despolarizacin;
la hipoxia celular causa una carencia de ATP que disminuye la actividad de la bomba sodiopotasio, lo que despolariza la membrana y causa taquicardia, pudiendo abolir la actividad del marcapasos (lo que ocurre en caso de isquemia coronaria).
Un automatismo anormal implica la despolarizacin espontnea anormal de las clulas del corazn. Tpicamente esto causa arritmias (ritmos irregulares) en el corazn. Algunas drogas que se utilizan para tratar arritmias tambin afectan a la actividad del nodo sinusal:
los bloqueadores de los canales de calcio generan bradicardia, porque inhiben los canales tipo L durante la fase 4 y fase 0;
drogas que afectan al sistema nervioso autnomo (como los -bloqueadores) afectan la actividad del nodo sinusal;
la digitalis causa bradicardia, ya que aumenta la actividad parasimptica y bloquea la bomba sodio-potasio, necesaria para la despolarizacin.
En casos en los que se produce un bloqueo cardaco, en el que la actividad del marcapasos primario no se propaga al resto del corazn, el nodo atrioventricular (AV) tomar el relevo, generando una despolarizacin espontnea y creando un PA.
Por razones mal conocidas, a veces clulas no-marcapasos pueden realizar despolarizaciones espontneas, bien durante fase 3 o en fase 4 temprana, generando PA anormales, denominadospost-despolarizaciones, que si tienen suficiente magnitud pueden producir taquicardia.
las post-despolarizaciones tempranas (early afterdepolarizations) ocurren durante fase 3; las post-despolarizaciones tardas (late afterdepolarizations) ocurren en fase 4 temprana.
Ambos casos parecen estar relacionados con un aumento en las concentraciones intracelulares de calcio, como ocurre en la isquemia, en la intoxicacin con digitalis o en la hiperestimulacin con catecolaminas.
Potrebbero piacerti anche
- Potencial de Accion CardiacoDocumento8 paginePotencial de Accion CardiacoAngelo Anaya CaponeNessuna valutazione finora
- Bases Iónicas Del Automatismo CardiacoDocumento28 pagineBases Iónicas Del Automatismo CardiacoAbigail AlvarezNessuna valutazione finora
- MIS OBJETIVOS Propiedades Electrofisiológicas Del Miocardio Contráctil y EspecializadoDocumento4 pagineMIS OBJETIVOS Propiedades Electrofisiológicas Del Miocardio Contráctil y EspecializadoPIKANessuna valutazione finora
- Fisiología Cardiovascular Electrocardiografía N°4 PDFDocumento22 pagineFisiología Cardiovascular Electrocardiografía N°4 PDFKevin Argotti CazarNessuna valutazione finora
- Fisiologia CardiacaDocumento11 pagineFisiologia CardiacaCarol IsidroNessuna valutazione finora
- Fisiología de La Célula CardíacaDocumento3 pagineFisiología de La Célula CardíacaAnahi JimenezNessuna valutazione finora
- Secme-4237 1Documento11 pagineSecme-4237 1JoséNessuna valutazione finora
- Nueva Guia AntiarritmicosDocumento12 pagineNueva Guia AntiarritmicosPaulina ArteagaNessuna valutazione finora
- Clase 1Documento74 pagineClase 1CinthiaFuenmayorVarelaNessuna valutazione finora
- Fisiología - Guía # 1. Actividad Electrica Cardiaca 2023-2Documento10 pagineFisiología - Guía # 1. Actividad Electrica Cardiaca 2023-2LAURA SOFIA PEREZ CUELLONessuna valutazione finora
- Actividades Electricas de Las MembranasDocumento18 pagineActividades Electricas de Las MembranasJunior Mejía PonceNessuna valutazione finora
- Electrofisiología Del Miocito VentricularDocumento4 pagineElectrofisiología Del Miocito VentricularUSMP FN ARCHIVOSNessuna valutazione finora
- Practica Potencial de Acción CardiacoDocumento9 paginePractica Potencial de Acción CardiacoXavi MGNessuna valutazione finora
- Clase 3 - PA CardíacoDocumento39 pagineClase 3 - PA Cardíacomartii17Nessuna valutazione finora
- Potencial de Acción Del Musculo EsqueléticoDocumento5 paginePotencial de Acción Del Musculo EsqueléticoLisset Gzc80% (5)
- Potencial de Acción de Las Células MiocárdicasDocumento2 paginePotencial de Acción de Las Células MiocárdicasRoberto TreviñoNessuna valutazione finora
- Cap - 9 (Musculo Cardiaco El Corazon)Documento85 pagineCap - 9 (Musculo Cardiaco El Corazon)JONATHAN ARIEL LUNA JIMENEZNessuna valutazione finora
- Electrofisiologia Cardiaca CMDM PDFDocumento10 pagineElectrofisiologia Cardiaca CMDM PDFWendy OrtizNessuna valutazione finora
- Clase 3 4-10Documento4 pagineClase 3 4-10Valentina UbillaNessuna valutazione finora
- Tema 3: Bloqueantes de Los Canales de Calcio: IntroducciónDocumento12 pagineTema 3: Bloqueantes de Los Canales de Calcio: IntroducciónRafa RiveraNessuna valutazione finora
- FisiologiaDocumento11 pagineFisiologiaMarjorie PérezNessuna valutazione finora
- Control de La Función CardiovascularDocumento10 pagineControl de La Función CardiovascularMartin Ojeda CarpioNessuna valutazione finora
- Teoria Delm Musculo CardiacoDocumento12 pagineTeoria Delm Musculo CardiacoAlbert KantNessuna valutazione finora
- Potencial de Acción de Las Células MiocárdicasDocumento1 paginaPotencial de Acción de Las Células Miocárdicasyeniffer mena palaciosNessuna valutazione finora
- Canales Ionicos Regulados Por VoltajeDocumento24 pagineCanales Ionicos Regulados Por VoltajeAlex Madera100% (1)
- Potencial de Acción de Las Células Del Músculo CardíacoDocumento2 paginePotencial de Acción de Las Células Del Músculo CardíacoAlanRodriguezMiñanoNessuna valutazione finora
- Potencial de AcciónDocumento5 paginePotencial de AcciónJose Cisneros0% (1)
- Preguntero Con Respuestas - CompletoDocumento55 paginePreguntero Con Respuestas - CompletoFranciscoMolinaNessuna valutazione finora
- UABP 2. Músculo Cardíaco y Ciclo CardíacoDocumento22 pagineUABP 2. Músculo Cardíaco y Ciclo CardíacoMartín PanicoNessuna valutazione finora
- Preguntas Del Pase de VisitaDocumento7 paginePreguntas Del Pase de VisitaIvet SuarezNessuna valutazione finora
- Fisiologia Cardiovascular Propiedades Del Miocito CardiacoDocumento45 pagineFisiologia Cardiovascular Propiedades Del Miocito CardiacoAlex Yvan Escobedo Hinostroza100% (3)
- Apunte de Farmaco CardiacoDocumento11 pagineApunte de Farmaco CardiacoEstefanía MansillaNessuna valutazione finora
- Fisiologia CardiovascularDocumento59 pagineFisiologia Cardiovascularfrank valdiviesoNessuna valutazione finora
- Fisiologia Cardiaca 1Documento93 pagineFisiologia Cardiaca 1soborno5656Nessuna valutazione finora
- Potencial de AcciónDocumento25 paginePotencial de Acciónviridiana coronaNessuna valutazione finora
- 16 Potencial de AcciónDocumento8 pagine16 Potencial de AcciónAnaNessuna valutazione finora
- Origen y Propagación 2Documento9 pagineOrigen y Propagación 2Gabriela GregórioNessuna valutazione finora
- CUESTIONARIO Tema 18Documento4 pagineCUESTIONARIO Tema 18Nicole AlejandraNessuna valutazione finora
- Anti ArritmicosDocumento23 pagineAnti ArritmicosMoronta Ortiz Hector ManuelNessuna valutazione finora
- Canales de CaDocumento14 pagineCanales de CaMiguel MendozaNessuna valutazione finora
- Revisión de Las Arritmias: Manual MSD Versión para ProfesionalesDocumento11 pagineRevisión de Las Arritmias: Manual MSD Versión para Profesionalesapi-664596295Nessuna valutazione finora
- Farmacologia 5Documento22 pagineFarmacologia 5BLAZE CANTNessuna valutazione finora
- Electrofisiología CardiacaDocumento34 pagineElectrofisiología Cardiacagalvis.hardyNessuna valutazione finora
- ArritmiasDocumento17 pagineArritmiasCamilo MontesNessuna valutazione finora
- Fisiologia Cardiovascular y HemodinamiaDocumento51 pagineFisiologia Cardiovascular y HemodinamiaRaquel VBNessuna valutazione finora
- Potencial de Acción - Wikipedia, La Enciclopedia LibreDocumento55 paginePotencial de Acción - Wikipedia, La Enciclopedia LibreCristobal Isaac Arthieedd Vera PalaciosNessuna valutazione finora
- Capitulo 2 Electrofisiologia CelularDocumento6 pagineCapitulo 2 Electrofisiologia CelularÁlvaro RuedaNessuna valutazione finora
- Taller de Arritmias CardiacasDocumento26 pagineTaller de Arritmias CardiacasAbisaid Jonathan Salinas MemijeNessuna valutazione finora
- Antagonistas Del Calcio en La Hipertensión ArterialDocumento22 pagineAntagonistas Del Calcio en La Hipertensión ArterialedisonNessuna valutazione finora
- 5-AQMED2014 Verano Fisio1Documento62 pagine5-AQMED2014 Verano Fisio1Jover Leonel MamaniNessuna valutazione finora
- Corrientes IonicasDocumento6 pagineCorrientes Ionicasoscar olivasNessuna valutazione finora
- El Ion CalcioDocumento19 pagineEl Ion CalcioLiz M VillaVqzNessuna valutazione finora
- (Estefany) Propiedades Electrofisiológicas Del Miocardio Contráctil y EspecializadoDocumento19 pagine(Estefany) Propiedades Electrofisiológicas Del Miocardio Contráctil y EspecializadoPIKANessuna valutazione finora
- Antagonistas de Canales de CalcioDocumento5 pagineAntagonistas de Canales de CalcioJose ShareNessuna valutazione finora
- Apuntes Biofisica Musculo CardiacoDocumento33 pagineApuntes Biofisica Musculo CardiacoCamila NievesNessuna valutazione finora
- CARDIO - Bases Biofísicas de La Actividad Cardiaca y Músculo Liso Vascular Con Proyección A Bases FisiopatológicasDocumento28 pagineCARDIO - Bases Biofísicas de La Actividad Cardiaca y Músculo Liso Vascular Con Proyección A Bases FisiopatológicasRomina NogueiraNessuna valutazione finora
- GUÍA DE PRACTICA 3 Efecto de Los Iones Sobre La Frecuencia CardíacaDocumento4 pagineGUÍA DE PRACTICA 3 Efecto de Los Iones Sobre La Frecuencia CardíacaArely Mical SánchezNessuna valutazione finora
- 2 Electrofisiología CardíacaDocumento6 pagine2 Electrofisiología CardíacaJhon NicolNessuna valutazione finora
- Caso 3 - Casos Integradores IIIDocumento6 pagineCaso 3 - Casos Integradores IIIAbish BreslinNessuna valutazione finora
- Castellano - Electrocardiografía Clínica, 2da Ed, 2004Documento299 pagineCastellano - Electrocardiografía Clínica, 2da Ed, 2004Marcos Miguel Huaco Romero100% (1)
- Nemotecnias PDFDocumento50 pagineNemotecnias PDFMarcos Miguel Huaco RomeroNessuna valutazione finora
- La Salud Publica Tiene Un Carácter Social e HistóricoDocumento1 paginaLa Salud Publica Tiene Un Carácter Social e HistóricoMarcos Miguel Huaco RomeroNessuna valutazione finora
- 2Documento35 pagine2Marcos Miguel Huaco RomeroNessuna valutazione finora
- Choque Cardiogenico 2011Documento77 pagineChoque Cardiogenico 2011Scott SummersNessuna valutazione finora
- Contol Inteno de Las Entidades HopitalariaDocumento40 pagineContol Inteno de Las Entidades HopitalariaMarcos Miguel Huaco RomeroNessuna valutazione finora
- Utilidades de Bacterias en Ing GeneDocumento1 paginaUtilidades de Bacterias en Ing GeneMarcos Miguel Huaco RomeroNessuna valutazione finora
- Economia 2Documento2 pagineEconomia 2Marcos Miguel Huaco RomeroNessuna valutazione finora
- Cateter SubclavioDocumento8 pagineCateter SubclavioCoquito Bonita CarrilloNessuna valutazione finora
- Sendero LuminosoDocumento21 pagineSendero LuminosoMarcos Miguel Huaco Romero0% (1)
- Sesión SAMU SHOCKDocumento29 pagineSesión SAMU SHOCKMarcos Miguel Huaco RomeroNessuna valutazione finora
- DiureticosDocumento7 pagineDiureticosMarcos Miguel Huaco RomeroNessuna valutazione finora
- Resumen de Conceptos Sobre Promocion y Proteccion de La SaludDocumento5 pagineResumen de Conceptos Sobre Promocion y Proteccion de La SaludMarcos Miguel Huaco RomeroNessuna valutazione finora
- Carta de Ottawa para La Promoción de La SaludDocumento4 pagineCarta de Ottawa para La Promoción de La Saludapi-318484644Nessuna valutazione finora
- 4 Tema Trastornos AlimenticiosDocumento31 pagine4 Tema Trastornos AlimenticiosTito Ramon Maceda BaldiviezoNessuna valutazione finora
- Lección Complejo de GolgiDocumento11 pagineLección Complejo de GolgiMPaz VelaNessuna valutazione finora
- Gerencia EstrategicaDocumento13 pagineGerencia EstrategicaHarold Cardenas TovarNessuna valutazione finora
- Algebra de BloquesDocumento8 pagineAlgebra de Bloqueslcrodriguaz100% (5)
- Influencia Del Numero de Reynolds en La CoeficientDocumento13 pagineInfluencia Del Numero de Reynolds en La CoeficientCarlos RamírezNessuna valutazione finora
- Proyectos Escolares 2017Documento15 pagineProyectos Escolares 2017Marco GarciaNessuna valutazione finora
- Catálogo de Correas para Techos Metálicos.Documento2 pagineCatálogo de Correas para Techos Metálicos.Kenyito2406Nessuna valutazione finora
- 1234 y Lo Que Siga Que No Se EntiendeDocumento28 pagine1234 y Lo Que Siga Que No Se EntiendeXiomi Rosas Rojas100% (2)
- Herrajes CaballosDocumento28 pagineHerrajes CaballosCarlos Xavier Rodriguez100% (1)
- 4CN U02 RefuerzoDocumento8 pagine4CN U02 Refuerzoapotorrent-7Nessuna valutazione finora
- Economía Circular VFDocumento26 pagineEconomía Circular VFAtenas Tutorias EducativasNessuna valutazione finora
- FNP FisioyKine CdemDocumento7 pagineFNP FisioyKine CdemLilian FloresNessuna valutazione finora
- Vigas EjerciciosDocumento11 pagineVigas EjerciciosMarysol RivasNessuna valutazione finora
- Traduccion Norma ASTM C-117-17Documento8 pagineTraduccion Norma ASTM C-117-17Jose Miguel Zuñiga PicadoNessuna valutazione finora
- ElectroimanDocumento4 pagineElectroimanEsthepany Santiago Soria100% (1)
- PastorelaDocumento13 paginePastorelaLourdes CastroNessuna valutazione finora
- Rosco Literario de Figuras Literarias Entre Otras Cosas.Documento3 pagineRosco Literario de Figuras Literarias Entre Otras Cosas.luis correaNessuna valutazione finora
- Numeros Combinatorios (Concepto de Orden)Documento12 pagineNumeros Combinatorios (Concepto de Orden)juan patricio ondo ona ayetebeNessuna valutazione finora
- Mecancia D FluidosDocumento382 pagineMecancia D FluidosgabrielNessuna valutazione finora
- Material de Apoyo Unidad Dos SemanaDocumento21 pagineMaterial de Apoyo Unidad Dos Semanahenry glidvan forbes dubonNessuna valutazione finora
- Examen Entrada QUIÑONES 2019Documento8 pagineExamen Entrada QUIÑONES 2019Alex FasabiNessuna valutazione finora
- Morfología de LeguminosasDocumento52 pagineMorfología de LeguminosasMagnolia TrejoNessuna valutazione finora
- Teoria-Iv Bimestre PDFDocumento28 pagineTeoria-Iv Bimestre PDFjoseph0% (1)
- Actividades 5, 6 y 7 de NoviembreDocumento24 pagineActividades 5, 6 y 7 de NoviembreEnrry SantistebanNessuna valutazione finora
- Modelos y PredicciónDocumento9 pagineModelos y PredicciónCarlos MartinezNessuna valutazione finora
- Cadena de Valor AM StarbucksDocumento1 paginaCadena de Valor AM Starbucksanyela martinez treviñosNessuna valutazione finora
- Humedal Puerto ViejoDocumento4 pagineHumedal Puerto ViejoMarco Cañari FloresNessuna valutazione finora
- 05.max Weber y La EducaciónDocumento11 pagine05.max Weber y La EducaciónAlejandro Esquivel100% (1)
- Anatomia Humana 2017Documento17 pagineAnatomia Humana 2017MARIA JULIA GARCIA PAZNessuna valutazione finora
- Factorización de PolinomiosDocumento5 pagineFactorización de PolinomiosDaikerlysNessuna valutazione finora