Documenti di Didattica
Documenti di Professioni
Documenti di Cultura
FINAL Práctica 1 - FRAGILIDAD OSMÓTICA DEL ERITROCITO
Caricato da
Cesar Toribio GamuzoCopyright
Formati disponibili
Condividi questo documento
Condividi o incorpora il documento
Hai trovato utile questo documento?
Questo contenuto è inappropriato?
Segnala questo documentoCopyright:
Formati disponibili
FINAL Práctica 1 - FRAGILIDAD OSMÓTICA DEL ERITROCITO
Caricato da
Cesar Toribio GamuzoCopyright:
Formati disponibili
UNIVERSIDAD NACIONAL FEDERICO VILLARREAL Facultad de Ciencias Naturales y Matemticas Escuela Profesional de Biologa
PRACTICA N1 FRAGILIDAD OSMOTICA DEL ERITROCITO
Docente: Blga. Rossalyn Acua Payano Estudiantes: Hidalgo Venegas, Carlos. Toribio Gamuzo, Csar. Vsquez Domnguez, Andrs. Grupo: Grupo E Viernes 16:20 18:00
2013
FRAGILIDAD OSMTICA DEL ERITROCITO
I. INTRODUCCIN La osmosis es un tipo especial de transporte pasivo en el cual slo las molculas de agua son transportadas a travs de la membrana. El movimiento de agua se realiza desde un punto en que hay mayor concentracin a uno de menor para igualar concentraciones. De acuerdo al medio en que se encuentre una clula, la osmosis vara. La funcin de la osmosis es mantener hidratada a la membrana celular. Dicho proceso no requiere gasto de energa. En otras palabras, la osmosis es un fenmeno consistente en el paso del solvente de una disolucin desde una zona de baja concentracin de soluto a una de alta concentracin de soluto, separadas por una membrana semipermeable. La membrana celular constituye una interfase entre el compartimento intra y extracelular que permite el libre recambio de molculas de agua, establecindose un gradiente osmtico. La membrana celular de los eritrocitos es flexible, pero prcticamente carece de elasticidad, lo que significa que la clula se rompe si le entra agua hasta exceder un volumen crtico. Cuando la clula enfrenta un ambiente hipotnico se genera un movimiento neto de agua libre hacia su interior. Segn el grado de hipotonicidad y la capacidad de la membrana para mantener su integridad, la clula se hincha y estalla permitiendo, en el caso de los eritrocitos, la salida de hemoglobina. Esta propiedad es utilizada en la prueba de la fragilidad osmtica eritrocitaria (FOE), que consiste en exponer alcuotas de eritrocitos a concentraciones decrecientes de NaCl, usualmente entre 0,85% y 0%, y luego cuantificar el grado de hemlisis en cada una de ellas. Por lo tanto, la FOE permite evaluar la resistencia y estabilidad de la membrana del eritrocito frente a un estrs osmtico. La ruptura de la membrana celular produce la salida del contenido de hemoglobina, por lo que se puede medir la ruptura de los eritrocitos midiendo y cuantificando la cantidad de hemoglobina liberada al medio mediante tcnicas espectrofotomtricas.
La fragilidad osmtica del eritrocito depende de caractersticas como la edad del eritrocito, su tamao, forma y las dems condiciones propias de la estructura interna de la clula. Como se emplea una poblacin de millones de clulas, la fragilidad osmtica sigue la distribucin de una curva normal. El objetivo de esta prctica, es conocer la fragilidad osmtica de los eritrocitos frente a diferentes efectos fsicos y qumicos; como la temperatura y el pH; en concentraciones decrecientes de NaCl. II. MARCO TERICO Eritrocitos Los eritrocitos son clulas sanguneas anucleadas que miden aproximadamente 8 m de dimetro (as, unos 3000 eritrocitos en fila ocupan 2,5 cm de longitud) y tienen forma de disco bicncavo. La membrana del eritrocito en un complejo de lpidos y protenas (bicapa lipdica), el cual es importante para mantener la elasticidad celular y la permeabilidad selectiva. Los eritrocitos pueden deformarse, sin llegar a lesionarse para poder pasar por los ms estrechos capilares. Este grado de deformidad o elasticidad influye en la rapidez del flujo sanguneo por la microcirculacin. Los eritrocitos son los elementos celulares ms abundantes de la sangre. En el varn adulto existen alrededor de 5.500.000 por cc de sangre, y en las mujeres unos 4.800.000 por cc. Un eritrocito contiene 200 a 300 millones de molculas de Hemoglobina (Hb). La Hb consiste en la combinacin de una molcula proteica de globina, con cuatro molculas de un compuesto pigmentado llamado grupo hemo. Cada molcula de hemo posee un tomo de hierro en su centro (Fe2+), por lo que, una molcula de Hb puede transportar hasta cuatro molculas de oxgeno y formar oxihemoglobina por medio de una reaccin reversible. La Hb tambin puede combinarse con dixido de carbono para formar carboxihemoglobina, tambin por una reaccin reversible. El CO2 se une a la porcin globina de la molcula de Hb. En un varn adulto normal, 100 cc de sangre contienen 14 a 16 g de Hb; la sangre de una mujer contiene de 12 a 14 g de Hb por 100 cc. El proceso de formacin de eritrocitos se denomina eritropoyesis. La vida promedio de un eritrocito circulante en el torrente circulatorio es de unos 120 das. Se fragmentan en los capilares y son fagocitados
por las clulas retculo-endoteliales de la cubierta de los vasos sanguneos en hgado, bazo y mdula sea. En condiciones fisiolgicas, los eritrocitos se encuentran en equilibrio osmtico con la sangre que los contiene (valor de osmolaridad del plasma sanguneo: 290 10 mOsm/L), por lo cual se dice que la sangre es una solucin isosmtica e isotnica. Si la osmolaridad del plasma llega a disminuir significativamente (plasma hipotnico), el agua como lquido, entra al interior celular aumentando su volumen. Si por el contrario, la osmolaridad del plasma se incrementa, este se torna hipertnico y el agua sale del eritrocito ocurriendo una reduccin del volumen celular. La forma y el volumen de los eritrocitos cambian cuando vara la cantidad de agua contenida en su interior, pudiendo tomar una forma estrellada o irregular al ocurrir prdida de volumen (fenmeno de crenacin) o bien aumentar su volumen hasta adquirir la forma de una esfera. Cuando la clula no puede resistir la carga de agua que recibe, la membrana se rompe (fenmeno de hemlisis) y se libera la hemoglobina la cual puede ser cuantificada por mtodos espectrofotomtricos. La hemlisis es un proceso que ocurre en una poblacin mixta de clulas por lo que no ocurre en un solo punto y a la misma velocidad en todos los casos. Como el efecto final es un tanto difcil de apreciar experimentalmente, debido a que la hemlisis ocurre en forma que se hace asinttica al 100 % (curva aplanada), se prefiere analizar el tiempo de hemlisis al alcanzar el 50%. Membrana del Glbulo Rojo La membrana del glbulo rojo es la responsable de las propiedades mecnicas y de la mayora de las funciones fisiolgicas de la clula. Est formada por una bicapa lipdica plana, donde predominan en el 80 % los fosfolpidos y el colesterol y en menor medida los glicolpidos y aminofosfolpidos, distribuidos asimtricamente. De igual forma, se encuentran embebidas parcial o totalmente en ella las protenas integrales de membrana, unidas fuertemente por enlaces apolares. Su libre desplazamiento a travs de esta bicapa contribuye a mantener su fluidez. Las protenas perifricas interactan entre s para formar una malla o enrejado que recubre la cara interior de la doble capa de fosfolpidos y son las responsables de la estabilidad y las propiedades viscoelsticas de la membrana. Entre estas protenas se destacan la espectrina (Sp), la ankirina (banda 2.1, 2.2, 2.3 y 2.6), la banda 4.1, la banda 4.2, la banda 4.9, la aducina, la
tropomiosina y la banda 7. Otras protenas perifricas se disponen hacia la cara exterior de la bicapa lipdica y ellas son fundamentalmente antgenos de grupo sanguneo (fig.1).
Fig. 1. Estructura de la membrana eritrocitaria. La banda 3 representa el 25 % del total de las protenas integrales. Est constituida por 2 dominios estructurales: el dominio citoplasmtico, que es el encargado de la unin con las protenas del esqueleto, y el sitio transmembranoso que mantiene el contacto con el medio extra e intracelular, proporcionando los canales responsables del transporte de iones bicarbonato (HCO3-) y cloruros (CI-). Adems, posee un sitio de glicosilacin capaz de unir antgenos para el grupo sanguneo I/i e interviene activamente en la eliminacin de eritrocitos envejecidos. Las glicoforinas son un grupo de protenas integrales caracterizadas por su elevado contenido en cido silico. Las glicoforinas A,B,C y D son las ms importantes y constituyen los sustratos antignicos de los diferentes grupos sanguneos. La glicoforina C contribuye a la estabilidad de la membrana gracias a su interaccin con protenas perifricas, adems de participar en el intercambio inico transmembranoso. La Sp es la protena ms abundante y adems la principal responsable del mantenimiento del enrejado proteico. Est compuesta por 2 subunidades a y b enrolladas de forma antiparalela, las que se unen por sus extremos para formar tetrmeros. Estas 2 subunidades estn constituidas por secuencias repetitivas de 106 aminocidos, las que se enlazan para formar una triple hlice (fig.2).
Fig.2. Estructura del tetrmero de espectrina (Sp). Se observa la triple hlice de las unidades repetitivas, los sitios de autoasociacin de la Sp y los sitios de nucleacin donde comienza la interaccin lateral entre las cadenas a y b de la Sp. La ankirina (ANK) est compuesta por 3 subunidades estructurales correspondientes a 3 dominios funcionalmente diferentes: regulador, de unin a la membrana y de unin a la Sp. Su contribucin a la integridad de la membrana es decisiva, ya que constituye un importante punto de anclaje a la doble capa lipdica a travs de la banda 3.1 La actina es una protena organizada en forma de protofilamentos helicoidales estabilizados por la interaccin con la Sp, la protena 4.1 y la tropomiosina. Otra de las protenas que integran el citoesqueleto es la protena 4.1, cuya funcin fundamental es estabilizar la unin espectrina-actina y contribuir a fijar el esqueleto a la bicapa lipdica. El mantenimiento de la forma y estabilidad de la tambin responsabilidad de otras protenas. Entre protena 4.2, que acta como modulador para interaccin ankirina-banda 3. La banda 4.9, la tropomiosina, protegen la estabilidad de la actina. membrana ellas est estabilizar aducina y es la la la
III.
MATERIALES: Tubos de ensayo. Rejilla. Estufa para Bao Mara. Termmetro. Micropipeta y Propipeta. Pipetas graduadas. Agua destilada. Solucin salnica amortiguadora (fosfato salino) a pH 7,4 de NaCl al 1% Solucin anticoagulante de ethylen diamine tetra-actico 0,1% Buffer a pH 5,6; 7,4 y 8,9. Muestra Biolgica: Sangre de Caballo.
IV.
METODOLOGA:
Experimento N1: Fragilidad Osmtica Para cada muestra sangunea realizar el siguiente esquema de evaluacin:
Reactivos Concentracin de NaCl % Sol. Fosfato salino (NaCl 1%) pH 7,4 mL Agua destilada mL Sangre total con EDTA mL. 1 0,00 0,00 1 0,01 2 0,10 0,1 0,9 0,01 3 0,35 0,35 0,65 0,01 4 0,45 0,45 0,55 0,01 5 0,5 0,5 0,5 0,01 6 0,55 0,55 0,45 0,01 7 0,6 0,6 0,4 0,01 8 0,7 0,7 0,3 0,01 9 0,85 0,85 0,15 0,01
Mezclar suavemente y dejar reposar a temperatura ambiente 30 minutos. Mezclar y centrifugar a 2000rpm/ 5 min. Leer en espectrofotmetro a 530 nm usando el tubo 9 como blanco (0% de hemlisis). Haga una grfica de los valores de hemlisis en % contra la concentracin de NaCl.
Experimento N2: Efecto de la temperatura sobre la fragilidad osmtica
Reactivos Concentracin de NaCl % Sol. Fosfato salino (NaCl 1%) pH 7,4 mL Agua destilada mL Sangre total con EDTA mL. Mezcla e incubar a C/30 min. 1 0,00 0,00 1 0,01 ambiente 2 0,85 0,85 0,15 0,01 Sobre hielo 3 0,85 0,85 0,15 0,01 ambiente 4 0,85 0,85 0,15 0,01 37 5 0,85 0,85 0,15 0,01 45
Mezclar y centrifugar a 2000rpm/ 5 min. Leer el sobrenadante en espectrofotmetro a 530 nm. Usar agua destilada como blanco. Expresar el resultado como el porcentaje de hemlisis a cada valor de temperatura de incubacin. Se calcula utilizando el valor de la absorbancia del sobrenadante del tubo donde ocurre la mxima hemlisis como el 100%.
Experimento N3: Efecto del pH sobre la fragilidad osmtica
Reactivos Concentracin de NaCl % pH Sol. Fosfato salino (NaCl 1%) mL Agua destilada mL Sangre total con EDTA mL. 1 0,00 2 0,85 5,6 0,00 1 0,01 4,25 0,15 0,01 3 0,85 7,4 4,25 0,15 0,01 4 0,85 8,9 4,25 0,15 0,01
Mezclar suavemente y dejar reposar a temperatura ambiente 30 minutos. Mezclar y centrifugar a 2000rpm/ 5 min. Leer el sobrenadante en espectrofotmetro a 530 nm. Usar agua destilada como blanco. Expresar el resultado como el porcentaje de hemlisis a cada valor de pH. Se calcula utilizando el valor de absorbancia del sobrenadante, del tubo donde ocurre la mxima hemlisis como el 100%.
V.
RESULTADOS Clculos Experimento N1: Fragilidad Osmtica
TUBO 1 2 3 4 5 6 7 8
ABSORBANCIA 0.737 0.715 0.541 0.462 0.251 0.211 0.152 0.065
Concentracion NaCl 0 0.1 0.35 0.45 0.5 0.55 0.6 0.7
% Hemlisis 100 97.01 73.41 62.69 34.06 28.63 20.62 8.82
9 0 0.85 0 Tabla 1.- Lectura de las absorbancias en el espectrofotmetro a 530nm
Experimento N1: Fragilidad Osmtica
120 100 80
%hemolisis
60 40 20 0 0 0.2 0.4 0.6 0.8 1 % Hemolisis
Concentracin de NaCl
Cuadro 1.- Grfico de la concentracin de NaCl respecto al porcentaje de hemolisis obtenido
Experimento N2: Efecto de la temperatura sobre la fragilidad osmtica TUBO 1 2 3 4 5 ABSORBANCIA 0.56 0.482 0.588 0.661 0.595 Efecto de T Ambiente (sin Sol. Salina) Hielo Ambiente (con Sol. Salina) 37 45 % Hemlisis 84.72 72.92 88.96 100 90.02
Tabla 2.- Lectura de las absorbancias en el espectrofotmetro a 530nm con relacin al efecto de temperatura y porcentaje de hemolisis.
Cuadro N 2: Experimento N 2: Efecto de la temperatura sobre la fragilidad osmtica; el porcentaje de hemlisis en relacin al efecto de la temperatura.
Experimento N3: Efecto del pH sobre la fragilidad osmtica TUBO 1 2 3 4 ABSORBANCIA 1 0.043 0.166 0.219 Efecto del pH 0 5.6 7.4 8.9 % Hemlisis ----------19.63 75.8 100
Tabla 3.- Lectura de las absorbancias en el espectrofotmetro a 530nm con relacin al efecto del pH y porcentaje de hemolisis.
Cuadro N 3: Efecto del pH sobre la fragilidad osmtica; el % de hemlisis en relacin al pH.
Cuestionario 1. Una solucin salina que es isotnica para eritrocitos es necesariamente isotnica para otro tipo de clulas? El paso del agua hacia dentro o fuera de las clulas es un proceso biolgico de importancia. Si las concentraciones mol/L de solutos en ambos lados de la membrana celular son las mismas, la presin osmtica es igual y las soluciones son isotnicas sin que haya paso neto de lquido en ningn sentido. Por lo tanto una solucin salina para eritrocitos o cualquier otra clula, es la misma. La concentracin de solutos en la sangre es isotnica con una solucin de 0,9% de cloruro de sodio. La concentracin de cloruro de sodio 0,85< 0,9%, se llama solucin salina normal o fisiolgica o suero fisiolgico. 2. Cules son las causas de la hipernatremia? El exceso de sodio en la sangre puede ser ocasionado por ciertas condiciones. Las causas especficas de la hipernatremia incluyen: Deshidratacin o prdida de fluidos corporales por vmitos prolongados, diarrea, sudoracin o fiebre alta. Deshidratacin por no beber la cantidad suficiente de agua. Frmacos tales como esteroides, regaliz y ciertos medicamentos para disminuir la presin sangunea. Ciertas enfermedades endocrinolgicas como diabetes (cuando la orina es muy frecuente) o aldosteronismo. Ingestin excesiva de sal. Hiperventilacin (respiracin demasiado rpida).
En todos los casos, la hipernatremia y por lo tanto la hipertonicidad plasmtica, induce la salida de agua del espacio celular al extracelular, lo que produce disminucin del volumen celular. La disminucin del volumen neuronal se manifiesta clnicamente por sntomas neurolgicos: letargia, reflejos hiperactivos, temblor muscular, convulsiones y coma. Con frecuencia, sobre todo en personas ancianas, se producen trombosis de los senos venosos craneales, y, al disminuir el tamao del cerebro, hemorragias cerebrales por traccin de las
estructuras vasculares. La salida del agua celular al espacio extracelular tiende a preservar la volemia, por lo que al principio no son aparentes los sntomas y signos de hipovolemia, que pueden aparecer, hasta la situacin de shock, en fases avanzadas. 3. Cmo se comportara el eritrocito en un estado de hipernatremia? Cuando sobreviene la hipernatremia, todas las clulas del organismo se reducen en tamao, que es proporcional al grado de reduccin del volumen celular; sin embargo, los mecanismos regulatorios internos permiten restaurar, en muchas clulas, su volumen casi normal. Los eritrocitos y las neuronas tienen esta habilidad para regular su volumen. Una vez que han pasado ms de 48 horas de hipernatremia; es decir, el inicio de considerarse crnica, tendr un volumen normal a expensas del contenido de solutos intracelular aumentado. En ese momento, rpidamente se restaura la osmolaridad que originar una hinchazn celular, lo que en la mayor parte de los rganos del cuerpo no tendr mayor consecuencia; sin embargo, en el cerebro es devastadora, pues aparecen: edema cerebral, herniacin y la muerte. De ah la importancia del tratamiento cauteloso en la hipernatremia crnica.
VI.
CONCLUSIONES A menor concentracin de NaCl se incrementa el porcentaje de hemolisis, debido a que ingresa agua al eritrocito liberando hemoglobina. La variacin del porcentaje de hemolisis influye directamente con la lectura de las absorbancias. En un ambiente salino se produce mayor cantidad de hemolisis comparado con un ambiente normal. La temperatura del hielo obtiene la menor hemolisis debido a que conserva a los eritrocitos sin ningn cambio y por consiguiente no hay liberacin de hemoglobina.
VII.
DISCUSIONES Para sta evaluacin tomamos en cuenta que los resultados obtenidos son de una especie de caballo sana y joven. Los efectos de temperatura, salinidad y pH frente a una muestra de sangre se ven influenciada de acuerdo a las condiciones inmunolgicas del animal (Forchetti, 2006). Los mrgenes de error para nuestros resultados se obtuvieron en las lecturas de las absorbancias, para i) la temperatura: sabemos que la temperatura fisiolgica es 37C y el porcentaje de hemolisis debe ser mnimo o nulo; sin embargo en los resultados obtenidos no se coincide esta afirmacin; ii) el pH: de la misma forma, sabemos que el pH fisiolgico es 7,4 y su hemolisis debe ser mnima; pero nuestras lecturas nos indican lo distinto comparadas con lo normal (Chihuailaf, 2006).
VIII.
REFERENCIAS BILIOGRFICAS
Granados J, Fragilidad osmtica de los eritrocitos de carnero en relacin con su uso en el laboratorio clnico, Hospital de San Juan de Dios, Costa Rica, 1993. Hariharan S.: Nutrition of laboratory animals. LAIS Centre News 1984; 12: 2- 35. Lovelock J, La hemolisis de clulas sanguneas por congelacin y descongelacin, Instituto Nacional para la investigacin mdica, Londres Inglaterra, 1953. Zou CG, Haemolisis of human and sheep redblood cells in glycerol media: the effect of pH and the role of band 3. School of biological science. Inglaterra. 2000. Forchetti, O.; Maffrand C.; Vissio C.; Boaglio C.; Cufr G.. Hipofosfatemia y fragilidad osmtica eritrocitica en cabras. Revista Electrnica de Veterinaria, Vol. VII, n 01, Enero/2006 Chihuailaf R H . Variaciones de la Fragilidad Osmtica Eritrocitaria en Bovinos a Pastoreo sobre praderas con bajo contenido de Selinio y Suplementados o no con Selenio, Instituto de Ciencias Clnicas Veterinarias. Chile, 2006 http://scielo.sld.cu/scielo.php?pid=S08642892002000100001&script =sci_arttext
Potrebbero piacerti anche
- Pruebas de HemostasiaDocumento19 paginePruebas de HemostasiaDiego Alexander Tipanguano SimbañaNessuna valutazione finora
- VSG y HematocritoDocumento3 pagineVSG y HematocritoKatha Elizabeth100% (4)
- Practik Fragilidad OsmoticaDocumento10 paginePractik Fragilidad OsmoticaAngelica Arteaga Arenas100% (9)
- Escherichia ColiDocumento1 paginaEscherichia ColiESTEFANIA CASTELLANOS MEJIANessuna valutazione finora
- LDH-40Documento2 pagineLDH-40Patricia Donaires100% (1)
- Alteraciones Morfologicas de Las PlaquetasDocumento9 pagineAlteraciones Morfologicas de Las Plaquetasmaria virginia guerraNessuna valutazione finora
- Reacciones FebrilesDocumento9 pagineReacciones FebrilesRocío Ivette Ramírez LópezNessuna valutazione finora
- Guia Fisiologia I PDFDocumento151 pagineGuia Fisiologia I PDFmadelyn aydeeNessuna valutazione finora
- Perfil Lipídico...Documento60 paginePerfil Lipídico...silvia XNessuna valutazione finora
- Porfirinas y Pigmentos BiliaresDocumento1 paginaPorfirinas y Pigmentos Biliaressalamancagrosso100% (2)
- LDH: Función, isoenzimas y aplicaciones clínicasDocumento23 pagineLDH: Función, isoenzimas y aplicaciones clínicasJosé Roberto Vides100% (1)
- Práctica #3 - Analisis Clinico IDocumento5 paginePráctica #3 - Analisis Clinico IKety León MoyaNessuna valutazione finora
- Extraccion de Lipidos de Cerebro Brain LDocumento4 pagineExtraccion de Lipidos de Cerebro Brain LJosue AlvarezNessuna valutazione finora
- Electrolitos Séricos CompletoDocumento22 pagineElectrolitos Séricos Completogabygon50% (2)
- EritropoyesisDocumento18 pagineEritropoyesisPaula Mc-NaughtNessuna valutazione finora
- PDF 20230119 201952 0000Documento21 paginePDF 20230119 201952 0000Karla JackeNessuna valutazione finora
- Marco de Inmuno3Documento3 pagineMarco de Inmuno3Ani NicolasNessuna valutazione finora
- Informe de Hemato Serie RojaDocumento6 pagineInforme de Hemato Serie RojaAnonymous BvzMO9Nessuna valutazione finora
- Semana X - Determinacion Del Tiempo de TromboplastinaDocumento11 pagineSemana X - Determinacion Del Tiempo de TromboplastinaXimena Garcia0% (1)
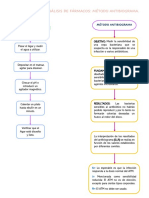
- Introducción al análisis de fármacos: método antibiogramaDocumento2 pagineIntroducción al análisis de fármacos: método antibiogramaAngie Galindo100% (1)
- CPKDocumento7 pagineCPKMiguel Arturo Guerrero AnicetoNessuna valutazione finora
- Prueba de Compatibilidad SanguíneaDocumento15 paginePrueba de Compatibilidad SanguíneaChristianGallegosPalermo100% (2)
- Antigenos e InmunogenosDocumento71 pagineAntigenos e InmunogenosSara Elizabeth Cisneros100% (2)
- Quimica Clinica "Determinación de Pruebas de Funcionamiento Hepático: Proteínas Totales, Albumina, (Método de Verde Bromocresol), Bilirrubina Total, Directa e Indirecta"Documento12 pagineQuimica Clinica "Determinación de Pruebas de Funcionamiento Hepático: Proteínas Totales, Albumina, (Método de Verde Bromocresol), Bilirrubina Total, Directa e Indirecta"Jair Emmanuel Rendon RendonNessuna valutazione finora
- ElectroquimioluminiscenciaDocumento1 paginaElectroquimioluminiscenciamonicaNessuna valutazione finora
- Realización y Tinción Del Frotis SanguíneoDocumento15 pagineRealización y Tinción Del Frotis Sanguíneoivancb39Nessuna valutazione finora
- FIBRINOLISISDocumento2 pagineFIBRINOLISISSara JimenezNessuna valutazione finora
- Obtención de muestras sanguíneas, anticoagulantes y tinción Wright-GiemsaDocumento5 pagineObtención de muestras sanguíneas, anticoagulantes y tinción Wright-GiemsaErica CrispinNessuna valutazione finora
- Aseguramineto de La Calidad en Hematologia y HemostasiaDocumento27 pagineAseguramineto de La Calidad en Hematologia y HemostasiaBernabéMaqueraQuispe0% (1)
- Perfil de CoagulaciónDocumento2 paginePerfil de CoagulaciónTatiana RamirezNessuna valutazione finora
- Determinación de salicilatos en orinaDocumento10 pagineDeterminación de salicilatos en orinaAriana MuñozNessuna valutazione finora
- Informe FlebotomíaDocumento9 pagineInforme FlebotomíaGabriel Figueroa PérezNessuna valutazione finora
- Análisis de electrolitos en orina: importancia clínica y métodosDocumento48 pagineAnálisis de electrolitos en orina: importancia clínica y métodosJhon Andy Ramos50% (2)
- Mecanismo de Acción Del OmeprazolDocumento7 pagineMecanismo de Acción Del OmeprazolMary Angelica Cruz RomeroNessuna valutazione finora
- Liquido PleuralDocumento21 pagineLiquido PleuralNora MaríaNessuna valutazione finora
- BioquimicaDocumento6 pagineBioquimicaveronicabriceNessuna valutazione finora
- Problemas y Soluciones en La TincionDocumento21 pagineProblemas y Soluciones en La Tincionmaria chulde57% (7)
- Tema 15. Función Tubular. Mecanismos de Concentración y Dilución de Orina.Documento36 pagineTema 15. Función Tubular. Mecanismos de Concentración y Dilución de Orina.Pilar del Pino67% (3)
- Practica 3 Sensibilidad GeneralDocumento4 paginePractica 3 Sensibilidad GeneralRemigio Rodríguez A.Nessuna valutazione finora
- Exposicion Control de Calidad Inmunohematologia 1Documento38 pagineExposicion Control de Calidad Inmunohematologia 1Ktalina BeltranNessuna valutazione finora
- Proteínas TotalesDocumento7 pagineProteínas TotalesAndres LlontopNessuna valutazione finora
- Cultivos CelularesDocumento35 pagineCultivos CelularesLori EsbeltoNessuna valutazione finora
- Depuración Renal, Aplicación de La Depuración Renal en La ClínicaDocumento28 pagineDepuración Renal, Aplicación de La Depuración Renal en La ClínicaVictorManuelAllendeQuispe100% (1)
- Clase 4 Funcion RenalDocumento49 pagineClase 4 Funcion RenalJaz Ntvg100% (1)
- Perfil LipidicoDocumento8 paginePerfil LipidicoMelany Rous Villegas RiveroNessuna valutazione finora
- GalactosuriaDocumento21 pagineGalactosuriaErcelyn Menjivar50% (2)
- Dosificación de Alcohol Etílico en Fluidos BiológicosDocumento5 pagineDosificación de Alcohol Etílico en Fluidos BiológicosRafaelita Osorio OjedaNessuna valutazione finora
- Practica 28. Proteinas en OrinaDocumento2 paginePractica 28. Proteinas en Orinajuan del ranchoNessuna valutazione finora
- Práctica 13Documento4 paginePráctica 13Alondra FortunatNessuna valutazione finora
- VDRL en Suero Serologia ABCDocumento6 pagineVDRL en Suero Serologia ABCgamalielNessuna valutazione finora
- Atresia Laringea Parte DanteDocumento5 pagineAtresia Laringea Parte DanteDanteIvanChungaSamillanNessuna valutazione finora
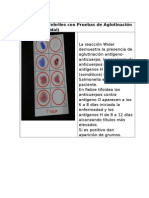
- Reacciones Febriles Con Pruebas de AglutinaciónDocumento1 paginaReacciones Febriles Con Pruebas de AglutinaciónMaurilio HuNessuna valutazione finora
- Pruebas PretransfusionalesDocumento12 paginePruebas PretransfusionalesJaneth Emily CqNessuna valutazione finora
- Caso Clinico Leucemia Linfocitica AgudaDocumento22 pagineCaso Clinico Leucemia Linfocitica AgudaLesly Del CarpioNessuna valutazione finora
- Metabolismo Del Grupo HemoDocumento31 pagineMetabolismo Del Grupo HemoYaritza PinargtNessuna valutazione finora
- Informe AspirnaDocumento7 pagineInforme AspirnabrayanmauriciolopezNessuna valutazione finora
- Prueba PretransfusionalesDocumento7 paginePrueba PretransfusionalesFernandoOviedoLópezNessuna valutazione finora
- FINAL Practica 1 FRAGILIDAD OSMOTICA DEL ERITROCITODocumento14 pagineFINAL Practica 1 FRAGILIDAD OSMOTICA DEL ERITROCITOAlex Ramos Mqr100% (1)
- Final Practica 1 Fragilidad Osmotica Del EritrocitoDocumento14 pagineFinal Practica 1 Fragilidad Osmotica Del EritrocitoOrlando Ascary Casados DNessuna valutazione finora
- El glóbulo rojo: constitución, función y destinoDocumento10 pagineEl glóbulo rojo: constitución, función y destinoCristian AgostiniNessuna valutazione finora
- Un 153 CDocumento12 pagineUn 153 CCesar Toribio GamuzoNessuna valutazione finora
- MODULO 1 Introduccion Al Estudio de La Anatomia Humana KINE 2013Documento15 pagineMODULO 1 Introduccion Al Estudio de La Anatomia Humana KINE 2013Brian Díaz FloresNessuna valutazione finora
- Diatomeas Planctónicas de Cursos de Agua. Cuenca Del Río Piedra Blanca (Córdoba, Argentina)Documento16 pagineDiatomeas Planctónicas de Cursos de Agua. Cuenca Del Río Piedra Blanca (Córdoba, Argentina)Cesar Toribio GamuzoNessuna valutazione finora
- Nuevo Documento de Microsoft WordDocumento9 pagineNuevo Documento de Microsoft WordCesar Toribio GamuzoNessuna valutazione finora
- Ejemplo 3 de Informe de PPDocumento14 pagineEjemplo 3 de Informe de PPCesar Toribio GamuzoNessuna valutazione finora
- Temario OpbDocumento6 pagineTemario OpbCesar Toribio Gamuzo100% (1)
- Maestría en Estadística MatemáticaDocumento3 pagineMaestría en Estadística MatemáticaCesar Toribio GamuzoNessuna valutazione finora
- Plantas CarnivorasDocumento11 paginePlantas Carnivorasosvenuc100% (1)
- Regresión Con Variables Independientes CualitativasDocumento11 pagineRegresión Con Variables Independientes CualitativasDiana Montoya CardonaNessuna valutazione finora
- Identificacion GenesDocumento1 paginaIdentificacion GenesCesar Toribio GamuzoNessuna valutazione finora
- Inf Urinaria Sanitarios Medicine2010Documento8 pagineInf Urinaria Sanitarios Medicine2010ximena_11Nessuna valutazione finora
- Nuevo Documento de Microsoft WordDocumento9 pagineNuevo Documento de Microsoft WordCesar Toribio GamuzoNessuna valutazione finora
- Conservas de PescadoDocumento72 pagineConservas de PescadoALex Villavicencio ArellanoNessuna valutazione finora
- Ejemplo 3 de Informe de PPDocumento14 pagineEjemplo 3 de Informe de PPCesar Toribio GamuzoNessuna valutazione finora
- Ejemplo 3 de Informe de PPDocumento14 pagineEjemplo 3 de Informe de PPCesar Toribio GamuzoNessuna valutazione finora
- Las principales hortalizas del PerúDocumento34 pagineLas principales hortalizas del PerúCesar Toribio GamuzoNessuna valutazione finora
- Ejemplo 3 de Informe de PPDocumento14 pagineEjemplo 3 de Informe de PPCesar Toribio GamuzoNessuna valutazione finora
- Clase Inmuno Semana 6Documento82 pagineClase Inmuno Semana 6Cesar Toribio GamuzoNessuna valutazione finora
- Pseudocereales, alimentos del futuroDocumento27 paginePseudocereales, alimentos del futuroCesar Toribio GamuzoNessuna valutazione finora
- Control MicrobiológicoDocumento19 pagineControl MicrobiológicoFrancesca MazzolaniNessuna valutazione finora
- Art 07Documento7 pagineArt 07Liidia Boada ArcuriNessuna valutazione finora
- Lace Sartori BioDocumento47 pagineLace Sartori BioCesar Toribio GamuzoNessuna valutazione finora
- Manual InmunologíaDocumento25 pagineManual Inmunologíaolga_bravo_19Nessuna valutazione finora
- Pseudocereales, alimentos del futuroDocumento27 paginePseudocereales, alimentos del futuroCesar Toribio GamuzoNessuna valutazione finora
- Manual InmunologíaDocumento25 pagineManual Inmunologíaolga_bravo_19Nessuna valutazione finora
- Reconocimiento y RecuDocumento8 pagineReconocimiento y RecuCesar Toribio GamuzoNessuna valutazione finora
- Pseudocereales, alimentos del futuroDocumento27 paginePseudocereales, alimentos del futuroCesar Toribio GamuzoNessuna valutazione finora
- Reconocimiento y RecuDocumento8 pagineReconocimiento y RecuCesar Toribio GamuzoNessuna valutazione finora
- Interferon 1Documento36 pagineInterferon 1Cesar Toribio GamuzoNessuna valutazione finora
- EncurtidoDocumento13 pagineEncurtidoCesar Toribio GamuzoNessuna valutazione finora
- Malformaciones Del Sistema Nervioso CentralDocumento9 pagineMalformaciones Del Sistema Nervioso CentralAlejandro ArellanoNessuna valutazione finora
- Operante LibreDocumento7 pagineOperante LibrecristhianNessuna valutazione finora
- GT Necropsias-Feminicidio 2014-06-19Documento32 pagineGT Necropsias-Feminicidio 2014-06-19DenisseNessuna valutazione finora
- Tinea CapitisDocumento1 paginaTinea CapitisMalk BoseNessuna valutazione finora
- ReumatologíaDocumento125 pagineReumatologíaRamón Gómez SalasNessuna valutazione finora
- Imageneolgia NuevoDocumento10 pagineImageneolgia NuevoIzaura ParraNessuna valutazione finora
- 1 Tema 07 Clasificacion SSVVDocumento14 pagine1 Tema 07 Clasificacion SSVVangelica ruiz huamanNessuna valutazione finora
- Interpreta una gasometría arterialDocumento2 pagineInterpreta una gasometría arterialJuan Cesar Diaz Sanchez100% (1)
- Síndrome de Brown: caso clínico de una niña de 3 añosDocumento2 pagineSíndrome de Brown: caso clínico de una niña de 3 añosNicolas IgnacioNessuna valutazione finora
- Negro OrtegaDocumento6 pagineNegro Ortegabrandansolis100% (1)
- 5to RV-PRIMARIADocumento20 pagine5to RV-PRIMARIAMANUELNessuna valutazione finora
- Consideraciones GerontologicasDocumento10 pagineConsideraciones GerontologicasArakíí MoreníìthoNessuna valutazione finora
- Desarrollo sistema venosoDocumento2 pagineDesarrollo sistema venosoWilly GutierrezNessuna valutazione finora
- La Química Del AmorDocumento10 pagineLa Química Del AmoraromeoNessuna valutazione finora
- Sistema TegumentarioDocumento34 pagineSistema Tegumentariojhony rojasNessuna valutazione finora
- Céstodos 2023 VeterinariaDocumento20 pagineCéstodos 2023 VeterinariaGisel Callejas GutierrezNessuna valutazione finora
- Triptico DengueDocumento2 pagineTriptico DengueAndré Luzuriaga CarreraNessuna valutazione finora
- Manchas de Sangre QuimicaDocumento19 pagineManchas de Sangre QuimicaYaayi Ibañez Carvallo0% (1)
- Examen físico segmentario completoDocumento4 pagineExamen físico segmentario completoRodrigo De PaulNessuna valutazione finora
- Procedimientos EcoguiadosDocumento79 pagineProcedimientos EcoguiadoseduardoNessuna valutazione finora
- Angioedema: causas, clasificación y tratamientoDocumento4 pagineAngioedema: causas, clasificación y tratamientoKathia Allison Cano FloresNessuna valutazione finora
- 50 Ejemplos de Animales Invertebrados y VertebradosDocumento2 pagine50 Ejemplos de Animales Invertebrados y VertebradosDiego M. López100% (1)
- Presentación Parasitología3.0Documento17 paginePresentación Parasitología3.0aliciaNessuna valutazione finora
- CAVIDAD BUCAL AnatomíaDocumento79 pagineCAVIDAD BUCAL AnatomíaLeo FaronaNessuna valutazione finora
- El arte rupestre de caza del CurutaránDocumento38 pagineEl arte rupestre de caza del CurutaránMorelianoLiveNessuna valutazione finora
- Trabajo Investigacion.Documento55 pagineTrabajo Investigacion.Ydalmis MarcanoNessuna valutazione finora
- Patología Aviar II Informe de Práctica #1 Cólera AviarDocumento5 paginePatología Aviar II Informe de Práctica #1 Cólera AviarAlejandra SánchezNessuna valutazione finora
- Valvulopatías SemDocumento50 pagineValvulopatías SemDaniela MoraNessuna valutazione finora
- ClodDocumento3 pagineClodEduardo de la CalNessuna valutazione finora
- El DesteteDocumento14 pagineEl DesteteCarmelita huancas ramirezNessuna valutazione finora